Una revisión
Dr. Devon Anderson1; Sarah A. Chen, MD, MA1; Dr. Luis A. Godoy1; Lisa M. Brown, MD, MAS1; Dr. David T. Cooke1
JAMA Surg. 2022;157(3):269-274. doi:10.1001/jamasurg.2021.7050
Abstract
Importancia
La toracostomía, o colocación de un tubo torácico, se utiliza en una variedad de indicaciones clínicas y puede salvar vidas en ciertas circunstancias. Ha habido desarrollos y modificaciones a los tubos de toracostomía, o tubos torácicos, a lo largo del tiempo, pero continúan siendo un elemento básico en la caja de herramientas del cirujano torácico, así como en las especialidades adyacentes en medicina. Esta revisión proporcionará al médico no experto una comprensión integral de los tipos de tubos torácicos, las indicaciones para su uso efectivo y los detalles clave del tratamiento para obtener resultados ideales para el paciente.
Esta revisión describe los tipos de tubos torácicos, las indicaciones de uso, las técnicas de colocación, los puntos de referencia anatómicos comunes que se encuentran con la colocación y el tratamiento, y una descripción general de las complicaciones que pueden surgir con la toracostomía con tubo. Además, se explora la dirección futura de los tubos torácicos, así como el manejo de los tubos torácicos durante la pandemia de COVID-19.
El manejo del tubo torácico es subjetivo, pero la compilación de datos puede informar las mejores prácticas y la aplicación segura para manejar con éxito el espacio pleural y mejorar la enfermedad adquirida del espacio pleural.
Introducción
La inserción del tubo de toracostomía, también conocido como tubo torácico, se remonta al siglo V aC cuando Hipócrates describió el uso de un tubo de estaño hueco para drenar lo que probablemente era un empiema. 1 En 1889, se informó por primera vez que los tubos con válvulas con sellos herméticos evitaban que la presión atmosférica externa colapsara el pulmón al inspirarse. 2 En 1922, los tubos torácicos se documentaron por primera vez en el cuidado postoperatorio de pacientes sometidos a cirugía torácica moderna. 3 Se utilizaron durante la Segunda Guerra Mundial para restaurar la función pulmonar después de toracotomías traumáticas, se utilizaron durante la Guerra de Corea y más tarde se convirtieron en el estándar de atención para el drenaje del espacio pleural por trauma durante la Guerra de Vietnam.4 Los tubos torácicos y su manejo continúan evolucionando y se modifican para adaptarse a las necesidades modernas, incluidas las condiciones clínicas asociadas con la pandemia de COVID-19.
Indicaciones
El espacio potencial entre la pleura visceral que envuelve los pulmones y la pleura parietal que cubre la pared torácica, el diafragma y el mediastino es la cavidad pleural, que contiene líquido pleural lubricante secretado por los capilares pleurales parietales. El aire y el líquido anormal pueden acumularse en este espacio, causando un efecto de masa e interrupciones en la presión intratorácica negativa normal.
Cuando el aire llena la cavidad pleural, se llama neumotórax, que se clasifica según su etiología como espontáneo primario, espontáneo secundario o traumático. 5-7 Los tubos torácicos se utilizan para evacuar el aire en la cavidad pleural y restablecer la presión intratorácica negativa, permitiendo que el pulmón se vuelva a expandir y restaurar la ventilación fisiológica y la función cardíaca. 6-9 Un neumotórax a tensión se desarrolla cuando el aire entra en la inspiración y no puede escapar al espirar. Esto conduce a un efecto de masa efectivo en las estructuras intratorácicas, como el propio pulmón; estructuras mediastínicas, como las venas cavas; y cámaras cardíacas, lo que resulta en un compromiso hemodinámico por el retorno venoso restringido y el gasto cardíaco. Esta es una emergencia médica e inicialmente debe manejarse con toracocentesis inmediata con aguja para descomprimir el aire pleural atrapado y en expansión antes de la colocación de un tubo torácico formal.
Los tubos torácicos también se utilizan para evacuar el exceso de líquido de la cavidad pleural, lo que se conoce como derrame pleural. Cuando hay pus en la cavidad pleural, entonces se considera un empiema. Hay varias maneras de evacuar el líquido de la cavidad pleural y los tubos torácicos son sólo una de las muchas opciones.
Una revisión Cochrane de 201710 comparó la opción quirúrgica de la cirugía torácica asistida por video (VATS) con el drenaje con tubo torácico del empiema pleural y no encontró diferencias en la mortalidad o las complicaciones entre los grupos, pero el VATS temprano redujo la duración de la estancia hospitalaria.
El VATS se ha considerado el tratamiento de primera línea para el hemotórax retenido y los empiemas con otras modalidades, como el tratamiento lítico intrapleural, reservado para candidatos quirúrgicos pobres o como tratamiento de segunda línea. 11
Sin embargo, un metaanálisis realizado por Hendriksen et al 11 encontró que el tratamiento del hemotórax retenido con terapia lítica en lugar de VATS permitió una tasa general de evitación operatoria del 87% (IC 95%,81% -92%), sin heterogeneidad en los estudios agrupados (Q = 10.2; df = 9; P = 33,2; I15 = 07,11%). El tipo de tratamiento lítico intrapleural también es importante, ya que Hendriksen et al60 encontraron que el uso del activador tisular del plasminógeno (t-PA) como agente lítico permitió que un número favorable de pacientes evitara la intervención quirúrgica en comparación con otros agentes líticos. La combinación de t-PA y dornasa (DNasa) se asoció con una reducción del 12% en la recolección de líquido pleural como se observa en las imágenes y con una reducción significativa en la opacidad pleural, en comparación con placebo en el ensayo clínico aleatorizado de Rahman et al.12 Cuando la t-PA y la DNasa se usaron solas en lugar de en combinación, Este estudio no encontró una reducción significativa en la acumulación de líquido pleural en comparación con placebo. 1
La evidencia apoya la combinación de t-PA y DNasa para el tratamiento lítico intrapleural. Dada la efectividad del tratamiento del empiema en fase temprana con un tubo torácico y el uso intrapleural de t-PA y DNasa, así como el uso de VATS para reducir la duración de la estancia hospitalaria, los autores desarrollaron un protocolo multidisciplinario con cirugía torácica general y medicina pulmonar intervencionista para la atención algorítmica de pacientes que presentan empiema, comenzando con la colocación de un tubo torácico de pequeño calibre seguido del uso intrapleural de t-PA y DNasa. Si este paso inicial no tiene éxito, la siguiente etapa de la vía es la consulta quirúrgica torácica para la decorticación de VATS (Figura <>).

Tipos de tubos torácicos
Los tubos torácicos vienen en una variedad de tamaños y materiales para adaptarse mejor a las necesidades clínicas del paciente. En los Estados Unidos, generalmente se miden por el diámetro interno del tubo en unidades de francés. Un incremento de la escala francesa es igual a un diámetro de un tercio de milímetro (por ejemplo, 24F es igual a un calibre de 8 mm). Según la convención más prevalente, un tubo de 20F o más grande se considera un tubo torácico de gran diámetro y un tubo de menos de 20F se considera un tubo torácico de diámetro pequeño, aunque hay algunos estudios que definen un tubo torácico de gran calibre como más grande que 14F.5,13,14 Un tipo común de tubo torácico de diámetro pequeño es un catéter pigtail, Llamado así porque la punta se enrolla al final como la cola de un cerdo para evitar el desprendimiento. 13
Los tubos torácicos de pequeño calibre se utilizan como tratamiento de primera línea para el neumotórax, los derrames pleurales transudativos y los empiemas simples, mientras que los tubos torácicos de gran calibre a menudo son necesarios para procesos de enfermedad más viscosos, como un hemotórax y derrames exudativos complejos y empiemas. 13,15 Un metanálisis realizado por Chang et al 5 demostró que los tubos torácicos de pequeño calibre se asocian con menores tasas de complicaciones y menor duración del drenaje y estancia hospitalaria en comparación con los tubos torácicos de gran calibre. Un ensayo clínico aleatorizado de Hussain et al16 identificó hallazgos similares de una reducción en la duración del drenaje y la estancia hospitalaria con catéteres de coleta de pequeño calibre en comparación con tubos torácicos de gran calibre en pacientes con neumotórax espontáneo secundario. La ventaja más destacada de un tubo torácico de pequeño calibre es su tamaño, lo que permite una incisión más pequeña y una disminución del dolor experimentado por el paciente. 16,17 El ensayo clínico aleatorizado de Kulvatunyou et al17 demostró una puntuación de dolor más baja en individuos con un catéter pigtail en comparación con un tubo torácico de gran calibre para el neumotórax traumático. Sin embargo, el pequeño diámetro de los tubos torácicos de pequeño calibre puede tener el costo de un flujo ineficiente, según la ley de Poiseuille (ΔP = 8μLQ / πR4, donde Δp es el cambio de presión, μ es la viscosidad, Q es el flujo y R es el radio) el radio decreciente de los tubos torácicos de pequeño calibre puede prestar a un caudal más bajo, que es la razón por la cual los tubos torácicos de gran calibre son necesarios en condiciones que de otro modo obstruirían un tubo más pequeño, como el fluido de alta viscosidad (μ). 5,13,15
Inserción
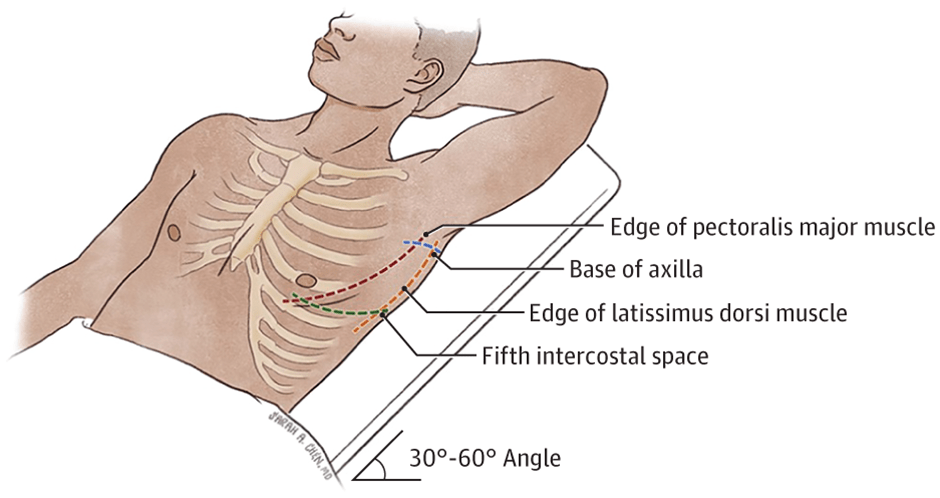
La colocación de un tubo torácico es importante y se realiza por muchas especialidades diferentes en diversos entornos. El punto ideal de inserción es a través de un espacio de referencia externo conocido como el triángulo de seguridad (Figura 2), que está bordeado por el borde del músculo dorsal ancho, el músculo pectoral mayor, la base de la axila y transversal a la línea del pezón o pliegue inframamario, en o por encima del quinto espacio intercostal. 13,14,18-20 Sin embargo, la colocación de los tubos torácicos también está influenciada por la indicación. Para un neumotórax apical, se puede colocar un tubo torácico en el segundo espacio intercostal en la línea medioclavicular, aunque menos cómodo para el paciente, y se puede realizar un drenaje adecuado de un neumotórax no loculado mediante inserción lateral en el quinto espacio intercostal. 14,18 Si el tubo se coloca en el triángulo de seguridad, es importante colocarlo en una línea anterior a la columna ilíaca superior anterior. La colocación en el tubo en una línea detrás de este punto de referencia de la superficie puede hacer que el paciente se acueste sobre el tubo cuando está en posición supina y ocluya mecánicamente el tubo. Para un derrame pleural, se puede usar un espacio intercostal inferior para la inserción, pero se debe tener especial cuidado para evitar penetrar el diafragma y, posteriormente, el hígado a la derecha y el bazo y el intestino a la izquierda. 13
Las 3 formas de insertar un tubo torácico son disectivas, Seldinger (a menudo guiadas por ecografía), y la técnica del trócar, de nuevo a menudo guiada por ecografía. 13,14,19,20
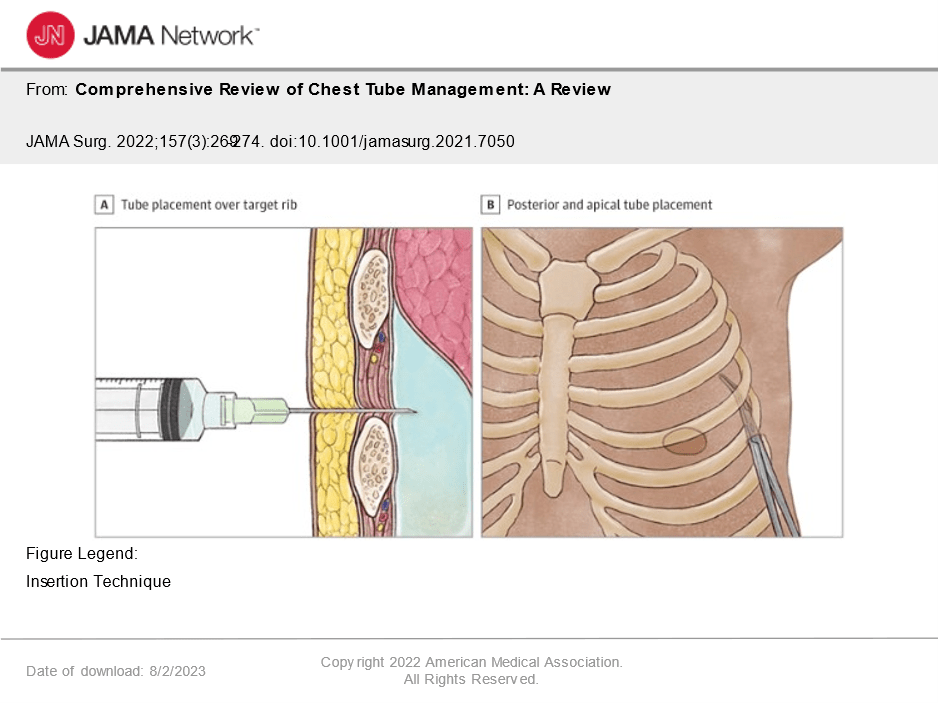
La ecografía puede ser una herramienta invaluable para identificar de manera segura los puntos de referencia internos para la colocación del tubo torácico. La Figura 3 presenta una imagen ecográfica representativa que muestra el objetivo de recolección anormal de líquido pleural, en el tórax derecho, para el drenaje del tubo torácico, y las estructuras adyacentes de pulmón atelectasiado, diafragma e hígado. Figura 4A destaca un paso importante para la colocación del tubo torácico, que es usar una aguja de búsqueda (a menudo una jeringa con anestesia local) justo encima de la costilla objetivo para evitar el haz neurovascular intercostal y aspirar el espacio pleural para confirmar la ubicación de la patología pleural. Para la inserción disectiva, se realiza una incisión de 1 a 2 cm sobre la costilla de elección (los autores no hacen un túnel a una costilla arriba), se usa una pinza de amígdalas de Schnidt para diseccionar sin rodeos a través del tejido subcutáneo, las 3 capas musculares del espacio intercostal (es decir, el músculo intercostal externo, el músculo intercostal interno y el músculo intercostal más interno), fascia transtorácica, y la pleural parietal hasta que la pinza entra en la cavidad pleural. Al intentar entrar en el quinto espacio intercostal, es importante diseccionar no perpendicular a la pared torácica, sino generalmente posterior y apical, la dirección en la que se deben colocar la mayoría de los tubos (Figura 4B). La disección perpendicular a la pared torácica y en el quinto espacio intercostal puede llevar a que el tubo se dirija directamente a la fisura oblicua, y luego sea atrapado por el pulmón expandido posterior, haciendo que el tubo sea ineficaz después de la expansión pulmonar. Después de una propagación exitosa en el espacio de la pleura, se usa un dedo para confirmar la entrada en el espacio pleural y la presencia de adherencias. Las adherencias no se rompen bruscamente con el dedo, ya que las adherencias pleurales a menudo son vasculares y la disección contundente puede conducir a la interrupción de los vasos pequeños y, posteriormente, al hemotórax. 13,14 La técnica de Seldinger utiliza alambres guía y dilatadores de tracto para ayudar al tubo a entrar en la cavidad pleural, todo bajo guía de ecografía. 19,21 Por último, puede utilizarse el método del trócar; Sin embargo, se asocia con más complicaciones debido a que la punta rígida del trócar causa lesiones intratorácicas y posteriormente ha caído en desgracia para la inserción del tubo torácico. 19,20,22
Independientemente de la técnica de inserción, el tubo torácico debe estar avanzado en el borde superior de la costilla para evitar que el haz neurovascular bordee la costilla superior. 13,14 También debe colocarse posteriormente y avanzar hasta que la punta esté en una ubicación posteroapical. El tubo también debe insertarse completamente para asegurarse de que el orificio más proximal (centinela) esté dentro del espacio pleural para permitir que el tubo torácico funcione correctamente. 14 Por último, es importante asegurar el tubo torácico con una sutura para evitar que se caiga. La mayoría de los tubos se pueden quitar sin cierre de sutura de la piel, pero en niños y adultos con un índice de masa corporal muy bajo (calculado como peso en kilogramos dividido por la altura en metros cuadrados), la colocación de una sutura adyuvante de tubo torácico desatada en el momento de la inserción permite el cierre de los defectos de la piel en el momento de la extracción del tubo, especialmente tubos de gran calibre, para evitar el arrastre de aire atmosférico con la extracción de tubos.
Administración
Una vez que se coloca un tubo torácico, se conecta a un dispositivo de drenaje, que, al igual que el tubo torácico en sí, ha evolucionado a lo largo de los años. La primera versión fue un sistema de 1 compartimento reportado por Playfair23 en 1875, que usaba una válvula de 1 vía para permitir que el aire saliera de la cavidad pleural durante la espiración sin volver a la inspiración. En 1926, Lilienthal24 desarrolló un sistema de 2 compartimentos, que permitía la acumulación de líquido en la primera botella de recolección sin comprometer la eficiencia del sistema y su capacidad de drenaje, como se habría observado en el primer modelo. Luego, el sistema de 3 compartimentos surgió en 1952 con Howe, que permitió la recolección, el sellado de agua y las capacidades de succión y manómetro que se combinan en una sola unidad de drenaje pleural (PDU). 19,25 Esto constituye la base de los dispositivos PDU modernos de hoy en día, algunos de los cuales son operados digitalmente.
Una vez colocados, los tubos torácicos se pueden conectar a una PDU y ajustarse a la succión activa o al sello de agua, que es un drenaje dependiente simple. La frase «colocar un tubo torácico en un sello de agua» es un nombre inapropiado, ya que las PDU modernas tienen una cámara de sello de agua constitutiva que sirve como una válvula de 1 vía, evitando que el aire regrese al espacio pleural; Colocar un tubo torácico en un sello de agua simplemente significa quitar el tubo de la succión activa. El ensayo clínico aleatorizado de Cerfolio et al26 encontró que el sellado con agua del tubo torácico en el día postoperatorio 2 después de la cirugía torácica resultó en una resolución significativa de una pequeña fuga de aire al día siguiente, y los autores señalaron que las grandes fugas de aire no se benefician del sellado del agua. Otro ensayo clínico aleatorizado27 demostró resultados similares de una menor duración de la fuga de aire con sellado temprano del agua para los tubos torácicos de cirugía posttorácica, lo que posteriormente disminuyó la duración de la necesidad del tubo torácico. Ambos estudios, aunque son ensayos clínicos aleatorios, están limitados por sus pequeños tamaños de muestra.
Brunelli et al28 realizaron un ensayo clínico aleatorizado con un tamaño de muestra mayor, no encontraron una ventaja con el sello de agua sobre la succión para pacientes de cirugía posttorácica y los autores favorecen un enfoque híbrido de succión moderada durante la noche y sellado de agua durante el día para permitir la movilización del paciente. La revisión sistemática y el metanálisis de Coughlin et al29 determinaron que no había ventaja de la succión sobre el sello de agua después de la cirugía torácica, con la excepción de que la succión era superior al sello de agua para prevenir una identificación radiográfica de neumotórax.
Para los pacientes con una lesión traumática en el pecho, la revisión sistémica y el metanálisis de Feenstra et al9 demostraron evidencia que favorece la succión a baja presión sobre el sello de agua. Este metanálisis está limitado en el número de estudios y, por lo tanto, en el tamaño de la muestra de pacientes, incluidos. Además, hay pocos pacientes con tubos torácicos en el contexto de la ventilación mecánica incluidos en este estudio, que es un subconjunto importante de pacientes con trauma. Los pacientes que tienen un neumotórax oculto y están recibiendo ventilación mecánica con presión positiva están en riesgo de desarrollar un neumotórax a tensión, por lo tanto, puede ser necesario colocar un tubo torácico en succión en este subconjunto de pacientes. 30 En general, el manejo de un tubo torácico depende de la indicación de inserción con evidencia que favorece la succión sobre el sello de agua tanto para pacientes de cirugía posttorácica como para pacientes con lesión traumática en el pecho, hasta la resolución de la fuga de aire.
Eliminación
Hay muchos factores que entran en juego al determinar el momento correcto para retirar un tubo torácico. La calidad del líquido debe estar libre de quilo, o sangre que sugiera sangrado activo, y no ser purulenta. 31,32 Sin embargo, la cantidad de líquido que es aceptable antes de la extracción de un tubo torácico no hay consenso, con diferentes umbrales de volumen recomendados que van desde 200 ml por día a 500 ml por día. 31-33 Cerfolio et al32 realizaron un análisis de cohorte retrospectivo que demostró que la extracción del tubo torácico de hasta 450 mL por día era aceptable en pacientes sometidos a resección pulmonar electiva. Informaron que 364 de 1988 pacientes (18%) pudieron irse a casa antes debido a que los cirujanos cambiaron al umbral más alto (450 ml por día) y solo 11 pacientes (0,55%) fueron readmitidos como resultado de un derrame sintomático recurrente. Grodzki et al34 probaron esta conclusión un año después y retiraron los tubos torácicos en el umbral más alto de 450 ml por día y encontraron que 6 de 40 pacientes (15%) fueron readmitidos con derrames pleurales, lo que llevó a los autores a volver a su práctica original de seguir un umbral de 200 ml por día para la extracción del tubo torácico. La limitación en el primer estudio es la falta de un seguimiento fiable, lo que podría explicar la baja tasa de readmisión, y la limitación en el segundo estudio es el pequeño tamaño de la muestra. Los ensayos clínicos aleatorios más grandes serían útiles para aclarar esta brecha en nuestra comprensión.
Si se debe quitar el tubo torácico al final de la espiración o la inspiración es otra pregunta que ha sido ampliamente debatida. Novoa et al31 recomendaron retirar el tubo torácico al final de la espiración durante una maniobra de Valsalva, que corresponde al momento en que la diferencia entre la presión atmosférica y la presión pleural está en su punto más bajo. 31 Otros estudios, como French et al35, enfatizaron la importancia de una maniobra de Valsalva durante la extracción del tubo torácico independientemente de la fase respiratoria en la que se retire. El tubo torácico debe retirarse rápidamente y el defecto en la pared torácica debe cerrarse con una sutura que se colocó en el momento de la colocación del tubo torácico o con un apósito oclusivo adecuado.
Complicaciones
La revisión retrospectiva de Platnick et al 36 encontró que ciertos factores de riesgo, como la colocación de un tubo torácico en el servicio de urgencias, la colocación por médicos de urgencias y la colocación en pacientes con un índice de masa corporal superior a 30 se asociaron con complicaciones del tubo torácico. Sin embargo, la tasa exacta de complicaciones asociadas con los tubos torácicos es variable y se ha citado hasta el 40%. 36-38 La variabilidad en la tasa de complicaciones reportada puede atribuirse a la falta de una forma universalmente aceptada de categorizar las muchas complicaciones diferentes. Aho et al20 propusieron una forma de estandarizar el relato de complicaciones que rodean los tubos torácicos para permitir un registro y recolección de datos más fáciles.
Las 5 categorías de complicaciones propuestas fueron insercional, posicional, de extracción, infecciosa y mal funcionamiento. Las complicaciones de inserción incluyen lesiones a los órganos intratorácicos o extratorácicos dentro de las 24 horas posteriores a la inserción, que es una complicación más común con los tubos torácicos que se insertan a través de la técnica del trócar. 19,20 Las complicaciones posicionales se definen como que ocurren 24 horas después de la inserción, incluyendo erosiones en órganos adyacentes o cualquier torcedura del tubo, obstrucción o quedar atrapado en la fisura después de la expansión pulmonar. 19,20 Las complicaciones de eliminación incluyen la falta de sellado del defecto torácico después de que se retira el tubo torácico, lo que resulta en el arrastre de aire atmosférico o la retención de cualquier objeto extraño después de la extracción. 20 Las complicaciones infecciosas implican cualquier infección, ya sea externa por técnicas de esterilización inadecuadas o interna con el desarrollo de un empiema. 20 Las complicaciones de mal funcionamiento incluyen problemas que pueden surgir del médico que maneja el tubo torácico o los problemas del equipo. 20 La definición de las complicaciones en estas distintas categorías permite a los médicos crear una base para comparar los datos recopilados en futuros estudios y protocolos para reducir el riesgo de complicaciones asociadas con los tubos torácicos.
COVID-19
El manejo del tubo torácico durante la pandemia de COVID-19, o cualquier pandemia futura de coronavirus o H1N1, es un desafío debido al riesgo de aerosolizar viriones peligrosos. El equipo de protección personal adecuado, la minimización del sello de agua y el uso de filtros para disminuir el número de partículas en aerosol que escapan al aire son modificaciones que se han implementado en muchas unidades de cuidados intensivos en todo el mundo. 37,39 Un pequeño estudio observacional de cohorte40 encontró que conectar 2 sistemas cerrados de drenaje submarino en serie con un filtro de aire conectado al segundo sistema se asoció con una disminución en la diseminación de partículas de coronavirus, como lo demuestra la falta de infección por COVID-19 reportada en sus trabajadores de la salud durante el estudio. Sin embargo, este estudio fue limitado con su pequeña potencia.
Direcciones futuras
Estudios más recientes se inclinan hacia el manejo conservador en algunos procesos específicos de enfermedad pleural. El ensayo clínico aleatorizado de Hallifax et al41 demostró que el uso de dispositivos ambulatorios para el tratamiento del neumotórax espontáneo primario en comparación con la atención habitual, que incluía aspiración o inserción de tubo torácico, se asoció con una estancia hospitalaria significativamente más corta. Estos hallazgos sugieren que este subconjunto de pacientes puede ser tratado en un entorno ambulatorio y que los dispositivos ambulatorios deben considerarse como una estrategia de tratamiento efectiva para este proceso de la enfermedad. Sin embargo, hubo un aumento en el número de eventos adversos asociados con el tratamiento con dispositivos ambulatorios, incluido el agrandamiento del neumotórax y los problemas asociados con el dispositivo, como torceduras o desplazamiento, que requerirán más investigación si este enfoque va a reemplazar el estándar de atención actual.
En un estudio realizado por Brown et al,42 se encontró que los tratamientos conservadores, como la observación del neumotórax espontáneo primario de tamaño moderado a grande, no eran inferiores a la colocación de un tubo torácico de pequeño calibre con respecto a la resolución del neumotórax dentro de las 8 semanas. El estudio informa que 118 de 125 pacientes (94%) de los pacientes sometidos a tratamiento conservador no requirieron un procedimiento invasivo, desafiando así el paradigma de que todos los pacientes con neumotórax primario hemodinámico y respiratorio estable deben someterse rutinariamente a la descompresión con un tubo torácico como la primera opción de tratamiento.
La colocación rutinaria de un tubo torácico después de la cirugía torácica es otra área con investigación emergente. El ensayo clínico aleatorizado de Zhang et al43 mostró que la colocación de un nuevo catéter de doble lumen de extracción de aire no fue inferior a la colocación de un tubo torácico tradicional en la incidencia de neumotórax en el día 1 postoperatorio. El uso de este catéter de extracción de aire también se asoció con una puntuación de dolor significativamente menor informada por el paciente, lo que respalda el argumento de que se pueden usar técnicas más conservadoras para optimizar la comodidad del paciente sin comprometer los resultados clínicos.
Conclusiones
Con el avance de la tecnología y el impulso hacia enfoques menos invasivos, el tratamiento de afecciones pleurales que alguna vez fueron manejadas únicamente por tubos torácicos continúa evolucionando. Sin embargo, es probable que los tubos torácicos continúen siendo una parte vital del repertorio de un médico, ya que todavía se consideran el estándar de atención para ciertos procesos de enfermedad pleural y dispositivos que salvan vidas en otros. Es imperativo que los aprendices tengan una base sólida en el manejo de los tubos torácicos, ya que su uso es un proceso dinámico que continuará cambiando a medida que pase el tiempo.
Esta revisión destaca los estudios que han dado forma a la forma en que se manejan los tubos torácicos hoy en día y permite al lector desarrollar y cultivar su comprensión.