Este artículo recientemente publicado en el New England, ofrece una forma de actuar en salud pública para evitar la propagación de una enfermedad mortal como el ébola, con la vacunación a contactos y contactos de los contactos, con lo cual se logra mitigar el impacto, desde los diez días de realizada la vacunación. Si como lo leen. Cuando estudiábamos originalmente la respuesta inmunitaria esta se producía a los catorce días. Ganar este tiempo para enfermedades como esta pueden ser muchas muertes evitadas. Además de la estrategia de vacunación.

Al comienzo del brote de enfermedad por el virus del Ébola (EVE) de 2018-2020 en el este de la República Democrática del Congo (RDC), no se había autorizado ninguna vacuna. Sin embargo, la evidencia aleatorizada por conglomerados de Guinea en 2015 había indicado que la vacunación en anillo alrededor de los nuevos casos (dirigida a los contactos y contactos de contactos) con el uso de la vacuna viva de replicación rVSV-ZEBOV-GP de dosis única reducía las tasas de EVE a partir de los 10 días posteriores a la vacunación. Por lo tanto, la vacunación en anillo se agregó a las medidas de control estándar para ese brote.

Métodos
En este estudio, evaluamos la incidencia de la EVE en los primeros 9 días posteriores a la vacunación (cuando se esperaba poca protección del aislamiento de casos o la vacunación en anillo), durante los días 10 a 29 y en períodos posteriores. Establecimos 1853 anillos alrededor de nuevos casos o grupos dentro de los 21 días posteriores a la aparición de los síntomas en el caso índice y ofrecimos la vacunación a los miembros del anillo. Se hizo un seguimiento de la aparición de la EVE en los vacunados hasta el final del brote a mediados de 2020.
Resultados
Del 8 de agosto de 2018 al 14 de enero de 2020, vacunamos a 265.183 participantes. De estos vacunados, 102.515 fueron monitoreados los días 0, 3 y 21 por seguridad. Entre los contactos y contactos de contactos, se diagnosticaron 434 casos de EVE (0,2 por anillo), casi todos entre 0 y 9 días (380 casos) o entre 10 y 29 días (32 casos) después de la vacunación. Se diagnosticaron 22 casos adicionales después del día 29 durante un promedio de 170 días más de seguimiento. Cuanto antes se iniciaran las medidas de control (incluida la vacunación en anillo) después de la aparición de EVE en el caso índice, antes se reducirían las tasas de EVE entre los contactos. En cada subgrupo, las tasas de EVE cayeron repentinamente alrededor del día 10. Entre los contactos y los contactos de contactos que todavía estaban libres de enfermedad el día 10, la tasa de aparición de EVE durante los días 10 a 29 fue de 0,16 por 1000 (en 32 de 194.019 participantes). Esta tasa fue mucho menor que la tasa de 4,64 por 1000 (en 21 de 4528 participantes) que se había observado entre los miembros del anillo definidos de manera similar en Guinea, en quienes se habían iniciado rápidamente las medidas de control estándar pero la vacunación se retrasó hasta 21 días después de la formación del anillo (cociente de tasas, 0,04; intervalo de confianza del 95%, 0,02 a 0,06). No se identificaron problemas de seguridad con la vacuna.

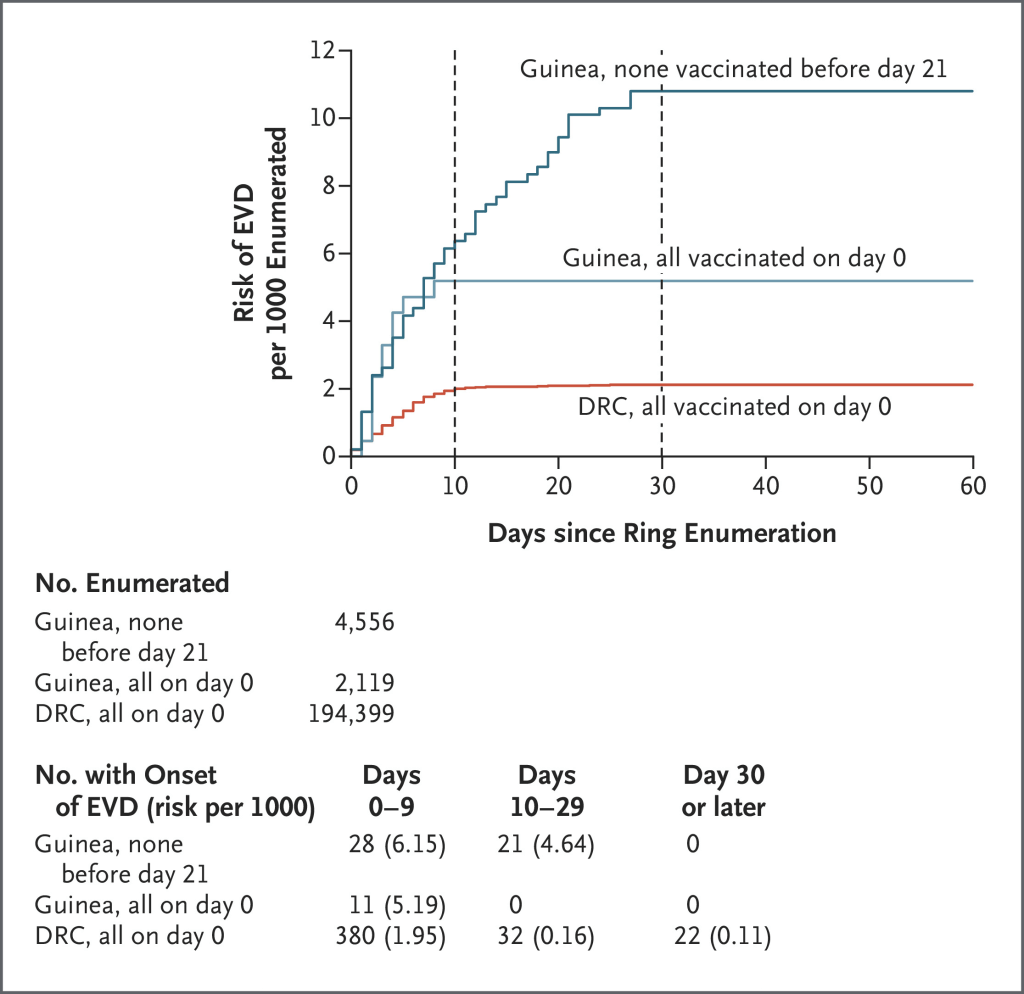
A pesar de un seguimiento minucioso de casi 200.000 contactos o contactos de contactos en la República Democrática del Congo, desde aproximadamente el día 10 después de la intervención con la vacunación en anillo y otras medidas de protección, se identificaron pocos casos adicionales de aparición de EVE entre los vacunados. Además, cuanto antes se aplicaron estas intervenciones después de la aparición de la EVE en el caso índice, antes disminuyó la incidencia de la EVE en los contactos. La asociación entre el momento de la disminución de la incidencia de la EVE entre los contactos de los participantes que recibieron el paquete de intervención proporciona evidencia de que este conjunto de intervenciones fue protector, pero no separa los efectos protectores de la vacunación de los de otras medidas. La evidencia de que la vacunación en anillo con rVSV-ZEBOV-GP mejora el efecto protector de las otras medidas se proporciona mediante la comparación de los vacunados en los anillos del este de la República Democrática del Congo con los miembros de los anillos de control en el ensayo aleatorizado por grupos de Guinea de 2015, en el que la vacunación se había pospuesto durante 21 días, pero los procedimientos para la formación del anillo y las medidas distintas de la vacunación habían sido similares a los utilizados en la República Democrática del Congo. Además, los síntomas en el tercer día de seguimiento que eran compatibles con una infección sistémica por vacuna se asociaron con una incidencia posterior ligeramente menor de EVE.La eficacia de la vacuna puede ser más fuerte contra la EVE mortal que contra la EVE no mortal, como se informó en un análisis de cohorte retrospectivo de pacientes que fueron hospitalizados durante el brote de 2018-2020 en el que los vacunados tuvieron una tasa de letalidad más baja que los no vacunados. 11 Los registros de vacunación más detallados en nuestro estudio actual proporcionan evidencia confirmatoria de una tasa de letalidad más baja entre los vacunados que entre los no vacunados y muestran una tasa de letalidad que es incluso más baja para los casos de EVE que se diagnosticaron 10 días o más después de la vacunación. En un ensayo controlado aleatorizado de terapias para la EVE entre pacientes hospitalizados, los investigadores encontraron que la tasa de letalidad podría reducirse con el uso apropiado de anticuerpos monoclonales. 12 Esos hallazgos aumentan la plausibilidad de que la vacunación no solo protegió contra la aparición de la EVE, sino que también redujo la tasa de letalidad. Durante todo el estudio se vacunó a niños y en la última parte del mismo se incluyeron bebés mayores de 6 meses, mujeres en período de lactancia y mujeres en el segundo o tercer trimestre del embarazo. Aunque nuestro estudio no incluyó un grupo de comparación controlado con placebo, no se observaron efectos secundarios graves. La vacuna rVSV-ZEBOV-GP que se utilizó en este brote ha sido precalificada por la OMS y aprobada para su uso en la Unión Europea, los Estados Unidos y varios países africanos.

La necesidad clave en un brote es la identificación rápida y confiable de los casos y la vacunación de los contactos. Los resultados de nuestro análisis de los anillos de contagio sugieren que la vacunación de los contactos de los contactos de los casos (aunque útil si las circunstancias operativas lo permiten) sería menos importante que centrarse en los contactos inmediatos. Además, la sorprendente diferencia en las tasas de aparición de la EVE entre los clasificados como contactos y los clasificados como contactos de contactos muestra que la identificación confiable de los contactos fue posible incluso en las difíciles condiciones de campo encontradas en el este de la República Democrática del Congo. Entre los vacunados, los trabajadores de la salud y los trabajadores de primera línea que no eran contactos ni contactos de contactos tenían un riesgo a corto plazo aún menor que los contactos de contactos y tendrían un riesgo a largo plazo aún menor en un brote que se hubiera controlado más rápidamente que los brotes de África occidental o el este de la República Democrática del Congo. Los contactos de tercer nivel que fueron vacunados tenían un riesgo muy bajo.
La integración de la investigación en la respuesta al brote de la República Democrática del Congo de 2018-2020 identificó tratamientos efectivos para pacientes hospitalizados y ha facilitado una mayor evaluación de la seguridad y eficacia de las vacunas, al tiempo que ayudó a controlar la transmisión de la enfermedad.
Este estudio ha demostrado la viabilidad de implementar la vacunación en anillo en un contexto de brote en combinación con las medidas tradicionales de control del ébola. La vacunación en anillo es eficaz, eficiente desde el punto de vista operativo y ahorra dosis en comparación con la vacunación de la población, y es factible para los equipos que operan en contextos inseguros.