jor Wissam Ghusn1,2,Jana Zeineddine3,Richard S. Betancourt4Aryan GajjarWah Yang5,Andrew G. Robertson6yOmar M. Ghanem4,*
1. Introducción
La diabetes tipo 2 (DM2), un trastorno metabólico crónico caracterizado por hiperglucemia, se ha convertido en una crisis de salud mundial que afecta a más de 500 millones de personas en todo el mundo y representa más del 10 % de la población [
1 ]. La carga de la diabetes es inmensa y contribuye a una morbilidad y mortalidad significativas debido a su asociación con complicaciones como enfermedades cardiovasculares, neuropatía, nefropatía y retinopatía [ 2 , 3 , 4 ]. El control de la diabetes es fundamental para reducir algunos de estos riesgos y mejorar la calidad de vida de millones de personas. Además, la DM2 es particularmente más prevalente en pacientes con obesidad (es decir, IMC > 30 kg/m² ) [ 5 , 6 , 7 ]. La relación entre la obesidad y la DM2 se debe a complejos procesos celulares y fisiológicos, que incluyen cambios en la función de las células β, alteraciones en la biología del tejido adiposo y resistencia a la insulina en múltiples órganos; todos estos procesos pueden mejorar o incluso normalizarse mediante una pérdida de peso suficiente [ 8 ].Entre las diversas opciones de tratamiento, las cirugías metabólicas y bariátricas (CMB) y las terapias bariátricas endoscópicas (TBE) se han consolidado como intervenciones altamente efectivas para lograr una pérdida de peso sostenida y mejorar el control glucémico en pacientes con diabetes tipo 2 [ 9 , 10 , 11 , 12 , 13 , 14 ]. Cabe destacar que las CMB han demostrado resultados notables en la remisión de la diabetes en una amplia población de pacientes, independientemente del IMC preoperatorio [ 12 , 15 ]. Procedimientos como el bypass gástrico en Y de Roux (BPGYR), la gastrectomía en manga (GM) y el cruce duodenal (CD) son particularmente notables por sus profundos efectos en la pérdida de peso y las mejoras metabólicas, incluyendo el potencial de remisión de la diabetes [ 16 ]. Las terapias basadas en la evidencia (TBE), que incluyen dispositivos intragástricos ocupantes de espacio (DIO), terapia de aspiración (TA), dispositivos de anastomosis sin incisión (DAI), dispositivos de aposición tisular (DAT; en particular, la gastroplastia endoscópica en manga [GEM]), derivación duodeno-yeyunal (DDY) y rejuvenecimiento de la mucosa duodenal (RMD), también han demostrado resultados prometedores en cuanto a la pérdida de peso y la remisión de la diabetes [ 17 ]. Sin embargo, se han realizado pocos estudios (por ejemplo, debido a limitaciones metodológicas y tamaños de muestra pequeños) para evaluar el efecto de las TBE en la remisión de la diabetes tipo 2.Comprender los efectos de la cirugía bariátrica mecánica (MBS) y la endotomía endoscópica (EBT) en la diabetes es de suma importancia, dada la creciente prevalencia de la obesidad y la diabetes tipo 2 (DM2) a nivel mundial [
18 , 19 ]. A medida que estos procedimientos se adoptan cada vez más para el manejo de la obesidad y los trastornos metabólicos relacionados, resulta crucial evaluar sus impactos a largo plazo en los resultados de la diabetes. Esta revisión tiene como objetivo proporcionar un resumen exhaustivo del conocimiento actual sobre los efectos de la MBS y la EBT en la diabetes, destacando la importancia de estos procedimientos para mejorar la salud metabólica. Además de resumir la literatura existente, se describirán los factores clave que influyen en la remisión de la diabetes tras estas cirugías, incluyendo parámetros específicos del paciente, como el estado diabético preoperatorio y las puntuaciones de glucosa en sangre. La revisión evaluará cómo estas variables, junto con los factores quirúrgicos/endoscópicos, contribuyen a los resultados de la remisión y al control glucémico a largo plazo.
2. Procedimientos bariátricos: Descripción
2.1. Cirugías bariátricas metabólicas (MBS) ( Tabla 1 )
El bypass gástrico en Y de Roux (RYGB) consiste en la creación de una pequeña bolsa gástrica que se conecta quirúrgicamente directamente al yeyuno, evitando el duodeno (
Figura 1A ) [ 20 , 21 ]. Esta alteración anatómica restringe la ingesta de alimentos al reducir la capacidad del estómago y limita la absorción de nutrientes debido a la porción del intestino delgado que se omite. El RYGB también afecta significativamente la secreción de hormonas intestinales, ya que los alimentos evitan el duodeno y la parte proximal del yeyuno. Esto aumenta notablemente los niveles del péptido similar al glucagón-1 (GLP-1), lo que mejora la sensibilidad a la insulina y favorece el control glucémico ( Tabla 1 ) [ 20 , 22 , 23 ]. Estos efectos combinados dan como resultado mejoras metabólicas sustanciales y una pérdida de peso sostenida [ 17 ].
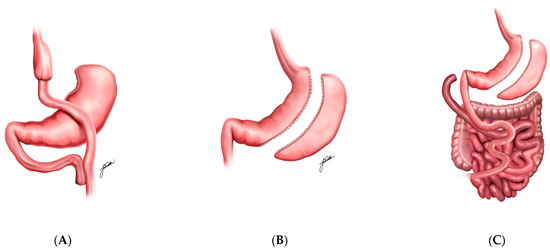
Figura 1. Ilustraciones de bypass gástrico en Y de Roux (
A ), gastrectomía en manga (
B ) y cruce duodenal (
C ).La gastrectomía en manga (GM) consiste en la extirpación quirúrgica de una gran parte del estómago, dejando una estructura estrecha y tubular ( Figura 1B ) [ 24 , 25 ]. Esta reducción del tamaño del estómago restringe la ingesta de alimentos al inducir una sensación de saciedad precoz y también afecta a las hormonas intestinales, en particular al reducir los niveles de grelina, una hormona fundamental para la regulación del hambre [ 26 , 27 ].Además, el procedimiento DS combina elementos de la gastrectomía en manga y el bypass intestinal, proporcionando efectos tanto restrictivos como hipoabsortivos [ 28 , 29 , 30 ]. En este procedimiento, se extirpa una porción del estómago para limitar la ingesta de alimentos, mientras que los intestinos se redirigen para reducir significativamente la absorción de calorías y nutrientes ( Figura 1C ) [ 30 ].
Tabla 1. Mecanismo de acción y resultados de pérdida de peso de los procedimientos bariátricos.
2.2. Terapias Bariátricas Endoscópicas (TBE) ( Tabla 1 )
El balón intragástrico (BIG) es un dispositivo colocado en el estómago que ejerce efectos mecánicos y hormonales que disminuyen la ingesta calórica (
Figura 2A ) [ 31 , 32 ]. Mecánicamente, el BIG ocupa físicamente el espacio gástrico, reduciendo la capacidad del estómago y ralentizando su vaciamiento, lo que prolonga la sensación de saciedad después de las comidas [ 33 , 34 , 35 , 36 , 37 ]. Además, la presencia del BIG se ha asociado con un aumento en la secreción de hormonas como el GLP-1 y el péptido YY (PYY), que potencian aún más las señales de saciedad y reducen el apetito [ 38 ].

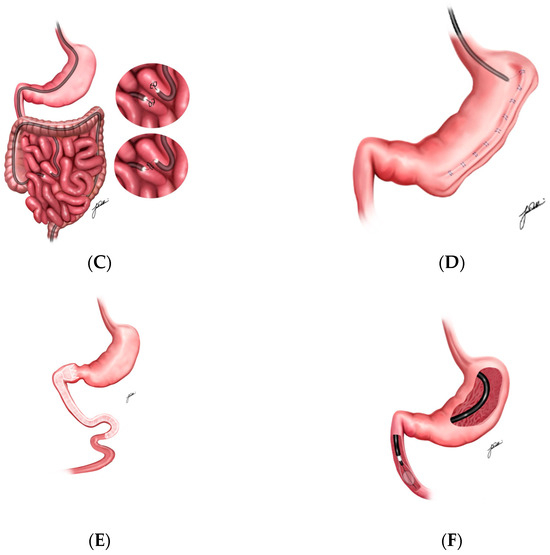
Figura 2. Ilustraciones de balón intragástrico (
A ), terapia de aspiración (
B ), dispositivos de anastomosis sin incisiones (
C ), gastroplastia endoscópica en manga (
D ), revestimiento de derivación duodeno-yeyunal (
E ) y rejuvenecimiento de la mucosa duodenal (
F ).La AT representa un enfoque novedoso para la pérdida de peso, en el que se implanta una sonda de gastrostomía con un sifón en el estómago para permitir la aspiración posprandial del contenido gástrico ( Figura 2B ) [ 39 , 40 , 41 , 42 ]. Al aspirar los alimentos 20 minutos después de una comida, el dispositivo puede eliminar aproximadamente el 30 % de las calorías ingeridas antes de que se absorban. Esta reducción inmediata de calorías se ve reforzada por modificaciones en el comportamiento; se anima a los pacientes a masticar bien los alimentos y a beber más agua con las comidas, lo que fomenta hábitos de alimentación más lentos y una mayor sensación de saciedad [ 43 , 44 , 45 ].Los dispositivos de acceso intraabdominal (DAI) permiten realizar conexiones quirúrgicas sin incisiones tradicionales, creando un bypass que altera el flujo de nutrientes y aumenta la saciedad ( Figura 2C ) [ 44 ]. Esta redirección del tracto digestivo puede reducir la absorción de calorías y nutrientes, lo que favorece la pérdida de peso y la mejora del metabolismo [ 17 , 44 ].Los TAD, incluidas técnicas como la ESG, son terapias bariátricas endoscópicas avanzadas que reducen el volumen gástrico mediante la creación de pliegues tisulares duraderos dentro del estómago [ 46 ] ( Figura 2D ). La ESG, en particular, utiliza suturas para formar una estructura tubular, similar a una manga, lo que restringe significativamente la capacidad del estómago y, por lo tanto, mejora la saciedad temprana con una menor ingesta de alimentos. Esta reducción del volumen gástrico lograda mediante los TAD y la ESG limita eficazmente la ingesta calórica, lo que favorece un control del peso sostenible y una mejor salud metabólica [
17 ].El bypass duodenal (DJBL) evita el duodeno y una porción del yeyuno, facilitando la pérdida de peso mediante mecanismos que incluyen la reducción de la absorción calórica y el aumento de cambios hormonales que regulan el apetito y el metabolismo de la glucosa (
Figura 2E ). Este dispositivo ha mostrado resultados prometedores en estudios, con una pérdida de peso significativa y una mejoría en el control glucémico, incluyendo la remisión de la diabetes en muchos pacientes [
17 ]. Sin embargo, los eventos adversos, como la formación de abscesos hepáticos, exigen una selección y un seguimiento cuidadosos de los pacientes [
17 ].La DMR es una terapia bariátrica endoscópica innovadora que emplea la ablación hidrotermal para rejuvenecer la mucosa duodenal (
Figura 2F ) [
47 ,
48 ,
49 ,
50 ,
51 ]. Este proceso promueve la regeneración de la mucosa, lo que se cree que restablece las vías de señalización normales entre el intestino y el hígado, mejorando así la sensibilidad a la insulina y el control glucémico en pacientes con trastornos metabólicos [
17 ,
47 ,
48 ,
49 ,
50 ,
51 ].
2.3. Procedimientos bariátricos: Pérdida de peso y remisión de la diabetes
En una revisión sistemática y un metaanálisis de ECA, el bypass gástrico en Y de Roux (RYGB) demostró una mayor tasa de remisión de la diabetes durante el primer año en comparación con la gastrectomía en manga (SG), con una tasa de remisión inicial de aproximadamente el 63 % para el RYGB frente al 52 % para la SG, lo que corresponde a un riesgo relativo de 1,21 a favor del RYGB [
52 ]. Sin embargo, durante el seguimiento de 3 a 5 años, las tasas de remisión convergen, y tanto el RYGB como la SG demuestran una eficacia similar para mantener la remisión de la diabetes, con aproximadamente un 50 % de remisión en ambos procedimientos. La mayor pérdida de peso observada con el RYGB, que promedia el 25 % de la pérdida de peso corporal total (PPT) en comparación con el 20 % con la SG, puede contribuir a su superioridad a corto plazo en el control glucémico, mientras que ambos procedimientos ofrecen beneficios duraderos para el control del peso y los resultados glucémicos en la diabetes tipo 2 a largo plazo [
52 ].En otro ensayo clínico aleatorizado (ECA), 60 pacientes con diabetes tipo 2 (DM2) fueron asignados a tratamiento médico, bypass gástrico en Y de Roux (RYGB) o derivación biliopancreática (DB). Tras dos años, la remisión de la diabetes se logró en el 0 % del grupo de tratamiento médico, el 75 % del grupo RYGB y el 95 % del grupo DB (
p < 0,05), según los valores de glucosa en ayunas < 100 mg/dL y HbA1c < 6,5 % sin farmacoterapia [
53 ]. De hecho, múltiples estudios también han demostrado que la DB es la cirugía bariátrica más eficaz para lograr la remisión de la diabetes, con tasas de remisión cercanas al 95 %, sostenidas durante seguimientos a largo plazo [
53 ,
54 ]. El RYGB también demuestra altas tasas de remisión, particularmente durante los dos primeros años, alcanzando entre el 60 % y el 75 % de remisión en pacientes con diagnóstico reciente de diabetes [
53 ,
55 ]. SG muestra tasas de remisión relativamente más bajas, con aproximadamente entre el 23 y el 47 % de remisión reportada al cabo de un año, aunque las tasas tienden a disminuir con el tiempo [
56 ,
57 ].Además, de los tres principales procedimientos de cirugía bariátrica, la derivación biliopancreática (DBP) ha demostrado lograr la mayor pérdida de peso. En un estudio que analizó a 73 702 pacientes de la Base de Datos Longitudinal de Resultados Bariátricos, quienes se sometieron a gastrectomía en manga (GM), DBP o bypass gástrico en Y de Roux (BPGYR), la DBP resultó en una mayor reducción del IMC (5,3 unidades) y el BPGYR (2,2 unidades), en comparación con la GM [
58 ]. En cuanto a la resolución de comorbilidades, el BPGYR fue más eficaz para la enfermedad por reflujo gastroesofágico (ERGE), con una razón de momios (RM) de 1,88, mientras que la DBP mostró mejores resultados para la hipertensión (RM = 2,12) y la diabetes mellitus (RM = 2,53) [
59 ]. La alta eficacia de la DBP se debe a su combinación de mecanismos restrictivos e hipoabsortivos. Sin embargo, su uso está limitado por ser un procedimiento más complejo, por lo que generalmente se reserva para pacientes que requieren intervenciones más agresivas [
60 ,
61 ].Los procedimientos menos invasivos (p. ej., EBT) presentan una menor eficacia en la pérdida de peso general y la remisión de la diabetes en comparación con las intervenciones quirúrgicas. Los EBT ofrecen diversos mecanismos para promover la pérdida de peso. Los balones gástricos implantables (BGI) actúan retrasando el vaciamiento gástrico, aumentando la acomodación gástrica e incrementando la secreción de GLP-1 y PYY. Logran una pérdida de peso total (PPT) de aproximadamente el 5-15 % a los 12 meses, y la mayoría de los dispositivos están diseñados para una colocación de 6 a 12 meses [
17 ]. Los dispositivos de aposición tisular, como la gastrectomía en manga endoluminal (ESG), la cirugía endoluminal primaria de obesidad y la plicatura gástrica endoscópica, promueven la restricción gástrica, reducen la acomodación y aumentan la colecistoquinina, lo que produce una PPT de alrededor del 7-20 % [
17 ,
62 ]. Un metaanálisis en red evaluó la eficacia y seguridad comparativas de los EBT, incluidos ESG y varios IGB, mediante el análisis de ensayos controlados aleatorios hasta mayo de 2023. El estudio encontró que todos los EBT dieron como resultado un %TWL significativamente mayor en comparación con los controles, y ESG y el balón ajustable Spatz3 demostraron un %TWL superior aproximadamente a los 12 meses posteriores al procedimiento en comparación con el balón Orbera®
[ 63
] .AspireAssisst®
, un dispositivo de terapia de aspiración, permite a los pacientes drenar los alimentos no digeridos e incluye modificaciones en el estilo de vida, mostrando una pérdida de peso total (PPT) de alrededor del 15-20 % en 12 meses [
17 ]. Los dispositivos de rejuvenecimiento de la mucosa duodenal, como Revita®
y Diagone®
, tienen mecanismos poco claros y resultados de pérdida de peso limitados. Los dispositivos de anastomosis endoscópica, como el Sistema de Anastomosis Magnética sin Incisión (IMAS®
) , Magnamosis®
y EasyByPass®
, crean anastomosis para facilitar el paso de los alimentos parcialmente digeridos al íleon distal, aumentando la secreción de GLP-1 y PYY; IMAS®
muestra una PPT del 10-15 %, mientras que otros presentan datos limitados [
17 ]. Por último, los revestimientos de derivación duodeno-yeyunal como EndoBarrier®
y ValenTx®
permiten que los nutrientes no digeridos eviten el intestino proximal, lo que conlleva un aumento de GLP-1 y PYY y una pérdida de peso total de entre el 15 % y el 20 %, con una duración de colocación de entre 3 y 12 meses. Cada tipo de dispositivo ofrece un mecanismo y un potencial de pérdida de peso únicos, lo que aporta flexibilidad a la hora de seleccionar el tratamiento específico para cada paciente [
17 ].Los balones intragástricos (BIG), como Orbera®
y el balón Bioenteric®
, han mostrado resultados modestos en la reducción de las comorbilidades relacionadas con la obesidad, incluida la diabetes tipo 2 (DM2). Una serie de casos con 143 pacientes reportó una reducción en la prevalencia de diabetes del 32,6 % al 20,9 % a los seis meses, manteniéndose la incidencia de diabetes baja incluso un año después del tratamiento [
63 ]. El dispositivo AspireAssist®
, una forma de terapia de aspiración, también demostró beneficios en el control de la diabetes en el ensayo PATHWAY, que mostró reducciones significativas en la hemoglobina glucosilada (HbA1c) junto con la pérdida de peso (−0,36 % en comparación con el 5,7 % basal,
p < 0,0001) [
64 ]. El bypass gástrico doble J (DBDJ), que evita el intestino proximal y aumenta la secreción de GLP-1 y PYY, produjo una disminución adicional del 1 % en la HbA1c con respecto a los controles en un metaanálisis con 105 pacientes, lo que sugiere un gran potencial para la remisión de la diabetes [
65 ]. Además, el IMAS®
, diseñado para simular el cruce duodenal, produjo reducciones de HbA1c del 1,9 % en pacientes con diabetes y del 1,0 % en pacientes con prediabetes, si bien los datos sobre la remisión a largo plazo son limitados [
66 ]. Asimismo, en pacientes sometidos a ESG, la HbA1c disminuyó significativamente en la cohorte total, de 6,1 ± 1,1 % a 5,5 ± 0,48 %, y en pacientes con diabetes o prediabetes, de 6,6 ± 1,2 % a 5,6 ± 0,51 %, tras 12 meses [
67 ].
3. Mecanismos subyacentes a la remisión de la diabetes
3.1. Mecanismos dependientes de la pérdida de peso
La restricción calórica en individuos ayuda a reducir la grasa acumulada alrededor de órganos específicos, como el hígado y el páncreas [
68 ]. El exceso de grasa alrededor del páncreas puede alterar la regulación de la glucosa en sangre, provocando picos en sus niveles [
69 ]. Mediante dietas hipocalóricas y la pérdida de peso, los depósitos de grasa en estos órganos disminuyen, lo que resulta en un mejor control glucémico y una regulación más eficaz de la glucosa en sangre [
69 ]. Además, la pérdida de peso derivada de la restricción calórica puede aliviar la presión mecánica sobre los tejidos periféricos, mejorando así la sensibilidad a la insulina en el músculo esquelético, un área clave para la homeostasis general de la glucosa [
70 ]. Diversos estudios han demostrado que las dietas muy bajas en calorías y la restricción calórica pueden mejorar la glucosa en sangre al reducir la toxicidad de la glucosa y los lípidos, disminuir los depósitos de grasa ectópica, aumentar la sensibilidad a la insulina y reducir la inflamación [
71 ]. La acumulación de grasa puede afectar la función de las células β y la liberación de insulina, mientras que el tejido adiposo actúa como un órgano endocrino que produce citocinas proinflamatorias, como TNF-α e IL-6, que alteran la función de la insulina [
72 ].La reducción de la acumulación de grasa alrededor de estos órganos también mejora la eficiencia en la producción de glucosa y el control glucémico. A medida que disminuye la grasa alrededor de los órganos viscerales, mejora la secreción de adipocinas, incluida la adiponectina, mientras que las citocinas proinflamatorias, como el TNF-α y la IL-6, disminuyen [
72 ]. Además, la reducción de peso mediante la restricción calórica o la cirugía bariátrica disminuye la producción de estas citocinas, lo que aumenta la sensibilidad a la insulina. La reducción de los niveles de citocinas, junto con marcadores inflamatorios como la proteína C reactiva, resalta el papel de la pérdida de peso en la remisión de la diabetes a través de la mejora de la absorción de glucosa y la función de la insulina [
73 ].Además, la resistencia hepática a la insulina debida a la infiltración grasa del hígado puede exacerbar la hiperglucemia. La cirugía bariátrica ayuda a reducir la producción hepática de glucosa y a disminuir los niveles de glucosa endógena [
74 ]. Asimismo, las intervenciones bariátricas reducen los niveles de ácidos grasos libres (AGL) y de tejido adiposo; los altos niveles de AGL pueden alterar la señalización de la insulina, impedir la supresión hepática de la glucosa y reducir la absorción de glucosa en los músculos, lo que conduce a la hiperglucemia [
75 ]. La pérdida de peso, lograda mediante la cirugía bariátrica, disminuye los ácidos grasos y la lipotoxicidad, mejorando la sensibilidad a la insulina y permitiendo a los pacientes alcanzar niveles estables de glucosa y una mejor función de la insulina [
76 ].
3.2. Mecanismos independientes de la pérdida de peso
Diversos procedimientos endoscópicos y bariátricos pueden influir en las hormonas intestinales, contribuyendo a la remisión de la diabetes. Estos procedimientos suelen aumentar los niveles de GLP-1 y PYY, hormonas similares al glucagón, esenciales para la regulación del apetito y el metabolismo de la glucosa. Por ejemplo, el bypass gástrico en Y de Roux (RYGB) y la gastrectomía en manga (SG) aumentan los niveles de GLP-1 y PYY, promoviendo la saciedad, retrasando el vaciamiento gástrico, incrementando la secreción de insulina y disminuyendo la producción de glucagón, lo que mejora el control glucémico incluso sin una pérdida de peso significativa [
77 ,
78 ,
79 ,
80 ,
81 ]. Además, estos procedimientos reducen la grelina, la «hormona del hambre», mediante la resección de parte del estómago donde se produce, disminuyendo así el apetito [
22 ].Los ácidos biliares desempeñan un papel crucial en el metabolismo de la glucosa como moléculas de señalización que activan receptores como TGR5 y FXR. Tras la cirugía bariátrica, el aumento de los niveles de ácidos biliares en el torrente sanguíneo estimula TGR5, lo que incrementa la secreción de GLP-1, una hormona que favorece la secreción adecuada de insulina y la regulación de la glucosa en sangre [
82 ,
83 ]. FXR, activado por los ácidos biliares en el hígado y los intestinos, ayuda a reducir la producción hepática de glucosa y a aumentar la sensibilidad a la insulina, contribuyendo así a la homeostasis de la glucosa [
83 ]. Además, la alteración de la circulación de ácidos biliares tras la cirugía afecta al eje intestino-hígado, mejorando el control metabólico al modular la sensibilidad a la insulina y los niveles de glucosa independientemente de la pérdida de peso [
84 ]. Diversos estudios han demostrado que estos cambios en el metabolismo de los ácidos biliares tras procedimientos como el bypass gástrico en Y de Roux (RYGB) pueden mejorar la sensibilidad a la insulina y la función de las células β, ambas esenciales para el control glucémico a largo plazo [
84 ].Los cambios en la composición de la microbiota intestinal también contribuyen a las mejoras metabólicas. La obesidad y la diabetes tipo 2 se asocian con una menor diversidad microbiana, pero los procedimientos quirúrgicos pueden aumentar bacterias beneficiosas como Akkermansia muciniphila y especies de Bifidobacterium, que reducen la inflamación, fortalecen la barrera intestinal y mejoran la sensibilidad a la insulina [
85 ,
86 ,
87 ]. Estos cambios microbianos dan lugar a una mayor producción de ácidos grasos de cadena corta (AGCC), como el butirato, que favorece la salud intestinal, reduce la inflamación sistémica y promueve la regulación de la glucosa [
88 ]. El eje intestino-cerebro también desempeña un papel importante, ya que la dieta, los medicamentos y la cirugía influyen en la microbiota intestinal, afectando el apetito, la regulación hormonal y la sensibilidad a la insulina independientemente de la pérdida de peso [
87 ,
89 ].
4. Factores predictivos de la remisión de la diabetes
Las características preoperatorias del paciente, como la duración de la enfermedad, la glucosa en ayunas, el uso de insulina, la HbA1c y los niveles de péptido C, se evalúan comúnmente para comprender la progresión de la DM2 [
90 ,
91 ].Una mayor duración de la enfermedad se asocia sistemáticamente con menores tasas de remisión, ya que la exposición prolongada a la hiperglucemia y la resistencia a la insulina puede provocar una disfunción irreversible de las células beta pancreáticas, lo que dificulta la reversión de la diabetes [
92 ]. Además, la presencia de complicaciones vasculares, tanto microvasculares como macrovasculares, refleja una mayor gravedad de la diabetes y reduce aún más la probabilidad de remisión; un estudio observó una razón de momios (RM) de 2,72 para lograr la remisión en pacientes sin complicaciones vasculares en comparación con aquellos que sí las presentaban [
93 ]. El uso preoperatorio de insulina también predice negativamente la remisión, ya que la dependencia de la insulina indica una etapa más avanzada de la enfermedad y una menor capacidad de producción endógena de insulina. Esto disminuye las probabilidades de lograr un control glucémico sostenido después de la cirugía [
94 ]. Asimismo, la dosis de insulina es un factor crítico; los pacientes que reciben dosis más altas de insulina experimentan tasas de remisión significativamente menores, lo que subraya el impacto dosis-dependiente de la insulina en los resultados de la remisión de la diabetes [
91 ].La sensibilidad a la insulina, la resistencia a la insulina y la función de las células beta influyen significativamente en la progresión de la diabetes tipo 2 (DM2) y la respuesta al tratamiento. Un estudio demostró que la cirugía bariátrica mejoró la sensibilidad a la insulina, redujo la resistencia a la insulina (medida mediante el índice HOMA-IR) y aumentó la capacidad compensatoria de las células beta (medida mediante el Índice de Disposición [ID]) en pacientes con y sin DM2. Los pacientes con un ID preoperatorio menor mostraron una menor mejoría en la sensibilidad a la glucosa de las células beta y en la secreción de insulina, lo que se tradujo en menores tasas de remisión a los 4 y 18 meses (0 % de remisión en el grupo con ID bajo frente al 57 % en el grupo con ID alto a los 4 meses; 38 % en el grupo con ID bajo frente al 71 % en el grupo con ID alto a los 18 meses) [
95 ]. Sin embargo, otro estudio halló que el índice HOMA-IR no fue un predictor significativo de la remisión de la DM2 (
p = 0,961) [
96 ]. Si bien estas métricas aportan información sobre los efectos de la cirugía bariátrica en la respuesta a la insulina y la función de las células beta, su utilidad para predecir los resultados quirúrgicos aún se encuentra en investigación.Para tener en cuenta la variabilidad entre los predictores, se han desarrollado sistemas de puntuación que ayudan a pronosticar la remisión de la diabetes tras la cirugía bariátrica. La puntuación de Cirugía Metabólica Individualizada (IMS), DiaRem, DiaRem avanzada (ad-DiaRem), ABCD y la puntuación de Robert et al. incorporan combinaciones de predictores como la duración de la diabetes, la HbA1c y el uso de insulina [
97 ]. Los componentes de la puntuación IMS incluyen la duración de la diabetes, el número de medicamentos para la diabetes, el uso de insulina y la HbA1c. Las puntuaciones se dividen en tres categorías: leve (≤25), moderada (26-95) y grave (>95), donde una puntuación más alta indica una enfermedad más grave [
97 ]. Los hallazgos son consistentes incluso en pacientes con obesidad grave (es decir, IMC > 50 kg/m²
) , con un AUC-ROC de 0,79 [
91 ]. En un análisis retrospectivo de 20 pacientes con diabetes tipo 2 sometidos a gastrectomía en manga, aquellos con puntuaciones más altas en la Escala de Gravedad de la Diabetes (IMS), indicativas de una enfermedad más grave, presentaron una probabilidad significativamente menor de alcanzar la remisión diabética (RD), con tasas de remisión del 60 % en la categoría leve, del 45,5 % en la moderada y del 0 % en la grave. Estos hallazgos sugieren que la puntuación IMS podría ser un predictor útil de los resultados de la RD tras la gastrectomía en manga, lo que permitiría planificar un tratamiento individualizado para la obesidad y la diabetes [
98 ].Además, la puntuación DiaRem oscila entre 0 y 22 e incorpora la HbA1c, el uso de insulina, la edad y otros medicamentos para la diabetes en su sistema de puntuación [
99 ]. La puntuación ad-DiaRem oscila entre 0 y 21 y, además de los componentes de DiaRem, incorpora varios medicamentos para la diabetes y la duración de la enfermedad [
100 ]. En ambos sistemas de puntuación, una puntuación más baja se asocia con una mayor probabilidad de remisión de la diabetes tipo 2.El modelo ABCD es un sistema de puntuación desarrollado para predecir la remisión de la diabetes tras la cirugía bariátrica mediante la evaluación de factores críticos relacionados con las características del paciente y su estado diabético. Este modelo incluye cuatro componentes principales: edad, IMC, niveles de péptido C y duración de la diabetes (de ahí el nombre «ABCD»). La edad se incluye porque los pacientes más jóvenes tienden a tener mejores resultados de remisión, mientras que el IMC tiene en cuenta la gravedad de la obesidad, que influye en la mejoría de la diabetes [
101 ]. Como se mencionó anteriormente, los niveles de péptido C indican la producción endógena de insulina y la función de las células beta; por lo general, los niveles más altos predicen un mayor potencial de remisión. Asimismo, la duración de la diabetes refleja la progresión de la enfermedad: las duraciones más cortas se asocian con una mayor probabilidad de remisión debido a un menor agotamiento de las células beta.La puntuación de Robert et al. combina factores como el IMC, la duración de la diabetes, la HbA1c, la glucosa en ayunas y el uso de insulina en un sistema de puntuación de 0 a 5, donde las puntuaciones más altas se correlacionan con una mayor probabilidad de remisión de la diabetes [
102 ]. Sin embargo, su eficacia para predecir la remisión puede ser limitada en pacientes sometidos a gastrectomía en manga (GM) [
91 ]. Un estudio demostró un área bajo la curva ROC (AUC-ROC) global de 0,75, sin diferencias significativas entre los subgrupos de procedimientos, aunque las tasas de remisión fueron notablemente superiores para el bypass gástrico en Y de Roux (BPGYR) en comparación con la GM en puntuaciones específicas: 68 % frente a 38 % para una puntuación de 3, 77 % frente a 50 % para una puntuación de 4 y 100 % frente a 71 % para una puntuación de 5 [
90 ].Además de resaltar la asociación entre la gravedad de la diabetes y la remisión de la diabetes tipo 2 (DM2), es fundamental subrayar la importancia de recomendar la cirugía bariátrica (MBS) de forma temprana, especialmente en pacientes con obesidad y DM2. La intervención quirúrgica precoz, incluso antes del desarrollo de obesidad grave o diabetes avanzada, puede maximizar las probabilidades de remisión al preservar la función de las células beta pancreáticas y mitigar los efectos nocivos de la hiperglucemia crónica [
92 ]. Por ejemplo, la evidencia también sugiere que los pacientes con una puntuación IMS más baja y una diabetes menos grave presentan tasas de remisión significativamente mejores [
93 ]. Asimismo, los pacientes que aún no han desarrollado enfermedades vasculares relacionadas con la DM2 tienen tasas de remisión de la diabetes más altas en comparación con los pacientes con complicaciones vasculares [
103 ]. Al priorizar la MBS en esta población, se pueden optimizar los resultados metabólicos y glucémicos a largo plazo, a la vez que se reduce la carga de las complicaciones relacionadas con la diabetes.
5. Limitaciones
Esta revisión narrativa presenta varias limitaciones que deben tenerse en cuenta. En primer lugar, la heterogeneidad de los estudios incluidos en cuanto a poblaciones, metodologías y duración del seguimiento puede afectar la generalización de los resultados. En segundo lugar, si bien el análisis destaca la eficacia tanto de la cirugía bariátrica como de la terapia endoscópica de la diabetes en la remisión de la diabetes, las comparaciones directas entre estas intervenciones siguen siendo limitadas. En tercer lugar, la dependencia de sistemas de puntuación predictivos, como IMS y DiaRem, puede no tener en cuenta todas las variables específicas del paciente que influyen en los resultados de la remisión. Por último, la falta de datos de seguimiento a largo plazo para las terapias endoscópicas limita la capacidad de evaluar la durabilidad de sus efectos en comparación con las intervenciones quirúrgicas establecidas. Se necesitan futuros estudios prospectivos con diseños estandarizados y evaluaciones de resultados a largo plazo para validar y ampliar estos hallazgos.
6. Conclusiones
Esta revisión subraya el valor de la estimulación magnética funcional (EMF) y las terapias basadas en la evidencia (TBE) como intervenciones eficaces para lograr la remisión de la diabetes tipo 2 (DM2), especialmente en pacientes con obesidad que presentan un mayor riesgo de complicaciones relacionadas con la diabetes. Mediante un análisis exhaustivo de factores predictivos, como la duración de la diabetes, la HbA1c, los niveles de péptido C y el uso de insulina, este estudio destaca cómo las características específicas de cada paciente pueden influir en los resultados de la remisión. Sistemas de puntuación como el IMS, DiaRem, Advanced-DiaRem, ABCD y el de Robert et al. proporcionan marcos valiosos para identificar a los candidatos con mayor probabilidad de beneficiarse de estas intervenciones, lo que permite una planificación del tratamiento personalizada que mejora el potencial de remisión de la diabetes. Dada la evidencia que respalda mejores resultados de remisión de la diabetes con EMF y TBE tanto en pacientes jóvenes como en aquellos con diabetes de menor duración, esta revisión apoya un mayor acceso temprano a la EMF y a estas terapias para que los pacientes tengan la oportunidad de lograr un resultado exitoso en su tratamiento.Las investigaciones futuras deberían centrarse en perfeccionar estos modelos predictivos en diversas poblaciones de pacientes y en explorar con mayor profundidad los efectos metabólicos a largo plazo de la MBS y la EBT para optimizar los resultados. Al adecuar las características de los pacientes a las intervenciones adecuadas, los profesionales sanitarios pueden abordar mejor la carga mundial de la diabetes tipo 2, mejorando así la calidad de vida de los pacientes y reduciendo los costes sanitarios asociados al tratamiento de la diabetes.