Autores : Heribert Schunkert , MD , Pradeep Natarajan , MD y Nilesh J. Samani , MD 4 de febrero de 2026
N Engl J Med 2026 ; 394 : 576 – 587 DOI: 10.1056/NEJMra240515
Resumen
Las investigaciones sobre la base genética de la enfermedad coronaria han impulsado avances significativos en el conocimiento de los mecanismos subyacentes, la terapéutica, la prevención y la predicción del riesgo. De hecho, la mayoría de los medicamentos actuales para la enfermedad coronaria se dirigen a las vías que promueven la aterosclerosis debido a mecanismos genéticos subyacentes complejos que se han identificado a lo largo de los años. Las causas monogénicas de la enfermedad coronaria se presentan en aproximadamente 1 de cada 250 personas y, en su mayoría, resultan en niveles de lípidos significativamente elevados, lo que subraya la importancia de identificar a los individuos en riesgo. A nivel poblacional, cientos de variantes comunes con tamaños de efecto pequeños, que pueden estar presentes en la mayoría de la población, tienen una influencia aún mayor en la predisposición a desarrollar esta condición. Estas variantes genómicas pueden combinarse en puntuaciones de riesgo poligénico, las cuales representan el riesgo genético de una persona en relación con el promedio de la población general. El riesgo entre las personas del 5% superior es de 3 a 5 veces mayor que entre las personas con una puntuación promedio; el riesgo relativo derivado de la puntuación de riesgo poligénico puede utilizarse para multiplicar el riesgo absoluto derivado de una puntuación de riesgo clínico, ofreciendo así un enfoque más personalizado en la evaluación del riesgo cardiovascular. Aún quedan preguntas clave sobre el valor clínico, la rentabilidad y las estrategias de implementación necesarias para integrar las puntuaciones de riesgo poligénico de la enfermedad coronaria en la práctica clínica, lo que podría revolucionar la forma en que los médicos abordan la prevención y el tratamiento de esta enfermedad prevalente en la sociedad actual.
En consecuencia, es fundamental llevar a cabo más estudios que permitan comprender completamente las implicaciones de estas investigaciones y su potencial para transformar nuestras estrategias de salud pública.
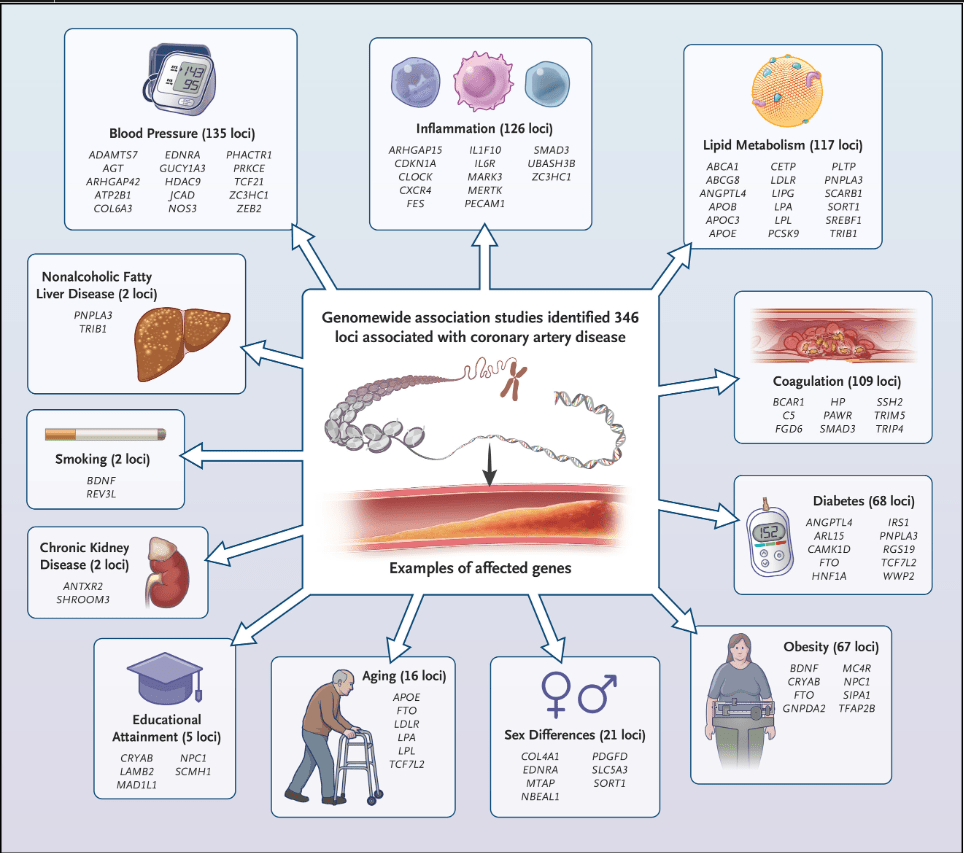
Loci genómicos asociados con la enfermedad arterial coronaria.Los estudios de asociación del genoma completo han mostrado 346 loci genómicos con asociaciones significativas con la enfermedad de la arteria coronaria. 4-7 La figura muestra, para algunos de estos loci, los genes causales que también se han encontrado significativamente asociados con factores de riesgo establecidos, modificadores de riesgo y condiciones clínicas relacionadas con la enfermedad. El número total de loci con señales de todo el genoma tanto para la enfermedad de la arteria coronaria como para los rasgos respectivos se muestra entre paréntesis (algunos loci están significativamente asociados con varios rasgos). Un total de 76 loci de riesgo no tienen asociación con estos rasgos; los mecanismos subyacentes a las respectivas asociaciones con la enfermedad de la arteria coronaria aún están por descubrirse. Los 346 genes candidatos, o, para los loci con genes candidatos inciertos, los polimorfismos de un solo nucleótido principales, se muestran en el gráfico interactivo.
Se puede encontrar información adicional en el Apéndice complementario , disponible con el texto completo de este artículo en NEJM.org.
La enfermedad coronaria se desarrolla a partir de una interacción de factores conductuales, ambientales, genéticos y aleatorios. El tabaquismo, la hipertensión, la hiperlipidemia y la diabetes mellitus son factores de riesgo modificables bien reconocidos para la enfermedad coronaria, que afecta a casi 1 de cada 2 hombres y 1 de cada 3 mujeres a lo largo de su vida.<sup> 1 </sup> Hace más de un siglo, Osler postuló que los factores hereditarios podrían causar enfermedad coronaria tras observar que la angina de pecho suele agruparse en familias.<sup> 2</sup> Hace aproximadamente 30 años, estudios en gemelos indicaron que la heredabilidad de la enfermedad coronaria mortal alcanzaba el 50 %.<sup> 3 </sup> Desde 2007, estudios a gran escala de genotipado y secuenciación genética han identificado cientos de variantes genéticas asociadas con una mayor susceptibilidad a la enfermedad coronaria ( Figura 1 y gráfico interactivo ). Los productos proteicos de algunos genes asociados ya constituyen dianas terapéuticas eficaces, y otros genes apuntan a mecanismos de la enfermedad aún inexplorados
La indagación sobre antecedentes familiares de enfermedad arterial coronaria es rutinaria en la evaluación clínica de pacientes con síndromes de dolor torácico. En este artículo, revisamos los descubrimientos recientes sobre el origen genético molecular de la aterosclerosis coronaria y analizamos los usos clínicos actuales y potenciales de esta información.
Formas monogénicas de la enfermedad arterial coronaria
La causa genética molecular arquetípica de la enfermedad arterial coronaria es la hipercolesterolemia familiar, una afección monogénica incompletamente dominante.<sup> 10 </sup> Fue descrita por primera vez por Müller en 1938 y se mantuvo como la única causa genética comprobada de enfermedad arterial coronaria durante aproximadamente 70 años.<sup> 11</sup> La hipercolesterolemia familiar se presenta en aproximadamente 4 de cada 1000 personas heterocigotas para la enfermedad y en aproximadamente 1 de cada 200 000 personas homocigotas para la enfermedad. A mediados de los cuarenta, aproximadamente el 20 % de las personas con hipercolesterolemia familiar heterocigota presentan afecciones ateroscleróticas.<sup> 12</sup> Las variantes genéticas causantes de la hipercolesterolemia familiar suelen provocar una disminución de la función del receptor de lipoproteínas de baja densidad (LDL),<sup> 10 </sup> una función alterada de la apolipoproteína B o un aumento de la función de la proproteína convertasa subtilisina/kexina tipo 9 (PCSK9).<sup>
Puntos clave
La base hereditaria de la enfermedad coronaria
•Las variantes raras de pérdida de función con grandes efectos han implicado directamente a genes específicos como objetivos terapéuticos, lo que ha proporcionado una fuerte validación genética humana para el desarrollo de fármacos.
•Los estudios de asociación del genoma muestran que las variantes genéticas comunes representan una proporción sustancial del riesgo hereditario de enfermedad de la arteria coronaria.
•Las variantes asociadas con el riesgo de enfermedad coronaria manifiestan efectos en diversos órganos y tejidos. Muchas de estas variantes median el riesgo a través de vías que se sabe que son fundamentales para el desarrollo de la enfermedad coronaria, pero el mecanismo subyacente de varias variantes aún se desconoce.
•Los datos de asociación genética han permitido realizar estudios de inferencia causal a través de la aleatorización mendeliana, que proporciona un marco para distinguir los factores de riesgo causales de los marcadores de riesgo correlacionados para la enfermedad de la arteria coronaria.
•Las puntuaciones de riesgo poligénico integran los efectos acumulativos de variantes comunes en una única medida de riesgo de enfermedad coronaria hereditaria, con una distribución poblacional continua y un marcado enriquecimiento de eventos en los extremos superiores.
•Las puntuaciones de riesgo poligénico brindan información en gran medida independiente de los factores de riesgo clínicos convencionales, incluidos los antecedentes familiares, y refinan la estratificación del riesgo tanto para la enfermedad coronaria incidente como para la recurrente.
•Aunque los alelos de riesgo genético se fijan en la concepción, sus consecuencias clínicas son modificables, y hay evidencia de que las intervenciones en el estilo de vida y la terapia para reducir los lípidos pueden atenuar el riesgo entre personas con puntajes altos de riesgo poligénico, en particular cuando se aplican de manera temprana.
•No hay consenso sobre el uso clínico de la puntuación de riesgo poligénico para la enfermedad de la arteria coronaria, y aún quedan dudas sobre su solidez entre poblaciones, su valor incremental, su relación coste-efectividad y su implementación.Se sospecha hipercolesterolemia familiar cuando los niveles de colesterol LDL están muy elevados (en adultos, >190 mg por decilitro [4,9 mmol por litro]; en niños, >150 mg por decilitro [3,9 mmol por litro]). La sospecha clínica es especialmente fuerte cuando estas elevaciones se presentan junto con antecedentes personales o familiares de enfermedad coronaria prematura, xantelasma o xantomas tendinosos; estos trastornos son los que tienen mayor peso, después de los niveles muy elevados de colesterol LDL, en los sistemas de puntuación clínica para la hipercolesterolemia familiar.<sup> 13 </sup> La prevalencia de variantes patógenas es de aproximadamente el 0,4 % en la población general y de aproximadamente el 3,5 % en personas con niveles de colesterol LDL superiores a 190 mg por decilitro.<sup> 14,15</sup> Entre las personas en quienes los hallazgos adicionales sugieren hipercolesterolemia familiar probable o definitiva, se detectan variantes en el 5 % y el 24 %, respectivamente.<sup> 15</sup>Establecer el diagnóstico genético molecular de la hipercolesterolemia familiar tiene implicaciones, ya que incluso con niveles similares de colesterol LDL, las personas con una variante definitoria de hipercolesterolemia familiar tienen un riesgo de enfermedad coronaria de 2 a 3 veces mayor que entre las personas que no presentan dicha variante. 14,15 Además, el beneficio de la reducción del colesterol LDL es aún mayor en personas con hipercolesterolemia familiar genéticamente probada . 16 Este beneficio se refleja en las directrices de la sociedad que recomiendan objetivos de LDL más bajos que los de prevención primaria en pacientes con hipercolesterolemia no familiar. 13 Desafortunadamente, la evaluación genética de la hipercolesterolemia familiar está infrautilizada en todo el mundo, lo que resulta en oportunidades perdidas para implementar el cribado en cascada recomendado por las directrices en familiares de primer grado. Actualmente se está analizando el cribado poblacional de la hipercolesterolemia familiar en niños para mitigar el riesgo de enfermedad coronaria mediante un tratamiento preventivo temprano. 17,18
Otras formas monogénicas de enfermedad de la arteria coronaria son muy raras y representan solo una pequeña fracción de la alta prevalencia general de la enfermedad. Las afecciones autosómicas recesivas, como la hipercolesterolemia autosómica recesiva (causada por variantes en LDLRAP1 ), 19 la sitosterolemia ( ABCG5 y ABCG8 ), 20 y el pseudoxantoma elástico ( ABCC6 ), 21 a menudo se asocian con enfermedad de la arteria coronaria prematura. Las variantes raras en genes involucrados en la vía del óxido nítrico ( GUCY1A1 y PDE5A ), 22,24 la regulación de triglicéridos ( APOA5 ), 23 y el transporte de colesterol ( SCARB1 ) 25 también se han relacionado con enfermedad de la arteria coronaria prematura. Las variantes clínicamente significativas en estos genes podrían considerarse en paneles expandidos para la evaluación genética molecular, junto con las variantes en los genes habituales asociados con la hipercolesterolemia familiar: LDLR , APOB y PCSK9 .
Contribución poligénica a la enfermedad arterial coronaria
Mientras que las variantes dañinas raras, como las del gen LDLR , pueden perjudicar gravemente la salud de las personas afectadas, los alelos de riesgo comunes con efectos leves parecen ser más relevantes a nivel poblacional. En la década de 1950, Platt y Pickering debatieron si la hipertensión se hereda de forma monogénica o poligénica. Posteriormente, la modelización matemática indicó que la presencia de múltiples alelos de riesgo comunes con efectos leves da lugar a más casos de hipertensión que las variantes raras con efectos fuertes.
26Los estudios de asociación de todo el genoma de la enfermedad de la arteria coronaria han validado esta hipótesis.
27,28 Las matrices de genotipado evalúan alelos de cientos de miles de polimorfismos de un solo nucleótido (SNP) en paralelo y, combinados con SNP no genotipados imputados estadísticamente, permiten un genotipado eficiente de todo el genoma de variantes comunes. Los estudios de asociación de todo el genoma comparan las frecuencias alélicas de cada SNP entre personas afectadas y no afectadas. Para tener en cuenta las pruebas múltiples, un valor P estricto inferior a 5 × 10 −8 establece la significancia de todo el genoma.
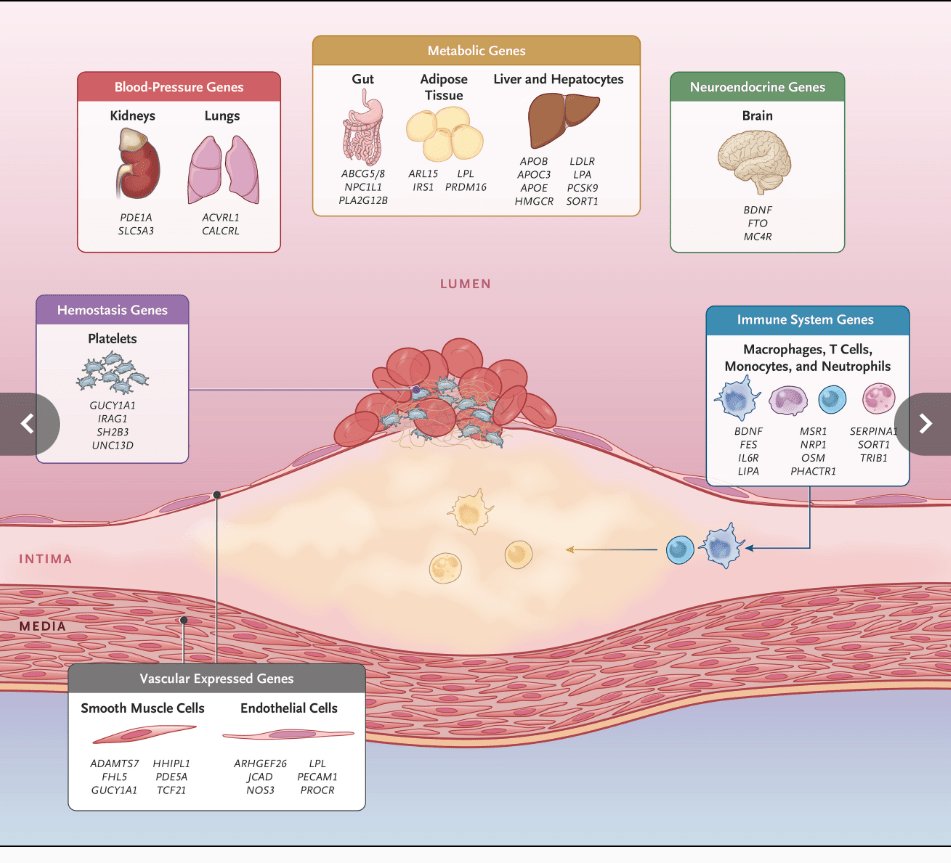
Los últimos metaanálisis de estudios de asociación de todo el genoma incluyeron más de 180 000 personas con enfermedad de la arteria coronaria y más de 1 millón de personas en total, 4,5,29 lo que arrojó 346 regiones de riesgo de significancia de todo el genoma, también conocidas como loci ( Figura 1 y gráfico interactivo ). 6 Se predice que existen muchas más variantes asociadas. Específicamente, los alelos de riesgo con frecuencias más bajas, 6 frecuencias marcadamente variadas a nivel mundial o tamaños de efecto más pequeños requerirán la identificación de cohortes aún más grandes y diversas. 4,29 Los estudios de secuenciación a gran escala pueden ayudar a llenar este vacío. Es notable que estas alteraciones genéticas afecten a genes que se expresan en un amplio espectro de tejidos y tipos de células, lo que contribuye conjuntamente a la susceptibilidad de las personas a la enfermedad de la arteria coronaria ( Figura 2 ). Los hallazgos que han surgido de estos esfuerzos de descubrimiento se están aplicando en dos áreas clave: la predicción del riesgo cardiovascular y el avance de los desarrollos terapéuticos.
Predicción del riesgo cardiovascular
Evaluación de riesgos clínicos
Se recomienda el cálculo de puntajes de riesgo que integren factores clínicos para personas sin enfermedad coronaria conocida con el fin de identificar a aquellos que tienen un riesgo suficientemente mayor de eventos cardiovasculares ateroscleróticos como para merecer terapias preventivas. 35,36 Estas estimaciones de riesgo están fuertemente influenciadas por la edad cronológica, lo que resulta en una menor probabilidad de identificar a personas más jóvenes con alto riesgo. 35,36 A pesar del reconocimiento de antecedentes familiares de enfermedad coronaria como un factor de riesgo importante, esta información no se incluye en los puntajes de riesgo clínico actuales porque no proporciona suficiente discriminación adicional.
Evaluación de riesgo poligénico
Los pequeños tamaños de efecto de los alelos de riesgo de enfermedad coronaria no son útiles individualmente para la predicción. Sin embargo, la información agregada en una puntuación de riesgo poligénico ofrece la oportunidad de refinar la predicción del riesgo.
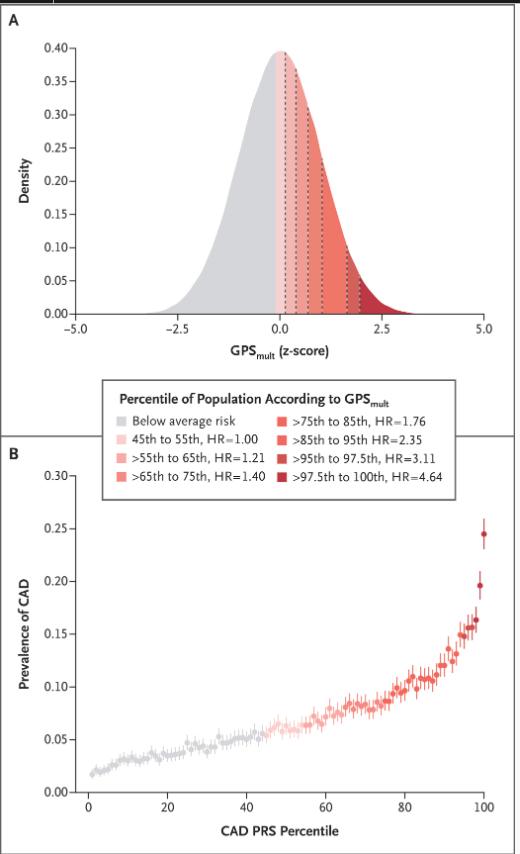
La herencia independiente de los numerosos alelos de riesgo comunes da como resultado una distribución gaussiana de la puntuación de riesgo poligénico para la enfermedad arterial coronaria en la población general ( Figura 3A ). El riesgo para las personas en el 5% superior de la distribución es de 3 a 5 veces mayor que el de las personas en los quintiles medios de la población (Fig. 3B) 37, un hallazgo que es independiente del estado con respecto a los antecedentes familiares de enfermedad arterial coronaria. 38 Dado que las variantes con significancia genómica ( Figura 1 y gráfico interactivo ) representan solo una pequeña fracción del número real de variantes asociadas con una enfermedad, la puntuación de riesgo poligénico actual incluye todas las variantes genéticas informativas, cada una con pequeñas asociaciones con la enfermedad coronaria o el ictus, para predecir la predisposición genética completa. Gracias a estudios de asociación genómica cada vez más amplios y diversos y a nuevos métodos, el rendimiento de las sucesivas puntuaciones de riesgo poligénico continúa mejorando. 39
Evaluación combinada de riesgos clínicos y poligénicos
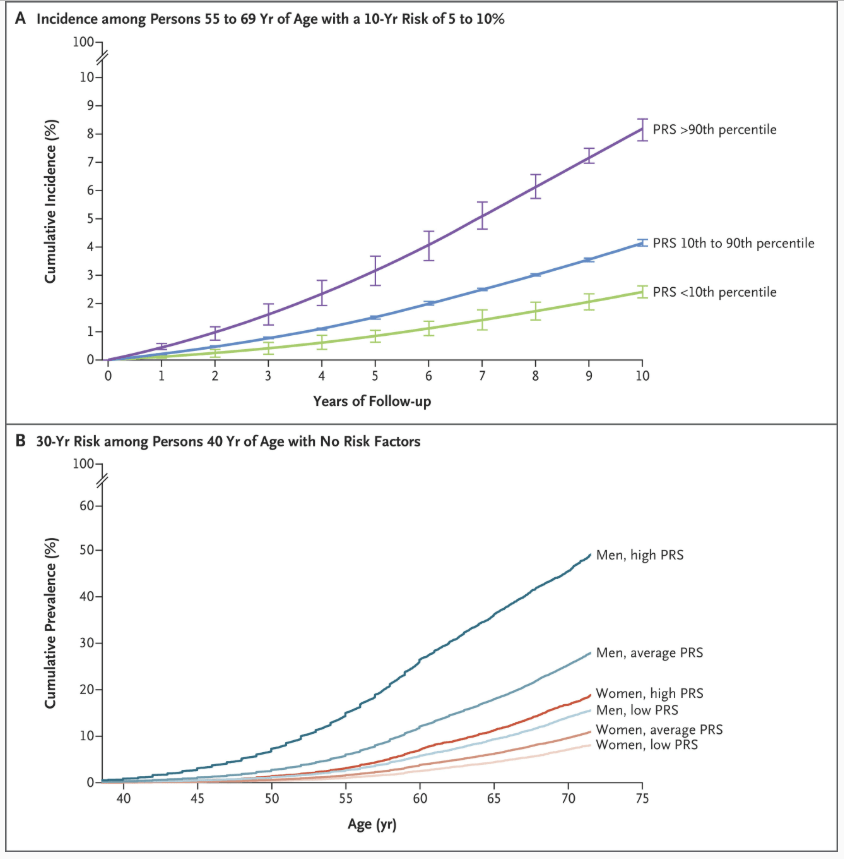
La puntuación de riesgo poligénico para la enfermedad de la arteria coronaria es más informativa cuando se ha realizado una evaluación de riesgo clínico basal. 39 El riesgo relativo derivado de la puntuación de riesgo poligénico se puede utilizar para multiplicar el riesgo absoluto derivado de una puntuación de riesgo clínico. 40 En consecuencia, si el riesgo clínico es pequeño, entonces las implicaciones de una puntuación de riesgo poligénico para la enfermedad de la arteria coronaria también son pequeñas. 39,41 Por ejemplo, en los participantes del Biobanco del Reino Unido que tenían entre 45 y 70 años de edad, la evaluación de la puntuación de riesgo poligénico mostró que solo prevendría 1 evento de enfermedad de la arteria coronaria por cada 5750 personas examinadas. 42 El rendimiento diagnóstico de una puntuación de riesgo poligénico alta puede ser mayor cuando hay antecedentes familiares de enfermedad de la arteria coronaria. 44 De igual manera, entre las personas con una probabilidad clínica intermedia de infarto de miocardio o accidente cerebrovascular (es decir, del 5 al 10 % en un plazo de 10 años), la puntuación de riesgo poligénico para la enfermedad de la arteria coronaria coloca al 10 % de estas personas en la categoría de alto riesgo, con el doble de riesgo de un evento de enfermedad cardiovascular, en comparación con aquellos que no se consideraron de alto riesgo según la puntuación de riesgo poligénico ( Figura 4A ). 40 Dicha estrategia podría prevenir 1 evento de enfermedad cardiovascular adicional por cada 340 personas examinadas, o aproximadamente el 7 % de todos los eventos. 42
Figura 4
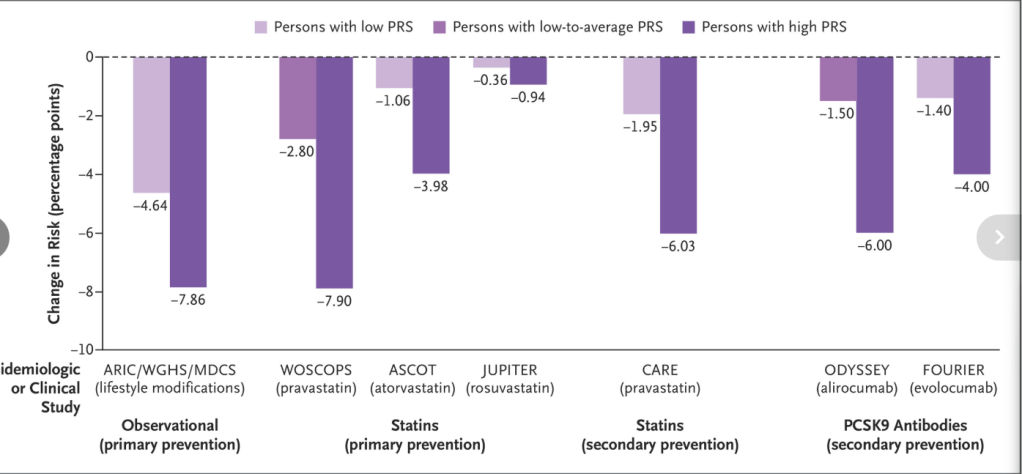
El uso de una puntuación de riesgo poligénico como medio para mejorar la evaluación del riesgo clínico armoniza con las directrices actuales, que sugieren el uso de factores adicionales para definir mejor el riesgo personalizado. Las directrices ya pueden informar a los médicos sobre las acciones apropiadas, incluyendo pruebas diagnósticas adicionales (p. ej., detección de calcio coronario) o el uso preventivo de terapia hipolipemiante para personas que se trasladan a una categoría de alto riesgo, como aquellas con una puntuación de riesgo poligénico alta. 45 Los análisis retrospectivos de ensayos aleatorizados han demostrado de forma consistente que las personas con una puntuación de riesgo poligénico alta para la enfermedad de la arteria coronaria tienen un mayor beneficio absoluto y relativo de la terapia hipolipemiante que aquellas con una puntuación de riesgo poligénico promedio ( Figura 5 ). En un ensayo aleatorizado de un solo centro que incluyó a adultos con riesgo intermedio de enfermedad de la arteria coronaria, la divulgación de la puntuación de riesgo poligénico condujo a una reducción en los eventos adversos mayores de enfermedad cardiovascular durante un período de casi 10 años. 48
Figura 5
Otra población en la que la puntuación de riesgo poligénico para la enfermedad de la arteria coronaria tiene valor son los adultos jóvenes, en quienes las puntuaciones de riesgo clínico no están bien calibradas e identifican solo aproximadamente a 1 de cada 4 personas que padecen un evento de enfermedad cardiovascular importante . 47 Estudios de cohorte han demostrado que a la edad de 40 años, un hombre promedio sin factores de riesgo clínicos que se encuentra en el quintil más alto de puntuaciones de riesgo poligénico tiene un riesgo del 30 al 40% de tener enfermedad de la arteria coronaria a la edad de 70 años, en comparación con un riesgo del 10% para un hombre en el quintil más bajo ( Figura 4B ). Dicha información puede ser relevante para la atención clínica, ya que se anticipa que las terapias preventivas, como las estatinas, serán más efectivas cuando se implementan más temprano en la progresión de la enfermedad. 47 Además, la contribución relativa del riesgo poligénico al riesgo general a largo plazo es mayor en etapas más tempranas de la vida, cuando los factores de riesgo tradicionales tienen una prevalencia menor. Los modelos de riesgo a lo largo de la vida que priorizan las terapias preventivas sobre la base de la puntuación de riesgo poligénico requieren una evaluación prospectiva. 43,47
La tercera población que podría beneficiarse de la evaluación del riesgo poligénico son las personas con enfermedad coronaria prematura, en quienes un alto riesgo poligénico podría haber contribuido a la manifestación de la enfermedad y, por lo tanto, ayudar a esclarecer la causa. En estos pacientes, una puntuación alta de riesgo poligénico predice eventos recurrentes, aunque menos que en el contexto de la prevención primaria. 32,33 Aunque la viabilidad clínica de una puntuación alta de riesgo poligénico en pacientes con enfermedad coronaria establecida es actualmente menos clara, una puntuación alta podría requerir la intensificación de las terapias cuando exista equilibrio.
Hay limitaciones relevantes en el uso de la puntuación de riesgo poligénico para la enfermedad de la arteria coronaria. 39 En primer lugar, dado que los datos subyacentes se derivan predominantemente de personas de ascendencia europea, las puntuaciones de riesgo poligénico actuales no predicen el riesgo igualmente bien en todas las ascendencias, un problema que se está abordando cada vez más en nuevos estudios de asociación del genoma completo de la enfermedad de la arteria coronaria. 37 En segundo lugar, no hay una puntuación única de consenso, ni hay estándares de informe acordados. 49 En tercer lugar, las directrices actuales aún no han incorporado la puntuación de riesgo poligénico para la enfermedad de la arteria coronaria. 39,41 En cuarto lugar, siguen existiendo brechas en la investigación y la implementación, como la evaluación del efecto de la puntuación de riesgo poligénico en la toma de decisiones clínicas, la determinación de la relación coste-efectividad y la calibración de la puntuación para la población de un sistema de atención médica. 39,50,51 Finalmente, hasta que haya una cobertura de seguro uniforme, el acceso equitativo puede ser limitado debido a los costos de bolsillo requeridos.
Tratamiento de personas con alto riesgo genético de enfermedad coronaria
Hipercolesterolemia familiar
Los ensayos clínicos han demostrado que los pacientes con hipercolesterolemia familiar se benefician del tratamiento intensivo para la reducción de lípidos incluso más, en términos absolutos, que otros grupos de pacientes en riesgo de enfermedad de la arteria coronaria. 16 En consecuencia, se recomienda el inicio del tratamiento para la reducción de lípidos para la prevención primaria en pacientes con hipercolesterolemia familiar, incluso en la edad adulta temprana, con un valor objetivo de colesterol LDL inferior a 70 mg por decilitro (1,8 mmol por litro). 13,46,52 En niños con una variante genética que causa hipercolesterolemia familiar e hipercolesterolemia persistente y clínicamente significativa, se puede iniciar una terapia con estatinas para reducir el nivel de colesterol LDL a menos de 135 mg por decilitro (3,5 mmol por litro), según las directrices europeas. 13 La hipercolesterolemia familiar homocigótica es una enfermedad potencialmente mortal, y la enfermedad de la arteria coronaria a menudo se desarrolla durante la infancia. Los niveles de colesterol LDL gravemente elevados requieren un tratamiento intensivo en centros especializados.
Alto riesgo poligénico
Mientras que las afecciones monogénicas, como la hipercolesterolemia familiar, actúan principalmente a través de un único factor de riesgo, la puntuación de riesgo poligénico para la enfermedad de la arteria coronaria representa una mezcla heterogénea de factores de riesgo causales y vías de riesgo desconocidas. Sin embargo, el riesgo poligénico para la enfermedad de la arteria coronaria también puede modificarse sustancialmente. Estudios observacionales han sugerido que un estilo de vida saludable puede contrarrestar en gran medida una puntuación de riesgo poligénico alta ( Figura 5 ). Además, los análisis post hoc de varios ensayos aleatorizados de prevención primaria y secundaria mostraron repetidamente que el tratamiento con estatinas o inhibidores de PCSK9 resulta en mayores reducciones del riesgo absoluto y relativo en personas con una puntuación de riesgo poligénico alta para la enfermedad de la arteria coronaria. 31,34 Estos estudios respaldan la premisa de que la reducción del colesterol LDL es una estrategia particularmente eficaz para reducir el riesgo de enfermedad de la arteria coronaria en personas con una puntuación de riesgo poligénico alta ( Figura 5 ). 32,33
Traduciendo la arquitectura genética a nuevas estrategias terapéuticas
Aprovechar la arquitectura genética de la enfermedad coronaria para avanzar en la terapéutica es una estrategia atractiva. Dado que la asignación de alelos es aleatoria y no cambia a lo largo de la vida, los alelos de riesgo apuntan a mecanismos causales que permiten priorizar las dianas terapéuticas. De hecho, los medicamentos en investigación con respaldo genético humano tienen mayor probabilidad de obtener la aprobación regulatoria que aquellos sin respaldo genético. 53El esclarecimiento de las variantes del receptor de LDL-LDL que causan hipercolesterolemia familiar y agrupamiento familiar de la enfermedad coronaria sentó las bases para el desarrollo de medicamentos que regulan positivamente el receptor de LDL en el hígado, como las estatinas. La observación de que variantes disruptivas raras en PCSK9 reducen los niveles de colesterol LDL y disminuyen el riesgo de enfermedad coronaria condujo al desarrollo de inhibidores de PCSK9. 9 La observación de que las variantes en los genes que codifican las proteínas diana de ezetimiba y ácido bempedoico ( NPC1L1 y ACLY , respectivamente) están asociadas con la enfermedad coronaria valida la observación previa de que su inhibición farmacológica disminuye los niveles de colesterol LDL y el riesgo de eventos de enfermedad coronaria. 8,54–56Uno de los primeros locus para la enfermedad coronaria identificados en estudios de asociación genómica, y el locus con la asociación más fuerte, alberga la apolipoproteína(a), 57 la cual determina los niveles séricos de lipoproteína(a), una macromolécula similar al colesterol LDL altamente heredable y un posible nuevo factor de riesgo modificable para la enfermedad coronaria. Con base en datos genéticos convincentes que vinculan la variación genética de LPA con la enfermedad coronaria, actualmente se están probando agentes que bloquean la transcripción o la función de su producto, la apolipoproteína(a), en ensayos clínicos de resultados cardiovasculares. Otras dianas farmacológicas en investigación son los productos de ANGPTL3 , ANGPTL4 y APOC3 , que han demostrado genéticamente que aumentan los niveles de triglicéridos y el riesgo de enfermedad coronaria. 58-60Algunas variantes raras y comunes que afectan la señalización del óxido nítrico, como NOS3 , GUCY1A1 y PDE5 , se asocian con un mayor riesgo de enfermedad de la arteria coronaria y un aumento de la presión arterial. 22,24 Un estudio observacional mostró que el tratamiento con un inhibidor de la fosfodiesterasa-5 se correlacionó con una reducción en las tasas de eventos de enfermedad de la arteria coronaria, 61 pero faltan datos de ensayos posteriores. Una variante que cambia un aminoácido en SVEP1 aumenta su función, lo que aumenta la inflamación en las células del músculo liso vascular y el riesgo de enfermedad de la arteria coronaria. 58,62 Además, estudios experimentales han demostrado que el uso de anticuerpos o vacunación para bloquear ADAMTS7 tiene potencial terapéutico. 63,64 Los análisis genéticos de moléculas inflamatorias relacionadas han priorizado las características causales probables en el inflamasoma NLRP3, como se mostró posteriormente en ensayos clínicos. 65 Un cambio de aminoácido común en SH2B3 se asocia con un mayor riesgo de enfermedad de la arteria coronaria a través del exceso de trampas extracelulares de neutrófilos y trombosis arterial. 66 Las señales en los estudios de asociación del genoma completo también han convergido en vías de señalización específicas de cada célula, como CCM2 y TLNRD1 , que afectan los procesos ateroprotectores en las células endoteliales. 67,68Elucidar la base genética de la enfermedad arterial coronaria ha ayudado a distinguir entre biomarcadores potencialmente causales y biomarcadores confusos. Este enfoque, a menudo denominado aleatorización mendeliana, utiliza variantes genéticas que se asocian únicamente con una posible exposición de interés; dichas variantes se denominan variables instrumentales. Si la asociación de la exposición con la enfermedad en cuestión es causal, las variantes genéticas también deberían estar asociadas con la enfermedad en la medida en que afecten a la exposición. Este enfoque se ha utilizado para validar factores de riesgo de enfermedad arterial coronaria, como niveles elevados de colesterol LDL y triglicéridos, hipertensión, obesidad, niveles elevados de lipoproteína(a) y diabetes tipo 2. 69 Como se mencionó anteriormente, varios fármacos que se dirigen a estos factores de riesgo interfieren en la función de genes que, según estudios de asociación de todo el genoma, están significativamente asociados con la enfermedad arterial coronaria, lo que confirma que estos fármacos abordan mecanismos relevantes. Estos estudios también han ayudado a despriorizar varios marcadores de riesgo como causales de enfermedad de la arteria coronaria, como los niveles plasmáticos bajos de colesterol de lipoproteína de alta densidad y vitamina D y los niveles plasmáticos altos de proteína C reactiva y ácido úrico. 71-74
A pesar de las fuertes correlaciones epidemiológicas para estos últimos biomarcadores, las variantes genéticas que modulan sus niveles plasmáticos no muestran una asociación convincente con el riesgo de enfermedad de la arteria coronaria.
Los estudios de aleatorización mendeliana también han aportado evidencia valiosa para comprender el riesgo de enfermedad coronaria cuando los ensayos aleatorizados no eran fácilmente factibles. Por ejemplo, los estudios de aleatorización indicaron que la asociación entre una menor estatura y un mayor riesgo de enfermedad coronaria es causal y que el consumo habitual de alcohol puede predisponer a un mayor riesgo de enfermedad coronaria. 75,76
Conclusiones
Estudios de asociación genómica y secuenciación aún más amplios en personas de todo el mundo proporcionarán información más precisa sobre las variantes de ADN implicadas, los genes causales y los mecanismos subyacentes que contribuyen al desarrollo de diversas enfermedades. Estos estudios también ayudarán a refinar y estandarizar las puntuaciones de riesgo poligénico para la enfermedad coronaria, permitiendo así una identificación más temprana de individuos en riesgo.
Una plétora de hallazgos genéticos derivados de exploraciones genómicas, a partir de 2007, continúa cambiando la percepción sobre cómo se desarrolla la enfermedad coronaria, desafiando muchas nociones tradicionales que se tenían hasta ahora. Cientos de variantes genéticas comunes que afectan a un amplio espectro de mecanismos patológicos se encuentran en cada persona; cuanto más porta una persona, mayor es el riesgo de enfermedad coronaria, lo que implica que una comprensión más profunda de estas variantes podría traducirse en intervenciones más efectivas.
La totalidad de la información genética sobre la enfermedad coronaria, capturada como variantes de hipercolesterolemia familiar, o agregada como una puntuación de riesgo poligénico, continúa abriendo nuevas oportunidades para la predicción, prevención y tratamiento tempranos del riesgo, lo que podría transformar significativamente la manera en que se aborda esta enfermedad en el futuro.
Muchos tratamientos establecidos se han validado sobre la base de estos datos, dado que la correlación entre las variantes genéticas y la respuesta a ciertos medicamentos se vuelve cada vez más clara. Actualmente, se está investigando el potencial terapéutico de varias vías patológicas de origen genético, lo que abre la puerta a tratamientos personalizados que consideren el perfil genético único de cada paciente.