Autores : Robert Chiesa , MD , Christos Georgiadis , Ph.D. , Hebatalla Rashed , MB,B.Ch. , Roland Preece , Ph.D. , Prudence Hardefeldt , MD , Jan Chu , M.Sc. , Jemma Selvage , B.Sc. ,+9 , para el grupo CAR T editado en base *
Publicado el 8 de diciembre de 2025
N Engl J Med 2026 ; 394 : 152 – 165 DOI: 10.1056/NEJMoa2505478
Nota del blog: La terapia con células T con receptor de antígeno quimérico (CAR) es
una inmunoterapia revolucionaria que modifica genéticamente las propias células T del paciente para que reconozcan y ataquen las células cancerosas. Utilizado principalmente para cánceres de sangre recidivantes o refractarios como la leucemia, el linfoma y el mieloma múltiple, actúa como un «fármaco vivo» que puede proporcionar una remisión a largo plazo. La terapia con células T CAR o terapia CAR T (abreviatura de terapia con células T con receptor de antígeno quimérico) es un tipo de terapia génica basada en células que altera los genes de las células T de una persona (un tipo de glóbulo blanco) para ayudarlas a atacar las células cancerosas. Este tipo de tratamiento puede ser útil para tratar algunos tipos de cáncer, incluso cuando otros tratamientos ya no funcionan, ofreciendo así una esperanza renovada a muchos pacientes que se encuentran en etapas avanzadas de la enfermedad. La eficacia de la terapia CAR T radica en su capacidad para personalizar el tratamiento, usando las propias células del paciente lo que minimiza el riesgo de rechazo. Además, este enfoque ha demostrado no solo eliminar las células cancerosas existentes, sino también provocar una respuesta inmunitaria que puede proteger contra futuras recaídas al entrenar al sistema inmunitario para que reconozca y ataque cualquier célula cancerosa emergente. El sistema inmunitario reconoce las sustancias extrañas en el cuerpo al encontrar proteínas llamadas antígenos en la superficie de esas células. Las células inmunitarias llamadas células T (a veces llamadas linfocitos T) tienen sus propias proteínas llamadas receptores que se unen a los antígenos extraños y ayudan a activar otras partes del sistema inmunitario para destruir la sustancia extraña, convirtiendo este proceso en una estrategia más avanzada y eficaz en la lucha contra el cáncer.
La relación entre antígenos y receptores inmunitarios es como la de una cerradura y su llave. Del mismo modo que una cerradura solo se puede abrir con la llave correcta, cada antígeno extraño tiene un receptor inmunitario único que puede unirse a él.
Las células cancerosas también tienen antígenos, pero si las células inmunitarias no tienen los receptores adecuados, no pueden unirse a los antígenos y ayudar a destruir las células cancerosas.
En la terapia con células T CAR, se extraen células T de la sangre del paciente y se modifican genéticamente en el laboratorio para que tengan un receptor llamado receptor de antígeno quimérico ( CAR ) en su superficie externa. Esto ayuda a que las células T se adhieran a un antígeno específico de las células cancerosas. Posteriormente, las células T CAR se reintroducen en la sangre del paciente.
Dado que los distintos tipos de cáncer tienen antígenos diferentes, cada CAR se diseña para el antígeno específico de un cáncer concreto. Esto significa que las terapias con células T CAR son monoclonales : cada una está diseñada para reconocer un único objetivo.
Por ejemplo, en ciertos tipos de leucemia o linfoma, las células cancerosas tienen un antígeno llamado CD19. Muchas de las terapias con células T CAR para tratar estos cánceres están diseñadas para unirse al antígeno CD19 y no funcionarán contra un cáncer que no tenga dicho antígeno.
Esto difiere de las terapias celulares policlonales , como la terapia con linfocitos infiltrantes de tumores (TIL), que pueden reconocer múltiples antígenos.
La terapia con células T CAR está aprobada por la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) para tratar algunos tipos de linfomas y leucemias, así como el mieloma múltiple. Generalmente, la terapia con células T CAR se utiliza después de haber probado otros tipos de tratamiento.
Algunos ejemplos de terapias con células T CAR aprobadas actualmente son:
- Tisagenlecleucel , también conocido como tisa-cel (Kymriah)
- Axicabtagene ciloleucel , también conocido como axi-cel (Yescarta)
- Brexucabtagene autoleucel , también conocido como brexu-cel (Tecartus)
- Lisocabtagene maraleucel , también conocido como liso-cel (Breyanzi)
- Idecabtagene vicleucel , también conocido como ide-cel (Abecma)
- Ciltacabtagene autoleucel , también conocido como cilta-cel (Carvykti)
- Obecabtagene autoleucel , también conocido como obe-cel (Aucatzyl)
Actualmente se están estudiando en ensayos clínicos muchas otras terapias con células T CAR (y tratamientos similares), con la esperanza de poder tratar también otros tipos de cáncer. Recibir terapia con células T CAR es bastante diferente de otros tipos de tratamientos de inmunoterapia. Implica lo siguiente: Recibir la infusión de células T CAR y ser monitoreado de cerca, a veces en el hospital durante 1-2 semanas.
La extracción de las células T de la sangre se realiza generalmente en uno o más procedimientos ambulatorios. Esperar varias semanas para que sean modificados y multiplicados en el laboratorio. En primer lugar, se extraen los glóbulos blancos (que incluyen las células T) de la sangre mediante un procedimiento llamado leucoaféresis . Se utilizan dos vías intravenosas:
- La sangre se extrae a través de una línea.
- Los glóbulos blancos se separan mediante una máquina especial ( aféresis ).
- Luego, la sangre restante se reintroduce en el cuerpo a través de la otra vía.
En ocasiones se utiliza un tipo especial de vía intravenosa llamada catéter venoso central , que incorpora ambas vías intravenosas. Este proceso suele durar varias horas y deberá permanecer sentado o acostado durante el mismo. Es posible que deba repetirse al día siguiente o más veces hasta que se recolecten suficientes células. En ocasiones, los niveles de calcio en sangre pueden disminuir durante la leucoaféresis, lo que puede provocar entumecimiento, hormigueo o espasmos musculares. Esto se puede tratar reponiendo el calcio, que se puede administrar por vía oral o intravenosa.
Abstract
Fondo
El CD7 es una diana atractiva para la terapia de células T con receptores de antígenos quiméricos (CAR) en la leucemia linfoblástica aguda (LLA) de células T recidivante o refractaria. Se han publicado previamente resultados que respaldan los primeros estudios en humanos de células T CAR anti-CD7 con edición de bases (BE-CAR7) con inactivación de TCRαβ, CD52 y CD7 mediada por la triple desaminación C→T.
Métodos
En un estudio de fase 1, administramos células T BE-CAR7 a niños (≤16 años) con LLA de células T en recaída o refractaria tras la linfodepleción con fludarabina, ciclofosfamida y alemtuzumab. También fueron elegibles adultos con acceso compasivo. Los pacientes que alcanzaron la remisión al día 28 tras la infusión de células T BE-CAR7 fueron sometidos a un trasplante alogénico de células madre hematopoyéticas. El criterio de valoración principal fue la seguridad. Los criterios de valoración secundarios incluyeron la duración de la remisión, la supervivencia libre de enfermedad y la supervivencia global.
Resultados
Se administraron células T BE-CAR7 a 9 niños y 2 adultos tratados bajo acuerdos de acceso compasivo. La linfodepleción y las infusiones de BE-CAR7 no provocaron eventos adversos inaceptables, y se detectaron células T CAR7 circulantes en todos los pacientes. Las complicaciones incluyeron síndrome de liberación de citocinas de grados 1 a 4, erupciones cutáneas transitorias, citopenia multilinaje e infecciones oportunistas. Todos los pacientes presentaron remisión morfológica completa con recuperación incompleta del recuento al día 28. Nueve pacientes (82%) presentaron remisión profunda (según citometría de flujo o reacción en cadena de la polimerasa) que les permitió proceder al trasplante de células madre, y 2 pacientes con enfermedad mínima residual cuantificable en médula ósea recibieron cuidados paliativos. El trasplante eliminó las células T BE-CAR7 restantes y favoreció la reconstitución multilinaje derivada del donante. Las reactivaciones virales fueron frecuentes, y 3 pacientes presentaron complicaciones clínicamente significativas relacionadas con el virus después del trasplante. En general, 7 de los 11 pacientes (64%) que recibieron la terapia en investigación estaban en remisión continua entre 3 y 36 meses después del trasplante, y se documentó leucemia con pérdida de la expresión de CD7 en 2 pacientes.
Conclusiones
Las células T universales BE-CAR7 indujeron la remisión leucémica en pacientes con LLA de células T en recaída o refractaria, lo que permitió un trasplante alogénico de células madre hematopoyéticas exitoso en la mayoría de los pacientes. (Financiado por el Consejo de Investigación Médica y otros; número de registro ISRCTN: ISRCTN15323014 ).
Los pacientes con leucemia linfoblástica aguda (LLA) de células T tratados con protocolos de quimioterapia estándar pueden anticipar buenos resultados, pero en caso de fracaso de la terapia de inducción o enfermedad mínima residual (ERM) detectable después de la terapia de consolidación, generalmente se recomienda un trasplante alogénico de células madre hematopoyéticas.<sup> 1</sup> El riesgo de recaída después de un trasplante alogénico de células madre es mayor cuando la ERM antes del trasplante es superior a 10−3 ( es decir, >1 célula por cada 1000 células normales), y generalmente se requiere una remisión profunda con un nivel de enfermedad inferior a 10−4 ( es decir, <1 célula por cada 10 000 células normales) para ser elegibles para el trasplante. La supervivencia entre los pacientes que presentan una recaída después de un trasplante alogénico de células madre es baja, con una supervivencia a largo plazo más allá de los 3 años inferior al 15 %.<sup> 2</sup>
Se han propuesto diversas estrategias de células T con receptores de antígenos quiméricos (CAR) dirigidas a antígenos adecuados en la leucemia linfoblástica aguda (LLA) de células T, 3-7 y el CD7 se ha convertido en uno de los objetivos más atractivos, ya que, a pesar de estar presente en linfocitos normales y precursores hematopoyéticos, su expresión se mantiene constantemente alta y estable en poblaciones de blastos de LLA de células T. Los efectos fratricidas entre células diseñadas para expresar CAR anti-CD7 se han abordado mediante el uso de subgrupos de células T CD7− 8 o mediante la coexpresión de bloqueadores de la expresión de proteínas para secuestrar y prevenir la expresión de CD7 en la superficie celular. 9 Se están realizando pruebas clínicas con estos enfoques en el contexto de donantes autólogos y alogénicos compatibles. 10-17 Como alternativa, se ha aplicado la edición genómica para interrumpir la expresión de CD7 18 y se ha combinado con la interrupción simultánea de la expresión génica del receptor de células T para la producción de células T CAR de donantes universales sin TCRαβ. 19-23
Anteriormente, la edición de bases (desaminación de citidina guiada por repeticiones palindrómicas cortas agrupadas y regularmente interespaciadas [CRISPR]) se ha aplicado para introducir codones de parada prematuros o modificar sitios de empalme críticos para TCRαβ, CD7 y efectos knockout multiplexados adicionales y se ha combinado con la transducción lentiviral de células T con un CAR anti-CD7 ( Figura 1A ). 20,24,25 Las ventajas de la edición de bases sobre la edición de nucleasas incluyen minimizar las aberraciones del cariotipo o las translocaciones cromosómicas, como se ha informado previamente para las nucleasas efectoras similares a activadores de la transcripción (TALEN) 26,27 y los productos mediados por la nucleasa CRISPR-Cas9. 28 Anteriormente informamos los resultados de un primer estudio en humanos de células T CAR anti-CD7 (BE-CAR7) editadas en bases que se infundieron para asegurar remisiones moleculares profundas de la LLA de células T refractaria antes del trasplante alogénico de células madre. 24 Los resultados en dos de los primeros tres niños que recibieron la terapia en investigación se actualizan en este informe de la cohorte pediátrica de fase 1 completada, junto con experiencia adicional de aplicaciones de uso compasivo en adultos con LLA de células T refractaria.
Figura 1
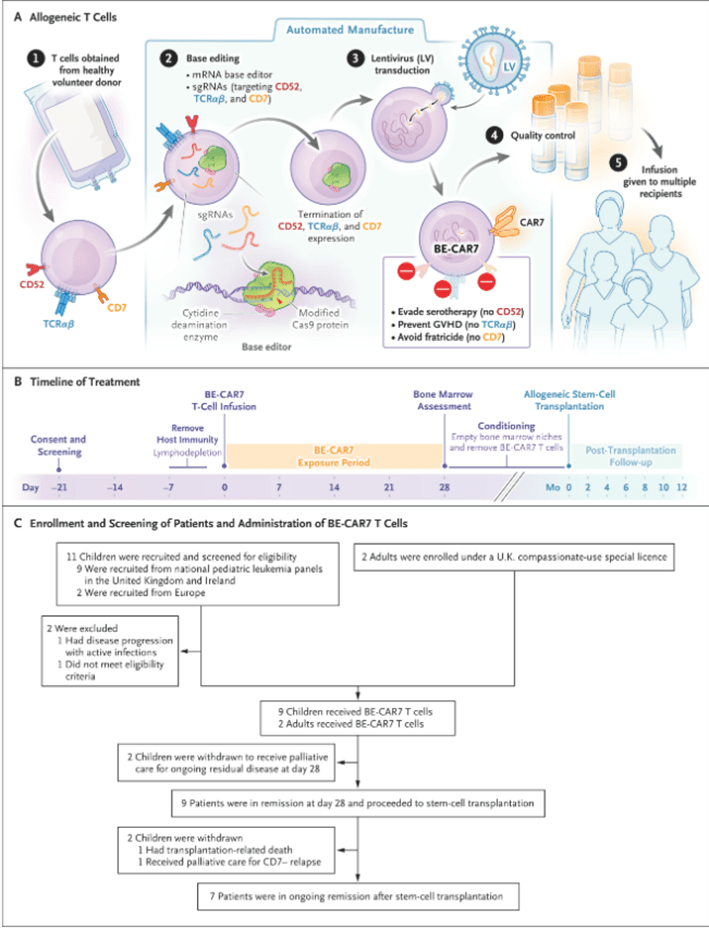
Producción de células T CAR7 con edición de base universal e inscripción, selección y tratamiento de pacientes.
Métodos
Células T CAR7 con edición de bases
El diseño, la fabricación, la caracterización y la liberación de los bancos de células T BE-CAR7 se han descrito previamente. 24 Todas las dosis del producto en investigación estaban contenidas en viales que se habían generado a partir del mismo donante del registro (Anthony Nolan Stem Cell Registry); el producto en investigación se generó en una sola campaña (Buenas Prácticas de Fabricación [GMP] 3) en la que el 59 % de las células CD45+ expresaron CAR7, con 3,6 copias del vector por célula y una expresión residual de TCRαβ del 0,1 %, y las células eran más del 99 % CD7− y más del 98 % CD52− (Tabla S1 en el Apéndice Suplementario , disponible con el texto completo de este artículo en NEJM.org). Los viales se criopreservaron en alícuotas de 10 millones, 20 millones o 50 millones de células mononucleares CD45+.
Programa de tratamiento
En este estudio de fase 1, incluimos a niños de 6 meses a 16 años con leucemia linfoblástica aguda (LLA) de células T CD7+ en recaída o refractaria, cuantificable en médula ósea (>10−4 mediante citometría de flujo o reacción en cadena de la polimerasa [PCR]). Los pacientes adultos fueron tratados bajo acuerdos de licencia especiales para el acceso compasivo en el Reino Unido para medicamentos sin licencia. Los criterios de exclusión clave fueron enfermedad progresiva, infección no controlada, enfermedad de injerto contra huésped (EICH) preexistente o presencia de anticuerpos anti-HLA contra lotes de BE-CAR7 (Tabla S2).
Los pacientes se sometieron a linfodepleción con fludarabina (150 mg por metro cuadrado de superficie corporal), ciclofosfamida (120 mg por kilogramo de peso corporal en pacientes ≤16 años o 1500 mg por metro cuadrado en pacientes >16 años) y alemtuzumab (1 mg por kilogramo). Tras la linfodepleción, se realizó una infusión dentro de un rango permitido de 0,2 × 10⁻¹ a 2,0 × 10⁻¹ de linfocitos T BE-CAR7 por kilogramo (con una dosis máxima de 5 × 10⁻¹ de linfocitos T TCRαβ+ por kilogramo, para limitar el riesgo de EICH). Los pacientes que estaban en remisión de MRD (evaluada según citometría de flujo o ensayo de PCR) el día 28 procedieron a un trasplante alogénico de células madre, momento en el cual las células T BE-CAR7 persistentes se agotaron mediante regímenes de acondicionamiento utilizados antes del trasplante ( Figura 1B ).
Supervisión del estudio
El estudio fue supervisado por Great Ormond Street Hospital for Children NHS Trust. El estudio fue aprobado por el Comité de Ética del Oeste de Londres. Se obtuvo el consentimiento informado por escrito de los padres de los pacientes de 16 años o menos y de los pacientes mayores de 16 años. Se proporcionó a los niños información escrita apropiada para su edad y se obtuvo su asentimiento cuando fue posible. Las células de donantes se obtuvieron de voluntarios a través del Registro Nolan. El protocolo del estudio , que incluye el plan de análisis estadístico, está disponible en NEJM.org. Los autores garantizan la exactitud e integridad de los datos, así como la fidelidad del estudio al protocolo.
Resultados
El resultado principal fue la seguridad, que se evaluó según los Criterios Terminológicos Comunes para Eventos Adversos, versión 5.0. Los resultados secundarios incluyeron la frecuencia y duración de la remisión, la supervivencia libre de enfermedad y la supervivencia global.
Análisis estadístico
Se utilizó un diseño adaptativo de dos etapas de Bryant y Day para evaluar simultáneamente los efectos tóxicos relacionados con el tratamiento y la eficacia de los linfocitos T BE-CAR7. La significancia estadística se estableció en un 15 % para cada resultado (seguridad y eficacia), y la potencia estadística se fijó en un 85 %. Una respuesta (definida como evidencia de una reducción de la EMR al día 28, lo que indica actividad antileucémica) en el 70 % o más de los pacientes era plausible; sin embargo, si el porcentaje de pacientes con respuesta era inferior al 30 %, el estudio se detendría.
Si se presentara síndrome de liberación de citocinas de grado 3 o mayor, efectos neurotóxicos o EICH de 7 días o más de duración en más del 40 % de los pacientes que recibieron la terapia en investigación, el estudio se suspendería y se realizaría una revisión de la dosis. Los análisis de supervivencia se realizaron mediante el método de Kaplan-Meier.
Resultados
Características de los pacientes
El reclutamiento para el estudio comenzó el 1 de abril de 2022 y la administración de la terapia en investigación estaba programada para completarse el 31 de mayo de 2025. Durante este período, se inscribieron 11 niños (de 5 a 15 años de edad) y se sometieron a pruebas de detección, de los cuales 9 cumplieron con los criterios de elegibilidad y recibieron la terapia antes del 31 de mayo de 2025 ( Figura 1C ). Un niño (Paciente P6) fue excluido debido a la progresión de la enfermedad a pesar de la citorreducción, y el tratamiento en el otro niño (Paciente P11) se aplazó para evaluaciones adicionales de la enfermedad. Además, dos mujeres, de 38 y 27 años de edad (Pacientes Sp1 y Sp2, respectivamente), fueron tratadas bajo acuerdos de licencia especiales para acceso compasivo. Las características de los pacientes se muestran en la Tabla 1 y la Tabla S3.
Tabla 1
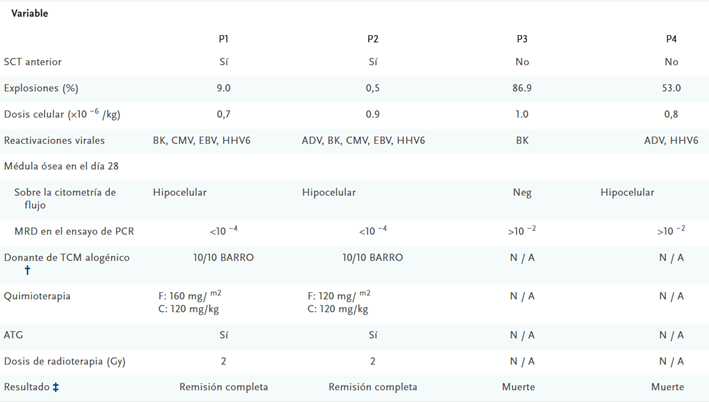
Características de los pacientes, intervenciones del estudio y resultados.
Todos los pacientes que recibieron la terapia en investigación (seis mujeres y cinco hombres) fueron categorizados como pacientes con LLA de células T refractaria con un inmunofenotipo cuantificable asociado a leucemia, evaluado mediante citometría de flujo como CD7 de más del 99% en médula ósea (Tabla S4). Todos los pacientes habían recibido previamente múltiples líneas de terapias estándar, y los pacientes P1, P2 y Sp2 se habían sometido al menos a un trasplante previo de un donante compatible no emparentado, que incluyó acondicionamiento con irradiación corporal total (12 Gy). En la última recaída, el paciente P2 tenía enfermedad documentada del sistema nervioso central, y el paciente Sp2 tenía afectación previa del sistema nervioso central y ocular.
La linfodepleción se completó con éxito en todos los pacientes (Fig. S1). Las infusiones no produjeron un nivel inaceptable de eventos adversos en niños que recibieron de 30×10⁻¹ a 50×10⁻¹ células en total, ni en adultos que recibieron 100×10⁻¹ células CD45+ en total, que comprenden de 0,7×10⁻¹ a 1,0×10⁻¹ células CAR7+ por kilogramo del banco BE-CAR7 (GMP3).
Complicaciones y efectos tóxicos
Entre 1 día y 5 días después de la infusión de células T BE-CAR7, se desarrolló síndrome de liberación de citocinas de grado 1 o 2 en nueve pacientes (82%) ( Figura 2A ), que se manejó bajo procedimientos institucionales estándar, incluido el seguimiento de biomarcadores de interleucina-6 y ferritina ( Figura 2B y Fig. S2). Dos pacientes (18%) tuvieron síndrome de liberación de citocinas de grado 3 o 4; el evento en el paciente P3 se describió previamente. 24 El paciente P3 tuvo una alta carga de enfermedad (80% blastos de médula ósea) e infecciones fúngicas diseminadas, que probablemente contribuyeron a complicaciones inflamatorias con biomarcadores elevados, incluyendo ferritina e interleucina-6, a pesar del uso de terapias anticitocinas y glucocorticoides. El paciente P4 también tuvo una alta carga de médula ósea (50% blastos de médula ósea) antes de la linfodepleción y tuvo síndrome de liberación de citocinas de grado 2 dentro de 1 día después de la infusión; El evento respondió a la terapia con tocilizumab, pero reapareció en grado 3 a partir del día 7, con niveles elevados de ferritina e interleucina-6, lo que llevó a intervenciones adicionales con tocilizumab, anakinra y apoyo inotrópico transitorio antes de que el evento se resolviera el día 11.
Figura 2
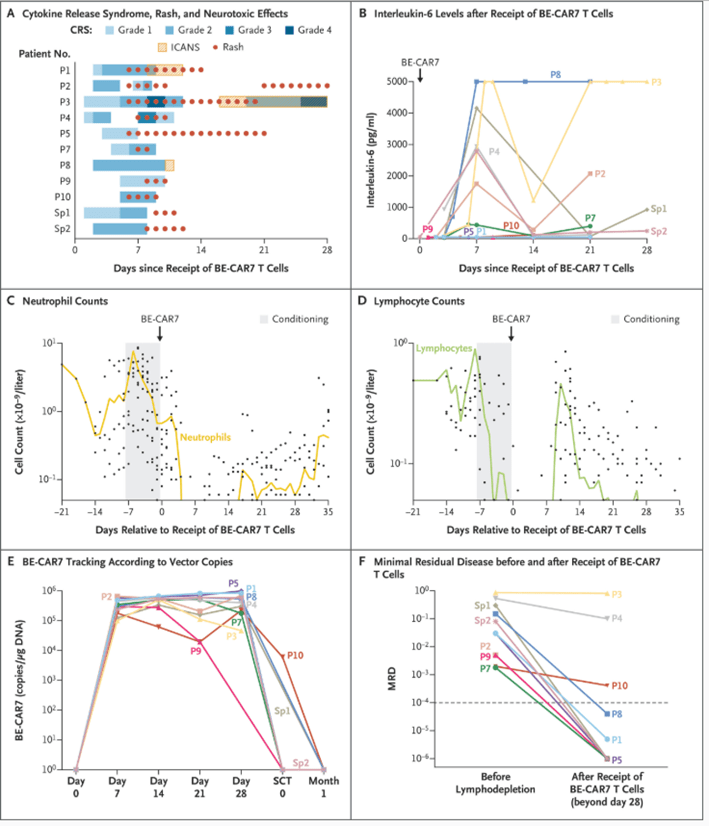
Complicaciones, biomarcadores, número de copias del vector y remisiones mediadas por células T CAR.
Simultáneamente con la resolución del síndrome de liberación de citocinas, todos los pacientes, excepto el paciente P8, presentaron erupciones maculopapulares eritematosas entre 6 y 10 días después de la infusión de células T BE-CAR7. Las erupciones se trataron con glucocorticoides tópicos o sistémicos según fuera apropiado y se resolvieron para el día 21 en todos los pacientes (Fig. S3). Cuando se realizaron biopsias cutáneas, los cambios observados en las muestras de biopsia cutánea se informaron como inespecíficos sin infiltración linfocítica notable. Se documentó síndrome de neurotoxicidad asociada a células efectoras inmunitarias (ICANS) de grado 1 en tres pacientes (pacientes P1, P3 y P8) ( Figura 2A y Tabla 2 ).
Tabla 2
Resumen de eventos adversos, según el grado máximo de gravedad.
Como se anticipó, se desarrolló citopenia multilinaje con neutropenia ( Figura 2C ), linfopenia ( Figura 2D ) y trombocitopenia desde el momento de la linfodepleción hasta el día 28 y posteriormente hasta el trasplante alogénico de células madre. Todos los eventos adversos, incluyendo los eventos adversos graves, registrados desde el inicio de la linfodepleción hasta 28 días después de la infusión de células T BE-CAR7 se resumen en la Tabla 2 .
Expansión y eliminación de células T BE-CAR7
El seguimiento multiparamétrico de las células T BE-CAR7 en la circulación y la médula ósea comprendió citometría de flujo (Fig. S4), PCR digital de gotas (ddPCR) para el número de copias del vector ( Figura 2E ), y firmas de quimerismo molecular (Fig. S5). A pesar de la linfopenia con recuentos absolutos bajos de células T, la ddPCR mapeó aumentos en las copias del vector en ADN aislado de células mononucleares de sangre periférica dentro de los 7 a 14 días posteriores a la infusión de células T BE-CAR7, y este hallazgo fue corroborado por el análisis de quimerismo (firmas de repetición en tándem de número variable). La citometría de flujo capturó la presencia de células T CAR7+TCR−CD52−CD7− circulantes en muestras de sangre seriadas y en muestras de médula ósea obtenidas el día 28. El condicionamiento para el trasplante aseguró la eliminación de las células T BE-CAR7 y la ausencia de una señal de ddPCR lentiviral, y se documentó un cambio al quimerismo completo del donante en todos los pacientes que procedieron al trasplante.
Actividad antileucémica
Se realizaron evaluaciones de citometría de flujo antes del inicio de la linfodepleción para confirmar más del 99% de expresión de CD7 en blastos de médula ósea y cuantificar la carga de la enfermedad. Nueve de los 11 pacientes tenían marcadores moleculares adecuados para la cuantificación basada en PCR de MRD. Las evaluaciones de médula ósea indicaron que todos los pacientes tuvieron respuestas antileucémicas, con reducciones en la enfermedad de la médula ósea que resultaron en una remisión morfológica completa en el contexto de recuperaciones de recuento incompletas y citopenia multilinaje. Nueve pacientes (82%) progresaron al trasplante en remisión profunda, según lo evaluado por citometría de flujo o ensayo de PCR (o ambos), con umbrales de MRD por debajo de 10 −4 en todos excepto 1 paciente (Paciente P10, que procedió al trasplante con MRD de menos de 10 −3 ) ( Tabla 1 , Figura 2F y Fig. S6).
El acondicionamiento para trasplantes fue de intensidad reducida en pacientes que habían recibido un primer trasplante previamente, habiendo recibido ya 12 Gy de irradiación corporal total. En estos pacientes, se administró irradiación corporal total de dosis baja a 2 Gy y se incluyó globulina antitimocítica (ATG) para asegurar la eliminación de células T BE-CAR7, un enfoque que se basó en estrategias previas en el contexto de la terapia alogénica CAR19. Los regímenes de acondicionamiento estándar para los primeros trasplantes incluyeron de 4 a 12 Gy de irradiación corporal total y ATG. Todos los pacientes habían mantenido remisiones completas después del trasplante, excepto el paciente P8, que tuvo una recaída de CD7− aproximadamente 3 meses después del trasplante de células madre ( Tabla 1 ).
Se encontró que los pacientes P3 y P4 tenían una EMR de más de 10−3 según lo evaluado por ensayo de PCR y no fueron elegibles para el trasplante alogénico de células madre. Las manifestaciones de enfermedad extramedular que afectaban la órbita izquierda habían aparecido por primera vez durante el período del síndrome de liberación de citocinas en el paciente P4, y la hinchazón localizada se investigó mediante imágenes de resonancia magnética y muestras obtenidas por biopsia abierta (Fig. S7). La citometría de flujo detectó la presencia de leucemia CD7−, con un inmunofenotipo distintivo similar a las poblaciones de blastos identificadas en muestras de médula ósea obtenidas el día 28; la detección de la enfermedad se corroboró mediante cuantificación de EMR basada en PCR. La presencia de células T BE-CAR7 se confirmó tanto en la médula ósea como en la sangre periférica, pero no en la muestra de biopsia orbitaria (Fig. S8). La secuenciación genética no detectó evidencia de mutaciones de escape en los exones 1 a 4 de CD7.
Complicaciones virales y reconstitución inmunitaria después del trasplante
Se instituyó una vigilancia rutinaria dos veces por semana para infecciones virales comunes debido al riesgo previsto de reactivaciones después de la linfodepleción y la terapia con células T BE-CAR7. Todos los pacientes tenían viremia documentada, con adenovirus, virus de Epstein-Barr (VEB), citomegalovirus (CMV) y virus del herpes humano 6 (HHV6) detectados con frecuencia en sangre y virus BK detectado en orina ( Tabla 1 ). Se administraron medicamentos antivirales cuando fue apropiado (cidofovir y brincidofovir para la infección por adenovirus y ganciclovir y foscarnet para la infección por CMV) hasta la recuperación inmunitaria de las células T y la depuración mediada por células ( Figura 3A , Fig. S9 y Fig. S10). En los pacientes P5, P8 y Sp2, las reactivaciones de adenovirus y BK contribuyeron al compromiso de la función cardiorrespiratoria y renal después del trasplante, lo que condujo a un apoyo terapéutico sustancial. El paciente Sp2 recibió asistencia ventilatoria prolongada y diálisis en curso después de cistitis hemorrágica, perforación de vejiga y compromiso renal. Después del trasplante, el paciente P1 tuvo una reactivación tardía del VEB asociada con derrame pericárdico (a los 11 meses después del trasplante alogénico de células madre), que se resolvió después de un ciclo corto de glucocorticoides sistémicos.
Figura 3
Reactivaciones virales y análisis de supervivencia.
La cinética de recuperación de neutrófilos y linfocitos después del trasplante de células madre fue generalmente como se anticipó, sin evidencia de posible actividad de células T BE-CAR7 en el injerto o la reconstitución ( Figura 3B y Figura 3C ). Todos los pacientes supervivientes tuvieron injerto derivado del donante dentro de 1 mes y recuperación de linfocitos estable aproximadamente 2 meses después del trasplante (media, 1,06 × 10 9 células por litro; rango, 0,46 × 10 9 a 1,46 × 10 9 ). La recuperación de recuentos de células T CD4 por encima de 250 por microlitro se consideró el umbral para la recuperación de células T suficiente para iniciar la retirada de la profilaxis para infecciones oportunistas (Fig. S11).
La supervivencia global entre todos los pacientes que habían recibido la terapia en investigación antes de la fecha límite (31 de mayo de 2025) fue del 73%, y la supervivencia libre de enfermedad fue del 64% después de considerar a un paciente (Paciente P8) que presentó una recaída de CD7− después del trasplante ( Figura 3D y Figura 3E ). El primer paciente tratado en este estudio ha estado libre de enfermedad durante más de 36 meses ( Figura 3F ). Los pacientes ingresaron a un seguimiento a largo plazo de hasta 15 años una vez que cumplieron 12 meses después del trasplante.
Discusión
Previamente, describimos cómo se aplicó la edición de bases C→T para generar células T BE-CAR7 con triple knockout para la terapia experimental contra la leucemia linfoblástica aguda (LLA) de células T en tres niños que participaron en un ensayo clínico pionero. 24 Dos de estos pacientes, que habían presentado una recaída tras un trasplante alogénico de células madre, se encuentran en remisión prolongada. La experiencia inicial demostró las posibles aplicaciones médicas de la edición de bases. En este trabajo, presentamos datos sobre el criterio principal de valoración de seguridad y los criterios secundarios de eficacia en la cohorte pediátrica del estudio, junto con datos adicionales de dos pacientes adultos tratados según el mismo protocolo bajo acuerdos de acceso compasivo.
El diseño y la estrategia del estudio buscaron maximizar la probabilidad de éxito, incluso en un estudio de fase 1, mediante criterios de inclusión rigurosos que estipulaban una cobertura completa de CD7 en toda la población de blastocitos y la exclusión de pacientes con anticuerpos anti-HLA preexistentes dirigidos contra el producto. Si bien se habían establecido dos bancos de donantes diferentes antes del inicio del estudio, hasta la fecha, este solo ha utilizado un donante para todos los pacientes que recibieron una dosis de la terapia en investigación; esta situación podría haber contribuido a la consistencia de las respuestas observadas en toda la cohorte.
En la mayoría de los casos, los pacientes presentaron fiebre seguida de exantema generalizado en la semana posterior a la infusión, con aumento de indicadores inespecíficos de inflamación, como la ferritina, así como de biomarcadores específicos de la actividad de CAR, como la interleucina-6. Las intervenciones para tratar el síndrome de liberación de citocinas y la ICANS, según correspondiera, siguieron los procedimientos institucionales estándar para el manejo de los efectos tóxicos predecibles de la terapia con células T CAR y priorizaron el uso de agentes biológicos anticitocinas para manejar las complicaciones sin impedir potencialmente la actividad antileucémica. El momento y la resolución de los exantemas sugirieron una base inmunológica y podrían haber sido mediados por células T alorreactivas TCRαβ+ residuales o el seguimiento de células T CD7− a la piel, pero la ausencia de evidencia de infiltración linfocítica en las muestras de biopsia cutánea contradice la mediación directa de las células efectoras transferidas adoptivamente. La mayoría de los episodios se resolvieron al disminuir la fiebre de los pacientes. Se estima que las manifestaciones cutáneas después de terapias CAR autólogas ocurren con hasta un 5% de los productos comerciales, pero se han reportado incidencias mucho más altas en algunos estudios.29
Reconocimos la importancia de la descitorreducción de la leucemia antes de la infusión de CAR7 para reducir el riesgo de síndrome de liberación de citocinas grave o efectos neurotóxicos, aunque notamos que no se encontraron problemas similares cuando se usaron productos CAR7 autólogos, un hallazgo que puede reflejar una aptitud y potencia celular más variables en ese contexto. 30 Las células alogénicas también tienen ventajas en la mitigación contra la posibilidad de transducción de blastos por vectores lentivirales durante la fabricación de células T CAR, lo que podría resultar en la expresión de CAR7 y enmascaramiento del antígeno CD7, como se ha informado para los vectores CAR19 dirigidos a la LLA de células B CD19+. 31 Finalmente, las células T autólogas podrían albergar predisposiciones genéticas subyacentes que son de mayor preocupación con respecto al riesgo de transformación después de que se observara un pequeño número de cánceres secundarios asociados con productos de células T CAR aprobados. 32
Los productos CAR7 pueden generarse sin edición genética mediante la transducción de subgrupos de células T que son CD7− de forma natural o que han enmascarado o secuestrado CD7 tras la expresión de CAR7. Estudios han demostrado remisiones morfológicas de la leucemia linfoblástica aguda (LLA) de células T con este enfoque, pero la supervivencia libre de progresión fue mayor en los pacientes sometidos a trasplante posterior que en los tratados sin trasplante. 10,11
Otra estrategia ha utilizado bloqueadores de la expresión de la proteína anti-CD7 para la captura y restricción dirigida de la expresión de CD7 para abordar los efectos fratricidas. 12,13 Un estudio reciente mostró negatividad de MRD en 16 de 17 pacientes, 30 y otro estudio utilizó células T CAR7 que se fabricaron a partir de donantes de células madre compatibles y mostraron una remisión completa en 18 de 20 pacientes, con 7 pacientes procediendo luego al trasplante de células madre. 14,15 En el contexto del desajuste de HLA, se han utilizado donantes parentales haploidénticos para la generación de células T CAR7 alogénicas antes del trasplante del mismo donante. 16 Las estrategias que utilizan donantes alogénicos universales completamente no compatibles han explotado pasos adicionales de edición genómica con el uso de CRISPR-Cas9 para interrumpir la expresión endógena de TCRαβ y CD7 para conducir a la remisión completa. 21–23,33,34
En todos estos enfoques, se documentaron efectos de citopenia o aplasia de médula ósea en entornos clínicos; estos efectos probablemente fueron multifactoriales debido a la quimioterapia, la liberación de citocinas y la actividad anti-CD7 directa contra precursores mieloides, células T y células asesinas naturales. 35,36 Dichos efectos se explotaron en una estrategia «todo en uno» en la que 10 pacientes que tuvieron remisión completa y pancitopenia después del tratamiento con CAR7 se sometieron a un trasplante rápidamente, sin el uso de acondicionamiento adicional o profilaxis de EICH de donantes haploidénticos, lo que resultó en una supervivencia del 68% a los 12 meses. 37
La linfopenia y la neutropenia prolongadas aumentan claramente el riesgo de complicaciones infecciosas, incluyendo las causadas por patógenos oportunistas y reactivaciones virales. Se han observado complicaciones previamente cuando se utilizó una linfodepleción aumentada de forma similar que incorporaba alemtuzumab en el contexto de células T CAR editadas genómicamente alogénicas para cánceres de células B. 38 Con los efectos adicionales de CAR7 que contribuyen a efectos inmunosupresores adicionales, documentamos la reactivación frecuente de virus latentes como el adenovirus, el virus BK y el HHV6, así como complicaciones relacionadas con hongos. Aunque la vigilancia intensiva y la profilaxis ofrecieron mitigaciones y el estudio se diseñó para reducir el riesgo mediante la reconstitución derivada del trasplante y del donante, las complicaciones relacionadas con el virus que se extendieron al período posterior al trasplante causaron complicaciones clínicamente significativas en dos niños y un adulto.
No obstante, nuestra experiencia sugiere que los efectos antileucémicos de la terapia con CAR7 alcanzan su punto máximo en dos semanas, y una vez resuelto el síndrome de liberación de citocinas, es posible proceder rápidamente al trasplante para asegurar una pronta reconstitución del donante y abordar las complicaciones infecciosas. Las estrategias de acondicionamiento para el trasplante también son cruciales y se basaron en los enfoques estándar para la leucemia linfoblástica aguda (LLA) de células T, que incluyen rutinariamente 12 Gy de irradiación corporal total, excepto en lactantes pequeños. De lo contrario, se utilizaron regímenes de intensidad reducida para promover un rápido injerto y recuperación, en lugar de proporcionar efectos antileucémicos adicionales.
También utilizamos el trasplante de sangre de cordón umbilical repleto de células T, que puede adaptarse para apoyar la recuperación acelerada de células T de células T inmunológicamente vírgenes portadas en el injerto. Los pacientes con seguimiento de más de 6 meses después del trasplante en nuestro estudio han documentado la recuperación de los compartimentos de células T sin EICH clínicamente significativa. Con poca frecuencia, la pérdida de antígeno CD7 y los fenómenos de escape se han documentado en estudios clínicos, y en un puñado de casos, se han dilucidado los mecanismos subyacentes, incluyendo mutaciones de cambio de marco y de sentido erróneo. 15,30 Verificamos la integridad de los exones CD7 mediante secuenciación genética de la enfermedad CD7− de bajo nivel en la médula ósea después de la terapia BE-CAR7 en un niño que también tenía enfermedad extramedular orbitaria de nueva aparición. Serán necesarias más investigaciones para interrogar los factores epigenéticos que involucran la metilación del ADN y la acetilación de histonas de CD7 que pueden haber regulado negativamente el CD7 en la leucemia linfoblástica aguda de células T primaria39,40 y para determinar si los clones leucémicos CD7− preexistentes estaban presentes por debajo de los umbrales de detección antes de la terapia o surgieron espontáneamente y se expandieron selectivamente bajo la presión del tratamiento con células T BE-CAR7.
Finalmente, se están desarrollando iteraciones universales de CAR de próxima generación que utilizan editores de bases avanzados, con una arquitectura compacta y una fidelidad de edición mejorada. 41 La edición de bases multiplexada adicional para promover la ocultación inmunológica mediante la interrupción de los HLA de clase I y II puede ofrecer una alternativa a la linfodepleción intensa, la seroterapia y los riesgos asociados de reactivación viral. 42 Es necesario perfeccionar la estrategia para minimizar el período de exposición a CAR7 y promover una transición fluida al trasplante alogénico tan pronto como se resuelvan los efectos de la liberación de citocinas. Mientras tanto, los datos de este estudio de fase temprana respaldan la investigación adicional de las células T BE-CAR7 para el tratamiento de la leucemia linfoblástica aguda (LLA) de células T recidivante o refractaria tanto en niños como en adultos en cohortes de ensayos ampliados. Entre las preguntas abiertas se encuentran la base molecular de las recaídas de CD7−, si el alemtuzumab podría eliminarse del régimen preparatorio para reducir la reactivación viral sin disminuir los efectos antitumorales y si las células T BE-CAR7 que se han generado a partir de otros donantes serían efectivas en un grado similar al observado en nuestro estudio.
En este estudio de fase 1, observamos que las células T universales BE-CAR7 indujeron respuestas antileucémicas en todos los pacientes con LLA de células T CD7+ en recaída o refractaria que recibieron el tratamiento, lo que permitió que 9 pacientes se sometieran a un trasplante alogénico de células madre hematopoyéticas en remisión profunda. Las limitaciones incluyeron la pérdida del antígeno CD7 y el riesgo de complicaciones virales.
Células T CAR7 universales con edición de bases para la leucemia linfoblástica aguda de células T
Autores y Publicación
Autores: Robert Chiesa, MD; Christos Georgiadis, Ph.D.; Hebatalla Rashed, MB, B.Ch.; Roland Preece, Ph.D.; Prudence Hardefeldt, MD; Jan Chu, M.Sc.; Jemma Selvage, B.Sc.; además de personas colaboradoras integrantes del grupo CAR T editado en base *. Para información detallada sobre las personas autoras y sus afiliaciones, puede consultarse el enlace correspondiente Información del autor y afiliaciones.
Fecha de publicación: 8 de diciembre de 2025
Referencia: N Engl J Med 2026 ; 394 : 152 – 165
DOI: 10.1056/NEJMoa2505478
Resumen
Antecedentes
El antígeno CD7 ha surgido como una de las dianas más relevantes y prometedoras para el diseño de nuevas estrategias de inmunoterapia en el tratamiento de la leucemia linfoblástica aguda (LLA) de células T en recaída o refractaria. A través del desarrollo de enfoques celulares como la terapia con células T con receptores de antígenos quiméricos (CAR), el uso de la edición de bases ha permitido la generación de células T CAR anti-CD7 (BE-CAR7), logrando la inactivación simultánea de genes como TCRαβ, CD52 y CD7 por medio de triple desaminación C→T. Estudios previos han evidenciado la factibilidad de este método en seres humanos, abriendo un horizonte terapéutico para quienes enfrentan opciones limitadas.
Métodos
En el marco de un estudio de fase 1, se administraron células T BE-CAR7 a una cohorte de nueve personas menores de 16 años con diagnóstico de LLA de células T recidivante o refractaria, quienes previamente recibieron un régimen de linfodepleción basado en fludarabina, ciclofosfamida y alemtuzumab. Este protocolo también incluyó la participación de personas adultas bajo condiciones de acceso compasivo. Una vez alcanzada la remisión al día 28 tras la infusión de células BE-CAR7, las personas participantes fueron candidatas para un trasplante alogénico de células madre hematopoyéticas. El objetivo primario del estudio fue documentar la seguridad del proceso; los objetivos secundarios incluyeron la determinación de la duración de la remisión, la supervivencia libre de enfermedad y la supervivencia global.
Resultados
Un total de once personas (nueve menores y dos adultas) recibieron el tratamiento. Tanto la linfodepleción como las infusiones no generaron eventos adversos inaceptables. En todos los casos, se detectó la presencia de células T CAR7 circulantes tras la infusión, evidenciando la viabilidad de la estrategia terapéutica. Entre las principales complicaciones observadas se encuentran el síndrome de liberación de citocinas, con una presentación que osciló entre los grados 1 y 4, la aparición de exantemas cutáneos transitorios, citopenias multilínea e infecciones oportunistas. Es importante resaltar que la totalidad de las personas tratadas alcanzó remisión morfológica completa con recuperación hematológica incompleta al día 28.
Nueve participantes (82%) lograron una remisión profunda que les permitió la realización de un trasplante alogénico posterior, mientras que las dos personas restantes, quienes presentaban enfermedad mínima residual, continuaron con cuidados paliativos. El trasplante resultó efectivo para eliminar las células T BE-CAR7 remanentes y favoreció la reconstitución multilinaje derivada del donante. Fue frecuente la reactivación de virus latentes, resultando en complicaciones clínicamente relevantes en tres pacientes durante el periodo posterior al trasplante. Globalmente, siete de once personas (64%) se mantuvieron en remisión continua entre 3 y 36 meses después del trasplante, aunque se documentó recaída leucémica acompañada de pérdida de expresión de CD7 en dos casos.
Conclusiones
Las células T universales BE-CAR7 demostraron una notable capacidad para inducir la remisión leucémica en personas con LLA de células T recidivante o refractaria, permitiendo en la mayoría de los casos la realización de un trasplante alogénico de células madre hematopoyéticas con éxito. El estudio fue financiado por el Consejo de Investigación Médica y otras entidades, y está registrado bajo el número ISRCTN: ISRCTN15323014. Estos resultados respaldan la continuidad de la investigación y el desarrollo de terapias avanzadas basadas en la edición genética de células T para el tratamiento de neoplasias hematológicas, marcando un hito en la innovación oncohematológica.