Ana Rita González 1,*,Lizbeth Alexandra Acuña Merchán 2,Jorge A. Alatorre Alejandro 3,Diego Kaen 4,Catalina López-Correa 5,Claudio Martín 6,Allira Attwill 1,Teresa Marinetti 1,Juan Víctor Rocha 1y Carlos Barrios 7
1Policy Wisdom LLC, Quebradillas 00678-2705, Puerto Rico
2Cuenta de Alto Costo, Cra. 45 #103 34 Oficina 802, Bogotá 110111, Colombia
3Investigación Profesional Farmacéutica de la Salud SA de CV, Av. Insurgentes Sur 662-Piso 3, Col. Del Valle, Benito Juárez, Ciudad de México 03100, México
4Centro Oncológico Riojano Integral, La Rioja F5300, Argentina
Int. J. Environ. Res. Salud Pública 2025 , 22 (8), 1220; https://doi.org/10.3390/ijerph22081220
Abstract
Este estudio presenta y analiza la evidencia sobre el valor de las pruebas de biomarcadores y la medicina de precisión en América Latina desde una perspectiva de equidad en salud. Es fundamental explorar cómo aprovechar los beneficios de la medicina de precisión para reducir la brecha de equidad en salud, garantizando que todos los pacientes tengan acceso al mejor tratamiento contra el cáncer. La metodología empleada para desarrollar este documento consiste en una revisión bibliográfica no sistemática, seguida de un proceso de validación y retroalimentación con un grupo de expertos en campos relevantes. La medicina de precisión podría ayudar a reducir las inequidades en salud en América Latina al brindar un mejor diagnóstico y tratamiento para todas las personas con cáncer. Sin embargo, su éxito en el logro de esto depende de la implementación de políticas que promuevan el acceso equitativo. Los hallazgos indican que el panorama político actual en la región latinoamericana no es propicio para mejorar el acceso, el alcance, la calidad o los problemas relacionados con los resultados en la atención del cáncer, ni para alcanzar el máximo potencial de la medicina de precisión. El estudio explora cómo la medicina de precisión puede promover la equidad en salud, y concluye con un análisis de los desafíos y recomendaciones para superarlos.
La OMS enumera las siguientes acciones basadas en evidencia que son necesarias para mejorar la equidad en salud:
- El sector de la salud debe garantizar que haya servicios eficaces y de alta calidad disponibles, accesibles y aceptables para todos, en todas partes, cuando los necesiten.
- El sector de la salud y otros sectores necesitan actuar sobre los determinantes estructurales más amplios de la salud para abordar la distribución desigual del poder y los recursos y mejorar las condiciones de vida diarias.
- El sector de la salud debe asumir el liderazgo en el seguimiento de las inequidades en materia de salud mediante el seguimiento de los resultados sanitarios y la prestación de servicios de salud, así como trabajando con otros sectores para supervisar las condiciones de vida de las personas.
La OMS también ofrece ejemplos clave de políticas y marcos que promueven la equidad en la atención sanitaria. Entre ellos se incluyen los siguientes:
- Rediseñar los sistemas de salud para lograr la equidad, por ejemplo, poniendo en común recursos financieros para mejorar la capacidad redistributiva.
- Priorizar el enfoque de atención primaria de salud, por ejemplo, inversión del 1% del PIB en APS.
- Abordar determinantes estructurales como el sexismo, el racismo, el edadismo, el clasismo y el capacitismo.
- Abordar las normas de género nocivas y las desigualdades de género en las políticas, servicios y programas de salud, y contar con más mujeres en puestos de liderazgo y en los procesos de toma de decisiones.
- Proteger y aumentar la inversión en salud y otros sectores sociales (a través de la cobertura sanitaria universal, la educación y una protección social más amplia).
- Garantizar servicios e infraestructura equitativos tanto en las zonas urbanas como rurales para asegurar que todos puedan llevar una vida saludable.
- Continuar monitoreando las desigualdades en salud y el impacto de las acciones.
Desafíos para la atención del cáncer en América Latina
La creciente carga del cáncer impone una presión significativa sobre las poblaciones y los sistemas de salud, independientemente del nivel de ingresos de cada país. Los elevados costos asociados al diagnóstico y tratamiento, la necesidad de profesionales médicos altamente capacitados, la infraestructura adecuada y la atención a largo plazo constituyen desafíos centrales. A esto se suma que los presupuestos asignados y la movilización de recursos a nivel global resultan claramente insuficientes para afrontar el problema.
Existen marcadas diferencias económicas entre los países de la región, evidentes al comparar sus niveles de ingresos nominales con los ajustados por la paridad del poder adquisitivo (PPA), que refleja el costo de vida. En 2023, por ejemplo, el PIB PPA per cápita y el PIB nominal per cápita fueron considerablemente diferentes en Argentina (USD 30.082 frente a USD 14.187), Brasil (USD 21.107 frente a USD 10.295), Colombia (USD 20.676 frente a USD 6.947), México (USD 24.767 frente a USD 13.790) y Panamá (USD 39.803 frente a USD 18.686).
Un fenómeno preocupante es el aumento de la incidencia del cáncer entre adolescentes y adultos jóvenes desde la década de 1990, cuyas causas siguen siendo poco comprendidas y en gran parte no evaluadas. Esta tendencia representa un reto importante para la detección, diagnóstico, tratamiento y manejo de los casos, y amenaza con incrementar la presión sobre los sistemas de salud y la sociedad en general.
Impacto socioeconómico y psicosocial
El cáncer genera profundas repercusiones socioeconómicas y psicosociales, que se traducen en costos directos e indirectos, alteraciones en el curso de vida, desventajas en el mercado laboral, dificultades en el acceso al apoyo social, afectación de la salud física y mental, y aumento de la vulnerabilidad social. Un estudio de 2023 estimó que el cáncer tendrá un costo de 25,2 billones de dólares internacionales a la economía mundial entre 2020 y 2050, lo que equivale al 0,55% del PIB mundial. En América Latina y el Caribe, los costos totales se estimaron en 960 mil millones de dólares internacionales, con los costos directos en salud representando solo el 12% y la pérdida de productividad el 88% restante. Para el periodo 2020-2050, los costos estimados por país fueron: Argentina, 106 millones; Brasil, 192 millones; Colombia, 91 millones; México, 172 millones; y Panamá, 16 millones (todos en dólares internacionales).
El impacto negativo del cáncer no solo afecta el bienestar físico y mental de los pacientes, sino también el de sus cuidadores y familias. La calidad de vida, entendida como el bienestar físico, mental y socioemocional integral, se ve notablemente reducida. Los tratamientos oncológicos pueden causar efectos secundarios significativos y angustia psicológica, lo que subraya la importancia de que cada paciente reciba el tratamiento más adecuado en el momento oportuno. Estudios realizados en Colombia y Brasil demostraron que los pacientes con cáncer presentan peor calidad de vida que la población general, incluyendo dificultades financieras, dolor, fatiga, trastornos del sueño, depresión y, en el caso de intervenciones médicas invasivas, una calidad de vida aún más deteriorada.
La evidencia proveniente de otros países latinoamericanos confirma que distintos tipos de cáncer afectan de distintas maneras la calidad de vida de los pacientes. Por ejemplo, en el cáncer de mama, los síntomas, los efectos adversos del tratamiento, la disminución del placer sexual y la reducción de expectativas futuras son factores asociados a una baja calidad de vida. La fase de la enfermedad también es determinante: quienes presentan enfermedad metastásica experimentan menor calidad de vida y mayor carga de síntomas. Pacientes mexicanos con cáncer de próstata sufren deterioro tras la cirugía debido a la incontinencia y disfunción eréctil, y los pacientes con cáncer colorrectal manifiestan angustia y estrés postraumático. Todo esto evidencia que el cáncer impone un enorme estrés físico, emocional y financiero no solo en los individuos, sino también en sus familias, comunidades y los sistemas sanitarios.
Frente a este panorama, es fundamental promover estrategias de prevención, diagnóstico temprano, tratamientos de alta calidad y cuidados adecuados para los sobrevivientes. Un diagnóstico precoz y preciso, así como un tratamiento personalizado y menos invasivo, cobran especial relevancia. En este sentido, la medicina de precisión representa una oportunidad para reducir el sufrimiento y los costos asociados al cáncer.
Impacto en cuidadores y contexto social
El cáncer no solo afecta a quienes lo padecen, sino también a sus familias y cuidadores, quienes enfrentan problemas emocionales, sociales, físicos y económicos que repercuten en su calidad de vida. Esta situación es aún más crítica en países con recursos limitados, donde el sistema formal de atención no puede cubrir todas las necesidades, lo que lleva a que familiares, amigos o vecinos asuman el rol de cuidadores informales.
En Latinoamérica, los cuidadores informales son la principal fuente de apoyo para personas en situación de dependencia. Estas personas suelen enfrentar el desafío de compatibilizar sus responsabilidades laborales y personales con el cuidado del paciente, llegando en muchos casos a reducir sus horas de trabajo o incluso abandonar sus empleos. Esto contribuye a agravar las desigualdades sociales y económicas existentes.
El avance en la comprensión de la base molecular de las enfermedades ha permitido a la ciencia médica desarrollar tratamientos innovadores, eficaces y específicos. Sin embargo, estos progresos han puesto de manifiesto desafíos importantes relacionados con la equidad, el acceso, la asequibilidad y la distribución de recursos en el ámbito de la medicina de precisión. Estos retos han intensificado el debate sobre «quién recibe, quién paga y quién cobra» en la atención médica, especialmente en el campo de la oncología.
El cáncer, por ser una enfermedad genética, se encuentra en el centro de esta transformación dada la influencia de las tecnologías genómicas y el desarrollo de fármacos dirigidos. Si bien las terapias dirigidas ofrecen la posibilidad de inhibir el crecimiento tumoral con menor daño a las células normales, enfrentan obstáculos como la resistencia que desarrollan las células cancerosas y la dificultad de crear tratamientos para ciertos objetivos moleculares.
Medicina de precisión y pruebas de biomarcadores
La medicina de precisión se define como un enfoque emergente que considera la variabilidad individual en genes, entorno y estilo de vida al tratar y prevenir enfermedades. Las pruebas de biomarcadores, por su parte, consisten en analizar muestras de tejido, sangre u otros fluidos para identificar genes, proteínas o moléculas asociadas a enfermedades como el cáncer. Estas pruebas pueden detectar alteraciones genéticas o cromosómicas que incrementan el riesgo de desarrollar cáncer y facilitan el diseño de terapias dirigidas, que actúan sobre proteínas responsables del crecimiento y propagación de las células cancerosas.
En el contexto oncológico, la medicina de precisión implica el análisis de mutaciones genéticas y características particulares del tumor de cada paciente para elegir tratamientos personalizados, basándose en el uso de biomarcadores. Este enfoque permite adaptar el tratamiento al perfil genético individual, mejorando la eficacia, reduciendo efectos secundarios innecesarios y evitando el proceso de prueba y error en la elección de terapias.
Desafíos y equidad en la atención oncológica
Pese a los avances en medicina de precisión, persisten disparidades socioeconómicas significativas que afectan los resultados de salud y el acceso a la atención médica. La salud sigue un gradiente social: quienes ocupan posiciones socioeconómicas más bajas enfrentan peores resultados y menor acceso a servicios esenciales, lo que afecta la equidad en la atención oncológica. Por ello, alcanzar la equidad en salud, entendida como la eliminación de diferencias evitables entre grupos sociales, económicos y demográficos, resulta crucial.
El acceso equitativo a la medicina de precisión es fundamental para reducir las desigualdades sanitarias y ofrecer una atención integral a todos los pacientes oncológicos. En América Latina, el cáncer representa una de las principales causas de morbilidad y mortalidad, con una incidencia menor que en países desarrollados pero una mortalidad considerablemente mayor. La razón de mortalidad por cáncer respecto a la incidencia es de 0,50 en la región, comparado con 0,25 en los Estados Unidos, evidenciando peores resultados. Esto se atribuye, en parte, al diagnóstico tardío y a barreras en el acceso al sistema de salud.
Las proyecciones para 2030 anticipan un aumento significativo de casos de cáncer en América del Sur y México, lo que refuerza la necesidad de implementar medicina de precisión para mejorar los resultados en la región.
Desafíos específicos en Latinoamérica
La atención médica eficaz, incluyendo la oncológica, enfrenta numerosos desafíos en Latinoamérica que contribuyen a las inequidades en salud. Entre ellos se encuentran las barreras para acceder a programas de detección temprana, la insuficiencia de infraestructura sanitaria, la escasez de profesionales especializados, la baja calidad de los servicios y la desigual disponibilidad de tratamientos avanzados.
La medicina de precisión tiene el potencial de disminuir las desigualdades en salud al mejorar el diagnóstico y tratamiento de personas con cáncer. Sin embargo, su implementación y aplicación deben ser intencionalmente equitativas para lograr estos objetivos.
Propósito de la revisión y proceso de consenso
Esta revisión sintetiza la evidencia disponible para su análisis y consulta por parte de expertos, con el fin de alcanzar un consenso sobre la relevancia y el valor de la medicina de precisión en la atención oncológica latinoamericana. Dada la ausencia de consenso previo, este trabajo representa un hito fundamental para mejorar el acceso de los pacientes a los mejores tratamientos y avanzar en la equidad en salud en la región.
El proceso de construcción de consenso busca debatir, comprender y acordar las mejores estrategias para aprovechar los beneficios de la medicina de precisión y reducir la brecha de equidad en salud.
Objetivos y metodología
El objetivo principal del documento es presentar y analizar la evidencia sobre el valor de las pruebas de biomarcadores y la medicina de precisión en Latinoamérica, centrándose en la equidad en salud. Se busca fomentar el diálogo sobre cómo ampliar el acceso de los pacientes a las mejores opciones de tratamiento oncológico, con especial atención a Argentina, Brasil, Colombia, México y Panamá.
Para ello, se realizó una revisión no sistemática de literatura, validada posteriormente por expertos. La evidencia se recopiló y analizó en tres niveles: global, regional y nacional, enfocándose en estudios revisados por pares, políticas nacionales e internacionales, y guías relevantes. Se priorizaron investigaciones que aportaran datos empíricos o análisis de políticas sobre: situación actual de la atención oncológica en Latinoamérica, panorama político y adopción de la medicina de precisión, beneficios y equidad en salud.
Los expertos seleccionados participaron en un proceso de revisión y validación, aportando sus conocimientos en oncología, cirugía, medicina interna, biociencias y genética humana. Los hallazgos fueron organizados en un documento de trabajo que aborda cáncer y equidad en salud, el rol de la medicina de precisión, el panorama político, los desafíos y las recomendaciones para superar las brechas identificadas.
Antecedentes: Cáncer en Latinoamérica y el Caribe
El cáncer constituye una de las principales causas de muerte en Latinoamérica y el Caribe, generando un importante problema de salud pública asociado a elevados costos sociales y económicos. Se estima que entre el 30% y el 50% de las muertes por cáncer podrían evitarse mediante la reducción de factores de riesgo y la implementación de estrategias de prevención basadas en evidencia. Además, la carga de cáncer en la región se prevé que aumente un 67% hacia 2040, impulsada por el crecimiento y envejecimiento poblacional y factores ambientales y de estilo de vida.
La atención oncológica más precisa y específica depende cada vez más de la medicina de precisión, donde las pruebas de biomarcadores guían las decisiones clínicas para lograr mejores resultados y calidad de vida en los pacientes.
Desigualdades socioeconómicas y equidad en salud
Las desigualdades socioeconómicas se observan en todo el espectro del cáncer, desde la exposición a factores de riesgo hasta el acceso a intervenciones eficaces, diagnóstico, tratamiento y cuidados paliativos. América Latina, con gran diversidad socioeconómica y altos índices de pobreza, enfrenta retos particulares en la equidad en salud.
Si bien las herramientas de medicina de precisión y biomarcadores pueden mejorar los resultados, su acceso e implementación también están condicionados por cuestiones de equidad, pudiendo ampliar o reducir las desigualdades existentes.
Impacto del cáncer en cifras y calidad de vida
En 2022, se notificaron 20 millones de nuevos casos de cáncer a nivel mundial, de los cuales aproximadamente 1,5 millones se registraron en Latinoamérica y el Caribe, con una mortalidad igualmente significativa. Se estima que hasta la mitad de estos casos podrían haberse evitado. Las proyecciones indican que el número anual de casos en la región se duplicará para 2050, lo que subraya la urgencia de mejorar la atención.
Las diferencias económicas entre los países de la región son notables y el impacto del cáncer se extiende más allá de los costos directos en salud, afectando la productividad, el bienestar psicosocial y la calidad de vida de pacientes y cuidadores. Los efectos adversos de los tratamientos y la carga emocional hacen indispensable asegurar que cada paciente reciba el tratamiento adecuado en el momento oportuno.
Desafíos para la atención del cáncer
El control efectivo del cáncer exige un enfoque integral que incluya prevención, cribado, diagnóstico temprano, tratamiento rápido, seguimiento y cuidados paliativos. Latinoamérica enfrenta obstáculos como retrasos en diagnóstico y tratamiento, falta de acceso a medicamentos de alto costo, inversión insuficiente y registros de cáncer deficientes.
Las barreras financieras, geográficas y organizacionales, junto con la fragmentación de los sistemas de salud y la baja alfabetización en salud, contribuyen al diagnóstico tardío y a peores resultados. Además, la atención pública suele tener menores tasas de detección y mayor prevalencia de enfermedad avanzada que la privada. La medicina de precisión, en muchos casos, está restringida al sector privado, lo que limita el acceso a terapias innovadoras.
Equidad en salud y cáncer
La equidad en salud, según la OMS, implica la ausencia de diferencias injustas, evitables o remediables entre grupos de población. La atención es equitativa cuando la asignación y acceso a recursos responde a las necesidades de salud, permitiendo a todos alcanzar su máximo potencial. La distinción entre desigualdad e inequidad es fundamental: la inequidad implica diferencias innecesarias, evitables y moralmente incorrectas, mientras que la desigualdad puede explicarse por factores naturales o inevitables.
La equidad en salud es un principio adoptado por organismos internacionales y ha sido central en los objetivos globales de desarrollo. La evidencia demuestra que las oportunidades para una buena salud dependen de factores sociales, económicos, demográficos y geográficos, que influyen en el acceso a tecnologías como la genómica y los biomarcadores.
La estructura de los sistemas de salud, especialmente en América Latina donde prevalece la fragmentación, influye directamente en la equidad. Lograrla requiere acciones intencionales desde la atención médica y políticas públicas que aborden la pobreza, discriminación y falta de acceso a recursos. Las políticas y marcos recomendados por la OMS incluyen rediseñar sistemas de salud para mejorar la redistribución, invertir en atención primaria y abordar los determinantes estructurales de la inequidad.
La equidad en atención oncológica se traduce en que todos tengan las mismas oportunidades de prevenir, detectar y tratar el cáncer adecuadamente, independientemente de su situación socioeconómica o ubicación.
Las barreras específicas para acceder a la atención médica incluyen factores económicos, geográficos, epidemiológicos y culturales [ 94 ]. Los altos costos de bolsillo para los servicios de atención médica pueden impedir que las personas accedan a la atención; las personas en áreas remotas o rurales pueden no tener suficientes instalaciones de atención médica o profesionales disponibles cerca, y pueden no llegar a centros de atención secundaria o terciaria capaces de confirmar diagnósticos de cáncer; los brotes y la prevalencia de enfermedades pueden sobrecargar los sistemas de atención médica, limitando su capacidad para brindar atención adecuada a todas las personas; los factores culturales pueden influir en el comportamiento de búsqueda de atención médica y la relación proveedor de atención médica-paciente; y los sistemas de salud débiles, que incluyen infraestructura insuficiente, sistemas de referencia ineficientes, falta de trabajadores de la salud y cadenas de suministro inadecuadas, pueden impedir la prestación de servicios de atención médica efectivos [ 15 , 95 , 96 , 97 , 98 , 99 , 100 ].
En América Latina, la cobertura universal de salud (CUS) aún es deficiente [ 101 ], a pesar de ser una agenda política importante para muchos países, incluidos los analizados en este estudio [ 102 ]. Lograr la cobertura universal por sí solo no garantiza un acceso equitativo, ya que las barreras sistémicas y los determinantes sociales de la salud a menudo impiden que ciertas poblaciones se beneficien plenamente de los servicios disponibles. De hecho, el concepto de cobertura universal a veces puede entrar en conflicto con el objetivo de equidad. Si bien la cobertura universal tiene como objetivo brindar acceso a la atención médica para todos, la equidad se centra en satisfacer las necesidades específicas de las personas y garantizar que participen en los procesos de toma de decisiones. Aunque la definición de cobertura universal de salud de la OPS incorpora la equidad, al afirmar que «La salud universal no se trata solo de garantizar que todos estén cubiertos, sino que todos tengan acceso a la atención cuando la necesiten, dondequiera que estén» [ 103 ], no todos los países de la región que han avanzado hacia la CUS tienen evidencia suficiente para evaluar si se ha logrado un acceso equitativo a la atención médica en la práctica [ 102 ]. Los servicios de atención sanitaria en los países de enfoque son generalmente accesibles y asequibles, pero aún existen desafíos para satisfacer las necesidades de salud de la población y gestionar los costos crecientes de la atención sanitaria [ 102 ]. Aunque la atención del cáncer está cubierta por casi todos los servicios públicos, los medicamentos de alto costo se incluyen con menos frecuencia en el paquete de servicios del sistema público y, por lo tanto, a menudo son inaccesibles [ 54 ].
En Argentina [ 104 ], Brasil [ 105 ], Colombia [ 106 ], México [ 107 ] y Panamá [ 108 ], los ciudadanos tienen derecho constitucional a la salud. El Estado debe proporcionar acceso integral, universal e igualitario al sistema de atención médica por ley, lo que puede desencadenar casos judiciales relacionados con la atención médica, donde se presenta una demanda contra el gobierno para obtener acceso a terapias. Este proceso puede aumentar la inequidad en el acceso a los medicamentos, ya que solo aquellos que pueden permitirse asumir los costos legales recurren a esta vía [ 109 ]. En general, la prestación de atención oncológica en los sistemas de salud de América Latina enfrenta importantes limitaciones con respecto al acceso a profesionales de la salud capacitados y nuevas terapias e instalaciones adecuadas para la atención oncológica, debido a presupuestos distribuidos inadecuadamente entre ubicaciones y barreras geográficas y culturales [ 110 ]. Los factores geográficos y relacionados con el servicio, como las distancias de viaje y los tiempos de espera, a menudo juegan un papel determinante en el acceso oportuno a la atención médica [ 111 ] y representan desafíos significativos en América Latina. En Brasil, por ejemplo, más de la mitad de los pacientes con cáncer deben viajar desde sus lugares de origen a otra ciudad para recibir tratamiento [ 112 ], y barreras geográficas similares, como la disponibilidad y el costo del transporte, la calidad de las carreteras y los largos tiempos de viaje, también se han reportado en estudios en Argentina, Colombia y México [ 113 , 114 ].
Los sistemas de salud deben promover el acceso a una atención oncológica social, cultural y lingüísticamente apropiada, respetuosa y de alta calidad [ 115 ], con el potencial de reducir las desigualdades en la incidencia del cáncer y promover la equidad en salud [ 116 ]. Promover una atención oncológica equitativa es necesario para garantizar que los pacientes puedan acceder a servicios de prevención y diagnóstico oportunos y adecuados, y recibir una atención óptima, logrando así resultados de salud equitativos. Este estudio busca resaltar la importancia y el valor de promover las pruebas de biomarcadores y la medicina de precisión en Latinoamérica, al tiempo que enfatiza la necesidad de garantizar la equidad en salud.
La genómica es el estudio del conjunto completo de ADN, incluyendo todos sus genes, en una persona u otro organismo [ 130 ]. Algunas tecnologías ómicas incluyen las siguientes [ 131 ]:
- Epigenómica: modificaciones químicas del ADN, histonas, proteínas de cromatina no histonas y ARN nuclear;
- Transcriptómica: Patrón de expresión genética en una célula/tejido;
- Proteómica: Proteínas expresadas por un sistema biológico;
- Metabolómica: Metabolitos y sus fluctuaciones relacionadas con factores internos (genéticos) y externos (ambiente);
- Fenómica: Resultados físicos y químicos mensurables de las interacciones entre los genes y el medio ambiente que experimentan los individuos y que influyen en sus fenotipos.
Revisión de la literatura
La revisión de la literatura se organiza en dos grandes apartados: la Sección 4.1, que aborda la medicina de precisión y su aplicación en oncología, y la Sección 4.2, que examina los desafíos científicos, de implementación, económicos, políticos y regulatorios en torno al desarrollo y la implementación de la medicina de precisión.
Revisión de la literatura sobre medicina de precisión, sus aplicaciones, avances y perspectivas futuras
Esta sección ofrece una visión general de la literatura relevante en torno a la medicina de precisión, enfocándose especialmente en su papel en el cuidado del cáncer a través del uso de biomarcadores. Se discuten los avances actuales, las perspectivas futuras para el diagnóstico y la eficacia del tratamiento, y se analizan aspectos vinculados a la equidad en salud.
Medicina de precisión
El Instituto Nacional de Investigación del Genoma Humano de EE. UU. define la medicina de precisión como un enfoque innovador que utiliza información genómica, ambiental y de estilo de vida de las personas para orientar sus decisiones médicas. Su objetivo principal es proporcionar mayor precisión en la prevención, el diagnóstico y el tratamiento de las enfermedades.
Históricamente, la medicina siempre ha perseguido la personalización, adaptando los tratamientos a las necesidades individuales. Ya en la antigua Grecia, se reconocía que no todos los tratamientos son adecuados para todos los pacientes y que las características individuales, como el estado de salud y el estilo de vida, deben ser consideradas.
Sin embargo, aunque la medicina de precisión está intrínsecamente centrada en el paciente, no necesariamente implica que la atención siempre lo esté. La atención centrada en el paciente requiere incorporar sus preferencias, necesidades e inquietudes, garantizando su participación informada en las decisiones de tratamiento. Un marco propuesto en 2021, denominado «PEAR» (repositorio de evaluación de evidencia basado en la población), busca personalizar tratamientos considerando tanto perfiles biológicos como preferencias de los pacientes, argumentando que estos enfoques graduales y centrados en el paciente mejoran la atención y los resultados.
El avance científico en genómica, especialmente tras la finalización del Proyecto Genoma Humano y la aparición de la secuenciación de próxima generación, ha reducido notablemente los costos y facilitado la identificación de marcadores genéticos asociados a enfermedades. Así, la medicina de precisión se ha expandido más allá de los genes, integrando también factores ambientales y de estilo de vida.
La incorporación de la medicina de precisión en la práctica clínica depende de herramientas como las ómicas (genómica, proteómica, transcriptómica), la inteligencia artificial y el aprendizaje automático, además de la integración de factores ambientales, sociales y conductuales. La genómica, por ejemplo, estudia el conjunto completo de ADN de un organismo, mientras que la epigenómica, transcriptómica, proteómica, metabolómica y fenómica exploran otros niveles de complejidad biológica.
Factores conductuales y sociales —dieta, ejercicio, salud mental, tabaco, apoyo social— y ambientales influyen en la salud y la enfermedad y son componentes relevantes en la medicina de precisión. Los estudios genómicos han evidenciado la necesidad de combinar datos genéticos y epigenéticos con información ambiental y conductual.
Para la aplicación clínica de la medicina de precisión, son esenciales datos, herramientas y sistemas robustos, una regulación clara y la participación de actores clave. El big data, la inteligencia artificial y el aprendizaje automático son fundamentales para el análisis de los complejos datos generados, contribuyendo al desarrollo de modelos predictivos y a la toma de decisiones clínicas. Asimismo, la regulación debe garantizar la privacidad y la ética, fomentando la confianza y la transparencia.
La formación de los profesionales médicos es crucial para prescribir pruebas e interpretar resultados genómicos, lo que puede requerir reformas en los planes de estudio y capacitación continua. Además, la colaboración entre universidades, sistemas de salud, industrias y gobiernos es necesaria para construir marcos regulatorios adecuados, especialmente en regiones como América Latina, donde las regulaciones pueden ser restrictivas o poco flexibles.
La medicina de precisión se basa en el uso de biomarcadores específicos de la enfermedad. Según la OMS, los biomarcadores son mediciones que reflejan interacciones entre sistemas biológicos y posibles peligros, y pueden ser funcionales, fisiológicas, bioquímicas o moleculares. El glosario BEST los clasifica en siete categorías: susceptibilidad/riesgo, diagnóstico, monitoreo, pronóstico, predictivo, farmacodinámico/respuesta y seguridad. Los biomarcadores pueden ser diagnósticos, pronósticos o predictivos, y su uso permite personalizar la atención, optimizar tratamientos y prever respuestas.
El valor de la medicina de precisión
La medicina de precisión representa un avance sustancial en el diagnóstico y tratamiento del cáncer, apoyada por una creciente literatura científica que describe sus beneficios y cómo ha transformado la atención oncológica. Esta aproximación contribuye de manera significativa a la atención centrada en el paciente, ya que permite una mejor comprensión de la patogénesis de las enfermedades e impulsa una transición desde la medicina empírica hacia estrategias terapéuticas dirigidas y personalizadas mediante el uso de biomarcadores y diagnósticos complementarios [188].
En el ámbito oncológico, la medicina de precisión cumple un rol crucial al personalizar las estrategias preventivas y adaptar los tratamientos a las características individuales de cada paciente, como los perfiles genéticos. Si bien se reconocen beneficios clínicos potencialmente importantes, su demostración en la práctica clínica puede presentar dificultades. Numerosos estudios sostienen que la adecuación de terapias según la composición genética del cáncer puede traducirse en mejores resultados, como un aumento en la supervivencia sin progresión, mayores tasas de respuesta, mayor tiempo hasta el fracaso del tratamiento y mejor supervivencia global en distintos tipos de cáncer [189, 190, 191, 192, 193]. Sin embargo, no todos los estudios han evidenciado resultados de salud positivos de manera consistente para todos los tipos de cáncer, y algunos hallazgos estadísticamente significativos pueden tener aplicabilidad limitada en el mundo real [189, 190, 191]. Esto resalta la importancia de sostener la inversión en investigación científica para maximizar el potencial de la medicina de precisión en oncología.
Por otro lado, la evidencia sobre los beneficios en costo-efectividad de la medicina de precisión resulta más difícil de establecer. Algunos trabajos sugieren que la medicina de precisión es al menos tan costo-efectiva como la atención habitual, aunque no pueden extraerse conclusiones firmes debido a limitaciones en el diseño de los estudios y en el manejo de los datos [194, 195]. Además, los pacientes que reciben terapias oncológicas de precisión suelen requerir tratamientos complementarios, como quimioterapia, radioterapia, manejo de toxicidad y cuidados de apoyo, factores que pueden incidir tanto en la efectividad como en la asequibilidad del tratamiento. Los biomarcadores permiten personalizar la elección entre modalidades terapéuticas, como quimioterapia o radioterapia [196], mientras que las toxicidades asociadas a nuevas terapias dirigidas exigen un manejo activo [197]. Los planes de cuidados de apoyo son esenciales para minimizar daños y optimizar resultados, atendiendo tanto al tumor como al bienestar general del paciente [198]. Por ello, la introducción de estos tratamientos paralelos debe contemplarse en el balance sobre la eficacia y asequibilidad de la medicina de precisión.
Es fundamental desarrollar estudios de costo-efectividad más robustos, que consideren diversos tipos de cáncer, ya que el impacto de la medicina de precisión varía según el tumor. El éxito de su implementación puede medirse por la reducción de costos asociados a tratamientos ineficaces y el ahorro general derivado de estos enfoques [141]. Así, la medicina de precisión posee un gran potencial para revolucionar la atención sanitaria al mejorar la precisión diagnóstica, la eficacia terapéutica, la minimización de efectos adversos y, en última instancia, su rentabilidad para pacientes y sistemas de salud.
El uso de biomarcadores en medicina de precisión orienta las decisiones terapéuticas a partir de características genéticas, moleculares o bioquímicas individuales, colocando al paciente como eje central de la atención. Existe una superposición entre la medicina de precisión y la atención centrada en el paciente, dado que la primera promueve una mayor consideración clínica de las capacidades y condiciones del paciente. De este modo, la medicina de precisión no solo dirige la terapia y los procedimientos preventivos a quienes pueden beneficiarse, sino que también facilita la toma de decisiones informadas sobre salud y estilo de vida, promoviendo la participación activa del paciente, incluso en el consentimiento informado para pruebas genéticas [199].
Las pruebas de biomarcadores en cáncer consisten en el perfilado de tumores o fluidos corporales para detectar alteraciones en ADN, ARN, proteínas u otras biomoléculas [200]. Estas pruebas tienen aplicaciones potenciales en la evaluación de riesgos, detección, diagnóstico diferencial, determinación de pronóstico, predicción de respuesta al tratamiento y seguimiento de la progresión, siendo fundamentales en todas las etapas de la enfermedad e incluso antes del diagnóstico clínico [201].
Hasta la fecha, los biomarcadores genómicos han sido los más exitosos, aunque se están desarrollando y evaluando otros, como los de proteínas y transcriptómica [157]. Se dispone de un número creciente de pruebas genómicas en la práctica clínica, incluyendo el análisis del genoma tumoral para terapias dirigidas [130]. Ejemplos de biomarcadores tumorales con aplicaciones clínicas incluyen HER2, EGFR y ALK, que han permitido desarrollar terapias dirigidas aprobadas por la FDA de EE. UU.:
- HER2: Sobreexpresado en el 15-20% de cánceres de mama y otros tumores como gástrico, colon y cabeza y cuello. Los tratamientos aprobados incluyen trastuzumab, pertuzumab, ado-trastuzumab emtansina, lapatinib y trastuzumab deruxtecán.
- EGFR: Expresado en la superficie celular, con mutaciones activadoras comunes en adenocarcinomas, especialmente en no fumadores, mujeres y personas de ascendencia asiática. Las terapias incluyen gefitinib, erlotinib, afatinib, dacomitinib y osimertinib.
- ALK: Las fusiones de ALK generan vías oncogénicas en cáncer de pulmón de células no pequeñas. Las terapias dirigidas incluyen crizotinib, ceritinib, alectinib y lorlatinib.
El Instituto Nacional del Cáncer de EE. UU. ofrece una lista más amplia de biomarcadores comúnmente estudiados en diferentes tipos de muestras [200, 203].
En el contexto de Latinoamérica, diversos estudios han evaluado los procesos de aprobación de nuevos medicamentos oncológicos en comparación con otras agencias regulatorias internacionales, como la FDA y la EMA, identificando menor cantidad de aprobaciones y plazos más extensos en la región [204, 205]. Además, se detectan barreras de acceso a terapias dirigidas, aun cuando estén aprobadas por las agencias regulatorias nacionales. Por ejemplo, el trastuzumab, aunque autorizado en la mayoría de los países latinoamericanos, suele no estar disponible en el sector público para tratamiento de la enfermedad metastásica [206, 207]. Esta situación también afecta la incorporación de pruebas de biomarcadores.
Panorama de políticas de medicina de precisión y oncología en América Latina
En esta sección se presenta un análisis detallado de las políticas y legislaciones tanto regionales como nacionales vigentes en materia de cáncer en América Latina, con especial atención a la integración de la medicina de precisión en dichos marcos y a las estrategias e iniciativas existentes en este ámbito. Este repaso es relevante, ya que los marcos de acción regionales y nacionales reflejan la inclusión de la temática en la agenda política y exponen las intenciones y métodos para abordarla.
Planes regionales y nacionales de control del cáncer
Los planes regionales contra el cáncer funcionan como guías estratégicas para orientar las intervenciones y la formulación de políticas en los países. Los planes nacionales de control del cáncer, en tanto, constituyen herramientas fundamentales para reducir la incidencia y mortalidad por cáncer, optimizando los recursos disponibles y mejorando la calidad de vida de los pacientes. El contexto político de cada región y país juega un papel esencial en la promoción de avances en la atención médica, a través de iniciativas que mejoran los resultados de diagnóstico y tratamiento, favorecen una asignación de recursos más eficiente y, en última instancia, impactan positivamente en la atención al paciente y la salud pública. Todo esto puede ser potenciado mediante la adopción de la medicina de precisión. Para brindar un punto de referencia, la sección incluye una breve comparación del panorama de políticas en Estados Unidos y Europa.
Situación regional: OPS y OMS
A nivel regional, la Organización Panamericana de la Salud (OPS) no cuenta con un plan de acción o política integral sobre el cáncer, aunque ha desarrollado iniciativas específicas como el Plan de acción para la prevención y el control del cáncer cervicouterino 2018-2030, resúmenes de conocimientos sobre el cáncer de mama y el Grupo de Trabajo de la Iniciativa Global de Cáncer Infantil para América Latina y el Caribe. Sin embargo, ni la OPS ni la Organización Mundial de la Salud (OMS) ofrecen actualmente marcos políticos que orienten la implementación de la medicina de precisión, y el tema ha recibido escasa atención por parte de estos organismos internacionales.
Políticas nacionales sobre cáncer y medicina de precisión
En el ámbito nacional, los cinco países analizados cuentan con planes nacionales de control del cáncer actualizados, los cuales contemplan estrategias para la atención clínica, la investigación, el desarrollo y la vigilancia. Por ejemplo, en Colombia, el plan nacional tiene vigencia entre 2012 y 2021; tras su vencimiento, el Ministerio de Salud y el Instituto Nacional del Cáncer decidieron integrar el nuevo Plan de Control del Cáncer dentro del Plan Decenal de Salud Pública 2022-2031. Además, en estos países se ha promulgado legislación destinada a respaldar la atención integral del cáncer, mediante la creación de comisiones para la detección temprana, la garantía de servicios integrales, la formación de unidades oncológicas y el establecimiento de sistemas de información. La actualización e implementación continua de estos planes es clave para enfrentar los desafíos y mejorar la atención en la región. Cabe mencionar que no todos los países de Latinoamérica disponen de planes nacionales de control del cáncer o de planes para enfermedades no transmisibles que incluyan el cáncer, y la existencia de un plan no garantiza su efectiva implementación. Adicionalmente, se ha observado que el principio de equidad no está suficientemente integrado en los planes nacionales de control del cáncer de la región.
Inclusión de biomarcadores y medicina de precisión en las políticas
A pesar de que todos los planes nacionales de los países estudiados fueron emitidos después de 2018, ninguno hace referencia explícita a biomarcadores ni marcadores genéticos, ni en la legislación de apoyo al cáncer ni en los documentos estratégicos. En relación con la medicina de precisión, el Plan Nacional de Control del Cáncer 2018-2022 de Argentina menciona la necesidad de fortalecer la investigación básica, clínica y traslacional para garantizar diagnósticos oportunos y tratamientos adecuados, con foco en el concepto general de medicina de precisión. Por su parte, la Política Nacional para la Prevención y el Control del Cáncer 2023 de Brasil contempla el objetivo de incorporar tecnologías diagnósticas y terapéuticas más precisas y menos invasivas. Sin embargo, ninguno de los planes profundiza en la medicina de precisión ni en los biomarcadores, ni incluye disposiciones concretas para su adopción y desarrollo. En general, pocos países latinoamericanos han incorporado la medicina de precisión en sus planes de control del cáncer, principalmente porque fueron elaborados antes de que existiera suficiente evidencia sobre su aplicación clínica. Tampoco existe evidencia que indique que los planes sucesores vayan a incluir la medicina de precisión como parte de sus estrategias. La existencia de políticas y leyes nacionales que contemplen la medicina de precisión podría facilitar su implementación en oncología a nivel nacional, pero la falta de estrategias específicas puede ser un obstáculo para su desarrollo y adopción en la región.
Estrategias e iniciativas nacionales en medicina de precisión
Si bien no se ha identificado legislación específica sobre medicina de precisión, en algunos países latinoamericanos se han impulsado estrategias e iniciativas para promover su desarrollo, reconociendo los beneficios potenciales para pacientes, proveedores de salud, sistemas sanitarios y desarrolladores de medicamentos. En Argentina y Brasil, por ejemplo, se han implementado proyectos para mapear los genomas de la población y crear biobancos genómicos, lo que permite una mejor investigación, capacitación de profesionales y beneficios para la población local. En Argentina, el gobierno ha financiado proyectos estratégicos a través del Ministerio de Ciencia, Tecnología e Innovación, orientados a avanzar en la medicina de precisión, tales como la implementación de plataformas de secuenciación masiva de segunda generación para mejorar tratamientos oncológicos y el desarrollo de plataformas de I+D para facilitar la rápida traducción de productos y servicios de diagnóstico en la clínica. El Ministerio de Ciencia, Tecnología e Innovación considera estos proyectos como una consecuencia natural de los avances recientes en tecnologías de análisis genómico y en informática médica, contribuyendo a crear sistemas de atención personalizados y eficientes.
En México, la Ley General de Salud contempla disposiciones para garantizar la propiedad del genoma por parte del individuo, prevenir la discriminación genética, exigir consentimiento explícito para estudios genómicos, proteger la confidencialidad de los datos genéticos, respetar las preferencias sobre el acceso a los resultados de pruebas genéticas y priorizar la protección de la salud en la investigación e innovación. En 2023, se propuso incorporar la medicina de precisión en la Ley General de Salud, promoviendo además la investigación genética y molecular. Estas iniciativas reflejan el creciente interés en la medicina de precisión a nivel mundial.
Comparación internacional: Estados Unidos y Europa
El desarrollo de políticas en medicina de precisión es considerablemente más avanzado en Estados Unidos y Europa, donde existen programas, estrategias e iniciativas específicas para fomentar su desarrollo e implementación. En Estados Unidos, se han observado tasas crecientes de pruebas de biomarcadores en cáncer colorrectal y de pulmón, aunque persisten desigualdades en el acceso y la cobertura por parte de los seguros de salud. En Europa, el acceso a las pruebas de biomarcadores varía entre países, siendo mayor en aquellos con procesos públicos de reembolso establecidos y con inversiones más altas en salud. Además, la calidad se mide por la participación en esquemas de garantía y acreditación.
El gobierno estadounidense ha lanzado varias iniciativas, como la Iniciativa de Medicina de Precisión de 2015, directrices de la FDA para agilizar pruebas genómicas, y programas del Instituto Nacional del Cáncer y de los Institutos Nacionales de Salud orientados a construir grandes cohortes de investigación, impulsar la equidad y avanzar en la ciencia de las disparidades en salud. En Europa, las políticas centrales buscan proteger la salud pública y abarcan la estandarización de prácticas médicas, big data, interoperabilidad, innovación, prevención y participación ciudadana. Países como Italia, Reino Unido, Estonia, Suecia, Dinamarca, Finlandia, Luxemburgo y España han integrado la medicina de precisión en sus estrategias nacionales, enfatizando la genómica, los biobancos y la salud basada en datos.
Lecciones de otras regiones: Asia
Las iniciativas en Asia ofrecen ejemplos adicionales de enfoques para la implementación de la medicina de precisión que pueden servir de referencia para Latinoamérica. En Tailandia, la colaboración entre organismos gubernamentales permitió el desarrollo de la iniciativa Genomics Thailand, destinada a crear una base de datos genómica a nivel poblacional y facilitar la integración de la genómica en políticas de salud. Singapur lanzó en 2017 una iniciativa nacional de medicina de precisión a diez años, con el objetivo de establecer la excelencia en investigación y mejorar la salud de la población mediante aplicaciones clínicas sostenibles y relevantes. En Indonesia, aunque no existe un marco jurídico integral, se han implementado decretos ministeriales para la gestión de biobancos y el desarrollo de servicios de medicina de precisión.
Perspectiva regional y conclusiones
La cronología de los hitos clave en medicina de precisión y genómica en Estados Unidos, Europa y Latinoamérica evidencia la importancia de contar con organismos regionales que supervisen y promuevan el avance y la adopción de la medicina de precisión. Mientras que en la Unión Europea los avances impulsan simultáneamente a varios países, en Latinoamérica los logros suelen ser aislados y corresponden a pocos países. Hasta el momento, no existe una iniciativa de alcance regional comparable en Latinoamérica, lo que subraya el valor de fomentar la colaboración y el desarrollo de estrategias comunes para avanzar en la medicina de precisión en la región.
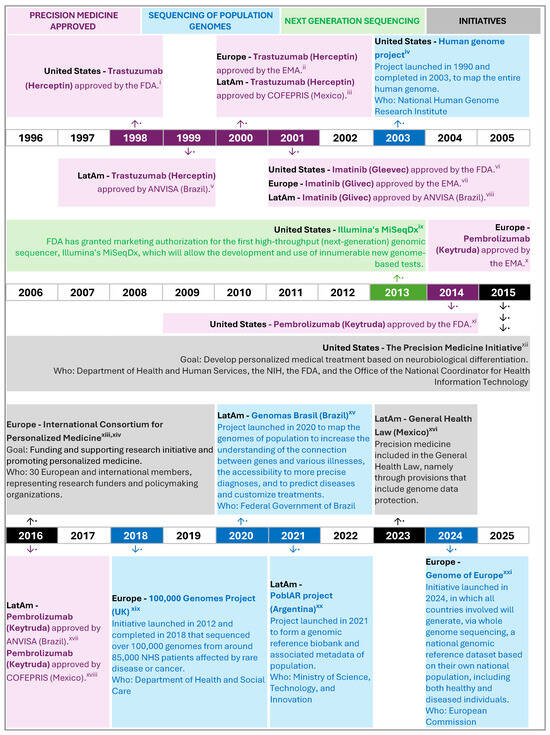
Iniciativas internacionales en genética médica y su impacto en la equidad en salud
Experiencias en Asia: el caso de Malasia y la cooperación regional
En Malasia, la existencia de una directriz nacional sobre los servicios de genética médica y/o pruebas genéticas proporciona un marco de supervisión ética para el uso de la genética en la atención sanitaria. Este lineamiento establece bases para garantizar la utilización responsable y segura de las tecnologías genéticas, con especial atención a la protección de los derechos de los pacientes y a la integridad del proceso asistencial.
Paralelamente, las sociedades médicas en el país han desempeñado un papel activo en la promoción de campañas de concienciación dirigidas a la terapia oncológica personalizada para determinados tipos de cáncer. Estas campañas buscan sensibilizar tanto a profesionales como a la población general sobre los beneficios potenciales de las terapias dirigidas, favoreciendo una mayor aceptación y demanda de este tipo de atención.
En el plano regional, desde 2012 se ha consolidado la Red de Investigación en Farmacogenómica del Sudeste Asiático. Esta iniciativa, que reúne a ocho países asiáticos, tiene como propósito central facilitar, fortalecer y coordinar la investigación en farmacogenómica. A través de la cooperación regional, se busca optimizar el desarrollo de capacidades, compartir recursos y generar evidencia relevante para la implementación de la farmacogenómica en la práctica clínica, contribuyendo a la equidad en el acceso a innovaciones terapéuticas en la región.
La experiencia africana: H3Africa como modelo de coordinación y desarrollo de capacidades
En África, la Iniciativa H3Africa, respaldada financieramente por los Institutos Nacionales de Salud (NIH) y el Wellcome Trust, representa un ejemplo destacado de apoyo a la investigación innovadora sobre los factores genéticos y ambientales que influyen en las enfermedades que afectan a las poblaciones del continente. Más allá del financiamiento de proyectos de investigación, H3Africa impulsa el fortalecimiento de la infraestructura a través del desarrollo de capacidades institucionales y la creación de biorrepositorios. Estos recursos compartidos permiten el almacenamiento y manejo de bioespecímenes, facilitando el acceso a materiales biológicos para la investigación colaborativa.
El consorcio H3Africa abarca más de 30 de los 55 países africanos, integrando a más de 500 miembros. Se ha destacado por el desarrollo de políticas robustas para el intercambio de muestras y datos, lo que promueve la colaboración interpaís y maximiza el impacto de los hallazgos científicos. Esta labor coordinada se considera un ejemplo de referencia en cuanto a la promoción de la genómica y la genética en el continente, ilustrando cómo la cooperación regional y el desarrollo de capacidades pueden acelerar el avance científico y mejorar el acceso equitativo a los beneficios de la medicina de precisión.
El potencial transformador de la medicina de precisión
La medicina de precisión ofrece enormes posibilidades para mejorar la atención preventiva, optimizar el diagnóstico, brindar tratamientos más eficaces y personalizados, reducir efectos secundarios y, potencialmente, aportar rentabilidad en la atención oncológica. Si se implementa de manera equitativa en los sistemas de salud, el uso de biomarcadores puede contribuir significativamente a la equidad sanitaria, garantizando que todos los pacientes reciban atención adaptada a sus perfiles genéticos, moleculares y ambientales, independientemente de su condición socioeconómica. De este modo, la medicina de precisión, centrada en el paciente, puede empoderarlo y fortalecer la relación con los profesionales sanitarios.
Inequidades en el acceso y la necesidad de evidencia local
Aunque la evidencia sobre la adopción de la medicina de precisión en cáncer en Latinoamérica es limitada, los datos disponibles muestran inequidades en el acceso a pruebas de biomarcadores, lo cual restringe los beneficios potenciales de esta estrategia. Actualmente, la industria farmacéutica lidera y financia la mayoría de las iniciativas en la región, promoviendo algunos biomarcadores mediante campañas y pruebas diagnósticas gratuitas. Sin embargo, es fundamental que los países fortalezcan sus propias capacidades, priorizando la identificación de aplicaciones costo-efectivas, la integración de la multiómica y la validación de nuevas técnicas adaptadas a los contextos latinoamericanos.
Riesgos y oportunidades en la implementación
La medicina de precisión está en pleno auge y puede transformar la medicina en todas sus áreas. No obstante, su adopción debe estar guiada por políticas estructuradas que aseguren una integración ordenada y equitativa; de lo contrario, existe el riesgo de profundizar las desigualdades. En las primeras etapas, es probable que la medicina de precisión amplíe la brecha de acceso, ya que se limitará a quienes puedan costearla o estén más cerca de hacerlo. Sin embargo, a largo plazo, su implementación estratégica y sistemática podría mejorar la equidad en salud.
Acceso, monitoreo y sostenibilidad
El acceso equitativo a pruebas diagnósticas es fundamental, aunque no garantiza el tratamiento inmediato, por lo que debe priorizarse su disponibilidad en todas las regiones. Es igualmente clave establecer mecanismos sólidos de monitoreo y evaluación para medir el impacto de la medicina de precisión en los sistemas sanitarios, así como asegurar la sostenibilidad económica de las políticas implementadas, equilibrando innovación, asequibilidad e inclusión. También resulta esencial considerar las perspectivas de poblaciones especialmente afectadas por la falta de acceso.
Desafíos inmediatos y áreas de inversión prioritaria
Para implementar la medicina de precisión en la atención del cáncer, se requieren inversiones inmediatas y significativas en los siguientes ámbitos:
- Explorar la heterogeneidad genética de las poblaciones latinoamericanas y aumentar el número de ensayos clínicos en terapias dirigidas.
- Desarrollar infraestructura adecuada, capacitar al personal sanitario y optimizar la distribución de recursos, incluyendo opciones de consulta virtual para superar barreras geográficas y culturales.
- Financiar de manera sostenible los sistemas de salud pública, simplificar los procesos de reembolso y abordar la asequibilidad y disponibilidad de medicamentos oncológicos específicos.
- Actualizar regulaciones y políticas para que acompañen los avances científicos, garantizando la seguridad y el cumplimiento normativo.
Políticas, colaboración y equidad
El contexto político actual en Latinoamérica no facilita abordar los desafíos existentes en el sistema de salud, y los beneficios de la medicina de precisión no se distribuirán equitativamente sin políticas deliberadas que garanticen su acceso amplio. Es fundamental incluir la medicina de precisión en los planes nacionales contra el cáncer, respaldados por evidencia científica y reformas en los procesos de aprobación y registro tanto de medicamentos como de ensayos clínicos.
Las mejoras en políticas requieren la colaboración entre actores clave: sociedades científicas, gobiernos, aseguradoras, proveedores, grupos de pacientes, centros de investigación y la industria farmacéutica. Estas alianzas son clave para avanzar hacia una atención verdaderamente centrada en el paciente, desarrollar evidencia, tecnologías, directrices y marcos regulatorios que garanticen el acceso equitativo a las innovaciones.
Limitaciones estructurales y esperanza de transformación
En general, la atención oncológica en Latinoamérica enfrenta limitaciones relacionadas con el acceso a profesionales capacitados, terapias innovadoras y centros especializados, debido a una inadecuada asignación de recursos y barreras geográficas y culturales. Sin cambios estructurales y de recursos, la equidad en la atención seguirá siendo una meta lejana. No obstante, existe la esperanza de que, mediante políticas equitativas y con visión de futuro, la medicina de precisión abra oportunidades para mejorar la equidad en la atención oncológica regional.
El rol de los financiadores y recomendaciones internacionales
La falta de cobertura para poblaciones excluidas de la seguridad social o de mecanismos públicos de financiamiento plantea la pregunta central de quiénes, entre financiadores públicos y privados, asumirán los costos de la medicina de precisión, determinando así la equidad en la distribución de sus beneficios.
Las acciones recomendadas por la Organización Mundial de la Salud (OMS) para mejorar la equidad en salud insisten en la necesidad de acciones basadas en la evidencia para asegurar servicios de salud de calidad, accesibles y aceptables para todos. Además, la OMS promueve la equidad y el acceso global a los datos genómicos, estableciendo principios para su uso responsable.
Conclusiones
La literatura médica identifica problemas complejos y persistentes en la atención oncológica, en su alcance, calidad y resultados, pero también evidencia que el acceso a la medicina de precisión aporta beneficios reales y potenciales en diagnóstico, tratamiento y resultados. El contexto político actual en Latinoamérica no favorece la mejora de estos aspectos ni el aprovechamiento pleno del potencial de la medicina de precisión, y la región muestra un rezago importante respecto a otras áreas del mundo. Esto subraya la necesidad de marcos políticos que trasciendan la mera regulación y aborden los componentes de acceso.
La medicina de precisión puede reducir desigualdades en salud al mejorar los resultados de todos los pacientes con cáncer, mediante diagnósticos y tratamientos específicos, pero para lograrlo debe implementarse en los sistemas de salud de manera intencionalmente equitativa.
Es el momento de desarrollar un marco de políticas equitativo que oriente las aplicaciones amplias y profundas de la medicina de precisión en América Latina y mejore los resultados de salud para todos los que la necesitan, no solo para quienes pueden costearla.
Resumen estructurado
Título
Medicina de precisión para el cáncer y la equidad en salud en América Latina: Generando comprensión para la formulación de políticas y sistemas de salud
Introducción
El estudio analiza la evidencia sobre el valor de las pruebas de biomarcadores y la medicina de precisión en América Latina, con un enfoque en la equidad en salud. Se destaca la importancia de políticas que promuevan el acceso equitativo y el papel de la medicina de precisión para reducir brechas sanitarias.
Metodología
Se empleó una revisión bibliográfica no sistemática, validada y enriquecida con la retroalimentación de un grupo de expertos en oncología y ciencias biomédicas de la región. El análisis incluyó literatura científica, políticas y marcos regulatorios relevantes a nivel global, regional y nacional.
Resultados
- Desafíos en la atención oncológica:
- La región enfrenta altos costos de diagnóstico y tratamiento, desigualdades socioeconómicas, insuficiencia de infraestructura, falta de profesionales capacitados y barreras geográficas y culturales en el acceso a servicios de calidad. El cáncer tiene un gran impacto socioeconómico y psicosocial, afectando a pacientes, cuidadores y la productividad.
- Medicina de precisión y equidad:
- La medicina de precisión permite adaptar el diagnóstico y tratamiento en función de biomarcadores y perfiles genéticos individuales, mejorando eficacia y reduciendo efectos adversos. Sin embargo, su acceso es desigual y suele estar restringido al ámbito privado. Su adopción puede reducir o profundizar inequidades según cómo se implemente.
- Panorama político y regulatorio:
- Los países analizados (Argentina, Brasil, Colombia, México y Panamá) cuentan con planes nacionales de control del cáncer, pero estos rara vez incluyen explícitamente la medicina de precisión o los biomarcadores. Existen iniciativas aisladas, como biobancos genómicos y proyectos de investigación, pero falta integración sistemática y políticas específicas.
- Comparativa internacional:
- Estados Unidos y Europa han avanzado más en la integración de la medicina de precisión, con marcos regulatorios, estrategias nacionales y mayor acceso equitativo. En Asia y África, la cooperación regional ha permitido desarrollar capacidades y compartir recursos.
- Desafíos y oportunidades:
- La falta de cobertura universal efectiva, las barreras económicas y geográficas, y la ausencia de marcos regulatorios claros dificultan la equidad en el acceso a la medicina de precisión. Sin embargo, existe potencial transformador si se implementan políticas inclusivas, inversiones en infraestructura, capacitación y monitoreo.
Conclusiones
La medicina de precisión puede contribuir a reducir las desigualdades en salud oncológica en América Latina, pero para lograrlo requiere marcos políticos equitativos, inversión en capacidades locales y colaboración multisectorial. Es fundamental que las políticas se orienten a garantizar el acceso para todos, más allá de la capacidad de pago individual, y que la equidad sea un eje central en la implementación de la medicina de precisión.
Recomendaciones
- Incluir explícitamente la medicina de precisión y pruebas de biomarcadores en los planes nacionales contra el cáncer.
- Desarrollar infraestructura y capacitar profesionales en toda la región, priorizando el acceso en zonas remotas y vulnerables.
- Garantizar mecanismos de financiamiento sostenibles que cubran tanto diagnósticos como tratamientos innovadores.
- Fomentar marcos regulatorios flexibles, éticos y transparentes, y la cooperación internacional y regional.
- Monitorear y evaluar continuamente el impacto en equidad y resultados de salud, adaptando las políticas según evidencia local.
