Nota del Blog
El panorama terapéutico del mieloma múltiple (MM) evoluciona rápidamente gracias a los avances en las estrategias inmunitarias. Los anticuerpos biespecíficos (BsAb), las terapias con receptores de antígenos quiméricos de células T (CAR-T) y los nuevos anticuerpos triespecíficos (TsAb) están redefiniendo las expectativas al ofrecer respuestas profundas y duraderas incluso en casos de enfermedad con un tratamiento previo intensivo.
Áreas cubiertas
Los anticuerpos monoclonales disponibles comercialmente, como teclistamab, elranatamab y talquetamab, muestran una actividad robusta en pacientes expuestos a triple clase de antígenos, y su uso temprano y los regímenes combinados mejoran aún más la profundidad de la respuesta. Sin embargo, persisten desafíos, como el agotamiento de las células T, el riesgo de infección, la hipogammaglobulinemia y los problemas logísticos relacionados con el aumento gradual de la dosis y el síndrome de liberación de citocinas.
Las terapias CAR-T, en particular idecabtagene vicleucel y ciltacabtagene autoleucel, logran altas tasas de respuesta y una rápida negatividad de la EMR, pero su uso más amplio se ve limitado por el tiempo de fabricación, el manejo de la toxicidad y los mecanismos de recaída, como la pérdida de antígenos.
Las innovaciones, como los CAR-T de doble diana, las construcciones blindadas y las plataformas alogénicas, buscan mejorar la durabilidad y ampliar el acceso. La evaluación de la EMR se ha convertido en un biomarcador que guía la intensidad y la duración del tratamiento. Paralelamente, una estratificación refinada del riesgo –especialmente para enfermedades citogenéticas, funcionales y extramedulares de alto riesgo– ayuda a identificar a los pacientes que pueden beneficiarse de una integración temprana de inmunoterapias.
Presento un artículo que ofrece un nuevo panorama en el arsenal terapéutico de esta enfermedad que puede mejorar la expectativa de Vida.

Autor : Rakesh Popat , MB, BS, Publicado el 18 de febrero de 2026 N Engl J Med 2026 ; 394 : 807 – 809 VOL. 394 NÚM. 8
El progreso en el tratamiento del mieloma múltiple en recaída o refractario ha sido rápido desde la introducción de las inmunoterapias de redirección de linfocitos T. La identificación del antígeno de maduración de linfocitos B (BCMA) condujo a la aprobación de tres anticuerpos biespecíficos, dos terapias con receptores quiméricos de antígenos de linfocitos T (CAR-T) y un conjugado anticuerpo-fármaco. El talquetamab, un anticuerpo biespecífico dirigido a GPRC5D (un receptor acoplado a proteína G) en las células de mieloma y a CD3 en los linfocitos T, también ha sido aprobado, y se están evaluando otras terapias nuevas, incluida la dirigida a antígenos duales.Aunque las aprobaciones de estos fármacos han proporcionado más opciones, la selección del fármaco más adecuado y la secuenciación correcta de las terapias se han vuelto más desafiantes. Las opciones recomendadas de BCMA en el momento de la primera recaída son ciltacabtagene autoleucel (terapia CAR-T dirigida a BCMA) y belantamab mafodotin (conjugado anticuerpo-fármaco dirigido a BCMA) con bortezomib o pomalidomida y dexametasona. 1 Ciltacabtagene autoleucel ha llevado a respuestas prolongadas entre los pacientes que han recibido una mediana de dos líneas de terapia previas, con un 76,4% de pacientes que sobreviven sin progresión de la enfermedad a los 30 meses después de una sola infusión. 2 El seguimiento a largo plazo en el momento de la recaída tardía mostró que aproximadamente un tercio de los pacientes habían estado vivos y sin progresión durante al menos 5 años. 3 Los anticuerpos biespecíficos actualmente están aprobados solo para pacientes con recaída tardía sobre la base de ensayos de un solo grupo, pero ahora se están evaluando antes como monoterapia o en combinaciones. En este número de la revista , Costa y sus colegas describen el análisis primario del ensayo MajesTEC-3 de teclistamab (un anticuerpo biespecífico dirigido a CD3 y BCMA) más daratumumab (un anticuerpo monoclonal dirigido a la proteína CD38) en pacientes con mieloma múltiple recidivante o refractario.4
En este ensayo de fase 3, los pacientes que habían recibido de una a tres líneas de terapia previas fueron asignados aleatoriamente para recibir terapia combinada con teclistamab–daratumumab o daratumumab combinado con dexametasona más la elección del investigador de pomalidomida o bortezomib (terapia estándar). Los investigadores hallaron una supervivencia libre de progresión estimada a 36 meses sin precedentes del 83,4 % con teclistamab-daratumumab, en comparación con el 29,7 % con la terapia estándar (cociente de riesgos instantáneos de progresión de la enfermedad o muerte: 0,17; intervalo de confianza del 95 %: 0,12 a 0,23; p < 0,001), junto con un beneficio asociado en la supervivencia global. La forma de las curvas de Kaplan-Meier es particularmente sorprendente, ya que sugiere una estabilización con una supervivencia del 92 % a los 6 meses y del 84 % a los 30 meses, aunque el seguimiento fue limitado. Los pacientes de alto riesgo también se beneficiaron. Estos resultados son realmente notables y representan no solo una mejora sustancial del tratamiento, sino también una esperanza real de que finalmente se logre la curación en algunos pacientes. Las infecciones graves fueron la principal preocupación. El ensayo, que incluyó a pacientes durante la pandemia de la enfermedad por coronavirus de 2019, presentó un exceso de muertes precoces por infección. De las 13 infecciones mortales, 12 ocurrieron durante los primeros 6 meses tras el inicio del tratamiento. Nueve de estos pacientes no habían recibido tratamiento con inmunoglobulina, lo que motivó una modificación del protocolo para recomendar dicho uso profiláctico independientemente de los niveles de IgG, una monitorización estrecha de los niveles de IgG y la administración profiláctica de antibióticos y antivirales. Estos hallazgos resaltan la necesidad de implementar estas recomendaciones lo antes posible, ya que las terapias con anticuerpos biespecíficos se asocian con hipogammaglobulinemia (nivel de IgG <400 mg por decilitro), lo que conduce a una inmunodeficiencia secundaria. La reducción de las infecciones también coincidió con la reducción de la administración de teclistamab (cada 4 semanas) a partir del ciclo 7. Esta correlación también se observó en el ensayo MajesTEC-1 de monoterapia con teclistamab, en el que la frecuencia de infecciones de grado 3 o superior se redujo con una dosificación menos frecuente. 5Aún quedan varias preguntas sobre este ensayo. Solo el 5% de los pacientes había estado expuesto previamente a un anticuerpo monoclonal anti-CD38, y la refractariedad a dichos anticuerpos fue un criterio de exclusión clave. Actualmente, los anticuerpos monoclonales anti-CD38 se recomiendan como terapia de primera línea en pacientes con mieloma múltiple, independientemente de si son elegibles para un trasplante.¹
Sin embargo, dicha administración normalmente se limita a una duración fija en pacientes elegibles para un trasplante. Los pacientes que no son elegibles para un trasplante reciben tratamiento continuo hasta la progresión, momento en el cual se consideran refractarios a la terapia anti-CD38. Este factor genera incertidumbre , ya que el tratamiento repetido con anticuerpos monoclonales anti-CD38 ha demostrado previamente una eficacia limitada.¹¹
Sin embargo, la principal justificación para el uso de daratumumab en el ensayo MajesTEC-3 no fue su actividad antitumoral directa, sino su actividad inmunomoduladora al eliminar células inmunosupresoras y promover la expansión de linfocitos T, que podría mantenerse a pesar de la exposición previa. En una actualización del ensayo de fase 1b TRIMM-2 de teclistamab más daratumumab, el 63,1 % de los pacientes fue refractario a los anticuerpos monoclonales anti-CD38 (con un período de lavado de 90 días), con una respuesta del 74 % al 100 %, lo que sugiere que la repetición del tratamiento con esta combinación podría seguir siendo eficaz. Dada la alta eficacia de este tratamiento, se debería explorar una duración fija de los anticuerpos biespecíficos como una línea de tratamiento más temprana. Este enfoque permite la reconstitución inmunitaria, reduce la carga del tratamiento para los pacientes y limita el costo. Si bien el ensayo MajesTEC-3 se diseñó con el uso de teclistamab como terapia continua, algunos pacientes inevitablemente interrumpirán el tratamiento por razones distintas a la progresión de la enfermedad, y la duración de su respuesta será de interés. Los ensayos en curso que exploran una duración fija de las terapias con anticuerpos biespecíficos podrían resolver definitivamente esta cuestión. La otra pregunta es si la transición temprana a una administración menos frecuente reduce el riesgo de infección en pacientes con mayor fragilidad, una práctica que aumentaría la tolerabilidad sin sacrificar la eficacia antitumoral. Finalmente, los impresionantes resultados de este ensayo cuestionan el papel de la terapia CAR-T, que sigue estando restringida a nivel mundial debido a su alto costo, los largos tiempos de fabricación y la necesidad de tratamiento en un centro CAR-T. En esta competencia, la disponibilidad inmediata supone una gran ventaja. Si bien el enfoque de «una sola dosis» sigue siendo atractivo, el uso de anticuerpos biespecíficos podría ser un tratamiento más realista para muchos pacientes. En conjunto, los resultados de este ensayo redefinen las expectativas sobre el tratamiento de pacientes con mieloma múltiple en recaída o refractario. Con más ensayos de inmunoterapia de fase 3 en curso, estamos presenciando una nueva era en la supervivencia del mieloma
Resultados
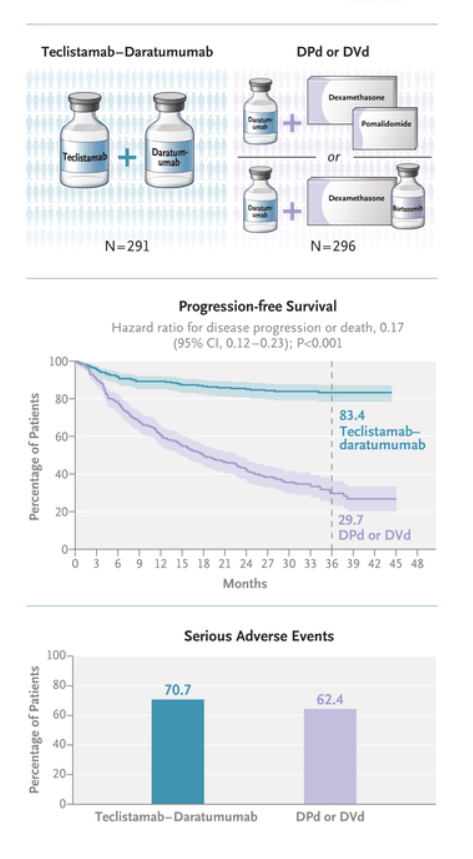
Un total de 587 pacientes fueron aleatorizados (291 para recibir teclistamab-daratumumab y 296 para recibir DPd o DVd). Con una mediana de 34,5 meses, la supervivencia libre de progresión fue significativamente mayor con teclistamab-daratumumab que con DPd o DVd. La supervivencia libre de progresión estimada a 36 meses fue del 83,4 % en el grupo de teclistamab-daratumumab y del 29,7 % en el grupo de DPd o DVd (cociente de riesgos instantáneos: 0,17; intervalo de confianza del 95 %: 0,12 a 0,23; p < 0,001).
Más pacientes en el grupo teclistamab-daratumumab que en el grupo DPd o DVd presentaron una respuesta completa o superior (81,8 % frente a 32,1 %), una respuesta global (89,0 % frente a 75,3 %) y una negatividad de la enfermedad mínima residual (10-5 ; 58,4 % frente a 17,1 %) (p < 0,001 para todas las comparaciones). Se produjeron eventos adversos graves en el 70,7 % de los pacientes del grupo teclistamab-daratumumab y en el 62,4 % de los del grupo DPd o DVd; el 7,1 % y el 5,9 % fallecieron por eventos adversos, respectivamente.
Conclusiones
En pacientes con mieloma múltiple que habían recibido de una a tres líneas de tratamiento previas, los del grupo teclistamab-daratumumab presentaron una supervivencia libre de progresión significativamente mayor que los del grupo DPd o DVd. (Financiado por Johnson & Johnson; número de ClinicalTrials.gov:
NCT05083169 ).
Aspectos destacados del artículo
- Los anticuerpos biespecíficos (BsAbs), las terapias con células CAR-T y los anticuerpos triespecíficos emergentes (TsAbs) han transformado el tratamiento del MM, permitiendo remisiones profundas y duraderas incluso en pacientes fuertemente pretratados.
- Teclistamab, elranatamab y talquetamab alcanzan tasas de respuesta del 60-70 % en MMRR, con mejoras adicionales cuando se utilizan en etapas más tempranas de la enfermedad o en regímenes combinados. Combinaciones novedosas, como daratumumab, carfilzomib o inhibidores de puntos de control, están demostrando una prometedora actividad sinérgica.
- El idecabtagén vicleucel y el ciltacabtagén autoleucel inducen tasas de respuesta y de negatividad de la EMR excepcionalmente altas. Sin embargo, su uso más amplio se ve limitado por retrasos en la fabricación, la gestión de la toxicidad, la infraestructura especializada y los mecanismos de recaída (p. ej., la pérdida de antígeno). Las terapias CAR-T alogénicas y de nueva generación buscan superar estas barreras.
- La negatividad de la EMR, especialmente cuando se mantiene, se correlaciona fuertemente con una SSP y una SG prolongadas. Los ensayos clínicos actuales incorporan cada vez más estrategias de escalada y desescalada adaptadas a la EMR, incluyendo la posibilidad de suspender el tratamiento en pacientes que alcanzan una negatividad de la EMR a largo plazo.
- Los marcadores de riesgo biológicos y funcionales refinados, como amp1q, pérdida bialélica de TP53, células plasmáticas circulantes, enfermedad extramedular e indicadores pronósticos basados en PET, permiten una mejor identificación de las poblaciones de alto riesgo.
Estos últimos años se modificó el tratamiento del mieloma múltiple, enfermedad que guardo un interés particular desde que hice mi tesis, de complicaciones renales agudas en esta enfermedad, y en cuatro décadas fui observando su mejora en control y sobrevida, especialmente en esta época en nuestra institución significa el 30% de todos los trasplantes de médula ósea.