Autores : Lana A. Castellucci , MD , Vivien M. Chen , MB, BS, Ph.D. , Michael J. Kovacs , MD , Alejandro LazoLangner , MD , Peter Greenstreet , Ph.D. , Susan Kahn , MD Benoit Côté , MD, CM
La tromboembolia venosa es una afección común y tratable; sin embargo, es la tercera causa más frecuente de eventos cardiovasculares agudos y muerte cardiovascular a nivel mundial. <sup>1,2</sup> La incidencia de tromboembolia venosa en la población general es de 1 a 2 casos por cada 1000 personas,<sup> 3,4 </sup> y aumenta con la edad. <sup> 5,6</sup> Se requiere terapia anticoagulante durante un mínimo de 3 meses después de una tromboembolia venosa para prevenir eventos trombóticos recurrentes.<sup> 1,7</sup>
Resultados
Un total de 2760 pacientes fueron aleatorizados: 1370 al grupo de apixabán y 1390 al grupo de rivaroxabán. Se produjo un evento de desenlace primario en 44 de 1345 pacientes (3,3 %) en el grupo de apixabán y en 96 de 1355 pacientes (7,1 %) en el grupo de rivaroxabán (riesgo relativo, 0,46; intervalo de confianza del 95 % [IC], 0,33 a 0,65; p < 0,001). Se produjo una muerte por cualquier causa en 1 paciente (0,1 %) en el grupo de apixabán y en 4 pacientes (0,3 %) en el grupo de rivaroxabán (riesgo relativo, 0,25; IC del 95 %, 0,03 a 2,26). Se produjeron eventos adversos graves no relacionados con hemorragias o trombosis venosa en 36 pacientes (2,7 %) del grupo de apixabán y en 30 pacientes (2,2 %) del grupo de rivaroxabán.
Conclusiones
En pacientes con tromboembolismo venoso agudo, el riesgo de hemorragia clínicamente relevante fue significativamente menor con apixabán que con rivaroxabán durante el período de tratamiento de 3 meses. (Financiado por los Institutos Canadienses de Investigación en Salud y otras entidades; número de registro en ClinicalTrials.gov de COBRRA: NCT03266783
Los anticoagulantes orales directos, incluidos rivaroxabán y apixabán, son los tratamientos más frecuentemente prescritos para la tromboembolia venosa aguda. En ensayos clínicos aleatorizados, rivaroxabán en una dosis de 15 mg dos veces al día durante 21 días seguido de 20 mg al día y apixabán en una dosis de 10 mg dos veces al día durante 7 días seguido de 5 mg dos veces al día no fueron inferiores a los antagonistas de la vitamina K en cuanto a eficacia (riesgo de tromboembolia venosa recurrente). 8,9 Estos ensayos mostraron que el sangrado clínicamente relevante, un compuesto de sangrado mayor o sangrado no mayor clínicamente relevante, ocurrió en el 4,3% de los pacientes que recibieron apixabán en comparación con el 9,7% de los que recibieron antagonistas de la vitamina K 9 y en el 8,1% de los pacientes que recibieron rivaroxabán en comparación con el 8,1% de los que recibieron antagonistas de la vitamina K. 8 Se planteó la hipótesis de que la diferencia entre la terapia con apixabán y rivaroxabán con respecto al riesgo de hemorragia clínicamente relevante estaba relacionada con la heterogeneidad en las poblaciones de pacientes y las diferencias en los diseños de los ensayos. 8,9 Debido a la falta de ensayos que hayan comparado rivaroxabán con apixabán con respecto al riesgo de hemorragia, las guías de práctica clínica no recomiendan un anticoagulante sobre el otro. 1,7 Realizamos el ensayo de comparación del riesgo de hemorragia entre rivaroxabán y apixabán (COBRRA) para evaluar si apixabán era superior a rivaroxabán con respecto a la seguridad en pacientes con tromboembolismo venoso agudo.
Métodos
Diseño y supervisión de ensayos clínicos
Este ensayo fue un ensayo pragmático e internacional con un diseño PROBE (prospectivo, aleatorizado, abierto, con evaluación de resultados a ciegas) que comparó apixabán con rivaroxabán en pacientes con tromboembolismo venoso agudo. El protocolo del ensayo está disponible junto con el texto completo de este artículo en NEJM.org. El primer y el último autor diseñaron el ensayo. Los miembros del comité directivo internacional tuvieron la responsabilidad final del diseño y la supervisión del ensayo, el desarrollo clínico y la implementación del protocolo, la redacción del manuscrito y la decisión de enviarlo para su publicación. El análisis de datos fue realizado en el Centro de Métodos de Ottawa por dos de los autores. Un comité independiente de monitorización de datos y seguridad y un estadístico supervisaron el progreso del ensayo y la seguridad de los pacientes. El comité de revisión institucional o el comité de ética de la investigación de cada uno de los centros participantes aprobó el protocolo. Los investigadores recopilaron los datos. El primer autor redactó el primer borrador del manuscrito. Los autores dan fe de la integridad y exactitud de los datos y del cumplimiento del protocolo por parte del ensayo.
Los pacientes dieron su consentimiento integrado o su consentimiento informado por escrito, según los requisitos locales. Con el enfoque de consentimiento integrado, el médico tratante utilizó un guion aprobado para proporcionar al paciente toda la información pertinente sobre el ensayo durante una consulta clínica. Posteriormente, se solicitó a los pacientes que dieran su consentimiento verbal para someterse a la aleatorización y recibir el tratamiento asignado durante al menos 3 meses. Encontrará información adicional sobre el consentimiento integrado en el Apéndice Suplementario , disponible en NEJM.org.
El ensayo fue coordinado y patrocinado por el Instituto de Investigación del Hospital de Ottawa, el Centro de Ensayos Clínicos del Consejo Nacional de Salud e Investigación Médica, la Universidad de Sídney, el Real Colegio de Cirujanos de Irlanda y el Centro de Investigación Clínica del University College de Dublín, bajo la supervisión del comité directivo. Los datos se recopilaron en los centros participantes y se introdujeron en una base de datos en línea gestionada por el personal del Centro de Métodos de Ottawa del Instituto de Investigación del Hospital de Ottawa. Un comité de adjudicación central independiente, cuyos miembros desconocían la asignación de tratamientos, revisó todos los eventos adversos sospechosos y las causas de muerte mediante una plataforma en línea (VERDICT).
El ensayo fue financiado por los Institutos Canadienses de Investigación en Salud, el Fondo para el Futuro de la Investigación Médica en Australia, el Real Colegio de Cirujanos de Irlanda y la Red Internacional de Redes de Investigación Clínica sobre Tromboembolia Venosa. Los financiadores no participaron en el diseño ni la realización del ensayo, la recopilación y el análisis de datos, la interpretación de los datos ni la revisión o preparación del manuscrito. El ensayo contó con el respaldo de la Red Internacional de Redes de Trombosis Venosa, la Red CanVECTOR y la Sociedad de Trombosis y Hemostasia de Australia y Nueva Zelanda.
Población del ensayo
Los adultos (≥18 años de edad) con tromboembolismo venoso agudo sintomático fueron elegibles para su inclusión en el ensayo. Los criterios de inclusión fueron trombosis venosa profunda proximal sintomática de las extremidades inferiores o embolia pulmonar segmentaria o más proximal y la capacidad de proporcionar consentimiento informado. Los pacientes fueron excluidos si habían recibido terapia anticoagulante terapéutica durante más de 72 horas inmediatamente antes de la visita de inscripción o tenían insuficiencia renal con un aclaramiento de creatinina de menos de 30 ml por minuto según la fórmula de Cockcroft-Gault. 10 Entre los otros criterios de exclusión se encontraban cualquier contraindicación para rivaroxabán o apixabán según lo determinado por el médico tratante local, incluyendo, entre otros, sangrado activo; cáncer activo 11 ; un peso de más de 120 kg, debido a las recomendaciones de la guía en el momento del diseño del ensayo 12 ; enfermedad hepática conocida (enfermedad de Child-Pugh B o C); uso de medicamentos contraindicados que interactúan (según la información proporcionada en el Apéndice suplementario ); embarazo o lactancia actual; o cualquier otra indicación para la terapia anticoagulante a largo plazo, como la fibrilación auricular.
Aleatorización e intervención en el ensayo
Los pacientes elegibles fueron asignados aleatoriamente en una proporción 1:1 para recibir 3 meses de tratamiento con rivaroxabán a una dosis de 15 mg dos veces al día durante 21 días, seguido de 20 mg al día, o apixabán a una dosis de 10 mg dos veces al día durante 7 días, seguido de 5 mg dos veces al día. La aleatorización se realizó mediante un sistema centralizado basado en la web y un diseño de bloques permutados con tamaños de bloque variables (4 y 6), con estratificación según la insuficiencia renal (aclaramiento de creatinina, <50 ml por minuto frente a ≥50 ml por minuto), el uso continuado previsto de terapia antiplaquetaria durante el período del ensayo (sí frente a no) y el centro participante.Los médicos tratantes y los pacientes estaban al tanto de la asignación del tratamiento. Los pacientes recibieron recetas locales para el medicamento asignado, las cuales debían surtir en farmacias comerciales locales. Los miembros del comité central de adjudicación independiente y los estadísticos desconocían la asignación del tratamiento. Las visitas del ensayo se programaron para el momento de la inscripción y a las 2 semanas (con un margen de ±1 semana) y 3 meses después de la aleatorización.
Resultados
El resultado primario fue la hemorragia clínicamente relevante, un compuesto de hemorragia mayor o hemorragia no mayor clínicamente relevante, según la definición de la Sociedad Internacional de Trombosis y Hemostasia (ISTH). La hemorragia mayor se definió como una hemorragia manifiesta que ocurrió en un sitio crítico, se asoció con una disminución de al menos 2 g por decilitro en el nivel de hemoglobina, condujo a la transfusión de 2 o más unidades de concentrado de glóbulos rojos o contribuyó a la muerte.<sup> 13</sup> La hemorragia no mayor clínicamente relevante se definió como una hemorragia que no cumplió con la definición de hemorragia mayor, pero que cumplió con al menos uno de los siguientes criterios: resultó en una intervención médica por parte de un profesional de la salud, condujo a la hospitalización o a un mayor nivel de atención, o motivó una evaluación presencial por parte de un profesional de la salud.<sup> 14</sup>
Los resultados secundarios incluyeron los componentes individuales del resultado primario y la tromboembolia venosa sintomática recurrente (un compuesto de trombosis venosa profunda recurrente o embolia pulmonar recurrente). 15 La trombosis venosa profunda recurrente se definió por un área no compresible en la vena poplítea o vena más proximal en la ecografía de compresión que no estaba presente en el momento del diagnóstico o por un defecto de llenado intraluminal constante en la vena poplítea o venas más proximales en la venografía. La embolia pulmonar recurrente se definió por anomalías en la gammagrafía de ventilación-perfusión, incluyendo un nuevo defecto de perfusión segmentario o más proximal no coincidente; un defecto de llenado intraluminal en un vaso segmentario o más proximal en la angiografía pulmonar por tomografía computarizada que previamente estaba libre de trombos; o un defecto de llenado intraluminal constante o una oclusión de un vaso de más de 2,5 mm de diámetro en la angiografía pulmonar. Otros resultados secundarios incluyeron muerte por hemorragia, muerte por tromboembolismo venoso recurrente (confirmada mediante certificado de defunción o autopsia), muerte por cualquier causa y adherencia al tratamiento en cada visita de seguimiento (véase el Apéndice complementario ). Todos los resultados del ensayo fueron evaluados por un comité de adjudicación central independiente cuyos miembros desconocían la asignación de los tratamientos.
Análisis estadístico
El ensayo actual se diseñó para tener una potencia del 80% para detectar un riesgo un 33% menor (reducción mínima clínicamente significativa) de hemorragia clínicamente relevante con apixabán que con rivaroxabán a un nivel alfa bilateral de 0,05. Este diseño se basó en la suposición de que un evento de resultado primario ocurriría en el 5,4% de los pacientes en el grupo de apixabán y en el 8,1% de los del grupo de rivaroxabán. Calculamos que se necesitaría un mínimo de 1352 pacientes en cada grupo de tratamiento para detectar dicha diferencia en el riesgo. La pérdida de seguimiento fue inferior al 1% en los ensayos EINSTEIN de rivaroxabán y en el ensayo AMPLIFY (Apixabán para el manejo inicial de la embolia pulmonar y la trombosis venosa profunda como terapia de primera línea) de apixabán. 8,9 Suponiendo una pérdida de seguimiento conservadora del 2% en el ensayo actual, planeamos reclutar 2760 participantes (1380 participantes por grupo de tratamiento).
El resultado primario de sangrado clínicamente relevante adjudicado se analizó en la población por intención de tratar, que incluyó a todos los pacientes que se sometieron a aleatorización y completaron el seguimiento, con datos analizados según el grupo de tratamiento asignado al paciente. En el análisis del resultado primario preespecificado, utilizamos una prueba de chi-cuadrado para calcular una razón de probabilidades no ajustada y su correspondiente intervalo de confianza del 95 %. En un análisis de sensibilidad del resultado primario, utilizamos regresión logística de efectos mixtos con ajuste para la variable de estratificación de enfermedad renal (aclaramiento de creatinina, <50 ml por minuto frente a ≥50 ml por minuto), uso continuo de antiagregantes plaquetarios (sí frente a no), edad (<75 años frente a ≥75 años) y sexo (masculino frente a femenino) y un efecto aleatorio para el centro del ensayo para calcular una razón de probabilidades ajustada y un intervalo de confianza del 95 %.
Se realizó un análisis de tiempo hasta el evento del resultado primario mediante el método de Kaplan-Meier. Los resultados secundarios de hemorragia mayor, hemorragia no mayor clínicamente relevante, tromboembolismo venoso recurrente y muerte por cualquier causa se analizaron con razones de probabilidades no ajustadas y sus correspondientes intervalos de confianza del 95 %.
A petición de los editores de la revista , calculamos los riesgos relativos y sus correspondientes intervalos de confianza del 95 % para todos los resultados primarios y secundarios, y utilizamos un modelo lineal generalizado de efectos mixtos con una función de enlace logarítmica para calcular el riesgo relativo ajustado en el análisis de sensibilidad del resultado primario. Los riesgos relativos se presentan en el texto principal, y las razones de probabilidades, calculadas según lo preespecificado en el plan de análisis estadístico (disponible con el protocolo), se presentan en el Apéndice Suplementario . Dado que el evento de interés es poco frecuente (incidencia <10 %), se esperaba que las razones de probabilidades fueran similares a los riesgos relativos. 16,17
En los análisis de resultados secundarios, las amplitudes de los intervalos de confianza no se han ajustado por multiplicidad, y los intervalos no deben usarse en lugar de la prueba de hipótesis. El principal riesgo competitivo fue la muerte; sin embargo, debido a que la mortalidad fue muy baja (<0,5 % de los pacientes), no ajustamos por este riesgo competitivo en los análisis de los resultados primarios y secundarios. Los análisis de los resultados primarios y secundarios y el análisis de regresión logística de efectos mixtos se realizaron según un enfoque de casos completos porque no faltaban datos entre las variables basales incluidas en los análisis. En los análisis de subgrupos preespecificados, se proporcionan razones de probabilidades no ajustadas y sus correspondientes intervalos de confianza del 95 %. Todos los análisis se realizaron en la población por intención de tratar.

Resultados
Pacientes
Desde el 13 de diciembre de 2017 hasta el 23 de enero de 2025, un total de 2760 pacientes fueron aleatorizados en 32 centros de Canadá, Australia e Irlanda ( Figura 1 ). Asignamos a 1370 pacientes a recibir apixabán y a 1390 a recibir rivaroxabán. Tras la exclusión de 60 pacientes (2,2 %) que habían sido aleatorizados, se evaluaron 1345 pacientes en el grupo de apixabán y 1355 en el grupo de rivaroxabán en el análisis por intención de tratar ( Figura 1 y Tabla S1 en el Apéndice Suplementario ).
Figura 1
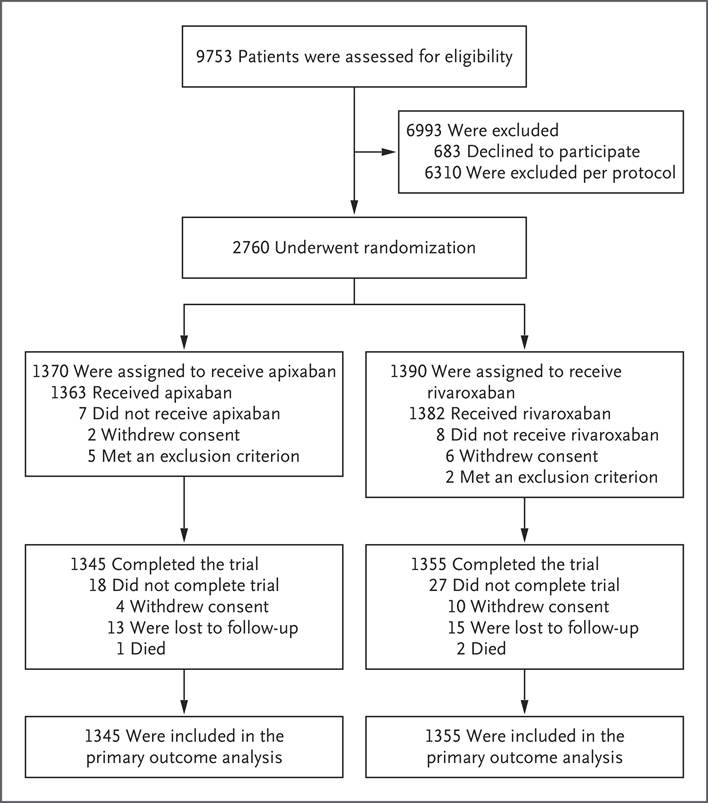
Aleatorización y seguimiento.
Las características demográficas y clínicas basales parecían estar bien equilibradas entre los grupos de tratamiento ( Tabla 1 ). La edad media fue de 58,3 años, y 1175 pacientes (43,5%) eran mujeres. Aproximadamente el 10% de los pacientes informaron ser de raza no blanca (Tabla S2). La mayoría de los pacientes (2087; 77,3%) tuvieron un evento de tromboembolismo venoso no provocado; 1409 pacientes (52,2%) tuvieron trombosis venosa profunda sola, y 1291 (47,8%) tuvieron embolia pulmonar con o sin trombosis venosa profunda. En total, 429 pacientes (15,9%) tenían antecedentes de tromboembolismo venoso.
Tabla 1
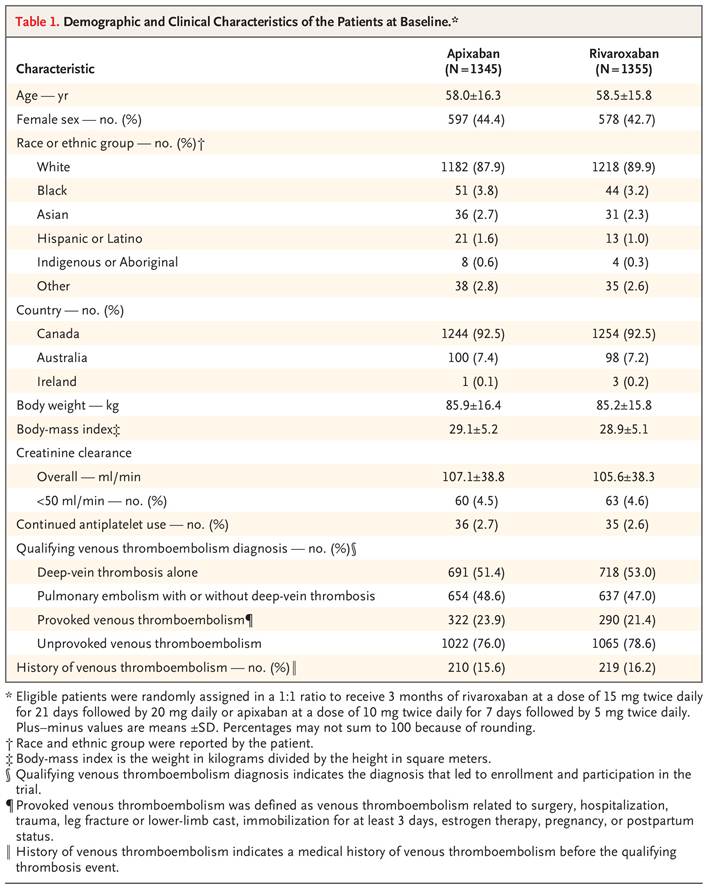
Características demográficas y clínicas de los pacientes al inicio del estudio.
Resultado principal y resultados secundarios clave
En el análisis por intención de tratar, se produjo sangrado clínicamente relevante durante el período de ensayo de 3 meses en 44 de 1345 pacientes (3,3 %) en el grupo de apixabán y en 96 de 1355 (7,1 %) en el grupo de rivaroxabán (riesgo relativo, 0,46; intervalo de confianza del 95 % [IC], 0,33 a 0,65; p < 0,001) ( Tabla 2 y Figura 2 ). Los hallazgos parecieron ser consistentes en todos los subgrupos preespecificados (Fig. S1). En el análisis de sensibilidad realizado con un modelo lineal generalizado de efectos mixtos, el riesgo relativo marginal ajustado fue de 0,45 (IC del 95 %, 0,32 a 0,64).
Figura 2
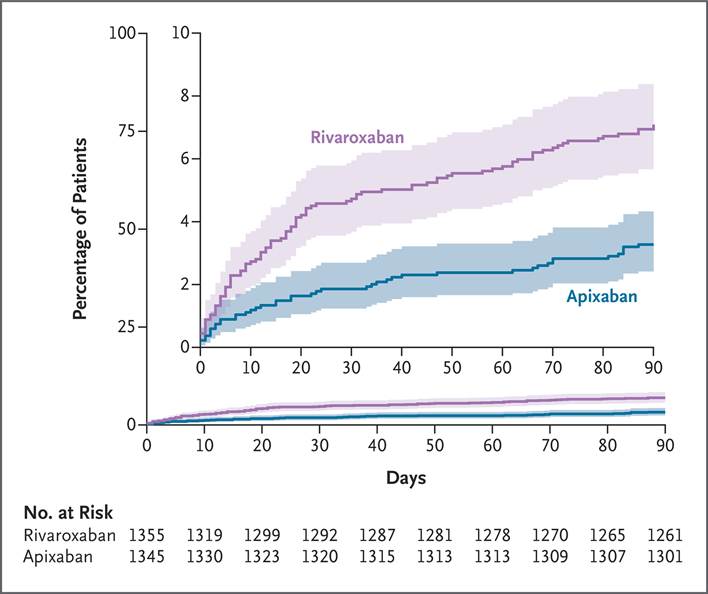
Hemorragia clínicamente relevante.
Tabla 2
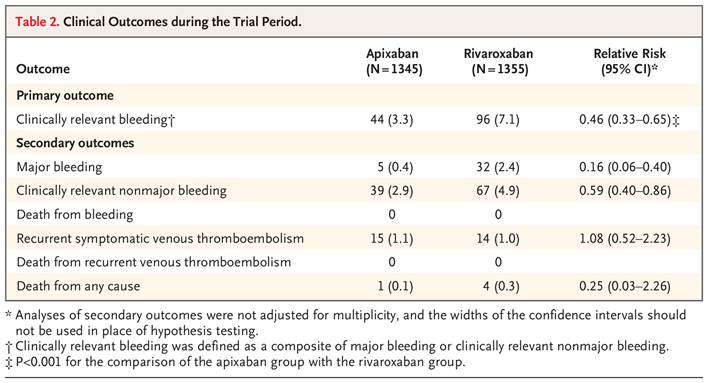
Resultados clínicos durante el período de ensayo.
Se produjo sangrado mayor en 5 pacientes (0,4 %) del grupo de apixabán y en 32 pacientes (2,4 %) del grupo de rivaroxabán (riesgo relativo: 0,16; IC del 95 %: 0,06 a 0,40). El sangrado mayor provocó una disminución del nivel de hemoglobina o una transfusión sanguínea en los 5 pacientes del grupo de apixabán. En el grupo de rivaroxabán, el sangrado mayor provocó una disminución del nivel de hemoglobina o una transfusión sanguínea en 28 pacientes y sangrado en un área u órgano crítico en 4 pacientes (Tabla S3). No se produjeron muertes por sangrado en ninguno de los grupos de tratamiento.
Se produjeron hemorragias clínicamente relevantes no mayores en 39 pacientes (2,9 %) tratados con apixabán y en 67 pacientes (4,9 %) tratados con rivaroxabán (riesgo relativo, 0,59; IC del 95 %, 0,40 a 0,86).Los tipos más comunes de hemorragia no mayor clínicamente relevante fueron hemorragia vaginal (en el 2,7% de los pacientes) y hemorragia gastrointestinal (en el 0,6%) en el grupo de apixabán y hemorragia vaginal (en el 3,8%), hematuria (en el 1,3%) y hemorragia gastrointestinal (en el 1,0%) en el grupo de rivaroxabán (Tabla S4). Se produjo tromboembolismo venoso sintomático recurrente en 15 pacientes (1,1%) en el grupo de apixabán y en 14 pacientes (1,0%) en el grupo de rivaroxabán (riesgo relativo, 1,08; IC del 95%, 0,52 a 2,23) ( Figura 3 ). Se produjo muerte por cualquier causa en 1 paciente (0,1%) en el grupo de apixabán y en 4 pacientes (0,3%) en el grupo de rivaroxabán (riesgo relativo, 0,25; IC del 95%, 0,03 a 2,26). No se registraron muertes atribuibles a tromboembolismo venoso recurrente en los grupos de tratamiento. Las razones de probabilidad para los resultados primarios y secundarios se presentan en la Tabla S5.
Figura 3
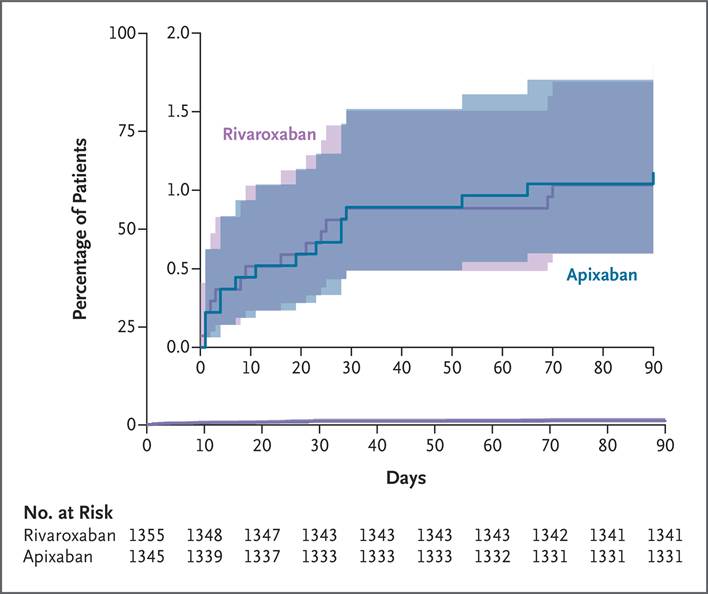
Tromboembolia venosa recurrente.
Adherencia a la medicación
En cada visita de seguimiento, se registró la adherencia a la medicación, según lo informado por el paciente, mediante una serie de preguntas diseñadas para evaluar la adherencia de diferentes maneras. El 65,7 % de los pacientes del grupo de apixabán y el 75,1 % de los del grupo de rivaroxabán informaron una adherencia completa (Tabla S6).
Seguridad
Se produjeron eventos adversos graves no relacionados con hemorragias o trombosis venosa en 36 pacientes (2,7 %) del grupo de apixabán y en 30 pacientes (2,2 %) del grupo de rivaroxabán (Tabla S7).
Discusión
El presente ensayo comparó los anticoagulantes orales directos apixabán y rivaroxabán con respecto al riesgo de hemorragia en pacientes con embolia pulmonar aguda o trombosis venosa profunda proximal. El ensayo demostró que apixabán (a una dosis de 10 mg dos veces al día durante 7 días, seguida de 5 mg dos veces al día) fue superior a rivaroxabán (a una dosis de 15 mg dos veces al día durante 21 días, seguida de 20 mg al día) en cuanto al criterio de valoración principal de hemorragia clínicamente relevante, un compuesto de hemorragia mayor o hemorragia no mayor clínicamente relevante, durante el período de ensayo de 3 meses. No se observaron diferencias aparentes en el riesgo del criterio de valoración secundario de tromboembolismo venoso recurrente entre los dos grupos.
Las guías de práctica clínica recomiendan los anticoagulantes orales directos como tratamiento de primera línea para la tromboembolia venosa aguda porque estos agentes tienen un mejor perfil de seguridad que los antagonistas de la vitamina K. 1,7,18 La falta de ensayos prospectivos de comparación directa ha limitado las recomendaciones sobre la preferencia de apixabán o rivaroxabán. Minimizar las complicaciones hemorrágicas durante el tratamiento es una consideración importante en el manejo de la tromboembolia venosa aguda. 19 En los ensayos de registro pivotales para apixabán y rivaroxabán, se observaron diferencias en el riesgo de hemorragia clínicamente relevante entre los dos anticoagulantes orales directos y los antagonistas de la vitamina K, mientras que el riesgo de trombosis recurrente fue similar. 8,9 Estos hallazgos impulsaron una consideración más profunda de las diferencias en los riesgos de hemorragia con respecto al diseño del ensayo y las características de los participantes. 20,21 Nuestro ensayo confirma el menor riesgo de hemorragia clínicamente relevante con apixabán que con los antagonistas de la vitamina K que se observó en el ensayo AMPLIFY. 9 En el presente ensayo, la incidencia a los 3 meses de hemorragia clínicamente relevante fue significativamente menor en el grupo de apixabán que en el grupo de rivaroxabán. Los tipos de hemorragia más comunes en el grupo de apixabán fueron la hemorragia vaginal (en el 2,7 % de los pacientes) y la hemorragia gastrointestinal (en el 0,6 %), con una menor incidencia de hemorragia vaginal que en el ensayo AMPLIFY (5,4 %). 9,22 En el grupo de rivaroxabán, los tipos de hemorragia más comunes fueron la hemorragia vaginal (en el 3,8 % de los pacientes), la hematuria (en el 1,3 %) y la hemorragia gastrointestinal (en el 1,0 %). La incidencia de hemorragia vaginal en el grupo de rivaroxabán fue menor en nuestro ensayo que en los ensayos EINSTEIN (9,5 %). 8,22
Nuestro ensayo no explica la diferencia en el riesgo de hemorragia entre los pacientes tratados con apixabán y los tratados con rivaroxabán. La adherencia a la anticoagulación a los 3 meses fue menor en el grupo de apixabán que en el grupo de rivaroxabán (65,7 % frente a 75,1 %). Sin embargo, el porcentaje de pacientes con tromboembolismo venoso recurrente durante el período de ensayo de 3 meses fue de aproximadamente el 1 % en cada grupo. No obstante, enfatizar la adherencia a la anticoagulación y discutir las barreras para la adherencia con los pacientes son fundamentales para el manejo del tromboembolismo venoso agudo. En nuestro ensayo, la diferencia en el riesgo de hemorragia clínicamente relevante puede estar relacionada con la dosis de rivaroxabán, dado que la mayor parte de la diferencia parece haber ocurrido durante las primeras 3 semanas de tratamiento, un período en el que se administró rivaroxabán a una dosis un 50 % superior a la dosis de mantenimiento ( Figura 2 ). A pesar de este factor, el riesgo de tromboembolismo venoso recurrente pareció ser similar en cada grupo de tratamiento. Se necesitan más evaluaciones en ensayos clínicos para confirmar si el régimen de dosificación de rivaroxabán contribuyó a los riesgos de hemorragia observados. Los hallazgos con respecto al resultado primario fueron consistentes en todos los subgrupos preespecificados (Fig. S1). La mortalidad a los 3 meses fue baja en cada grupo de tratamiento, un hallazgo que también es consistente con los datos publicados. 23
Nuestro ensayo tiene limitaciones. El diseño abierto podría haber introducido un sesgo de detección . Los datos emergentes durante el ensayo podrían haber influido en la percepción de los médicos sobre el riesgo de hemorragia con apixabán y rivaroxabán. Sin embargo, es improbable que exista un sesgo de detección, ya que los episodios hemorrágicos evaluados en el ensayo son, por definición, manifiestos y requieren una visita a un centro médico. Asimismo, es improbable que el conocimiento del anticoagulante recibido haya influido en la decisión de transfundir o proceder con una intervención.Recopilamos datos únicamente durante los primeros tres meses de la terapia anticoagulante; se desconoce si las diferencias en el riesgo de hemorragia persisten más allá de este período. Las definiciones de hemorragia utilizadas en este ensayo no incorporan el uso de recursos sanitarios para el manejo de la hemorragia, ni consideran la percepción de los pacientes sobre la gravedad clínica y los efectos de la hemorragia en la calidad de vida.
Entre las limitaciones adicionales se encuentra la exclusión de pacientes con un peso corporal superior a 120 kg de acuerdo con las directrices de la ISTH vigentes en el momento del diseño del ensayo, 12 lo que limita los datos sobre pacientes con sobrepeso u obesidad.Los pacientes con trombosis asociada al cáncer también fueron excluidos del ensayo porque la heparina de bajo peso molecular era el tratamiento estándar en el momento del diseño del ensayo. Los ensayos de registro pivotales de apixabán y rivaroxabán en esa población se completaron después de que comenzara nuestro ensayo. La diversidad según la raza y el grupo étnico fue limitada en la población del ensayo. Finalmente, el ensayo no tuvo la potencia suficiente para detectar diferencias en el riesgo de tromboembolismo venoso recurrente. Los hallazgos de nuestro ensayo no deben extrapolarse a otras indicaciones, incluida la prevención secundaria extendida del tromboembolismo venoso con una dosis completa o reducida de anticoagulantes orales directos, el tromboembolismo venoso agudo asociado al cáncer y la fibrilación auricular; un ensayo clínico que evalúa el riesgo de hemorragia con rivaroxabán y apixabán en pacientes con fibrilación auricular está en curso (número de ClinicalTrials.gov, NCT04642430 ).
Entre los pacientes con tromboembolismo venoso agudo, el riesgo de hemorragia clínicamente relevante a los 3 meses fue significativamente menor con apixabán que con rivaroxabán.
Notas
La declaración sobre el intercambio de datos proporcionada por los autores está disponible junto con el texto completo de este artículo en NEJM.org.
Financiado por subvenciones (PJT-153267 y PJT-189981) de los Institutos Canadienses de Investigación en Salud , una subvención (MRF1192408) del Fondo para el Futuro de la Investigación Médica para Colaboraciones Internacionales en Ensayos Clínicos en Australia , apoyo en especie del Real Colegio de Cirujanos de Irlanda y la Red Internacional de Redes de Investigación Clínica sobre Tromboembolia Venosa .
Agradecemos a la red CanVECTOR; a la Red Irlandesa para la Investigación de la Tromboembolia Venosa; a Marc Blondon, Lisa Baumann-Kreuziger y Sameer Parpia (del comité de monitorización de datos y seguridad); y a Margaret Ostrowski (paciente colaboradora de CanVECTOR).