Autores : Michelle Haber , Ph.D. , y Murray D. Norris , Ph.D. .Publicado 8 de abril de 2026 N Engl J Med 2026 ; 394 : 1447 – 1450 DOI: 10.1056/NEJMcibr2516825
No faltan consejos sobre qué comer después de recibir un diagnóstico de cáncer. La posibilidad de que las intervenciones dietéticas puedan mejorar los resultados del tratamiento oncológico ha generado un interés considerable entre pacientes, médicos e investigadores. Estudios mecanicistas emergentes sugieren que modificaciones dietéticas específicas pueden influir en el metabolismo tumoral y el microambiente tumoral, y potencialmente mejorar las respuestas a terapias convencionales como la quimioterapia y la radioterapia.<sup> 1 </sup> Sin embargo, a pesar de esta plausibilidad biológica y la prometedora evidencia preclínica, su traslación a la práctica clínica se ha visto obstaculizada por una importante laguna de conocimiento. La mayoría de los ensayos de intervenciones dietéticas han sido pequeños y a corto plazo, y se han centrado en resultados inespecíficos en lugar de en criterios de valoración clínicos del cáncer.<sup> 2</sup> El campo se enfrenta ahora al reto de ir más allá de las recomendaciones dietéticas generales para evaluar rigurosamente factores dietéticos específicos en ensayos controlados, aleatorizados y a largo plazo con la potencia estadística adecuada, con el fin de establecer guías nutricionales basadas en la evidencia para la atención oncológica.Los estudios preclínicos cuidadosamente diseñados son valiosos para identificar y refinar las preguntas que deben abordarse clínicamente. Un estudio de Cherkaoui et al., ³ realizado en un modelo de ratón ampliamente utilizado de neuroblastoma impulsado por MYCN , demostró cómo la manipulación dietética precisa puede reprogramar las características biológicas del cáncer. Su trabajo demostró que combinar la restricción dietética de aminoácidos específicos con un agente farmacológico que inhibe el metabolismo de las poliaminas (véase Conceptos clave ) puede tratar eficazmente la enfermedad de rápida progresión mediante un mecanismo novedoso que reprograma las células cancerosas para que dejen de proliferar y se diferencien en células más maduras.El neuroblastoma se origina en las células progenitoras de la cresta neural del sistema nervioso simpático, formando tumores con mayor frecuencia en las glándulas suprarrenales. El neuroblastoma impulsado por la amplificación del oncogén MYCN es uno de los cánceres más letales en niños. Al igual que muchos cánceres, el neuroblastoma impulsado por MYCN depende en gran medida de las poliaminas, que son pequeñas moléculas esenciales para el crecimiento y la proliferación celular. La eflornitina (también llamada difluorometilornitina), un fármaco que inhibe la síntesis de poliaminas al unirse irreversiblemente a la enzima limitante de la velocidad (ornitina descarboxilasa) en esta vía, ha mostrado resultados prometedores en la práctica clínica y recientemente recibió la preaprobación de la Administración de Alimentos y Medicamentos (FDA) para reducir el riesgo de recaída del neuroblastoma. 4 Sin embargo, la eficacia de este fármaco como monoterapia sigue siendo limitada.Cherkaoui y sus colegas combinaron eflornitina con una dieta libre de dos aminoácidos no esenciales, arginina y prolina, ambos metabolizables a ornitina, precursora de las poliaminas ( Figura 1A ). Mediante el seguimiento de metabolitos marcados con isótopos estables, los investigadores descubrieron que los tumores de neuroblastoma acumulan niveles inusualmente altos de prolina, pero aún dependen de la arginina y la ornitina circulantes para la producción de poliaminas. La arginina y la prolina se convierten en ornitina en otras partes del cuerpo, que los tumores luego importan como materia prima para la síntesis de poliaminas. Aunque la prolina puede catabolizarse a ornitina, los neuroblastomas con amplificación de MYCN presentan baja actividad de la enzima esencial para esta conversión (ornitina aminotransferasa). Por lo tanto, la dieta deficiente en arginina y prolina priva a los tumores de ornitina, mientras que la eflornitina bloquea la conversión de ornitina en poliaminas.
Figura 1
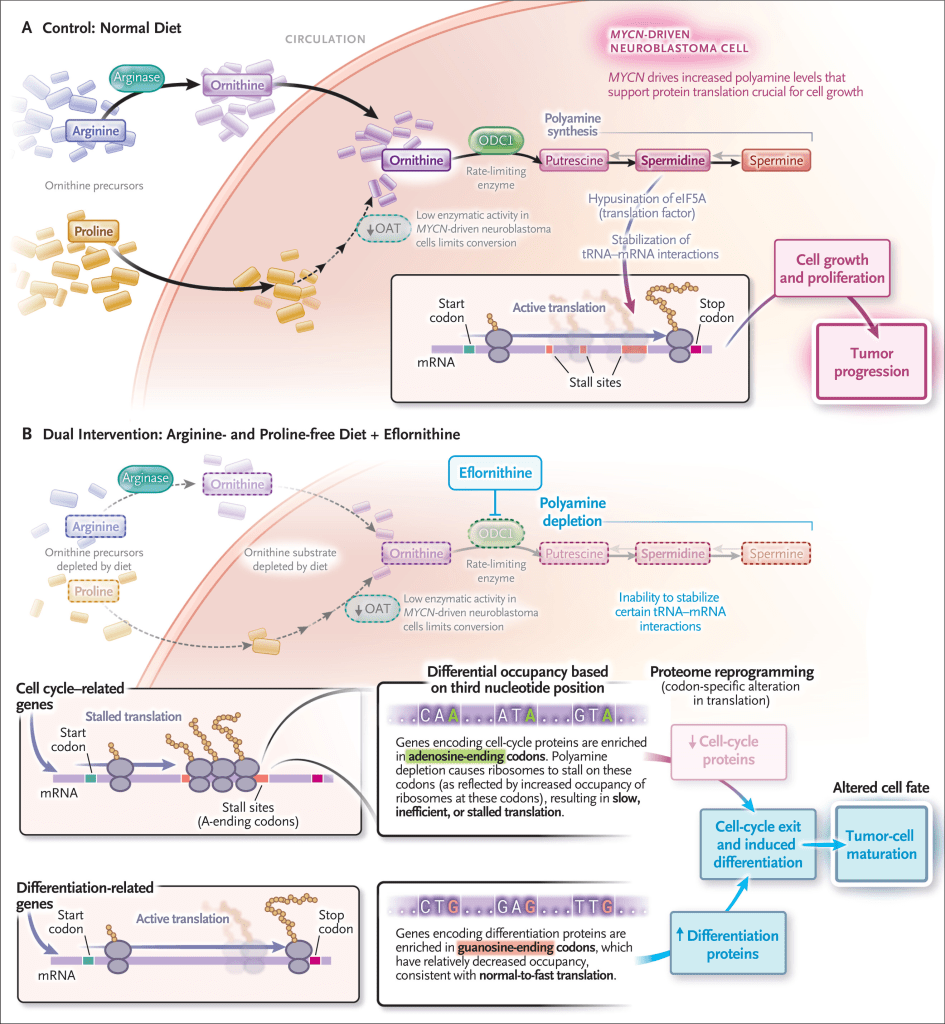
Un hallazgo sorprendente de esta investigación fue el mecanismo subyacente al efecto terapéutico. La deficiencia de poliaminas afecta la hipusinación del factor de traducción eIF5A, para el cual la espermidina (una poliamina) es un precursor esencial.
La hipusina es un aminoácido modificado único, derivado de la lisina y la espermidina, que se encuentra exclusivamente en la proteína eIF5A. Su deficiencia se produce sin suficiente espermidina, lo que resulta en un funcionamiento defectuoso de esta proteína. Si bien eIF5A también actúa como factor de exportación nuclear, transportando
ARN mensajeros (ARNm) específicos del núcleo al citoplasma, se le reconoce principalmente como factor de elongación de la traducción, promoviendo la
traducción de ARNm específicos, en particular aquellos que codifican secuencias de poliprolina u otras secuencias que provocan el bloqueo del ribosoma.Cherkaoui et al. probaron la hipótesis de que la base del efecto terapéutico observado era una reducción de eIF5A hipusinado que ocurría como resultado del agotamiento de poliaminas. Realizaron un perfilado de ribosomas, que mostró que el agotamiento de poliaminas provoca que los ribosomas se detengan, dependiendo de la identidad del nucleótido (adenosina, guanosina, uracilo o citosina) en la tercera posición («de balanceo») dentro del codón ( Figura 1B ). Los ribosomas se detenían específicamente en los codones que terminaban en adenosina en la posición de balanceo. Esta especificidad a nivel de codón del detención ribosomal tuvo consecuencias importantes. Los genes que codifican proteínas del ciclo celular están enriquecidos en codones que terminan en adenosina, mientras que los genes de diferenciación neuronal contienen menos de estos codones. En consecuencia, cuando se agotaron las poliaminas, los ribosomas tuvieron dificultades para traducir las proteínas del ciclo celular, pero continuaron traduciendo las proteínas necesarias para la diferenciación celular a una velocidad normal. Esta traducción selectiva generó un proteoma que favorecía la diferenciación, provocando que las células de neuroblastoma abandonaran el ciclo celular y se diferenciaran hacia neuronas más maduras. La ablación genética de la hipusinación no reprodujo estos efectos, lo que demuestra que el agotamiento de poliaminas, que no depende de aminoácidos específicos, es el principal impulsor de la reprogramación traslacional específica de codones observada tras una dieta deficiente en arginina y prolina añadida al tratamiento con eflornitina.Este estudio de Cherkaoui et al. tiene implicaciones importantes. Primero, proporciona una prueba de concepto de que las intervenciones metabólicas pueden desencadenar la diferenciación en cánceres infantiles, que a menudo surgen de células con desarrollo detenido que conservan características embrionarias.
5 Este enfoque de inducción de la diferenciación complementa las terapias existentes, como el ácido retinoico, pero opera a través de un mecanismo diferente: la reprogramación del proteoma mediante traducción selectiva, en lugar de la reprogramación transcripcional. Segundo, el hallazgo de que los programas celulares han desarrollado patrones de uso de codones distintos sugiere un mecanismo regulador que vincula el metabolismo con el destino celular. Los codones que requieren una abundancia de poliaminas para una traducción eficiente están enriquecidos en genes de proliferación y escasos en genes de diferenciación. Esta traducción selectiva implica que el uso de codones ha sido seleccionado evolutivamente para permitir respuestas coherentes y generalizadas a los cambios metabólicos; esencialmente, se ha codificado un interruptor metabólico en el genoma. Tercero, los principios pueden extenderse más allá del neuroblastoma. Es probable que el eje poliamina-codón-traducción opere en otros cánceres impulsados por
MYC , y el descubrimiento de que el estrés metabólico puede reconfigurar la traducción en función de la composición de codones puede revelar nuevas oportunidades terapéuticas en diversos tipos de cáncer.Al demostrar que la restricción de aminoácidos en la dieta puede potenciar la acción de fármacos específicos para inducir la diferenciación del cáncer, Cherkaoui et al. han proporcionado una hoja de ruta para el desarrollo clínico. El reto ahora consiste en sentar las bases para ensayos con la potencia estadística adecuada que permitan determinar si este enfoque sería beneficioso en niños con neuroblastoma agresivo.
Conceptos clave
CodónUna secuencia de tres nucleótidos de ADN o ARN que especifica un solo aminoácido o una señal de inicio o de parada.
ARN mensajero (ARNm)El ARN es una molécula que sirve de plantilla para la síntesis de proteínas. Se deriva del pre-ARNm, que se transcribe directamente del ADN. El pre-ARNm se procesa en el núcleo: los exones (segmentos de secuencia codificante) se unen, los intrones (segmentos de secuencia no codificante) se excluyen y se añade una «capuchón» de N7-metilguanosina en un extremo y una cola de poli-A en el otro. El pre-ARNm puede sufrir empalme alternativo, dando lugar a dos o más isoformas de ARNm y proteínas. El ARNm maduro se transporta del núcleo al citoplasma, donde el ribosoma lo traduce en proteína.
PoliaminaUna molécula policatiónica con dos o más grupos amino, sintetizada a partir de la ornitina, que a su vez se deriva de la arginina, la prolina y el glutamato. Las poliaminas también se obtienen de fuentes dietéticas y son producidas por bacterias intestinales. Las tres poliaminas principales son la putrescina, la espermidina y la espermina. Debido a su bajo peso molecular, adaptabilidad conformacional y alta carga positiva a pH fisiológico, las poliaminas interactúan fácilmente con moléculas cargadas negativamente, como el ADN, el ARN, el ATP y las proteínas. Mediante estas interacciones, regulan el metabolismo celular, la proliferación, la diferenciación y la apoptosis. Un metabolismo anormal de las poliaminas provoca la desregulación de estos procesos y se asocia con el cáncer y el envejecimiento.
Trascripción Proceso mediante el cual se lee la secuencia de nucleótidos en una molécula de ARN mensajero, codón por codón, para crear una secuencia de aminoácidos para la síntesis de proteínas.
- Stine ZE, Schug ZT, Salvino JM, Dang CV. Targeting cancer
metabolism in the era of precision oncology. Nat Rev Drug Discov
2022;21:141-62. - Ilerhunmwuwa NP, Abdul Khader AHS, Smith C, et al. Dietary interventions in cancer: a systematic review of all randomized controlled trials. J Natl Cancer Inst 2024;116:1026-34.
- Cherkaoui S, Turn CS, Yuan Y, et al. Reprogramming neuroblastoma by diet-enhanced polyamine depletion. Nature 2025;646:707-15.
- Duke ES, Bradford D, Sinha AK, et al. US Food and Drug Administration approval summary: eflornithine for high-risk neuroblastoma after prior multiagent, multimodality therapy. J Clin
Oncol 2024;42:3047-57.5. Marshall GM, Carter DR, Cheung BB, et al. The prenatal origins of cancer. Nat Rev Cancer 2014;14:277-89.