Targets of T cells responses to SARS CoV 2 Coronavirus in humans with COVID 19 Disease and no exposed Individuals
Alba Grifoni Daniela Weiskopf Sydney I. Ramírez Davey M. Smith Shane Crotty Alessandro Sett
Grifoni et al., 2020, Cell 181, 1489–1501 25 de junio de
Dr. Carlos Alberto Díaz.
Hipótesis que formulo desde la lectura de trabajos científicos: 1-Si bien la transmisión se frenó en las grandes urbes con seroconversiones de 12 a 20%, es porque el resto tiene inmunidad celular, para constituir la inmunidad de rebaño, 2- y como memoria inmunológica cruzada en algunos países asiáticos, que la enfermedad se auto limitó, a pesar de no tener sistemas de salud, despliegues epidemiológicos, o 3- son responsables de la reacción inflamatoria.
En los esfuerzos por desarrollar una comprensión clara de la inmunidad protectora SARS-CoV-2, el análisis de anticuerpos ha sido paralelo por estudios de células T cell a través de COVID-19 asintomática, leve y grave. Altmann y col. 2020. CORONAVIRUS SARS-CoV-2 T cell immunity: Specificity, function, durability, and role in protection
Definir las funciones de efector CD4 y CD8 en la protección es importante teniendo en cuenta que las respuestas de anticuerpos aparecen de corta duración y la memoria de células T cell es potencialmente más duradera. CORONAVIRUS SARS-CoV-2 T cell immunity: Specificity, function, durability, and role in protection
Para comprender completamente la inmunidad a nivel de población, sería beneficioso el cribado de anticuerpos y la inmunidad de células T mediante métodos de prueba estandarizados.
El análisis de la inmunidad de los células T al SARS-CoV-2 ha progresado rápidamente. La atención inicialmente se centró en la caracterización de las respuestas de anticuerpos, dictadas por la necesidad traslacional de pruebas diagnósticas y datos de seroprevalencia. Con respecto a la vacuna y la terapia, el impulso provino de la probabilidad de que los anticuerpos neutralizantes anti-picos sean un correlato de protección (CoP). Con el tiempo ha llegado la apreciación de que entre los individuos PCR+ son aquellos que muestran la inmunidad de células B y células T cell y aquellos con una respuesta discordante.
Se supone una respuesta relativamente efímera a los anticuerpos y una inmunidad más duradera a los células T fueron pronosticadas por experiencias con las infecciones por MERS y SARS-CoV-1 estrechamente relacionadas.
De todo lo que se conoce de la inmunología viral en general y la inmunidad de células T coronavirus específicamente, se podría suponer que la memoria de células T SARS-CoV-2 probablemente dura años y confiere protección.
La linfopenia es un marcador y correlato comúnmente observado de gravedad (según se juzga clínicamente y por proteína C reactiva elevada, dímero D y ferritina), especialmente dentro del subconjunto CD8
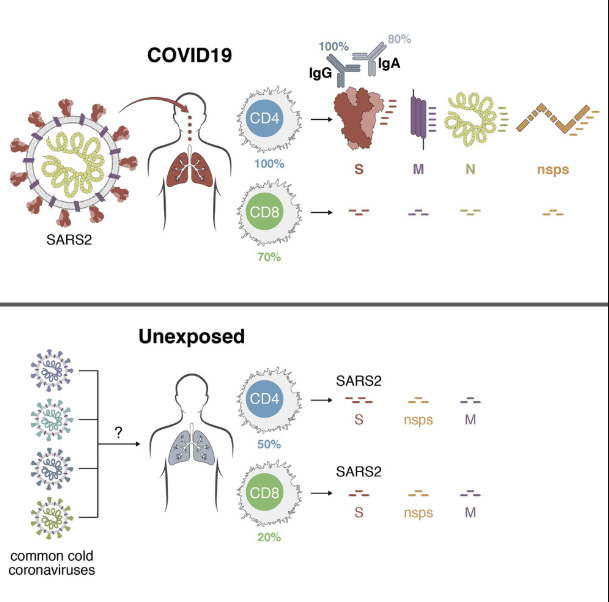
Los primeros pasos para tal comprensión radica en la capacidad de cuantificar las células T CD4 y CD8 específicas del virus.
Estos conocimientos son de importancia concreta, ya que proporcionarán información sobre la inmunidad y la patogénesis de la infección por SARS-CoV-2, y los mismos conocimientos ayudarán a diseñar y evaluar las vacunas candidatas.
Las estimaciones de inmunidad también son fundamentales para la estimación del modelo epidemiológico de futuras medidas de control pandémico de distanciamiento social (Kissler et al., 2020).
Estas proyecciones son dramáticamente diferentes dependiendo de si la infección por SARS-CoV-2 crea inmunidad sustancial, y si existe alguna inmunidad reactiva cruzada entre el SARS-CoV-2 y los coronavirus humanos estacionales circulantes «resfrío común» de circulación.
La definición y evaluación de las respuestas de células T SARS-CoV2 específicas del antígeno humano se hacen mejor con ensayos directos de células T ex vivos utilizando grupos de epítopos de base amplia y ensayos capaces de detectar células T de cualquier polarización de citoquinas. Aquí, hemos completado esta evaluación con muestras de sangre de pacientes COVID-19.
También existe una gran incertidumbre sobre si las respuestas inmunitarias adaptativas al SARS-CoV-2 son protectoras o patógenas, o si ambos escenarios pueden ocurrir dependiendo del momento, la composición o la magnitud de la respuesta inmunitaria adaptativa.
Las hipótesis abarcan toda la gama (Peeples, 2020), basada en los datos clínicos disponibles del síndrome de enfermedad respiratoria aguda grave (SARS) o el síndrome respiratorio de Oriente Medio (MERS) (Alshukairi et al., 2018, Wong et al., 2004, Zhao et al., 2017) o datos de modelos animales con SARS en ratones (2009, Zhao et al., 2010, Zhao et al., 2016), SARS en primates no humanos (NHPs) (Liu et al., 2019, Takano et al., 2008) o virus de peritonitis infecciosa felina (FIPV) en gatos (Vennema et al., 1990).
La inmunidad protectora, la inmunopatogénesis y el desarrollo de vacunas para COVID-19 se discuten brevemente a continuación, relacionados con la introducción de la importancia de definir las respuestas de los linfocitos T al SARS-CoV-2.
Sobre la base de datos de pacientes con SRAS en 2003-2004 (causado por SARS-CoV, el betacoronavirus humano más estrechamente relacionado con SARS-CoV-2), y sobre la base del hecho de que la mayoría de las infecciones virales agudas resultan en el desarrollo de inmunidad protectora (Sallusto et al., 2010), una probable posibilidad ha sido que la célula T CD4 sustancial, Las respuestas de células T CD8 y anticuerpos neutralizantes se desarrollan a SARS-CoV-2, y todas contribuyen al aclaramiento de la infección aguda, y, como corolario, algunas de las células T y B se retienen a largo plazo (es decir, varios años) como memoria inmunológica e inmunidad protectora contra la infección SARS-CoV-2 (Guo et al., 2020b, Li et al., 2008).
Sin embargo, un punto de vista contrario también es legítimo. Si bien la mayoría de las infecciones agudas dan lugar al desarrollo de inmunidad protectora, los datos disponibles para los coronavirus humanos sugieren la posibilidad de que no se produzcan respuestas inmunitarias adaptativas sustantivas(Choe et al., 2017, Okba et al., 2019, Zhao et al., 2017) y una inmunidad protectora sólida puede no desarrollarse (Callow et al., 1990).
Una falta de desarrollo de inmunidad protectora podría ocurrir debido a una respuesta de células T y/o anticuerpos de magnitud o durabilidad insuficientes, con la respuesta de anticuerpos neutralizantes dependiendo de la respuesta de los células T CD4(Crotty, 2019, Zhao et al., 2016).
Por lo tanto, es urgente comprender la magnitud y la composición de las respuestas humanas de los células T CD4 y CD8 al SARS-CoV-2. Si la infección natural con SARS-CoV-2 provoca potentes respuestas de células T CD4 y CD8 comúnmente asociadas con la inmunidad antiviral protectora, COVID-19 es un candidato fuerte para el desarrollo rápido de vacunas.
La inmunopaogénesis en COVID-19 es una grave preocupación científica (se trata de limitar farmacológicamente(Cao, 2020, Peeples, 2020). Es muy probable que una respuesta temprana de los glóbulos CD4 y CD8 contra SARS-CoV-2 sea protectora, pero una respuesta temprana es difícil de generar debido a los mecanismos de expresión inmune innatos y eficientes del SARS-CoV-2 en humanos (Blanco-Melo et al., 2020).
La expresión inmune por SARS-CoV-2 es probablemente exacerbada por la reducción de la función o disponibilidad de la célula de presentación de antígenos mieloides (APC) en los ancianos (Zhao et al., 2011).
En tales casos, es concebible que las respuestas de células T tardías puedan en cambio amplificar los resultados inflamatorios patógenos en presencia de altas cargas virales sostenidas en los pulmones, por múltiples mecanismos hipotéticos posibles(Guo et al., 2020a, Li et al., 2008, Liu et al., 2019).
Los resultados críticos (UCI) y fatales COVID-19 (y SARS) se asocian con niveles elevados de citoquinas inflamatorias y quimioquinas, incluyendo interleucina-6 (IL-6) (Giamarellos-Bourboulis et al., 2020, Wong et al., 2004, Zhou et al., 2020++)
El desarrollo de vacunas contra infecciones víricas agudas se centra clásicamente en la recapitulación provocada por la vacunación del tipo de respuesta inmunitaria protectora provocada por una infección natural. Este conocimiento fundamental está actualmente ausente para COVID-19, incluyendo cómo el equilibrio y los fenotipos de las células que responden varían como una función del curso de la enfermedad y la gravedad. Estos conocimientos pueden guiar la selección de las estrategias de vacunas con mayor probabilidad de obtener inmunidad protectora contra el SARS-CoV-2. Además, el conocimiento de las respuestas de los células T a COVID-19 puede guiar la selección de las variables inmunológicas adecuadas para los ensayos clínicos de vacunas candidatas COVID-19, que ya están comenzando.
También se dispone de información limitada sobre qué proteínas SARS-CoV-2 son reconocidas por las respuestas inmunitarias de células T humanas. En algunas infecciones, las respuestas de las células T están fuertemente sesgadas hacia ciertas proteínas virales, y los objetivos pueden variar sustancialmente entre las células T CD4 y CD8(Moutaftsi et al., 2010, Tian et al., 2019).
El conocimiento de las proteínas y epítopos SARS-CoV-2 reconocidos por las respuestas de células T humanas es de importancia inmediata, ya que permitirá el seguimiento de las respuestas inmunitarias COVID-19 en laboratorios de todo el mundo. Los conocimientos de los epitopos también ayudarán al diseño de vacunas candidatas y facilitarán la evaluación de la inmunogenicidad de los candidatos a la vacuna. Casi todos los candidatos actuales a la vacuna COVID-19 se centran en la proteína spike.
Una última cuestión clave a considerar en el estudio de la inmunidad SARS-CoV-2 es si existe algún grado de inmunidad al coronavirus reactivo cruzado en una fracción de la población humana, y si esto podría influir en la susceptibilidad a la enfermedad de COVID-19. Esta cuestión también es pertinente para el desarrollo de vacunas, ya que la inmunidad transfronteriza podría influir en la capacidad de respuesta a las vacunas candidatas (Andrews et al., 2015).
En resumen, la capacidad de medir y comprender las respuestas humanas de los células T CD4 y CD8 a la infección por SARS-CoV-2 es una importante brecha de conocimiento que actualmente obstaculiza el desarrollo de vacunas COVID-19, la interpretación de la patogénesis de la enfermedad COVID-19 y la calibración de futuras medidas de control pandémico de distancía social.

Identificación y cuantificación de respuestas específicas de células T CD4 de SARS-CoV-2+
Utilizamos ensayos de marcadores inducidos por activación dependiente del receptor de células T (TCR) para identificar y cuantificar células T CD4 específicas de SARS-CoV-2 en pacientes CON COVID-19 recuperados. La definición inicial y la evaluación de las respuestas de células T SARS-CoV-2 específicas del antígeno humano se hacen mejor con ensayos directos de células T ex vivo utilizando grupos de epítopos de base amplia, como MPs, y ensayos capaces de detectar células T de polarización de citoquinas desconocidas y atributos funcionales. Los ensayos AIM son ensayos independientes de la citoquina para identificar células T CD4 específicas de antígenos (Havenar-Daughton et al., 2016, Reiss et al., 2017). Los ensayos AIM se han utilizado con éxito para identificar células T CD4 específicas de virus, específicas de vacunas o tuberculosis en una serie de estudios (Dan et al., 2016, Dan et al., 2019, Herati et al., 2017, Morou et al., 2019).
Estimulamos los PBMC de 10 casos COVID-19 y 11 controles saludables (SARS-CoV-2 sin explotar, recogidos en 2015-2018) con un MP pico (MP_S) y el MP de clase II que cubre el resto del SARS-CoV-2 (no pico», MP CD4_R). Se utilizó un CMV MP como control positivo, mientras que DMSO se utilizó como control negativo.
Las respuestas de células T CD4 específicas de SARS-CoV-2 (OX40CD137) se detectaron en el 100% de los casos COVID-19 (p < 0.0001 frente a los donantes no expuestos spike MP, p a 0.002 frente al control DMSO,
Las respuestas de los células T CD4 al resto del SARS-CoV-2 también se detectaron en el 100% de los casos DE COVID-19 (p < 0.0079 frente a donantes no expuestos MP sin pico, p a 0.002, control no pico frente a DMSO, La magnitud de las respuestas de células T CD4 específicas del SARS-CoV-2 medidas fue similar a la del CMV MP.
La concordancia entre las mediciones de células T CD4 específicas de SARS-CoV-2 en experimentos independientes fue alta (p < 0.0002, .
Para evaluar la funcionalidad y la polarización de la respuesta de células T CD4 específicas de SARS-CoV-2, medimos las citoquinas secretadas en respuesta a la estimulación de MP. Las células T CD4 específicas de SARS-CoV-2 eran funcionales, ya que las células produjeron IL-2 en respuesta a los MPs sin pico y pico.
La polarización de las células parecía ser una T clásica. Se ha producido un tipo de interferón sustancial (IFN), mientras que poco o ningún tipo de IL-4, IL-5, IL-13 o IL-17 G-S3J).

Por lo tanto, los pacientes con COVID-19 recuperados generaron consistentemente una respuesta sustancial de células T CD4 contra SARS-CoV-2. Se llegaron a conclusiones similares utilizando el índice de estimulación. En términos de respuesta total de células T CD4 por donante, en promedio ∼50% de la respuesta detectada se dirigió contra la proteína de espiga, y ∼50% se dirigió contra el MP que representa el resto del SARS-CoV-2. Esto es importante, ya que la proteína de pico SARS-CoV-2 es un componente clave de la gran mayoría de las vacunas CANDIDAB-19 candidatas en desarrollo. Cabe destacar que, dada la naturaleza de las predicciones de péptidos MP_R, la respuesta real de los células T CD4 que se atribuiyó a los ORF no picos probablemente sea mayor, abordando en otros experimentos a continuación.
Identificación y cuantificación de respuestas específicas de células T CD8 de SARS-CoV-2+
Para medir las células T CD8 específicas de SARS-CoV-2 en los pacientes COVID-19 recuperados, utilizamos dos metodologías complementarias, ensayos AIM y tinción de citoquinas intracelulares (ICS). Se utilizaron los dos MP de clase I SARS-CoV-2, CD8-A y CD8-B, con CMV MP y DMSO que sirven como controles positivos y negativos, respectivamente. Las respuestas de los células T CD8 fueron detectadas por AIM (CD69CD137) en el 70% de los casos COVID-19 (p < 0.0011 frente a los donantes no explorados «CD8 total»,; p a 0.002, CD8-A o CD8-B frente al control DMSO. MP CD8-A contiene epitopos de espiga, entre epítopos a otras proteínas. La magnitud de las respuestas reactivas de células T CD8 DE SARS-CoV-2 medidas por AIM fue algo menor que la CMV MP. Se llegaron a conclusiones similares utilizando el índice de estimulación.

De forma independiente, los ensayos ICS detectaron células T CD8 específicas de IFN—COV-CoV-2 en la mayoría de los casos COVID-19. La mayoría de las células IFN-o co-expresadas enzima B. Una fracción sustancial de las células de IFN-o expresó el factor de necrosis tumoral (TNF) pero no IL-10. Por lo tanto, la mayoría de los pacientes recuperados con COVID-19 generaron una respuesta de células T CD8 contra SARS-CoV-2
Relación entre las respuestas específicas de los células T CD4 de SARS-CoV-2 y los títulos IgG e IgA+
La mayoría de las respuestas de anticuerpos protectores dependen de la ayuda de los células T CD4. Por lo tanto, evaluamos si las respuestas más sólidas de células T CD4 específicas de SARS-CoV-2 se asociaron con títulos de anticuerpos más altos en casos COVID-19. Dado que el pico es el objetivo principal de los anticuerpos neutralizantes del SRAS, examinamos las células T CD4 específicas de picos. Las respuestas de células T CD4 específicas de spike se correlacionaron bien con la magnitud de los títulos igG de RBD anti-spike (R a 0,81; p < 0,0001;. Se obtuvieron resultados similares utilizando el índice de estimulación. La respuesta de células T CD4 no-spike SARS-CoV-2 no se correlacionó también con los títulos igG de RBD anti-spike, de acuerdo con un requisito común para la ayuda de células T CD4 intramoleculares. Los títulos IgA anti-spike también se correlacionan con células T CD4 específicas de picos (p < 0.0002,. Por lo tanto, los pacientes con COVID-19 hacen que las respuestas de anticuerpos anti-spike RBD sean proporcionales a la magnitud de su respuesta específica de células T CD4 específicas de pico. A continuación, evaluamos la relación entre las respuestas de los células T CD4 y CD8 con el SARS-CoV-2. Las respuestas de células T CD4 y CD8 específicas de SARS-CoV-2 estaban bien correlacionadas (R a 0,62. p a 0,0025, Por lo tanto, las respuestas de los anticuerpos, CD4 y células T CD8 al SARS-CoV-2 estaban generalmente bien correlacionadas
Células T específicas del coronavirus reactivo cruzado preexistentes
Mientras que las respuestas de células T CD4 no específicas de picos y no picos eran detectables en todos los casos COVID-19, las células también se detectaron en individuos no expuestos . Estas respuestas fueron estadísticamente significativas para la reactividad de células T CD4 no específicas (no pico, p a 0,039; pico, p a 0,067;. Las respuestas no específicas de los células T CD4 estaban por encima del límite de detección en el 50% de los donantes sobre la base del índice de estimulación (SI). Todos los donantes fueron contratados entre 2015 y 2018, excluyendo cualquier posibilidad de exposición al SARS-CoV-2. Cuatro coronavirus humanos son causas conocidas de infecciones estacionales del tracto respiratorio «común» : HCoV-OC43, HCoV-HKU1, HCoV-NL63 y HCoV-229E. Probamos a los donantes no expuestos SARS-CoV-2 en busca de seroreactividad a HCoV-OC43 y HCoV-NL63 como un betacoronavirus representativo y alfacoronavirus, respectivamente. Todos los donantes eran seropositivos IgG a HCoV-OC43 y HCoV-NL63 RBD, en diferentes grados(Figura 5C), de acuerdo con la naturaleza endémica de estos virus (Gorse et al., 2010, Huang et al., 2020, Severance et al., 2008). Por lo tanto, examinamos si representaban verdaderas células T pan-coronavirus capaces de reconocer epítopos SARS-CoV-2.