Impact of circulating SARS-CoV-2 variants on mRNA vaccine-induced immunity in uninfected and previously infected individuals
Carolina Lucas1,9, Chantal B. F. Vogels2,9, Inci Yildirim3,4,9, Jessica E. Rothman2 , Peiwen Lu1 , Valter Monteiro1 , Jeff R. Gelhausen1,5, Melissa Campbell6 , Julio Silva1 , Alexandra Tabachikova1 , M. Catherine Muenker2 , Mallery I. Breban2 , Joseph R. Fauver2 , Subhasis Mohanty1,6, Jiefang Huang1,6, Yale SARS-CoV-2 Genomic Surveillance Initiative*, Albert C. Shaw1,6, Albert I. Ko2,6, Saad B. Omer2,4,6,10, Nathan D. Grubaugh2,7,10 & Akiko Iwasaki1,8,10†
En este complejo trabajo de investigación, los autores intentan descifrar cual sería la combinación más efectiva para prevenir la propagación del coronavirus en sus nuevas variantes, con la vacunación de ARNm. Si bien no son concluyentes los hallazgos, las respuestas de los que han tenido la infección más dos dosis desarrollan más capacidad neutralizante. Esto podría por efecto de intervalo o por algo que la inmunidad natural que prepara mejor la respuesta inmunitaria, o porque en la práctica recibió tres dosis de antígenos una natural y dos de ARN m. No lo sabemos. Pero dejan instalada la hipótesis. Pero puede estar vinculado a la cantidad de dosis, tres. Aún el CDC no se expide si es conveniente una tercera dosis. Tal vez porque primero gran parte del planeta debería estar vacunado, para no dar lugar a que existan nuevas cepas o linajes por la transmisión interhumana. En este momento la principal potencia del mundo y otros países desarrollados entienden que debe recuperarse más nivel de vacunación en los países más pobres y en las poblaciones marginadas, como también intentar convencer a los adultos que se resisten a vacunarse. Debería ser obligatoria la vacunación de covid. Esto luego del tiempo y la cantidad de dosis administradas tendrìamos que plantearlo. Entiendo que terminaremos al año de la vacunación aplicando un refuerzo, que podría ser heterólogo. Como así también poder utilizar vacunas de distintas plataformas entre primera y segunda dosis.
Resumen
La aparición de variantes del SARS-CoV-2 con mutaciones en los principales sitios de enlace de anticuerpos neutralizantes puede afectar la inmunidad humoral inducida por la infección o la vacunación1-6.
Se analizó el desarrollo de anticuerpos anti-SARS-CoV-2 y respuestas de células T en individuos previamente infectados (recuperados) o no infectados (ingenuos) que recibieron vacunas de ARNm al SARS-CoV-2.
Mientras que los individuos previamente infectados sufrieron títulos de anticuerpos más altos que los individuos no infectados después de la vacunación, estos últimos alcanzaron niveles comparables de respuestas de neutralización a la cepa ancestral que los individuos previamente infectados 7 días después de la segunda dosis de la vacuna. Los marcadores de la activación de la célula de T medidos sobre el estímulo in vitro del péptido del pico o de la nucleocáppmente mostraron un aumento progresivo después de la vacunación en los tiempo-puntos analizados.
El análisis comprensivo de la neutralización del plasma usando 16 aislantes auténticos de las variantes localmente de circulación distintas SARS-CoV-2 reveló una gama de reducción en la capacidad de la neutralización asociada a mutaciones específicas en el gene del punto: los linajes con E484K y N501Y/T (e.g., B.1.351 y P.1) tenían la reducción más grande, seguida por linajes con L452R (e.g., B.1.617.2) o con E484K (sin N501Y/T).
Si bien ambos grupos conservaron la capacidad de neutralización contra todas las variantes, el plasma de individuos vacunados previamente infectados mostró una mejor capacidad general de neutralización en comparación con el plasma de individuos no infectados que también recibieron dos dosis de vacunas, lo que apunta a los refuerzos de vacunas como una estrategia futura relevante para aliviar el impacto de las variantes emergentes en la actividad neutralizante de anticuerpos.
Desarrollo:
La evolución en curso y la aparición de variantes del coronavirus 2 del síndrome respiratorio agudo severo (SARS-CoV-2) suscitan preocupación sobre la eficacia de los anticuerpos monoclonales (mAbs) terapias y vacunas.
Las vacunas basadas en ARNm Pfizer-BioNTech BNT162b2 y Moderna mRNA-1273 codifican un ectodominio de espiga de SARS-CoV-2 de longitud completa estabilizado derivado de la secuencia genética wuhan-hu-1 y provocan potentes anticuerpos neutralizantes (MAbs)7,8.
Sin embargo, las variantes emergentes de SARS-CoV-2 con mutaciones en el gen spike (S), especialmente en atrapar sitios de unión, se han asociado con el aumento de la transmisibilidad9,10, así como la resistencia a la neutralización a mAbs, plasma convaleciente y sueros de individuos vacunados1–6.
Para comprender mejor cómo las respuestas inmunitarias desencadenadas por la infección por SARS-CoV-2, y / o la vacunación, se comparan con las variantes de virus emergentes, reunimos una cohorte de ARNmindividuos vacunados, previamente infectados o no, y perfiles inmunológicos específicos del virus.
Se examinó el impacto de las variantes de SARS-CoV-2 que contienen muchas mutaciones clave en el gen S diferentes en individuos vacunados con ARNm utilizando un conjunto completo de aislados auténticos de SARS-CoV-2 de longitud completa. Nuestro grupo especial de variantes incluyó representantes que actualmente están clasificados como «variantes de preocupación» (linajes B.1.1.7 [Alfa], B.1.351 [Beta], P.1 [Gamma] y B.1.617.2 [Delta]), y «variantes de interés» (B.1.427/B.1.429 [Epsilon], B.1.525 [Eta], B.1.526 [Iota] y B.1.617.1 [Kappa]).
En primer lugar, para caracterizar las respuestas inmunitarias adaptativas específicas del SARS-CoV-2 post mRNA VACUNAS COVID (Moderna o Pfizer), cuarenta trabajadores sanitarios (HHC) del Hospital Yale-New Haven (YNHH), se inscribieron en este estudio entre noviembre de 2020 y enero de 2021, con un total de 198 muestras.
Se estratificó a los participantes vacunados en función de la exposición previa al SARS-CoV-2 en grupos previamente infectados (recuperados) o no infectados (ingenuos). La infección anterior fue confirmada por RT-qPCR y SARS-CoV-2 IgG ELISA.
Los TCM recibieron vacunas de ARNm, ya sea Pfizer o Moderna, y las seguimos longitudinalmente pre y post vacunación (Figura 1a). Los datos demográficos básicos de la cohorte, la información de vacunación y el estado serológico se resumen en la Tabla de datos extendida 1. Recogimos el plasma y las células mononucleares de la sangre periférica (PBMCs) secuencialmente en 5 puntos del tiempo que cubrían un período de 98 días después de la primera dosis de la vacunación. Las muestras se recogieron al inicio (antes de la vacunación), 7 y 28 años después de la primera dosis de vacunación, y 7, 28 y 70 días después de la segunda dosis de vacunación. (Figura 1a). Determinamos perfiles del anticuerpo, usando análisis de ELISA y de las neutralizaciones; y la inmunorespuesta celular evaluada, perfilada por cytometry de flujo usando PBMCs congelados. Encontramos que las vacunas del mRNA indujeron altos títulos de los anticuerpos virus-específicos que disminuyeron en un plazo, como previamente reported6,11 (Figura 1b, c). Después de la primera dosis de la vacuna, más del 97% de los participantes vacunados desarrollaron títulos de IgG específicos del virus, que aumentaron al 100% después de la segunda dosis. Los títulos de IgG contra la proteína S, la subunidad de espiga 1 (S1) y el dominio de unión al receptor (RBD) alcanzaron su punto máximo 7 días después de la segunda dosis de vacunación (Figura 1 b, c). No se observaron diferencias en los niveles de anticuerpos entre los participantes vacunados de diferentes sexos y después de la estratificación por edad (Datos Extendidos Figura 1a).
De acuerdo con informes anteriores7,12, encontramos que los niveles de IgG específicos del virus fueron significativamente más altos en el grupo vacunado previamente infectado que en el grupo vacunado no infectado (Datos Extendidos Figura 1b y Figura 1c).
Como era de esperar, dada la ausencia de secuencias que codifican antígenos de nucleocáppsidos (N) en las vacunas de ARNm, los títulos de anticuerpos anti-N permanecen estables en el tiempo para los individuos vacunados previamente infectados, y no se vieron afectados por la vacunación tanto en el grupo no infectado como en el previamente infectado (Figura 1 b, c).
A continuación, evaluamos la actividad de neutralización plasmática longitudinalmente contra una cepa auténtica de SARS-CoV-2 USA-WA1/2020 (linaje A), con una secuencia de aminoácidos del gen S similar a la de Wuhan-Hu-1 utilizada para el diseño de la vacuna de ARNm, mediante un ensayo de neutralización de reducción de placa (PRNT50) del 50%. La actividad de neutralización se correlaciona directamente con los títulos de anticuerpos anti-S y anti-RBD, alcanzando también su punto máximo a los 7 días después de la segunda dosis (Figura 1 d, e).
Sin embargo, ambos grupos mostraron títulos de neutralización similares contra el aislado del virus del linaje A en el pico de respuesta (Figura 1 d, e). Nuestros datos indican que a pesar de respuestas más rápidas y más exuberantes del anticuerpo a las proteínas virales por los individuos vacunados previamente infectados que los no infectados vacunados, la vacunación llevó a los niveles similares totales de anticuerpos neutralizantes (atrapar) después de la segunda dosis. Una respuesta robusta de las células T también se ha relacionado con una inmunidad protectora eficiente contra el SARSCoV-213–15.
Por lo tanto, analizamos longitudinalmente siguientes respuestas de las células de T S y N-reactivas en individuos vacunados. Para detectar poblaciones de células T específicas de péptidos de baja frecuencia, primero expandimos las células T específicas de los antigénicos mediante la estimulación de los PBMCs de individuos vacunados con grupos de péptidos S y N ex vivo durante 6 días, seguidos de la reimulación con los mismos grupos de péptidos y el análisis de los marcadores de activación después de 12 horas. Para cubrir la proteína S entera, dos piscinas del péptido fueron utilizadas (S-I y S-II), mientras que una sola piscina del péptido fue utilizada para el estímulo de la nucleocápmenteide. Las células T S-reactivas CD4+ y CD8+ aumentaron en un plazo que seguía vacunación (Figura 2 a, b), como lo demuestra un aumento de las células que expresan los marcadores de activación CD38 y HLA-DR; no se observaron diferencias entre los grupos vacunados previamente infectados y no infectados.
De acuerdo con informes anteriores16,17, las respuestas S reactivas de células T CD4+ fueron comparables entre los aislados de virus de linaje A y P.1 de longitud completa. Por el contrario, las respuestas de las células T CD8+ reactivas S sólo se observaron en el linaje A, y no en P.1, 28 días después de la segunda dosis de vacunación, lo que sugiere que las respuestas de las células T CD8 específicas de S pueden verse afectadas por las mutaciones dentro del gen S de las variantes de SARS-CoV-2 (Figura 2b).
Como era de esperar, las células T N reactivas inducidas después de la estimulación con un pool de N-péptidos derivados del aislado del virus del linaje A se observaron principalmente en los individuos vacunados previamente infectados (Figura 2b). Inesperadamente, también observamos células T CD4 N reactivas elevadas en individuos previamente infectados a los 28 días después de la segunda dosis, paralelamente a la activación general de las células T CD4 (Figura 2b y Datos Extendidos Figura 2a). Por otra parte, observamos niveles crecientes de CD4+ activado T, Tfh, y células secretoras de anticuerpos 28 días después del refuerzo de la vacunación (Datos Extendidos Figura 2). Por lo tanto, las respuestas de las células T en los individuos vacunados muestran una dinámica similar a la de las respuestas de anticuerpos.
Para investigar las posibles diferencias en atrapar escape entre las variantes de SARS-CoV-2, se analizó la capacidad de neutralización de muestras plasmáticas de individuos vacunados contra un panel de 18 aislados de SARS-CoV-2 genéticamente distintos y auténticos. Entre los aislados, 16 eran de nuestro programa de vigilancia genómica sars-cov-2 de Connecticut que representan variantes de la misma región geográfica que nuestra cohorte HCW18.
Nuestro panel de variantes incluye representantes de todos los linajes actualmente clasificados como variantes de interés (B.1.1.7, B.1.351, P.1 y B.1.617.2), así como linajes clasificados como variantes de interés (B.1.427, B.1.429, B.1.525, B.1.526, y B.1.617.1)19. Además, seleccionamos linajes con mutaciones clave en el gen S (B.1.517 con N501T, y B.1 y R.1 con E484K)20, y incluyó el linaje A como comparación (Figura 3a). Para ayudar a desconvoluir los efectos de mutaciones individuales, incluimos 4 diversos aislantes de B.1.526 (etiquetados como B.1.526a-d) que representan diversos clados filogenéticos y mutaciones de gene dominantes de S (L452R, S477N, y E484K; Datos extendidos Figura 3b), dos diferentes aislados B.1.1.7 con (B.1.1.7b) y sin E484K (B.1.1.7a, el más común), y dos aislados B.1.351 con (B.1.351b) y sin L18F (B.1.351a, el más común; Figura 3a &Tabla de datos extendida 2). Excepto el linaje A, todos los aislados (linajes B, P y R) tienen la mutación del gen S D614G localizada en el motivo de unión al receptor, que se ha reportado que no afecta la neutralización provocada por la vacuna21. Para cada aislado destacamos diferencias adicionales de aminoácidos clave concentradas en la subunidad 1, incluyendo RBD y sitios antigénicos adicionales de la proteína S (Figura 3a): L18F y ΔH69/V70 (deleciones) situado en el amino-terminal dominio (NTD); K417N y L452R situados en los epítopos del RBD; S477N, T478K, E484K/Q y N501T/Y ubicados en la interfaz RBD-ACE2; y P681H/R situado en el sitio de escisión. Una lista completa de sustituciones y deleciones de aminoácidos de todos los genes se proporciona en la Tabla de Datos Extendida 2.
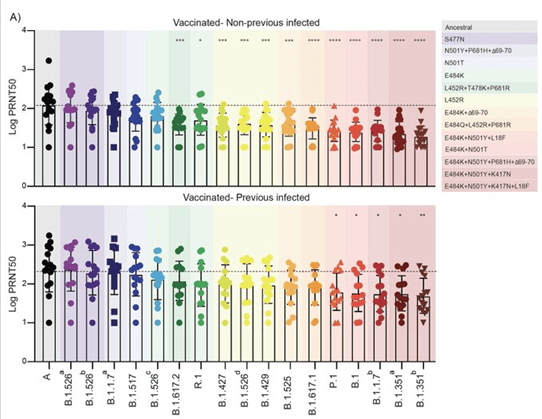
Utilizamos un análisis PRNT50 para determinar los títulos de la neutralización del plasma recogido a partir de 32 HCWs 28 días después de la segunda dosis de la vacunación a cada aislante. Al comparar la neutralización inducida por la vacuna contra los diferentes aislados en comparación con el aislado del virus del linaje A, observamos una reducción significativa de los títulos de PRNT50 para 12 de los 17 aislados, y el orden de rango de neutralización reducida agrupado principalmente por las diferencias clave de aminoácidos del gen S (Figura 3a). Aislados de virus con las mutaciones E484K y N501Y (o N501T) (B.1.351 ter , B.1.351a , B.1.1.7b , B.1, y P.1) redujo la neutralización más (4.6-6.0 doblez disminución en títulos PRNT50). Aislados de virus con la mutación L452R (B.1.617.1, B.1.429, B.1.526 ter , B.1.427, y B.1.617.2) estaban en la agrupación siguiente de la neutralización disminuida (disminución del doblez 2.5-4.1), que traslapado parcialmente con los aislantes con E484K pero sin N501Y/T (B.1.525, R.1, y B.1.526c; disminución del doblez 2.0-3.8). Estos datos sugieren que las mutaciones de gene de S L452R, E484K, y N501Y tengan los efectos individuales más grandes sobre la neutralización de disminución.
Para evaluar más a fondo esta posibilidad, construimos un modelo mezclado linear con efectos al azar del sujeto-nivel para explicar las diferencias en el resultado de la neutralización (títulos transformados logarítmico PRNT50) por cada mutación individual con respecto al linaje A (sin mutación; Figura 3b). De nuestro modelo, estimamos que 8 de las 11 mutaciones de gene dominantes de S que investigamos tenían efectos negativos significativos sobre la neutralización, y que L452R (2.8 dobleces disminución de los títulos de PRNT50 [media]; p< 2e-16) y E484K/Q (disminución del doblez 2,0; p< 2e-16) tenían los efectos individuales más grandes.
Como las combinaciones de mutaciones pueden alterar los efectos de manera diferente que el valor añadido de cada una individualmente (es decir. interacciones epistáticas), también creamos un segundo modelo mezclado linear que controló para todas las mutaciones individuales en el primer modelo así como tres combinaciones comunes de mutaciones de gene dominantes de S encontradas en nuestros aislantes: ΔH69/V70 y E484K, L452R y P681R, y E484K y N501Y. Estas combinaciones de mutaciones nos permitieron evaluar si la contribución de las mutaciones juntas es sinérgica, antagónica o ninguna de las dos. Nuestro modelo sugiere que el ΔLa combinación H69/V70 y E484K fue sinérgica (es decir. disminuyó la neutralización más que los efectos añadidos de cada uno; β=-0,182; p=0,005), L452R y P681R eran antagónicos (es decir neutralización disminuida menos que los efectos añadidos de cada uno; β=0,228; p=0,003), y E484K y N501Y no eran ninguno de los dos (es decir, la neutralización probablemente la suma de los efectos individuales de cada uno; β=0,060; p=0,248). Por lo tanto, a partir de nuestro gran panel de aislados de virus, encontramos que el genotipo del virus juega un papel importante en la neutralización inducida por la vacuna, con L452R probablemente teniendo el el mayor impacto individual, pero los efectos añadidos de E484K y N501Y hacen que los virus con esta combinación sean quizás los más preocupantes para las vacunas. Aunque los factores específicos del virus pueden desempeñar un papel significativo en la neutralización, las diferencias en la actividad de neutralización entre los TCM vacunados individuales fueron mucho mayores (hasta ~ 2 títulos de registro PRNT50) que las diferencias entre los aislados de virus (en su mayoría
Por lo tanto, nuestros datos sugieren que la actividad de neutralización plasmática contra las variantes de SARS-CoV-2 mejore en individuos vacunados previamente infectados con el virus. Estos resultados sugieren que los futuros refuerzos de la vacuna (tercera dosis) pueden ayudar a superar la reducción de la capacidad de neutralización observada para las variantes, en particular las de los genotipos con el L452R (por ejemplo, B.1.617.2) o la combinación E484K y N501Y (por ejemplo, P.1 y B.1.351).
Discusión
Los NAbs humanos contra el SARS-CoV-2 pueden clasificarse como pertenecientes a cuatro clases sobre la base de sus regiones objetivo en el RBD. Aunque la RBD es inmunodominante, hay evidencia de un papel sustancial de otras regiones espigas en la antigenicidad, sobre todo el supersitio ntd22-24.
Estos anticuerpos se dirigen a los epítopos que están estrechamente asociados con los residuos de NTD y RBD L18 y ΔH69/V70, y K417, L452, S477, T478, E484 y N501.
Estudios previos utilizando construcciones de pseudovirus relataron un impacto significativo de sustituciones de aminoácidos S individuales, incluyendo S477N, E484K y N501Y, localizadas en la interfaz RBD-ACE2, en la actividad de neutralización del plasma de individuos vacunados1–5.
Usando un panel grande de aislados auténticos genéticamente diversos de SARS-CoV-2, encontramos que las disminuciones en la capacidad de neutralización inducida por la vacuna de ARNm podrían clasificarse generalmente en tres niveles basados en la presencia de L452R, E484K y / o N501Y / T.
Nivel 1, que encontramos para disminuir los títulos de neutralización por >10 veces en individuos vacunados previamente no infectados, incluye linajes con las mutaciones E484K y N501Y / T como B.1.351 (Beta) y P.1 (Gamma), apoyando aún más su importancia en lo que respecta a las vacunas. Interesante, también encontramos que un aislante genérico del linaje B.1 con E484K y N501T, y un aislante raro de B.1.1.7 (alfa) con E484K (también con la mutación común de N501Y) tienen impactos similares en la neutralización como B.1.351 y P.1.
Mientras que las combinaciones de mutaciones en el B.1 y B.1.1.7 con los aislantes de E484K probablemente no aumentan transmisibilidad, los efectos aditivos de estas dos mutaciones apoyan que los programas de la vigilancia deben seguir todos los virus con E484K y N501Y/T además de variantes de la preocupación/del interés.
El nivel 2 consiste en linajes sars-CoV-2 con la mutación L452R, y el nivel 3 consiste en linajes con E484K pero sin N501Y/T. Notablemente, los linajes con la mutación L452R incluyen B.1.617.2 (Delta). Encontramos que B.1.617.2 tenía un impacto comparativamente modesto en títulos de la neutralización: disminución de 6,9 dobleces en no infectado y disminución de 1,5 dobleces en individuos vacunados previamente infectados (disminución de 2,5 dobleces combinada) con respecto al linaje A. A partir de estos datos, esperamos que la mayoría de los individuos completamente vacunados estén protegidos contra B.1.617.2, y que el aumento de los avances en la vacuna asociados con esta variante se asocien más probablemente con su alta transmisibilidad25-28. Nuestra inclusión de 4 versiones diferentes de B.1.526 (Iota, detectada por primera vez en Nueva York) muestra la jerarquía de virus con L452R, S477N o E484K con respecto a la neutralización de la vacuna. Mientras que algunos han especulado que B.1.526 con E484K puede tener las mayores implicaciones para la salud pública29,30, encontramos que B.1.526 con L452R disminuye la neutralización más que las otras versiones. En general, encontramos que L452R tiene el mayor efecto individual sobre la neutralización a través de varios linajes, y los virus sin L452R o E484K tienen efectos insignificantes sobre la neutralización (esto incluye B.1.526 con S477N).
Las discrepancias de nuestros resultados en comparación con otros estudios pueden señalar la importancia de utilizar virus auténticos completamente intactos para los ensayos de neutralización para detectar los efectos de la epistasis entre las mutaciones del virus en los ensayos de neutralización.
Sin embargo, sigue siendo posible que los factores adicionales también contribuyan a algunas de las discrepancias entre nuestras observaciones y las de estudios anteriores, incluyendo la composición de nuestras cohortes, predominantemente mujeres caucásicas jóvenes.
Las discrepancias entre las cohortes también podrían explicar las diferencias sutiles en las respuestas de las células T observadas en nuestro estudio en comparación con las reportadas recientemente por Alter et al., y Tarke et al.
Si bien observamos una disminución de la reactividad cruzada de las células T CD8+ S reactivas contra los péptidos P.1 S, los estudios anteriores encontraron que las respuestas de las células T se conservan en gran medida contra las variantes16,17.
Además de la composición de cohortes, utilizamos grupos de péptidos superpuestos en nuestros ensayos, por lo tanto, no podemos descartar la posibilidad de que algunas mutaciones afecten al procesamiento de antígenos antes de la presentación. Además, Alter et al. utilizaron una vacuna AdV1,2616, mientras que la nuestra y Tarke et al. utilizaron vacunas de ARNm17.
Una limitación potencial en nuestro estudio es que, incluso con nuestro estímulo de 7 días antes de análisis, sigue siendo posible que nuestro análisis de las células de T no pudo detectar las copias infrarrepresentadas del glóbulo de T afectadas por secuencias variables cuando estaba muestreada en presencia de la mayoría de los péptidos conservados.
En general, nuestros datos apuntan a la necesidad de un seguimiento activo de la reactividad de las células T en el contexto de la evolución del SARS-CoV-2. La magnitud de los títulos de anticuerpos en pacientes de COVID-19 después de una infección natural se ha correlacionado directamente con la duración de la infección y la gravedad31.
Aquí, encontramos que los individuos vacunados previamente infectados muestran una mayor resiliencia en las respuestas de anticuerpos contra «solo» y la combinación de sustituciones en la región de RBD, que de lo contrario disminuyó gravemente la actividad de neutralización de los individuos vacunados no infectados.
Nuestras observaciones del impacto de la inmunidad preexistente en individuos vacunados en su capacidad de neutralizar variantes podrían explicarse por la ventana de tiempo entre la exposición inicial (infección) y la vacunación.
Aún así, nuestras observaciones proporcionan una justificación importante para los esfuerzos mundiales en la caracterización de la contribución de la inmunidad preexistente al SARS-CoV-2 al resultado de varias estrategias de vacunación.
Junto con las pruebas serológicas recientemente introducidas32, estos estudios podrían informar la evaluación de riesgos basada en la evidencia, el monitoreo del paciente, la adaptación de los métodos de contención y el desarrollo y despliegue de vacunas.
Por último, estos hallazgos sugieren que una tercera dosis de vacunación adicional puede ser beneficiosa para conferir una mayor protección contra los linajes del SARS-CoV-2, como B.1.351 y P.1.