Apuntes propios de la conferencia de la PhD Akiko Iwasaki. Universidad de Yale.
Utilidad del posteo:
Quiero señalar ocho conceptos dianas expresados por Akiko Iwasaki, que escuche y leí de esta investigadora invitada a un webinar de la Sociedad Argentina de Inmunología y en sus publicaciones:
1-porque el virus tiene «éxito» en generar una infección y como se propaga, como el virus evita los mensajeros para desencadenar respuestas adaptativas.
2-Una respuesta inadecuada por esta misma razón falla en producir interferón 1, de la respuesta innata.
3-La respuesta inmune es tanto por células B y T, y cuanto durarían las respuestas inmunes, los anticuerpos bajan luego de ocho semanas de producida la infección.
4. Describe que el sistema inmune se confunde. cómo se genera la confusión en el sistema inmune, con respuestas inmunes mal dirigidas.
5. Uno de los aspectos más interesantes desde lo conceptual es como explica desde el punto de vista inmunológico el Long Covid, o el post covid, desde tres mecanismos: reservorio viral en alguna parte del cuerpo no descubierto, lo segundo el estímulo antigénico por partículas virales, tercero respuestas de características autoinmunes, algo que he escrito hace pocos días.
6. Señala que hay que tener cuidado con intentar generar o esperar inmunidad de rebaño, magnitud y algo que no es correcto esperar.
7. la humedad para aumentar la productividad del movimiento mucociliar. Todos estos conceptos me parecen reveladores, apasionantes, disruptivos y muy importantes para acortar el camino de la investigación a la clínica. Realizó pruebas de sobrevida en ratos con diferente humedad en su hábitat, demostrando mayor mortalidad en los ratones hACE2, con ambientes más secos.
8. Revela Tres mecanismos inmunológicos que explican la gravedad evolutiva de la enfermedad y el aumento de la mortalidad.
Son conceptos sumamente esclarecedores para alguien como el autor de este blog saludbydiaz, que sabe poco, pero escuchando a esta persona, tan claramente y respaldado, logró entender algunas conceptos, describiendo en toda su dimensión la importancia de como los conocimientos deben trasladarse de la investigación a la clínica.
Desarrollo:
Comprender la naturaleza de la respuesta inmune que conduce a la recuperación de una enfermedad grave es clave para desarrollar tratamientos efectivos para COVID-19. Los coronavirus, incluido el síndrome respiratorio agudo severo (SARS-CoV) y el síndrome respiratorio del Medio Oriente (MERS), suelen inducir fuertes respuestas inflamatorias y linfopenia asociada
«Las respuestas inmunes contra los patógenos se dividen aproximadamente en tres tipos.
La inmunidad de tipo 1, caracterizada por respuestas que dependen del factor de transcripción T-bet (también conocido como TBX21) y la expresión de interferón-γ (IFNγ), se genera contra patógenos intracelulares como los virus. En la inmunidad de tipo 1, la eliminación de patógenos está mediada por células efectoras que incluyen linfocitos innatos del grupo 1 (ILC1), células asesinas naturales (NK), linfocitos T citotóxicos y T helper 1 (T H1) celdas.
La inmunidad de tipo 2, que se basa en el factor de transcripción GATA 3, que media la defensa contra los helmintos a través de moléculas efectoras como IL-4, IL-5, IL-13 e IgE que trabajan para expulsar estos patógenos a través de la acción concertada de las células epiteliales, mastocitos células, eosinófilos y basófilos.
La inmunidad de tipo 3, que está orquestada por las citocinas IL-17 e IL-22 inducidas por RORγt secretadas por las células ILC3 y T H 17, se monta contra hongos y bacterias extracelulares para provocar el aclaramiento dependiente de neutrófilos.
Su equipo de investigación se centró en el análisis longitudinal de estos tres tipos de respuesta inmune en pacientes con COVID-19 e identificaron correlaciones entre distintos fenotipos inmunes y el curso de la enfermedad.
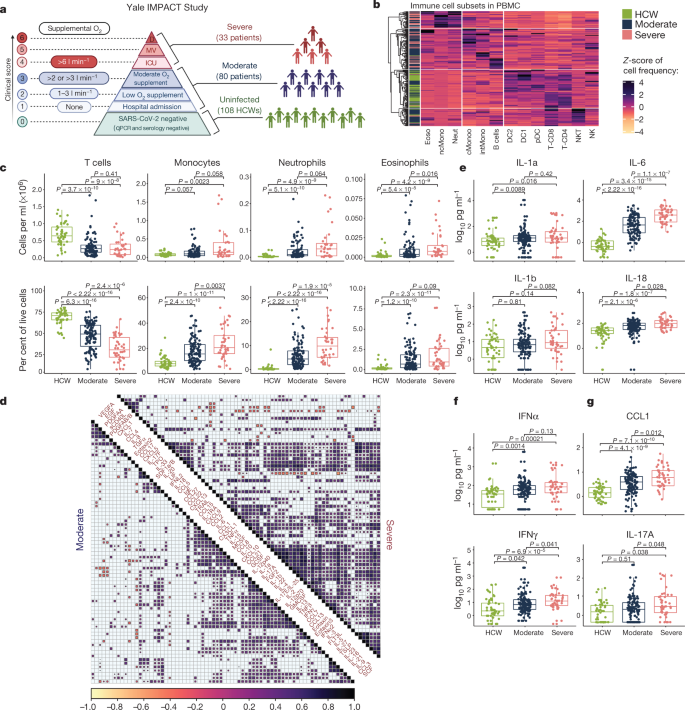
La agrupación no supervisada reveló tres perfiles distintos que influyeron en la evolución y la gravedad de COVID-19. El grupo 1, caracterizado por baja expresión de citocinas proinflamatorias y enriquecimiento en genes de reparación tisular, siguió una trayectoria de enfermedad que se mantuvo moderada y condujo a una eventual recuperación.
Los grupos 2 y 3 se caracterizaron por citocinas proinflamatorias muy elevadas (el grupo 3 es más intenso), peor evolución de la enfermedad y muerte. Por lo tanto, además de las citocinas proinflamatorias relacionadas con CRS conocidas, proponemos estas tres características o perfiles de respuesta inmune que dividen con mayor precisión a los pacientes en distintos cursos de enfermedad COVID-19.
«Nuestro sistema inmunológico consta de dos respuestas, capas o niveles diferentes. La primera línea de defensa es el sistema inmune innato, que actúa en cuestión de minutos de infección para proporcionar una especie de respuesta rápida. Esto no requiere ninguna especificidad; se activa después de cualquier tipo de infección. Pero esta activación innata es importante para activar la segunda capa del sistema inmunitario, que es el sistema inmunitario adaptativo«.
«En el sistema inmunitario adaptativo, los actores clave son las células B y las células T; finalmente adquieren especificidad y memoria, que son la base de las vacunas. Tener esos linfocitos T y B que son específicos de un patógeno en particular y proporcionan una respuesta de memoria a largo plazo es muy importante».
«La longevidad de la respuesta inmune es con lo que contamos para la protección de toda la población. Eso es lo que se supone que deben hacer las vacunas. Si sigue a pacientes infectados por COVID con el tiempo, sus niveles de anticuerpos parecen disminuir hasta cierto punto en un plazo de 2-3 meses. Pero eso no es una causa de alarma porque eso es lo que sucede cuando te infectas o cuando te inmunizas por primera vez. Los niveles de anticuerpos alcanzan su punto máximo en las primeras dos semanas y luego finalmente bajan durante unos meses. Eso está bien porque todavía tienes células de memoria B específicas de ese antígeno, así como una respuesta inmune de células T al antígeno viral. Por lo tanto, la segunda vez que te expones al mismo virus, puedes montar una respuesta inmunitaria rápida, específica y robusta. Es probable que no sientas nada la segunda vez que te infectas. Será una infección bastante leve o asintomática».
«Quiero dejar claro que la disminución de los niveles de anticuerpos por sí solas no es un gran motivo de preocupación. El segundo punto que quiero hacer es que con las vacunas, solemos dar vacunas de refuerzo, que estimulan una inmunidad mucho más robusta y duradera. Esa inmunidad debe mantenerse durante años. Así que de nuevo, tener una respuesta de anticuerpos menguante a la infección natural no debería ser una gran preocupación para seguir adelante con la vacunación».
«Publicó recientemente un artículo en la revista Nature, donde alerta conceptualmente: las diferentes respuestas en personas con enfermedad moderada vs grave, es esta respuesta deficiente de Interferón en algunas personas, y si eso se puede impulsar temprano con algún tipo de IFN».
«El interferon tipo I tipo I IFN tiene que ser entregado en el momento adecuado con la dosis correcta y el tipo correcto. Lo que está saliendo, incluso de nuestro propio estudio, es que un nivel prolongado de IFN de tipo I, especialmente tarde durante la enfermedad, puede estar asociado con un peor resultado de la enfermedad. ocurre más en los hombres que en las mujeres, (que podría explicar algo del mal pronostico en nuestro género, no vinculado a mecanismos hormonales sino al HDLA DR) Por lo tanto, dar a los pacientes con COVID IFN recombinante al final de la enfermedad probablemente no será una buena idea. Mientras que el uso de IFN recombinante como profilaxis contra la infección, o si puede atrapar a los pacientes muy temprano durante la infección y dar suficiente IFN para cerrar la replicación viral, esas estrategias son prometedoras. Estoy esperando a ver qué pasa en los ensayos clínicos. Pero creo que el momento temprano y dar la dosis suficiente para bloquear la replicación del virus va a ser clave en el futuro».
«Odio añadir a este desconcierto, (dice sin solemnidad) pero la típica tormenta de citoquinas que se ha reportado incluye IL-1, IL-6, factor de necrosis tumoral, este tipo de citoquinas innatas agudas. Pero en nuestro informe reciente,también encontramos citoquinas que pertenecen a tipos completamente diferentes de respuestas inmunitarias que también se producen, como las que se dedican a la respuesta fúngica o a la respuesta de helmintos: las respuestas inmunitarias de tipo III y tipo II. Así que en casos graves, el sistema inmunitario se ve confundido y desorientado, generando todo tipo de citoquinas que también están causando algún tipo de tormenta. Creo que la enfermedad de COVID puede comenzar con la típica tormenta de citoquinas, pero luego extenderse a diferentes tipos de tornados y huracanes y todo tipo de respuestas inmunitarias mal dirigidas».
Ella tiene tres hipótesis para explicarlo, para explicar el «Long Covid» pero también podría ser una combinación de estas.
La primera hipótesis es que un reservorio de virus se esconde en algún lugar que se está activando y reactivando periódicamente para causar este tipo de respuestas. Los hisopos nasofaríngeos que actualmente usamos para detectar el virus son incapaces de recoger ese tipo de reservorios.
La segunda hipótesis está relacionada con esto. Tal vez no son los reservorios de virus infecciosos, sino los trozos de ARN viral o proteína que se están reteniendo en algún lugar del cuerpo que están activando una respuesta inmune contra el virus y causando estos síntomas cambiantes y prolongados.
La tercera hipótesis es que la infección genera una enfermedad autoinmune. Tal vez el virus está imitando los antígenos o la infección por el virus, siendo tan inflamatorio en este caso, y está provocando células automáticas T y B. Estamos tratando de entender cuál de estas posibilidades es verdadera. Pero tal vez todas estas cosas están sucediendo al mismo tiempo.
Algo relacionado es el síndrome inflamatorio multisistésistema en niños (MIS-C). Obviamente es una variante de Kawasaki, pero es diferente con respecto a los niños algo mayores, tal vez más corazón y otra afectación de órganos. Y eso parece ser una historia inflamatoria, de tipo autoinmune.
«Para entender si la autoinmunidad está involucrada, necesitamos identificar autoantígenos. Sé que muchos grupos están trabajando en ello, pero actualmente no sabemos realmente la relación entre la exposición COVID y el desarrollo de autoanticuerpos o incluso células T autoreactivas que pueden causar este tipo de enfermedades inflamatorias. Así que la identificación del antígeno culpable va a ser clave».
Dice la investigadora «Estamos viendo todo tipo de elementos de respuesta inmune, diferentes tipos de células, diferentes citoquinas, y su relación con la protección contra este virus, y también la patología que resulta de la activación inmune. En ese primer artículo, pudimos examinar el papel de las Interferón de tipo I, volviendo a la pregunta, y mostramos que, al menos en el modelo de ratón, el tipo I IFN parece ser incompetente para bloquear la replicación de virus. Si nos fijamos en el título viral de los animales que son de tipo salvaje o knocaut del receptor IFN, los títulos no son muy diferentes en diferentes días de infección. Lo que es diferente es la patología que vemos en la línea. El IFN tipo I induce una gran cantidad de quimioquinas que atraen a los leucocitos al pulmón. Desafortunadamente, está alimentando el fuego reclutando estos leucocitos en el pulmón, y al mismo tiempo, no siendo muy competente para bloquear la replicación del virus. Atrae células inflamatorias sin evitar su replicación».
«Este tipo de imita lo que encontramos en pacientes, que fue esta respuesta IFN de tipo I a largo plazo y exagerada que se asoció con la mortalidad y la duración de la estancia hospitalaria. En el animal, estamos viendo lo mismo: el IFN endógeno no es muy competente para bloquear la replicación del virus y en su lugar está dando lugar a efectos patológicos. Esta es la primera visión que podemos ver en paralelo, desde humanos hasta ratón y ratón de vuelta a humanos. Ahora estamos viendo otros tipos de respuestas inmunitarias y si también están contribuyendo a la patología vs protección».
¿Cree que esto es un problema con el nivel de IFN o es un defecto cualitativo en la capacidad de IFN para manejar este virus en particular?
Iwasaki: Probablemente sea una mezcla. Probablemente no estamos recibiendo una respuesta robusta inducida por IFN porque SARS-CoV-2 codifica numerosos mecanismos de evasión para bloquear la inducción de IFN e incluso la señalización del receptor IFN en conjunto. Es por eso que cuando eliminamos el receptor IFN del huésped, no vemos mucha diferencia en la bioreplicación. Habla de la capacidad de este virus para evadir y tipo de suprimir la respuesta IFN. Es por eso que tener un tratamiento recombinante de IFN temprano podría tener sentido.
Una de las cosas que ha defendido es que no estamos prestando suficiente atención a la inmunidad a la mucosa, la inmunoglobulina A (IgA). Casi todos estos 200 programas de vacunas están trabajando en inyecciones de proteína de pico o algún componente del virus para proporcionar el anticuerpo y la respuesta de las células T. Pero hay otro camino, que sería llegar a la inmunidad de la mucosa. Tal vez podrías decirnos más sobre la respuesta de IgA y por qué crees que eso no se le está dando suficiente prioridad.
Iwasaki: Debido a la naturaleza de esta pandemia, la gente está tratando de desarrollar una vacuna lo antes posible, lo cual es importante para nosotros volver a la sociedad regular. Así que creo que las primeras generaciones de vacunas serán las que provocan el anticuerpo neutralizante más robusto de la circulación. Eso tiene una gran importancia para prevenir una mayor propagación de este virus. Pero dado un poco de tiempo y más esfuerzo, las personas también están empezando a mirar las vacunas mucosas y potencialmente administrar el mismo tipo de vacuna a través de la nariz en lugar de en el músculo. Cuando esas vacunas se prueban una al lado de la otra, creo que veremos una diferencia en proporcionar una inmunidad esterilizante en la mucosa vs inhibir la enfermedad después de la exposición. No me desanima el hecho de que estas compañías de vacunas estén desarrollando una vacunación sistémica. Pero en el futuro, creo que deberíamos estar buscando más en las vacunas que generen inmunidad mucosas de IG A secretora.
Uno de los temas controvertidos en este momento es lo que se ha llamado inmunidad efectiva en el rebaño, una inmunidad natural que se está debatiendo. La mayoría de los expertos están de acuerdo en que usted necesita conseguir 60% u 80% de las personas para ser inmune para establecer la inmunidad del rebaño. Pero recientemente hemos visto casos en los Estados Unidos, particularmente en estados que fueron duramente golpeados, como Texas, Arizona y Florida, donde, por alguna razón peculiar, parece que sus números de infección están disminuyendo, y no sólo porque hay menos pruebas, que es otro tema confuso. Eso ha llevado a algunas personas teorizando que tal vez este 20% de las personas que están infectadas está proporcionando una menor cantidad de propagación. ¿Qué tiene de entender esto? ¿Es una explicación para la reducción de los casos?
«Es un poco peligroso depender de la inmunidad del rebaño en este punto para abrir la sociedad porque la inmunidad del rebaño requiere una proporción significativa de la población para ser inmune al virus. Incluso si hay una comunidad en la que el 20% de la gente tiene inmunidad, no sabemos cuánto dura esto porque la adquirieron a través de una infección natural. Simplemente no sabemos lo suficiente sobre el nivel protector de anticuerpos y células T en personas que se recuperan de esta infección para saber cuánto tiempo durará una inmunidad protectora de este tipo. Además, cada individuo puede ser ligeramente diferente. Creo que es prematuro y peligroso depender de esas cifras sin una vacuna que se pueda distribuir por toda la población».
«Vimos que una humedad relativa del 40%-60% ayudó al animal a ser capaz de eliminar el virus del tracto respiratorio a través del movimiento mucociliar. Mientras que si mantienes a los ratones en un 20% de humedad, que encontrarás en interiores durante los meses de invierno, esos animales lo hicieron mal porque no fueron capaces de eliminar el virus. Así que hay un mecanismo natural para eliminar el virus, que podemos aprovechar, manteniendo la humedad relativa en ciertos niveles».
“Hemos estado examinando activamente las diferencias de sexo en la inmunidad a COVID-19. Hasta ahora, hemos descubierto que los pacientes varones que desarrollan COVID grave tienden a tener una activación muy baja de las células T, mientras que las pacientes femeninas que desarrollan COVID grave tienen citoquinas inmunitarias innatas elevadas. Por lo tanto, parece haber una manera diferente en que las mujeres y los hombres responden al virus. La falta de inmunidad de células T en los hombres es interesante, porque cuando nos fijamos en la edad en el eje X y la activación de células T en el eje Y, vemos una disminución dependiente de la edad en la activación de células T en los hombres, pero no en las mujeres. Así que esto puede tener algo que ver con por qué hay una enfermedad más grave en los hombres que están infectados”.
Estamos frente a opciones múltiples, a un gran ejemplo de la complejidad, es mucho lo que falta por descifrar y lo más efectivo es por un lado modificar los comportamientos sociales, identificar los casos, evitar los transmisores asintomáticos, y realizar un plan de vacunación en cuanto este lista la vacuna.
Este blog es realmente un paseo a través de toda la información que necesitaba sobre este este tema tan complejo y no sabía a quién preguntar .
Me gustaMe gusta
Gracias es un gran estímulo para mi.
Me gustaMe gusta