- David B. Beck, Ivona Aksentijevick
Desde Abril que empezamos a ver casos de covid, en Argentina, nos preguntamos porque algunos pacientes desarrollaban formas más graves. No tenemos explicación cierta por ello vuelco este trabajo en el blog. Estos trabajos involucran más a las modificaciones genómicas del virus, como factores preponderantes. Se abre un gran camino de investigación, para ver quienes desarrollan formas más graves.
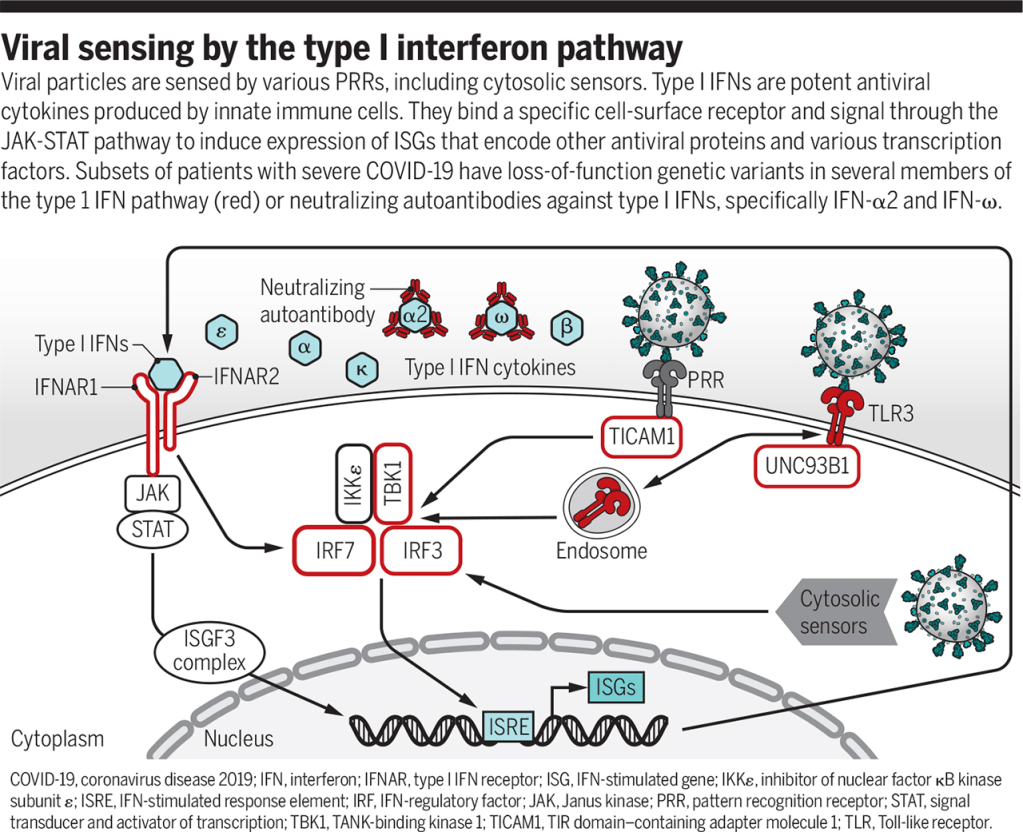
Detección viral por la vía de interferón tipo I
Las partículas virales son detectadas por varios PRR, incluyendo sensores citosólicos. Las IFN de tipo I son potentes citoquinas antivirales producidas por células inmunitarias innatas. Unen un receptor específico de la superficie celular y señalan a través de la vía JAK-STAT para inducir la expresión de ISG que codifican otras proteínas antivirales y varios factores de transcripción. Los subconjuntos de pacientes con COVID-19 grave tienen variantes genéticas de pérdida de función en varios miembros de la vía IFN tipo 1 (rojo) o autoanticuerpos neutralizantes contra IFN de tipo I, específicamente IFN-2 y IFN-o.
La pandemia de la enfermedad del coronavirus 2019 (COVID-19) ha dado lugar a cambios sin precedentes en todos los aspectos de nuestras vidas y ha puesto la investigación biomédica a la vanguardia. Una de las muchas preguntas apremiantes que rodean las infecciones por coronavirus 2 (SARS-CoV-2) de síndrome respiratorio agudo grave es la identificación de los determinantes del espectro clínico, desde personas con enfermedad asintomática hasta pacientes con COVID-19 grave. Hasta el 40% de las infecciones pueden ser asintomáticas, lo que sugiere que una gran proporción de personas pueden estar protegidas de enfermedades. En el otro extremo del espectro se encuentra la enfermedad grave, con una tasa de mortalidad estimada global cercana al 1%. En las páginas 422 y 424 de este número, Zhang et al. y Bastard et al, respectivamente, informan de análisis de >1600 pacientes infectados con SARS-CoV-2 de >15 países para identificar factores endógenos que determinan la susceptibilidad a COVID-19 grave.
Muchos estudios se han centrado en caracterizar la heterogeneidad de COVID-19 en términos demográficos, con evidencia clara de mayor mortalidad en hombres y personas mayores. Recientemente se ha reconocido que el sistema inmunitario adaptativo, incluidos los células B y T, desempeña un papel fundamental en el suministro de inmunidad preexistente al SARS-CoV-2 (5–7). Estos estudios han puesto de relieve mecanismos que protegen contra los síntomas graves pero no han revelado factores que predisponen a la mortalidad. En consecuencia, las respuestas inmunitarias adquiridas a infecciones anteriores pueden explicar un gran porcentaje de la variabilidad en la presentación de la enfermedad, aunque persisten preguntas sobre determinantes adicionales de la enfermedad, como las comorbilidades preexistentes. Los factores de riesgo genéticos del huésped también han surgido como una explicación potencial para la heterogeneidad clínica y, además, ofrecen el potencial de comprender las vías moleculares para la intervención terapéutica personalizada.
Los estudios a pequeña escala han implicado la vía de interferón tipo I (IFN) como protección contra SARS-CoV-2 (8, 9). La vía IFN tipo I desempeña un papel crucial en la mediación de las respuestas inmunitarias innatas a las infecciones virales. Esta familia de citoquinas se compone de 13 subtipos IFN-α, IFN-β, IFN-o, IFN-, y IFN-ε, que todos señalan a través del receptor IFN I heterodimérico, compuesto por IFN-α/β receptor 1 (IFNAR1) y IFNAR2 (ver la figura). En las células huésped, las IFN de tipo I se expresan en cantidades bajas, preparadas para combatir las infecciones. Tras la infección, son rápidamente producidas por células inmunitarias, como macrófagos y células dendríticas, para limitar la propagación de patógenos. Además, los IFN de tipo I inducen la expresión de varios cientos de genes estimulados por interferón que pueden limitar aún más la replicación de patógenos a través de diversos mecanismos. Sin embargo, esta respuesta inmune típicamente protectora puede, cuando está sobreactivada, conducir a enfermedades autoinmunes. Por el contrario, las variantes de pérdida de función en genes que codifican miembros de la vía IFN tipo I conducen a inmunodeficiencias graves caracterizadas por infecciones virales potencialmente mortales. Recientemente, múltiples estudios demostraron que las respuestas DE IFN de tipo 1 deterioradas pueden ser un sello distintivo de COVID-19 grave (10–12), pero por qué esta vía fue suprimida seguía sin estar clara.
Zhang y otros informan de un gran esfuerzo de secuenciación genética para definir los factores de riesgo del huésped a la infección por SARS-CoV-2, analizando secuencias de exoma o genoma de 659 pacientes con COVID-19 grave para variantes patógenas raras que podrían estar asociadas con enfermedades potencialmente mortales. Los autores se centraron en la vía IFN tipo I y analizaron 13 genes candidatos que previamente se han relacionado con la susceptibilidad a otras infecciones virales. Las variantes norias que pueden afectar la función génica se identificaron en el 3,5% (23/659) de los casos. Los defectos en la expresión del gen IFN de tipo I y los niveles de proteínas se recapitularon en células de pacientes que albergaban estas variantes, lo que demuestra una disminución recurrente de la actividad de esta vía en la enfermedad grave. Las cargas virales de SARS-CoV-2 fueron mayores en las células inmunitarias de los pacientes que en las células de donantes sanos (que eran infecciones negativas y seronegativas para sarS-CoV-2), lo que demuestra una incapacidad para eliminar adecuadamente el virus. Juntos, estos datos implican la importancia de la señalización IFN de tipo I en defensa contra la infección POR SARS-CoV-2 y sugieren que las variantes nocirios heredadas explican un subconjunto de COVID-19 grave.
Identificado autoanticuerpos neutralizantes como otra causa potencial de COVID-19 grave. Los autoanticuerpos reconocen y, por lo tanto, pueden inhibir las proteínas huésped; son un sello distintivo de muchas enfermedades autoinmunes y se cree que contribuyen a la fisiopatología autoinmune. Los autoanticuerpos neutralizantes frente a los IFN de tipo I, en su mayoría IFN-2 y IFN-o, se encontraron en hasta el 13,7% (135/987) de los pacientes con COVID-19 potencialmente mortal y se demostró que neutralizan la activación de la vía in vitro. Por el contrario, estos autoanticuerpos no estaban presentes en 663 pacientes con COVID-19 asintomático o leve y sólo se encontraron en individuos sanos del 0,33% (4/1227) no expuestos a SARS-CoV-2. La presencia de autoanticuerpos neutralizantes correlacionados con bajas concentraciones séricas de IFN-α. También se detectaron autoanticuerpos contra ifNs de tipo I en muestras de sangre de algunos pacientes obtenidos antes de la infección por SARS-CoV-2, lo que indica que su producción no fue provocada por el virus en esos pacientes. En particular, la inactivación de los autoanticuerpos se identificó principalmente en los hombres (94%) y puede ser una causa de las mortalidades por enfermedades específicas masculinas más altas.
Al analizar pacientes con COVID-19 grave, estos dos estudios proporcionan evidencia de que los IFN de tipo I son protectores contra COVID-19 y que limitar esta respuesta a través de mutaciones genéticas o autoanticuerpos conduce a enfermedades graves. Los autoanticuerpos contra otras citoquinas proinflamatorias, como el IFN tipo II (IFN-γ), la interleucina-6 (IL-6), el IL-17A y el IL-17F, se han notificado en individuos sanos, pacientes con enfermedades autoinmunes y otras infecciones oportunistas, aunque la función de estos autocuentos no siempre se entiende(13). El estudio de los mecanismos de inmunodeficiencia adquirida, tal vez relacionados con el sexo y el envejecimiento, podría ayudar a reducir la morbilidad y mortalidad de las enfermedades infecciosas.
Las concentraciones de IFN de tipo I están estrechamente reguladas, con varios trastornos autoinflamatorios e inmunodefirios monogénicos raros causados por una producción de interferón demasiado o muy poco, respectivamente. Las personas sanas pueden tener respuestas IFN de tipo I deterioradas debido a variantes heredadas de pérdida de función en genes que codifican componentes de la cascada de señalización IFN de tipo I, pero permanecen clínicamente silenciosas hasta que encuentran virus u otros microbios en particular (8). Este puede ser el caso en pacientes graves con COVID-19 que no tienen antecedentes de inmunodeficiencia clínica.
Colectivamente, este trabajo tiene importantes implicaciones terapéuticas. Se están estudiando β IFN inhaladas y terapias antivirales sistémicas para COVID-19 en ensayos clínicos (14). Los estudios de Zhang et al. y Bastard et al. ofrecen una vía potencial para identificar a las personas que están en riesgo de desarrollar una infección por SARS-CoV-2 potencial, principalmente hombres mayores, mediante un cribado presintomático de sus muestras de sangre para autoanticuerpos de tipo I IFN. La identificación de estos pacientes también puede ser importante para evitar el uso terapéutico potencial de su plasma convaleciente (que contendrá los autoanticuerpos neutralizantes de citoquinas) en los ensayos clínicos en curso. Además, el tratamiento recombinante de IFN-β puede no beneficiar a los pacientes con autoanticuerpos neutralizantes, mientras que puede funcionar bien para los pacientes que llevan variantes de pérdida de función en genes IFN de tipo I, distintos de IFNAR1 o IFNAR2. En pacientes con autoanticuerpos, el tratamiento con IFN-β puede ser beneficioso porque neutralizar los autoanticuerpos contra esta citoquinas parece ser menos frecuente (4, 14). Los resultados de estos estudios han allanado el camino para la medicina de precisión y estrategias de tratamiento personalizadas para COVID-19.
Lo que sigue siendo desconocido son las contribuciones de la variación genética fuera de la vía IFN tipo I para la defensa contra la infección SARS-CoV-2. Además, aunque Zhang y otros se centraron en la variación rara de la línea germinal, es necesario investigar las funciones de los polimorfismos comunes de un solo nucleótido (SNP) y las mutaciones somáticas adquiridas en las células inmunitarias, que se acumulan con la edad. Otros estudios genéticos integrales también podrían ayudar a proporcionar información sobre la posible contribución de la variación notoria en el síndrome inflamatorio multisistémico asociado al SARS-CoV-2 grave en niños (15). Aunque los estudios de Zhang et al. y Bastard et al. iluminan la importancia de las vías responsables de eliminar las infecciones, también es posible que las variantes proinflamatorias puedan reducir o mejorar la gravedad de la enfermedad. Por qué algunos pacientes que llevan variantes patógenas en genes inmunes innatos, como los genes relacionados con ifN, permanecen asintomáticos hasta que su exposición a un patógeno específico probablemente se explica por la presencia de otros alelos modificadores genéticos o factores epigenéticos. Los estudios genómicos imparciales pueden responder a algunas de estas preguntas; sin embargo, es necesario ampliarlas a poblaciones más grandes y diversas (más allá de la ascendencia mayoritariamente europea) para abordar significativamente la susceptibilidad al SARS-CoV-2 y otras infecciones virales potencialmente pandémicas. En última instancia, a través de esfuerzos de colaboración, la investigación biomédica debe y ayudará a combatir la propagación del virus mediante la identificación de personas en riesgo con pruebas diagnósticas rápidas y la facilitación de nuevas terapias dirigidas.