Konstantin Chumakov, Michael S. Avidan, Christine S. Benn, Stefano M. Bertozzi, Mount Sinai New York
Justificación conceptual de este posteo:
La inmunidad innata es fundamental para la capacidad de defensa del huésped de mamíferos para combatir las infecciones. Las respuestas inmunes innatas, desencadenadas por una familia de receptores de reconocimiento de patrones, inducen interferones y otras citoquinas y activan células inmunes mieloides y linfoides para proporcionar protección contra una amplia gama de patógenos. La evidencia epidemiológica y biológica sugiere que las vacunas atenuadas vivas (LAV) dirigidas a la tuberculosis, el sarampión y la poliomielitis inducen inmunidad innata protectora mediante una forma recién descrita de memoria inmunológica llamado «inmunidad entrenada». Un LAV diseñado para inducir inmunidad adaptativa dirigida a un patógeno en particular también puede inducir inmunidad innata que mitiga otras enfermedades infecciosas, incluyendo COVID-19, así como futuras amenazas pandémicas.
Desarrollo:


Esta figura ilustra cómo un sistema inmunitario innato saludable protege a la mayoría de las personas dentro de la población contra las infecciones. Con un sistema inmunitario innato ya robusto o entrenado, la abrumadora mayoría de las personas infectadas con un nuevo patógeno, como el SRAS-CoV-2, son capaces de erradicar la infección a tiempo durante la fase asintomática o levemente sintomática de la infección. Sin exposición previa o vacunación (por ejemplo, con una vacuna de ARN mensajero), la inmunidad adaptativa tarda días o semanas en entrar en vigor y a menudo se suprime en casos graves, contribuyendo a una respuesta hiperinflamatoria autoperpetuante y perjudicial. El sistema inmunitario innato a menudo pierde potencia con la edad, ciertas comorbilidades, inmunosupresión y con susceptibilidad genética.
El poder de la inmunidad innata reside en su amplia y inespecífica activación, y la capacidad de inhibir múltiples patógenos. Se basa en sensores llamados receptores de reconocimiento de patrones (PRR) que reconocen patrones moleculares asociados a patógenos (PAMPs) y activan múltiples vías que hacen que un huésped sea resistente a la infección (5).
En el caso de virus de ARN como SARS-CoV-2, el disparador de reconocimiento se encuentra dentro de la secuencia de nucleótidos del ARN del virus. La respuesta es inmediata y comienza con la estimulación de receptores celulares clave del huésped, como el receptor similar a Toll (TLR)3 y TLR7, lo que conduce a la activación de células asesinas naturales (NK), monocitos y expresión de genes de interferón (IFN). A su vez, ifn sirve como mediador mediante la unión de receptores IFN en la superficie de la célula huésped y el lanzamiento de la expresión de genes estimulados por IFN (ISG) (6). Las proteínas codificadas por estos genes inducen el llamado estado antiviral al hacer que las células no puedan soportar la replicación del virus.
Tabla 1.
Comparación de las características de las dos formas de respuesta inmune
| Innata | Adaptable |
| Mediado por células mieloides y linfoides (NK, T) | Involucra células linfoides (linfocitos B y T) |
| Basado en la fagocitosis directa y la matanza de microbios, liberación de citoquinas y quimioquinas, matanza mediada por NK de células infectadas por virus | Mecanicistamente involucran anticuerpos y células T específicas |
| Funciona casi inmediatamente | Toma de 1 a 2 wk para desarrollarse después de la exposición a un patógeno o vacuna |
| Presente en todos los organismos multicelulares | El sistema está presente en vertebrados pero no en invertebrados o plantas |
| Ampliamente específico, puede ser eficaz contra grupos de microorganismos | Específico para un microorganismo o incluso cepa |
Por el contrario, la característica definitoria de la respuesta inmune adaptativa es su singular especificidad patógena y memoria inmunológica que permite al cuerpo producir anticuerpos y activar células T más rápido si es reinfectado por ese patógeno en particular. La inducción de inmunidad adaptativa que puede durar toda la vida (por ejemplo, sarampión, poliomielitis) es el principio subyacente detrás de las vacunas profilácticas. Sin embargo, la muy alta especificidad de la inmunidad adaptativa es el «talón de Aquiles» de las vacunas, porque aunque puede existir cierto grado de reactividad cruzada(8), protegen predominantemente contra un patógeno, y a menudo contra una sola cepa específica. Por esta razón, las vacunas que dependen de anticuerpos protectores y células T pueden perder eficacia si surgen mutaciones en los epítopos protectores virales. Si esto sucede, se tendrán que desarrollar nuevas vacunas específicas de patógenos desde cero (como es el caso de las vacunas antigripales). Por el contrario, los virus no pueden desarrollar fácilmente resistencia a la inmunidad innata que seguirá garantizando una amplia protección contra los patógenos, incluso si se someten a deriva antigénica.
La durabilidad y la memoria del sistema de inmunidad adaptativa a menudo se citan como su superioridad sobre las respuestas inmunes innatas. Sin embargo, los resultados recientes resumidos en este informe mostrarán que estas características distintivas entre estímulos adaptativos e innatos pueden no estar tan ampliamente separadas como se pensaba. De hecho, algunas vacunas (por ejemplo, la gripe y el VIH) inducen una respuesta inmune adaptativa que dura sólo meses(9, 10)y la activación de la inmunidad innata a largo plazo también puede durar tanto tiempo. La inmunidad innata también se sabe ahora para adaptarse a los insultos anteriores, de hecho para desarrollar una memoria inmune innata de facto, que facilita respuestas más fuertes a los posteriores ataques patógenos de naturaleza heterogénea (11). Esta memoria inmune innata, también llamada «inmunidad innata entrenada», está mediada por la reprogramación epigenética, transcripcional y funcional de las células inmunes innatas y sus progenitores de médula ósea. La inmunidad innata entrenada se describirá a continuación con más detalle. En este artículo, proponemos que durante una pandemia (o epidemia), la ciencia médica podría aprovechar rápidamente el poder de la inmunidad innata para inducir protección parcial contra nuevas (como el SRAS-CoV-2) o reemerging amenazas patógenas y sugerir que esto podría lograrse mediante la reutilización de algunas vacunas establecidas atennuadas vivas (LAV), que son poderosos inductores de inmunidad innata.
La inmunidad innata es clave para controlar la pandemia SARS-CoV-2
Varias observaciones dejan clara la importancia central de la inmunidad innata en el control del SRAS-CoV-2. En primer lugar, los coronavirus humanos, incluido el SRAS, el síndrome respiratorio de Oriente Medio (MERS) y el SARS-CoV-2, han desarrollado mecanismos especiales para suprimir las respuestas inmunitarias. Los virus dedican parte de su información genética al código de proteínas que se dirigen específicamente a nuestros mecanismos inmunes innatos, a saber, las vías de respuesta ifn, mediante la inhibición de la señalización TLR3/7 (12⇓⇓–15). En segundo lugar, la expresión de genes humanos que favorecen las respuestas inmunes innatas se correlaciona con una mejor respuesta clínica. De hecho, en un estudio estos fueron los únicos genes de respuesta inmune correlacionados con un pronóstico favorable (16). En tercer lugar, mutaciones específicas que reducen la producción o función de la IFN se correlacionan con la morbilidad y mortalidad graves (17). En línea con otros estudios que muestran una correlación entre la expresión inmune innata y un mejor pronóstico son los hallazgos que correlacionan la morbilidad grave y la mortalidad con mutaciones que conducen a la producción o producción defectuosa de IFN tipo I o la producción de autoanticuerpos neutralizantes dirigidos a IFN tipo I (18, 19). En consonancia con esto, el uso terapéutico del TIPO I IFN (IFN-x2b) en la fase viral de COVID-19 redujo la duración del virus detectable en las vías respiratorias y mejoró el pronóstico (20, 21).
Por último, el control de coronavirus por murciélagos se asocia casi exclusivamente con un equilibrio adecuado de las respuestas inmunes innatas entre la resistencia y la tolerancia. Muchas especies de murciélagos pueden albergar coronavirus de forma segura que causan enfermedades en otros mamíferos, incluidos los humanos (22). Los murciélagos muestran un número inusualmente alto de células NK activadas, así como una expresión constitutiva de IFN. Estos estudios también muestran una respuesta inflamatoria menor a estos virus (23). Colectivamente, estos hallazgos presentan argumentos muy sólidos de que la inmunidad innata es fundamental para el control de las enfermedades coronavirus. Al inicio de la pandemia, esto provocó que algunos de nosotros consideráramos las estrategias basadas en la estimulación de la inmunidad innata como complemento a las vacunas específicas de la enfermedad al reducir el período hasta su desarrollo y superar algunas de sus limitaciones (11, 24, 25).
Vacunas específicas: Una herramienta crucial contra el COVID-19, pero se necesita más ayuda
Las vacunas se encuentran entre nuestras intervenciones de salud pública más exitosas(26),lo que nos permite superar muchos contagios mortales y evitar medidas de «plaga» de cierres y distanciamiento social. Estamos centrados en la búsqueda de una vacuna como antídoto contra la carnicería clínica, la devastación social y la crisis económica causada por el SRAS-CoV-2. El rápido desarrollo de varias vacunas altamente eficaces utilizando la nueva tecnología avanzada de ARNm es un logro extraordinario en la batalla contra el COVID-19. Se espera que la vacunación generalizada disminuya significativamente la propagación del SRAS-CoV-2. Sin embargo, el despliegue masivo no puede ocurrir a tiempo para salvar decenas de miles de vidas humanas, decenas de millones de empleos más y evitar el hambre severa que enfrentan varios millones de niños. Quedan muchos obstáculos.
En primer lugar, las vacunas específicas COVID-19 parecen ser altamente protectoras, llegando en algunos casos al 95% de eficacia clínica. Sin embargo, la eficacia se refiere únicamente a la prevención de enfermedades, no a la prevención de infecciones o a la propagación posterior, la verdadera clave para alcanzar la inmunidad de los rebaños. Tomará varios meses llevar a cabo una evaluación posmercado para determinar si las vacunas detienen la transmisión del virus en los adultos más jóvenes, el grupo de edad responsable de la mayor propagación. Como la prevención de la infección requiere un mayor nivel de anticuerpos que la prevención de enfermedades graves, es probable que la eficacia para prevenir la infección sea menor que la eficacia clínica. Aún no se ha establecido la seguridad de vacunas específicas en mujeres embarazadas, un grupo de alto riesgo que representa una proporción significativa de la fuerza de trabajo de atención médica y de ancianos.
Si las vacunas son eficaces para prevenir la transmisión, la obtención de inmunidad de rebaño requerirá que entre el 60 y el 70% de la población se vacune (una estimación que se está revisando al alza) (27).
En segundo lugar, si bien el requisito de almacenamiento a temperaturas muy frías y la necesidad de una cadena ultracold para la vacuna contra el ARNM presentan dificultades(28),un desafío mayor es el nacionalismo vacunal: el acaparamiento de vacunas por parte de los países ricos mientras la propagación continúa en los países más pobres, a solo un viaje en avión. Un desafío aún mayor es producir suficientes vacunas para la población mundial, obstaculizadas por las protecciones de propiedad intelectual que impiden la ampliación de las primeras vacunas exitosas y limitan el acceso a miles de millones de personas.
En tercer lugar, incluso una vez superados estos obstáculos, convertir las vacunas en vacunas utiles, aprobadas y difundidas depende de la confianza. Incluso las mejores soluciones biomédicas requieren tracción social para la captación.
Es probable que la politización de la pandemia, la erosión de la confianza en las autoridades y las vacunas, junto con las preocupaciones sobre la seguridad de las vacunas de reciente desarrollo, limiten la absorción y eviten la creación de inmunidad de la población (29). El uso de LAVS probados en el tiempo podría ayudar a superar este problema.
A diferencia de la inmunidad de por vida a la poliomielitis, el sarampión y la viruela, la inmunidad a los coronavirus parece evanescente, que dura sólo meses a años(30⇓–32). Los casos de reinfección que subrayan la inmunidad natural limitada se notifican cada vez más. Además, la medida en que el virus puede mutar no ha sido debidamente aclarada. Las mutaciones en nuevas cepas variantes, como 501.V2, pueden afectar la eficacia de la vacuna, lo que combinado con un aumento del contagio elevaría los umbrales de inmunidad de los rebaños, lo que dificultaría el alcance. Otras mutaciones pueden tener el potencial de obstaculizar la inmunidad duradera dependiente de anticuerpos (33).
Otro obstáculo importante para eliminar una enfermedad infecciosa se presenta cuando el patógeno tiene reservorios no humanos sustanciales. Algunos otros patógenos infecciosos importantes, como la poliomielitis y el sarampión, no tienen reservorios animales notables, y a pesar de las vacunas muy eficaces no hemos sido capaces de erradicarlos. Por el contrario, el SARS-CoV-2 es capaz de cruzar entre humanos y múltiples especies animales, incluyendo pangolines, murciélagos, tortugas, serpientes, visón, gatos y gorilas (34).
Las vacunas basadas en la inducción de la respuesta adaptativa a la inmunidad son muy importantes. A falta de un tratamiento eficaz o de una cura fiable, la capacidad de las vacunas para prevenir enfermedades graves y la muerte es especialmente vital para los grupos vulnerables, como los ancianos. Sin embargo, estas nuevas vacunas que generan anticuerpos específicos y células T no pueden estar disponibles inmediatamente durante esta o cualquier pandemia futura. Estas advertencias a un futuro dependiente únicamente de vacunas basadas en la inmunidad adaptativa exigen una expansión de nuestro armamento protector actual.
LAVS como potentes inductores de inmunidad innata: evidencia epidemiológica de efectos beneficiosos no específicos de las vacunas
El paradigma predominante en la vaccinología se centra casi exclusivamente en la inmunidad adaptativa basada en anticuerpos específicos de patógenos y células T. Sin embargo, el impacto de la vacuna también se logra a través de una serie de efectos no específicos beneficiosos (NSE). La acumulación de pruebas sugiere que los LAV proporcionan protección no sólo contra el agente infeccioso objetivo, sino también contra una amplia gama de otros patógenos (35).
La primera indicación provino de observaciones hechas hace casi 100 años en París con la vacuna Bacillus Calmette-Guérin (bacillus Calmette-Guérin) contra la tuberculosis(36). Calmette, uno de los inventores de bacillus Calmette-Guérin, señaló una disminución cuatro veces mayor de la mortalidad infantil no causada por la tuberculosis en niños vacunados por bacilos calmette-guérin en comparación con sus pares no vacunados.
En las décadas de 1950 a 1960, los primeros ensayos clínicos de la vacuna oral contra la poliomielitis (OPV) revelaron efectos protectores inespecíficos de la inmunización. Los ensayos clínicos prospectivos multicéntricos de la OPV durante el brote estacional de gripe mostraron que la vacunación con OPV redujo la incidencia de gripe de dos a cuatro veces(33, 34).
Un examen sistemático de las ENSE beneficiosas de los LAV comenzó con el descubrimiento de que una campaña de vacunación contra el sarampión en 1979 en Guinea-Bissau, África Occidental, redujo la mortalidad por todas las causas en casi un 70%, mucho más de lo que podría explicarse mediante la prevención de la infección por sarampión (37). El hallazgo, cuando se confirmó en otros entornos de bajos ingresos, condujo a la formulación de la hipótesis de que la vacuna contra el sarampión tiene EEB, fortaleciendo el sistema inmunitario y proporcionando una mayor protección contra una amplia gama de infecciones (38). Desde entonces, décadas de observaciones clínico-epidemiológicas apoyan el efecto protector beneficioso de los LAV y, en particular, de las vacunas contra el bacilo Calmette-Guérin, la OPV, la pequeña viruela y las vacunas contra el sarampión(35, 39). Por ejemplo, los ensayos aleatorizados mostraron que bacillus Calmette-Guérin(40),la vacuna contra el sarampión vivo(41)y la OPV(42)reducen la mortalidad por todas las causas mucho más de lo previsto por sus efectos solo en la enfermedad objetivo. Estudios históricos de cohortes encontraron la misma NSE beneficiosa de la vacuna contra la viruela (38). La reducción de la mortalidad se debe principalmente a una reducción de la mortalidad debida a infecciones respiratorias (35). Las vacunas contra la tuberculosis y la viruela se han asociado con una mejor supervivencia a largo plazo (38). Curiosamente, la NSE beneficiosa de LAV puede llegar a ser más pronunciada con dosis posteriores (43). Por ejemplo, las campañas de OPV en África Occidental se han asociado con una reducción del 25% en la mortalidad por todas las causas, y cada dosis adicional reduce la mortalidad en un 14% adicional (44).
El Cuadro 2 compara las características de los efectos protectores de los LAV basados en estimular la inmunidad innata y las vacunas específicas de patógenos que inducen respuestas inmunes adaptativas. La dificultad para caracterizar los efectos fuera del objetivo de los lavs, la controversia sobre la necesidad de cambiar los calendarios de inmunización, la preocupación por la fabricación limitada de vacunas sin fines de lucro, así como la contribución potencial a la vacilación de las vacunas han retrasado los ensayos controlados aleatorizados a gran escala muy necesarios y la investigación sobre la NSE de vacunas. Las pruebas emergentes y las publicaciones recientes de datos sólidos apoyan la asociación entre bacillus Calmette-Guérin, mortalidad neonatal y riesgo de paludismo(45⇓–47),y subrayan el imperativo de que la investigación examine y explote este efecto.
Table 2.
Ventajas y desventajas de las vacunas convencionales de respuesta inmune adaptativa frente a las vacunas innatas que estimulan el sistema inmunitario mediante el uso de LAV «antiguos» para la pandemia SARS-CoV-2
En 2014, un examen encargado por la Organización Mundial de la Salud por recomendación del Grupo Asesor Estratégico de Expertos sobre vacunas concluyó que los LAV redujeron la mortalidad infantil en más de lo esperado mediante la prevención específica de las enfermedades objetivo (37). Se observaron los mismos patrones en entornos de altos ingresos: Por ejemplo, en los Estados Unidos, tener una vacuna viva como la vacuna más reciente se asoció con una reducción a la mitad del riesgo de hospitalización por infecciones no detectadas (48). La revisión aconsejó más investigación sobre los efectos heterólogos beneficiosos de los LAV, y en particular si una secuencia diferente de inmunizaciones podría explotar los efectos beneficiosos (48). Estos estudios aún no se han llevado a cabo.
Los estudios en animales proporcionan evidencia adicional de los efectos protectores fuera del objetivo de los LAV. Por ejemplo, la inmunización de ratones con vacuna antigripal H3N2 adaptada en frío los protegió de la enfermedad tras un desafío con el virus respiratorio sincitial (RSV), acompañados de inducción de citoquinas e infiltración de vías respiratorias con leucocitos (49). La inmunización con la vacuna antigripal inactivada como control no indujo un efecto protector contra el VRR. El efecto de la vacuna antigripal atenuada se redujo en TLR3/TLR7− ratones, apoyando otras pruebas de que estas vías están involucradas en la activación de la inmunidad innata. Una vacuna experimental contra la tos ferina hecha de pertusa bordetella atenuada en vivo también previno la inflamación causada por infecciones respiratorias no relacionadas, como la gripe y el RSV en ratones(50),y la reducción de la inflamación no infecciosa, incluida la dermatitis de contacto(51).
Inmunidad innata entrenada: Mecanismos inmunológicos
Se cree que dos mecanismos inmunológicos importantes contribuyen a la NSE beneficiosa de las vacunas vivas: inmunidad celular heterologosa e inmunidad innata entrenada. En las décadas de 1960 y 1970, los estudios seminales de Mackaness et al. (52, 53) demostraron la protección inducida por la vacunación bacillus Calmette-Guérin contra infecciones con Listeria monocytogenes o Salmonella typhimurium. Más adelante se ha notificado una protección heterologosa similar contra infecciones que dependen de la activación de células T en estudios adicionales (para su revisión, ver refs. 54, 55). Curiosamente, algunos de estos estudios han demostrado que la interacción de las células T con macrófagos es crucial para que esta protección sea eficaz, lo que plantea la posibilidad de adaptación a largo plazo y aumento de la actividad antimicrobiana en células inmunes innatas (56).
La acumulación de evidencia reciente sugiere que algunos tipos de vacunas, especialmente los LAV que imitan estrechamente la infección natural, inducen la mejora a largo plazo de la función antimicrobiana de las células inmunes innatas que contribuye a la protección contra la reinfección posterior. El término «inmunidad entrenada» se refiere a esta reprogramación funcional de células inmunes innatas, como mieloides y células NK (57).
La inducción de inmunidad entrenada por la LAV está mediada por una compleja, finamente sintonizada, interacción entre señales inmunológicas, metabolismo celular y reprogramación epigenética (58). El metabolismo celular se vuelve a conectar para aumentar la glucólisis (59), glutaminolisis (60), y síntesis de colesterol (61) para proporcionar la energía y bloques de construcción para las células, y para la modulación de los procesos epigenéticos. Al mismo tiempo, la arquitectura de cromatina se cambia en los genes de codificación loci importantes para la defensa del huésped, con cromatina más abierta caracterizada por las marcas de histona H3K4me1, H3K4me3 y H3K27Ac (62). La metilación y acetilación de histonas después de la vacunación con un LAV «marcan» el gen necesario para la defensa del huésped: al inferse con un patógeno, estos genes se transcribirán más rápido y más fuerte, mejorando la respuesta inmune y la supervivencia del huésped. Este proceso se puede comparar con poner un marcador en un libro: si es necesario, el libro se puede abrir más fácilmente en el lugar correcto (Fig. 2).
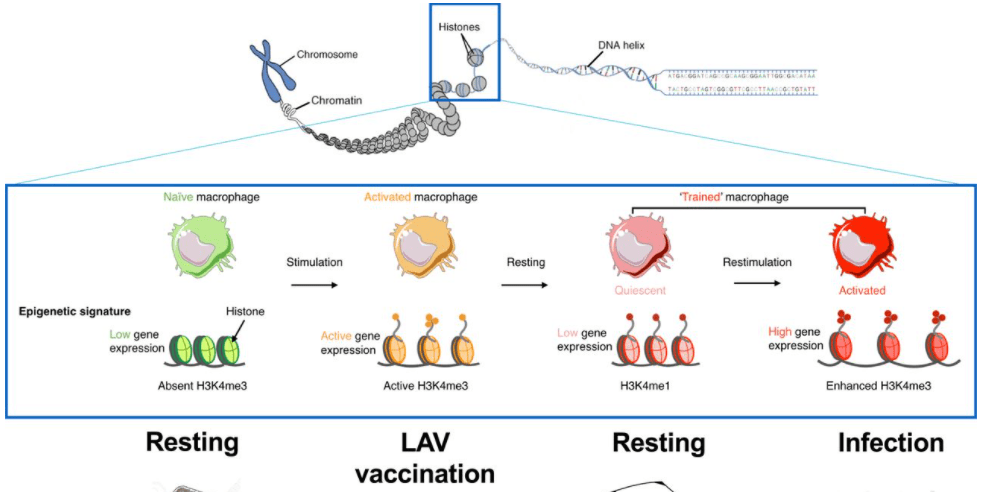
El mecanismo epigenético inducido por los LAV en las células inmunes innatas y sus precursores: la metilación y acetilación de histonas después de la vacunación «marcan» el gen necesario para la defensa del huésped, lo que conduce a cambios a largo plazo en la arquitectura de cromatina que conducen a una expresión más fuerte sobre los estímulos posteriores.
Se ha informado de la inducción de inmunidad entrenada para mediar al menos en parte los efectos biológicos no específicos de la vacunación Bacillus Calmette-Guérin a través de un mecanismo dependiente de LAD2 (63). Es importante destacar que también se ha demostrado que la reprogramación funcional a largo plazo de las respuestas inmunes innatas está mediada por procesos transcripcionales y epigenéticos en los progenitores de células mieloides en la médula ósea, explicando el efecto a largo plazo del bacilo Calmette-Guérin en las células mieloides circulantes (64, 65). El efecto de refuerzo de bacillus Calmette–Guérin en la función celular se extiende más allá de las células mieloides a otras poblaciones innatas de células inmunes, como las células NK (66). En conjunto, la evidencia acumulada durante la última década apoya el concepto de que la inmunidad innata entrenada es responsable de una gran parte de los efectos protectores heterólogos de los LAV. Dado que la mayoría de estas pruebas han sido proporcionadas por estudios sobre la vacunación Bacillus Calmette-Guérin, se necesitan urgentemente estudios para descifrar la inducción de inmunidad entrenada por sarampión, paperas-rubéola (MMR), OPV y otros LAV. En el caso de MMR, será importante evaluar la NSE de cada cepa atenuada por separado, ya que puede llegar a ser importante tener varios LAV disponibles para la administración en serie.
Cabe destacar que recientemente se ha demostrado que la cepa Ty21 a de Salmonella Typhi, atenuada en vivo, induce entrenamiento a largo plazo de inmunidad innata (67).
Evidencia epidemiológica de los efectos de los LAVS contra covid-19
La pandemia COVID-19 impulsó la investigación sobre los efectos protectores de los LAV contra covid-19. Una misión a China a finales de enero llevó al Director General de la Organización Mundial de la Salud a considerar si bacillus Calmette-Guérin podría proteger a los trabajadores sanitarios en primera línea del brote. A mediados de febrero, la primera conferencia mundial sobre la EEB de vacunas llevó a muchos investigadores presentes en la conferencia a iniciar ensayos clínicos de la vacuna bacillus Calmette-Guérin contra covid-19(25, 68). Actualmente hay ensayos ∼20 bacillus Calmette-Guérin que proporcionarán estimaciones sobre el efecto del bacilo Calmette-Guérin contra infecciones, incluyendo COVID-19, en los trabajadores de la salud y los ancianos. Estudios similares están en curso con respecto a OPV (69) y MMR (70).
Tabla 3.
LAVS existentes y sus características
| criterios | Sarampión/MMR | OPV | Bacillus Calmette–Guérin |
| ruta | subcutáneo | oral | Intradérmica |
| Vacunas combinadas | Vacuna MMR y MMR combinadas con la vacuna contra la varicela | bOPV (OPV1 y OPV3) | solo |
| Contraindicaciones | Inmunosupresión, embarazo, VIH con células T CD4 cuenta <15% | Inmunosupresión, VIH, embarazo | Inmunosupresión, tuberculosis activa, embarazo |
| Eventos adversos | Enfermedad sérica como artralgias. Convulsiones febriles. Reacciones alérgicas (anafilácticas) raras pero graves. | Vacuna asociada a la poliomielitis paralítica (VAPP) (1/millones) sólo en niños no vacunados | Enfermedad diseminada en inmunosupresor (CGD, defectos gamma IFN) |
| Complicación rara | SSPE (0,7/millones) | VAPP (1/millones) sólo en niños no vacunados | Bacillus Calmette–Osteitis Guérin |
| Estimulación de la inmunidad innata | Sí | Sí | Sí |
Un estudio observacional reciente de los trabajadores de la salud en Los Ángeles mostró que la seroprevalencia de los IgG anti-SARS-CoV-2, así como la incidencia de síntomas covid-19 autoinformes, se redujeron significativamente entre los trabajadores de la salud con antecedentes de vacunación bacillus Calmette-Guérin en comparación con aquellos sin vacunación bacillus Calmette-Guérin. Ningún efecto se asoció con antecedentes de vacunas inactivadas, como el meningococo, el neumococo o la vacunación antigripal (71).
Varios estudios observacionales han examinado la asociación entre la reciente vacunación contra el LAV y el riesgo de COVID-19. Un estudio holandés mostró menos síntomas de COVID en cohortes vacunadas por bacillus Calmette-Guérin en comparación con cohortes no vacunadas (72). Un estudio de los Emiratos Árabes Unidos mostró que la revacunación bacillus Calmette-Guérin se asoció con la protección contra covid-19 (73). Un estudio reciente en México encontró enfermedades menos graves en individuos vacunados recientemente con MMR (74).
Las limitaciones de fabricación de vacunas COVID-19 y la logística de entrega (dos dosis, requisitos de cadena fría) podrían dejar plausiblemente a la mitad o más de la población mundial sin vacunarse a finales de 2021.
Un segundo uso complementario para un LAV sería entonces proporcionar protección durante lo que a menudo serán largos retrasos antes de la administración de la serie COVID-19. Una vez más, ese uso no sería una alternativa a una vacuna COVID-19, sino una forma de proporcionar protección provisional con un calendario de dos vacunas de «LAV pronto, vacuna COVID-19 cuando esté disponible». La familiaridad de la OPV en muchas partes del mundo, el bajo costo y la logística de entrega fácil pueden hacer que sea particularmente adecuada para el papel de la primera vacuna en un calendario de dos vacunas.
Los lAVS podrían ofrecer una herramienta esencial para «doblar la curva pandémica», evitando el agotamiento de los recursos de salud pública y previniendo muertes innecesarias y también pueden tener beneficios terapéuticos si se utilizan para la profilaxis postexposición de la enfermedad.