Dr. Carlos Alberto Díaz. Profesor Titular Universidad ISALUD.
Introducción: El precio que deben costar los medicamentos es desconocido para los que lo prescriben, lo sufren los que financian (además no saben si el paciente es lo que necesita) y los pacientes lo padecen con el pago de bolsillo, estos fármacos aumentan por fuera de toda lógica, sustentada en una estructura de costos transparente, en todo el mundo, y particularmente en Argentina, estos incrementos no son por la innovación que significan, ni por los costos, sino por la presión de la industria farmacéutica que es la que más factura en el planeta y no detiene su crecimiento; que es innovadora ciertamente, que ha logrado avances en las tecnologías muy importante y en el tratamiento de las enfermedades que eran invalidantes o mortales, por ello, estos bienes no pueden generar sacrificios, que lo conviertan en bienes de lujo inaccesibles, infinanciables o que generen quebrantos familiares o en los financiadores, pero es notorio que colocan unos precios que no se condicen con otros bienes de la economía, existiendo ejemplos innumerables, por ello siempre es conveniente tener este tema en la conciencia de los que dirigen los sistemas de salud o intentan comprender su funcionamiento, puesto que cada vez tienen que realizar un esfuerzo mayor para poder sostener la provisión y el acceso a los medicamentos de sus afiliados, y los tratamientos de muchas enfermedades oncológicas o potencialmente invalidantes reumáticas o del sistema nervioso, requieren tratamientos que originan gastos catastróficos para las familias, obras sociales y los prepagos, no existiendo una solución única o mágica, sino un conjunto de acciones, como instalar capacidad de producción local, competencia contra biosimilares o genéricos, acuerdos con economías de escala, guías clínicas, evitar amparos judiciales que indican medicamentos a pacientes que ya no lo necesitan, compras centralizadas, disminuir impuestos, e intermediación, desarrollar seguros para enfermedades catastróficas. Por ello consulte la base de datos y evaluaciones actualizadas. Las cadenas de comercialización, la intermediación, los acuerdos de mercado, el silencio de las autoridades, la connivencia con dirigentes políticos son otros factores que influyen en esto.
¿Medicamentos perennes o ganancias perennes?
Simran Siddalingaiah MS,Adriane Fugh-Berman
Antecedentes : los medicamentos de marca contribuyen de manera desproporcionada al alto gasto en medicamentos recetados. Las compañías farmacéuticas utilizan técnicas de extensión de patentes «perennes» que contribuyen a los altos costos de los medicamentos.
Objetivos : este artículo describe varias técnicas de extensión de patentes y analiza la táctica de combinar medicamentos genéricos con medicamentos de marca, utilizando combinaciones de metformina para el tratamiento de la diabetes como estudio de caso. Examina el argumento de que las CDF mejoran la adherencia y compara el costo de varias combinaciones de dosis fijas de marca con el costo de sus constituyentes individuales.
Materiales y Métodos: Revisamos la literatura sobre técnicas de extensión de patentes tanto en la literatura médica como en la de marketing, complementada con nuestros propios archivos extensos. Realizamos un análisis de precios de varios productos farmacéuticos de marca y equivalentes genéricos disponibles. Los precios de los medicamentos recetados se determinaron utilizando GoodRx.com, y los precios de los productos de venta libre se establecieron con base en los precios de dos cadenas mayoristas. La información sobre patentes y formulaciones se tomó del Libro Naranja de la FDA: Medicamentos aprobados con la base de datos de Evaluaciones de Equivalencia Terapéutica.
Resultados: Las tácticas de extensión de patentes «perennes» incluyen la liberación secuencial de diferentes formulaciones, cambios menores de dosificación y combinaciones de dosis fijas (FDC). Un «nuevo uso» brinda una oportunidad para que una empresa vuelva a patentar, cambiar la marca y volver a comercializar un medicamento para múltiples indicaciones. No está claro si las CDF mejoran o no la adherencia. Las combinaciones de dosis fijas de marca generalmente cuestan mucho más que sus componentes individuales. Las FDC que combinan metformina con otros medicamentos son una excepción y suelen costar lo mismo que el componente sin metformina.
Discusión: Las tácticas de extensión de patentes aumentan los costos de los medicamentos y brindan pocos beneficios adicionales a los pacientes. Es posible que modificaciones menores en las formulaciones o la dosificación no brinden beneficios clínicos. Muchas FDC son costosas y no brindan mejoras en los resultados clínicos justificadas por el costo, en comparación con medicamentos genéricos equivalentes que ahorrarían dinero y brindarían el mismo nivel de atención. La combinación de fármacos hipoglucemiantes más nuevos con metformina, un fármaco económico, genérico y de referencia, no parece costar más que los componentes individuales, pero no ofrece ninguna ventaja clínica sobre la metformina sola.
Conclusión: Las tácticas perennes deben controlarse, ya que representan un costo significativo para el sistema de salud y para los pacientes. Los médicos y otros prescriptores deben evitar prescribir FDC o medicamentos «nuevos» ligeramente modificados. Las combinaciones de medicamentos patentados generan ganancias sin innovación.
Mejorar la calidad de las patentes de medicamentos estadounidenses a través de la conciencia internacional
BMJ2022
Los medicamentos recetados son una de las intervenciones más frecuentes y útiles en medicina, y representan el 13,7 % del gasto en atención médica de EE. UU. 1 El gasto per cápita en medicamentos en los EE. UU. es mayor que en países comparables de ingresos altos, impulsado por los altos precios de los medicamentos de marca (medicamentos recientemente aprobados vendidos por un solo fabricante y generalmente protegidos de la competencia directa por patentes). 2 Cuando expiran las patentes y las protecciones reglamentarias de un medicamento de marca, termina su exclusividad en el mercado, lo que significa que los fabricantes de genéricos o biosimilares pueden vender sus versiones del producto, a menudo a precios sustancialmente más bajos. Esto conduce a reducciones en el gasto general y a un mayor acceso de los pacientes al medicamento.
Debido a que la exclusividad del mercado es fundamental para sus fuentes de ingresos, los fabricantes de medicamentos de marca han desarrollado estrategias para retrasar la entrada de genéricos. Según la ley de los EE. UU., algunas patentes de medicamentos se pueden usar para retrasar automáticamente la entrada de los fabricantes de genéricos al mercado. 3 Por lo tanto, los fabricantes de medicamentos de marca tienen interés en obtener múltiples patentes para crear una “maraña de patentes” que proteja su producto. 4 5 Algunas empresas han obtenido docenas de patentes secundarias sobre sus productos, patentes que protegen aspectos de un fármaco distintos de su nuevo ingrediente activo. 4 Dichas patentes pueden, por ejemplo, proteger compuestos modificados, formulaciones y métodos de uso, y en un caso incluso protegieron la adición de algodón de azúcar y saborizante de menta a un medicamento contra el VIH.6 Para competir con los tratamientos patentados, los fabricantes de genéricos o biosimilares deben intentar diseñar medicamentos para evitar reclamos por infracción o demandar para invalidar patentes individuales. 6
Tendencias y determinantes de los costos minoristas de medicamentos recetados
Objetivo
Caracterizar las tendencias y variaciones de los precios de los medicamentos genéricos y de marca de los EE. UU. a nivel minorista en relación con los costos de adquisición de las farmacias y los factores del mercado local.
Fuentes de datos
Datos de precios de medicamentos que consisten en reclamos de farmacias de EE. UU. de 2014 a 2019 recopilados y autorizados por GoodRx, una herramienta en línea para comparar precios de medicamentos.
Diseño del estudio
Se midieron las tendencias temporales de los precios medios de los medicamentos y los coeficientes de variación de los medicamentos genéricos y de marca, incluidos los subgrupos basados en la condición clínica (es decir, diabetes y cáncer). La competencia de las farmacias se midió utilizando el índice Herfindahl-Hirschman (HHI) a nivel de código postal. El análisis de regresión lineal multivariable evaluó el impacto de los factores a nivel del mercado local en los precios y la variación de los medicamentos.
Hallazgos principales
De 2014 a 2019, los mercados minoristas de farmacias tendieron hacia una mayor competencia: el HHI promedio por código postal disminuyó un 15,0 % ( p < 0,001). El precio medio en efectivo aumentó significativamente para los medicamentos genéricos (6,58 %, p < 0,001) y de marca (84,10 %, p < 0,001). Cuando se normalizó a los costos de adquisición, los precios en efectivo de los medicamentos genéricos aumentaron un 22,03 % ( p < 0,001), mientras que los de los medicamentos de marca disminuyeron un 2,31 % ( p < 0,001). Los medicamentos para la diabetes mostraron un margen general inicial más alto de los precios en efectivo en relación con los costos de adquisición (10,54, rango intercuartílico (RIC) 3,28–18,43) que los medicamentos para el cáncer (1,88, RIQ 1,36–3,08). Ni la competencia de las farmacias locales ni el ingreso medio predijeron significativamente el precio o la variación de los medicamentos.
Conclusión
Las medidas del precio de los medicamentos genéricos y la variación de precios son altas a pesar de la disminución de los costos al principio de la cadena de suministro farmacéutica, lo que desafía las expectativas de lo que sucedería en un mercado competitivo. Los esfuerzos para eludir el modelo de beneficios de farmacia para medicamentos genéricos pueden ofrecer a los consumidores la oportunidad de obtener ahorros sustanciales.
Integración horizontal estratégica para la reducción de costos de medicamentos en la cadena de suministro farmacéutica
Reflejos
Las asociaciones coordinadas específicas de medicamentos se pueden utilizar para aumentar las ganancias de la cadena de suministro.•
Las farmacias de cadena y de correo independientes pueden beneficiarse a través de la asociación.•
Click & Collect de la demanda de pedidos por correo en la cadena de farmacias puede aprovechar el beneficio de los socios.•
Asociaciones más coordinadas pueden generar ganancias adicionales para ambos socios.•
La magnitud del beneficio de la asociación depende de la estructura de costos y la respuesta del mercado.
Los recientes aumentos en los precios de los medicamentos recetados han llamado la atención de los legisladores y los medios de comunicación. Un informe de 2018 del Departamento de Salud y Servicios Humanos de EE. UU. indicó que los precios de los medicamentos de marca aumentaron seis veces más rápido que la inflación entre 2011 y 2015. Incluso la presencia de genéricos puede no reducir los precios de manera efectiva. Durante los últimos cinco años, el gasto de Medicare en medicamentos de marca aumentó en un 77 % incluso cuando el uso disminuyó (NBC News, 2018). Varios estudios también indican que ciertas clases terapéuticas de medicamentos se están volviendo costosas y pueden tener un impacto financiero a largo plazo en la Parte D de Medicare. reducir los costos de los medicamentos y/o aumentar las ganancias de la cadena de suministro. Específicamente, desarrollamos un modelo de optimización para determinar cuántas y cuáles de las regiones de una cadena de farmacias deben configurarse para manejar la demanda de pedidos por correo de medicamentos particulares con el objetivo de maximizar la ganancia total para los socios. Los resultados computacionales ilustran el valor de tales asociaciones para la reducción de costos de medicamentos y resaltan hasta qué punto un esfuerzo unificado puede generar ganancias adicionales para ambas partes y, por lo tanto, afectar los precios para los clientes de hacer clic y recolectar.
Valor y precio de los medicamentos contra el cáncer con indicaciones múltiples en EE. UU., Alemania, Francia, Inglaterra, Canadá, Australia y Escocia
Incentivos económicos bajo las políticas actuales de fijación de precios de medicamentos
El modelo de fijación de precios de medicamentos más prevalente, es decir, “mecanismos de precio único (más bajo)” con “un precio para un medicamento”, desvincula el precio y el valor de los medicamentos con múltiples indicaciones. Bajo una política de precio único, se puede incentivar a los fabricantes para que prioricen, retrasen, retengan o marquen ciertas indicaciones con el fin de lograr el precio y la ganancia más altos posibles [ 6 , 7 ]. La teoría sugiere que los fabricantes primero lanzan medicamentos para indicaciones con alto beneficio clínico y fuerte evidencia clínica entre pequeños grupos de población (Fig. 1A). Con base en esta sólida evidencia clínica, los fabricantes pueden exigir el precio de lista máximo para medicamentos con múltiples indicaciones, lo que impacta mínimamente en los presupuestos de atención médica debido a un pequeño grupo de población objetivo. A partir de entonces, los fabricantes pretenden expandir los medicamentos a indicaciones en una población de pacientes más grande con un beneficio clínico más bajo. Posteriormente, las políticas de fijación de precios de un solo medicamento pueden hacer que los fabricantes retengan o retiren indicaciones debido al posible uso no indicado en la etiqueta o al deterioro de los precios de las indicaciones lanzadas anteriormente.
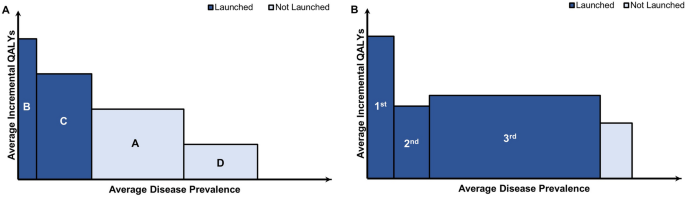
Precios para indicaciones específicas
La fijación de precios por indicación específica (ISP), también conocida como fijación de precios basada en la indicación (IBP) o fijación de precios multiindicación (MIP), es un método de fijación de precios diferencial que fija claramente el precio de un medicamento de acuerdo con el valor adicional que ofrece para cada indicación [ 8 ]. Por lo tanto, ISP restablece el vínculo precio-valor [ 9 ]. Hay un debate teórico en curso sobre los pros y los contras de ISP [ 7 , 10 , 11]. Los principales beneficios del ISP son la racionalización de los precios de los medicamentos, el aumento de la transparencia, el acceso oportuno a los medicamentos para los pacientes y el fomento del lanzamiento dinámico de indicaciones al reducir los riesgos de investigación y desarrollo (I+D) para los fabricantes. Por lo tanto, el ISP podría servir a todas las partes al ampliar el acceso a los pacientes, contener los costos de los pagadores a través de un excedente adicional del consumidor y aumentar los ingresos para los fabricantes. Por el contrario, Chandra y Garthwaite señalaron que, con un ISP, la distribución del excedente del consumidor puede favorecer a los fabricantes y, por lo tanto, aumentar el impacto en el presupuesto de los pagadores al menos a corto plazo [ 12 ]. Aunque los académicos reconocen este riesgo, argumentaron que el aumento de la competencia resultante del lanzamiento dinámico de nuevas indicaciones reducirá los precios y el impacto en el presupuesto de los pagadores a largo plazo [6 , 7 , 10 , 11 , 13 ].
La fijación de precios para indicaciones específicas es de especial interés para las agencias de autorización de comercialización (MA) y evaluación de tecnologías sanitarias (HTA), ya que el aumento de medicamentos oncológicos para múltiples indicaciones con características de valor y costo diferenciales aún no se refleja en la mayoría de los procesos regulatorios rígidos. La aprobación de la comercialización específica de la indicación es crucial para tener en cuenta los diferentes perfiles de seguridad y eficacia. Más importante aún, las agencias de HTA deben abordar la eficiencia, la eficacia y la asequibilidad fluctuantes en un nivel de indicación. El precio de los medicamentos debe ajustarse al valor diferencial con distintos mecanismos de fijación de precios para restablecer la eficiencia y la asequibilidad. Por lo tanto, los gobiernos y las aseguradoras se enfrentan a varios dilemas políticos sobre cómo reflejar el valor diferencial de las indicaciones en sistemas de reembolso ya estrictamente definidos. Supervisión a nivel de indicación,7 , 14 , 15 ]. Los países intentaron abordar los desafíos de la fijación de precios de múltiples indicaciones a través de métodos ISP indirectos, como descuentos diferenciales, precios promedio ponderados, restricciones clínicas, así como acuerdos de entrada administrados (MEA) financieros y basados en resultados [ 6 , 15 , 16 , 17 ].
¿Cuál es el impacto de las normas de propiedad intelectual en el acceso a los medicamentos? Una revisión sistemática
El Acuerdo sobre los Aspectos de los Derechos de Propiedad Intelectual relacionados con el Comercio (ADPIC) es uno de los principales acuerdos de la Organización Mundial del Comercio (OMC) y entró en vigor en 1995 [ 1 ]. Incluye estándares legales mínimos de protección de la propiedad intelectual (PI), incluidas las patentes para productos farmacéuticos. Todos los Estados miembros de la OMC deben cumplir con los ADPIC implementando sus requisitos en sus leyes nacionales de PI. TRIPS también contiene flexibilidades diseñadas para responder a las preocupaciones de que las patentes y los precios de monopolio son barreras para el accesoNota1 a medicamentos [ 2 , 3 ]. Estas flexibilidades incluyen, entre otras, la concesión de licencias obligatorias, las disposiciones Bolar, los límites al alcance de la patentabilidad, las definiciones de invención, la importación paralela y el período de transición de los países menos adelantados (PMA).
| Definiciones de algunas flexibilidades de los ADPIC | |
| términos | sentido |
| Licencias obligatorias | La licencia obligatoria es la autorización de la producción de un producto patentado o el uso de un proceso patentado sin el consentimiento del titular de la patente. El licenciatario obligatorio debe pagar una regalía al titular de la patente [ 4 ]. |
| Provisión de trabajo temprano/bolar | Una disposición de «Bolar/trabajo temprano» permite a los fabricantes de medicamentos genéricos utilizar la invención patentada para obtener la aprobación de comercialización sin el permiso del propietario de la patente, de modo que el producto genérico sea aprobado para ingresar al mercado tan pronto como expire la patente [ 5 ]. Está dentro del alcance del ‘Artículo 30 Exención de los derechos conferidos’ del Acuerdo sobre los ADPIC [ 6 ]. |
| Importación paralela | La importación paralela es cuando un país importa un producto patentado autorizado (presumiblemente a un precio más barato) de otro país sin el permiso del propietario de la patente [ 2 ]. Esto es efectivamente el agotamiento internacional de los derechos de patente, permitido por el Artículo 6 de los ADPIC [ 6 ]. |
| Período de transición de los PMA | El período de transición de los PMA libera a los PMA de las obligaciones relativas a los ADPIC relacionadas con las patentes de productos farmacéuticos hasta 2033 o hasta que dejen de ser un PMA [ 7 ]. Esto permite a los PMA comprar y/o producir medicamentos genéricos más baratos. |
«El precio de muchos medicamentos existentes, tanto de marca como genéricos, puede aumentar sustancialmente con el tiempo, y con frecuencia surgen preguntas sobre si estos aumentos de precios están justificados. Los formuladores de políticas estatales han sido particularmente activos en la búsqueda de medidas para abordar este problema«.
«En 2019, lanzamos una nueva línea de informes ICER, denominada informes de aumento de precio no respaldado (UPI), para identificar los principales medicamentos con aumentos de precio sustanciales sin evidencia adecuada para justificar los aumentos. Para guiar nuestro trabajo, recibimos aportes de un grupo asesor de múltiples partes interesadas compuesto por representantes de organizaciones de defensa de pacientes, fabricantes de medicamentos y aseguradoras. Cada año, ICER propone generar un informe de hasta 13 medicamentos que han experimentado aumentos sustanciales de precios durante un período de un año. ICER revisará los cambios en la base de evidencia para estos medicamentos e informará si se encontró un apoyo probatorio potencial para los aumentos de precios»
A muchos países, especialmente los países de ingresos bajos y medianos (LMIC), les preocupaba que tener que otorgar patentes para medicamentos aumentaría los precios y comprometería la capacidad de los gobiernos para proteger la salud pública. La Declaración de Doha de la OMC de 2001 sobre el Acuerdo sobre los ADPIC y la salud pública (Declaración de Doha) reafirma los derechos de los Estados miembros a hacer pleno uso de las flexibilidades del Acuerdo sobre los ADPIC para proteger la salud pública y maximizar el acceso a los medicamentos [ 8 ].
La ley de PI también puede verse influenciada por acuerdos comerciales negociados fuera de la OMC. En los últimos años, algunos países, especialmente aquellos que son exportadores netos de PI como EE. UU., Japón y la Unión Europea (UE), han buscado acuerdos comerciales bilaterales y/o plurilaterales que incluyen reglas de PI que van más allá de las requeridas por los ADPIC. Estas reglas TRIPS-plus pueden incluir extender los términos de las patentes más allá de los 20 años, expandir la patentabilidad, limitar el otorgamiento de licencias obligatorias y extender la exclusividad de datos [ 9 , 10 , 11 , 12 ]. Sin embargo, no todas las leyes nacionales de PI son consecuencia de acuerdos comerciales. Muchos países han introducido unilateralmente leyes ADPIC-plus IP independientes de los acuerdos comerciales, algunos antes del Acuerdo TRIPS.
A lo largo de los años, los investigadores de diversos campos de estudio, incluidos el derecho, la salud pública y la economía, se han propuesto cuantificar el impacto de las normas de PI, como el fortalecimiento de la protección de patentes, la exclusividad de datos y la extensión del plazo de patentes en el precio y la disponibilidad de medicamentos. La exclusividad de datos se refiere a la protección de los datos de ensayos clínicos de medicamentos presentados a las autoridades reguladoras de medicamentos para su aprobación comercial. Funciona para prohibir a las compañías de medicamentos genéricos que se basen en los datos de ensayos de medicamentos existentes presentados a las autoridades reguladoras para obtener la aprobación comercial de un medicamento genérico [ 13 , 14 ].
Hasta la fecha, ha habido revisiones sistemáticas que han resumido la evidencia sobre el impacto en la salud de los acuerdos comerciales [ 15 ], los impactos de las disposiciones de PI en los acuerdos comerciales sobre el acceso a los medicamentos en los LMIC [ 16 ] y el impacto de acuerdos comerciales plurilaterales específicos en la accesibilidad y asequibilidad de los medicamentos [ 17 ]. Los hallazgos de estas revisiones sugieren que los acuerdos comerciales plantean riesgos significativos para la salud [ 15 ], la protección de la PI en los acuerdos comerciales aumenta los precios de los medicamentos y disminuye el bienestar del consumidor en los LMICS [ 16 ] y el Acuerdo de Asociación Transpacífico (TTPA) podría dificultar la asequibilidad y accesibilidad de los medicamentos [ 17]. Sin embargo, ninguna revisión sistemática ha capturado la gama completa de estudios empíricos que se han centrado en el impacto de las reglas de PI en el acceso a los medicamentos a nivel mundial.
El objetivo de este estudio es revisar sistemáticamente la literatura que mide el impacto de las reglas de PI en el acceso a los medicamentos. Esta evidencia se puede utilizar para informar el desarrollo de políticas y leyes comerciales y de propiedad intelectual relevantes para mejorar el acceso a medicamentos asequibles o al menos minimizar los efectos negativos. Definimos ‘impacto’ como la disponibilidad, costo o precioNota2 de medicamentos. Las reglas de PI relevantes para el acceso a los medicamentos incluyen, entre otras, patentes de productos farmacéuticos, exclusividad de datos, patentes secundarias, extensión del plazo de la patente, vinculación de patentes, junto con las flexibilidades de los ADPIC, incluidas las licencias obligatorias, las disposiciones Bolar y la importación paralela. La vinculación de patentes vincula la aprobación de la comercialización por parte del regulador de medicamentos con el estado de la patente del medicamento [ 18 ]. Una patente secundaria es una patente sobre aspectos distintos del ingrediente activo original del fármaco, como variantes químicas, nuevas formulaciones del fármaco o métodos de administración [ 19 ]. Se utiliza para extender la vida efectiva de la patente de un medicamento.
Discusión
El principal hallazgo de esta revisión es que las reglas de propiedad intelectual ADPIC-plus están asociadas con precios de medicamentos más altos, pérdidas en el bienestar de los consumidores y mayores costos para los consumidores y los gobiernos.
Acuerdos comerciales
Si bien las disposiciones de propiedad intelectual más amplias y los períodos de monopolio más prolongados están siendo impulsados en gran medida por las negociaciones comerciales, la mayoría de los estudios no examinaron principalmente los acuerdos comerciales. Los que sí lo hicieron, se centraron en los acuerdos comerciales de EE. UU. y la UE. Esto no es sorprendente dado que estas jurisdicciones son exportadoras netas de medicamentos y, por lo tanto, es más probable que busquen disposiciones ADPIC-plus IP en los acuerdos comerciales. Los acuerdos comerciales de la UE estudiados incluyeron CETA y el TLC UE-Andina. Se encontró que las disposiciones de PI en estos acuerdos comerciales de la UE tienen posibles implicaciones negativas para el acceso a los medicamentos en Canadá [ 22 , 23 , 24 ], Perú [ 37 ] y Colombia [ 38 ].] al retrasar la entrada de la competencia de genéricos y aumentar el gasto farmacéutico.
Los acuerdos comerciales de EE. UU. estudiados abarcaron una gama más amplia de países. Algunos de los estudios incluyeron acuerdos comerciales regionales que incluían a los EE. UU., sin embargo, sus hallazgos se limitaron al impacto de las disposiciones de PI en un país específico. Esto incluyó el impacto en Tailandia [ 25 , 26 , 27 ], Jordania [ 28 , 39 ], Corea [ 29 , 30 ], Canadá [ 31 , 32 ], Chile [ 34 ], Guatemala [ 33 ] y Vietnam [ 35 ].]. Todos estos estudios encontraron implicaciones negativas para el acceso a medicamentos en el país seleccionado. Estas implicaciones negativas incluyeron el aumento de los costos del programa de tratamiento y la disminución de la cobertura del tratamiento [ 35 ], aumentos en los precios de los medicamentos [ 26 , 27 , 32 , 34 , 39 ], acceso restringido o retrasado a genéricos [ 26 , 27 , 28 , 33 , 39 ] y medicamentos biosimilares [ 32 ], ahorros perdidos [ 31 ], consumidores [ 25 , 29 ] y pérdidas totales de bienestar [ 29], y aumento del gasto farmacéutico [ 26 , 28 ]. Además, Son descubrió que el acuerdo comercial entre Corea y EE. UU. no logró aumentar la disponibilidad de nuevos medicamentos en Corea y no acortó el retraso en la disponibilidad de nuevos medicamentos [ 30 ].
De los 18 estudios que se centraron principalmente en los acuerdos comerciales, los resultados de uno se desviaron significativamente del resto. Bollyky se centró en el impacto en todos los países con acuerdos comerciales de EE. UU. y no encontró aumentos en el precio promedio de los medicamentos originales sin patente, el gasto farmacéutico, el consumo de productos farmacéuticos, la proporción de medicamentos de marca versus genéricos o en el gasto nacional en productos farmacéuticos como porcentaje. del gasto total en salud [ 36 ]. Kapczynski et al. criticó el análisis de Bollyky como «engañoso porque no considera los medicamentos correctos en los momentos correctos, pasa por alto las dimensiones temporales de la implementación de las disposiciones de los acuerdos comerciales anteriores e ignora el contexto más amplio en el que se negocian e implementan los acuerdos comerciales» [ 112]. Sugieren que se necesita más trabajo empírico para comprender mejor el impacto de las disposiciones de PI más amplias sobre el acceso a los medicamentos en los países de bajos ingresos [ 112 ]. De relevancia aquí son las observaciones de Shadlen et al de que las disposiciones de PI en los acuerdos comerciales entran en vigor en diferentes momentos, lo que complica el análisis [ 10 ]. Muchos países con acuerdos comerciales introdujeron patentes de productos farmacéuticos solo después de TRIPS (1995). Dados los plazos de patente de 20 años, es prematuro evaluar los impactos de las disposiciones ADPIC-plus hasta el vencimiento de la patente en 2015 o más tarde para los países que aprovechan al máximo los períodos de transición [ 10 ].
Quince de los 18 estudios sobre acuerdos comerciales eran estudios de modelos prospectivos basados en texto filtrado para evaluar los impactos potenciales de los acuerdos antes de que se firmaran. islam et al. describir en detalle las ventajas y desventajas de los análisis prospectivos versus retrospectivos de los impactos de los acuerdos comerciales [ 16 ]. Afirman que si bien ambos tipos de estudios generalmente encuentran que los acuerdos comerciales dan como resultado aumentos de precios y una disminución del bienestar del consumidor, generalmente hay una diferencia en el tamaño del impacto con estudios retrospectivos que tienden a ser más modestos en sus estimaciones de impacto [ 16 ]. Esto se atribuyó a las suposiciones realizadas en los modelos ex-ante ya las limitaciones de los estudios ex-post [ 16 ].
Políticas de patentes
Varios estudios comparativos de países que midieron el impacto de los regímenes de patentes en el momento del lanzamiento de medicamentos encontraron que las disposiciones de patentes más estrictas aceleran la entrada en el mercado de nuevos medicamentos, [ 81 , 82 , 83 , 85 , 94 ] especialmente los medicamentos de gran éxito [ 82 , 94 ]. Algunos de estos estudios encontraron que este fenómeno es cierto solo para los países de ingresos altos y no para los países de ingresos bajos y medios [ 82 , 83]. Esto podría reflejar un simple comportamiento de maximización de ganancias, centrándose en mercados más lucrativos y drogas más lucrativas. Por el contrario, dos estudios encontraron que los niveles más altos de protección de la PI se asociaron con un menor acceso a los medicamentos [ 85 , 87 ]. Incluso en estudios que mostraron una asociación positiva entre una mayor protección de la propiedad intelectual y la disponibilidad de nuevos medicamentos, el alto precio del producto farmacéutico patentado resultó en un efecto neto de ventas significativamente reducidas [ 85 ]. Hellerstein también descubrió que los países con mercados de medicamentos en gran parte originales estaban pagando significativamente más por los ARV que los países proveedores de genéricos [ 86 ].]. Aquí es relevante un hallazgo importante de los estudios sobre la entrada de genéricos: esto da como resultado caídas significativas de precios solo cuando hay competencia entre los genéricos [ 113 ].
Los hallazgos de dos estudios comparativos de patentes contrastaron marcadamente con los estudios anteriores. Rozek y Berkowitz encuentran que ‘mejorar’ los regímenes de PI no cambia los precios de los productos farmacéuticos de marca y que los países con regímenes de PI ‘mejorados’ no tienen medicamentos de mayor precio que los países sin [ 88 ]. La PI ‘mejorada’ en este caso se equiparó con una mayor protección de la PI, pero no se definió el significado exacto de esto. Además, hubo controles inadecuados para otras variables relevantes [ 88 ]. Djolov también descubrió que una fuerte protección de patentes se asociaba con un mejor acceso a los medicamentos esenciales [ 89 ]. En el estudio Djolov [ 89] casi todos los medicamentos esenciales están sin patente y, por lo tanto, no se ven afectados por la fuerza de las disposiciones de patente. El período de tiempo estudiado no fue lo suficientemente largo como para captar el impacto de las nuevas disposiciones sobre patentes [ 89 ]. Para medir con mayor precisión la relación entre la patente y los precios, solo se deben incluir en el análisis los nuevos medicamentos no patentados introducidos después del nuevo régimen de patentes de productos [ 114 , 115 ].
Los nueve estudios de un solo país que se centraron en el impacto de patentes más sólidas encontraron implicaciones negativas para el acceso a los medicamentos. Se descubrió que las patentes causan una pérdida significativa de bienestar [ 90 , 91 , 93 ] y un aumento en los precios de los medicamentos en India [ 92 ]. Respaldando estos hallazgos, la disponibilidad de medicamentos genéricos y medicamentos yo también condujo a mejoras en el bienestar del consumidor [ 80 ].
Los estudios centrados en la India son particularmente pertinentes para comprender el impacto de la introducción de patentes para productos farmacéuticos. India aprovechó al máximo el período de transición de 10 años para introducir dichas patentes [ 116 ]. Además, India diseñó su legislación de patentes para garantizar que no se puedan patentar compuestos médicos muy similares a menos que haya un nuevo beneficio terapéutico. Antes de esto, los fabricantes indios producían legalmente versiones genéricas de muchos medicamentos bajo patente en otros países. El régimen de patentes de India tiene implicaciones para el acceso a medicamentos no solo en India, sino en todo el mundo, ya que puede inhibir la producción de medicamentos genéricos. India es el mayor productor mundial de medicamentos genéricos y representa más del 80% de los volúmenes de compra anual de ARV [ 117]. Aunque estos estudios se centraron únicamente en el mercado indio, las patentes de productos farmacéuticos en India podrían potencialmente reducir el suministro de medicamentos genéricos para muchos de los países más pobres del mundo.
Reglas ADPIC-plus: extensiones del plazo de patentes y patentes secundarias
Los artículos que midieron el impacto de las reglas ADPIC-plus se centraron en las extensiones de los plazos de las patentes y las patentes secundarias. Diez de los 13 estudios TRIPS-plus eran de América del Norte, dos eran de Australia y uno era un estudio de varios países que incluía a los EE. UU.
Todos los estudios de extensión del plazo de las patentes encontraron impactos negativos para el acceso a los medicamentos, que incluyeron un mayor gasto público en atención médica [ 99 , 100 , 101 , 102 , 103 ], mayores precios de los medicamentos [ 98 , 100 ] y demoras en la disponibilidad de medicamentos [ 100 ].
De manera similar, todos los artículos que examinaron las patentes secundarias encontraron impactos negativos para el acceso a los medicamentos, incluidos períodos de monopolio más prolongados que retrasaron la entrada al mercado de genéricos más baratos [ 19 , 104 , 106 , 107 ], mayores costos para los contribuyentes [ 109 ] y pérdidas en el bienestar social [ 107 ]. . El único artículo que se centró en entornos de escasos recursos descubrió que las medidas para restringir el patentamiento secundario tenían una eficacia limitada en Argentina y ningún impacto medible en India y Brasil [ 110 ]. Los autores sugieren que las características administrativas y procesales de los sistemas de patentes pueden tener una mayor influencia en la concesión de patentes secundarias que las propias leyes de patentes.110 ]. Abordar este problema significaría abordar el tipo de asistencia técnica que se brinda a las oficinas de patentes en los países de bajos y medianos ingresos [ 118 ]. Este es un tema prioritario dado el costo de impugnar las patentes concedidas y el impacto que las duraciones más largas de las patentes podrían tener en el acceso a los medicamentos en países menos capaces de pagar precios altos por medicamentos. Las patentes secundarias en India podrían tener ramificaciones negativas para los países que dependen de India para obtener medicamentos genéricos asequibles.
Entrada genérica/caducidad de patente
Los medicamentos genéricos son más asequibles que los medicamentos patentados, ya que suelen tener un precio más cercano al costo marginal de producción cuando hay tres o más medicamentos genéricos disponibles [ 113 ]. Por lo tanto, no sorprende encontrar que todos los artículos que exploraron varias facetas de la entrada al mercado de genéricos o la expiración de la patente encontraron impactos positivos para el acceso a los medicamentos. Por ejemplo, el hallazgo más destacado en este grupo de 22 artículos fue que la entrada al mercado de genéricos resultó en reducciones significativas en el costo de los medicamentos [ 23 , 58 , 60 , 61 , 64 , 65 , 66 , 67 , 69 , 73 ,75 , 76 , 77 , 78 , 119 ] pero no necesariamente en el precio del fármaco original [ 72 ]. Un estudio encontró que el estado genérico es el predictor más consistente del precio de un medicamento [ 61 ].
La introducción de la Ley Hatch-Waxman de EE. UU. en 1984 fue diseñada, entre otras cosas, para promover el acceso temprano y eficiente a los medicamentos genéricos. Esto se haría facilitando la aprobación acelerada por parte de la Administración de Alimentos y Medicamentos (FDA), el regulador nacional, para permitir la entrada en el mercado de genéricos tan pronto como expiraran las patentes, o se descubriera que no eran válidas o no se habían infringido [ 14 ]. Los estudios que se centraron en la entrada al mercado de genéricos en los EE. UU. encontraron que la introducción de la Ley Hatch-Waxman resultó en un aumento en los desafíos de patentes [ 63 ], un aumento en el número de patentes asociadas con cada medicamento [ 105 ] un aumento en el genérico cuota de mercado [ 64 ], aumento del bienestar del consumidor [ 62] y una disminución en los costos diarios de tratamiento [ 64 ]. Sin embargo, para maximizar las ganancias, muchas marcas originales reformulan patentes para disminuir el impacto financiero de la expiración de la patente [ 68 ]. Entre los medicamentos más vendidos, Feldman descubrió que más del 70 % de los medicamentos enumerados en el Libro Naranja añadían patentes adicionales o privilegios de exclusividad de datos al medicamento, lo que indica un uso extensivo de patentes secundarias [ 105 ].
Casi todos estos estudios se llevaron a cabo en países de ingresos altos; sin embargo, incluso entre los Estados miembros de la UE existen importantes disparidades de riqueza y el acceso a los medicamentos no es uniforme. Un estudio de varios países de la UE encontró que las restricciones de asequibilidad impactaron en el acceso a los medicamentos y cuando las alternativas genéricas entraron en el mercado, mejoró el acceso a medicamentos efectivos, sobre todo en los Estados miembros de la UE de bajos ingresos [ 57 ]. Estos hallazgos tienen implicaciones para entornos donde las patentes y los altos precios de los medicamentos comprometen el acceso de las personas a genéricos asequibles.
Licencias obligatorias, comercio paralelo y otras flexibilidades
Las flexibilidades de los ADPIC, como las licencias obligatorias o incluso la amenaza de licencias obligatorias, aumentan la disponibilidad de medicamentos [ 48 ], aumentan la cobertura del tratamiento y reducen los precios de los medicamentos [ 48 , 49 ]. La concesión de licencias obligatorias se ha implementado más comúnmente para facilitar un mayor acceso a los medicamentos ARV [ 48 , 49 , 50 ]. Curiosamente, las licencias obligatorias parecen haberse vuelto menos frecuentes desde 2006. El comercio paralelo parece tener un impacto más modesto en los precios de los medicamentos [ 52 , 53] que las licencias obligatorias, sin embargo, hubo muy pocos estudios sobre el comercio paralelo, todos los cuales se centran en los Estados miembros de la UE. A pesar de esto, la mayoría mostró ahorros de costos gracias al comercio paralelo [ 54 , 55 , 56 ]. Estos hallazgos están en consonancia con el propósito original de las flexibilidades de los ADPIC: proporcionar a los gobiernos el «espacio político» para mitigar los impactos negativos de las patentes, como los precios de los medicamentos excesivamente altos y la falta de competencia [ 120 ].
Otras revisiones sistemáticas
Los hallazgos de este estudio brindan abundantes detalles empíricos y hallazgos que se suman a otras revisiones sistemáticas. La revisión sistemática de Barlow et al sobre el impacto en la salud de los acuerdos comerciales y de inversión también encontró un estudio [ 35 ] que muestra un mayor acceso a los medicamentos debido a las licencias obligatorias. La revisión de Islam et al de las disposiciones de PI en los tratados comerciales sobre el acceso a los medicamentos en los LMIC también encontró que las disposiciones de PI en los acuerdos comerciales aumentaron los precios de los medicamentos y redujeron el bienestar del consumidor [ 16 ]. Sin embargo, esta revisión no incluyó países de altos ingresos o reglas de PI no relacionadas con acuerdos comerciales. El resumen de políticas de Trachtenberg et al sobre acuerdos comerciales y acceso a medicamentos tenía un alcance de revisión más limitado pero incluía una crítica útil de los métodos empleados en los estudios [ 121]. Esta revisión incluyó algunos de los mismos artículos y llegó a las mismas conclusiones que el estudio actual; Las disposiciones de PI en los acuerdos comerciales tienen un impacto negativo en el precio y la disponibilidad de los medicamentos. La revisión actual incluyó un conjunto más amplio de estudios y es útil para proporcionar una evaluación más completa del estado actual del conocimiento.
Conclusiones
Los artículos de esta revisión abarcan varias disciplinas, incluidas la economía, la salud pública y las ciencias sociales. Gran parte de la evidencia proviene de estudios centrados no en el impacto de acuerdos comerciales específicos, sino en disposiciones ADPIC-plus específicas implementadas independientemente de los acuerdos comerciales.
Con muy pocas excepciones, los artículos de esta revisión encontraron que la introducción de patentes luego de la implementación de las reglas de TRIPS y las disposiciones de PI de TRIPS-plus relacionadas con productos farmacéuticos están asociadas con un aumento en los precios de los medicamentos, pérdidas en el bienestar del consumidor y mayores costos para los consumidores de productos farmacéuticos y gobiernos nacionales. Los estudios en este campo pueden ser complejos y la calidad de los hallazgos depende de cuándo se miden los impactos, el contexto y la elección de los métodos.
Existe evidencia de que las flexibilidades de los ADPIC pueden facilitar el acceso a los medicamentos, aunque su uso es limitado y su implementación a veces desafiante; por sí solos, no pueden ser una panacea para las disposiciones de PI que aumentan los monopolios. Sin embargo, pueden ofrecer a los países cierta flexibilidad y poder de negociación con las empresas farmacéuticas para determinar su acceso y fijación de precios con respecto a los mercados nacionales. Lo mismo ocurre con algunas políticas nacionales diseñadas para aumentar el acceso a medicamentos genéricos asequibles. Las leyes de PI no operan fuera de los contextos sociales, políticos y económicos, ya sea a nivel local o global. En particular, interactúan con una variedad de otras leyes que probablemente afecten el acceso a los medicamentos en una jurisdicción determinada, lo que, aunque está fuera del alcance de este documento, merece una mayor investigación.122 ].
References
- World Trade Organization. UNDERSTANDING THE WTO: THE AGREEMENTS. Intellectual property: protection and enforcement. 2021. Available from: https://www.wto.org/english/thewto_e/whatis_e/tif_e/agrm7_e.htm.
- World Trade Organization. FACT SHEET: TRIPS AND PHARMACEUTICAL PATENTS. Obligations and exceptions. Under TRIPS, what are member governments’ obligations on pharmaceutical patents? 2006. Available from: https://www.wto.org/english/tratop_e/trips_e/factsheet_pharm02_e.htm.
- World Health Organization. Promoting access to medical technologies and innovation: intersections between public health, intellectual property and trade. Geneva: World Health Organization; 2020.
- World Trade Organization. TRIPS AND HEALTH: FREQUENTLY ASKED QUESTIONS. Compulsory licensing of pharmaceuticals and TRIPS. 2021. Available from: https://www.wto.org/english/tratop_e/trips_e/public_health_faq_e.htm.
- WTO OMC. FACT SHEET TRIPS and pharmaceutical patents. 2003 [15th Feb 2021]. Available from: https://www.wto.org/english/tratop_e/trips_e/tripsfactsheet_pharma_e.pdf.
- TRIPS: Agreement on Trade-Related Aspects of Intellectual Property Rights., Annex 1C, 1869 U.N.T.S. 299, 33 I.L.M. 1197 (Apr. 15, 1994).
- United Nations LDC Portal International Support Measures for Least Developed Countries. WTO drugs patent waiver for LDCs extended until 2033. Available from: https://www.un.org/ldcportal/wto-drugs-patent-waiver-for-ldcs-extended-until-2033/. Accessed 9 Mar 2021.
- DOHA WTO MINISTERIAL 2001: TRIPS WT/MIN(01)/DEC/2 20 November 2001, (Adopted on 14 November 2001). Accessed 13 Jan 2021.
- Said MKE. Public health related TRIPS-plus provisions in bilateral trade agreements: a policy guide for negotiators and implementers in the eastern Mediterranean Region; 2010.
- Shadlen KC, Sampat BN, Kapczynski A. Patents, trade and medicines: past, present and future. Rev Int Polit Econ. 2020;27(1):75–97.
- Sell SK. TRIPS-plus free trade agreements and access to medicines. Liverpool Law Rev. 2007;28(1):41–75.
- t Hoen EF. The global politics of pharmaceutical monopoly power: drug patents, access, innovation and the application of the WTO Doha Declaration on TRIPS and public health. Diemen: DiemenAMB; 2009.
- World Health Organization- Regional Office for South East Asia. Data exclusivity and other “trips-plus” measures 2017.
- Behrendt KE. The Hatch-Waxman Act: balancing competing interests or survival of the fittest. Food Drug LJ. 2002;57:247.
- Barlow P, McKee M, Basu S, Stuckler D. The health impact of trade and investment agreements: a quantitative systematic review and network co-citation analysis. Glob Health. 2017;13(1):1–9.
- Islam MD, Kaplan WA, Trachtenberg D, Thrasher R, Gallagher KP, Wirtz VJ. Impacts of intellectual property provisions in trade treaties on access to medicine in low and middle income countries: a systematic review. Glob Health. 2019;15(1):88.
- Yap YY, Wong CP, Lee KS, Ming LC, Khan TM. Trans-Pacific partnership agreement and its impact on accessibility and affordability of medicines: a meta-synthesis. Ther Innov Regul Sci. 2017;51(4):446–59.
- Baker BK. Ending drug registration apartheid: taming data exclusivity and patent/registration linkage. Am J Law Med. 2008;34(2-3):303–44.
- Amin T, Kesselheim AS. Secondary patenting of branded pharmaceuticals: a case study of how patents on two HIV drugs could be extended for decades. Health Aff (Millwood). 2012;31(10):2286–94.
- Liberati A, Altman DG, Tetzlaff J, Mulrow C, Gøtzsche PC, Ioannidis JP, et al. The PRISMA statement for reporting systematic reviews and meta-analyses of studies that evaluate health care interventions: explanation and elaboration. J Clin Epidemiol. 2009;62(10):e1–e34.
- Hawker S, Payne S, Kerr C, Hardey M, Powell J. Appraising the evidence: reviewing disparate data systematically. Qual Health Res. 2002;12(9):1284–99.
- Grootendorst P, Hollis A. The 2011 Canada-European Union Comprehensive Economic and Trade Agreement: an economic impact assessment of the EU’s proposed pharmaceutical intellectual property provisions. J Generic Med. 2011;8(2):81–103.
- Lexchin J, Gagnon MA. CETA and pharmaceuticals: impact of the trade agreement between Europe and Canada on the costs of prescription drugs. Glob Health. 2014;10:30.
- Beall RF, Hardcastle L, Clement F, Hollis A. How will recent trade agreements that extend market protections for brand-name prescription pharmaceuticals impact expenditures and generic access in Canada? Health Policy. 2019;123(12):1251–8.
- Yoongthong T. Social cost of market exclusivity extension for patented medicines in Thailand: analysis of the effect of trips-plus provisions. Bangkok: National Institute of Development Administration; 2012.
- Kessomboon N, Limpananont J, Kulsomboon V, Maleewong U, Eksaengsri A, Paothong P. Impact on access to medicines from TRIPS-Plus: a case study of Thai-US FTA. Southeast Asian J Trop Med Public Health. 2010;41(3):667–77.
- Akaleephan C, Wibulpolprasert S, Sakulbumrungsil R, Luangruangrong P, Jitraknathee A, Aeksaengsri A, et al. Extension of market exclusivity and its impact on the accessibility to essential medicines, and drug expense in Thailand: analysis of the effect of TRIPs-Plus proposal. Health Policy. 2009;91(2):174–82.
- Malpani R. All costs, no benefits: how the US-Jordan free trade agreement affects access to medicines. J Generic Med. 2009;6(3):206–
- Oh K-Y, Kim T. Measuring the welfare effects of intellectual property rights changes on the Korean pharmaceutical industry: the case of Korea–US Free Trade Agreement AU – Oh, Keun-Yeob. Asia-Pac J Account Econ. 2012;19(3):278–91.
- Son K-B. Do free trade agreements matter to drug lag? Recent evidence from Korea after the Korea–US free trade agreement. Int J Health Serv. 2020;50(2):147–55.
- Lexchin J. Increase in drug spending in Canada due to extension of data protection for biologics: a descriptive study. Healthc Policy. 2019;14(3):10.
- The Parliamentary Budget Office. The impact of the Canada – United States – Mexico agreement on prescription drug expenditures in Canada. 2019.
- Shaffer ER, Brenner JE. A trade agreement’s impact on access to generic drugs. Health Aff (Millwood). 2009;28(5):w957–68.
- Trachtenberg D, Kaplan WA, Wirtz VJ, Gallagher KP. The effects of trade agreements on imports of biologics: evidence from Chile. J Glob Dev. 2020;1(ahead-of-print):1–20.
- Moir HVJ, Tenni B, Gleeson D, Lopert R. The Trans Pacific Partnership Agreement and access to HIV treatment in Vietnam. Glob Public Health. 2018;13(4):400–13. https://doi.org/10.1080/17441692.2016.1256418.
- Bollyky TJ. A Dose of TPP’s medicine: why U.S. trade deals have not exported U.S. drug prices (March 22, 2016). Council on Foreign Relations Working Paper. Available at SSRN: https://ssrn.com/abstract=2755754.
- IFARMA FM, Salud. Impact of the EU-Andean Trade Agreement on Access to Medicines in Peru. 2009.
- IFARMA FM, Salud. Impact of the EU-Andean Trade Agreement on Access to Medicines in Colombia. Bogota: IFARMA; 2009.
- Abbott RB, Bader R, Bajjali L, ElSamen TA, Obeidat T, Sboul H, et al. The price of medicines in Jordan: the cost of trade-based intellectual property. J Generic Med. 2012;9(2):75–85.
- Mohara A, Yamabhai I, Chaisiri K, Tantivess S, Teerawattananon Y. Impact of the introduction of government use licenses on the drug expenditure on seven medicines in Thailand. Value Health. 2012;15(1 Suppl):S95–9.
- Yamabhai I, Mohara A, Krichanan W, Chaisiri K, Tantivess S, Teerawattananon Y. Government use licenses in Thailand: an assessment of the health and economic impacts. Glob Health. 2011;7(28):1–12.
- Yamabhai I, Mohara A, Tantivess S, Chaisiri K, Teerawattananon Y. Assessing the implications of Thailand’s Government Use Licenses, issued in 2006 – 2008. Bangkok: Ministry of Public Health Thailand; 2009.
- Scopel CT, Chaves GC. Initiatives to challenge patent barriers and their relationship with the price of medicines procured by the Brazilian Unified National Health System. Cad Saude Publica. 2016;32(11):12.
- Ramani SV, Urias E. When access to drugs meets catch-up: Insights from the use of CL threats to improve access to ARV drugs in Brazil. Res Policy, Elsevier. 2018;47(8):1538–52.
- Ortiz-Prado E, Cevallos-Sierra G, Teran E, Vasconez E, Borrero-Maldonado D, Ponce Zea J, et al. Drug prices and trends before and after requesting compulsory licenses: the Ecuadorian experience. Expert Opin Ther Pat. 2019;29(8):653–62.
- Chatterjee C, Kubo K, Pingali V. The consumer welfare implications of governmental policies and firm strategy in markets
- ‘t Hoen EF, Veraldi J, Toebes B, Hogerzeil HV. Medicine procurement and the use of flexibilities in the agreement on trade-related aspects of intellectual property rights, 2001–2016. Bull World Health Organ. 2018;96(3):185.
- Cherian N. Using compulsory licenses to access pharmaceuticals: a cross case analysis on outcomes. Oslo: University of Oslo; 2016.
- Son KB, Lee TJ. Compulsory licensing of pharmaceuticals reconsidered: Current situation and implications for access to medicines. Glob Public Health. 2017. https://doi.org/10.1080/17441692.2017.1407811.
- Beall R, Kuhn R. Trends in compulsory licensing of pharmaceuticals since the Doha declaration: a database analysis. PLoS Med. 2012;9(1):e1001154.
- Beall RF, Attaran A. A method for understanding generic procurement of HIV medicines by developing countries with patent protection. Soc Sci Med. 2017;185:118.
- Kanavos P, Costa-Font J, Gollier C. Pharmaceutical parallel trade in Europe: stakeholder and competition effects. Econ Policy. 2005;20(44):753–98.
- Kyle MK, Allsbrook JS, Schulman KA. Does reimportation reduce price differences for prescription drugs? Lessons from the European Union. Health Serv Res. 2008;43(4):1308–24.
- Duso T, Herr A, Suppliet M. The welfare impact of parallel imports: a structural approach applied to the German market for oral anti-diabetics. Düsseldorf: DICE Discussion Paper, No. 137, Düsseldorf Institute for Competition Economics (DICE); 2014.
- Mendez SJ. Parallel trade of pharmaceuticals: the Danish market for statins. St. Louis: Federal Reserve Bank of St Louis; 2016.
- Granlund D, Koksal-Ayhan MY. Parallel imports and a mandatory substitution reform: a kick or a muff for price competition in pharmaceuticals? Eur J Health Econ. 2015;16(9):969–83.
- Elek P, Harsányi A, Zelei T, Csetneki K, Kaló Z. Policy objective of generic medicines from the investment perspective: the case of clopidogrel. Health Policy. 2017;121(5):558.
- European Commission. Final report: pharmaceutical sector inquiry. 2009.
- Morton FMS, Stern AD, Stern S. The impact of the entry of biosimilars: evidence from Europe. Rev Ind Organ. 2018;53(1):173–210.
- Berndt ER, Dubois P. Impacts of patent expiry on daily cost of pharmaceutical treatments in eight OECD countries, 2004-2010. Int J Econ Bus. 2016;23(2):125–47.
- Liu Y, Galárraga O. Do national drug policies influence antiretroviral drug prices? Evidence from the southern African development community. Health Policy Plan. 2017;32(2):170–7.
- Branstetter L, Chatterjee C, Higgins MJ. Regulation and welfare: evidence from paragraph IV generic entry in the pharmaceutical industry. RAND J Econ. 2016;47(4):857–90.
- Grabowski H, Brain C, Taub A, Guha R. Pharmaceutical patent challenges: company strategies and litigation outcomes. Am J Health Econ. 2016;3(1):33–59.
- Berndt ER, Aitken ML. Brand loyalty, generic entry and price competition in pharmaceuticals in the quarter century after the 1984 Waxman-Hatch legislation. Int J Econ Bus. 2011;18(2):177–201.
- Bokhari FAS, Fournier GM. Entry in the ADHD drugs market: welfare impact of generics and me-too’s. J Ind Econ. 2013;61(2):339–92.
- Castanheira M, de Frutos MA, Ornaghi C, Siotis G. The unexpected consequences of asymmetric competition. An application to big pharma. CEPR discussion paper no DP11813 2017.
- Frank RG, Salkever DS. Generic entry and the pricing of pharmaceuticals. J Econ Manag Strategy. 1997;6(1):75–90.
- Huckfeldt P, Knittel C. Pharmaceutical use following generic entry: paying less and buying less. Cambridge: National Bureau of Economic Research; 2011.
- Shih YCT, Bekele NB, Xu Y. Use of Bayesian net benefit regression model to examine the impact of generic drug entry on the cost effectiveness of selective serotonin reuptake inhibitors in elderly depressed patients. Pharmacoeconomics. 2007;25(10):843–62.
- Hemphill CS, Sampat BN. Evergreening, patent challenges, and effective market life in pharmaceuticals. J Health Econ. 2012;31(2):327–39.
- Hemphill CS, Sampat BN. When do generics challenge drug patents? J Empir Leg Stud. 2011;8(4):613–49.
- Lexchin J. The effect of generic competition on the price of brand-name drugs. Health Policy. 2004;68(1):47–54.
- Jones JCH, Potashnik T, Zhang A. Patents, brand-generic competitions and the pricing of ethical drugs in Canada: some empirical evidence from British Columbia, 1981-1994. Appl Econ. 2001;33(7):947–56.
- Gleeson D, Townsend B, Lopert R, Lexchin J, Moir H. Financial costs associated with monopolies on biologic medicines in Australia. Aust Health Rev. 2019;43(1):36–42.
- Hill A, Redd C, Gotham D, Erbacher I, Meldrum J, Harada R. Estimated generic prices of cancer medicines deemed cost-ineffective in England: a cost estimation analysis. BMJ Open. 2017;7(1):e011965.
- Kaier K. The impact of pricing and patent expiration on demand for pharmaceuticals: an examination of the use of broad-spectrum antimicrobials. Health Econ Policy Law. 2012;8(1):7–20.
- Boersma C, Klok RM, Bos JM, Naunton M, Van Den Berg PB, De Jongvan Den Berg LTW, et al. Drug costs developments after patent expiry of enalapril, fluoxetine and ranitidine: a study conducted for the Netherlands. Appl Health Econ Health Policy. 2005;4(3):191–6.
- Manova MM, Stoimenova A, Clerfeuille F, Petrova GI. Impact of generic competition on market share and prices of cardiovascular medicines on the Bulgarian pharmaceutical market. J Public Health. 2011;19(1):91–100.
- Asif M, Tasleem S, Akram M. Access to medicine: induction of novel drugs in the post era of new patent regulation in Pakistan. Biosci Res. 2019;16(2):5.
- Arcidiacono P, Ellickson PB, Landry P, Ridley DB. Pharmaceutical followers. Int J Ind Organ. 2013;31(5):538–53.
- Cockburn I, Lanjouw JO, Schankerman M. Patents and the global diffusion of new drugs. Am Econ Rev. 2014;106(1):136–64.
- Lanjouw JO. Patents, price controls, and access to new drugs: how policy affects global market entry. NBER working paper no. 11321; 2005.
- Watal J, Dai R. Product patents and access to innovative
- Kyle M, Qian Y. Intellectual property rights and access to innovation: evidence from TRIPS. Cambridge: National Bureau of Economic Research; 2014.
- Borrell JR, Watal J. Impact of patents on access to HIV/AIDS drugs in developing countries. Cambridge: Center for International Development at Harvard University; 2003.
- Hellerstein R. What do drug monopolies cost consumers in developing countries? Econ Lett. 2012;116(1):108–11.
- Jung Y, Kwon S. The effects of intellectual property rights on access to medicines and catastrophic expenditure. Int J Health Serv. 2015;45(3):507–29.
- Rozek R, Berkowitz R. The effects of patent protection on the prices of pharmaceutical products: is intellectual property protection raising the drug bill in developing countries? J World Intellect Prop. 2005;1(2):179–243.
- Djolov GG. Patents, price controls, and pharmaceuticals. J World Intellect Prop. 2005;6(4):611–31.
- Dutta A. From free entry to patent protection: welfare implications for the Indian pharmaceutical industry. Rev Econ Stat. 2011;93(1):160–78.
- Chaudhuri S, Goldberg PK, Jia P. Estimating the effects of global patent protection in pharmaceuticals: a case study of quinolones in India. Am Econ Rev. 2006;96(5):1477–514.
- Duggan M, Garthwaite C, Goyal A. The market impacts of pharmaceutical product patents in developing countries: evidence from India. Am Econ Rev. 2014;106(1):99–135.
- Watal J. Pharmaceutical patents, prices and welfare losses: policy options for India under the WTO TRIPS agreement. World Econ. 2000;23(5):733–52.
- Berndt ER, Cockburn IM. The hidden cost of low prices: limited access to new drugs in India. Health Aff (Project Hope). 2014;33(9):1567–75.
- Challu PM. Effects of the monopolistic patenting of medicine in Italy since 1978. Int J Technol Manag. 1995;10:237–50.
- Yamabhai I, Smith RD. To what extent are pharmaceutical prices determined by patents? A case study of oncology medicines in Thailand. J Intellect Prop Rights. 2015;20(2):89.
- Grootendorst P, Shim M, Falconi A, Robinson T, Lexchin J. Intellectual property protection and drug plan coverage: evidence from Ontario. Int J Health Serv. 2018;48(4):702–15.
- Kesselheim A, Solomon D. Incentives for drug development: the curious case of colchicines. N Engl J Med. 2010;362:2045–7.
- Nelson RE, McAdam-Marx C, Evans ML, Ward R, Campbell B, Brixner D, et al. Patent extension policy for paediatric indications: an evaluation of the impact within three drug classes in a state Medicaid programme. Appl Health Econ Health Policy. 2011;9(1):171–81.
- Kesselheim AS, Fischer MA, Avorn J. Extensions of intellectual property rights and delayed adoption of generic drugs: effects on medicaid spending. Health Aff (Project Hope). 2006;25(6):1637–47.
- The Parliamentary Budget Office. Patent restoration and the cost of pharmaceuticals. 2018.
- Di Matteo L, Grootendorst P. Federal patent extension, provincial policies, and drug expenditures, 1975-2000. Can Tax J. 2002;50(6):1913–48.
- Harris T, Nicol D, Gruen N. Pharmaceutical patents review report [Online]; 2013.
- Kapczynski A, Park C, Sampat B. Polymorphs and prodrugs and salts (Oh my!): an empirical analysis of “secondary” pharmaceutical patents. PLoS One. 2012;7(12):e49470.
- Feldman R. May your drug price be evergreen. J Law Biosci. 2018;5(3):590–647.
- Beall RF, Nickerson JW, Kaplan WA, Attaran A. Is patent “evergreening” restricting access to medicine/device combination products? PLoS One. 2016;11(2):e0148939.
- Yin N. Pharmaceuticals, incremental innovation and market exclusivity. New Orleans: Tulane University: Department of Economics and the Murphy Institute; 2015.
- Hao J, Rodriguez-Monguio R, Seoane-Vazquez E. Fixed-dose combination drug approvals, patents and market exclusivities compared to single active ingredient pharmaceuticals. PLoS One. 2015;10(10):e0140708.
- Moir HVJ. Exploring evergreening: insights from two medicines. Aust Econ Rev. 2016;49(4):413–31.
- Sampat BN, Shadlen KC. Secondary pharmaceutical patenting: a global perspective. NBER Work Pap Ser. 2017;46:693–707.
- Sampat BN, Shadlen KC. TRIPS implementation and secondary pharmaceutical patenting in Brazil and India. Stud Comp Int Dev. 2015;50(2):228–57.
- Kapczynski A, Sampat BN, Shadlen KC. Trade agreements, patents, and drug prices: continuing the debate. Yale Law Economics Res Paper. 2017:572. Available at SSRN: https://ssrn.com/abstract=2933574, https://doi.org/10.2139/ssrn.2933574.
- National Academies of Sciences E, Medicine. Making medicines affordable: a national imperative. Washington, DC: National Academies Press; 2018.
- Gupta R. Patent and access to drugs – myths and realities. In: 5th East-West Center international graduate student conference. Honolulu: East West Centre; 2006.
- Pecoul B, Chirac P, Trouiller P, Pinel J. Access to essential drugs in poor countries: a lost battle? JAMA. 1999;281(4):361–7.
- World Trade Organization. FACT SHEET: TRIPS AND PHARMACEUTICAL PATENTS. Developing countries’ transition periods. 2006. Available from: https://www.wto.org/english/tratop_e/trips_e/factsheet_pharm04_e.htm. Cited 2021 3rd Feb 2021.
- Waning B, Diedrichsen E, Moon S. A lifeline to treatment: the role of Indian generic manufacturers in supplying antiretroviral medicines to developing countries. J Int AIDS Soc. 2010;13(1):1–9.
- Drahos P. “Trust me”: patent offices in developing countries. Am J Law Med. 2008;34(2-3):151–74.
- Lima J. Global health and Brazilian foreign policy: the negotiations on innovation and intellectual property. Cien Saude Colet. 2017;22(7):2213–21.
- The World Health Organization. The Doha Declaration on the TRIPS Agreement and Public Health. 2021. Available from: https://www.who.int/medicines/areas/policy/doha_declaration/en/. Cited 2021 2nd Feb 2021.
- Trachtenberg D, Kaplan WA, Wirtz VJ, Gallagher K. Trade treaties and access to medicines: what does the evidence tell us? GEGI Policy Brief. 2019;6:1–8.
- Thrasher RD, Wirtz VJ, Kaplan W, Gallagher KP, Werk H. Rethinking trade treaties and access to medicines by the working group on trade, investment treaties, and access to medicines. Boston: Boston University; 2019.
Muy bueno!!
Me gustaMe gusta