Yin Liu1; Xiaoli Guo, PhD1; Ranran Qie, PhD1
JAMA Netw Abierto 20 de marzo de 2026 2026;9;(3):e261913. doi:10.1001/jamanetworkopen.2026.1913
Pregunta: ¿Cuál es la relación entre el estado de tabaquismo, los paquetes-año y la duración del abandono del hábito con el riesgo de cáncer de pulmón a largo plazo después de obtener resultados negativos en la tomografía computarizada de baja dosis (TCBD) inicial?
Hallazgos En este estudio de cohorte de 30 565 participantes con resultados negativos en la tomografía computarizada de baja dosis (TCBD) inicial, los fumadores, especialmente aquellos con un historial de tabaquismo de 20 paquetes-año o más, tuvieron un riesgo de cáncer de pulmón significativamente mayor que los no fumadores al tercer año después de la detección inicial, con una mayor susceptibilidad en las mujeres y sin una reducción significativa del riesgo con el abandono del hábito a corto plazo (<15 años).
Significado: Estos hallazgos sugieren que es conveniente ampliar el intervalo de detección inicial e implementar un seguimiento personalizado a largo plazo basado en el historial de tabaquismo.
Abstract
Importancia El cáncer de pulmón (CP) sigue siendo la principal causa de mortalidad relacionada con el cáncer en todo el mundo, siendo el tabaquismo el principal factor de riesgo. Sin embargo, el riesgo de CP a largo plazo entre las personas con resultados negativos en la tomografía computarizada de baja dosis (TCBD) y el papel del tabaquismo en la estratificación del riesgo aún no se comprenden del todo, lo que limita la elaboración de guías basadas en la evidencia para los intervalos de cribado posteriores.
Objetivo : Evaluar la asociación entre el tabaquismo y el riesgo de cáncer de pulmón a largo plazo tras un resultado negativo en la tomografía computarizada de baja dosis inicial, y proporcionar información para optimizar las estrategias de cribado.
Diseño, entorno y participantes Este estudio de cohorte prospectivo, basado en la población, se llevó a cabo en el marco del Programa de Detección de Cáncer en la China urbana. Se incluyeron personas de entre 40 y 74 años con resultados negativos en la tomografía computarizada de baja dosis (TCBD) inicial (del 1 de octubre de 2013 al 31 de diciembre de 2021), con seguimiento hasta diciembre de 2023. Se realizó un seguimiento de todos los participantes para detectar la incidencia de cáncer de pulmón.
Variables de exposición: Estado de fumador autoinformado, años-paquete y tiempo transcurrido desde que dejó de fumar.
Principales resultados y medidas El resultado principal fue la incidencia de cáncer de pulmón, analizada mediante los métodos de Kaplan-Meier y modelos de regresión de riesgos proporcionales de Cox multivariables. Se evaluó la asociación entre la exposición al tabaquismo y el riesgo de cáncer de pulmón, mediante análisis estratificados por tiempo y asociaciones dosis-respuesta.
Resultados Entre 30 565 participantes (14 761 no fumadores y 15 804 fumadores; edad media [DE], 57,1 [7,7] años; 15 693 [51,3%] mujeres), se produjeron 76 casos de LC durante 139 011,51 personas-año (tasa de incidencia bruta, 54,67 por 100 000 personas-año). Los fumadores tuvieron un mayor riesgo de LC que los no fumadores (cociente de riesgos ajustado [CRA], 2,73; IC del 95%, 1,49-5,01), impulsado por aquellos con un historial de tabaquismo de 20 paquetes-año o más (por ejemplo, ≥30 paquetes-año: CRA, 3,22; IC del 95%, 1,85-5,58). No se observó un riesgo elevado a los 2 años (AHR, 2,07; IC del 95 %, 0,91-4,69), pero el riesgo aumentó significativamente a los 3 años (AHR, 2,54; IC del 95 %, 1,19-5,41) y posteriormente. Se encontró una asociación dosis-respuesta no lineal entre los paquetes-año y el riesgo de cáncer de pulmón, con un riesgo que superó los umbrales clínicamente relevantes a partir de los 20 paquetes-año (p. ej., de 20 a <30 paquetes-año: AHR, 2,48; IC del 95 %, 1,14-5,40). Las mujeres mostraron una mayor susceptibilidad que los hombres con una exposición comparable (≥30 paquetes-año: AHR, 5,78 [IC del 95 %, 1,87-17,83] para mujeres frente a 1,36 [IC del 95 %, 0,18-10,39] para hombres). Se observó un riesgo significativo en personas de 50 a 54 años (≥30 paquetes-año) y de 55 a 74 años (≥20 paquetes-año). El abandono del tabaquismo a corto plazo (<15 años) no se asoció significativamente con una reducción del riesgo de cáncer de pulmón.
Conclusiones y relevancia: En este estudio de cohortes, los fumadores con resultados negativos en la tomografía computarizada de baja dosis (TCBD) basal mostraron un riesgo de cáncer de pulmón a largo plazo considerablemente elevado, que solo se hizo significativo dos años después de la detección. Estos hallazgos respaldan la ampliación del intervalo de detección inicial y la implementación de un seguimiento personalizado a largo plazo basado en el historial de tabaquismo.
En síntesis, el presente estudio de cohorte prospectivo proporciona evidencia sólida sobre la relevancia de la vigilancia a largo plazo en personas con TCBD basal negativa, especialmente en aquellas fumadoras y en subgrupos con exposiciones específicas, como mujeres expuestas a humos de cocina. Los resultados destacan la necesidad de ajustar los criterios de detección, incorporando factores de riesgo adicionales más allá del tabaquismo, así como la conveniencia de intervalos de cribado extendidos para optimizar la eficacia y reducir diagnósticos en etapas avanzadas. Asimismo, la estratificación por edad y sexo se presenta como elemento crucial para la adecuada asignación de recursos y la prevención del cáncer de pulmón. Se recomienda la integración de biomarcadores objetivos y la ampliación de investigaciones en cohortes diversas, a fin de validar estos hallazgos y perfeccionar las guías de detección y estrategias de control del tabaquismo en distintas poblaciones.
Introducción
El cáncer de pulmón (CP) es la principal causa de mortalidad relacionada con el cáncer a nivel mundial, con un estimado de 1,8 millones de muertes anuales. 1 En China, se estima que ocurrieron 733 291 muertes por CP en 2022, lo que representa el 40,3 % del total mundial de muertes por CP. 2 Se ha determinado que la detección mediante tomografía computarizada de baja dosis (TCBD) mejora la detección temprana y reduce la mortalidad entre las poblaciones de alto riesgo. 3 , 4 Sin embargo, aproximadamente el 80 % de las pruebas de detección iniciales arrojan resultados negativos, incluso entre individuos con alto riesgo de CP, 3 , 5 , 6 dejando una gran cohorte cuyas trayectorias de riesgo de CP a largo plazo siguen sin estar claras.
El tabaquismo sigue siendo la causa predominante de cáncer de pulmón (CP), contribuyendo al 80% al 90% de los casos a nivel mundial. 7 Si bien la relación dosis-respuesta entre la exposición al tabaco y el riesgo de CP está bien establecida, 8 , 9 aún no se comprende bien cómo la exposición al tabaco se asocia con el riesgo posterior de CP tras resultados negativos en la tomografía computarizada de baja dosis (TCBD). Esto se agrava por el hecho de que, a pesar de los avances en nuestra comprensión del cáncer de pulmón, existe una notable falta de consenso en la comunidad médica sobre cómo abordar la vigilancia y el seguimiento a largo plazo de los pacientes que han dejado de fumar. Aunque el Ensayo Nacional de Detección de Cáncer de Pulmón (NDCT) informó una menor incidencia de CP entre fumadores empedernidos con un resultado negativo en la prueba de detección inicial, 10 no logró cuantificar cómo el tabaquismo influye en el riesgo de CP a lo largo del tiempo, lo que genera incertidumbre sobre la duración y los métodos óptimos para la vigilancia post-detención. Esta laguna dificulta la adaptación de los intervalos de vigilancia basada en la evidencia, ya que las pautas actuales no ofrecen una orientación clara sobre el tiempo necesario para que el riesgo de CP disminuya significativamente después de dejar de fumar, lo que podría llevar a una planificación inapropiada de los cuidados a largo plazo para los exfumadores.
Las guías clínicas reflejan aún más esta incertidumbre, mostrando una variabilidad sustancial en las recomendaciones de detección mediante LDCT. 11 Por ejemplo, la guía de 2021 del Grupo de Trabajo de Servicios Preventivos de los Estados Unidos (USPSTF) recomienda la detección en personas de 50 a 80 años con un historial de tabaquismo de 20 paquetes-año o más que actualmente fuman o dejaron de fumar en los últimos 15 años. 12 En China, la guía de 2021 se dirigió a personas de 50 a 74 años con un historial de tabaquismo de 30 paquetes-año o más, 13 mientras que la actualización de 2024 redujo el umbral a 20 paquetes-año o más, 14 lo que pone de relieve el debate en curso sobre la elegibilidad óptima. Además, aunque la detección anual se recomienda comúnmente, la evidencia sugiere que extender el intervalo puede mejorar la rentabilidad sin comprometer los resultados. 15-17 La integración del abandono del tabaquismo en los programas de detección también mejora la rentabilidad, 18 , 19 pero la duración necesaria del abandono para una reducción significativa del riesgo sigue sin estar clara. Por lo tanto, se necesitan urgentemente estudios poblacionales para fundamentar el perfeccionamiento de las directrices.
Para abordar esta laguna de conocimiento, examinamos la asociación entre la exposición al tabaquismo (estado, años-paquete y abandono del hábito) y la incidencia de cáncer de pulmón en individuos con resultados negativos en la tomografía computarizada de baja dosis (TCBD), y caracterizamos la evolución temporal del riesgo de cáncer de pulmón tras dichos resultados. Este estudio tuvo como objetivo generar evidencia práctica para perfeccionar las guías de detección mediante TCBD y orientar estrategias de control del tabaquismo dirigidas a esta población poco estudiada.
Métodos
Diseño del estudio y participantes
Este estudio de cohorte prospectivo, basado en la población, se llevó a cabo en el marco del Programa de Detección de Cáncer en Zonas Urbanas de China (CanSPUC). El programa está dirigido a residentes de entre 40 y 74 años, centrándose en los cinco tipos de cáncer más prevalentes (cáncer de pulmón, cáncer de mama femenino, cáncer de hígado, cáncer del tracto gastrointestinal superior y cáncer colorrectal) en las zonas urbanas de China. Se han publicado previamente descripciones detalladas del CanSPUC.²⁰ El estudio fue aprobado por el comité de ética del Hospital Oncológico de Henan. Se obtuvo el consentimiento informado por escrito de todos los participantes. El estudio siguió las directrices STROBE (Fortalecimiento de la Notificación de Estudios Observacionales en Epidemiología ) .²¹
Brevemente, los participantes completaron un cuestionario autoadministrado al inicio para evaluar la exposición a factores de riesgo y cuantificar el riesgo de cáncer con base en un sistema de puntuación derivado del Índice de Riesgo de Cáncer de Harvard por el Centro Nacional del Cáncer. Los detalles sobre el sistema de puntuación se han publicado en otra parte. 22 Solo aquellos identificados como de alto riesgo de LC fueron remitidos para LDCT complementaria en hospitales designados. La LDCT se realizó utilizando un escáner CT multidetector de 16 cortes (LightSpeed-16, GE Healthcare). Según el protocolo CanSPUC, 23 los hallazgos positivos de TC basales se definieron como (1) nódulos sólidos o parcialmente sólidos con un diámetro medio mayor de 5 mm, (2) nódulos no sólidos con un diámetro mayor de 8 mm, (3) nódulos luminales traqueales, (4) patología de las vías respiratorias que requiere biopsia bronquial y (5) LC sospechada o confirmada. Los participantes que no cumplieron con ninguno de estos criterios de evaluación positiva se definieron como con un hallazgo negativo. El proceso de selección de participantes se describe en la Figura 1 . De los 31 799 individuos con resultados negativos en la TC de baja dosis inicial, 1208 (3,8 %) no estaban disponibles para el seguimiento, y sus características iniciales eran en general similares a las de los que se mantuvieron (Tabla electrónica 1 en el Suplemento 1 ).
CanSPUC significa Programa de Detección de Cáncer en la China Urbana; LC, cáncer de pulmón; LDCT, tomografía computarizada de baja dosis.
Este análisis utilizó datos de CanSPUC de 8 ciudades de la provincia de Henan (Zhengzhou, Anyang, Luoyang, Nanyang, Zhumadian, Puyang y Xinxiang) entre el 1 de octubre de 2013 y el 31 de diciembre de 2021. Se incluyeron individuos con resultados negativos en la tomografía computarizada de baja dosis (TCBD) basal. También se excluyeron aquellos que no estaban disponibles para el seguimiento, que tenían antecedentes de cáncer y aquellos diagnosticados con cáncer de pulmón dentro de los 6 meses posteriores al seguimiento.
Definición de parámetros de exposición al tabaquismo
Los datos sobre el estado de tabaquismo (nunca fumador o fumador), los paquetes-año y el tiempo transcurrido desde que dejó de fumar se recopilaron mediante autoinforme al inicio del estudio. Se definió como fumador a la persona con antecedentes de tabaquismo diario actual o anterior (≥1 cigarrillo diario durante >6 meses). Se registró el consumo diario de cigarrillos y la duración del tabaquismo (años). La duración del tabaquismo se calculó desde el inicio hasta la edad de abandono (exfumadores) o la edad basal (fumadores actuales). Los paquetes-año se calcularon como el número de paquetes (20 cigarrillos) por día multiplicado por la duración del tabaquismo (años). A los no fumadores se les asignó 0 paquetes-año, mientras que los fumadores se estratificaron en menos de 20, de 20 a menos de 30 y 30 o más paquetes-año. Para los exfumadores, el tiempo transcurrido desde que dejaron de fumar se categorizó como menos de 5, de 5 a menos de 15 o 15 o más años.
Definición de covariables
Se evaluaron trece covariables potenciales asociadas con el riesgo de LC 13 , 24 y se categorizaron en 5 dominios: (1) factores sociodemográficos: edad, sexo, nivel educativo y antecedentes familiares de LC en parientes de primer grado (padres o hermanos); (2) factores conductuales: actividad física (categorizada como intensa [ejercicio ≥3 días/semana y >90 min/semana] o moderada/ninguna) y consumo de alcohol (clasificado como alguna vez/actual [semanal o más durante >1 año] o nunca); (3) antecedentes de enfermedades respiratorias crónicas: presencia (sí) o ausencia (no) de afecciones como enfermedad pulmonar obstructiva crónica, enfisema, silicosis, neumoconiosis o tuberculosis; (4) exposiciones ocupacionales o ambientales: exposición ocupacional a sustancias peligrosas durante al menos 1 año (no o sí), exposición al humo de segunda mano (no o sí), combustible sólido utilizado para calefacción en invierno (no o sí), combustible sólido utilizado para cocinar (no o sí) y exposición al humo del aceite de cocina (ninguna o poca o mucha); y (5) factores de riesgo metabólico: índice de masa corporal (IMC), calculado como el peso en kilogramos dividido por el cuadrado de la altura en metros, con un IMC alto definido como 24 o más según los criterios chinos. 25 Para el dominio de exposición ocupacional o ambiental, las sustancias peligrosas abarcaron asbesto, radón, berilio, uranio, cromo, cadmio, níquel, silicio, gases de escape diésel, humo de carbón y ceniza de carbón. El humo de segunda mano se definió como la inhalación involuntaria de humo de tabaco en el hogar o el entorno laboral durante más de 20 años. El combustible sólido incluyó madera, carbón, estiércol animal y residuos de cultivos. La exposición a los humos del aceite de cocina se clasificó según la tecnología de cocción utilizada: una exposición nula o escasa indicaba el uso de chimeneas, extractores de humos o ollas sin humo durante la cocción, mientras que una exposición elevada indicaba su ausencia.
Seguimiento y determinación de los resultados
El resultado principal fue la incidencia de cáncer de pulmón, codificado como C34 según la Clasificación Estadística Internacional de Enfermedades y Problemas de Salud Relacionados, Décima Revisión (CIE-10) . Las personas con resultados negativos en la tomografía computarizada de baja dosis (TCBD) inicial no fueron incluidas en la vigilancia activa dentro del propio CanSPUC. Para reflejar los patrones de diagnóstico reales tras un resultado negativo en la prueba de detección, se implementó una combinación de enfoques de seguimiento pasivo y activo.
El seguimiento pasivo se realizó mediante la vinculación de datos con el Registro Provincial de Cáncer de Henan (HPCR). El HPCR agrega informes de registros a nivel de condado, hospitales, centros de salud comunitarios y una red de médicos de tres niveles, complementados con bases de datos de seguros de salud y estadísticas vitales. La calidad de los datos del HPCR se adhiere a los estándares nacionales 26 e internacionales 27 ; sus procedimientos detallados se han descrito en otra parte. 28 El seguimiento activo se realizó por teléfono o visitas domiciliarias por médicos del proyecto, coordinadores locales y personal de CanSPUC para verificar los resultados del cáncer, incluyendo la fecha de diagnóstico, el estadio y la muerte relacionada con el cáncer. Este enfoque dual aseguró la captura de todos los casos incidentes de LC independientemente del contexto clínico (por ejemplo, detectados a través de síntomas, chequeos de salud de rutina o investigaciones para otras afecciones), reflejando así la práctica diagnóstica real posterior al cribado.
Análisis estadístico
Las características basales se presentaron como número (porcentaje) para las variables categóricas y media (DE) o mediana (RIC) para las variables continuas. En la estimación de la incidencia de LC, los años-persona de seguimiento se calcularon desde la fecha de la LDCT basal hasta la fecha del diagnóstico de LC, muerte o censura (diciembre de 2023), lo que ocurriera primero. La incidencia acumulada se estimó mediante el método de Kaplan-Meier. Se utilizaron modelos de regresión de riesgos proporcionales de Cox multivariables para estimar las asociaciones entre la exposición al tabaquismo (estado, paquetes-año y tiempo desde que dejó de fumar) y el riesgo de LC, ajustando por covariables. El supuesto de riesgos proporcionales se verificó globalmente y para las covariables utilizando los residuos de Schoenfeld (todos los P > 0,05; no se detectaron violaciones). Se informaron las razones de riesgo brutas y ajustadas (RRA) con IC del 95 %. Se examinó la relación dosis-respuesta entre los años de tabaquismo y el riesgo de cáncer de pulmón mediante splines cúbicos restringidos (RCS) con nodos en 0, 20 y 30 años de tabaquismo, lo que refleja las directrices de cribado actuales. 12 , 13 , 29
Se ajustaron modelos de regresión de riesgos proporcionales de Cox estratificados por tiempo mediante intervalos anuales (años 1-5) para alinearlos con las guías de detección y evaluar las tendencias temporales en el riesgo de cáncer de pulmón. Se realizaron análisis de subgrupos por sexo y grupo de edad (40-49, 50-54 y 55-74 años) para explorar la heterogeneidad de la asociación. Los análisis estratificados por tiempo no se extendieron a los subgrupos debido a la limitada potencia estadística.
Se realizaron tres análisis de sensibilidad: (1) exclusión de participantes con menos de 3 años de seguimiento (n = 9610) para reducir el sesgo de enfermedad subclínica, (2) consideración del riesgo competitivo de mortalidad por todas las causas mediante modelos de riesgo de subdistribución, y (3) ajuste de un modelo parsimonioso ajustado únicamente por edad, sexo, antecedentes familiares de LC en parientes de primer grado y antecedentes de enfermedades respiratorias crónicas para reducir el posible sobreajuste. Todos los análisis se realizaron con el software R, versión 4.3.0 (R Foundation for Statistical Computing). Se consideró estadísticamente significativo un valor de p bilateral < 0,05.
Resultados
La cohorte final incluyó a 30 565 individuos (edad media [DE], 57,1 [7,7] años; 15 693 [51,3%] mujeres), compuesta por 14 761 no fumadores y 15 804 fumadores (1534 exfumadores y 14 270 fumadores actuales). Las características basales estratificadas por estado de tabaquismo y paquetes-año se resumen en la Tabla y la Tabla electrónica 2 en el Suplemento 1 , respectivamente. En comparación con los no fumadores, los fumadores eran más jóvenes y predominantemente hombres, tenían tasas más bajas de antecedentes familiares de cáncer de pulmón de primer grado, tenían niveles educativos más altos y tenían una mayor prevalencia de consumo de alcohol alguna vez o actual. Los fumadores también informaron una mayor exposición a riesgos laborales, una menor prevalencia de enfermedades respiratorias crónicas, un mayor uso de combustibles sólidos para calefacción y cocina, una menor exposición a humos de aceite de cocina y tasas más altas de IMC alto.
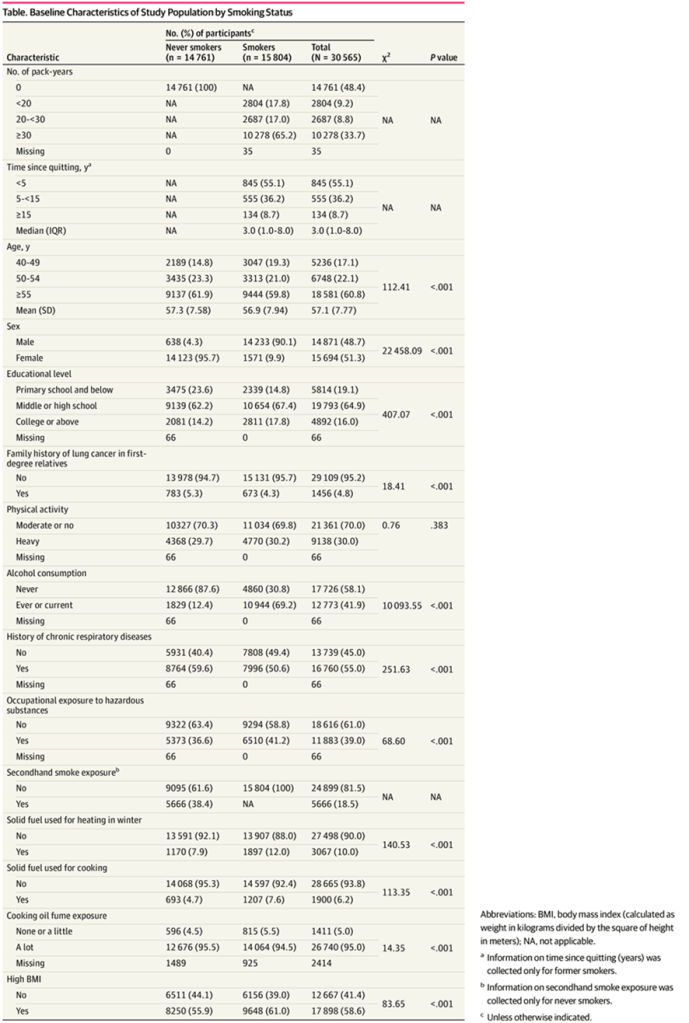
Tabla. Características basales de la población de estudio según el estado de tabaquismo.
| Característica | N.º (%) de participantes c | χ 2 | PAGvalor | ||
| Nunca fumadores (n = 14 761) | Fumadores (n = 15 804) | Total (N = 30 565) | |||
| Número de paquetes-año | |||||
| 0 | 14 761 (100) | N / A | 14 761 (48,4) | N / A | N / A |
| <20 | N / A | 2804 (17.8) | 2804 (9.2) | ||
| 20-<30 | N / A | 2687 (17.0) | 2687 (8.8) | ||
| ≥30 | N / A | 10 278 (65.2) | 10 278 (33,7) | ||
| Desaparecido | 0 | 35 | 35 | ||
| Tiempo desde que lo dejé, y a | |||||
| <5 | N / A | 845 (55.1) | 845 (55.1) | N / A | N / A |
| 5-<15 | N / A | 555 (36,2) | 555 (36,2) | ||
| ≥15 | N / A | 134 (8.7) | 134 (8.7) | ||
| Mediana (RIC) | N / A | 3.0 (1.0-8.0) | 3.0 (1.0-8.0) | ||
| Edad, y | |||||
| 40-49 | 2189 (14.8) | 3047 (19.3) | 5236 (17.1) | 112.41 | <.001 |
| 50-54 | 3435 (23.3) | 3313 (21.0) | 6748 (22.1) | ||
| ≥55 | 9137 (61.9) | 9444 (59.8) | 18 581 (60,8) | ||
| Media (DE) | 57,3 (7,58) | 56,9 (7,94) | 57.1 (7.77) | ||
| Sexo | |||||
| Masculino | 638 (4.3) | 14 233 (90.1) | 14 871 (48,7) | 22 458,09 | <.001 |
| Femenino | 14 123 (95,7) | 1571 (9.9) | 15 694 (51,3) | ||
| Nivel educativo | |||||
| Escuela primaria y niveles inferiores | 3475 (23,6) | 2339 (14.8) | 5814 (19.1) | 407.07 | <.001 |
| escuela secundaria o preparatoria | 9139 (62.2) | 10 654 (67,4) | 19 793 (64,9) | ||
| Universidad o superior | 2081 (14.2) | 2811 (17.8) | 4892 (16.0) | ||
| Desaparecido | 66 | 0 | 66 | ||
| Antecedentes familiares de cáncer de pulmón en parientes de primer grado. | |||||
| No | 13 978 (94,7) | 15 131 (95,7) | 29 109 (95.2) | 18.41 | <.001 |
| Sí | 783 (5.3) | 673 (4.3) | 1456 (4.8) | ||
| Actividad física | |||||
| Moderado o no | 10327 (70.3) | 11 034 (69.8) | 21 361 (70.0) | 0,76 | .383 |
| Pesado | 4368 (29,7) | 4770 (30.2) | 9138 (30.0) | ||
| Desaparecido | 66 | 0 | 66 | ||
| Consumo de alcohol | |||||
| Nunca | 12 866 (87,6) | 4860 (30.8) | 17 726 (58.1) | 10 093.55 | <.001 |
| Alguna vez o actualmente | 1829 (12.4) | 10 944 (69,2) | 12 773 (41,9) | ||
| Desaparecido | 66 | 0 | 66 | ||
| Antecedentes de enfermedades respiratorias crónicas | |||||
| No | 5931 (40.4) | 7808 (49.4) | 13 739 (45.0) | 251,63 | <.001 |
| Sí | 8764 (59.6) | 7996 (50.6) | 16 760 (55.0) | ||
| Desaparecido | 66 | 0 | 66 | ||
| Exposición laboral a sustancias peligrosas | |||||
| No | 9322 (63.4) | 9294 (58.8) | 18 616 (61.0) | 68,60 | <.001 |
| Sí | 5373 (36,6) | 6510 (41.2) | 11 883 (39.0) | ||
| Desaparecido | 66 | 0 | 66 | ||
| Exposición al humo de segunda mano b | |||||
| No | 9095 (61,6) | 15 804 (100) | 24 899 (81,5) | N / A | N / A |
| Sí | 5666 (38.4) | N / A | 5666 (18.5) | ||
| Combustible sólido utilizado para calefacción en invierno | |||||
| No | 13 591 (92.1) | 13 907 (88.0) | 27 498 (90.0) | 140,53 | <.001 |
| Sí | 1170 (7.9) | 1897 (12.0) | 3067 (10.0) | ||
| Combustible sólido utilizado para cocinar | |||||
| No | 14 068 (95.3) | 14 597 (92,4) | 28 665 (93,8) | 113,35 | <.001 |
| Sí | 693 (4,7) | 1207 (7.6) | 1900 (6.2) | ||
| Exposición a los vapores del aceite de cocina | |||||
| Ninguno o un poco | 596 (4.5) | 815 (5.5) | 1411 (5.0) | 14.35 | <.001 |
| Mucho | 12 676 (95,5) | 14 064 (94,5) | 26 740 (95,0) | ||
| Desaparecido | 1489 | 925 | 2414 | ||
| IMC elevado | |||||
| No | 6511 (44.1) | 6156 (39.0) | 12 667 (41,4) | 83,65 | <.001 |
| Sí | 8250 (55.9) | 9648 (61.0) | 17 898 (58,6) | ||
La mediana (RIC) de seguimiento fue de 4,35 (2,56-6,22) años para toda la cohorte, 3,86 (2,26-5,98) años para los no fumadores y 4,63 (3,23-6,42) años para los fumadores. Para los participantes con menos de 20, de 20 a menos de 30 y 30 o más paquetes-año, la mediana (RIC) de seguimiento fue de 5,39 (4,19-7,09), 5,10 (4,22-6,95) y 4,34 (2,43-5,91) años, respectivamente. Durante un total de 139 011,51 personas-año, se identificaron 76 casos incidentes de LC, lo que arroja una tasa de incidencia bruta de 54,67 por 100 000 personas-año. Las características de los casos de cáncer de pulmón se detallan en la Tabla electrónica 3 del Suplemento 1. De ellos, 20 se presentaron en personas no fumadoras y 56 en fumadoras. Las personas no fumadoras eran predominantemente mujeres (19 de 20 [95,0%]). Los diagnósticos en etapas tempranas (etapas I-II) representaron el 48,2% de los casos en fumadores y el 45,0% en personas no fumadoras.
Las asociaciones entre el tabaquismo y el riesgo de LC después de un hallazgo basal negativo se muestran en la Figura 2. Todas las covariables cumplieron el supuesto de riesgos proporcionales. Después del ajuste multivariable, los fumadores mostraron un mayor riesgo de LC que los no fumadores (AHR, 2,73; IC del 95 %, 1,49-5,01). Los análisis estratificados por tiempo no indicaron un aumento significativo del riesgo durante los primeros 2 años (año 1 AHR, 1,81; IC del 95 %, 0,54-6,08; año 2 AHR, 2,07; IC del 95 %, 0,91-4,69), pero el riesgo aumentó significativamente a partir del año 3 (AHR, 2,54; IC del 95 %, 1,19-5,41) en adelante, con un HR que se estabilizó en aproximadamente 2,7 para el año 5 (AHR, 2,70; IC del 95 %, 1,41-5,18) ( Figura 2 A). Cuando se analizó por paquetes-año, se observaron riesgos significativamente elevados solo entre aquellos con un historial de tabaquismo de 20 paquetes-año o más (20 a <30 paquetes-año: AHR, 2,48; IC del 95 %, 1,14-5,40; ≥30 paquetes-año: AHR, 3,22; IC del 95 %, 1,85-5,58). Los patrones estratificados por tiempo fueron consistentes con los del estado de tabaquismo. Las curvas de incidencia acumulada confirmaron este patrón, con curvas superpuestas en los primeros 2 años y divergencia significativa a partir de entonces ( Figura 3 ). El análisis RCS reveló una asociación no lineal significativa entre los paquetes-año de tabaquismo y la incidencia de LC (χ 2 3 = 11,78, P = ,008), con un riesgo que aumenta notablemente más allá de los 20 paquetes-año y se estabiliza en exposiciones altas ( Figura 4 ).
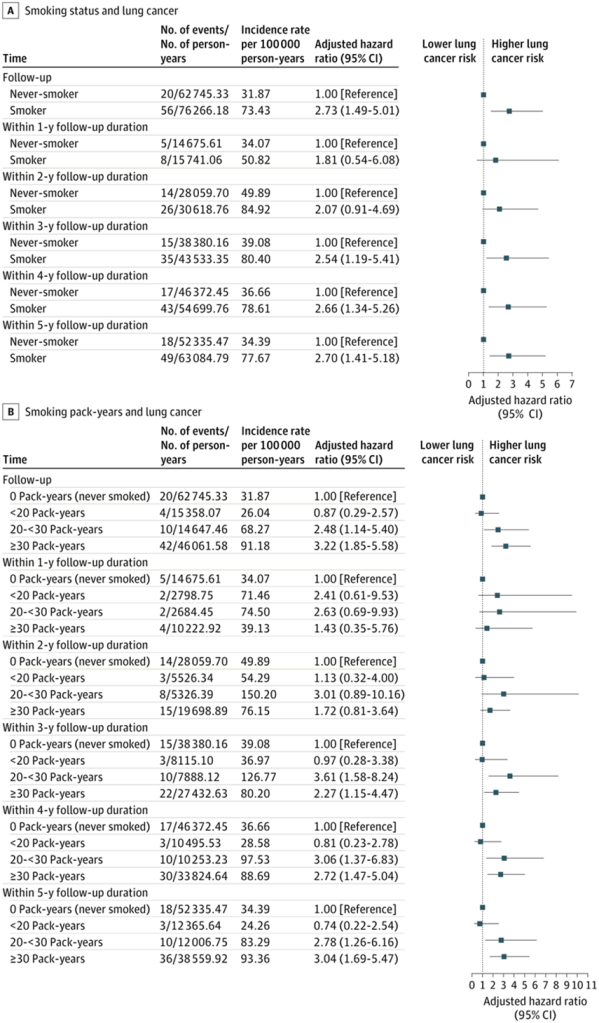
Figura 2. Gráfico de bosque de la asociación entre el tabaquismo y el riesgo de cáncer de pulmón según la duración del seguimiento después de hallazgos negativos en la tomografía computarizada de baja dosis inicial
Las barras de error indican intervalos de confianza del 95%.
Figura 3. Gráficos de supervivencia de la incidencia acumulada de cáncer de pulmón después de resultados negativos en la tomografía computarizada de baja dosis inicial.
Figura 4. Gráfico lineal de la relación dosis-respuesta entre los años de tabaquismo (en paquetes) y el riesgo de cáncer de pulmón.
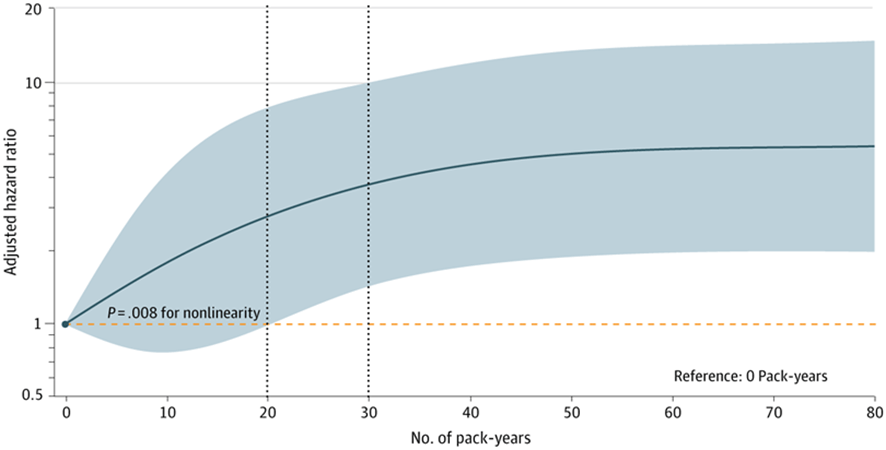
El área sombreada indica los intervalos de confianza del 95%; la línea horizontal discontinua representa la razón de riesgo de referencia de 1; las líneas verticales discontinuas representan los nodos de spline cúbico restringido.
El análisis de subgrupos específicos por sexo indicó una asociación más fuerte entre el tabaquismo y la incidencia de LC entre las mujeres en niveles de exposición comparables. Específicamente, las mujeres con un historial de tabaquismo de 30 paquetes-año o más tuvieron un riesgo marcadamente mayor (AHR, 5,78; IC del 95 %, 1,87-17,83) que los hombres con una exposición similar (AHR, 1,36; IC del 95 %, 0,18-10,39). El análisis específico por edad mostró un riesgo significativamente mayor en un historial de tabaquismo de 20 paquetes-año o más en participantes de 55 a 74 años, mientras que no se observó un aumento de riesgo estadísticamente significativo en un historial de tabaquismo de 30 paquetes-año o más en aquellos de 50 a 54 años (tablas electrónicas 4 y 5 en el Suplemento 1 ). Los análisis de sensibilidad respaldaron estos hallazgos (tablas electrónicas 6-17 en el Suplemento 1 ).
Entre 1534 exfumadores, se produjeron 3 casos de LC (tasa de incidencia, 43,35 por 100 000 personas-año), y todos los participantes tenían un historial de tabaquismo de 30 paquetes-año o más y menos de 15 años de abstinencia. En comparación con los fumadores actuales, una menor duración de la abstinencia (<15 años) no se asoció con una reducción significativa del riesgo de LC (Tabla electrónica 18 en el Suplemento 1 ). Los análisis de sensibilidad arrojaron resultados consistentes (Tablas electrónicas 19-21 en el Suplemento 1 ).
Discusión
Hasta donde sabemos, este es el primer estudio de cohorte prospectivo de base poblacional que caracteriza exhaustivamente el riesgo de cáncer de pulmón a largo plazo entre individuos con resultados negativos en la tomografía computarizada de baja dosis (TCBD) basal, con especial atención a la exposición al tabaco. Observamos un riesgo de cáncer de pulmón significativamente elevado en fumadores, particularmente en aquellos con 20 paquetes-año o más de exposición acumulada al tabaco, pero este riesgo no fue estadísticamente significativo dentro de los 2 años posteriores a la detección. El abandono del tabaquismo a corto plazo no mitigó el riesgo de cáncer de pulmón a largo plazo entre individuos con alta exposición. También identificamos un riesgo residual no despreciable en ciertos subgrupos de personas que nunca fumaron. Estos hallazgos cuestionan los paradigmas de detección actuales y proporcionan evidencia práctica para perfeccionar las directrices de la TCBD y las estrategias de control del tabaco.
Este estudio también encontró que una LDCT basal negativa no eliminó el riesgo de LC a largo plazo, lo que subraya la necesidad de una vigilancia continua más allá del cribado inicial. En los análisis estratificados por tiempo, los fumadores no mostraron un aumento estadísticamente significativo del riesgo durante los primeros 2 años después de la LDCT, y la distribución del estadio clínico fue similar entre fumadores y no fumadores. Este patrón temporal se alinea con la latencia biológica de la carcinogénesis inducida por el tabaco en la que las lesiones premalignas probablemente requieren varios años para convertirse en tumores detectables radiológicamente. 30 Estos hallazgos sugieren que el cribado anual dentro de los primeros 2 años ofrece un beneficio limitado y respalda la evaluación de intervalos de cribado extendidos. En vista de la proporción sustancial de diagnósticos en estadio tardío en nuestra cohorte, junto con la evidencia del ensayo NELSON de que un intervalo de 2,5 años se asoció con más cánceres en estadio tardío, 31 un intervalo de cribado bienal parece más aceptable que intervalos más largos para minimizar el riesgo de diagnóstico en estadio tardío y mortalidad. Se necesitan futuros estudios de costo-efectividad para definir el intervalo de vigilancia óptimo.
El análisis RCS reveló una asociación dosis-respuesta no lineal significativa entre los paquetes-año y la incidencia de LC, con un umbral clínicamente relevante de aproximadamente 20 paquetes-año. Este hallazgo respalda empíricamente los umbrales de detección de 20 paquetes-año del USPSTF 12, al tiempo que cuestiona la rigurosidad del criterio de 30 paquetes-año de China. 13 Es importante destacar que este umbral se modificó según la edad. Se observó un aumento significativo del riesgo a partir de 20 paquetes-año en participantes de 55 a 74 años, pero solo a partir de 30 paquetes-año en aquellos de 50 a 54 años. Estos hallazgos resaltan el valor de la estratificación del riesgo específica por edad en las guías de detección para mejorar la eficacia y la asignación de recursos, en particular al reducir potencialmente el umbral de paquetes-año para personas mayores, manteniendo umbrales más altos para grupos de edad más jóvenes.
Aunque estudios previos respaldan la rentabilidad de combinar el cribado con el abandono del tabaquismo, 18 , 19 nuestros datos sugieren que el abandono a corto plazo (<15 años) no redujo significativamente el riesgo de cáncer de pulmón dentro del seguimiento disponible. El número limitado de personas que dejaron de fumar a largo plazo en nuestra cohorte restringe las conclusiones definitivas sobre la reducción del riesgo más allá de los 15 años. Esta observación coincide con la evidencia molecular de que el tabaquismo intenso induce daño genético irreversible 32 y que los exfumadores pueden tardar aproximadamente 22 años en alcanzar perfiles de metilación comparables a los de las personas que nunca han fumado. 33 Por lo tanto, se justifica una vigilancia prolongada para los exfumadores, especialmente aquellos con un historial de tabaquismo sustancial.
Cabe destacar que observamos diferencias significativas basadas en el sexo en el riesgo de LC, con mujeres que mostraron AHR marcadamente más altas con una exposición al tabaquismo comparable. La interpretación de esta diferencia de sexo está limitada por los escasos eventos en el grupo de referencia de hombres no fumadores (solo 1 caso de LC), lo que podría inflar la aparente mayor susceptibilidad en las mujeres. Sin embargo, esta observación fue consistente con informes previos que sugieren una mayor vulnerabilidad femenina a los carcinógenos del tabaco. 34 , 35 Los mecanismos potenciales pueden involucrar la activación mediada por estrógenos de los carcinógenos del tabaco 36 , 37 y la reparación del ADN ligada al cromosoma X. 38 A medida que las tasas de tabaquismo entre las mujeres en países de ingresos bajos y medios continúan aumentando, 39 estos hallazgos subrayan la necesidad de investigación mecanicista sobre las diferencias de sexo en la carcinogénesis pulmonar y respaldan el desarrollo de programas de detección y cesación específicos para cada sexo.
Aunque la detección mediante LDCT está establecida, persisten las preocupaciones sobre los resultados falsos positivos, el sobrediagnóstico y la radiación. 40 Las guías actuales priorizan a los fumadores empedernidos para maximizar la rentabilidad. 41 , 42 Sin embargo, nuestros hallazgos revelan una limitación sustancial de este enfoque centrado únicamente en fumadores. Sorprendentemente, 19 de 20 casos de LC (95%) en personas que nunca fumaron ocurrieron en mujeres, todas con alta exposición a humos de cocina. Este hallazgo coincide con la evidencia de que la detección no basada en el riesgo detecta cánceres en personas no elegibles 43 y que los criterios centrados en fumadores pueden subdiagnosticar a muchas personas en riesgo, en particular a las mujeres chinas (solo el 1,0% elegibles). 44 Por lo tanto, es crucial adoptar criterios de elegibilidad basados en modelos de riesgo que incorporen factores de riesgo no relacionados con el tabaquismo, en lugar de basarse únicamente en el historial de tabaquismo. Los estudios futuros también deberían explorar la integración de biomarcadores de exposición objetivos para refinar la estratificación.
Limitaciones
Este estudio tiene varias limitaciones. Primero, aunque nuestra cohorte urbana china ofrece información para poblaciones de alto riesgo similares, la generalización a áreas rurales o poblaciones con diferentes patrones de tabaquismo puede ser limitada. Segundo, el historial de tabaquismo y el estado de cesación fueron autoinformados y sujetos a sesgos de recuerdo y deseabilidad social. En particular, la subnotificación en mujeres debido al estigma cultural podría haber influido en las estimaciones de diferencias de sexo. Los estudios futuros podrían incorporar biomarcadores objetivos (por ejemplo, cotinina 45 ) para mejorar la evaluación de la exposición. Tercero, el ajuste por múltiples covariables, los factores de confusión no medidos, como la contaminación del aire 46 y los factores genéticos, 47 podrían afectar las estimaciones de riesgo. Cuarto, la potencia estadística limitada en ciertos análisis, particularmente entre exfumadores y en comparaciones de subgrupos, podría haber oscurecido asociaciones sutiles. Por lo tanto, estos hallazgos deben considerarse exploratorios y requieren validación en cohortes más grandes. Quinto, la determinación de casos de LC se basó en datos de registro y seguimiento activo, lo que podría haber pasado por alto casos en etapa temprana o asintomáticos; Sin embargo, es probable que la evaluación uniforme de los resultados haya provocado una clasificación errónea no diferencial, lo que ha dado lugar a estimaciones de asociación conservadoras. Se justifican estudios futuros que incorporen datos de reevaluación mediante LDCT.
Conclusiones
Este amplio estudio de cohorte prospectivo reveló que los resultados negativos de la TCBD basal no proporcionaron una protección uniforme a largo plazo contra el cáncer de pulmón. El tabaquismo intenso (≥20 paquetes-año) se asoció con un riesgo significativamente mayor de cáncer de pulmón, con una latencia biológicamente plausible de 3 años o más. La heterogeneidad del riesgo según la edad y el sexo respaldó la necesidad de estrategias de cribado personalizadas. La limitada reducción del riesgo tras la cesación tabáquica a corto plazo puso de manifiesto la importancia de combinar los programas de cesación tabáquica con el seguimiento a largo plazo mediante TCBD. La aparición de cáncer de pulmón en personas que nunca habían fumado puso de relieve la necesidad de ampliar los criterios de cribado más allá del historial de tabaquismo. La investigación futura debería centrarse en análisis de coste-efectividad de intervalos de cribado más amplios, seguimiento a largo plazo en poblaciones diversas y estudios mecanicistas de las diferencias de sexo para avanzar en la prevención de precisión en personas con resultados negativos en la TCBD.