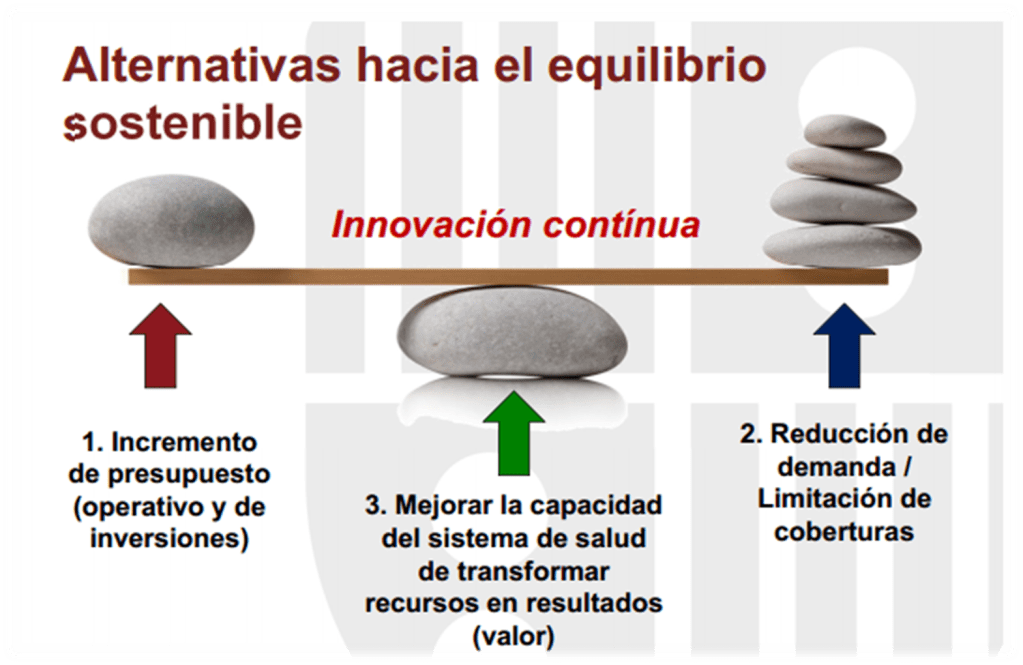
Este artículo de la revista Health Affairs publicado bajo la autoría de Preston Atteberry Peter B. Bach Jennifer A. Ohn Mark R. Trusheim, ofrece una visión interesante del porqué, los medicamentos biológicos, podrían comportarse como monopolios naturales en la visión de la economía de la salud, y analizan, con ejemplos el porqué una política de biosimilares podría fracasar, esto ocurre asimismo, en varios aspectos de la gestión, por la complejidad, por la respuesta de los otros actores como reacción a las modificaciones, por las barreras de ingreso por altos niveles de inversión que exige la producción de los medicamentos biológicos, porque quienes son los que lideran pueden crear su propia competencia, para limitarla al resto, o ceder utilidades para hacer dificultoso el ingreso de otras empresas, esto, está ocurriendo con las insulinas, también, y es lo que vengo postulando en los abordajes de esta semana. Los autores proponen un enfoque basado en lo regulatorio, en estrategias de grandes compradores. Es válido. Pero sería importante tener alternativas, desarrollar capacidades en la fabricación, para mejorar el acceso, especialmente en países pobres, con mercados pequeños. La cantidad de diabéticos crecerán inexorablemente año tras año. Pero por las proyecciones crecerá más el precio y esto afecta las dos variables del PxQ clásico. Esto compromete la sostenibilidad del sistema y especialmente el acceso a los diabéticos para mejorar su calidad de vida. Es un volumen de negocios tan magnífico, que admite, por el lado del crecimiento poblacional y mayor sobrevida, una abordaje de precios diferenciales.
No obstante las observaciones que termina el artículo un sana política de biosimilares, podría en mercados periféricos, en países de ingreso medio bajo, lograr rebajas sustanciales, que mejore la equidad via acceso asequible.
Reflejando que la legislación que facilita la introducción de medicamentos genéricos para competir con los medicamentos de molécula pequeñas, de marca, los legisladores crearon un camino para la aprobación de «biosimilares» para reducir los precios al competir con los biológicos de marca después de que expire su exclusividad en el mercado. Sin embargo, la entrada de biosimilares en el mercado de EE. UU. ha sido lenta, rara y mínimamente efectiva a la hora de reducir los precios. A Europa no le ha ido mucho mejor.
Argumentan que, a diferencia de las moléculas pequeñas a las que se les otorgan monopolios artificiales, los productos biológicos se describen mejor como monopolios naturales.
Están protegidos por barreras de entrada derivadas de la incertidumbre científica que surge de su complejidad estructural; estas barreras son costosas, consumen mucho tiempo y son riesgosas de violar. Por lo tanto, proponemos abandonar el uso de biosimilares a precios más bajos a favor de regulaciones de precios posteriores a la exclusividad en productos biológicos innovadores; los posibles métodos de reducción de precios incluyen el costo incrementado, los márgenes específicos o las tasas de retorno de la inversión.
Este enfoque regulatorio es una mejor manera que los biosimilares para lograr un precio de costo económico marginal no monopólico después de que expire la exclusividad del mercado. Durante un período de cinco años a partir de 2018, en comparación con el enfoque actual, esto podría haber generado entre $250 y $300 mil millones en ahorros netos en los EE.
La primera parte de esta publicación, que se vuelca a continuación, describe las fallas en el intento de usar biosimilares para competir con los biológicos y precios más bajos. La segunda parte presenta un enfoque alternativo propuesto para bajar los precios después de que expire la exclusividad del mercado.
La recompensa de dos partes para la innovación biofarmacéutica
En los Estados Unidos, el sistema de recompensas farmacéuticas tiene dos fases de fijación de precios. La primera fase está diseñada para fomentar la innovación: los gobiernos otorgan monopolios por tiempo limitado a través de patentes y exclusividades regulatorias, lo que permite a las compañías farmacéuticas cobrar precios más altos. Después de este período de monopolio, otras empresas ingresan al mercado y producen el mismo producto, lo que lleva a la competencia y la posterior caída de precios. Idealmente, el precio neto durante este segundo período de competencia entre productos se acerca al costo económico marginal, es decir, el precio al que el productor obtiene una ganancia similar a la que podría obtener en otro mercado competitivo.
Para los medicamentos de molécula pequeña, este sistema de recompensa de dos partes funciona razonablemente bien. Según la Ley Hatch-Waxman de 1984, las empresas innovadoras reciben un mínimo de 5 años de exclusividad reglamentaria para un nuevo medicamento. Las patentes sobre aspectos de esa droga pueden extender la duración del monopolio y hacerlo con frecuencia. Durante el período de monopolio, los medicamentos de molécula pequeña pueden obtener precios más altos que el costo en efectivo por unidad de investigación y fabricación del medicamento. Posteriormente, numerosos competidores genéricos ingresan rápidamente al mercado de la mayoría de los medicamentos de molécula pequeña, lo que reduce los precios, a menudo entre un 85 y un 95 por ciento .
Para productos biológicos, la primera parte de este sistema también parece funcionar bien; las empresas pueden generar ganancias sustanciales. Adalimumab (Humira, Abbvie), el producto biológico de mayor venta en EE. UU., tiene un costo de adquisición mayorista de $57 805 por año y tuvo ventas netas en EE. UU. en 2018 de $13 700 millones .
El incentivo se hace aún más fuerte por el período de exclusividad de doce años que los legisladores han otorgado a los productos biológicos, más del doble del período que disfrutan la mayoría de los medicamentos de molécula pequeña. Las patentes también se utilizan para ampliar aún más el período de monopolio de los productos biológicos.
Sin embargo, la segunda parte del sistema de recompensas no funciona tan bien para los productos biológicos como para los medicamentos de molécula pequeña. Los biosimilares, una categoría de medicamentos creada por la Ley de innovación y competencia de precios biológicos (BPCIA) de 2010, pretenden desempeñar un papel paralelo al papel que desempeñan los medicamentos genéricos con respecto a las moléculas pequeñas innovadoras. Al ingresar al mercado después del período de monopolio, tienen la intención de reducir los precios a través de la competencia.
Pero a diferencia de los medicamentos genéricos, los biosimilares han fracasado en gran medida en este objetivo. Primero, no han ingresado al mercado en grandes cantidades (Anexo 1). La primera presentación de biosimilares no se produjo hasta 2014, aproximadamente dos años después de que la Administración de Alimentos y Medicamentos (FDA) emitiera las primeras regulaciones de biosimilares en 2012. A partir de marzo de 2019, solo se han presentado 29 solicitudes de biosimilares a la FDA, y muchas de ellas esas solicitudes no han tenido éxito: ocho de las 21 sobre las que la FDA ha dictaminado fallaron inicialmente, y solo cinco de ellas han sido aprobadas desde entonces. Del total de 18 biosimilares aprobados por la FDA, diez siguen sin comercializarse(Anexo 2). Para la mayoría de los productos biológicos que ya han superado el final del período de monopolio o están a punto de hacerlo, no hay solicitudes de biosimilares pendientes.
En aquellos casos en los que se han introducido biosimilares, la competencia ha sido escasa y las reducciones de precios modestas. La entrada de dos filgrastim de la competencia (uno de los cuales era un biosimilar regido por BPCIA) en 2013 y 2015 en el mercado de filgrastim de marca (Neupogen) de $1100 millones simplemente aplanó la trayectoria de precios de Neupogen (Anexo 3), pero a partir del primer trimestre de 2018 , Neupogen aún conservaba la mayor parte del mercado de filgrastim. Un tercer biosimilar de filgrastim (Nivestym, Pfizer) ingresó al mercado en octubre de 2018, pero es demasiado pronto para conocer su impacto en el mercado. Una versión biosimilar de infliximab ($3600 millones en ventas en EE. UU. en 2018) ingresó al mercado con solo un 15 por ciento de descuento en el precio de lista en comparación con el infliximab de marca (Remicade).
Las proyecciones a largo plazo de las reducciones de precios y los ahorros que generarán los biosimilares no son favorables: para el subconjunto de productos biológicos que finalmente enfrenta la competencia de los biosimilares, los precios pueden disminuir en promedio entre un 20 y un 30 por ciento , y los ahorros proyectados a diez años en EE. UU. (2017-2026) total de sólo $ 54 mil millones . En Europa, a lo largo de una experiencia más larga que comenzó en 2006, hay muchos productos que aún no tienen competencia biosimilar. Entre los que lo hacen, las caídas de precios promediaron alrededor del 30 por ciento, un ahorro que evoluciona en promedio a un 3,5 por ciento por año luego de la entrada del biosimilar.
Las experiencias atípicas en Europa tienden a eclipsar los promedios. Por ejemplo, la licitación ganadora se lleva todo ha resultado en un descuento informado del 69-72 por ciento para infliximab en Noruega . Pero, en general, incluso para los productos biológicos que se enfrentan a la competencia de los biosimilares, los ahorros siguen estando lejos de la magnitud de las reducciones que podrían lograrse mediante una competencia robusta.
¿Por qué no funciona la competencia biosimilar?
Una característica necesaria de la competencia de precios es la presencia de una competencia efectiva de productos. Los competidores potenciales deben ser capaces de introducir productos totalmente sustituibles de forma rápida, económica y con un riesgo limitado de fracaso. Cuando se cumplen estas condiciones, los productos comercializados que obtienen ganancias superiores inducen a las nuevas empresas a producir sustitutos que rebajan el precio existente mientras siguen obteniendo ganancias aceptables para el nuevo competidor. El precio promedio pagado luego cae a medida que los compradores cambian con confianza y rapidez al producto de menor precio, sabiendo que les brindará los mismos beneficios. El proceso continúa, aumentado por continuas reducciones de precios por parte de los titulares que buscan participación de mercado, hasta que las ganancias caen lo suficiente como para dejar de atraer nuevos participantes.
La competencia en el mercado de medicamentos de molécula pequeña después de la entrada de medicamentos genéricos se aproxima a este patrón en la mayoría de los casos. Esto se debe a que, en general, el monopolio de los medicamentos de molécula pequeña es un producto intencional pero artificial de las políticas gubernamentales, como la exclusividad regulatoria. Después de que se levante este monopolio regulatorio, múltiples competidores pueden ingresar con réplicas. Para la mayoría de los medicamentos de molécula pequeña con un volumen de ventas suficiente, entran muchos competidores idénticos y los precios caen, aunque investigaciones recientes plantean preocupaciones sobre el mantenimiento de esa competencia a lo largo del tiempo.
Pero las características de los productos biológicos difieren fundamentalmente de las de las moléculas pequeñas en formas que dificultan la sustitución del producto, un requisito clave para las reducciones de precios basadas en la competencia.
Si bien el monopolio que tienen las moléculas pequeñas innovadoras es producto de las políticas gubernamentales, las terapias biológicas innovadoras poseen incertidumbres científicas intrínsecas que hacen que la creación de réplicas sea difícil, costosa, lenta y riesgosa. Los competidores de los productos biológicos de marca se denominan biosimilares en lugar de «bioidénticos» o genéricos para reflejar esta diferencia.
La incertidumbre se puede reducir, pero hacerlo es costoso y arriesgado. Por lo tanto, los biosimilares no satisfacen el primer principio de una exitosa competencia de precios basada en el mercado: la sustitución del producto. Ningún biosimilar ha cumplido aún con los requisitos de la FDA para la «intercambiabilidad», el análogo más cercano a la sustituibilidad en este campo.
El segundo criterio para las disminuciones de precios basadas en la competencia es que los fabricantes competidores enfrenten barreras de bajo costo, rápidamente satisfechas y de bajo riesgo para ingresar al mercado. Sin embargo, se ha proyectado que todo el proceso de desarrollo de biosimilares dure entre 8 y 10 años y cueste más de $ 100 millones . Los ensayos clínicos en humanos que involucran a cientos de pacientes pueden costar entre 20 y 40 millones de dólares simplemente para confirmar que el biosimilar candidato generalmente replica los efectos clínicos positivos y negativos a corto plazo del producto de referencia. Por el contrario, el medicamento genérico típico lleva a las empresas de 1 a 3 años , $ 1- $ 5 millones y no se introducen ensayos clínicos en humanos.
Las diferencias biológicas y químicas entre los medicamentos de molécula pequeña y los biológicos, no las decisiones políticas, explican la razón de esta brecha (Anexo 4). Los genéricos de molécula pequeña se producen mediante síntesis química altamente replicable y se puede demostrar que son molecularmente idénticos al original.
Los biosimilares mucho más grandes (10 000 átomos o más en comparación con los 100 o menos de los genéricos) se producen en las células a través de un proceso de inserción (transfección) de ADN más variable.
Las células resultantes crean productos que pueden variar ligeramente en comparación con el producto de referencia con respecto a la secuencia de moléculas centrales, las moléculas adicionales que se unen a esa estructura central y el plegado del biosimilar en su forma final. Por lo tanto, se requieren análisis moleculares detallados de los biosimilares , y los métodos actuales no pueden caracterizar completamente los productos biológicos grandes, incluso después de un proceso de varios pasos para comparar su estructura, función y efecto animal.
Una vez aprobados, los biosimilares enfrentan más barreras para su adopción. Estas barreras pueden interpretarse simplemente como un producto de malas elecciones de políticas, pero al menos tienen sus raíces en las preocupaciones sobre la sustitución de productos. Incluso después de la aprobación, los reguladores de EE. UU. revisan de manera regular y exhaustiva los procesos de biofabricación y las instalaciones de productos biosimilares. Requieren que los nombres moleculares biosimilares usen sufijos distintivos de cuatro letras (por ejemplo, infliximab-dyyb) y códigos de reembolso («J») , una medida justificada porque permite un seguimiento continuo de las diferencias clínicas.
Estos pasos impiden la entrada al mercado y la adopción clínica, lo que a su vez reduce los volúmenes de productos esperados y las ganancias para el nuevo participante. Estas menores expectativas de ganancias afectan las decisiones de entrada de las empresas que buscan el mercado de biosimilares; en los últimos años, muchas empresas han abandonado algunos o todos sus programas de biosimilares, incluidas Boehringer Ingelheim, Sandoz, Merck & Co. y Oncobiologics.
Otra barrera de entrada para los biosimilares que reduce los rendimientos esperados para los fabricantes potencialmente competidores es que los médicos los perciben como menos seguros y menos efectivos.
Esta impresión se ha visto reforzada por informes de casos sobre nuevos efectos secundarios, lo que reduce la propensión de los médicos a prescribir biosimilares. A diferencia de los genéricos de molécula pequeña, los biosimilares no pueden «pasar por alto» al médico a través de la sustitución automática a nivel de farmacia sin obtener primero una designación «intercambiable» de la FDA.
Abordar estos desafíos consume tiempo y dinero de desarrollo, aumenta el riesgo de fallas regulatorias, aumenta los costos de ventas y marketing, y eleva el umbral de ganancias esperado que requiere un posible fabricante de biosimilares antes de considerar ingresar al mercado. Los analistas han concluido que los biosimilares no son viables para ningún producto de referencia con ingresos anuales inferiores a $897 millones , un umbral que muchos productos biológicos no alcanzan (consulte el Anexo 1). En la actualidad, no se han lanzado ni aprobado biosimilares para ningún producto biológico con ventas anuales máximas en los EE. UU. por debajo de $ 1,16 mil millones, y solo unos pocos productos biológicos por encima de ese umbral han obtenido aprobaciones de biosimilares. Algunos productos biológicos han visto competencia de medicamentos que técnicamente no califican como «biosimilares», como Granix, un competidor de Neupogen, y Basaglar y Lusdana, competidores de Lantus.
Anexo 2. Aplicaciones biosimilares de la FDA y productos biológicos de seguimiento no biosimilares de la competencia (a fecha de 3/2019)
Reconocer que los productos biológicos disfrutan de monopolios naturales, no solo de los creados por políticas, ayuda a explicar la mala experiencia hasta la fecha con la entrada competitiva de biosimilares. Para los monopolios naturales, ajustar las regulaciones, aumentar la conciencia del mercado, enfocarse en las prácticas anticompetitivas o simplemente esperar a que ingresen los competidores será, en última instancia, ineficaz para reducir rápidamente los precios netos a un nivel que se aproxime al costo marginal de producción del producto original. Dicho de otra manera, los obstáculos para la entrada competitiva son una característica estructural de los productos biológicos mismos.
Los precios de los monopolios naturales se fijan mejor mediante la regulación (no los mercados)
Cuando los formuladores de políticas construyeron un camino hacia la entrada de biosimilares en 2010, solo tenían un objetivo: bajar los precios de los productos biológicos después del período de exclusividad del monopolio. Después de todo, se acepta ampliamente que las recompensas por la innovación se obtendrán principalmente durante el período de exclusividad definido por las políticas gubernamentales. Los biosimilares deben verse como un medio para lograr el objetivo político singular de bajar los precios después del período de exclusividad, no como un fin en sí mismos.
Para los monopolios naturales, la regulación de precios en lugar de la competencia puede ser mucho más eficaz. En otras palabras, los formuladores de políticas deberían reconsiderar su confianza en la competencia de biosimilares para lograr las reducciones de precios deseadas; en cambio, deberían considerar exigir a los fabricantes de productos biológicos innovadores que bajen sus precios después de su período de exclusividad en el mercado.
El precio reducido debe ser igual a los costos de producción (incluidas la reparación y el reemplazo de las instalaciones) y la distribución en el mercado, más una ganancia adecuada. Este precio podría determinarse a través de varias fórmulas, a partir de un costo informado más un margen de utilidad, un margen de beneficio definido sobre los ingresos, el rendimiento del capital o una combinación de estos. Lo que es crítico es que la fórmula sea clara; ser relativamente fácil de determinar y auditar; proteger a los pagadores de precios sustancialmente superiores al costo económico marginal de producción; y proteger a los fabricantes de los precios excesivamente bajos resultantes del ejercicio del poder adquisitivo de monopsonio por parte del regulador gubernamental. El regulador de precios debe mantener la independencia tanto de quienes pagan como de quienes producen.
Si bien los precios regulados no se han aplicado a los medicamentos en los EE. UU., se usan de manera más general en el reembolso de la atención médica. Medicare basa sus pagos a los hospitales por servicios de hospitalización en los costos informados de esos servicios más un margen de beneficio regulado, por ejemplo. La justificación del reembolso de costo más margen, en términos generales, es garantizar el suministro continuo de los servicios reembolsados. En muchos sentidos, la creación de un mercado competitivo para medicamentos de molécula pequeña que dependa de la entrada de genéricos tiene el mismo objetivo: reducir los precios a un nivel que sea lo suficientemente rentable para mantener el suministro, pero no más allá.
Ahorros significativos posibles
El impacto de un cambio a precios regulados después de la exclusividad podría ser considerable. Usando nuestras estimaciones del tamaño del mercado, las fechas de finalización de la exclusividad y un rango de costos de producción, estimamos que una política de este tipo a partir de 2018 habría generado $250-$300 mil millones de ahorros netos en EE. UU. durante cinco años (2018-2022), incluidos más de $87 mil millones para Medicare y Medicaid. Esta estimación se basa en el período de exclusividad actual de 12 años y en la suposición de que los descuentos se acercan a los descuentos genéricos tradicionales del 70 al 90 por ciento. Este rango abarca el 80 por ciento de descuento que AbbVie acaba de proponer cuando socavó su propio producto para bloquear los biosimilares de la competencia en el mercado de la UE. Las estimaciones de participación de mercado por pagador provienen de los datos de ventas de Bloomberg para una muestra de productos biológicos.
Incluso si las patentes de composición de la materia extienden la exclusividad biológica promedio a 15 años, los ahorros en cinco años aún superarían los $200 mil millones (Anexo 1). Estas estimaciones se construyeron a partir de las fechas de pérdida de exclusividad (LOE) para las 200 principales indicaciones biológicas (que abarcan 152 medicamentos) que derivamos al agregar doce años a las fechas de lanzamiento individuales. Utilizando los datos obtenidos a través de Cello Health BioConsulting sobre los ingresos en EE. UU. a partir de 2018 o en la fecha LOE, lo que ocurra más tarde, medimos la diferencia entre los ingresos proyectados actualmente de estas 200 indicaciones y los ingresos esperados bajo un rango de suposiciones de reducción de precios, de 30 por ciento del precio actual hasta el 10 por ciento del precio actual.
ANEXO 1: Ahorros en cinco años (2018-22) basados en varias estimaciones de precios posteriores a la exclusividad, calculados a partir de los ingresos proyectados en EE. UU.
Las previsiones de ingresos de Cello Health BioConsulting, contra las cuales se midieron nuestras estimaciones de ahorro, ya representan los cambios proyectados en los precios y la utilización de medicamentos según la política biosimilar actual. Por lo tanto, nuestras estimaciones de ahorro tienen en cuenta estos cambios proyectados. Pero no tomamos en cuenta el LOE rodante entre las indicaciones, acumulamos ahorros al evitar los costos de construcción de instalaciones de fabricación e investigación de biosimilares, o consideramos cambios en el volumen de prescripción debido a la disminución de precios. Por lo tanto, nuestra estimación es cruda, aunque da una idea de la magnitud de los ahorros disponibles si las autoridades adoptan este enfoque.
Compensación de transición para desarrolladores de biosimilares de buena fe
La implementación de este cambio de política impondría algunos costos de transición que no se incorporaron en la estimación anterior. Si bien el futuro de las empresas a menudo se ve afectado por las oscilaciones en la política regulatoria y de pago, la fuerte señal de varios años de un mercado emergente de biosimilares ha llevado a inversiones sustanciales en investigación y desarrollo de biosimilares, y esas inversiones se devaluarían considerablemente. Las empresas que han invertido con la esperanza de ingresar al mercado de biosimilares deben ser compensadas por el valor presente neto de sus inversiones.
Estimamos un rango de $ 10 a $ 20 mil millones para la recompensa requerida: un gasto único que asciende al 4-6 por ciento o menos de los ahorros potenciales de cinco años. Triangulamos este rango estimando primero el valor presente neto (VAN) de los trece biosimilares más destacados (pendientes o posteriores al lanzamiento) a través del modelo lineal simple establecido en Brill 2015 ; asumimos que cada biosimilar alcanzaría una participación de mercado del 35 por ciento, siendo el NPV una función lineal de los ingresos anuales del fármaco innovador. Esto generó una estimación de $ 10.6 mil millones a $ 20 mil millones al incluir empresas menos maduras y contabilizar la inflación. Luego evaluamos las estimaciones del VPN de la literatura publicada , así como de un tercero.source , que generalmente proporcionan más análisis basados en casos pero ofrecen un acuerdo razonable.
Finalmente, examinamos los costos irrecuperables de las empresas activas de biosimilares al multiplicar las estimaciones publicadas de los costos iniciales para llevar un biosimilar al mercado de $150 millones por la cantidad de fabricantes de biosimilares. Estimar generosamente que hay 60 fabricantes de biosimilares en una etapa avanzada de desarrollo, además de los 18 productos ya aprobados, arroja un pago de $10,650 millones. Para resumir, tres métodos diferentes respaldan el rango de compensación de $ 10-20 mil millones para las empresas biosimilares existentes.
También es posible que las empresas innovadoras lamenten las ganancias perdidas que de otro modo habrían obtenido debido a la débil competencia de biosimilares. Si bien esos beneficios no estaban garantizados ni pretendidos por los formuladores de políticas, anticiparlos es válido bajo la política actual. Según nuestra propuesta, esos ingresos proyectados podrían disminuir en algunos casos. No estamos a favor de otorgar una recompensa a las empresas innovadoras biológicas solo porque las mejoras en las políticas logran mejor los objetivos claramente articulados de la competencia por el fin de la exclusividad. Pero extender la exclusividad regulatoria quizás por uno o dos años podría resultar un compromiso aceptable para todas las partes y alentar a las empresas innovadoras a participar en el cambio de enfoque.
Posibles preocupaciones
Algunos pueden no estar de acuerdo con que los productos biológicos se entiendan mejor como monopolios naturales. Pueden pretender que las altas barreras de entrada para los biosimilares de la competencia son enteramente producto de malas decisiones políticas que pueden abordarse mediante reformas. Estamos de acuerdo en que las reformas pueden ayudar, pero no pueden eliminar la incertidumbre subyacente y los costos resultantes del monopolio natural de base biológica. El objetivo de la política es indiscutiblemente bajar los precios a los costos marginales económicos, no solo bajar un poco los precios de algunos productos.
Otros pueden argumentar que los productos biológicos no pueden ser monopolios naturales porque algunos biosimilares han ingresado a los mercados de EE. UU. y Europa y los precios se han nivelado o disminuido en algunos casos. Los monopolios naturales no son absolutos. Más bien, simplemente están bien blindados contra la entrada de la competencia. Es posible construir cuatro carreteras de peaje para inducir la competencia de precios, pero en general se reconoce que lo mejor es una sola carretera con peaje regulado.
No afirmamos que los biosimilares no puedan ser clínicamente viables o que no puedan introducirse en algunos casos, particularmente para aquellos productos con mercados muy grandes. Pero incluso para aquellos con mercados muy grandes, los ahorros anticipados serán más lentos y de menor grado que los que se logran con los genéricos de molécula pequeña. Esto se debe a que los biosimilares son un enfoque costoso, riesgoso, lento e incierto para lograr reducciones de precios comparativamente más pequeñas que las que se pueden obtener a través de la regulación de precios independiente del producto de monopolio natural del innovador. Este último enfoque puede lograr el singular objetivo de bajar los precios al costo marginal después de la exclusividad, y puede hacerlo rápidamente y sin riesgo clínico.
Resumiendo
Casi todos los economistas prefieren firmemente la competencia basada en el mercado por la regulación de precios, pero reconocen que los monopolios naturales son una rara excepción a esa preferencia. Cuando se trata de productos biológicos, los formuladores de políticas deben evaluar qué enfoque se alineará mejor con la estructura de recompensa temporal para las nuevas invenciones farmacéuticas que es el corazón de los incentivos a la innovación.
La competencia de biosimilares es un enfoque económicamente ineficiente que no puede lograr su objetivo total de reducción de precios.
Las reducciones automáticas de precios establecidas por una combinación de datos específicos del producto y puntos de referencia económicos en un proceso independiente bien regulado parecen superiores para los productos biológicos en el futuro previsible.
Por supuesto, hay preocupaciones. Como en cualquier enfoque de reembolso basado en costos, se pueden manipular los informes requeridos de costos, márgenes u otros datos necesarios. Una salvaguardia contra los informes erróneos notorios, más allá de la auditoría, sería que varias empresas informaran sus costos, proporcionando un medio para que los reguladores detecten valores atípicos. El exceso de ganancias que una empresa con precios regulados podría obtener a través de informes de costos inflados probablemente no se acerque a los niveles de precios y plazos actuales bajo la competencia de biosimilares.
El gobierno también podría intentar manipular la regulación de precios para obtener un precio inapropiadamente bajo para reducir sus costos de atención médica. Para evitar un posible uso indebido por parte del gobierno de su poder regulador de fijación de precios, abogamos por una orientación legal clara que consagre los principios económicos de costo marginal, incluidas las ganancias y la inversión adecuadas en la capacidad de fabricación. Además, la entidad encargada de establecer las normas para el mecanismo de fijación de precios y administrarlo no debe estar bajo el control de ningún programa de beneficios de salud.
Por último, algunas empresas pueden optar por interrumpir la fabricación de productos con precios regulados: pueden encontrar poco atractivas las ganancias administradas posteriores a la exclusividad para sus productos heredados, o pueden desear cambiar la prescripción a otros productos que aún disfrutan de precios de monopolio. Proponemos que se exija a las empresas que garanticen el suministro o que vendan el negocio de hacerlo, incluidos todos los derechos de propiedad intelectual y de conocimiento, a otra empresa dispuesta a atraer ganancias confiables. Si bien nuestra propuesta con toda probabilidad dependería de un solo productor para estos productos después de la exclusividad, las ganancias razonables garantizadas deberían sustentar la disponibilidad de la misma manera que la compañía innovadora sustenta la disponibilidad.
La posición de que se necesitan múltiples intervenciones políticas para aumentar el éxito de los biosimilares está ampliamente aceptada. Tales intervenciones pueden mejorar algunos aspectos de la entrada y adopción de biosimilares. Sin embargo, no pueden superar la incertidumbre científica con respecto a los biosimilares que requiere un largo proceso de investigación, desarrollo clínico, desarrollo y construcción del proceso de fabricación, supervisión regulatoria y precaución clínica. Reconocer los productos biológicos como monopolios naturales y exigir reducciones automáticas de precios cuando pierden la exclusividad del mercado puede lograr de manera más eficiente el único propósito de los biosimilares: reducir el costo de los productos biológicos para la sociedad después de que un período de exclusividad haya recompensado a sus innovadores.