Exceso de mortalidad por la pandemia en Argentina. ¿por la demora en la vacunación?
Mejorando la Comunicación entre Anestesiólogos y Pacientes
La comunicación efectiva entre el anestesiólogo y el paciente es esencial para garantizar una atención de calidad, que no solo considera los aspectos técnicos de la anestesia, sino también los valores y preferencias del paciente respecto a su atención perioperatoria y postoperatoria.

Problemática Actual
Uno de los principales desafíos identificados es la falta de interacción adecuada entre anestesiólogos y pacientes antes de la cirugía. Tradicionalmente, la visita preanestésica se realiza en un contexto subóptimo, como la sala de preparación quirúrgica, donde el paciente ya se encuentra en una situación de vulnerabilidad. Esto limita la capacidad del paciente para discutir sus preferencias, preocupaciones y comprender los riesgos asociados a la anestesia y la cirugía.
Resultados de la Revisión Sistemática
La revisión realizada por Tylee et al. (2020) muestra que:
Limitada Discusión de Cuidados Pre y Postoperatorios: La conversación entre los anestesiólogos y los pacientes se centra mayoritariamente en la planificación anestésica y logística, con escasa mención de las implicaciones posoperatorias de la anestesia. Solo un pequeño porcentaje de las sesiones incluyó discusiones precauciones antes de la inducción y sobre eventos adversos intra y posoperatorios.
Consentimiento Informado Deficiente: Aunque se abordan los riesgos y beneficios de manera variable, la comprensión del paciente sobre estos temas es frecuentemente inadecuada. Muchos pacientes no comprenden plenamente los riesgos asociados con la anestesia.
Deseo de Participación: Los pacientes desean participar en las decisiones sobre su atención, pero las interacciones actuales a menudo no fomentan esta participación activa.
Estrategias para Mejorar la Comunicación
Para abordar estas deficiencias en la comunicación, se pueden considerar las siguientes estrategias:
Visitas Preoperatorias Efectivas: Establecer protocolos que lleven a los anestesiólogos a realizar visitas a pacientes en sus habitaciones, permitiendo una interacción más cómoda y menos apresurada.
Formación en Comunicación: Capacitar a los anestesiólogos en habilidades de comunicación para que puedan abordar de manera efectiva temas complejos como cuidados postoperatorios y toma de decisiones compartidas.
Herramientas de Evaluación: Implementar listas de verificación o guías que aseguren que se aborden todas las preocupaciones relevantes del paciente durante la consulta.
Inclusión de Valores y Preferencias: Fomentar la recopilación de valores y preferencias del paciente sobre su atención, lo que podría ayudar a guiar las decisiones anestésicas y postoperatorias.
Aprovechar Tecnología: Utilizar plataformas digitales o aplicaciones para compartir información de forma segura y para tener un espacio donde los pacientes puedan formular preguntas antes de la cirugía.
Conclusión
Una mejor comunicación entre anestesiólogos y pacientes no solo contribuiría a aumentar la satisfacción del paciente, sino que también podría mejorar los resultados clínicos y la recuperación postoperatoria. Para lograr cambios significativos, es necesario que esta transformación se convierta en parte de la cultura clínica, donde la comunicación efectiva y la consideración de las preferencias del paciente sean prioridades en la atención anestésica
Comunicación entre el anestesiólogo y el paciente.
La comunicación clara y efectiva con los pacientes y sus familias es esencial para la calidad de atención, la elección informada, la coparticipación, la comprensión de riesgos y la tranquilidad del equipo. Una deficiencia en nuestro país es la falta de comunicación adecuada entre el paciente y el anestesiólogo en todas las instituciones, sean grandes o pequeñas, académicas, públicas o privadas. Los anestesiólogos, como los cirujanos, a menudo conocen al paciente en la antesala del quirófano, un entorno poco propicio para discutir opciones. Los anestesiólogos tienen una visita preanestésica incluida en sus honorarios, pero no siempre se especifica cómo debe realizarse. Generalmente, se hace en la sala de preparación antes de entrar al quirófano, cuando el paciente ya está listo para la intervención. El anestesiólogo se presenta, hace algunas preguntas para reducir riesgos, pero no hay oportunidad para discutir preferencias sobre la anestesia, el manejo del dolor, ni el seguimiento posterior. Si no hay complicaciones, el paciente probablemente no volverá a ver a ese médico. Es necesario actuar de manera conjunta y coordinada; esto debe ser parte de la función de supervisión. Esta comunicación mejora los resultados y la recuperación postoperatoria.
Parece que los anestesiólogos no consideran visitar a los pacientes en su habitación o tener horas de consulta externa como parte de su trabajo preoperatorio.
Hemos logrado que un internista también evalúe al paciente junto con el cirujano. En cirugía cardiovascular, un cardiólogo explica riesgos, cuidados preoperatorios, baño prequirúrgico, prevención de colonización y conciliación de medicación.
Para ilustrar esta nota, se hace referencia a una revisión sistemática muy bien fundamentada escrita por Tylee MJ et al 2020, y discutir cómo se podría mejorar esta deficiencia.
Una revisión sistemática
Dr. Michael J. Tylee ; Gordon D. Rubenfeld, MD, Dra Duminda Wijeysundera,
JAMA. 2020;3(11):e2023503. doi:10.1001/jamanetworkopen.2020.23503
Pregunta ¿Los anestesiólogos u otros profesionales de la anestesia participan en discusiones con los pacientes sobre decisiones que tienen implicaciones más allá del quirófano?
Resultados En esta revisión sistemática de la literatura sobre la comunicación entre pacientes y profesionales de la anestesia, se encontraron datos limitados sobre la comunicación relacionada con las decisiones perioperatorias con implicaciones que llegan más allá del quirófano. Estos datos sugieren que la comunicación entre pacientes y profesionales de la anestesia durante los encuentros preoperatorios está dominada por la discusión de la planificación anestésica y la logística perioperatoria, con una discusión variable de los riesgos frente a los beneficios y una discusión poco frecuente de los cuidados posoperatorios o la obtención de los valores y preferencias del paciente.
Significado Estos hallazgos sugieren que es poco probable que los pacientes que enferman gravemente después de intervenciones quirúrgicas programadas hayan hablado con su anestesiólogo sobre valores y preferencias para abordar decisiones complejas de atención posoperatoria, como ventilación invasiva prolongada, estadía hospitalaria prolongada con recuperación incompleta o cuidados al final de la vida.
Abstract
Importancia Muchos pacientes ingresan en cuidados intensivos tras una cirugía, y algunos no se recuperan completamente. Las conversaciones preoperatorias sobre los valores y preferencias del paciente pueden guiar las decisiones de atención. La literatura muestra que es raro que los cirujanos tengan estas conversaciones antes de la operación; tampoco está claro si los anestesiólogos las tienen.
Objetivo Revisar la literatura sobre la comunicación entre pacientes y anestesiólogos, con énfasis en los cuidados críticos postoperatorios.
Método Se buscaron estudios en MEDLINE y Web of Science desde enero de 1980 hasta abril de 2020, describiendo encuentros entre pacientes y anestesiólogos, siguiendo las pautas PRISMA.
Resultados Se incluyeron 12 estudios con 1284 encuentros. La comunicación sobre cuidados postoperatorios es rara: solo 2 estudios informaron sobre eventos adversos, presentes en solo 46 de 1284 consultas (3.6%). La conversación se centra en la planificación anestésica y logística perioperatoria, con poca discusión sobre riesgos y beneficios y raramente se abordan valores y preferencias del paciente. Algunos pacientes desean participar en decisiones perioperatorias, pero frecuentemente desconocen los riesgos y beneficios completos.
Conclusiones La comunicación en anestesia se enfoca en la planificación y logística preoperatoria, mientras que los cuidados críticos postoperatorios son raramente discutidos. La mayoría de los pacientes en cuidados intensivos tras una cirugía importante no habrán discutido objetivos específicos de recuperación prolongada o cuidados intensivos con su anestesiólogo.
Introducción
La comunicación con los pacientes sobre las opciones terapéuticas y los planes de atención es un componente fundamental de la toma de decisiones compartida y es particularmente importante cuando una decisión puede resultar en un cambio importante o permanente en el estado de salud de un paciente. Esta situación es relativamente común para los pacientes que se someten a una cirugía mayor. Los cirujanos y anestesiólogos son los principales médicos clínicos con la oportunidad y, podría decirse, la responsabilidad de obtener valores y preferencias sobre el cuidado posoperatorio de los pacientes quirúrgicos para informar las decisiones de atención si los pacientes enferman gravemente y pierden la capacidad de decisión después de la operación. Trabajos previos sugieren que los cirujanos rara vez obtienen las preferencias de los pacientes con respecto a la enfermedad crítica posoperatoria antes de la operación, incluso para pacientes de alto riesgo. 1 , 2 Los anestesiólogos también tienen la oportunidad de obtener los valores y preferencias de los pacientes antes de la operación, y algunos miembros de la especialidad tienen interés en expandir el papel de los anestesiólogos en la medicina perioperatoria. 3 – 5 El conocimiento y la comunicación de las complicaciones médicas y quirúrgicas después de la cirugía, a diferencia de las complicaciones de la anestesia, son esenciales para esta función. Sin embargo, el alcance de la responsabilidad de los anestesiólogos y su capacidad para desempeñar esta función no está claro, y es probable que existan expectativas profesionales variables para la comunicación entre el paciente y el anestesiólogo en diferentes sistemas y entornos de atención médica.
Existen pocos datos sobre la comunicación durante las consultas de anestesia . Aunque se han revisado de forma narrativa los estudios sobre la comunicación entre anestesiólogos y pacientes, 6,7 no existe una revisión sistemática sobre este tema. En esta revisión, se utilizó una estrategia de búsqueda sistemática para extraer y cotejar datos sobre la comunicación entre profesionales de la anestesia y pacientes, y se evaluó la calidad metodológica de los estudios existentes. Se presenta una síntesis de los datos centrados en la comunicación sobre enfermedades críticas posoperatorias.
Métodos
Se realizó una revisión sistemática de la literatura sobre la comunicación entre los profesionales de la anestesia y los pacientes para abordar la siguiente pregunta: en los encuentros anestésicos preoperatorios, ¿cuáles son los patrones y el contenido de la comunicación entre los profesionales de la anestesia y los pacientes según la evaluación mediante métodos cualitativos o mixtos? Los informes son coherentes con la guía de informes de Elementos de informe preferidos para revisiones sistemáticas y metaanálisis ( PRISMA ). 8
Fuentes de información y búsqueda
Se realizó una búsqueda en MEDLINE (desde 1980 hasta abril de 2020) para recuperar cualquier estudio centrado en la comunicación entre pacientes y profesionales de la anestesia (Apéndice electrónico 1 en el Suplemento ). Luego se realizó una búsqueda de una generación, hacia adelante y hacia atrás, en Web of Science utilizando cada uno de los estudios incluidos en la búsqueda en MEDLINE para identificar estudios relevantes adicionales.
Elegibilidad, selección y extracción de datos para el estudio
Sólo se incluyeron estudios con datos que describieran encuentros específicos entre pacientes y profesionales de la anestesia. Se excluyeron los estudios con un enfoque principal distinto a la comunicación, los estudios sobre la comunicación durante los procedimientos de anestesia y los estudios que examinaran la comunicación con niños (consulte el Apéndice electrónico 2 y el Apéndice electrónico 3 en el Suplemento ). Además, se excluyeron los estudios que desarrollaron o evaluaron intervenciones de comunicación porque estos estudios prescribían estrategias de comunicación en lugar de evaluar prácticas de comunicación establecidas. La búsqueda se limitó a estudios publicados en inglés, que generalmente proporciona una evaluación suficiente de un tema determinado, 9 , 10 y a estudios publicados después de 1980. Tres revisores (MJT, SH y MCS) realizaron una selección de títulos y 1 revisor (MJT) recuperó el texto completo de los títulos relevantes, seleccionó los estudios y extrajo los datos.
Revisión de la calidad metodológica
Un revisor (MJT) evaluó la calidad de todos los estudios utilizando la herramienta previamente validada del Programa de Habilidades de Evaluación Crítica (CASP) para Estudios Cualitativos. 11 Un segundo revisor (NKJA) verificó estas evaluaciones.
Análisis estadístico
Se presentan los resultados de los estudios individuales y las revisiones de calidad, y los resultados generales se sintetizan descriptivamente. Las variables y los resultados extraídos de los estudios individuales fueron demasiado diversos para la síntesis cuantitativa. Los datos continuos se expresan como medias con DE o como medianas con rangos intercuartiles (RIC). No se realizó ninguna prueba estadística.
Resultados
Búsqueda y selección de estudios
La figura muestra una descripción general de la selección de estudios. Se revisaron treinta artículos de texto completo de la búsqueda, de los cuales se excluyeron 20 estudios (consulte el Apéndice electrónico 4 en el Suplemento ). Diecisiete de estos estudios se excluyeron porque no incluían ningún dato sobre la comunicación entre anestesiólogo y paciente durante los encuentros de rutina. Se excluyeron tres estudios porque trataban sobre la comunicación durante los procedimientos. Se incluyeron los 10 estudios restantes y la búsqueda en Web of Science arrojó 2 estudios más, lo que dio como resultado 12 estudios para revisión. 12 – 23
Características del estudio
Las características del estudio se resumen en la Tabla 1. Todos los estudios incluyeron estadísticas descriptivas y 5 estudios 13 – 15 , 20 , 23 realizaron algún modelo estadístico. Diez estudios recopilaron datos de comunicación sin procesar sobre encuentros clínicos mediante grabación de audio, 15 , 17 – 20 , 22 , 23 grabación de vídeo, 16 u observación directa con un observador experimentado. 12 , 13 Un estudio recopiló datos utilizando solo cuestionarios, 14 y otro utilizó entrevistas semiestructuradas. 21 De los estudios que realizaron análisis cualitativos, solo 1 estudio 15 especificó un enfoque de análisis cualitativo y un marco 24 para la codificación de datos.
Calidad metodológica
El resumen de la calidad metodológica se muestra en la Tabla 2. Solo 4 estudios 14 , 16 , 18 , 20 utilizaron herramientas previamente validadas para recopilar o codificar datos, y 1 estudio 21 creó y validó una encuesta. Ocho estudios 12 , 15-20 , 22 utilizaron 2 o más evaluadores para codificar los datos registrados. Once estudios 12 , 13 , 15-23 se evaluaron en todos los criterios CASP, con una puntuación mediana (RIC) de 4 de 5 (3-5). Un estudio 14 solo se evaluó en 4 de los criterios CASP y obtuvo una puntuación de 3 de 4. Las cuestiones metodológicas y la evaluación de los análisis cuantitativos para los estudios que realizaron modelos estadísticos se muestran en la Tabla 3 .
Descripción del contenido de la comunicación
Solo 2 estudios informaron sobre la comunicación con respecto a eventos médicos posoperatorios adversos, y esta conducta de comunicación se informó en solo 46 de 1284 consultas (3,6 %) en todos los estudios. Se tomó una decisión a priori para evaluar específicamente los artículos en busca de datos de comunicación en las siguientes categorías: (1) discusión de opciones terapéuticas, incluido el consentimiento informado, la comprensión del paciente y los riesgos/beneficios, (2) obtención de valores y preferencias, (3) toma de decisiones compartida y (4) comunicación sobre el cuidado posoperatorio. Estas categorías se eligieron porque resaltan la comunicación que es central para las consultas entre pacientes y médicos en torno a intervenciones importantes. Debido a los amplios tipos de datos encontrados en la revisión, la segunda y tercera categorías se fusionaron en una sola categoría, y se agregaron otros datos como categoría para capturar datos que no encajaban en categorías definidas previamente. Los resultados del estudio se resumen en la Tabla 4 .
Consentimiento informado y comprensión del paciente
Diez estudios 12 , 13 , 15 – 17 , 19 – 23 incluyeron datos sobre estos temas. Dos estudios 16 , 23 examinaron la comunicación en general sin un enfoque específico. Un estudio de los enunciados de pacientes y anestesiólogos durante las consultas 16 identificó una media del 23% de los enunciados relacionados con el asesoramiento al paciente (no se proporcionó la proporción exacta); sin embargo, el método de codificación utilizado sugiere que la mayoría de los enunciados codificados como asesoramiento probablemente estaban relacionados con aspectos técnicos y logísticos de la atención. Se observó un resultado similar en un estudio de consultas de anestesia con pacientes estandarizados, 23 que utilizó escenarios de pacientes simulados y 2 pacientes estandarizados diferentes. En este estudio, solo se dedicó una media de menos de 1 minuto a elaborar un plan en cada encuentro. 23
Siete estudios 13 , 15 – 17 , 20 , 22 , 23 contenían datos sobre discusiones de riesgos y beneficios; 3 estudios 13 , 17 , 22 evaluaron específicamente la comunicación de riesgos. Un estudio 17 encontró que durante 91 encuentros clínicos con padres de niños sometidos a anestesia, en 27 consultas (29,6%) no se discutieron riesgos, y en otras 23 consultas (25,3%), solo se incluyó una declaración general de riesgo. Los riesgos graves solo se discutieron en 4 encuentros (4,4%). En adultos sometidos a cirugía electiva, otro estudio 13 encontró que durante 40 encuentros de rutina, solo 31 consultas preoperatorias (77,5%) incluyeron la discusión de al menos 1 riesgo. Cuando el riesgo era parte de las consultas (n = 151), los pacientes casi siempre estaban satisfechos y no angustiados por la discusión (146 de 151 consultas [96,7%]). Por el contrario, en las consultas en las que no se discutieron riesgos (n = 115), la mayoría de los pacientes (96 [83,5%]) creían que no había ningún riesgo en la anestesia. 13 Un pequeño estudio sobre la inserción epidural22 encontró un grado similar de variabilidad, donde el número de riesgos discutidos en las conversaciones de consentimiento varió de 0 a 11 por encuentro. En estudios con un enfoque diferente a la comunicación de riesgos que tenían datos auxiliares sobre las discusiones de riesgos, hubo un grado similar de variabilidad. 15 , 16 , 20 , 23 La mayoría de los riesgos evaluados específicamente en estos estudios fueron riesgos menores y de corto plazo. La evaluación global del consentimiento informado se evaluó en solo 1 estudio, 15 que encontró que en las conversaciones con los padres de los niños sometidos a anestesia, los requisitos mínimos para el consentimiento informado se incluyeron en 68 de 97 casos (70,1%). Solo una minoría de las conversaciones (12%, proporción exacta no proporcionada) incluyeron los 7 aspectos del consentimiento completamente informado según lo definido por los autores.
Los datos relacionados con la comprensión del paciente de la información comunicada por los anestesiólogos se extrajeron de 4 estudios. 12 , 15 , 19 , 21 Entre los estudios con medidas objetivas de comprensión del paciente, la comprensión del paciente de los riesgos y beneficios de varias opciones anestésicas fue deficiente. Por ejemplo, un estudio mostró que muchos padres recordaban una descripción de la anestesia planificada para su hijo (96,2 %, proporción exacta no proporcionada) y planes para el control del dolor posoperatorio (81,2 %, proporción exacta no proporcionada), pero las preguntas de seguimiento sugirieron que muy pocos padres comprendían completamente los riesgos, beneficios y complicaciones (28 de 263 padres [10,6 %]). 21 En otro estudio, los padres informaron con frecuencia que comprendían los riesgos, los beneficios y el plan anestésico (88 %, 96 % y 96 %, respectivamente; proporciones exactas no proporcionadas). 15 Sin embargo, este estudio solo incluyó la comprensión autoinformada de los padres. Al considerar palabras específicas utilizadas en las consultas, un estudio 12 demostró que, si bien los pacientes no comprendían una minoría de los términos técnicos utilizados por los anestesiólogos (49 de 484 términos [10,1 %] no comprendidos en todos los encuentros), hubo al menos 1 caso de malentendido de los pacientes en 32 de 68 encuentros individuales (47,1 %). 12 Otro aspecto de la comunicación relacionado con la comprensión del paciente fue evaluado por un estudio que midió la cantidad de información brindada a los pacientes preoperatoriamente por los profesionales de la anestesia. 19 Este estudio encontró que la capacidad de almacenamiento de información de los pacientes se excedía constantemente en los encuentros preoperatorios. 19
Los datos relacionados con la comprensión del paciente de la información comunicada por los anestesiólogos se extrajeron de 4 estudios. 12 , 15 , 19 , 21 Entre los estudios con medidas objetivas de comprensión del paciente, la comprensión del paciente de los riesgos y beneficios de varias opciones anestésicas fue deficiente. Por ejemplo, un estudio mostró que muchos padres recordaban una descripción de la anestesia planificada para su hijo (96,2 %, proporción exacta no proporcionada) y planes para el control del dolor posoperatorio (81,2 %, proporción exacta no proporcionada), pero las preguntas de seguimiento sugirieron que muy pocos padres comprendían completamente los riesgos, beneficios y complicaciones (28 de 263 padres [10,6 %]). 21 En otro estudio, los padres informaron con frecuencia que comprendían los riesgos, los beneficios y el plan anestésico (88 %, 96 % y 96 %, respectivamente; proporciones exactas no proporcionadas). 15 Sin embargo, este estudio solo incluyó la comprensión autoinformada de los padres. Al considerar palabras específicas utilizadas en las consultas, un estudio 12 demostró que, si bien los pacientes no comprendían una minoría de los términos técnicos utilizados por los anestesiólogos (49 de 484 términos [10,1 %] no comprendidos en todos los encuentros), hubo al menos 1 caso de malentendido de los pacientes en 32 de 68 encuentros individuales (47,1 %). 12 Otro aspecto de la comunicación relacionado con la comprensión del paciente fue evaluado por un estudio que midió la cantidad de información brindada a los pacientes preoperatoriamente por los profesionales de la anestesia. 19 Este estudio encontró que la capacidad de almacenamiento de información de los pacientes se excedía constantemente en los encuentros preoperatorios. 19
Toma de decisiones compartida
Cinco estudios 14 – 16 , 20 , 23 tenían datos sobre la obtención de preferencias del paciente y la toma de decisiones compartida. En los 2 estudios 16 , 23 que evaluaron la comunicación en general, la obtención de preferencias y valores del paciente fue poco común. En 1 estudio, 23 anestesiólogos pasaron menos de 1 minuto obteniendo perspectivas del paciente durante encuentros que tuvieron una media (DE) de 15,9 (4,9) minutos de duración. Otro estudio 16 no mostró enunciados que provocaran preferencias del paciente durante las consultas. En 21 encuentros en este estudio que requirieron una decisión compartida, las puntuaciones de Observación de la Participación del Paciente (puntuaciones OPTION 25 ) fueron deficientes, y la obtención de categorías de aportes del paciente recibió las puntuaciones más bajas. 16 Hubo hallazgos similares en un estudio de consentimiento informado en anestesia pediátrica, 15 que mostró que la obtención de preferencias de los padres fue poco común (18% de las consultas, proporción exacta no proporcionada). Dos estudios 20 , 14 examinaron la toma de decisiones compartida. En un estudio de decisión compartida sobre anestesia neuroaxial vs. anestesia general, 20 las puntuaciones OPTION mostraron que los profesionales de la anestesia rara vez explicaban los beneficios y riesgos de las opciones anestésicas y no obtenían ni hacían intentos adecuados para integrar las preferencias de los pacientes en la toma de decisiones. Otro estudio 14 tuvo hallazgos similares: la mayoría de los pacientes (>90%) querían participar en las decisiones sobre su atención, y los anestesistas tendían a subestimar el deseo de los pacientes de una toma de decisiones compartida.
Discusiones sobre cuidados postoperatorios
Las discusiones sobre el cuidado posoperatorio fueron poco frecuentes: este tipo de comunicación se describió en 5 estudios, 13 , 16 , 17 , 21 , 23 y el control del dolor posoperatorio dominó estas discusiones. Solo 2 estudios 13 , 17 presentaron datos sobre la comunicación sobre resultados adversos específicos. En estos estudios, hubo 4 instancias de comunicación sobre eventos posoperatorios en 91 entrevistas (4,4%) en 1 estudio, 17 y muerte o daño permanente grave discutidos en 20 de 272 entrevistas (7,4%) y 22 entrevistas (8,1%), respectivamente, en otro estudio. 13 Ninguno de los estudios tenía datos sobre la obtención de las preferencias del paciente con respecto a la dirección de la atención en el caso de eventos adversos graves.
Otros datos
Ocho estudios 13-16 , 18 , 20 , 21 , 23 aportaron datos adicionales sobre la satisfacción del paciente o la percepción de la calidad del encuentro tras las consultas de anestesia. La satisfacción fue generalmente alta, independientemente de los componentes específicos incluidos en las entrevistas, 15 , 20 y la satisfacción puede tener una asociación positiva con el grado de participación del paciente en las decisiones de atención 14 y con profesionales de la anestesia más experimentados. 23
Discusión
Esta revisión sistemática sobre la comunicación entre profesionales de anestesia y pacientes encontró solo 12 estudios relevantes, con una calidad metodológica moderada. Principalmente, se observa que la comunicación sobre cuidados posoperatorios es rara en las consultas preoperatorias. No hay datos sobre la interacción entre anestesiólogos y pacientes respecto a estadías prolongadas en UCI o cuidados al final de la vida.
La literatura muestra que el consentimiento informado varía mucho y los pacientes a menudo no comprenden bien los riesgos y beneficios de sus tratamientos. Además, los anestesiólogos suelen brindar demasiada información técnica y rara vez involucran a los pacientes en la toma de decisiones compartida.
Las directrices recomiendan incluir a los pacientes en la toma de decisiones médicas, pero existen barreras como la falta de tiempo y la presión financiera. Identificar a los pacientes en riesgo de complicaciones posoperatorias podría mejorar la toma de decisiones. En comparación con otras especialidades, la anestesiología tiene menos investigaciones sobre la comunicación con los pacientes.
Mejorar la comunicación puede requerir adaptar la información a las necesidades del paciente y enfocarse en la medicina perioperatoria, especialmente para aquellos con alto riesgo de recuperación incompleta. Las intervenciones para la planificación anticipada del tratamiento perioperatorio ofrecen orientación para los anestesiólogos que buscan expandir su práctica hacia esta área.
Limitaciones
Esta revisión sistemática tiene varias limitaciones. En primer lugar, la búsqueda se limitó a estudios publicados en inglés desde 1980 hasta abril de 2020. Aunque es posible que se hayan publicado datos adicionales antes o que se hayan indexado en otro lugar, es poco probable que sean relevantes para la práctica actual. La búsqueda solo encontró 12 estudios con diferentes diseños, entornos y resultados, lo que dificulta la síntesis. Las limitaciones comunes de los estudios que se revisaron incluyeron el sesgo de selección inevitable debido a la participación selectiva; el efecto Hawthorne en los estudios que emplearon la observación directa (2 de 12 estudios) y el uso poco frecuente de herramientas de análisis o codificación validadas (solo 4 de 12 estudios utilizaron herramientas validadas). Los estudios basados en encuestas (3 de 12 estudios) estuvieron limitados por el sesgo de recuerdo de los pacientes y los profesionales de la salud. Nueve estudios implementaron estrategias de mitigación para estos sesgos. Por último, solo 3 estudios proporcionaron datos sobre la categoría de riesgo de los pacientes en sus análisis, y la mayoría de los pacientes se consideraron de bajo riesgo de complicaciones. La comunicación preoperatoria con pacientes con mayor riesgo puede ser sustancialmente diferente en comparación con los patrones de comunicación encontrados en esta revisión. Estas limitaciones dificultan sacar conclusiones concretas sobre la comunicación en anestesia y sus implicaciones para los pacientes con recuperación incompleta.
Conclusiones
Esta revisión sistemática de la literatura sobre la comunicación entre el paciente y el anestesiólogo indica que la comunicación en anestesia rara vez incluye una discusión sobre los cuidados posoperatorios o los valores y preferencias del paciente, sino que se enfoca principalmente en la planificación anestésica y la logística perioperatoria. Estos hallazgos, junto con datos similares de la literatura quirúrgica, muestran que la mayoría de los pacientes que ingresan a la unidad de cuidados intensivos después de una operación importante no han tenido una discusión preoperatoria sobre los valores, las preferencias y los objetivos de la atención específicos para la recuperación prolongada o los cuidados intensivos prolongados.
LAS COMPETENCIAS COMO BASE DE LA FORMACIÓN MÉDICA
7 entrega de las habilidades blandas.
El futuro depende de la formación de médicos que hayan alcanzado la capacidad en competencias de gestión relevantes en una etapa temprana de sus carreras y, por lo tanto, estimulen un grupo más amplio y experimentado de candidatos para puestos de liderazgo en el futuro. Que sepan mucha medicina que estén bien formados, que practiquen una medicina cercana, basada en las personas y los datos que surjan de los pacientes procesados correctamente, que sepa trabajar en equipo, que lidere los cambios, que avance hacia cuidados integrales basados en el valor, en la época neovesaliana de la medicina de las 6 P.
LAS COMPETENCIAS COMO BASE DE LA FORMACIÓN MÉDICA
Peter Spurgeon. John Clark
Los rápidos cambios en el entorno sanitario han presionado a las organizaciones sanitarias y a los profesionales médicos, a los organismos reguladores y educativos a empezar a examinar más detenidamente lo que significa ser un médico plenamente competente. Como resultado, el interés en desarrollar y utilizar las competencias para influir en la forma en que los profesionales de la salud se educan, capacitan y trabajan ha aumentado en las últimas décadas. De particular interés es el énfasis en las competencias de gestión y liderazgo. Existen varias definiciones de competencia, aunque todas son Muy similares y centrados principalmente en la situación laboral/laboral. Desde la perspectiva de los recursos humanos, la competencia podría definirse como los conocimientos, habilidades y actitudes que
1. Afectar una parte importante del trabajo (rol o responsabilidad)
2. Se correlaciona con el rendimiento en el trabajo
3. Se miden en función de normas bien aceptadas
4. Se mejoran mediante la formación y el desarrollo (Lucia y Lepsinger, 1999, p.5)
Wass y van der Vleuten (2009), en Carter y Jackson, definen la competencia en el contexto clínico como «la capacidad de manejar una tarea profesional compleja mediante la integración de las habilidades cognitivas, psicomotrices y afectivas relevantes» (p. 105). Antes de la introducción y el uso generalizado de las competencias, las pruebas de inteligencia y aptitud se usaban comúnmente para determinar la idoneidad de un individuo para roles y responsabilidades particulares. McClelland (1973) sugirió que tales mediciones eran inadecuadas debido a su escasa relación con los resultados prácticos y propuso que las competencias serían un enfoque más útil. Las competencias tienen muchas ventajas en el sentido de que «incluyen una amplia gama de conocimientos, actitudes y patrones de comportamiento observables que, en conjunto, dan cuenta de la capacidad de prestar un servicio profesional específico» (McGaghie et al., 1978, p. 19) y pueden utilizarse para aplicarse a una serie de profesiones y niveles o etapas de carrera. En 2002, los tres Reales Colegios de Médicos del Reino Unido publicaron los primeros planes de estudios basados en competencias (Comité Conjunto para la Formación Médica Superior). Se trata de una reestructuración de la formación y la evaluación de los registradores especializados. Los planes de estudio se basaron en el logro de una serie de competencias consideradas necesarias para que los médicos trabajen como consultores independientes. Se describieron los conocimientos, habilidades y actitudes requeridos para cada competencia. También se definió la evaluación de cada competencia, que debía ser continua, en el puesto de trabajo, con tutores que cruzaran conocimientos y experiencia (Mayor, 2002). El proceso de adquisición o desarrollo de competencias o la definición de los diferentes niveles de desarrollo de competencias puede describirse utilizando la pirámide de Miller (Miller, 1990) o la taxonomía seminal de Bloom (Bloom, 1956). Para la pirámide de Miller, desde la base de la pirámide hacia arriba, sabe indica el conocimiento básico, sabe cómo es el conocimiento aplicado (destacando que hay más en la competencia clínica que el conocimiento por sí solo), muestra cómo representa una función conductual y hace pruebas de rendimiento. Este sistema se utiliza a menudo en la evaluación de las habilidades y el rendimiento en medicina. La taxonomía original de Bloom (1956), sin embargo, se centra más en el conocimiento cognitivo que en el rendimiento.
Este marco tiene seis categorías o niveles principales que consisten en conocimiento, comprensión, aplicación, análisis, síntesis y evaluación.
Con la excepción de «conocimientos», las otras cinco categorías se presentaron como habilidades y destrezas. Bloom reconoció que estos eran necesarios para transferir el conocimiento a la práctica. Al desarrollar las competencias básicas que se aplican a los profesionales de la salud, Shewcuk et al. (2005) destacan varios factores importantes que vale la pena considerar. En primer lugar, a menudo existen numerosos entornos organizativos en términos de enfoque y misión; Por ejemplo, los médicos pueden trabajar en muchos entornos diferentes, desde la atención primaria hasta la aguda, la salud mental, el tercer sector, etc.
En segundo lugar, en el ámbito sanitario, existen múltiples profesiones con conocimientos y habilidades propias basadas en numerosas disciplinas y especialidades. Para los médicos en el Reino Unido, ¡hay una selección de 57 especialidades diferentes! Dicho esto, en muchos casos, más de una profesión y más de una especialidad tendrán o utilizarán parte del mismo cuerpo de conocimientos en un campo en particular.
En tercer lugar, pueden surgir diferentes competencias en diferentes momentos de una trayectoria profesional. Para un estudiante de medicina, las oportunidades para desarrollar y demostrar competencias particulares serán diferentes a las de un médico en formación o un consultor o médico general (GP); por lo tanto, se desarrollarán con el tiempo a través de su educación, capacitación y práctica. En cuarto lugar, la atención médica es un campo específico del contexto. Si las competencias se retiran de contextos específicos y los comportamientos reales casi no tienen significado en términos de cómo se relacionan con resultados y objetivos importantes de la formación, es poco probable que tengan valor. Además, Shewcuk et al. (2005) sostienen que es probable que las competencias no integradas en un marco tengan poco valor duradero.
5.3 MARCOS DE COMPETENCIAS EN EL REINO UNIDO
Históricamente, ha habido una serie de revisiones y publicaciones dentro de la profesión médica, por ejemplo, la Asociación Médica Británica (2004), GMC (2006) y el Real Colegio de Cirujanos de Inglaterra (2007), que se centran en las competencias no clínicas, el papel directivo de los médicos y la gestión eficaz de los médicos por parte de los médicos (Davies et al., 2003). Más adelante en el capítulo, revisaremos la versión actualizada de las Buenas Prácticas Médicas del GMC (2013a). Además, se han realizado múltiples estudios que han desarrollado marcos de competencias genéricos para todos los niveles de médicos en formación, los de nivel de consultor y para los puestos de gerente clínico-líder sénior, por ejemplo, directores clínicos y médicos. El mensaje esencial de estos estudios es que el conocimiento y la habilidad clínica suficientes son la línea de base; Sin embargo, para que un médico sea un profesional eficaz y seguro en un sistema de salud complejo, se requiere una gama adicional de competencias no clínicas, incluidas la gestión y el liderazgo. En el Reino Unido, la gestión y el liderazgo generalmente no se consideraban parte del plan de estudios básico de pregrado (escuela de medicina), ya que se ha centrado en las habilidades clínicas necesarias para convertirse en un médico competente. Sin embargo, muchos elementos de lo que podría considerarse gestión y liderazgo, por ejemplo, la comunicación, el trabajo en equipo y el autoconocimiento, se han enseñado históricamente bajo diferentes epígrafes como la profesionalidad o el desarrollo personal y profesional. Algunos módulos seleccionados por los estudiantes introducen los conceptos de liderazgo y gestión fuera del currículo básico. Sin embargo, hasta hace poco, ha habido una falta de un marco global y común para estas competencias. En la etapa de fundación, la mayor parte de la capacitación se ha realizado a través de acuerdos internos con decanatos de posgrado y sus organismos sucesores y fideicomisos del NHS. El Programa Básico (www.foundationprogramme.nhs.uk/pages) detalla una serie de competencias profesionales básicas que abarcan 12 áreas:
1. Profesionalidad
2. Relación y comunicación con los pacientes
3. Seguridad y gobernanza clínica
4. Cuestiones éticas y jurídicas
5. Enseñanza y formación
6. Mantener una buena práctica médica
7. Buena atención clínica
8. Reconocimiento y gestión
9. Reanimación y cuidados al final de la vida
10. Pacientes con enfermedades a largo plazo
11. Investigaciones
12. Procedimientos
El liderazgo se menciona explícitamente en la categoría de «profesionalismo», que también incluye el comportamiento en el lugar de trabajo, la gestión del tiempo y el trabajo en equipo. Durante la etapa de formación de posgrado o especialidad, históricamente se ha puesto el énfasis en la formación de médicos para el futuro. Si bien algunos decanatos locales ofrecían algunos programas específicos sobre gestión y liderazgo, muchos médicos no accedieron a estos programas hasta los últimos seis meses de su formación en la especialidad para prepararse para el nombramiento como médico de cabecera o puesto de consultor. En la actualidad, el desarrollo y la evaluación de las competencias genéricas no han sido lo suficientemente sólidos o coherentes a lo largo de esta etapa, y existe un acuerdo general entre los dirigentes médicos y los responsables de las políticas sanitarias de que todos los médicos, independientemente de su especialidad, deben tener un conjunto mínimo de habilidades de gestión y liderazgo para poder desempeñar sus funciones de profesional de forma más eficaz. Una vez que un médico es nombrado para un puesto de consultor o médico de cabecera en el Reino Unido, se convierte ipso facto en líderes dentro del sistema de salud, no necesariamente en roles de liderazgo formales, sino como profesionales de los que se espera que lideren tanto la salud como la comunidad en general. Durante la última década, ha habido una comprensión y aceptación mucho más claras de la necesidad de que los médicos calificados hayan desarrollado, o adquieran rápidamente, una gama de competencias de liderazgo y gestión. En el Reino Unido, hasta 2008, no existía un marco de competencias de gestión y liderazgo común y reconocido para los médicos, aunque en los últimos años se han publicado varios documentos y marcos por parte de diversas organizaciones médicas y no médicas.
Esto fue reemplazado por una nueva guía del GMC en 2012 titulada Liderazgo y Gestión para Todos los Médicos (GMC, 2012), que plantea y actúa sobre las preocupaciones sobre la seguridad del paciente y escribe referencias. Esta guía proporciona consejos más detallados sobre cómo se aplican los principios de las «Buenas prácticas médicas», la orientación básica del GMC para los médicos, en el contexto del papel de los médicos en el lugar de trabajo. Estas incluyen responsabilidades relacionadas con cuestiones de empleo, enseñanza y capacitación, planificación, uso y gestión de recursos, plantear preocupaciones y actuar sobre ellas y ayudar a desarrollar y mejorar los servicios. Apoya nuestra opinión de que ser un buen médico significa más que simplemente ser un buen experto clínico. La guía cubre una amplia gama de deberes, pero en esencia, los médicos, independientemente de su función, deben hacer lo siguiente:
1. Comprometerse con colegas para mantener y mejorar la seguridad y la calidad de la atención al paciente
2. Contribuir a las discusiones y decisiones sobre la mejora de la calidad del servicio y los resultados
3. Plantear y actuar sobre las preocupaciones sobre la seguridad del paciente
4. Demostrar un trabajo en equipo y un liderazgo efectivos
5. Promover un entorno de trabajo libre de discriminación injusta, intimidación y acoso, teniendo en cuenta que los colegas y los pacientes provienen de diversos orígenes
6. Contribuir a la enseñanza y la formación de médicos y otros profesionales de la salud, en particular actuando como un modelo positivo
7. Utilizar los recursos de manera efectiva para el beneficio de los pacientes y el público.
5.4 ENFOQUES COMPETENCIALES EN OTROS PAÍSES
Otros países con historias similares de escasa participación médica en la planificación, prestación y transformación de los servicios también están reconociendo que es poco probable que se logren mejoras en el sistema de salud sin crear culturas organizativas que alienten a los médicos a querer participar. Esto requiere un cambio de paradigma en la forma en que la profesión médica ve el papel futuro del médico y, por lo tanto, cómo se forman en el futuro. Tanto Dinamarca como Canadá se destacan en su enfoque para definir el papel de un médico y las competencias requeridas, incluida la gestión y el liderazgo, para ser profesionales eficaces. El Real Colegio de Médicos y Cirujanos de Canadá desarrolló el Marco de Roles de CanMEDS y las competencias asociadas. CanMEDS «es un marco de competencias, una guía de las habilidades esenciales que los médicos necesitan para obtener resultados óptimos para los pacientes» (Frank, 2005, p. 1). «Constituye la base de los estándares de la misión educativa del Royal College y se ha incorporado a la acreditación, la evaluación y los exámenes, así como a los objetivos de formación y a los estándares para el desarrollo profesional continuo» (Frank, 2005, p. 1). Puede 5.4 Enfoques por competencias en otros países 65 ser utilizados por educadores, maestros, pasantes, médicos en ejercicio, investigadores y otros profesionales de la salud. Es importante destacar que puede utilizarse como «base para los planes de estudio de medicina y a lo largo de todo el continuo de aprendizaje del médico, desde el nivel de pregrado, durante la residencia y el desarrollo profesional continuo» (Frank, 2005, p. v). Se trata de seis funciones con competencias asociadas que se combinan para proporcionar un papel central de «experto médico». Estas funciones son, en efecto, lo que se espera de un buen médico; Es decir, además de ser un experto médico, un médico debe ser un
● Profesional
● Comunicador
● Colaborador
● Gerente
● Defensor de la salud
● Erudito Curiosamente, desde el marco original, ‘gerente’ se ha cambiado por ‘líder’.
CanMEDS enfatiza que los médicos se comprometen con otros para contribuir a una visión de un sistema de atención médica de mayor calidad y asumen la responsabilidad de brindar una excelente atención al paciente a través de sus actividades como clínicos, administradores, académicos o maestros.
El modelo CanMEDS ha sido adaptado por un gran número de países. CanMEDS no es un grupo de competencias de gestión y liderazgo médico. Se establece en un alto nivel de descripción e implica una serie de subconjuntos subyacentes de competencias en términos de cómo se lograrían realmente en la práctica mediante la aplicación de habilidades y conocimientos específicos a situaciones particulares.
La Junta del Sindicato Nacional de Consultores de la Asociación Médica Danesa desarrolló un modelo de liderazgo, que incluía cinco competencias básicas de liderazgo:
● Liderazgo personal
● Liderazgo en un contexto político
● Calidad líder
● Liderar el cambio
● Profesionales líderes: También incluyeron ocho roles para el consultor como líder profesional (estos son similares a los roles de CanMEDES):
● Perito médico
● Profesional
● Líder/administrador
● Académica
● Colaborador
● Comunicador
● Promotor de la salud
● Asesor (Colegio Médico Danés, 2006).
Estas funciones forman parte de la cultura médica danesa e influyen en los comportamientos y el plan de estudios, y también forman parte de los criterios de nombramiento. Los planes de estudio, tanto a nivel de pregrado como de posgrado, se basan en estos ocho roles. Esto incluye la formación obligatoria en gestión y liderazgo antes de que se otorgue el equivalente a un Certificado de Finalización de la Formación (CCT), lo que proporciona acceso para solicitar puestos de consultor y GP. Inmediatamente después de su nombramiento, se espera que todos los nuevos consultores hospitalarios, como parte de su desarrollo profesional continuo, participen en otros programas de desarrollo de liderazgo dirigidos conjuntamente por la Asociación de Consejos de Condado de Dinamarca y la Asociación Médica Danesa, por ejemplo, «Eres un buen médico, ¿también eres un buen líder?» La RACMA es una de las pocas facultades de medicina en el mundo acreditada para ofrecer administración médica como especialidad.
El Colegio se creó en 1963 como respuesta a la necesidad de una asociación profesional que se ocupara de la especialidad de la administración médica. A diferencia de otros países, los médicos en formación pueden optar por seguir la especialidad de administración médica. El programa de formación de RACMA tiene como objetivo desarrollar médicos capaces de liderar desde puestos de alta dirección y dirección ejecutiva. Un número significativo de Directores de Servicios Clínicos en Australia y Nueva Zelanda son becarios de RACMA. Por lo tanto, los becarios de RACMA han experimentado el mundo clínico como estudiantes y pasantes de posgrado antes de decidir que la administración médica es su interés. El Plan de Estudios de Liderazgo y Gestión Médica de RACMA define las capacidades y competencias para la formación, el logro y la mejora de las habilidades del administrador médico especialista. El plan de estudios está acreditado por el Consejo Médico Australiano. Los médicos que completen satisfactoriamente el programa de formación son elegibles para unirse a RACMA como becarios. MacCarrick (2014) confirma que RACMA ha adaptado el marco de CanMEDS conceptualizando el liderazgo como el principal pilar que sustenta las siete competencias de CanMEDS, es decir, experto médico, comunicador, defensor, académico, profesional, colaborador y gerente/líder. En la figura 5.1 se resumen estas siete competencias de rol y el tema de competencia de cada una. Dentro de cada uno de los temas de competencias de rol, el currículo define un conjunto de metas que se clarifican a través de un conjunto de competencias y objetivos facilitadores. CanMEDS ha tenido un impacto significativo en los planes de estudio de medicina en muchas partes del mundo. Influyó en el desarrollo del programa canadiense LEADS in a Caring Environment (Colegio Canadiense de Líderes en Salud, 2013). Como confirman Sebastian et al. (2014), Health LEADS Australia, un marco nacional de liderazgo en salud, fue desarrollado por el nuevo Health Workforce Australia basado en el marco canadiense. Como parte del desarrollo de Health LEADS Australia, se consultó a los educadores médicos, y se esperaba que el marco pudiera incorporarse a todos los planes de estudio de las escuelas de medicina y especialidades de posgrado, pero, por desgracia, hay poca evidencia de que tuviera algún impacto en este momento.

● Creando la visión
● Implementación de la estrategia La Academia de Liderazgo del NHS produjo un nuevo Modelo de Liderazgo en la Atención Médica (2013) para ayudar al personal a convertirse en mejores líderes en su función diaria, independientemente de si se encuentra en un entorno clínico o no clínico. Comprende nueve dimensiones:
● Inspirar un propósito compartido
● Liderar con cuidado
● Evaluación de la información
● Conectando nuestro servicio
● Compartir la visión
● Involucrar al equipo
● Rendir cuentas
● Desarrollar la capacidad
● Influir en los resultados
Roles y modelos de liderazgo
Diplomatura en modernos hospitales
6 Entrega de habilidades blandas
Peter Spurgeon. John Clark
Introducción
Muchos de los comentaristas que defienden la necesidad de un mayor liderazgo médico tienen una experiencia considerable en la configuración y prestación de servicios de salud a nivel estratégico y operativo, aunque, curiosamente, la mayoría no tiene experiencia académica particular en el estudio del concepto de liderazgo en sí. Como consecuencia, muchos defensores escriben sobre el liderazgo como si hubiera un solo concepto al que todos se adhieren o, alternativamente, sin especificar ningún enfoque o modelo particular de liderazgo.
¿Importa este enfoque poco específico del concepto de liderazgo?
Probablemente no demasiado en el nivel más general, donde hay consenso en cuanto a la necesidad de una mayor implicación positiva de los médicos en la gestión y el desarrollo de las organizaciones en las que trabajan. Sin embargo, con respecto al concepto de compromiso, que cuando se trata de vincular comportamientos particulares o de desarrollar el liderazgo, se vuelve bastante más importante comprender y diferenciar algunos de los muchos enfoques del liderazgo. No es apropiado explorar más de un siglo de investigación sobre el liderazgo, pero puede ser útil discutir uno o dos aspectos clave y ver cómo estos podrían relacionarse con los posibles roles de los líderes médicos y cómo los médicos podrían estar preparados para tales roles. Para una discusión completa de los enfoques del liderazgo, se remite al lector a Northouse (2010).
4.2 LIDERAZGO: EL CONCEPTO
La forma en que hablamos de liderazgo y el lenguaje utilizado para describirlo a menudo sugiere un modelo o concepto implícito de liderazgo.
Como sugieren Spurgeon y Cragg (2007), existe una tendencia a confundir la pregunta «¿quiénes son los líderes?» con «¿qué hacen los líderes?»
El primer enfoque enfatiza la noción de liderazgo como una capacidad personal y ha tendido a producir una serie interminable de listas de cualidades personales que un individuo designado como líder podría poseer. Inevitablemente, no existe un parangón que esté a la altura de todas estas cualidades. Las listas parecen implicar algún tipo de tipo ideal, mientras que la realidad es que un individuo puede poseer algunas de estas características personales hasta cierto punto. Nunca se especifica cuánto de cada uno se necesita para ser un líder. Como las personas funcionan como líderes, se deduce que hay un conjunto casi infinito de combinaciones de características personales que pueden permitir a alguien ser un líder, y la conclusión crítica que sigue es que hay muchas formas diferentes en las que se puede ejercer el liderazgo. Comprender que no existe un único conjunto universal de características que definan a un líder explica en gran medida por qué el término liderazgo y todas las cualidades asociadas con él pueden crear confusión. Además, de manera más constructiva, sugiere que muchos individuos pueden contribuir como líderes, pero de maneras muy diferentes, dependiendo de su propio conjunto particular de fortalezas y debilidades.
Grint (2001) sugiere que el término liderazgo es tan «multifacético» y que existen tantas construcciones que muchos autores, al escribir sobre liderazgo, no definen exactamente lo que significan. En gran medida, este es exactamente el caso en el contexto del liderazgo médico. Una de las definiciones más comúnmente aceptadas de liderazgo proviene de Northouse (2010, p. 3), un autor importante en el campo que ofrece «un proceso mediante el cual un individuo influye en un grupo de individuos para lograr un objetivo común». Spurgeon y Klaber (2011) se basan en esta noción, sugiriendo que el liderazgo podría considerarse como un «proceso de influencia mediante el cual aquellos sujetos a él se inspiran, motivan o están dispuestos a emprender las tareas necesarias para lograr un objetivo acordado».
Este enfoque tiene dos implicaciones particulares e importantes en la forma en que pensamos sobre el liderazgo. En primer lugar, es especialmente relevante para el concepto de liderazgo colectivo, compartido o distribuido, ya que sugiere que muchos pueden contribuir al liderazgo (tener influencia) en lugar de invertir todo el poder de liderazgo en un solo individuo. En segundo lugar, permite que el liderazgo sea visto como un conjunto de comportamientos -que influyen en los demás- y que pueden desarrollarse y mejorarse. Como consecuencia, el proceso de investigación en el trabajo de liderazgo se ha centrado en gran medida en identificar cuáles son las fuentes de influencia ejercidas por el individuo en el ejercicio del liderazgo.
Willcocks (2005) ofrece una descripción muy sucinta de los principales enfoques para entender el liderazgo y, lo que es más importante, intenta relacionar estos modelos en términos de su aplicabilidad al mundo médico.
Los enfoques que describe se agrupan bajo el epígrafe de
● Teoría de los rasgos
● Estilos de liderazgo
● Teoría de la contingencia
● Liderazgo transaccional/transformacional
● Liderazgo compartido o distribuido
Existe una secuencia temporal para la posición relativa de cada uno de estos enfoques, comenzando con los modelos de rasgos que dominaron hasta la década de 1930. Aunque cada modelo ha adquirido un cierto dominio en un período determinado en el tiempo, el modelo anterior no ha desaparecido por completo. Las líneas de pensamiento de un enfoque tienden a resurgir o persistir y quedar abarcadas en enfoques posteriores, a menudo reformulados.
4.2.1 Teoría de los rasgos
Este fue el primero de los enfoques y puso gran énfasis en las características personales que poseían los líderes eminentes, generalmente líderes militares o políticos. A pesar de una gran cantidad de investigación y a pesar de una lista muy grande y larga de características potenciales, ha surgido un conjunto bastante limitado de características: inteligencia, confianza en sí mismo, impulso, integridad y logros. No es de extrañar que se trate de una lista y que parezca casi una reafirmación semántica del propio término liderazgo. Higgs (2003) ha sugerido añadir la inteligencia emocional a la lista. Tal vez no sea sorprendente que la inteligencia emocional, con su énfasis en la lectura de las emociones, la comprensión de las señales, la confianza social y la comunicación, se perciba como relevante para la dinámica de la gestión moderna. Jung y Sosik (2006) informan que los líderes carismáticos individuales están interesados en la gestión de la impresión, el logro del poder y la autorrealización. A fin de que tengan valor práctico, las características que surjan en relación con el liderazgo tendrían que ser estables en una variedad de situaciones, y existe un consenso en cuanto a los elementos de la lista. Desafortunadamente, ninguna de las dos posiciones se mantiene. El enfoque de los rasgos también ve implícitamente el liderazgo como un conjunto innato de cualidades que poseen algunos y no otros, por lo tanto, niega muchos de los intentos de entrenar o desarrollar tales cualidades. Más recientemente, Alimo-Metcalfe y Alban-Metcalfe (2001) han reavivado el interés en las características clave y en cómo podrían permitir el liderazgo.
Los descriptores son más sofisticados (inspirador, íntegro, interés genuino, accesible) y más complacientes con un contexto moderno, pero siguen siendo una lista y se mantienen todas las advertencias: ¿es esta la única lista acordada?, ¿un líder necesita todo o algo y cuánto de cada uno?, ¿se aplican por igual en todas las circunstancias? Se podría argumentar que el enfoque de rasgos tiene cierta resonancia con la profesión médica, dado el énfasis puesto en las características personales clave en el proceso de selección de pregrado. Pero como señala Willcocks (2005), si bien muchos médicos tienen muchas cualidades de liderazgo, no todos los médicos poseen las mismas cualidades. Puede haber una distribución diferente en las diferentes especialidades y, además, el médico puede emplear cualidades personales en un contexto principalmente paciente-médico y no necesariamente en el contexto dinámico del grupo de liderazgo. Aunque intuitivamente atractivo, el enfoque de rasgos parece tener un valor bastante limitado en organizaciones complejas y diversas y en la sociedad.
4.2.2 Estilos de liderazgo
El enfoque de estilo es en parte una reacción a las deficiencias del enfoque de rasgos y a su incapacidad para reconocer el impacto de la situación en la que se produjo el liderazgo.
Es esencialmente un modelo dicotomizado en el que los líderes se centran en la tarea o en las personas involucradas. Es útil entender que el liderazgo necesita atender a la tarea o a las relaciones dentro del grupo. Lo ideal es atender implícitamente a ambos de manera simultánea e igualitaria, pero realmente depende de la situación y más aún de las necesidades de los seguidores. La noción de una elección de un estilo de liderazgo se hunde un poco en el fracaso de determinar si hay un «mejor» estilo o cómo se determina qué estilo es apropiado en un momento dado. Esta misma deficiencia es evidente en el contexto de la medicina, donde puede ser bastante incierto si las diferentes especialidades o grupos de especialidades exigen características personales particulares, por no mencionar la gama de tipos de seguidores dentro de los equipos o grupos.
4.2.3 Enfoque de contingencia
Una vez más, en una consecuente evolución del modelo descrito anteriormente, este enfoque trata de reconocer y describir la complejidad de las diferentes situaciones de tal manera que sugiera qué estilo puede ser el más apropiado. Si bien es un modelo atractivo para tratar de integrar el estilo y el contexto, ha sido criticado por tomar un conjunto de situaciones bastante estrechamente definidas y, como sugiere Darmer (2000), depende más bien de quién defina la situación en cuestión. El enfoque también exige una conciencia de los diferentes modelos de liderazgo y la nada desdeñable doble capacidad de reconocer cuándo se requiere un enfoque particular, es decir, ser capaz de reconocer las demandas de la situación y también ser capaz de poner en práctica cualquier modelo que parezca apropiado. El modelo situacional, tal como lo respaldan Hersey y Blanchard (1993), resulta útil de nuevo cuando intentan describir qué tipo de comportamiento se necesita —más directivo o más de apoyo— dependiendo de las características de los seguidores. Sin embargo, también es este enfoque bastante prescriptivo el que puede ser una debilidad del modelo, ya que asume que los componentes del modelo son los únicos factores que influyen en los comportamientos de liderazgo, ignorando una serie de otros factores. En la práctica, en un entorno sanitario, la experiencia sugiere que es poco probable que exista una selección lo suficientemente amplia de posibles líderes clínicos como para poder adaptarse al estilo y al contexto, o incluso que el contexto sea lo suficientemente susceptible de adaptación en caso de que el líder designado intente modificarlo. Aquí se puede ver una explicación para muchos de los enfrentamientos entre un director clínico y otros colegas clínicos que, o bien no ven el contexto de la misma manera que el líder, o bien no están dispuestos a cambiarlo.
4.2.4 Enfoque transaccional/transformacional
Esta corriente más reciente de pensamiento sobre el liderazgo deriva en parte de los procesos de globalización que provocan una mayor inestabilidad y turbulencia en los entornos externos. En estas circunstancias, ser capaz de hacer frente al cambio constante y de motivar e inspirar a otros a ver más allá de la dislocación inicial de las fuerzas de cambio se considera clave, y esta es la característica definitoria del liderazgo transformacional. Se define en contraste con el enfoque de gestión más tradicional (descrito como transaccional), que busca establecer orden y control y quizás esté más en sintonía con entornos externos más estables. Esta noción de liderazgo transformacional ha demostrado ser bastante atractiva, ya que proyecta a los líderes enfrentando circunstancias impredecibles y dinámicas en contraposición a la imagen más seria y estable del gerente. Sin embargo, el liderazgo transformacional corre el riesgo de volver a caer en el enfoque de rasgos, ya que es bastante difícil de medir y parece enfatizar la naturaleza carismática y heroica (y, por lo tanto, rara) del liderazgo en circunstancias difíciles. A menudo hay un deseo en algunos de ver la gestión y el liderazgo como algo muy distinto, lo que a menudo plantea la pregunta: «¿Pero está usted hablando de gestión o liderazgo?» Spurgeon y Cragg (2007, p. 98) argumentan que se trata más bien de una falsa dicotomía, ya que las ven más como una dimensión y tienen una relación complementaria. Sugieren que «lograr y mantener un cambio inspirado por los líderes requiere experiencia en gestión. Por lo tanto, las dos funciones se apoyan y complementan entre sí. Varían en énfasis y son más o menos apropiados en diferentes momentos dependiendo de las circunstancias. Ambos roles son necesarios, pero está claro que algunos gerentes podrán ofrecer liderazgo adicional, mientras que otros no. Del mismo modo, muchos líderes sobresalientes también son gerentes muy competentes, pero ese no es necesariamente el caso de todos los líderes. Grint (2002) da una mirada bastante irónica al tema, señalando que los políticos suelen culpar de los males del Servicio Nacional de Salud (NHS) a los gerentes por su falta de control y a los líderes por no dar dirección. Al menos, es un conveniente desplazamiento de la culpa. Grint plantea la fascinante pregunta de qué hacen realmente los líderes. Al explorar esto, describe la relación entre líderes y seguidores como crucial. Este último debe asentir a lo que el líder prescribe o el líder se vuelve impotente. La noción de que hay un líder perfecto que tomará todas las decisiones correctas o un sistema perfectamente administrado que no permitirá errores es bastante fantasiosa. Los 50 años de programas de desarrollo de liderazgo seguramente ya habrían resuelto todo esto si pudiéramos invertir esta experiencia perfecta en un individuo. Es más probable, como sugiere Grint, que reconozcamos que el liderazgo funciona en muchos niveles de la organización y que alentar a todos a persuadir e influir en otros para que tomen la acción apropiada es la forma en que el liderazgo será realmente efectivo. Esta es en gran medida la filosofía detrás del surgimiento del Marco de Competencias de Liderazgo Médico (MLCF), descrito más adelante en este texto, ya que ve la adquisición de competencias básicas en habilidades de liderazgo por parte de todos los médicos como una parte común y universal de la capacitación y el desarrollo como la forma en que se ubicará un liderazgo más efectivo en los sistemas de salud (y a otros grupos profesionales, ya que el MLCF se ha extendido a otros grupos clínicos como el Marco de Competencias de Liderazgo Clínico). El liderazgo transformacional es muy atractivo y tiene el potencial de provocar una coalescencia en torno a una idea o dirección entre líderes y seguidores. Por otra parte, Yuki (1999) reporta evidencia de que el liderazgo transformacional es una forma efectiva de liderazgo. El enfoque en las características personales del líder ha hecho que muchos critiquen el liderazgo transformacional como una redirección de nuestra comprensión del liderazgo hacia atrás hacia los rasgos personales y una noción del líder «heroico», rechazada en gran medida en el contexto de organizaciones complejas (King’s Fund, 2012). Sin embargo, Kouzes y Posner (2002) articularon el liderazgo transformacional como un conjunto de comportamientos clave (Modelar el Camino, Inspirar una Visión Compartida, Desafiar el Proceso, Permitir que Otros Actúen, Alentar el Corazón) que, según argumentan, se pueden aprender y adquirir, por lo tanto, no dependen de rasgos de personalidad sobresalientes. Al considerar la aplicabilidad del liderazgo transformacional al contexto de la atención médica, es atractivo ver cómo los líderes médicos con este enfoque podrían crear un estado de ánimo para el cambio en sus colegas clínicos. Sin embargo, persiste la tensión en el hecho de que el origen del cambio propugnado a menudo parece surgir de fuentes externas y, como consecuencia, puede ser visto con recelo por muchos (especialmente los clínicos) que trabajan dentro del sistema. Para tener éxito, el liderazgo transformacional parece requerir un verdadero compromiso y pasión por los objetivos del cambio. Es posible que esto no siempre se alinee bien cuando parece que muchos cambios inspirados externamente buscan dirigir y controlar la operación de grupos previamente autónomos. Una articulación más reciente de esta cuestión, es decir, si los líderes realmente creen en lo que dicen y hacen, es el concepto de «liderazgo auténtico» (Northouse, 2010). Como su nombre lo indica, estos líderes se describen como genuinos, que actúan con convicción y representan en gran medida sus propios valores personales en lo que hacen. Este es un modelo de liderazgo relativamente nuevo, y aunque tiene el atractivo de una base moral para el comportamiento del liderazgo, sigue sin estar claro cómo se traducen los valores en acción y, por supuesto, las guerras también se han librado en torno a la convicción moral de un líder. Claramente, no todos vemos la base moral de las acciones de la misma manera. De hecho, dentro del NHS, existen cuestiones importantes en torno a quién está desarrollando y definiendo la visión que persigue el auténtico líder. A menudo se anima a las personas que ocupan puestos de alto nivel en el NHS a crear culturas excelentes e inspiradoras en su organización. Sin embargo, esto supone más bien una mayor influencia y control sobre el contexto externo que en un servicio tan acosado por un intenso escrutinio e intervención política. Estos son, pues, los principales enfoques históricos tanto para el estudio como para la aplicación del liderazgo. Seguramente hay otros que podrían ser discutidos como sutiles desviaciones y adaptaciones de estos modelos principales. Probablemente sea importante considerar solo uno o dos más, sobre todo el liderazgo compartido y el liderazgo adaptativo, ya que son particularmente relevantes para el contexto de la atención médica, uno en particular que sustenta el enfoque del MLCF, descrito y defendido en este texto.
4.2.5 Liderazgo compartido
El liderazgo compartido es una concepción más moderna del liderazgo que se aleja de los modelos carismáticos o jerárquicos tradicionales. Los problemas y las organizaciones cada vez más complejos han visto una dependencia cada vez mayor de los equipos multidisciplinarios.
El liderazgo compartido es un enfoque que puede apoyar y apuntalar esta forma de trabajar. El liderazgo compartido puede definirse como un proceso dinámico, interactivo e influyente entre individuos en grupos, con el objetivo de guiarse mutuamente al logro de objetivos grupales u organizacionales. Una distinción clave entre los modelos de liderazgo compartidos y tradicionales es que el proceso de influencia implica algo más que la influencia descendente sobre los subordinados por parte de un líder posicional. El liderazgo se distribuye entre un conjunto de individuos en lugar de estar centralizado en manos de un solo individuo que actúa en el papel de líder (Pearce y Conger, 2003). La experiencia, el conocimiento y la capacidad individual de cada miembro del equipo se valoran y son utilizados por el equipo para distribuir o compartir el trabajo de liderazgo a través del equipo en respuesta a cada contexto y desafío que se enfrenta. El equipo multidisciplinar se ha convertido en la unidad organizativa de más rápido crecimiento. Ya no es posible que una persona o una disciplina tenga todo el conocimiento y la experiencia para resolver la complejidad de los problemas actuales.
Por ejemplo, los gobiernos, al tratar de encontrar una solución al calentamiento global, deben asegurarse de que los científicos, ingenieros, geógrafos, meteorólogos, biólogos, botánicos, oceanógrafos, médicos, programadores informáticos, ecologistas y fabricantes aporten sus conocimientos y experiencia únicos a este complejo problema. Es más probable que los avances provengan de la interacción entre todas las diferentes disciplinas en lugar de que una sola disciplina funcione por sí misma. Este enfoque es igualmente relevante dentro de un entorno clínico.
Los médicos se están especializando cada vez más como resultado directo de los avances en tecnología y ciencia que mejoran nuestro conocimiento médico. Por ejemplo, en el caso de los pacientes con cáncer, los equipos de diferentes especialidades y con diferentes áreas de especialización, por ejemplo, cirujanos, oncólogos, anestesistas, especialistas en cuidados paliativos, enfermeras especialistas, enfermeras generales, terapeutas alternativos, radiólogos, enfermeras Macmillan, médicos generales, fisioterapeutas y otros, todos tienen una contribución que hacer a la planificación y prestación de la atención.
Dentro de un modelo de liderazgo compartido, el liderazgo pasa de individuo a individuo a lo largo del camino de atención del paciente. Esto proporciona continuidad de la atención para el paciente a través de un trabajador clave o asistente social sin comprometer los estándares de atención. A este equipo clínico le apoyan otras redes, como servicios de apoyo, servicios de laboratorio, fabricantes, administradores y gerentes. Pearce et al. (2009) proporcionan una serie de ejemplos de éxito de liderazgo compartido en una variedad de sectores.
Konu y Viitanen (2008) también sugieren en el sistema de salud finlandés que vieron que el liderazgo compartido resultó en un aumento de la innovación, la motivación y la preparación para el desarrollo.
En el ámbito de la salud, un modelo de liderazgo compartido vería la atención del paciente en cualquier punto de su viaje dirigida por la persona más capaz, con la experiencia clave para llevar a cabo la tarea.
El liderazgo compartido tiene que ver con la calidad de la interacción más que con la posición formal de un individuo.
El potencial del uso del MLCF en la formación de médicos para desarrollar una mejor comunicación, trabajo en equipo e innovación es una razón clave por la que el modelo es tan importante para toda la iniciativa. Esto pone de relieve lo señalado anteriormente en el sentido de que el uso del término liderazgo sin una explicación más detallada del modelo o enfoque puede ser inútil.
El liderazgo compartido o distribuido es el modelo que tiene más probabilidades de abarcar y liberar el considerable potencial de liderazgo del personal médico y clínico. Serg et al. (2016) han desarrollado recientemente el concepto de liderazgo compartido al distinguir los tipos de liderazgo compartido. Reafirman que los modelos de liderazgo colectivo emergen como particularmente relevantes en el contexto de las organizaciones de salud, ya que se ajustan mejor a la complejidad inherente de estas organizaciones. Pero igualmente, reconocen que no siempre está claro cómo se promulgará un modelo de liderazgo compartido.
Sugieren dos dimensiones útiles para comprender mejor ese proceso.
El primero de ellos se construye en torno a la noción de formalidad: ¿se identifica a individuos particulares como líderes en momentos particulares y en circunstancias particulares, o es un papel que simplemente surge durante el proceso de trabajo? Estos los describen como estructurados o emergentes.
La segunda dimensión se relaciona con quién, tanto los líderes como los seguidores, están involucrados en un proceso en particular. A estos los etiquetan como coalicionales (donde un grupo de líderes influye en un grupo mucho más grande) y mutuos (donde los miembros de un grupo acuerdan liderarse mutuamente según la necesidad y el requisito del contexto).
Es útil tener una mayor comprensión del funcionamiento del liderazgo compartido, ya que parece ser el modelo preferido en las organizaciones modernas y, sin embargo, existe cierta incertidumbre sobre cómo funciona en un momento determinado. Esto, por supuesto, es parte del desafío del liderazgo para reconocer y adaptarse a las necesidades específicas de una situación dada. Curiosamente, este número también se refiere a una crítica estándar de los modelos de liderazgo basados en competencias.
Boden y Gosling (2006) argumentan que los modelos de competencias enfatizan el liderazgo individual, ignorando el contexto y la situación, y se vuelven estáticos y mecanicistas. Esto es, en parte, una crítica a los modelos de competencias basados en un mal uso de las competencias. En primer lugar, se pueden actualizar cuando sea necesario. Además, representan una gama de habilidades que todos los individuos pueden adquirir, abriendo así el proceso de liderazgo a todos en lugar de a un individuo clave. Por último, el comentario de que reconocer las demandas de las situaciones particulares es, por supuesto, importante, pero suponer que estas señales contextuales pueden enseñarse y reconocerse para que se produzca el comportamiento de liderazgo adecuado es en sí mismo extremadamente mecanicista.
4.3 ¿CÓMO SUSTENTA EL LIDERAZGO COMPARTIDO EL MLCF?
El MLCF se basa en el concepto de liderazgo compartido, en el que el liderazgo no se limita a las personas que desempeñan funciones de liderazgo designadas y en el que existe un sentido compartido de responsabilidad por el éxito de la organización y sus servicios. Los actos de liderazgo pueden provenir de cualquier persona de la organización, según corresponda en diferentes momentos, y se centran en el logro del grupo más que en el de un individuo. Por lo tanto, el liderazgo compartido apoya activamente el trabajo en equipo efectivo. En el complejo mundo de la salud, la creencia de que una sola persona es el líder o gerente está lejos de la realidad. El liderazgo es un comportamiento basado en competencias que debe provenir de todos los implicados en la atención sanitaria.
Los médicos trabajan en equipos multidisciplinarios enfocados en las necesidades y seguridad del paciente, donde el liderazgo se convierte en responsabilidad del equipo.
Si bien hay un líder formal del equipo que es responsable del desempeño del equipo, la responsabilidad de identificar problemas, resolverlos e implementar la acción apropiada es compartida por el equipo.
El papel del líder formal es crear el clima en el que el equipo pueda prosperar a través de la construcción de equipos, la resolución de conflictos y la claridad de la visión. La evidencia muestra que el liderazgo compartido puede aumentar la asunción de riesgos, la innovación y el compromiso, lo que debería resultar en una mejor atención para el paciente y una organización que sea receptiva, flexible y exitosa.
Los miembros del equipo pueden demostrar actos de liderazgo desafiando al equipo mientras el equipo establece las normas y protocolos en los que trabaja el equipo, gestionando las diferencias utilizando todas las habilidades, conocimientos y juicio profesional de los miembros individuales en beneficio de todo el equipo.
4.4 ¿CÓMO SE RELACIONA EL LIDERAZGO COMPARTIDO CON EL LIDERAZGO POSICIONAL Y EL AUTOLIDERAZGO?
4.4.1 Liderazgo posicional
Los roles de liderazgo posicional son aquellos que los individuos asumen dentro de la estructura formal de su organización. Las personas son designadas para esos roles sobre la base de su experiencia pasada y su potencial futuro para ser parte de la estructura formal de responsabilidad dentro de una organización. Los roles en sí mismos tienen un conjunto de expectativas a su alrededor, independientemente de las personas que los ocupen. Ejemplos de roles de liderazgo posicional dentro de la atención médica son gerentes de sala, matronas, directores clínicos, directores médicos, directores de enfermería, directores financieros, directores, directores ejecutivos, directores no ejecutivos y presidentes. Comprendemos, en principio, las responsabilidades de estos roles y no tendríamos dificultad en ubicarlos en un diagrama formal de la jerarquía organizacional.
El liderazgo compartido es producto de la cultura de la organización. Cuando una organización está dominada por el conocimiento e involucra equipos de individuos que trabajan colectivamente hacia un objetivo compartido (como el NHS), entonces florecerá el liderazgo compartido.
Donde la norma cultural es la jerarquía con el poder y la influencia provenientes de la cima, entonces tenderá a existir una norma de líder/seguidor más posicional. De alguna manera, la atención médica ha liderado el camino, incorporando cada vez más individuos a equipos multidisciplinarios para la atención de los pacientes. Los niños con necesidades especiales tienen paquetes de atención complejos que dependen de los conocimientos y habilidades de un equipo muy variado que cruza los límites entre la atención médica, la atención social y la educación. En el caso de un niño con parálisis cerebral, esto puede incluir maestros especialistas, un coordinador de necesidades educativas especiales, fisioterapeutas, terapeutas ocupacionales, un audiólogo, un optometrista, un pediatra comunitario, un pediatra general hospitalario, un cirujano pediátrico, un neurólogo, equipos de enfermería comunitaria y hospitalaria, cuidadores de relevo, trabajadores sociales y otros. Diferentes acontecimientos influirán y cambiarán los aspectos clave para el niño y su familia, por lo que el foco principal de la atención tendrá que moverse en consecuencia. Un enfoque de liderazgo compartido es el modelo que mejor apoya esto.
El MLCF proporciona un medio útil para integrar el liderazgo compartido en la práctica. Por ejemplo, si el líder de posición (en este caso, el director clínico) le pide al equipo que atiende a niños con necesidades complejas que revise su servicio actual, podría comenzar por establecer la dirección del servicio; A continuación, buscarían formas de mejorar el servicio a través de su experiencia en la gestión del servicio. Examinarían cómo trabajaban en equipo y las cualidades personales de todos los miembros del equipo. Ningún individuo podría tener el conocimiento y la experiencia para incorporar todas las dimensiones, por lo que utilizarían el liderazgo compartido para incorporar los puntos de vista de todos los miembros del equipo y utilizarían la interrelación para innovar nuevas soluciones. Hartley y Benington (2010) analizaron recientemente el liderazgo específicamente en el contexto de la atención médica. Es interesante observar en su análisis de los cambios en la prestación de servicios de salud por qué ven una mayor demanda de nuevos y mejores líderes en atención médica. Cambiar los patrones de la enfermedad con mayor énfasis en la prevención, los cambios en el estilo de vida, las intervenciones basadas en la comunidad y un público más educado y exigente requerirá una forma de respuesta de liderazgo más orientada hacia el exterior. Del mismo modo, sugieren que la necesidad de un mayor trabajo en equipo en la forma en que se presta la atención, el ritmo de la innovación y el cambio y la demanda de una mejora continua del servicio, especialmente con respecto a la seguridad del paciente, plantearán enormes demandas a los líderes profesionales que trabajan en entornos sanitarios.
4.4.2 Autoliderazgo
El autoliderazgo está en el corazón del liderazgo compartido. Los líderes deben ser autolíderes efectivos, comprendiéndose a sí mismos y su impacto en los demás a través de la autorregulación, la autogestión y el autocontrol. Ser consciente de sí mismo es preguntarse: ‘¿Qué impacto estoy teniendo?’ ¿Quién es mejor que yo en esto?’ y ‘Esto no funciona, ¿qué tengo que cambiar? Los autolíderes necesitan aprender a liderarse a sí mismos antes de que puedan liderar a otros en el equipo u organización (Houghton et al., 2002, pp. 126-132). El autoliderazgo y el liderazgo compartido son complementarios, y los autolíderes aceptarán de buena gana y con entusiasmo los roles y responsabilidades de liderazgo compartidos, ya que esta puede ser la única forma de hacer el trabajo en organizaciones complejas. El MLCF reconoce que el autoliderazgo es un componente básico para el liderazgo, y esto se articula dentro del dominio de la Demostración de Cualidades Personales (véase el Capítulo 5). El MLCF también reconoce dentro de su dominio de Trabajo con Otros que, si bien algunos médicos asumirán roles de liderazgo posicional, todos los médicos, como individuos, serán líderes trabajando con otros en equipos multidisciplinarios, tomando decisiones sobre la atención al paciente, así como siendo miembros de equipos organizacionales tomando decisiones sobre recursos, personas y estrategia.
4.5 LIDERAZGO ADAPTATIVO
Este modelo descrito por Heifetz (1994) puede resonar con aquellos que luchan con problemas aparentemente intratables en el NHS y también con el debate en torno a la gestión y el liderazgo. Heifetz sugiere que hay que hacer una distinción entre los problemas principalmente técnicos, para los que hay un acuerdo general sobre lo que hay que hacer, y los problemas adaptativos, en los que hay incertidumbre y desacuerdo sobre lo que hay que hacer. Con el fin de abordar los problemas adaptativos, Heifetz describe un marco o conjunto de procesos que involucran esencialmente al equipo o la comunidad donde se basa el problema y proporcionan un entorno seguro pero desafiante donde se alienta a las personas a concentrarse en crear una solución al problema «perverso». Es evidente que hay aspectos del enfoque que se prestan para promover la innovación y, como tales, pueden ser útiles para los retos a los que se enfrentan muchos sistemas de salud. Aunque todavía no es una fuerza importante en términos de liderazgo, el enfoque puede proporcionar principios útiles en términos del «debate» que muchos han pedido con respecto al futuro del NHS y su nivel de financiación.
4.6 ROLES CLAVE DE LOS LÍDERES MÉDICOS
Durante la última década, ha habido un crecimiento constante en el número de roles de liderazgo médico designados. Ya hemos hablado de cómo han evolucionado estos roles, pasando de una posición bastante vacilante en la que había incertidumbre sobre el valor de los roles y un entusiasmo limitado por parte de quienes ocupaban estos puestos. Hoy en día, los empleados eficaces en estos puestos son fundamentales para el cambio del sistema y la organización. Curiosamente, a pesar de la criticidad de estos roles, es probable que la mayoría de los titulares tengan poca relación directa con el debate anterior sobre los modelos de liderazgo. Por lo tanto, el éxito (o no) en el ejercicio de las funciones ha dependido hasta ahora en gran medida de las cualidades personales que los individuos aportan al puesto. Es vital para el futuro que se adopte un enfoque más profesional de la preparación que implique una formación sistemática y sostenida de todos los clínicos en materia de gestión y liderazgo. De esta manera, se puede mejorar todo el nivel de prestación de servicios, cambio e innovación para hacer frente a los desafíos que se avecinan.
4.7 LIDERAZGO Y EDUCACIÓN MÉDICA
Angood y Shannon (2014), al escribir en el contexto del sistema de salud estadounidense, respaldan la opinión de que en tiempos financieros difíciles, habrá una demanda cada vez mayor de médicos líderes. Elaboran su posición para sugerir que los médicos están excepcionalmente calificados para el rol, como profesionales con una orientación natural hacia la medicina basada en la evidencia y un enfoque en la mejor atención para el paciente. También proporcionan una interfaz crucial entre la gestión y la medicina, con experiencia directa de cómo las presiones y decisiones organizativas afectan a la prestación de servicios en primera línea. Sin embargo, también señalan una brecha significativa en la provisión de capacitación para que los médicos adquieran las competencias de liderazgo necesarias. Creen que este proceso debería estar disponible a lo largo de todas las etapas de la carrera médica, como se ilustra en la implementación del MLCF McKimm y O’Sullivan (2016), en un texto editado recientemente, proporcionaron varias perspectivas útiles sobre el liderazgo clínico.
No menos importante es la contribución de Burr y Leung (2016), quienes, apoyando la importancia del liderazgo, también consideran que el papel es crucial para crear el nivel de compromiso en la fuerza laboral médica que crea una mejor calidad de la atención. En general, el texto conserva algunos elementos problemáticos. Su título es liderazgo clínico, pero casi todos los capítulos individuales se refieren a los médicos. Además, los propios editores concluyen que es probable que el MLCF sea reemplazado por el Modelo de Liderazgo en Salud. Este comentario ignora el hecho de que este último modelo no tiene currículo, esencial para la educación de pregrado y posgrado. También se asocia con material de aprendizaje y cursos que tienen un costo significativo y, por lo tanto, es casi seguro que nunca estarán disponibles para todos los médicos en formación. El comentario representa una visión bastante histórica de que, si algunos médicos asisten a algunos cursos, se hacen provisiones de liderazgo. Las últimas cuatro décadas indican claramente que esto no funcionará y que una provisión consistente de un modelo de liderazgo dentro del marco de la educación médica es esencial para proporcionar desarrollo para todos dentro de una profesión.
Una revisión de liderazgo del NHS dirigida por Lord Rose (2015) refleja este tipo de pensamiento al informar de una falta de liderazgo bueno y claro, especialmente en el personal clínico.
El modelo de implementación de la capacitación en liderazgo basado en el MLCF representa un enfoque que incorpora a todo el personal en un grupo profesional y también es neutral en cuanto a costos y, por lo tanto, alcanzable de manera realista.
La introducción e implementación del MLCF para todos los médicos proporcionará una plataforma básica de habilidades de gestión y liderazgo, aunque se requerirá más capacitación específica a medida que las personas pasen a puestos de liderazgo más formales.
El Impacto del Racismo en la Medicina: Una Investigación Necesaria
El racismo como tal no esta internalizado en Argentina, pero es innegable que existe discriminación, porque lo atiendan médicos de otros países que trabajan en las principales entidades sanatoriales de la Ciudad de Buenos Aires, es común escuchar me atendió un hermano latinoamericano (que formamos nosotros en las escuelas de residentes y en los cursos superiores) por lo tanto si los criticamos, lo estamos haciendo a nosotros mismos. Por ello me parece fundamental incorporar este análisis muy bien realizado y publicado hace unos meses, que se muestra por esta corriente artificiosa, maniatada y forzada, discriminatoria y que se opone a formas de discriminación positiva que esta proliferando el los nuevos gobiernos del planeta. Es importante dar un debate informado, las intenciones y los fundamentos, que esta detrás de lo que se dice, este puede ser un inicio de un proceso que avanzado puede ir hacia el odio racial y hacia determinadas minorías, puede ser, pero tenemos que impedirlo. Por ello les recomiendo leer este artículo y el incluido en otro posteo
Que se puede leer y cumplimenta este análisis.

El racismo que perjudica a los pacientes y a los médicos ha sido bien documentado en la literatura revisada por pares [ 1 , 2 ], en los informes gubernamentales [ 3 , 4 ] y en los medios de comunicación [ 5 , 6 , 7 ], en Canadá [ 8 ], en los Estados Unidos [ 9 ] y en el extranjero [ 10 ]. Si bien el antirracismo puede parecer que ha surgido recientemente en los comentarios y en las declaraciones institucionales [ 11 ], se han hecho llamamientos regulares [ 3 , 4 , 12 ] para que los médicos aborden el racismo desde al menos principios de los años 1990 [ 13 ]. A pesar de esto, el racismo en el campo médico ha persistido y continúa siendo malinterpretado [ 6 ] o negado [ 14 ], lo que causa daño a los médicos [ 15 , 16 ] y a los pacientes [ 8 , 17 ].
Una encuesta transversal de médicos en Alberta para explorar el racismo encontró que los médicos negros, indígenas y personas de color (BIPOC) experimentan una mayor prevalencia de racismo en el lugar de trabajo que sus pares blancos [ 18 ]. El análisis de las respuestas de texto en esta encuesta y otras [ 15 , 19 ] proporciona cierta comprensión de las formas en que el racismo se manifiesta en la atención médica, su impacto en los médicos y los pacientes, y propone posibles intervenciones para abordar el racismo; [ 20 , 21 , 22 ] sin embargo, el análisis cualitativo de los datos de las entrevistas que exploran profundamente las experiencias y creencias sobre el racismo en la medicina son menos comunes [ 23 ]. Además, no existe un marco unificador de múltiples niveles para comprender los impulsores del racismo persistente en el lugar de trabajo médico para informar el diseño de la intervención. El objetivo de este estudio actual fue explorar las experiencias y percepciones de los médicos sobre el racismo en una universidad canadiense utilizando entrevistas semiestructuradas para informar un modelo de impulsores del racismo persistente.
Terminología
La raza es una construcción social sin significado biológico que se utiliza para categorizar a las personas en grupos según su apariencia, a los que luego se les asigna un valor social [ 24 ]. La discriminación racial es poner en desventaja a una persona en función de su raza percibida, y el racismo es la discriminación racial más el uso del poder para alterar los resultados de un grupo de personas [ 24 ]. Las personas blancas pueden experimentar discriminación racial, pero no racismo, debido a su privilegio en la sociedad [ 24 , 25 ].
En este estudio, agrupamos las identidades raciales de los participantes en blancos o negros o indígenas, asiáticos y personas de color (POC) para evitar la posible identificación de participantes de categorías distintas. Esta categorización tiene como objetivo diferenciar a los participantes que pueden experimentar racismo (BIPOC) y aquellos que no (blancos); sin embargo, estas categorías son heterogéneas y arbitrarias. Muchos grupos sienten que el término BIPOC impone jerarquías entre las personas de color [ 26 ]. Usamos este término en este manuscrito después de discutirlo con miembros del equipo de estudio con experiencia vivida de racismo y colonización, a pesar de estas limitaciones.
Configuración
Alberta tiene un único sistema de atención médica universal que atiende a 4,4 millones de personas. Hay aproximadamente 11 000 médicos en ejercicio, de los cuales el 59 % son hombres y el 41 % son mujeres [ 27 ]. Los datos de la encuesta sugieren que menos del 3 % de los médicos en ejercicio en Alberta son de género diverso, transgénero, género no binario o de dos espíritus [ 28 ]. Según los datos de la encuesta y el censo, se estima que entre el 3 y el 5 % de los médicos de Alberta son negros, entre el 1 y el 3 % son indígenas, entre el 1 y el 3 % son latinos/hispanos, el 5 % son de Oriente Medio, el 10 % son del sur de Asia, el 7 % son del este de Asia y entre el 50 y el 70 % son blancos [ 28 ]. Se ha documentado racismo interpersonal explícito e implícito contra los negros [ 6 ] y los indígenas [ 29 ] en Alberta [ 30 ], y este racismo da como resultado una prestación de atención médica diferencial para los grupos racializados [ 1 , 31 ].
Métodos
Este estudio de entrevistas cualitativas fue aprobado por el Comité de Ética de Investigación en Salud Conjunta de la Universidad de Calgary (REB20-1688) y se informa de acuerdo con las pautas de los Criterios consolidados para informar investigaciones cualitativas (COREQ) [ 32 ].
Participantes
Todos los miembros clínicos (médicos, residentes y enfermeras practicantes) de los Departamentos de Medicina ( n = 420), Medicina Familiar (solo miembros académicos; n = 40), Ciencias Cardíacas ( n = 125) y Medicina de Emergencia ( n = 220) en la Facultad de Medicina Cumming, Universidad de Calgary ( n = 774) fueron invitados a ser entrevistados sobre el racismo en el lugar de trabajo a través de un solo correo electrónico del liderazgo del departamento. Estos departamentos fueron seleccionados porque cada uno tiene un comité EDI (equidad, diversidad e inclusión) que puede actuar sobre los resultados de este estudio para implementar soluciones. Todos los participantes elegibles fueron entrevistados, sin restricción ni muestreo intencional por raza, con el imperativo ético de que a todos los participantes interesados se les ofreciera la oportunidad de participar. Además, la inclusión de perspectivas de participantes racializados y blancos fue necesaria para abordar el objetivo del estudio de comprender las experiencias y percepciones del racismo médico. Se envió una única invitación para reducir la carga de correos electrónicos y tareas durante la pandemia de COVID-19. La saturación se evaluó mediante la saturación temática inductiva, que considera la aparición de nuevos códigos o temas en lugar del desarrollo de temas existentes [ 33 ]. La participación fue voluntaria y se compensó con una tarjeta de regalo de $50. Todos los participantes dieron su consentimiento informado, incluido el consentimiento para el uso de citas en materiales de difusión del conocimiento.
Entrevistas
La guía de entrevistas se desarrolló con base en las preguntas del estudio y una revisión de la literatura (Apéndice 1 ). Debido a que el objetivo de este proyecto era explorar las experiencias de racismo en la medicina de los médicos de manera amplia, la guía de entrevistas debía permitir a los participantes guiar la entrevista en función de sus motivaciones y prioridades. La guía de entrevistas propuesta se distribuyó entre varios comités universitarios de EDI para recibir comentarios antes de su uso; es posible que los participantes del estudio hayan aportado información a la guía de entrevistas desarrollada. Las entrevistas semiestructuradas se llevaron a cabo de forma virtual entre abril y agosto de 2021 debido a los protocolos locales de la pandemia de COVID-19. Cada entrevista se grabó en audio y se transcribió textualmente. Los entrevistadores desidentificaron las transcripciones antes del análisis. Los participantes revisaron sus transcripciones para sugerir modificaciones a su propia discreción.
Análisis
El análisis de contenido temático [ 34 ] fue guiado por el constructivismo, que permite la existencia de múltiples verdades y realidades [ 35 ], y realizado en NVivo (versión 12.3.0, QSR International, Inc., Doncaster, Australia). Los códigos iniciales se desarrollaron deductivamente utilizando el marco de Niveles de Racismo del Dr. Camara Jones [ 36 ], que organiza el racismo en tres niveles: institucional, interpersonal e internalizado. Los códigos adicionales se generaron inductivamente a través de la lectura atenta de todas las transcripciones por SMR y CRM. La codificación se completó de forma independiente, en paralelo, por SMR y CRM con tres transcripciones para generar un libro de códigos. El libro de códigos se presentó a todo el equipo de estudio con citas ejemplares para evaluar la validez. Luego, el libro de códigos final se aplicó a todas las transcripciones (Apéndice 2 ). Cada transcripción fue analizada de forma independiente por dos miembros del equipo de estudio con capacitación en análisis de datos cualitativos (SMR y KCL o CRM) y los desacuerdos se conciliaron mediante discusión con el equipo de estudio más amplio.
Los temas se desarrollaron examinando los códigos más frecuentes para las relaciones, patrones, puntos en común y diferencias entre los participantes. Después del análisis inicial, quedó claro que la mayoría de las descripciones de los participantes de una experiencia de racismo tenían elementos repetitivos y ordenados: una descripción, una reacción interna, una racionalización y una reacción externa. Por lo tanto, organizamos cada narrativa sobre una experiencia de racismo en componentes ordenados para crear un marco lógico para abordar el racismo. Los marcos lógicos se utilizan a menudo para definir el propósito y las actividades de un programa organizando los pasos necesarios para lograr el objetivo general del proyecto [ 37 ]. En nuestro marco lógico, el objetivo era abordar el racismo en el lugar de trabajo médico, donde «abordar» podría significar cualquier intervención personal u organizacional para mitigar el racismo. Luego intentamos identificar la barrera o facilitador del abordaje del racismo para cada narrativa preguntando «¿Qué permitió (o impidió) que el participante (o la institución) abordara el racismo en esta experiencia?». Cada narrativa se volvió a examinar en este modelo y las barreras o facilitadores en cada paso se tabularon y consolidaron en categorías principales (Apéndice 3 ).
Para plantear hipótesis sobre soluciones relacionadas con cada barrera o facilitador, buscamos literatura revisada por pares y consultamos a colegas con experiencia en EDI. La consulta con expertos se solicitó por correo electrónico y mediante un debate formal durante las reuniones del comité de EDI en los departamentos participantes.
Reflexividad
Los participantes pudieron seleccionar entre cuatro entrevistadores capacitados (CRM, PR, ANC y SMR), que son diversos en identidad racial, género, profesión y afiliación departamental. CRM es una trabajadora social cisgénero blanca y PR es una mujer mestiza e investigadora principal. ANC es un médico negro. SMR es una médica cisgénero blanca. CRM, SMR y KCL participaron en el análisis de datos. KCL es una médica cisgénero blanca. Los miembros restantes del equipo de estudio, que proporcionaron comentarios provisionales y validación del diseño del estudio, la recopilación de datos y el análisis de datos, también incluyeron médicas cisgénero mestiza (CB) y blancas (JHL).
Resultados
Descripción general
Se completaron diecinueve entrevistas (17-90 min), con encuestados que representaban a todos los departamentos participantes (tasa de participación del 2,5%). Los encuestados eran diversos en cuanto a raza e identidad de género (Tabla 1 ). Se alcanzó la saturación en la creación del marco lógico después de 12-15 entrevistas, ya que no se desarrollaron códigos o temas adicionales después de este punto. Todos los participantes, excepto uno (blanco), compartieron experiencias de racismo médico o presenciaron este tipo de racismo. Las reacciones de los participantes al racismo interpersonal explícito variaron; mientras que algunos participantes se sintieron tranquilos al saber que «había una razón para su (comportamiento), no es una razón racional, pero al menos parece haber una explicación» (Participante BIPOC (BP)1), otros sintieron que «cada vez que sucede, es un poco como una bofetada en la cara» (BP7). Muchos dudaron en atribuir estas experiencias al racismo. En cambio, ofrecieron otras explicaciones potenciales, entre ellas “ignorancia” (BP4), “sorpresa genuina” (BP2), “curiosidad” (BP16) y “pereza” (BP3).
Abordar el racismo abordando las barreras y aprovechando los facilitadores: un marco lógico antirracismo
El marco lógico incluía la comprensión, el reconocimiento, la denominación y la confrontación del racismo como procesos necesarios para abordarlo (Tabla 2 ; Fig. 1 ). Las narraciones de los participantes ilustraron cómo cada paso de este modelo interactuaba para evitar abordar el racismo; por ejemplo, si los participantes no entendían el racismo, no podían reconocerlo cuando ocurría, y los participantes que no nombraban una experiencia como racismo no podían enfrentarlo. Este marco nos permitió identificar barreras para abordar el racismo que podrían ser abordadas por intervenciones. Nuestro análisis se presenta aquí en detalle.
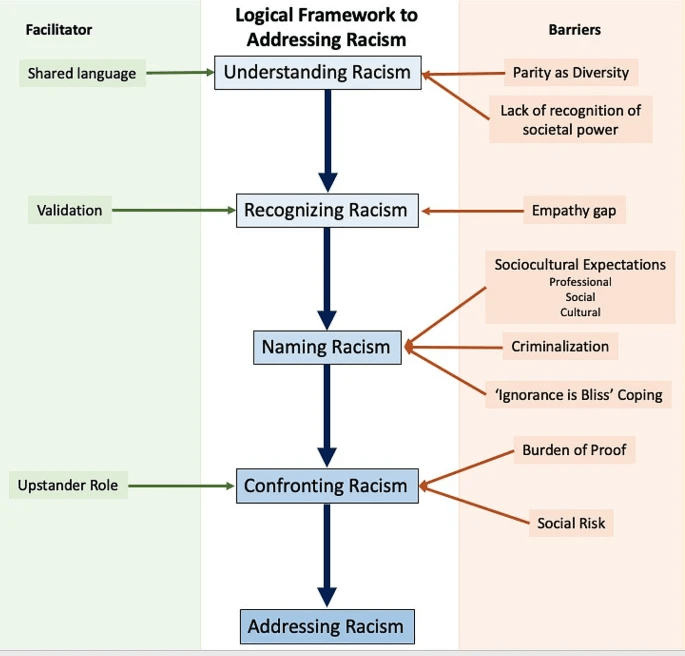
Entendiendo el racismo
La mayoría de los participantes tuvieron dificultades para conceptualizar el racismo. No estaban seguros de si se requería mala intención en lugar de “ignorancia o pereza” (BP7). Algunos participantes describieron un cambio en su comprensión de la intención frente al impacto a lo largo de sus carreras y a medida que avanzaban las conversaciones sociales sobre el racismo, haciendo hincapié en el aprendizaje sobre el racismo como un facilitador para definir el racismo. Además, la mayoría de los participantes no tenían una comprensión conceptual del racismo como la combinación de sesgo racial y diferencia de poder que resulta en desventajas. Por ejemplo, cuando se les preguntó sobre experiencias de racismo, un participante compartió que un trabajador de un servicio de alimentos le dijo que una comida tenía cerdo y lo describió como “discriminación, pero en realidad están tratando de ser útiles… porque son conscientes culturalmente de que las personas que se parecen a mí a veces no comen carne o tocino” (BP17). Casi todos los participantes proporcionaron ejemplos de representación como evidencia de la falta de racismo.
Reconociendo el racismo
Muchos participantes BIPOC se preguntaron “en el fondo” (BP9, BP16, BP19) si el racismo había afectado su trayectoria profesional. Algunos sintieron que, si bien no podían señalar un caso en particular, podría haber evidencia de efectos sutiles a lo largo de toda su carrera: “Nunca pensé que la raza tuviera un impacto en términos de… oportunidades de avance profesional. Pero recientemente, cuando lo pienso, me pregunto si eso influyó en cierto grado” (BP9) y “No sentí que se haya intentado frenarme debido a mi raza (aunque) a veces piensas que podría ser así porque te lleva un poco más de tiempo llegar allí que a otras personas que pueden ser de otros orígenes raciales” (BP16). Para algunos, esta pregunta ocupó un espacio mental significativo: “Te quedas sentado y dices ‘¿Es porque soy mujer? ¿Es porque soy una minoría visible?’ Y realmente no puedes separarlo. Entonces, encuentro que a veces es un desafío” (BP14). De manera similar, la invisibilidad del privilegio blanco quedó demostrada por los múltiples participantes blancos que asumieron que su raza “probablemente permitió que algo de buena suerte se cruzara en mi camino”, aunque “no recuerdan ninguna instancia específica en la que eso haya sucedido” (participante blanco (WP) 15). A diferencia de los participantes BIPOC, ningún participante blanco informó angustia ante la posibilidad de que la raza hubiera influido en sus trayectorias profesionales.
Los participantes BIPOC percibieron una brecha de empatía cuando sus colegas blancos no reconocieron sus experiencias de racismo. Algunos participantes blancos eran conscientes de la brecha entre su reconocimiento del racismo en el lugar de trabajo y las experiencias de sus colegas, y afirmaron que su visión del lugar de trabajo como equitativo es «una suposición importante que hago al no ser parte de un grupo minoritario racializado» (WP18). De esta manera, los espacios seguros donde se compartían y validaban experiencias como racismo fueron un facilitador para contrarrestar la creencia de que «pensé que [el racismo] me pasaba solo a mí, pensé que era normal» (BP8).
Tener un lenguaje compartido para hablar sobre el racismo fue un factor que facilitó su reconocimiento. Un participante compartió que “no estaba familiarizado con el término (microagresiones) hasta que asistí a una charla. Y desde esa charla, he escuchado hablar de ello en todo tipo de lugares… realmente me resonó” (BP2).
Ponerle nombre al racismo
Las expectativas socioculturales, que hacen referencia a las normas profesionales, sociales o culturales que rigen el comportamiento policial, fueron una importante barrera para nombrar el racismo. Por ejemplo, los participantes se mostraban cautelosos a la hora de “causar un alboroto” (BP2), “hacer olas” (BP4), “alborotar las aguas” (BP12) o ser una “molestia” (BP3) al “jugar la carta racial” (BP3, BP9) para describir una experiencia, pues les preocupaba que eso “perjudicara mi carrera” (BP8). Los participantes sentían que “es un gran problema llamar racista a alguien, es casi una de esas terminologías tabú que se reservan para aquellas personas que acosan y linchan a la gente” (BP2). Esta “criminalización” de la raza y el racismo contribuye a “una regla tácita… en la atención médica y la sociedad” de no hablar de la raza y el racismo (BP12) y dejó a los participantes sin el lenguaje para describir sus experiencias.
Los participantes compartieron que los educaron para “estar agradecidos” por sus oportunidades, para “trabajar el doble que los demás” (BP1, BP8) y para no “quejarse” ni causar problemas (BP2, BP4, BP19), valores que a menudo atribuían a sus padres o a su cultura. Con los pacientes, los participantes sentían que debían ser “la mejor persona… el profesional” para evitar que los pacientes se sintieran “incómodos” (BP1). Varios participantes compartieron que suprimieron sus sentimientos o incluso sus recuerdos de eventos racistas como mecanismo de afrontamiento porque “si lo piensas, te enojas todo el tiempo” (BP1).
Enfrentando el racismo
Los participantes que reconocieron el racismo dudaron en denunciar o confrontar estas experiencias porque se sentían obligados a «probar» sus experiencias a los demás. Esto fue especialmente cierto en el caso del sesgo racial implícito y la discriminación sistémica. Los participantes sintieron que «es un caso difícil de defender, a menos que se esté discriminando de manera muy obvia y se tenga una base realmente sólida» (BP2) y «las personas dentro de los grupos minoritarios no se sienten cómodas al plantear estas cuestiones, porque entonces, de repente, hay que demostrárselo a todo el mundo» (BP9).
Además, los participantes sintieron que arriesgaban su reputación al denunciar el racismo, porque “la gente va a pensar que no puedo lograrlo por mis propios méritos” (BP2). Un lenguaje compartido para hablar sobre el racismo facilitó la confrontación con el racismo; por ejemplo, un participante encontró útil hacer referencia a una sesión educativa: “Puedo simplemente decir ‘¿Recuerdas eso de lo que hablamos? Lo estás haciendo ahora mismo’” (WP13). El riesgo social de enfrentar el racismo se superó cuando los participantes presenciaron que sus colegas eran los objetivos. Un participante utilizó la necesidad de que los aprendices “estén en un lugar donde puedan sentirse seguros y cómodos aprendiendo” (WP6) como justificación para despedir a un paciente explícitamente racista de su práctica, mientras que ser ellos mismos el objetivo del racismo no era una justificación. Algunos participantes blancos se sintieron cautelosos al hablar en nombre de sus colegas marginados racialmente: “¿Cómo apoyas a esas personas sin quitarles su capacidad de acción… pero también asegurándote de que se sientan seguros y puedan hablar?” (WP13).
Intervenciones contra el racismo
Identificamos barreras y facilitadores para abordar el racismo (Fig. 1 ) y luego los relacionamos con intervenciones antirracistas sugeridas directamente por los participantes, desarrolladas utilizando la experiencia de los miembros del equipo de estudio y/o basadas en literatura revisada por pares. Estas se resumen en la Tabla 3 y se describen brevemente aquí.
Desarrollar conocimientos para comprender el racismo
Las organizaciones pueden adaptar las estrategias de seguridad ocupacional [ 46 ] para centrarse en el racismo y otros conceptos de EDI. Por ejemplo, para generar conocimiento colectivo y organizacional, los líderes podrían reservar tiempo al comienzo de las reuniones para presentaciones breves sobre un solo tema de EDI [ 41 ].
Desarrollar habilidades para reconocer el racismo
Los médicos pueden aprender a reconocer el racismo médico a través de rondas formales sobre raza y racismo, inspiradas en las rondas de morbilidad y mortalidad, donde se explicitan y discuten los resultados clínicos adversos atribuibles al racismo estructural e interpersonal [ 42 ]. De manera similar, el racismo en el lugar de trabajo se puede compartir a través de la narración formal de historias; en estos programas, se comparten y discuten las narrativas publicadas de médicos que han experimentado racismo o discriminación [ 43 , 44 , 47 ] para generar empatía y comprensión para todos los médicos. Por último, los talleres facilitados de capacitación sobre sesgo implícito pueden desarrollar habilidades para reconocer el racismo [ 48 ].
Apoyos estructurales para nombrar el racismo
Las organizaciones pueden desarrollar políticas que orienten la toma de decisiones cuando se produce racismo. Por ejemplo, una directiva que establezca los pasos que se seguirán cuando un paciente solicite un médico blanco elimina la necesidad de que los médicos individuales defiendan sus intereses. De manera similar, la creación de espacios seguros donde los médicos que experimentan racismo puedan establecer contactos y compartir sus experiencias puede eliminar las barreras que enfrentan los médicos BIPOC cuando buscan apoyo. Los programas de apoyo entre pares pueden vincular a los médicos que experimentan acoso o discriminación con pares capacitados con experiencias vividas similares. Todos los líderes médicos deben tener las habilidades para responder adecuadamente a las revelaciones de racismo de sus colegas, para evitar la experiencia común de ser despedido o no recibir apoyo cuando denuncian el racismo. La cantidad y el manejo de las inquietudes sobre acoso y discriminación deben informarse periódicamente a los miembros de la organización para promover la rendición de cuentas [ 45 ].
Tomar medidas para enfrentar el racismo
A medida que se abordan las barreras para comprender, reconocer y nombrar el racismo, las organizaciones deben crear estructuras para facilitar la confrontación del racismo médico. La capacitación en intervención de testigos presenciales puede brindar habilidades para que los médicos aprovechen su privilegio para enfrentar el racismo de manera segura en tiempo real [ 49 ]. Las organizaciones deben desarrollar mecanismos de denuncia del acoso basados en evidencia que aborden las barreras conocidas para la denuncia [ 50 , 51 ] e incorporen enfoques de justicia restaurativa y de reparación para el acoso.
Discusión
Este estudio de 19 profesores blancos y BIPOC de una sola facultad de medicina identificó que la mayoría de los participantes tenían dificultades para comprender, reconocer, nombrar y enfrentar el racismo debido a factores individuales y estructurales. En un marco lógico, estas barreras trabajaban juntas para evitar que las personas y los sistemas abordaran el racismo en el lugar de trabajo médico. Combinamos estas barreras con intervenciones propuestas para reducirlas o amplificar los facilitadores del abordaje del racismo en la medicina. Los líderes médicos pueden usar estos resultados para identificar las barreras y los facilitadores más relevantes para su contexto e implementar intervenciones que se dirijan a estos impulsores del racismo en curso.
Encuestas transversales previas de médicos canadienses negros estimaron una prevalencia de racismo en el lugar de trabajo del 71% [ 15 ], lo que concuerda con la prevalencia observada entre los médicos BIPOC en Alberta y en toda América del Norte [ 19 , 28 ]. Si bien muchos de estos estudios realizaron un análisis cualitativo de las respuestas de los textos de las encuestas, el análisis de los datos de las entrevistas puede proporcionar detalles contextuales importantes sobre cómo se puede manifestar el racismo en la medicina [ 34 ]. Varios estudios cualitativos de profesores académicos negros, nativos americanos e hispanos [ 20 , 23 ], médicos [ 22 , 23 ] y residentes [ 21 ] informaron sobre la ubicuidad de las microagresiones raciales, el requisito de «representar» a toda la raza o etnia de uno, y la exclusión social y profesional, incluida la falta de tutoría. Nuestro estudio se basa en los resultados de estos estudios al examinar las reflexiones de los participantes sobre el racismo, además de describir su prevalencia e impacto. Esto nos permite identificar las barreras para abordar el racismo y hacer coincidir las intervenciones con cada barrera.
Son comunes los editoriales que instan a los médicos a abordar el racismo en la medicina [ 52 ] y los médicos no deben olvidar que abordar el racismo en la medicina es una obligación ética de su profesión [ 4 , 53 ]. Es poco probable que las intervenciones para abordar el racismo en la medicina que no se dirigen a los contribuyentes subyacentes tengan éxito. Esto puede explicar los datos contradictorios sobre la eficacia de intervenciones como la capacitación sobre sesgos implícitos [ 54 ] o el enmascaramiento demográfico de candidatos [ 55 , 56 ], que es poco probable que sean efectivas en entornos donde el sesgo implícito no es el principal contribuyente al racismo. Los marcos conceptuales pueden ayudar a los investigadores a comprender y abordar fenómenos complejos [ 57 ] y se han utilizado para examinar el sexismo persistente en la medicina [ 58 , 59 ]. Nuestro marco tiene similitudes con el Modelo de información-motivación-habilidades conductuales adaptado desarrollado por Jindal y colegas para comprender cómo un plan de estudios antirracismo podría abordar el racismo médico entre los residentes pediátricos [ 60 ]. Este modelo ayuda a comprender los factores que impiden o promueven las intervenciones conductuales al describir la relación entre la información, la motivación para cambiar, las habilidades necesarias para cambiar, la planificación de acciones y el cambio de comportamiento. Los dominios de motivación y planificación de acciones observados en el modelo de Jindal no se identificaron entre nuestros datos, aunque la necesidad de información (por ejemplo, comprensión) y habilidades (por ejemplo, reconocimiento) para abordar el racismo fueron comunes a ambos. Este hallazgo puede deberse en parte a las diferencias en la población del estudio; en el estudio de Jindal et al., el 67% de los participantes eran blancos en comparación con el 5% de nuestros participantes. Los participantes blancos mencionaron con mayor frecuencia que están motivados para cambiar, dado su «sentido de responsabilidad al notar su agencia para nombrar el racismo en el momento» [ 60 ] y «la propia participación en sistemas [racistas]» [ 60 ] que los participantes BIPOC. Además, en contraste con nuestra exploración de las experiencias de racismo de los participantes, Jindal et al. preguntó específicamente a los participantes sobre cómo sus planes de estudio antirracistas pueden conducir a cambios en la práctica clínica, lo que probablemente provocó más respuestas relacionadas con el dominio de planificación de acciones [ 60 ].
Nuestro marco proporciona información sobre cómo las instituciones pueden evaluar dónde existen lagunas en su trabajo actual contra el racismo a lo largo de este marco y proporciona una justificación para seleccionar intervenciones que se dirijan a estas lagunas. Por ejemplo, los líderes pueden utilizar encuestas [ 38 ] para determinar si sus miembros tienen una conceptualización precisa del racismo (comprensión) antes de intentar implementar la capacitación para la intervención de los espectadores (confrontación) [ 49 ]. De manera similar, las instituciones pueden beneficiarse de las directrices locales para orientar a los médicos en el abordaje del acoso de los pacientes solo después de que sus miembros puedan reconocer el racismo y su impacto en sus colegas.
Este estudio tiene varias limitaciones. La primera es un posible sesgo de selección, ya que se trata de un estudio que examina un tema delicado, por lo que nuestros resultados pueden representar solo las opiniones de quienes están más interesados o más seguros sobre este tema. El sesgo de deseabilidad social puede haber influido en las respuestas de los participantes debido a la presencia de un entrevistador. El sesgo de selección y deseabilidad social puede ser la razón por la que no identificamos el racismo interpersonal explícito como una barrera importante para abordar el racismo en este estudio, aunque el racismo explícito existe entre los médicos [ 43 ] y seguramente juega un papel en la persistencia del racismo en la medicina. Por esta razón, nuestro marco lógico solo puede aplicarse cuando las instituciones han abordado el racismo explícito. De manera similar, no buscamos probar el modelo lógico desarrollado a partir de nuestros datos, por lo que esto es solo para generar hipótesis. El modelo lógico debe examinarse en otros entornos; sería importante ver si este marco puede usarse para predecir qué intervenciones antirracistas serán más efectivas. Nuestros resultados representan las experiencias de médicos en diferentes departamentos académicos en una sola universidad y los facilitadores del racismo pueden ser diferentes en entornos con diferentes historias o estructuras de racismo y opresión. Por ejemplo, en entornos donde el trabajo contra el racismo actualmente enfrenta la oposición del gobierno y de grupos de presión [ 39 ] o donde el prejuicio antimexicano es una forma de racismo más predominante que la que se observa típicamente en nuestro entorno [ 40 ], puede haber diferentes barreras y facilitadores.
Conclusiones
En general, este análisis temático de datos cualitativos se basa en datos de prevalencia transversales y otras exploraciones cualitativas de las experiencias de los participantes para describir cómo los médicos de una sola facultad de medicina perciben el racismo en su entorno. Estos resultados informaron un modelo lógico que requiere que las personas comprendan, reconozcan, nombren y enfrenten el racismo antes de que las personas y las organizaciones puedan abordarlo de manera efectiva. Las intervenciones dirigidas a las brechas en este modelo lógico pueden estar mejor posicionadas para abordar el desafío y la persistencia del racismo en la medicina que perjudica a los pacientes, los residentes y los médicos.
Capacidades Dinámicas en la Atención Médica
Dr. Carlos Alberto Díaz
Las capacidades dinámicas son las características organizacionales y de los equipos de gestión, es entonces un enfoque de fortalecimiento hacia la relación de agencia entre los pacientes hospitalarios y los equipos de atención.
Este objetivo se logra colocando los incentivos alineados con la calidad de la prestación y los menores costos de la resolución integral de las patologías, y del gasto a los financiadores. También requiere la integración y la formación de equipos multi e interdisciplinarios: de médicos internistas, enfermeros administrativos, especialistas en calidad y financieros – costos – facturación, en nuestra experiencia también bioingenieros, en una modalidad de gestión Lean para disminuir los desperdicios en la atención médica.
Es adaptarse, innovar, utilizar información, controlar adecuada e integralmente a los pacientes, incluyendo a estos y sus familias en los equipos de atención. La búsqueda de una atención basada en el valor para los pacientes y el sistema de salud, también para los integrantes de los equipos de salud, que puedan vivir de hacer bien su trabajo
Estas capacidades dinámicas deben actualizarse para adaptarse a los cambios del entorno y mantener un buen desempeño. Esto incluye el desarrollo de servicios digitales, la historia clínica electrónica única, equipos de enfermería capacitados, el uso adecuado de tecnología rentable, cirugía segura, uso correcto de medicamentos, enfoque en el paciente y diseño de procesos de atención continuos.
Enfocándonos en mejorar la eficiencia: en gestionar los registros de admisión correctamente y en diseñar itinerarios adecuados para los pacientes. Esto es mucho más profundo que las medidas implementadas para la reducción de los costos. Las capacidades dinámicas (CD) se definen como la capacidad de integrar, construir y reconfigurar los activos internos y externos de la organización para abordar los entornos que cambian rápidamente. Por lo tanto, son fundamentales para el éxito de la transformación estratégica de los proveedores de atención sanitaria. Sustentados en los valores organizacionales sinceros, en los paradigmas de complejidad que constituyan los cánones de una cultura de la calidad prestacional y la seguridad de los pacientes.
Es crucial romper con los silos del conocimiento, que la información fluya para abastecer al sistema técnico de toma de decisiones, extendiendo las fronteras de los servicios asistenciales, reconociendo los momentos en los cuales matricialmente en redes internas cumplen el rol de compradores y proveedores de información o logística.
Esto implica una reevaluación de las estrategias, así como de la formación médica y de enfermería, incorporando un aprendizaje incremental y una toma de riesgos calculada.
En resumen, el desempeño hospitalario depende de los activos intangibles y el capital intelectual, las competencias básicas y la capacidad de gestionar y mejorar estos activos. Es un ciclo recursivo entre la gestión del conocimiento y el aprendizaje organizacional.


Importancia del Trabajo en Equipos Multidisciplinarios en Salud
Nota del blog: Trabajar, aprender, estudiar, formarse, en equipos es fundamental en una disciplina compleja como es la atención de la salud, repleta de responsabilidades individuales y colectivas. Hoy no solo es equipo, sino que ese equipo debe ser multidisciplinar, con gran capacidad de adaptación a los cambios del entorno. Es otra de las habilidades blandas que debemos aprender. Que rol y como nos sumamos a ese equipo. Como llegamos a él. Cuales son la dinámicas de trabajo y que debemos aportar. Con generosidad y buena comunicación.

La formación de médicos y otros profesionales sanitarios se ha centrado tradicionalmente en el desarrollo de conocimientos y habilidades técnicas pertinentes a cada especialidad. Se asumía que, una vez formados de esta manera, serían capaces de trabajar eficazmente en equipo con otros profesionales. El trabajo multidisciplinario es ahora un estándar en la prestación de servicios sanitarios, y el trabajo en equipo se enseña como parte de los planes de estudio actuales. El aprendizaje interdisciplinario es cada vez más común, y los estudiantes de medicina, enfermería y otras profesiones relacionadas con la salud aprenden conjuntamente durante su formación. Sin embargo, el personal sanitario cualificado no siempre ha recibido formación específica para trabajar eficazmente como parte de equipos diversos ni para identificar y superar barreras en el trabajo en equipo. Todos debemos desarrollar estas habilidades para garantizar que nuestros pacientes reciban la mejor atención posible.
La atención sanitaria es cada vez más compleja, y ningún médico, enfermero u otro profesional dispone de tiempo, conocimientos o experiencia suficientes para atender a los pacientes de forma individual. Trabajamos en equipos multidisciplinarios (EMD) y lo haremos cada vez más a medida que la población envejezca. El 80% de los pacientes mayores de 80 años viven con dos o más enfermedades crónicas, lo que genera una carga creciente de enfermedades crónicas en el NHS (Gowing et al, 2016).
El nuevo kit de herramientas para equipos multidisciplinarios de Health Education England (HEE) (HEE, 2021) nos insta a reevaluar la forma en que trabajamos en EMD. Abarca seis dominios esenciales: comunicación, trabajo a través de fronteras, metas y objetivos compartidos, planificación y diseño, combinación de habilidades y aprendizaje, y cultura. El objetivo general es considerar al equipo multidisciplinario desde una perspectiva más amplia, derribando barreras en todos los sectores de atención, en lugar de centrarse en departamentos individuales.
El término «equipo multidisciplinario» suele evocar reuniones organizadas y formales dentro de sectores como la oncología, que surgieron en la década de 1980 debido a los beneficios observados en tratamientos adyuvantes, como la quimioterapia y la radioterapia (Taberna et al, 2020). Sin embargo, para la mayoría de los profesionales de la salud, el trabajo en EMD implica interacciones diarias, informales y no planificadas, tanto clínicas como no clínicas. Trabajar en equipo es una habilidad que se puede aprender y practicar, por lo que ahora está incluida en el plan de estudios de pregrado de muchas facultades de medicina. Esta formación debe continuar en nuestra práctica diaria como médicos cualificados para optimizar los resultados de los pacientes. La mala comunicación y el trabajo en equipo ineficaz en interacciones aparentemente rutinarias se han identificado como factores contribuyentes en el 70% de los incidentes graves (Rabol et al, 2011). Es probable que surjan nuevos desafíos para el trabajo en equipo con el uso creciente del trabajo remoto y la atención mejorada por la tecnología.
Barreras para el funcionamiento eficaz de equipos multidisciplinarios
A pesar de los bien documentados beneficios del trabajo en EMD, implementar y mantener una colaboración eficaz en toda la atención sanitaria es un desafío. Pueden aparecer problemas que obstaculicen la comunicación interdisciplinaria, como el uso de terminología médica, la comprensión diferencial de conceptos y las barreras lingüísticas, comunes en un NHS étnicamente diverso. Además, los equipos pueden recibir información inadecuada si algunas disciplinas están subrepresentadas, lo que podría sesgar los objetivos del tratamiento. Las relaciones dentro de los equipos pueden ser difíciles debido a diferentes perspectivas sobre la atención/tratamiento, estructuras jerárquicas persistentes y desequilibrios de poder percibidos y reales. Todas estas barreras pueden provocar la ruptura de la comunicación y empeorar los resultados de los pacientes, incluso cuando todos trabajan apasionadamente por obtener buenos resultados (Zajac et al, 2021).
Las barreras organizativas también pueden dificultar el desarrollo y mantenimiento de relaciones laborales eficaces, como la escasez de personal, modelos de trabajo híbridos y recursos limitados en un sistema sanitario sobrecargado.
Explorando el alcance del equipo multidisciplinario en el ámbito clínico
Establecer y mantener la confianza entre compañeros es fundamental para la eficacia de la colaboración en equipo. El término «seguridad psicológica» describe una cultura en la que todo el personal es tratado con respeto, se aceptan distintas opiniones y el personal se siente seguro para hablar, hacer sugerencias, desafiar a otros y admitir errores. Un buen liderazgo es crucial para desarrollar y mantener la seguridad psicológica dentro de los equipos. Medidas prácticas incluyen el uso rutinario de reuniones informativas durante rondas de sala y sesiones de informe, reduciendo gradientes de autoridad y promoviendo la comodidad de todos los miembros del equipo al compartir observaciones y opiniones. La comprensión mutua de los roles mejora la dinámica de trabajo y la productividad, inspirando la colaboración necesaria en situaciones críticas.
Habilidades no técnicas y trabajo en equipo multidisciplinario
Las habilidades no técnicas incluyen comportamientos como toma de decisiones, liderazgo, seguimiento, relaciones sociales y habilidades cognitivas superiores. Estas habilidades son más efectivas para reducir riesgos a pacientes que el conocimiento clínico y pueden mejorarse con entrenamiento en simulación (Abildgren et al, 2022). Capacitación «in situ» y formación de equipos mejoran la comprensión y el respeto entre disciplinas.
¿Cómo podemos saber si nuestros equipos trabajan bien juntos?
Encuestas al personal del NHS y encuestas nacionales de formación proporcionan información sobre interacciones y seguridad en el lugar de trabajo. Las encuestas centradas en la experiencia de pacientes también miden la eficacia de los EMD. Evaluaciones objetivas realizadas por psicólogos y antropólogos sociales capacitados pueden identificar áreas de dificultad y enfocar intervenciones efectivas.
El futuro del trabajo en equipos multidisciplinares
La pandemia de COVID-19 ha impulsado el trabajo remoto y el uso de plataformas de videoconferencia, pero queda mucho por integrar esta tecnología en entornos clínicos directos. En el período pospandémico, la atención médica mejorada por la tecnología tiene potencial para mejorar la atención al paciente, permitiendo la colaboración remota de expertos multidisciplinares. Sin embargo, aún quedan desafíos por superar, como la falta de software compatible para compartir datos entre organizaciones.
Conclusiones
En resumen, el trabajo en equipo multidisciplinario eficaz ofrece muchos beneficios, todos centrados en optimizar la atención al paciente. Los EMD son vitales en áreas específicas como la geriatría, oncología y cuidados intensivos. Este nivel de trabajo en equipo debe extenderse a todos los ámbitos hospitalarios y comunitarios. Lograr un respeto mutuo interdisciplinario es crucial para mantener un equipo exitoso. Esto requiere motivación para mejorar los propios equipos y conciencia de las barreras actuales. Aunque es un esfuerzo a largo plazo, se pueden tomar medidas inmediatas evaluando conscientemente nuestras interacciones diarias con colegas.
Puntos clave
- Elimine o minimice la jerga confusa para mejorar la inclusión.
- Sea consciente de los desequilibrios de poder y anime a los miembros más tranquilos a ofrecer sus opiniones.
- Comprenda los roles y perspectivas de los diferentes miembros del equipo.
- Incluya siempre al paciente como parte del equipo de toma de decisiones.
- Realice informes y reuniones periódicas para reevaluar la función y eficacia de sus equipos.
- Fomente la socialización entre el MDT.
Impacto de la Remuneración en el Desempeño Hospitalario
Nos debatimos en la gestión para lograr los objetivos que incentivos agregar en la relación de agencia para gestionar la medicina basada en el valor y el desempeño de las organizaciones, recordando que existen otros estímulos del complejo industrial médico, que con sus evidencias publicadas inciden en la conducta médica. Brasil es un país con sistema único de salud, pero que año tras año crece la medicina prepagada, que financia por presupuesto los hospitales estaduales y por cápita a la atención primaria.

El texto presenta un estudio que explora la percepción de la remuneración entre empleados de dos hospitales en Brasil: uno público y otro privado. A continuación, se ofrece un análisis detallado de varios aspectos clave del trabajo.
Objetivo del Estudio
El principal objetivo de la investigación es analizar cómo los sistemas de remuneración influyen en el comportamiento de los empleados hospitalarios. Se busca entender si existen diferencias significativas en la percepción de la remuneración en función de la gestión pública versus la privada y cómo factores como la ocupación, el género, la edad y la experiencia afectan estas percepciones.
Metodología
Tipo de Estudio: Se realizó una encuesta descriptiva con un enfoque cuantitativo en dos grandes hospitales, uno privado y uno público.
Muestra: La muestra incluyó a 109 empleados (54 del hospital privado y 55 del público).
Cuestionario: Se utilizó un cuestionario con preguntas que exploraban las percepciones de la remuneración a través de variables como restricción, control, motivación y aprendizaje.
Resultados
Principales Diferencias en la Percepción: Se encontraron diferencias significativas en cómo los empleados de hospitales públicos y privados perciben aspectos de la remuneración, como el control y la motivación.
Los empleados de hospitales privados parecían ver la remuneración más como un mecanismo de control, mientras que los del sector público mostraron diferentes respuestas.
Influencias de la Ocupación: Las percepciones también variaron según la ocupación, con diferencias significativas en la forma en que los empleados administrativos y de salud respondieron a la remuneración. Esto indica que el contexto profesional puede influir en cómo se interpreta la remuneración.
Género, Edad y Experiencia: Contrario a lo esperado, el género no fue un factor determinante en la percepción de la remuneración, excepto en la percepción de restricciones. Además, no hubo diferencias significativas en el comportamiento entre empleados mayores y jóvenes, ni tampoco entre aquellos con más o menos experiencia.
Implicaciones Gestión Hospitalaria: Los resultados sugieren la necesidad de que la gestión hospitalaria, tanto pública como privada, considere las percepciones de los empleados sobre la remuneración para mejorar la motivación y el desempeño.
Desarrollo de Políticas Remunerativas: Las políticas de remuneración deben ser adaptadas teniendo en cuenta el tipo de hospital y las características del personal para maximizar la eficacia y satisfacción laboral.
Futuras Investigaciones: Se sugiere investigar más a fondo las respuestas a la remuneración en otros contextos y profundizar en el impacto de la remuneración variable en la motivación y el desempeño.
Conclusiones
El estudio concluye con la idea de que la remuneración no solo actúa como un incentivo económico, sino que su percepción está intrínsecamente ligada a varios factores, incluyendo el estilo de gestión del hospital. Las diferencias en la percepción entre hospitales públicos y privados y entre diferentes ocupaciones destacan la complejidad que rodea la gestión de recursos humanos en el sector salud. Esto invita a un análisis más profundo de las relaciones entre comportamiento, remuneración y evaluación del desempeño en el ámbito hospitalario.
En resumen, el análisis de la remuneración es esencial no solo para la gestión eficaz de los recursos humanos en hospitales, sino también para entender cómo estas percepciones pueden afectar la calidad del servicio y el bienestar de los empleados.
Nota del blog: en el sector público tenemos que hablar de remuneración fija, acompañado de un pequeño componente variable por desempeño que se explicite por ausentismo menor y cumplimiento horario, disminución de pago de horas extras del hospital, diseñar una carrera y crecimiento profesional, capacitaciones pagas, posibilidad de cobro de un porcentaje pequeño de una prestación, sostenimiento de la producción del servicio. Los servicios que no sean productores finales, cobrarían lo que se facture a las obras sociales por partes iguales. Siempre los pagos tienen que consolidar trabajo en equipo y la atención centrada en el paciente. Este concepto no es etéreo o cualitativo sino medible, como disminuir las esperas, evitar las suspensiones, certificar los informes. , cumplimiento los horarios, avanzar sobre la atención sociosanitaria.
En las empresas privadas, también hay que ir al pago por desempeño. Porque los pagos fee for service, aumentan la producción pero no la calidad, hacer más no siempre es mejor, por lo tanto tenemos que ver que metas le pedimos a cada equipo, los médicos pueden operar pacientes en su responsabilidad, pero siempre lo hacen con un equipo, los médicos de la emergencia, los especialistas en las interconsultas, estar a disposición del sanatorio. Pagar más por buenos resultados. Los esquemas contractuales que tengan incentivos económicos tienen que ser negociados periódicamente para evitar comportamientos oportunistas de los que trabajen con determinados financiadores lo que puede afectar la imagen de la institución.
Este tema es crítico, las remuneraciones y los honorarios se han atrasado con respeto a los otros rubros del costo en la salud, y para contener la inflación, la retribución a los profesionales se ha pauperizado, debe ser abordada para su mejora progresiva y la orientación hacia la atención basada en el valor. Es un aspecto estratégico, y como tal debe evaluarse. También hay un componente de como está el mercado en cada jurisdicción, no es igual en todas las latitudes. Nuestro país son muchos países, cada provincia tiene particularidades. Falta de especialistas. Carencias de servicios. Un sector privado más fuerte o débil. Entonces hay que hacer un análisis meduloso, pelearlo en el ámbito político y con los financiadores, que son formadores de precio. No olvidar que la inflación esta disminuyendo y por lo tanto no ocultará en el tiempo errores de negociación. También se deben evaluar las tasas de uso, porque comportamientos inescrupulosos en este aspecto afecta la deontología de la profesión.
Transformación del Liderazgo en el Sector Salud
Dr, Carlos Alberto Díaz. Profesor titular Universidad ISALUD.
5 Entrega sobre las habilidades blandas. Liderazgo.

- Transaccional.
- Adaptativo
- Transformacional.
- Servicio.
La alineación de los modelos de liderazgo con la industria de la salud es crucial para enfrentar los desafíos contemporáneos y mejorar el valor de la atención al paciente. A continuación, se presenta un resumen de los modelos de liderazgo discutidos y su relación con el contexto de atención médica.
- Liderazgo Transaccional
Descripción: Este modelo se basa en un sistema de recompensas y castigos, donde se establecen objetivos claros y se suministran incentivos monetarios a quienes los cumplen.
Alineación con la salud: Si bien es el más extendido, el liderazgo transaccional puede resultarle contraproducente a los profesionales de la salud que están motivados intrínsecamente por el deseo de ayudar a otros. Este modelo no logra captar la complejidad de las motivaciones en el ámbito de la salud y puede socavar la confianza y las relaciones esenciales entre el proveedor y el paciente.
- Liderazgo Adaptativo
Descripción: Se enfoca en enfrentar y superar desafíos que surgen de cambios en el entorno. Esto incluye la regulación de la angustia del grupo y la facilitación de la colaboración para buscar soluciones innovadoras.
Alineación con la salud: El liderazgo adaptativo es excelente para abordar la complejidad y cambiante naturaleza de la atención médica. Sin embargo, puede ser menos efectivo en situaciones de emergencia donde se requiere una acción rápida y decisiva, así como en la consideración explícita de aspectos éticos cruciales.
- Liderazgo Transformacional
Descripción: Este modelo busca inspirar a los seguidores a trascender sus intereses personales en pro de un objetivo mayor, articulando una visión convincente y alentando el rendimiento excedente.
Alineación con la salud: Aunque la inspiración es crucial en la atención médica, el enfoque en la visión del líder puede limitar la flexibilidad necesaria para personalizar la atención al paciente. No siempre permite respuestas individuales a las necesidades concretas del paciente, lo cual es crítico en esta industria.
- Liderazgo de Servicio
Descripción: Este modelo se centra en servir a los demás y desarrollar la conciencia y el autoconocimiento del líder. Promueve la construcción de relaciones sólidas y la confianza.
Alineación con la salud: El liderazgo de servicio se postula como el más adecuado para la atención médica, dado que enfatiza las necesidades del paciente y fomenta relaciones de alta confianza, esenciales para la atención de calidad. Este modelo permite a los proveedores involucrarse de manera más profunda en el bienestar del paciente, así como en el fomento de un ambiente colaborativo entre el personal de salud.
Conclusiones Generales
Los desafíos actuales en el sistema de salud requieren un enfoque de liderazgo multifacético que pueda adaptarse a diversas situaciones.
Cada modelo de liderazgo ofrece beneficios y limitaciones que deben considerarse según el contexto específico de atención médica:
Flexibilidad y Adaptación: La capacidad de un líder para ajustar su estilo según la situación es fundamental, y muchos líderes pueden necesitar aplicar una combinación de estos modelos.
Enfoque en la Confianza y la Ética: La atención centrada en el paciente y la creación de un ambiente confiable son esenciales para lograr resultados positivos. El liderazgo de servicio destaca en este sentido, alineando los objetivos de los proveedores con las expectativas del paciente.
Innovación y Colaboración: La promoción de un cambio colaborativo a través del liderazgo adaptativo y transformacional puede ser esencial para enfrentar los desafíos de un entorno de atención médica en constante evolución. En definitiva, al combinar estas perspectivas de liderazgo, los proveedores de atención médica pueden crear un sistema más efectivo y sostenible que mejore tanto la calidad de la atención como la experiencia del paciente.
Los modelos de liderazgo transaccional y transformacional son dos enfoques distintos que pueden influir en la manera en que se maneja la atención médica y la relación entre los líderes y su equipo.
A continuación, se presentan las principales diferencias entre ambos modelos en el contexto de la salud:
- Enfoque Motivacional
Liderazgo Transaccional: Se basa en la motivación extrínseca. Los líderes establecen objetivos claros y recompensan a los empleados cuando los alcanzan, utilizando incentivos como compensaciones monetarias. También pueden aplicar medidas disciplinarias si no se cumplen las expectativas. Ejemplo en Salud: Un director de un hospital que ofrece bonificaciones a los médicos que alcanzan ciertos indicadores de calidad o desempeño (como el volumen de pacientes atendidos o la satisfacción del paciente).
Liderazgo Transformacional: Se centra en la motivación intrínseca. Los líderes transformacionales buscan inspirar a su equipo a trascender sus intereses personales y a comprometerse con una visión compartida, fomentando la pasión y el compromiso con la misión organizacional. Ejemplo en Salud: Un jefe de departamento que motiva a su equipo a adoptar una nueva práctica de atención centrada en el paciente, usando su propia pasión y visión para inspirar a otros.
- Relación Líder-Seguidor
Liderazgo Transaccional: La relación es más contractual y basada en resultados. Los líderes y seguidores tienen intercambios claros y enfocados en cumplir objetivos concretos. Ejemplo en Salud: Un supervisor que se reúne regularmente con su personal para revisar el cumplimiento de metas y discutir incentivos o sanciones.
Liderazgo Transformacional: Fomenta una relación más profunda y emocional. Los líderes se preocupan por el desarrollo personal y profesional de sus seguidores, promoviendo la confianza y la colaboración. Ejemplo en Salud: Un gerente que dedica tiempo a escuchar las preocupaciones de su equipo, apoya su desarrollo profesional y fomenta un ambiente de trabajo positivo, resiliente y cooperativo.
- Objetivos
Liderazgo Transaccional: Se centra en objetivos a corto plazo y en la eficiencia operativa. La atención está en resultados tangibles y mediciones de desempeño. Ejemplo en Salud: Mejorar la productividad del hospital mediante la gestión de recursos y el cumplimiento de estándares administrativos.
Liderazgo Transformacional: Enfocado en objetivos a largo plazo, como el cambio cultural y la mejora continua. Busca innovar y guiar a la organización hacia una nueva dirección y mejores prácticas.
Ejemplo en Salud: Un líder que promueve un cambio significativo en la cultura del hospital hacia un enfoque más holístico y centrado en el paciente, impulsando una mejora en la atención y la satisfacción.
Ética y Valores
Liderazgo Transaccional: Puede descuidar aspectos éticos y valores en favor de resultados medibles y logros inmediatos. Las decisiones pueden estar más centradas en satisfacer intereses personales o las expectativas administrativas. Ejemplo en Salud: Un enfoque en los números que prioriza el volumen de pacientes atendidos sobre la calidad de la atención recibida.
Liderazgo Transformacional: Enfatiza la ética, los valores y la misión del cuidado centrado en el paciente. Busca promover un sentido de pertenencia y responsabilidad compartida hacia el bienestar del paciente. Ejemplo en Salud: Un líder que se asegura de que todas las decisiones operativas reflejen los valores de compasión, respeto y atención de calidad hacia el paciente.
Cambio e Innovación
Liderazgo Transaccional: Tiende a ser más reactivo, respondiendo a problemas y cambios de manera establecida, con poca apertura a la innovación.
Ejemplo en Salud: Reacción a problemas de calidad a través de supervisiones y revisiones de desempeño, sin necesariamente involucrar el feedback del equipo para la innovación.
Liderazgo Transformacional: Proactivamente busca el cambio e innovación, alentando el pensamiento crítico y la creatividad entre los miembros del equipo.
Ejemplo en Salud: Un líder que invita a su equipo a proponer y probar nuevas intervenciones clínicas o metodologías de trabajo, fomentando un entorno de aprendizaje constante.
Conclusión
Si bien ambos modelos de liderazgo pueden coexistir en el ámbito de la salud, el liderazgo transformacional generalmente se considera más adecuado para abordar las complejidades y necesidades del cuidado centrado en el paciente, promoviendo un entorno dinámico y colaborativo que valora tanto el bienestar de los pacientes como el desarrollo y la satisfacción del personal. El liderazgo transaccional puede ser efectivo en situaciones que requieren la consecución de objetivos específicos y cuantificables, pero puede resultar limitado en la promoción de una atención de calidad y relaciones significativas entre el personal y los pacientes.
El liderazgo transformacional ofrece una serie de beneficios significativos en la atención médica, impactando tanto en la calidad de la atención al paciente como en el ambiente laboral para los profesionales de la salud.
A continuación, se detallan los principales beneficios de este modelo de liderazgo en el contexto de la atención médica:
1. Mejora de la calidad de la atención al paciente
Compromiso del personal: Los líderes transformacionales inspiran a los equipos a comprometerse con una misión compartida de atención al paciente, lo que suele traducirse en un aumento de la calidad de la atención. Enfoque en el paciente: Al promover una cultura centrada en el paciente, se fomenta un entorno donde las decisiones se toman considerando las necesidades y deseos de los pacientes.
Motivación y satisfacción del personal
Aumento de la satisfacción laboral: Al involucrar y empoderar a los empleados, los líderes transformacionales crean un ambiente de trabajo positivo, lo que puede aumentar la satisfacción y el bienestar del personal.
Desarrollo profesional: Este tipo de liderazgo fomenta el crecimiento y desarrollo profesional, alentando a los miembros del equipo a aprender y avanzar en sus carreras, lo cual es crucial en el campo dinámico de la salud.
Fomento de la innovación
Estimulación del pensamiento crítico: Los líderes transformacionales desafían a su equipo a cuestionar el status quo y a buscar nuevas formas de mejorar procesos y prácticas, promoviendo la innovación en la atención. Implementación de nuevas ideas: Al crear un entorno donde se valora la creatividad y el cambio, se facilita la implementación de nuevas tecnologías y prácticas de atención que pueden beneficiar a los pacientes.
Fortalecimiento de la colaboración y el trabajo en equipo
Relaciones sólidas: Este modelo promueve la confianza y la comunicación abierta entre los miembros del equipo, lo que fortalece las relaciones interpersonales y fomenta un trabajo en equipo eficaz. Cohesión del equipo: Al trabajar hacia una visión común, se fomenta una mayor cohesión y colaboración, mejorando la dinámica del equipo y el desempeño colectivo.
Reducción del desgaste profesional (burnout)
Apoyo emocional: Los líderes transformacionales suelen ser empáticos y comprensivos, lo que ayuda a reducir el estrés y el agotamiento entre los profesionales de la salud.
Establecimiento de un propósito: Al conectar el trabajo diario del personal con una misión más profunda y significativa, se puede disminuir la sensación de agotamiento y desmotivación.
Aumento de la retención de personal
Menor rotación: Al generar un entorno de trabajo positivo y motivador, las organizaciones que aplican el liderazgo transformacional suelen experimentar menores tasas de rotación de personal, lo que también reduce los costos de contratación y capacitación.
Adaptabilidad al cambio
Manejo de la incertidumbre: En el contexto de la atención médica, donde los cambios en políticas y tecnologías ocurren con frecuencia, el liderazgo transformacional permite que los equipos se adapten más fácilmente y sean resilientes ante nuevos desafíos.
Ética y cuidado del paciente
Fomento de altos estándares éticos: Los líderes transformacionales suelen enfatizar la importancia de la ética y la moral en la atención, promoviendo un enfoque centrado en el bienestar del paciente y la equidad en la atención.
Conclusión
El liderazgo transformacional no solo impacta en la efectividad del servicio de salud, sino que también tiene un efecto positivo en la cultura organizacional, mejorando la satisfacción y el bienestar tanto de los profesionales de la salud como de los pacientes. Al fomentar un ambiente de empoderamiento, innovación y colaboración, este modelo de liderazgo se ha convertido en una herramienta valiosa para enfrentar los desafíos complejos de la atención médica moderna.
Las características clave del liderazgo transformacional en el ámbito de la atención médica son fundamentales para crear un entorno de trabajo efectivo y motivador que fomente la mejora continua y la atención centrada en el paciente. A continuación, se describen estas características:
- Visión Inspiradora
Descripción: Los líderes transformacionales articulan una visión clara y convincente del futuro que inspira a su equipo a comprometerse con ella. Establecen una dirección que entusiasma y motiva a los miembros del equipo.
Aplicación en salud: En un hospital, esto podría manifestarse en la promoción de una nueva filosofía de atención centrada en el paciente o en el objetivo de alcanzar la excelencia en los resultados clínicos.
- Motivación Inspiradora
Descripción: Tienen la capacidad de motivar a otros a superarse y alcanzar su máximo potencial, fomentando el orgullo y la confianza en el equipo.
Aplicación en salud: Los líderes que reconocen los logros del personal y celebran sus contribuciones ayudan a fomentar un sentido de pertenencia y responsabilidad compartida.
- Consideración Individual
Descripción: Muestran interés genuino por el bienestar y el desarrollo personal y profesional de cada miembro del equipo. Dan soporte y orientan a los empleados a nivel individual.
Aplicación en salud: Un líder transformacional podría implementar programas de mentoría o coaching que apoyen el crecimiento de sus colaboradores.
- Estimulación Intelectual
Descripción: Fomentan un ambiente donde la innovación y el pensamiento crítico son valorados. Desafían las ideas y los métodos establecidos, alentando a todos a contribuir con nuevas soluciones.
Aplicación en salud: Los líderes pueden invitar a su equipo a participar en la mejora de procesos o en el desarrollo de nuevas prácticas, promoviendo la investigación y la discusión.
- Ética y Valores
Descripción: Mantienen altos estándares éticos y morales, guiando sus decisiones y acciones con principios sólidos.
Aplicación en salud: Promueven la atención centrada en el paciente y se aseguran de que todas las decisiones reflejen estos valores éticos.
- Empoderamiento
Descripción: Fomentan la autonomía y la toma de decisiones entre los miembros del equipo, permitiéndoles influir en el proceso y los resultados de su trabajo.
Aplicación en salud: Esto puede manifestarse en la delegación de responsabilidades y la confianza en el equipo para tomar decisiones en la atención al paciente.
- Comunicación Abierta y Transparente
Descripción: Establecen canales de comunicación efectivos que promueven la retroalimentación y el diálogo continuo.
Aplicación en salud: Reuniones regulares y foros donde el personal puede expresar sus ideas y preocupaciones, creando un ambiente en el que todos se sientan escuchados.
- Desarrollo de Cultura
Descripción: Trabajan para construir una cultura organizacional que valore la colaboración, la innovación y el respeto por todos los miembros del equipo.
Aplicación en salud: Implementación de estrategias y prácticas que refuercen la importancia del trabajo en equipo y el apoyo mutuo en la atención al paciente.
Conclusión
Las características del liderazgo transformacional son esenciales para el éxito en la atención médica, donde el trabajo en equipo, la innovación, la ética y la atención centrada en el paciente son primordiales. Estos líderes no solo buscan alcanzar metas y resultados, sino que se comprometen a crear un entorno positivo y enriquecedor para todos los involucrados en la prestación de atención médica.
Liderazgo en servicio
El liderazgo en servicios de salud es una habilidad blanda fundamental que se destaca debido a varias características clave:
Comunicación Efectiva: Un líder en el ámbito de la salud debe ser capaz de comunicarse claramente con su equipo, otros profesionales de la salud y los pacientes. Esto incluye tanto la transmisión de información como la escucha activa.
Empatía: La empatía es esencial en la atención de la salud, ya que permite a los líderes conectar con sus equipos y comprender mejor las necesidades y preocupaciones de los pacientes.
Trabajo en Equipo: Fomentar un ambiente de trabajo colaborativo es crucial. Los líderes deben ser capaces de unir a diversos profesionales de la salud para alcanzar objetivos comunes y proporcionar una atención integral al paciente.
Resolución de Conflictos: La habilidad para manejar y resolver conflictos de manera constructiva es una característica vital, dado que los entornos de atención médica pueden ser estresantes y cargados de emociones.
Toma de Decisiones: Los líderes en el sector salud deben ser capaces de tomar decisiones rápidas y efectivas, a menudo bajo presión, lo que requiere tanto habilidades analíticas como instinto.
Adaptabilidad: La capacidad de adaptarse a cambios en las políticas de salud, avances tecnológicos y necesidades del paciente es esencial para los líderes. Visión Estratégica: Los líderes deben tener una visión clara y ser capaces de inspirar a otros para que trabajen hacia metas a largo plazo, siéndolos para mejorar la calidad de la atención.
Desarrollo de Otros: Invertir en el desarrollo profesional de su equipo mediante capacitación y mentoría es una responsabilidad clave de los líderes en la salud. Estas características, que forman parte de las habilidades blandas del liderazgo, son fundamentales para crear un entorno de trabajo positivo y eficaz, lo que se traduce en una atención de salud de mayor calidad.
Liderazgo Adaptativo:
El liderazgo adaptativo en organizaciones de salud es un enfoque fundamental para enfrentar los cambios y desafíos que caracterizan al sector salud, especialmente en un contexto de rápida evolución como el actual. Este tipo de liderazgo se centra en la capacidad de los líderes para adaptarse a las condiciones cambiantes y a las necesidades de sus equipos y pacientes, fomentando un entorno de trabajo flexible y colaborativo.
Características del liderazgo adaptativo en organizaciones de salud:
Flexibilidad: Los líderes deben ser capaces de ajustar sus estrategias y enfoques en función de las circunstancias cambiantes, ya sea en respuesta a nuevas políticas, avances tecnológicos o crisis sanitarias.
Escucha activa: Establecer canales de comunicación abiertos con el personal médico, administrativo y los pacientes es esencial. Escuchar las preocupaciones y sugerencias del equipo promueve un clima de confianza y colaboración.
Colaboración y trabajo en equipo: Fomentar un ambiente donde se valore el trabajo en equipo permite abordar problemas complejos de manera más eficaz, al integrar diversas perspectivas y experiencias.
Desarrollo continuo: Los líderes deben promover una cultura de aprendizaje continuo, donde se apoye la capacitación y el desarrollo profesional del personal, asegurando que se mantengan actualizados sobre las mejores prácticas y avances en el área de la salud.
Toma de decisiones basada en evidencia: Utilizar datos y evidencias para guiar las decisiones ayuda a asegurar que las opciones elegidas sean las más efectivas y adecuadas para los desafíos presentes.
Enfoque en el bienestar del paciente: Priorizar siempre la atención centrada en el paciente es esencial. Esto incluye asegurarse de que las prácticas de atención médica se adapten a las necesidades y preferencias individuales de los pacientes.
Resiliencia: Fomentar resiliencia tanto en líderes como en el equipo permite enfrentar la adversidad de manera efectiva y recuperarse rápidamente de situaciones difíciles.
Implementación del liderazgo adaptativo en organizaciones de salud:
Formación y capacitación: Implementar programas de formación para líderes y personal en habilidades adaptativas y de liderazgo.
Modelar comportamientos adaptativos: Los líderes deben mostrar a través de su comportamiento cómo adaptarse a los cambios, lo que puede inspirar a otros a hacer lo mismo.
Evaluación y retroalimentación: Establecer mecanismos para evaluar el desempeño y obtener retroalimentación puede ayudar a identificar áreas de mejora y ajustar enfoques.
Fomentar la innovación: Crear un entorno donde se valore la innovación y se permita experimentar con nuevas ideas puede contribuir a resolver problemas antiguos de maneras nuevas y efectivas.
Establecer redes de colaboración: Facilitar la creación de redes entre diferentes áreas de la organización y con otras instituciones de salud puede enriquecer el intercambio de ideas y soluciones.
En resumen, el liderazgo adaptativo en organizaciones de salud es crucial para navegar en un entorno en constante cambio. Al enfocarse en la flexibilidad, la colaboración y el aprendizaje, los líderes pueden guiar a sus equipos hacia la mejora continua y la atención de calidad, garantizando así un impacto positivo en la salud de la comunidad
Diez Américas: un análisis sistemático de las disparidades en la esperanza de vida en EE.UU.
Nota del blog: Este trabajo sostiene lo que también vemos por otras razones más fuertes sobre la desigualdad en la salud, y la inequidad, que hace a la importancia del lugar donde se habita, se trabaja y las diferencias en la distribución de la riqueza, por la perdida de oportunidades que esto genera, junto al factor de la educación, muchas de las explicaciones de este trabajo de las diez américas en un mismo país no son extrapolables, pero si alertan que el desarrollo sin equidad excluye a muchas personas, que la meritocracia es un bien en la sociedad, pero no debe ser despiadada ni excluyente, sino un incentivo y un premio al esfuerzo, pero también a los que se reconvierten y encauzan su vida, no eliminar de entrada, sin importar desde donde se parte. Se debe actuar para evitar la pobreza dinástica, que se está gestando en estas latitudes.

Diferencias por ingresos

Diferencias por educación


Fondo
Hace casi dos décadas, el estudio Eight Americas ofreció una lente novedosa para examinar las inequidades en salud en los EE. UU. al dividir la población estadounidense en ocho grupos según la geografía, la raza, la urbanidad, el ingreso per cápita y la tasa de homicidios. Ese estudio encontró brechas de 12,8 años para las mujeres y 15,4 años para los hombres en la esperanza de vida en 2001 en estos ocho grupos. En este estudio, nuestro objetivo fue actualizar y ampliar el estudio original de las Ocho Américas, examinando las tendencias en la esperanza de vida de 2000 a 2021 para diez Américas (análogas a las ocho originales, más dos grupos adicionales que comprenden la población latina de los Estados Unidos), por año, sexo y grupo de edad.
Evidencias previas a este estudio
En 2006, el estudio de las Ocho Américas examinó las inequidades en la salud y la esperanza de vida de los Estados Unidos utilizando un marco novedoso que simultáneamente consideró una constelación de factores contextuales interrelacionados, que van desde el lugar hasta la raza y la etnia, entre otros. Este estudio dividió la población estadounidense en ocho grupos en función de la raza, la región geográfica, la urbanidad, el ingreso per cápita y la tasa de homicidios, y al hacerlo, encontró brechas en la esperanza de vida en 2001 en estas ocho Américas de más de una década (12,8 años para las mujeres y 15,4 años para los hombres). Otras investigaciones, tanto anteriores como posteriores, han encontrado sistemáticamente desigualdades en la esperanza de vida en los Estados Unidos, incluso por ubicación geográfica, urbanidad, raza y etnia, ingresos, logros educativos y otras dimensiones. Aunque algunos otros estudios han considerado dos de estas dimensiones simultáneamente (por ejemplo, cómo varía la esperanza de vida según la ubicación geográfica y la raza y el origen étnico), y por lo general encuentran más desigualdades e interacciones complejas, los estudios que examinan la intersección de más de dos de estas dimensiones siguen siendo raros, debido a las pequeñas cifras y otros desafíos de datos. Se realizaron búsquedas en PubMed desde el inicio de la base de datos hasta el 23 de agosto de 2024, utilizando la cadena de búsqueda («Estados Unidos») AND («esperanza de vida») AND («desigualdad» O «disparidad») AND («geografía» O «región» OR «estado» O «condado») Y («raza» O «etnia») Y («urbano» O «rural») Y («socioeconómico» O «ingresos» O «educación») para estudios que examinaran las disparidades en la esperanza de vida en los EE. UU. por ubicación geográfica, raza y etnia, estado urbano y rural, y estatus socioeconómico. Identificamos solo dos estudios, aparte del estudio de las Ocho Américas, que estratificaron la esperanza de vida en al menos tres de estas dimensiones simultáneamente (en ambos casos por raza, una medida del estatus rural-urbano y una medida del estatus socioeconómico). Además, aunque el análisis detallado de las dimensiones interactivas de la disparidad en salud es crucial para comprender plenamente la naturaleza del problema y, en el caso de los estudios geográficos detallados, también es útil para la planificación y la adopción de decisiones a nivel local, el gran volumen de resultados puede dificultar su interpretación y actuación a escala nacional.
Valor añadido de este estudio
Este estudio actualiza y amplía el estudio original de las Ocho Américas, proporcionando información sobre el tamaño y la evolución de las desigualdades de los Estados Unidos en la longevidad en el siglo XXI, incluidos los primeros 2 años de la pandemia de COVID-19. Mientras que el estudio original de Eight Americas solo podía considerar la raza y no la etnia latina, esta actualización agrega dos nuevas Américas que comprenden la población latina de EE. UU., lo que eleva el total a diez. También refinamos el enfoque metodológico para incorporar nuevas fuentes de datos y ajustes más matizados para la clasificación errónea de raza y etnia en los certificados de defunción, y para evaluar la incertidumbre para todas las cantidades estimadas.
Implicaciones de toda la evidencia disponible
Las disparidades en la esperanza de vida entre las Américas ya eran grandes a principios de siglo, pero aumentaron aún más durante las décadas de 2000 y 2010 y aún más durante los primeros 2 años de la pandemia de COVID-19. La trayectoria de la esperanza de vida, tanto antes como durante la pandemia, varió entre las Américas, lo que llevó a varios cambios en el ordenamiento de las Américas entre 2000 y 2021. Es probable que las diferencias en los ingresos y el nivel educativo expliquen algunas de las diferencias observadas en la esperanza de vida, pero es evidente que no son la única fuerza impulsora. Además de la inquietante magnitud de las disparidades, han surgido otras tendencias alarmantes. De 2000 a 2019, las personas estadounidenses blancas en los condados de bajos ingresos de los Apalaches y el Valle del Bajo Mississippi (America 8) no experimentaron un aumento en la esperanza de vida, mientras que las personas indígenas americanas o nativas de Alaska en el oeste (America 10) experimentaron una disminución sustancial. Las otras ocho Américas experimentaron aumentos en la esperanza de vida entre 2000 y 2010 (en particular en las tres Américas Negras [6, 7 y 9], que tuvieron la esperanza de vida más baja en 2000); Sin embargo, hubo mejoras mínimas entre 2010 y 2019. La esperanza de vida disminuyó en las diez Américas en 2020 y se recuperó parcialmente en solo tres Américas en 2021, y las Américas que estaban peor antes de la pandemia sufrieron algunas de las mayores pérdidas generales entre 2019 y 2021. Debemos tomar medidas colectivas para invertir en atención médica, educación y oportunidades de empleo equitativas, y para desafiar las barreras sistémicas que crean y perpetúan estas desigualdades.
Métodos
En este análisis sistemático, definimos diez Américas mutuamente excluyentes y colectivamente exhaustivas que comprendían toda la población de los EE. UU., comenzando con todas las combinaciones de condados, razas y etnias, y asignando cada una a una de las diez Américas en función de la raza y el origen étnico y una combinación variable de ubicación geográfica, estatus metropolitano, ingresos y segregación residencial entre negros y blancos.
Ajustamos las muertes del Sistema Nacional de Estadísticas Vitales para tener en cuenta los informes erróneos de raza y etnia en los certificados de defunción. A continuación, tabulamos las muertes del Sistema Nacional de Estadísticas Vitales y las estimaciones de población de la Oficina del Censo de EE. UU. y el Centro Nacional de Estadísticas de Salud desde el 1 de enero de 2000 hasta el 31 de diciembre de 2021, por América, año, sexo y edad, y calculamos las tasas de mortalidad específicas por edad en cada uno de estos estratos. Finalmente, construimos tablas de vida abreviadas para cada América, año y sexo, y extrajeron la esperanza de vida al nacer, la esperanza de vida parcial dentro de cinco grupos de edad (0-4, 5-24, 25-44, 45-64 y 65-84 años) y la esperanza de vida restante a los 85 años.
Resultados
Definimos las diez Américas como:
América 1—individuos asiáticos;
America 2: personas latinas en otros condados;
América 3: personas blancas (mayoritarias), asiáticas e indígenas americanas o nativas de Alaska (AIAN) en otros condados;
America 4: personas blancas en zonas no metropolitanas y de bajos ingresos del norte;
America 5: personas latinas en el suroeste;
America 6: personas negras en otros condados;
America 7—Personas negras en áreas metropolitanas altamente segregadas;
America 8: personas blancas en los Apalaches de bajos ingresos y el valle inferior del Mississippi;
America 9—Personas negras en el sur no metropolitano y de bajos ingresos; y
America 10: individuos AIAN en el Oeste.
Las grandes disparidades en la esperanza de vida entre las Américas fueron evidentes a lo largo del período de estudio, pero se volvieron más sustanciales con el tiempo, particularmente durante los primeros 2 años de la pandemia de COVID-19. En 2000, la esperanza de vida osciló entre 12,6 años (intervalo de incertidumbre del 95% 12,2-13,1), de 70,5 años (70,3-70,7) para América 9 a 83,1 años (82,7-83,5) para América 1. La brecha entre las Américas con las esperanzas de vida más bajas y más altas aumentó a 13,9 años (12,6–15,2) en 2010, 15,8 años (14,4–17,1) en 2019, 18,9 años (17,7–20,2) en 2020 y 20,4 años (19,0–21,8) en 2021.
Las tendencias a lo largo del tiempo en la esperanza de vida variaron según América, lo que llevó a cambios en el orden de las Américas durante este período de tiempo. America 10 fue el único Estados Unidos que experimentó disminuciones sustanciales en la esperanza de vida entre 2000 y 2019, y experimentó las mayores disminuciones entre 2019 y 2021. Las tres Américas Negras (Américas 6, 7 y 9) experimentaron aumentos relativamente grandes en la esperanza de vida antes de 2020 y, por lo tanto,
las tres tenían una esperanza de vida más alta que América 10 en 2006, a pesar de comenzar en un nivel más bajo en 2000.
Para 2010, el aumento en América 6 fue suficiente para superar también a América 8, que tuvo una tendencia relativamente plana de 2000 a 2019. América 5 tenía una esperanza de vida relativamente similar a la de las Américas 3 y 4 en 2000, pero una tasa de aumento más rápida en la esperanza de vida entre 2000 y 2019 y, por lo tanto, una esperanza de vida más alta en 2019; sin embargo, America 5 experimentó un descenso mucho mayor en 2020, revirtiendo esta ventaja. En algunos casos, estas tendencias variaron sustancialmente según el sexo y el grupo de edad.
También hubo grandes diferencias en los ingresos y el nivel educativo entre las diez Américas, pero los patrones de estas variables diferían entre sí y de los patrones de la esperanza de vida en algunos aspectos notables. Por ejemplo, America 3 tuvo el ingreso más alto en la mayoría de los años y la mayor proporción de graduados de secundaria en todos los años, pero ocupó el cuarto o quinto lugar en esperanza de vida antes de 2020.
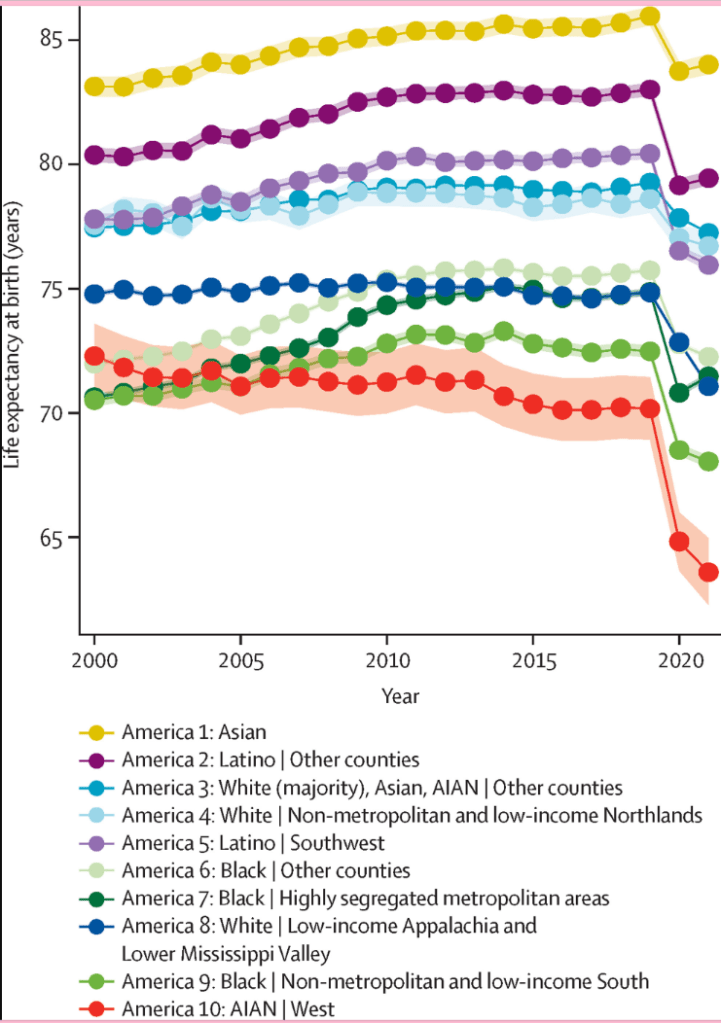
Interpretación
Nuestro análisis confirma la existencia continua de diferentes Américas dentro de los EE. UU. La esperanza de vida varía drásticamente dependiendo de dónde se vive, las condiciones económicas de ese lugar y la identidad racial y étnica de una persona. Este abismo era grande a principios de siglo, no hizo más que crecer durante las dos primeras décadas y se vio dramáticamente exacerbado por la pandemia de COVID-19. Estos resultados subrayan la necesidad vital de reducir la inequidad masiva en la longevidad en los EE. UU., así como los beneficios de análisis detallados de los factores que interactúan entre los factores que impulsan las disparidades en la salud para comprender completamente la naturaleza del problema. Dichos análisis hacen posible la acción específica —planificación local, priorización nacional y asignación de recursos— para abordar las causas fundamentales de la mala salud de los más desfavorecidos, de modo que todos los estadounidenses puedan vivir vidas largas y saludables, independientemente de dónde vivan y de su raza, etnia o ingresos.
Habilidades Blandas en Gerencia Hospitalaria
Dr. Carlos Alberto Díaz. Profesor Titular Universidad ISALUD.
4 Entrega habilidades blandas.
Las habilidades blandas las observo como una parte importante de las capacidades adaptativas a los entornos cambiantes actuales, no se busca solamente una buena relación entre el equipo de salud y sus pacientes, sino mejor desempeño, adherencia a los tratamientos en las enfermedades crónicas, disminuir el hospitalo centrismo, fortalecer ámbitos de atención ambulatoria, resultados, menos complicaciones, rápidas respuestas, continuidad de los cuidados, involucramiento adecuado, empatía, preservar el sistema al cual pertenece y le otorga el ámbito para un buen ejercicio de su profesión. Las habilidades de gestión en el ámbito de la atención de salud se componen de conjuntos de competencias esenciales para los profesionales de la salud que gestionan de manera eficaz y eficiente una variedad de recursos médicos, de enfermería o de salud pública para alcanzar objetivos que se alinean idealmente con la mejora de la salud general de la población y el sistema de atención de salud.
Los gerentes de atención médica eficaces y eficientes requieren elementos de habilidades de liderazgo para cumplir con los roles y responsabilidades gerenciales al mejor nivel posible. Las habilidades necesarias de los gerentes de atención médica incluyen habilidades de planificación, organización, implementación, monitoreo y evaluación. La planificación se refiere a la preparación de los pasos y protocolos necesarios para lograr un objetivo final y la asignación adecuada de los recursos previstos (incluidos los recursos humanos) a los objetivos y metas de la organización de atención médica. El desarrollo de un plan puede referirse a planes de acción que aborden actividades a pequeña escala para el personal individual, así como planes operativos y estratégicos para grupos pequeños (es decir, secciones, unidades, departamentos) o a nivel de toda la organización. Un requisito previo para un plan bien desarrollado con objetivos SMART (específicos, medibles, alcanzables, realistas y limitados en el tiempo) es que el gerente de atención médica debe ser capaz de realizar habilidades adecuadas de escaneo y enfoque, que en realidad son «prácticas de liderazgo». El análisis se refiere al conocimiento de uno mismo y del entorno, junto con las oportunidades, amenazas y riesgos para el personal y la organización en su conjunto, mientras que el enfoque se refiere a la concentración del trabajo de cada miembro del personal en la organización de atención médica en relación con sus declaraciones de visión y misión. La organización es la capacidad de reunir los sistemas, procesos y procedimientos con el personal designado en una organización para que las personas adecuadas puedan hacer el trabajo adecuado para el propósito correcto. Las habilidades de implementación, por otro lado, se centran en el desempeño del trabajo asignado en función de las actividades planificadas. Como gerente de atención médica, uno debe saber cómo armonizar el flujo de trabajo dentro de todo el personal involucrado, asegurando que los planes individuales y generales se implementen de manera efectiva. Las prácticas de liderazgo esenciales para organizar e implementar habilidades (de gestión) incluyen la alineación y movilización del personal. Si bien las habilidades de gestión se centran en el uso de los recursos organizacionales como se mencionó, el objetivo de las habilidades de liderazgo se centra en la movilización de los miembros de la organización.
Un buen gerente de atención médica puede brindar confianza y seguridad al personal y puede apreciar los esfuerzos del personal. La inspiración del personal puede manifestarse al brindar una supervisión de apoyo a todos los miembros de la organización. Al practicar estas habilidades de gestión de la atención médica, es evidente que las habilidades de liderazgo son igualmente vitales.
Las organizaciones de atención médica no deben desarrollar profesionales que solo puedan administrar o que sean líderes solos, porque ese tipo de persona no tendrá éxito, sino que evolucionen desarrollando capacidad de trabajo en equipo, comunicación efectiva, negociación, pensamiento innovador, capacidad para resolver conflictos, enseñar con el ejemplo, saber tomar decisiones con los pacientes, su servicio y la imagen institucional, tener habilidades estratégicas.
La gestión sanitaria, como profesión específica, destaca su valor e importancia más allá de los aspectos clínicos que se realizan en la cabecera del paciente de estas habilidades. Es importante destacar que las habilidades de gestión aplicadas en los campos de la medicina y la salud pública no sólo pretenden brindar mejores servicios de salud, sino también optimizar el estado de salud de los pacientes y de la comunidad en general.
La formación de estos directivos debe ser ya en sus puestos de trabajo, y también un proyecto prospectivo, para que logren incorporar estas habilidades antes que asumen, de esa forma, en un proyecto estratégico, de gran alcance profesionalizar la gestión de los hospitales, especialmente en las jurisdicciones que estos no dependan de su filiación política, sino de los alineamientos estratégicos con la gestión de las provincias.
Probablemente con esta afirmación que sigue uno sea injusto o simplificando, pero en algunos ámbitos que conozco como Chubut, Ciudad Autónoma de Buenos Aires, La Pampa, Mendoza, San Luis, pueden ser provincias en los cuales se pueda implementar una capacitación que sería una inversión con rápido retorno en cuanto a la mejora de la gestión y el desempeño de los hospitales, ya que los gerentes de los hospitales no dependen de una pertenencia política sino de un alineamiento de proyectos y propósitos. Espero que estos modelo de Gobernanza Clínica puedan difundirse a otros lugares de la Geografía.
Competencias requeridas y desafíos futuros de los gerentes de hospitales: un estudio cualitativo
Farideh Moradi 1 , Razie Toghroli 1 , Jaffari Abbas 2 , Arash Ziapour 3 , Javad Yoosefi Lebni 4 , Amin Aghili 5 , Nadya Baharirad 1 , Mohammad Mohseni 6 , Ali Soroush 1,

| Tema | Subtema |
| Habilidad estratégica | Análisis ambiental |
| El poder del futurismo | |
| Análisis del entorno externo | |
| Habilidad perceptiva | Diagnosticar la posición de las operaciones individuales en la organización |
| Priorizar los problemas hospitalarios | |
| Proceso de resolución de problemas | |
| Toma de decisiones en situaciones inestables | |
| Habilidad en relaciones humanas | Participación y trabajo en equipo |
| Comunicación con los demás | |
| Experiencia laboral | Experiencia en gestión |
| Experiencia en gestión | |
| Característica personal | Motivación e interés |
| Conocimientos de gestión | |
| Autoconfianza y coraje en la toma de decisiones | |
| Autogestión | |
| Desarrollo individual continuo |
Las habilidades y cualificaciones requeridas por los gerentes de hospitales
La habilidad de las relaciones humanas
La habilidad de relaciones humanas se refiere a la capacidad y habilidad para crear un ambiente de coordinación y colaboración, delegar tareas a otros, realizar actividades efectivas como miembro de un grupo, comprender las motivaciones de los individuos e influir en sus comportamientos. Desde el punto de vista de la mayoría de los participantes, la habilidad de relaciones humanas y la capacidad de interactuar con los demás se encuentran entre las habilidades más importantes y básicas que requieren los gerentes, ya que esta habilidad es la clave del éxito del gerente del hospital. “ Creo que la clave del éxito de un buen gerente es su capacidad para establecer buenas relaciones con sus colegas y subordinados ” (Participante 5). “ De hecho, un buen gerente debe querer a sus empleados y debe tener buenos encuentros con ellos y ser capaz de establecer buenas relaciones con ellos ” (Participante 12).
Experiencia laboral
Una de las cualidades que los participantes destacaron como necesarias para el éxito de un gerente fue la experiencia en gestión, donde la experiencia de trabajar en el hospital y tener experiencia en puestos directivos se encontraban entre los casos mencionados. “ Tener el conocimiento y la experiencia necesarios en el campo de la gestión no será suficiente; más bien, el gerente también debe tener experiencia trabajando en un hospital para comprender los matices de varias cuestiones ” (Participante 21). “ En mi opinión, una de las cualidades necesarias para convertirse en gerente debe ser una experiencia laboral de al menos 5 años en un hospital; no debería ser el caso de que después de obtener un título, obtengan puestos de gestión fácilmente” (Participante 14).
Habilidad perceptiva
La capacidad perceptiva es una de las habilidades necesarias para un gerente exitoso. Las cuestiones en las que se debe prestar atención en este sentido incluyen la discreción del gerente en función de la adecuación de cada empleado a su puesto, la priorización de los problemas del hospital y la selección del proceso adecuado para resolver o mitigar estos problemas. “ El gerente debe ser capaz de determinar la posición de los individuos en función de su pericia y experiencia” (Participante 3). “El gerente debe priorizar los problemas del hospital. No debería suceder que el gerente se olvide de las bonificaciones de los empleados y se dedique a ampliar las salas del hospital o a decorar los departamentos” (Participante 2).
Tener habilidades estratégicas
Entre los elementos considerados por los participantes como competencias y habilidades del director de un hospital se encuentran la visión estratégica a largo plazo y la capacidad de predecir el futuro. “Un director exitoso debe ser capaz de guiar a la organización hacia perspectivas adecuadas a largo plazo y debe dirigir el hospital de manera que mejore año tras año” (Participante 11). “Un buen director debe tener una visión a largo plazo y debe ser capaz de realizar un análisis adecuado de las externalidades e internas de la organización y basar sus planes en estas cuestiones” (Participante 18).
Características personales
Algunos de los participantes indicaron que las personas que solicitan convertirse en gerentes de hospitales deben tener características personales específicas, como estar interesados en adquirir ese puesto directivo. Estar motivado para trabajar, tener autoestima y tener suficiente información sobre el entorno hospitalario se encuentran entre otros elementos mencionados. “ Estar motivado e interesado es muy importante y necesario para un gerente. Un gerente desmotivado hará que la mayoría de los empleados también pierdan su motivación” (Participante 7). “El gerente debe ser decisivo en su toma de decisiones y debe ser franco con todo el mundo. Debe ver a los subordinados como amigos o conocidos cuyos errores debe ignorar” (Participante 2). “El gerente debe ser capaz de adaptarse a los problemas modernos y debe estar actualizado . Sus pensamientos también deben estar actualizados” (Participante 8).
Desafíos que enfrentan los gerentes de hospitales
Políticas y regulaciones
Uno de los retos mencionados por los entrevistados fue el tema de los rápidos cambios en las políticas y regulaciones del Ministerio de Salud. Al respecto, uno de los participantes dice: “Las políticas del Ministerio de Salud cambian rápidamente y deprisa, y cuando todavía estás intentando familiarizarte con una política y aprender de qué se trata, de repente te cambian la política” (Participante 10). Con respecto a la falta de regulaciones claras, uno de los entrevistados dijo: “Las regulaciones y burocracias restringen la libertad de los gerentes y de hecho le atan las manos ya que no puede cambiar ninguna parte de ellas” (Participante 22).
Recursos y activos
Entre los desafíos mencionados por los entrevistados se encuentra la falta de recursos y de activos financieros y humanos. En este sentido, el entrevistado 17, como uno de los gerentes de alto nivel, afirma: “Los hospitales se enfrentan a una escasez de recursos, en particular en lo que respecta al número de enfermeras. También nos enfrentamos a problemas relacionados con el dinero y el presupuesto. Por ejemplo, cuando se estropea un equipo, no hay dinero para repararlo. Las compañías de seguros, por otro lado, no tienen dinero para darnos” (Participante 13). “En este momento, la principal preocupación de los gerentes es la escasez” (Participante 10).
Educación
Entre los desafíos mencionados por los directivos se encuentran la escasa formación y la falta de adecuación entre la formación y los títulos de los individuos y su área ocupacional. En este sentido, el entrevistado 10 afirmó: “No existe una relación entre la carrera universitaria de los directivos y su área ocupacional. Por ejemplo, las personas que han estudiado gestión hospitalaria deben convertirse en gerentes de hospitales porque tienen la experiencia necesaria, pero eso no se ve en la práctica” (Participante 6). “Hoy en día vemos que la mayoría de los médicos son gerentes de hospitales y, si se mira más de cerca, ni siquiera saben lo que significa gestión” (Participante 4).
Discusión
En este estudio, se identificaron las habilidades necesarias para los gerentes de hospitales y los desafíos que enfrentan. Con base en los resultados obtenidos del estudio, la habilidad de las relaciones humanas es una de las habilidades necesarias para los gerentes de hospitales. Los resultados de Pillay muestran que la gestión de individuos y las habilidades humanas son las habilidades más importantes para los gerentes de atención médica.[ 18 ]
Además, Asiabar et al . y Majid et al . muestran una relación significativa entre la habilidad humana de los gerentes y la motivación de los empleados.[ 19 , 20 ] Los resultados de una encuesta nacional en los EE. UU. muestran que la habilidad y calificación más importante necesaria para los gerentes de enfermería eran las relaciones efectivas e influyentes.[ 21 , 22 ]
Otros estudios también enfatizan la importancia de la habilidad de las relaciones para los gerentes de centros de atención médica, particularmente hospitales.[ 23 , 24 , 25 ] El estudio realizado por Khadka et al . enfatiza la importancia de las habilidades comunicativas para los gerentes de hospitales, y los autores sugieren que las habilidades de liderazgo y comunicación son los factores competitivos más importantes entre los gerentes de hospitales.[ 26 ] Los resultados de Stefl muestran que la gestión de las relaciones y las comunicaciones, que incluyen habilidades comunicativas, facilitadoras y de negociación, se encuentran entre las habilidades importantes para un gerente.[ 27 ] Además, los resultados de Kalargyrou et al . indican la importancia de la habilidad de las relaciones humanas entre las habilidades de los gerentes. Los resultados de estos estudios están en línea con los resultados del estudio actual.[ 28 ]
Las habilidades de los gerentes conducen al aumento de su aceptación y atractivo entre los empleados, lo que resulta en una reducción del estrés y un mejor desempeño de los empleados.[ 29 , 30 ] Kebede et al . muestran que la capacitación de los gerentes de hospitales basada en la mejora de sus habilidades gerenciales resulta en una mejora significativa en el desempeño de los sistemas de atención de la salud.[ 31 ] Por lo tanto, se sugiere que la evaluación de las relaciones de los gerentes con los empleados se realice regularmente, y se sugiere que se realicen talleres para gerentes sobre los métodos de interacción adecuada con los empleados, incluyendo simpatizar con los empleados y escucharlos efectivamente.
El conocimiento gerencial fue uno de los elementos mencionados en la mayoría de las entrevistas. Los resultados de un estudio sobre hospitales supervisado por la Universidad Médica de Teherán muestran que el campo del conocimiento gerencial se divide en cuatro categorías, es decir, planificación, organización, control y liderazgo. Entre estas, el liderazgo tiene la mayor prioridad desde el punto de vista de los gerentes intermedios de los hospitales.[ 32 ] A pesar de este hecho, en su estudio, Khadka et al . señalan que el conocimiento gerencial es menos importante. Sin embargo, su estudio se llevó a cabo en hospitales privados y públicos, mientras que el 59% de los gerentes participantes no tenía educación o capacitación gerencial previa.[ 26 ] Un estudio de Rivkani muestra que, si bien el 70% de los gerentes de hospitales han aprobado el curso de capacitación para la gestión de asuntos hospitalarios, no todos ellos poseen el conocimiento y la experiencia gerenciales adecuados.[ 33 ]
Otro resultado de este estudio fue el enfoque en la visión estratégica y de largo plazo como una de las habilidades de los gerentes de hospitales. Crear y desarrollar una mentalidad estratégica es uno de los requisitos del campo de la gestión, y este tipo de mentalidad es necesaria y crítica para todos los niveles organizacionales, particularmente para la alta gerencia.[ 34 ] Los hospitales, como las organizaciones más importantes y más complejas que brindan atención médica, requieren mentalidades sistémicas y sistemáticas más que cualquier otra organización. La mentalidad sistémica es un marco conceptual para resolver problemas, que ocurre al enfocarse en los problemas y durante la ejecución. La resolución de problemas en este método se obtiene al encontrar un patrón para aumentar la percepción y la comprensión organizacional y enfocarse en los problemas.[ 19 ] La relación entre pensar y enfocarse en problemas sistémicos y mejorar el desempeño de los empleados ha sido probada en un estudio.[ 35 ] Amini et al . concluyen que el estado del factor de pensamiento sistémico entre la mayoría de los gerentes de la Universidad Médica de Teherán está en un nivel deseado y estos gerentes se rigen por el pensamiento sistémico.[ 36 ] Terzic-Supic et al . se dieron cuenta de que la enseñanza de la planificación y la gestión estratégicas desempeña un papel eficaz en la toma de decisiones óptima de los gerentes de hospitales.[ 37 ]
Tener motivación e interés en convertirse en gerente y trabajar en un hospital fue otro requisito del gerente de hospital mencionado en algunas de las entrevistas. Según el modelo propuesto por la Organización Mundial de la Salud, las calificaciones de gestión se clasifican en tres grupos que incluyen la creación de un entorno empoderador y motivador que, a su vez, incluye guiar y crear motivación en los empleados para superar los desafíos ambientales y alcanzar los objetivos, garantizar la utilización eficaz de los recursos y ampliar el nivel de participación en toda la organización y fuera de ella. [ 38 ] Las autoridades deben prestar atención al punto de que la motivación es uno de los pilares principales de la gestión [ 4 ] y un individuo desmotivado no puede ser un gerente exitoso en la organización. Por lo tanto, al seleccionar gerentes de hospitales, se debe considerar esta cuestión y se debe priorizar a las personas que estén interesadas y motivadas para obtener los puestos de gerentes de hospitales.
Un gerente desmotivado puede propagar esta falta de motivación entre los demás empleados. Por otro lado, los gerentes motivados que saben cómo motivar a los empleados pueden trabajar para lograr los objetivos de la organización con la ayuda de los empleados y también tendrán éxito en el desempeño de sus otras funciones. Para que el departamento de recursos humanos tenga un buen desempeño y pueda seleccionar gerentes calificados para el sistema de atención médica, también debe tener un gerente calificado. [ 35 ] Por lo tanto, se sugiere que la selección de gerentes se base en una evaluación integral y de largo plazo de los individuos y, en este sentido, se deben considerar y ser la base de la evaluación medidas como tener relaciones humanas, los métodos de interacción con colegas y subordinados, visión estratégica, tener el poder de planificación, las estrategias para enfrentar los problemas y tener creatividad e iniciativa. Además, también se debe considerar la experiencia ejecutiva y la pericia de los gerentes, y es obvio que se deben seleccionar gerentes que tengan una formación académica en los campos relacionados con la gestión hospitalaria, ya que los resultados del estudio muestran que los estudiantes de gestión hospitalaria que pasan más tiempo en su hospital estarán más familiarizados con el sistema y los requisitos y necesidades del instituto.[ 26 ]
Los resultados de Ahmad et al . y Romdhane et al . muestran que uno de los desafíos que enfrentan los gerentes de hospitales es el rápido cambio en las políticas del Ministerio de Salud. En otras palabras, cuando se nombra un nuevo ministro, se diseñan nuevas políticas basadas en las nuevas prioridades y planes del ministro y se asignan recursos para implementar estas políticas y los planes operativos se ejecutan rápidamente y, en efecto, algunos de los sistemas anteriores dejan de funcionar o no hay suficiente oportunidad para implementar esos sistemas. El problema de la falta de estabilidad política y gerencial se observa en la mayoría de los países en desarrollo. Ejemplos de ello son Siria y Túnez.[ 39 , 40 ] Además, los efectos del clima político sobre las políticas sanitarias en Pakistán muestran que el cambio rápido de los gobiernos afecta a las políticas, causando la implementación imperfecta de varias políticas.[ 41 ] Además, el mismo problema se experimentó en la India, donde, en períodos de tiempo específicos, las políticas se implementan seriamente sólo para detenerse o ralentizarse en el futuro cercano debido a problemas financieros y la baja capacidad de implementación del sistema de atención de la salud.[ 42 ] Como sabemos, el campo de la formulación de políticas macro y la toma de decisiones depende directamente de la calidad de los recursos humanos en términos de su conocimiento y comportamiento. Naturalmente, cuanto mayores sean las calificaciones y la calidad de los individuos, mayor será la calidad y la eficacia de las decisiones. Es obvio que cuando se implementa un plan estratégico profundo e informado para cada una de las políticas y planes, podemos esperar reducir los efectos de los gustos personales y asegurar su implementación continua después de que se designe otra autoridad.
Uno de los desafíos mencionados por los entrevistados fue la escasez de recursos financieros y humanos. Con base en los resultados del estudio de Delgoshaie et al . la escasez de recursos financieros es uno de los desafíos operativos para los programas hospitalarios, lo cual está en línea con los resultados del estudio actual.[ 43 ] Hilal et al . también afirmó que la falta de tiempo y recursos es un desafío para los gerentes.[ 21 , 34 ] En muchos estudios se ha reportado un número menor que el umbral estándar determinado por el Ministerio de Salud para los recursos humanos en los hospitales.[ 44 ] Los resultados obtenidos de los estudios de Mehrolhasani y Farzianpour et al . que evalúan la eficiencia de los hospitales muestran que uno de los factores que influyen en la falta de eficiencia en los hospitales es la gran cantidad de recursos humanos en los hospitales, particularmente en los hospitales académicos, lo cual no está en línea con los resultados del estudio actual.[ 45 , 46 ] Parece que el tipo de estudio puede haber afectado la variación en los resultados.
Este estudio examina por primera vez las habilidades y los desafíos que enfrentan los gerentes de hospitales en Irán desde su propia perspectiva, de modo que pueda proporcionar información adecuada para que los gerentes controlen los desafíos. Una de las limitaciones de este estudio fue la demora en la realización de algunas de las entrevistas, y los investigadores hicieron todo lo posible para obtener tiempo oportuno y suficiente de los entrevistados. Sin embargo, la debilidad del presente estudio fue la falta de generalización de los datos debido a la característica cualitativa del estudio, el tamaño de la muestra y el método de muestreo.
Conclusión
Entre las competencias requeridas para los gerentes de hospitales se encuentran las habilidades de relaciones humanas, visión estratégica y percepción, así como experiencia laboral y características personales. Por su naturaleza y diferencia con las demás secciones de servicios, los hospitales y su gestión son mucho más sensibles a estos aspectos.
En este sentido, el papel del gerente de hospital es muy importante; por lo tanto, para lograr la satisfacción de las personas que reciben los servicios y mejorar la salud de los miembros de la comunidad, que es uno de los objetivos del sistema de atención de salud, así como para garantizar la eficiencia y productividad de los recursos de atención de salud, los encargados de la toma de decisiones y los encargados de la formulación de políticas que trabajan en la selección y nombramiento de gerentes de hospitales deben pensar dos veces y, en este sentido, evaluar a este grupo en términos de las capacidades y habilidades requeridas para el trabajo de gestión hospitalaria.
El Poder del Trabajo en equipo en la Atención de salud
Dr. Carlos Alberto Díaz. Profesor Titular Universidad ISALUD. Buenos Aires. Argentina.
Tercer entrega de la serie habilidades blandas: trabajo en equipo.
La importancia de las habilidades blandas en las carreras de atención médica
La importancia del liderazgo y del trabajo en equipo son dos de las habilidades blandas más importantes de las ventajas competitivas de nuestras instituciones. El poder de la atención colaborativa del equipo, el compromiso, la cooperación, la colaboración, la sinergia, la cobertura de funciones. El problema de estos posteos sobre las habilidades blandas ocurre en la poca bibliografía específica que se encuentra, y el escaso interés por investigar estos temas importantes para la mejora prestacional. Porque no difunden una nueva tecnología ni un tratamiento distinto sumamente costoso.
Trabajo en equipo: el poder de la atención colaborativa
- La atención sanitaria es un trabajo en equipo. Ya sea en un hospital, una clínica o cualquier otro entorno sanitario, los profesionales deben trabajar juntos para ofrecer la mejor atención posible. El trabajo en equipo implica colaborar con colegas, compartir responsabilidades y apoyarse mutuamente de manera cohesiva. El trabajo en equipo en el ámbito sanitario implica una amplia gama de trabajadores sanitarios, incluidos enfermeros, médicos, kinesiólogos, trabajadores sociales, terapeutas y personal administrativo, que trabajan todos juntos para ofrecer una atención integral. En un equipo como este cada uno de los integrantes deben considerarse responsables. Ese grupo de personas, que tienen una tarea común, y al mismo tiempo muy diversa, que no se puede hacer de forma individual, sino por la interactuación entre ellos.
- El producto fundamental de un equipo es hacer las cosas juntos. Complementarse. Organizarse. Cumplir las tareas. El producto fundamental de un equipo que hacen las cosas juntos. La necesidad de un equipo es la búsqueda de la calidad, de la seguridad de los pacientes, de la mejora de los resultados, mediante el aporte de ideas, la colaboración, la cooperación, la búsqueda de la mejora continua, es la finalidad basada en un trabajo compartido: de hacer correctos diagnósticos, buenas indicaciones en tiempo, revisar todos los días a los pacientes, escuchar sus inquietudes, que se administren los fármacos en forma segura, que al paciente se les de confort y confortabilidad, respetarles el sueño, su dignidad, que no sufran dolor, que se sienta escuchado, la búsqueda de una atención centrada en las personas, compartir lo que se hace entre los integrantes del equipo.
- El compromiso es la cualidad fundamental de los integrantes del equipo. Con el propósito del servicio, con los pacientes, con la misión de la institución. Mostrar un compromiso intenso más allá de las diferencias que se puedan tener entre los integrantes.
- El equipo, sus jefes e integrantes deben tomar decisiones, compartirlas, comunicarlas, explicarlas, fundarlas. Saber tomar decisiones, quien lo tiene que hacer y en que momento. Como se comunican las mismas en el equipo, y hacia sus pacientes y familias. Tomar decisiones implica lo que se llaman ciclos recursivos, donde cada paso del ciclo es productor del próximo paso. Esto implica: definir el tema, generar opciones, establecer criterios, analizar las opciones, consultar en relación al impacto sistémico de estas decisiones, entonces tomar una decisión, aplicar la decisión, evaluar la decisión adoptada. El proceso engloba como se observa ocho elementos, cinco de ellos deben ser previos a tomar una decisión, especial es el de evaluación del impacto que generó en el resto. El sexto es tomar la decisión, llevar a la práctica lo acordado, y evaluar los resultados de la decisión adoptada. Definir el tema sobre lo que se tomará una decisión. Muchas veces se conversa en equipo sin tener una definición clara sobre el tema real que se está discutiendo. Que está detrás de esa decisión. Cuidado con la infiltración en estas decisiones del complejo industrial médico y su capacidad de influencia sobre los médicos, en ocasiones con un claro conflicto de intereses. Es frecuente que los equipos y sus lideres rehúsen discutir temas de gestión de procesos, si de pacientes complejos y difíciles, de decisiones terapéuticas comprometidas, pero no como dar las altas temprano o dejar de utilizar medicamentos o prácticas innecesarias.
- El equipo debe generar un ámbito de trabajo que se disfrute, trabajando mucho, cumpliendo, con productividad, con organización, horarios, terminar las tareas, no dejando todo para mañana. Generar un ámbito de trabajo apacible, contenedor, de aprendizaje y crecimiento profesional, y también mostrar altos niveles de confianza entre los ejecutantes. Sostener un elevado grado de entusiasmo y energía. Historias compartidas de momentos vividos, que los una.
- Conocerse entre los integrantes, especialmente en los momentos difíciles para generar confianza. Confianza en la habilidad técnica de los integrantes de los equipos, confianza entre lo que se dice y se hace, confianza en la sinceridad y el cuidado mutuo. Que los acuerdos y compromisos se cumplan escrupulosamente y cuando no sea posible, se gestiona el incumplimiento y se explican sus causas. Humor, diversión, buen ánimo.
- Los equipos deben gestionar los conflictos inmanentes. Aceptar los conflictos gestionarlos constructivamente y promuevan soluciones divergentes. Saber decirse las cosas. Exigir a los proveedores que actúen en consonancia con el modelo asistencial y no afecten con demoras los resultados. Crear un gran número de nexos, sinergia y conectividad. Tener en claro el propósito. Que sea compartido y que se aprenda. Que se aprenda y se desarrollen, si los miembros del equipo crecen, lo harán sus líderes. Congeniar tareas asistenciales, académicas, de figuración y mostrar siempre lo que se realiza como una cuestión de conjunto.
- Los equipos deben identificar el sentido de su trabajo. Conocer claramente el sentido del trabajo que es la medida de lo posible mejorar la calidad de vida de las personas, lograr su bien-estar. Esto hará identificar el sentido del trabajo. Que la cultura de lo que se hace fomente el trabajo en equipo. El equipo no es un ente aislado y autosuficiente. El entorno organizativo debe ser un potenciador del potencial del equipo de trabajo. El equipo debe saber cuando esta generando un producto asistencial y cuando es proveedor de información para otros servicios. De forma tal que no afecten el trabajo de otros equipos, como por ejemplo enviando Inter consultores de poca experiencia.
- Ajustar los sistemas retributivos en los equipos de trabajo. Los sistemas retributivos, de incentivos, de pago por desempeño no deben ser individuales, sino al equipo, distinguiendo claramente quien ha estado.
- Algunos integrantes son sumamente individualistas y sus consecuencias. Existen personas, profesionales formados en niveles académicos, no saben trabajar en equipo, y no aportan todo su potencial al logro de los resultados. Son lobos solitarios, «que solo se limitan a realizar su trabajo» Esto nos ocurre en frecuentes ocasiones porque los integrantes tienen muchos empleos y a cada uno le resta horas, y no se puede quedar un poco más de tiempo o concurrir en los horarios que los otros integrantes están. Se debe tratar que existan comunicaciones responsable a responsable, que no dialoguen por interpósitas personas, porque eso no contribuye al resultado y afecta el ánimo de los integrantes, que se sienten ninguneados por esos especialistas que le hablan solo a los residentes. Los integrantes de los equipos, servicios o microgestión, no deben tener agendas personales contradictorias. Dificulta las reuniones de agenda y priorización diarias. La distribución de tareas y la comunicación. Algunas personas tiene puesta la mirada fuera del equipo. Ocurre tanto en los médicos como en las enfermeras. Porque este, es su segundo trabajo. El otro, es en el que colocan toda su fuerza.
- Respeto de las relaciones de poder en un equipo horizontal, una responsabilidad compartida. El desarrollo del trabajo en equipo no debe afectar el devenir de las relaciones de poder, el jefe tiene una responsabilidad mayor, es el gerente de un equipo, no hace todo, y se lo debe respetar, aunque el equipo sea horizontal y todos ser escuchados como corresponde. En los hospitales existen relaciones de poder, jerarquías, jefaturas, pero estas tienen que liderar equipos de trabajo sin ellos no se podrá dar una buena atención.
- Generar en el equipo un ámbito de formación y aprendizaje constante. Integrar un buen equipo es un ámbito de formación, mediante información nueva cada día, de aprender algo que esta publicándose. La colaboración está en el estudio compartido, en que personas con desinterés compartan la información, el conocimiento, que es lo que mantiene unido al servicio y lo hace crecer.
- Equipos anclados en el recuerdo, en el pasado. También corresponden que no se oculten hechos del pasado que puedan interferir en las relaciones actuales, estos hechos son desvinculaciones, despidos, negar ascensos, cualquier decisión que es percibida como injusta porque genera desconfianza y poco compromiso. Existen equipos que se encuentran amarrados en ese pasado y no pueden despegar entonces tenemos que ayudar para que se empiece a construir el futuro.
- Relaciones personales conflictivas dentro de los equipos. También cuando hay relaciones personales conflictivas. El equipo asistencial es un sistema en el cual se generan patrones y relaciones que van más allá de lo individual. Sin embargo, siguen siendo las persona que lo componen y, en ocasiones, las relaciones personales entre algunos de sus miembros serán los factores determinantes para el funcionamiento del equipo. Deben ser capaces de relacionarse lo suficiente como para contribuir al equipo al máximo nivel. Cuando no es así, el equipo queda atrapado en esa conflictividad individual y necesita encontrar la forma de superarla para alcanzar los mejores rendimientos.
- Conversar en equipo. Una tarea que tenemos que aprender y respetar son las tareas en las cuales hablamos o conversamos en equipo, sobre los pacientes, sobre los integrantes, sobre las evaluaciones de desempeño y que tienen que mejorar y como lo harán. Cuando se habla frente a un grupo de personas las cosas se amplifican. se difunden tienen otro impacto. Cambian las interpretaciones y las emociones. Mostrar las situaciones críticas de mal rendimiento, sus causas, y las acciones para que no se repitan en un marco de respeto y constructivo. Tener claridad sobre el fin para el que se presenta correctamente el tema, la mejor forma de estructurarlo. Que las personas sepan los temas que se van a tratar y la finalidad que tienen. Conversaciones para informar sobre la evolución de los indicadores. Para decidir el lanzamiento de nuevos programas asistenciales, en los cuales los equipos participan. Las conversaciones tienen cuatro tipos básicos que se deben conocer: Seguimiento. Información. Decisión. Debate. El seguimiento es importante para revisar los acuerdos anteriores y haciendo la continuidad de la situación. Los acuerdos están para seguirlos y cumplirlos. También para seguir en el caso de los proyectos. Esto sirve para aumentar la conciencia de los micrologros. Los equipos y las organizaciones son de memoria frágil. No evitar las explicaciones sobre los incumplimientos y sus justificaciones. Los resultados son las medidas a tomar en el futuro. Realizar ajustes rápidos. Revisar los acuerdos. Medidas para evitar los desvíos. Recursos a destinar. Nuevas fechas.
LAS CINCO CLAVES DE LOS EQUIPOS DE ALTO RENDIMIENTO:
- Confianza entre los integrantes del equipo.
- Roles, estructura y claridad de tareas.
- Sentido y propósito del trabajo.
- Impacto esperado del trabajo.
- seguridad psicológica.
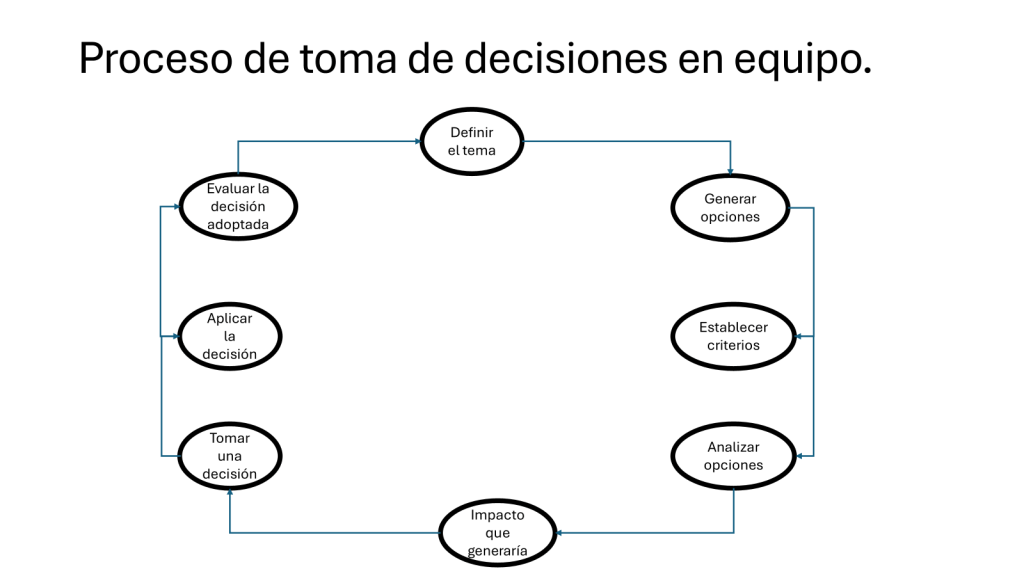
Se puede pensar en el trabajo en equipo como alguien que es capaz de colaborar con compañeros de trabajo. Esto es definitivamente una parte clave, pero específicamente en el cuidado de la salud, los atributos individuales como la confiabilidad, la adaptabilidad y el respeto también juegan un papel fundamental en el éxito de un equipo de atención médica. Los trabajadores de la salud con fuertes habilidades de trabajo en equipo administran eficazmente su tiempo, cumplen con los compromisos y brindan una calidad de atención constante. Se ganan y respetan a los demás (pacientes y colegas). En una industria que cambia continuamente, los jugadores de equipo aceptan y se adaptan a los cambios.
Trabajar en equipos eficaces mejora los resultados clínicos, aumenta la satisfacción profesional y brinda un apoyo crucial entre pares. Sin embargo, el trabajo en equipo como valor fundamental suele faltar en la atención médica, lo que limita los beneficios que logramos.
Un único encuentro de atención médica puede implicar interacciones con varios profesionales de la salud en diversos entornos clínicos. Reconocer que una atención de alta calidad requiere una cuidadosa coordinación y colaboración ha impulsado numerosas iniciativas destinadas a mejorar el trabajo en equipo clínico.
El trabajo en equipo requiere algo más que habilidades de comunicación, coordinación o incluso objetivos mutuos. Como principio rector, el trabajo en equipo eficaz requiere una mentalidad colaborativa que reconozca el valor inherente del modelo de equipo y un compromiso con la construcción de relaciones efectivas.
Adoptar una mentalidad colaborativa genera un mayor respeto por nuestros compañeros de trabajo y sus contribuciones únicas a la atención al paciente. Además, esta mentalidad nos hace ser más conscientes de cómo nuestras acciones afectan a las de nuestros compañeros de equipo y, en última instancia, influyen en los resultados clínicos.
Cuando se adopta una mentalidad colaborativa, los equipos se convierten en oportunidades naturales para la integración, la innovación y la mejora de la calidad. Sin embargo, cuando el trabajo en equipo no es un valor fundamental, hacemos las cosas por inercia, pero carecemos de la convicción subyacente necesaria para una colaboración eficaz.
La personalidad de un jugador de equipo es una característica importante en el personal de atención médica. Algunas áreas de la atención de la salud podrían compararse con los deportes profesionales, con muchos personas que se unen para brindar atención a los pacientes. Con el mejor interés de la A pesar de todo, todos deben entender cómo tratar a todos los demás miembros del equipo. Equipo superior funcionamiento se relaciona con mejores resultados en los pacientes, según un estudio publicado en la revista Revista del Colegio Americano de Cirujanos (Gibert, Tozer y Westoby 2017).
La personalidad es la clave para el éxito del trabajo en equipo. Trabajar en un equipo que funciona bien ofrece grandes oportunidades de aprendizaje a todos los miembros del equipo. (De hecho, 2021).
Construir relaciones positivas con los compañeros de trabajo es importante, y esto se puede lograr de la siguiente manera: tener conversaciones abiertas y francas sobre planes y actividades de tiempo libre, familias, e intereses. Encontrar similitudes en la vida y la historia de uno con sus compañeros de trabajo construye buena relación, lo que a su vez afecta al ambiente de trabajo, la confianza y la fluidez de trabajo. (2021).
Empatía: Es importante en el cuidado de la salud ser capaz de empatizar con los pacientes y a pesar de que las condiciones son difíciles. A menudo se cita a la empatía como una característica central de la consultas clínicas cesantes, a pesar de que no existe un estudio sobre sus consecuencias. (Ratka, John y College 2018).
Adaptabilidad: La palabra adaptar deriva de la palabra latina adaptus, que significa confirme o entrar. La adaptabilidad se refiere a la capacidad de un individuo para mezclarse dentro de un conjunto de metodologías y cultura de trabajo cuando se trabaja bajo los límites de fuentes y la satisfacción de las necesidades. La adaptabilidad a menudo se conoce como la capacidad de discriminar entre lo que sucede objetiva y subjetivamente, para adaptar eficazmente los propios sentimientos, emociones y acciones a la situación, y a considerar, describir y proporcionar Alternativas. (Sirotiak y Sharma, 2019).
El papel integral de las habilidades blandas en la industria de la salud
Si bien las habilidades técnicas y los conocimientos médicos son fundamentales para la atención médica, las habilidades interpersonales son igualmente importantes. Permiten a los profesionales de la salud comunicarse de manera eficaz, empatizar con los pacientes, trabajar en colaboración, resolver problemas de manera eficiente y liderar con confianza. Al perfeccionar estas habilidades, los profesionales de la salud pueden brindar una atención integral que aborde tanto las necesidades físicas como emocionales de los pacientes, lo que en última instancia conduce a mejores resultados de salud y una experiencia de atención médica más positiva para todos.
Las habilidades blandas también son esenciales para tareas como programar citas, que requieren que los profesionales de la salud sean organizados y se comuniquen eficazmente con pacientes y colegas.
A medida que la industria de la salud continúa evolucionando, la demanda de profesionales con sólidas habilidades interpersonales no hará más que crecer. Invertir en el desarrollo de estas habilidades es crucial para cualquiera que aspire a destacarse en una carrera en el área de la salud . Ya sea a través de capacitación formal, tutoría o autorreflexión, mejorar las habilidades interpersonales no solo beneficiará a los profesionales individuales, sino también a los pacientes y las comunidades a las que sirven.
El éxito en el ámbito de la atención sanitaria requiere algo más que conocimientos clínicos y habilidades técnicas. En entornos sanitarios de alto contacto donde la colaboración es fundamental, los trabajadores sanitarios deben demostrar habilidades esenciales. Estas habilidades los hacen más eficaces a la hora de trabajar dentro de un equipo sanitario y, en última instancia, ayudar a los pacientes a alcanzar sus objetivos de salud.
Las habilidades blandas esenciales (habilidades personales como la comunicación y el profesionalismo) suelen abordarse en los programas de capacitación para empleadores del sector de la salud. Si bien estas habilidades no son tan fáciles de enseñar como la capacitación técnica, son igualmente vitales para el éxito de cualquier organización de atención médica.
Conclusiones de la tercer entrega: Trabajo en equipo.
Todos los miembros del equipo de atención deben comprender y aplicar estas habilidades, comunicándose de manera eficaz para interactuar mejor con los pacientes y sus compañeros de trabajo.
La atención médica está avanzando increíblemente rápido, y el ritmo del cambio requiere que los médicos y administradores se adapten y piensen de manera creativa. No es fácil abordar el cambio organizacional y al mismo tiempo garantizar que los equipos tengan las herramientas para hacer su trabajo con éxito. Las habilidades blandas como la adaptabilidad, la creatividad, la toma de decisiones y el liderazgo son esenciales durante el cambio organizacional para garantizar la implementación y el apoyo efectivos de los procesos. Los médicos, administradores y líderes deben tomar decisiones inteligentes, creativas, estratégicas y basadas en evidencia en condiciones de relativa incertidumbre. Las habilidades blandas hacen que los miembros del equipo se involucren
Con tantos profesionales de diversos orígenes involucrados en la toma de decisiones en el ámbito de la atención médica, el trabajo en equipo es esencial. Los líderes de la atención médica deben abordar situaciones, conversaciones, procesos y decisiones de alta presión sin ser confrontativos.
Los desafíos comunes que enfrentan los equipos de atención médica incluyen la rendición de cuentas, los conflictos, la toma de decisiones y la evaluación del progreso. Una gestión de personas eficaz e impulsada por la comunicación promueve el trabajo en equipo en todos los niveles de las organizaciones de atención médica a través de habilidades blandas relacionadas con el pensamiento estratégico, la comunicación, la colaboración y la cultura organizacional.
Las Soft Skills Esenciales para Gerentes de Salud en Hospitales
Habilidades Blandas de los Gerentes de Hospitales. 2 entrega.
Nota del blog: Esta serie que estoy elaborando está dedicada a las denominadas soft skills, esas habilidades que deben tener los directores y los gerentes medios, con algunos matices diferentes de acuerdo a las áreas, a los hospitales, a los sanatorios, pero existen aspectos que conviene señalarlos como comunes, frecuentes, y que se deben contar. Esto se logra con una buena selección y con capacitación formal, incidental y también fuera de la institución. Con cierta periodicidad los jefes medios deben ver otras instituciones, distintos desarrollo, con cuidado porque vendedores interesados por entrar al mercado podrían incidir en sus peticiones hacia la dirección. La capacitación tiene que ser independiente. No patrocinada. Es difícil de encontrar. Los sesgos son frecuentes. Las considero con convicción que son ventajas que hacen la diferencia, y cuando se constituye una masa crítica entre los jefes de servicio esto se puede lograr: gestión por procesos, gestión Lean, atención centrada en la persona, gestión eficiente, de calidad y segura. Son fuerzas poderosas, que no se compran, hay que seleccionar adecuadamente y desarrollar un verdadero coach, que consista en explorar la situación actual, identificar que debe y quieren hacer las personas, fijar metas, específicas, medibles y alcanzables, y finalmente tener un plan de acción, acciones detalladas y con un calendario.
El liderazgo de servicio podría ser capaz de ofrecer un enfoque de liderazgo que pueda lidiar con los desafíos del lugar de trabajo moderno y, al mismo tiempo, satisfacer nuestras necesidades de pertenencia de cazadores-recolectores. Esta podría ser la razón por la que las organizaciones que implementan prácticas de liderazgo de servicio (por ejemplo, Starbucks, Southwest Airlines, Ritz-Carlton, ServiceMaster, TDIndustries, SAS, Zappos.com , Container Store, Intel, Marriott, Synovus Financial) siguen en aumento, impulsando la investigación sobre el liderazgo de servicio.
Los mayores impedimentos para el cambio y los mayores obstáculos para el éxito de una organización se encuentran dentro de la propia organización. El desafío para la alta gerencia es determinar cómo eliminar los impedimentos y los obstáculos. En otras palabras, para cambiar una organización, hay que empezar por los comportamientos, y especialmente por el modelo de la alta dirección de los comportamientos deseados. Los cambios necesarios requieren de un liderazgo fuerte, una gestión técnica profesional y alineamiento de los objetivos de los servicios con los del hospital.
El liderazgo de servicio, un modelo que se centra en atender las necesidades más elevadas de los demás en un esfuerzo por ayudarlos a alcanzar sus metas. El liderazgo de servicio se centra en el desarrollo del líder a través de la conciencia y el autoconocimiento. La autorreflexión y la conciencia permiten al líder comprender su propósito, creencias y características individuales.
Las cualidades y características del liderazgo de servicio: escuchar, empatía, conciencia, persuasión, conceptualización, previsión, administración, compromiso con el crecimiento de las personas y construcción de comunidad. Estas características, junto con un núcleo moral, impulsan a los líderes de servicio a ayudar a las personas a alcanzar sus metas y superar los desafíos.

Introducción
El liderazgo de servicio ha atraído la atención de los líderes del sector salud y otras partes interesadas que buscan mecanismos para lograr la excelencia en áreas de liderazgo, gestión, servicio y crecimiento profesional.1–3 La naturaleza inherentemente servicial de la atención médica crea un terreno fértil para la implementación del liderazgo servicial en los entornos de atención médica.4 El liderazgo de servicio es un liderazgo basado en la moral, impulsado principalmente por la idea de que servir es un componente natural (“llamado altruista”) o convicción interna del líder servidor, donde el enfoque está en el crecimiento personal y el bienestar de los demás. En esencia , el liderazgo de servicio ofrece un estilo de liderazgo que trasciende el interés propio para servir las necesidades de los demás.
Se supone que los líderes servidores deben poner el corazón en el trabajo de todos en las organizaciones de atención médica. La teoría del liderazgo de servicio abarca de manera única una motivación combinada de ser un líder con una fuerte convicción de servir.5 ,Las investigaciones revelan que el liderazgo de servicio tiene una alineación moral y profesional con los valores fundamentales que sustentan el entorno de trabajo en el ámbito de la atención médica.9–12 El liderazgo de servicio ofrece una experiencia de supervisión de apoyo para los empleados,13 muestra cuidado y compasión por los pacientes,14 y mejora el desempeño de seguridad de los hospitales,11 lo que hace que la teoría sea congruente con el panorama de la atención sanitaria.
El liderazgo de servicio se ha estudiado constantemente en múltiples contextos industriales y culturales, incluida la atención sanitaria.5 ,15 Sigue demostrando relaciones positivas con resultados valiosos, como la satisfacción del paciente,16 calidad del servicio,17 calidad de las relaciones líder-seguidor,18 y el desempeño organizacional.19 Con un creciente volumen de publicaciones científicas que demuestran las relaciones entre el liderazgo de servicio y los resultados en la atención de la salud, existe una necesidad imperiosa de integrar los detalles importantes de los estudios existentes en una revisión sistemática. Hasta donde sabemos, no existe ninguna revisión sistemática exhaustiva de estudios que desarrolle redes nomológicas de investigaciones previas sobre liderazgo de servicio en la atención de la salud.
Las revisiones existentes específicas sobre atención médica brindan información valiosa sobre la literatura sobre liderazgo.4 ,20 ,21 Sin embargo, en la literatura no se han realizado trabajos de investigación integrados que ofrezcan una imagen holística de la trayectoria de los estudios sobre liderazgo de servicio en sectores específicos de la atención sanitaria. Nuestra revisión se propone avanzar en la investigación mediante un análisis sistemático de los marcos teóricos, las herramientas de medición y las redes nomológicas (antecedentes, mecanismos, resultados y moderadores) asociados con la investigación sobre liderazgo de servicio en el ámbito de la atención sanitaria. Por lo tanto, nuestro objetivo es ofrecer una imagen integral del valor y el posicionamiento de la teoría del liderazgo de servicio en la atención sanitaria mediante la síntesis y evaluación de estudios conceptuales y empíricos específicos de cada sector que han explorado la teoría y la investigación sobre liderazgo de servicio.
Esta revisión estará guiada por las siguientes preguntas de investigación:
- ¿Cómo se conceptualiza el liderazgo de servicio en la literatura sanitaria?
- ¿Qué teorías subyacentes guían la investigación sobre liderazgo de servicio en el ámbito sanitario?
- ¿Qué metodologías se utilizan en el estudio del liderazgo de servicio en el ámbito sanitario?
- ¿Qué antecedentes, mecanismos de mediación, resultados y condiciones límite del liderazgo de servicio se investigan en la investigación en atención de salud?
Greenleaf fue pionero en sentar las bases para el surgimiento de teorías, marcos y modelos que mejoran nuestra comprensión del liderazgo de servicio. Conceptualizó el liderazgo de servicio como una forma de vida que “comienza con el sentimiento natural de que uno quiere servir, servir primero. Luego, la elección consciente lleva a uno a aspirar a liderar” (p. 7). Spears22 estableció diez características esenciales del liderazgo de servicio: escuchar, empatía, sanación, conciencia, persuasión, conceptualización, previsión, administración, compromiso con el crecimiento de las personas y construcción de la comunidad. Una proliferación de estudios continuó describiendo diferentes variaciones de estas características del liderazgo de servicio.5 ,8 ,9 ,23–25 5 Esta revisión exhaustiva proporciona una claridad conceptual del liderazgo de servicio en comparación con el liderazgo transformacional, el liderazgo auténtico y el liderazgo ético. Los autores definieron el liderazgo de servicio utilizando las características de motivación (“enfoque de liderazgo orientado a los demás”), modo (“interacciones uno a uno entre líderes y seguidores”) y mentalidad (“una preocupación general por el bienestar de los demás”). Sin embargo, no hay consenso sobre la definición de liderazgo de servicio en la literatura y, como resultado, se desarrollaron diversas herramientas de medición.15 ,26 lo que plantea cuestiones sobre la validez de los hallazgos empíricos.
El nombramiento de líderes de atención médica basándose únicamente en el título médico o las habilidades técnicas ya no es factible en las organizaciones de atención médica modernas.La presencia de diversas áreas de enfermedad, objetivos multidireccionales e interacciones complejas no lineales de personal multidisciplinario hacen que la tarea de liderazgo sea un desafío en la atención médica.28 ,29 Mahón13 afirma que el liderazgo de servicio puede actuar como un “lenguaje de liderazgo universal”, justificable en entornos de atención médica multiculturales cada vez más sobrecargados. Se cree que una mentalidad de liderazgo de servicio es una combinación cultural natural con la atención médica. 21 ,30–32 relevantes para abordar los desafíos en el complejo sector de la salud.
Si bien la literatura sobre liderazgo ha observado una proliferación de estudios sobre liderazgo de servicio específicos para el sector de la salud, se ha hecho muy poco en términos de establecer integraciones significativas. Uno de los trabajos destacados en este sentido es el de Aij y Rapsaniotis.Citación20 revisión que integró la evidencia de estudios existentes sobre el liderazgo lean y el liderazgo de servicio en la atención médica. La revisión sugirió que ambos son modelos prometedores que pueden contribuir a la prestación de atención al paciente de alto valor. Esto sienta las bases para la revisión sistemática actual, que busca ofrecer nuevos conocimientos sobre la teoría del liderazgo de servicio a través de una síntesis integral de estudios específicos del sector en la atención médica.
Mediadores del liderazgo de servicio en la investigación sanitaria
El liderazgo de servicio mejora el desempeño laboral a través de la mediación de la felicidad de los empleados53 y aumenta la intención de los empleados de permanecer en la organización a través del empoderamiento.60 Los líderes servidores también promueven un comportamiento proactivo al mejorar la calidad de las relaciones de intercambio.48 y eleva el desempeño organizacional al infundir confianza.76 Además, los estudios revelan que un líder servidor con inclinaciones ambientales podría mejorar significativamente el comportamiento proambiental específico en materia de energía de los empleados del hospital a través de los mecanismos de mediación de la autoeficacia verde y el apoyo organizacional percibido como verde.49
Además, el liderazgo de servicio reduce las desviaciones en el lugar de trabajo a través de la justicia organizacional.86 y disminuye el agotamiento a través de la seguridad psicológica.51 Además, la identificación organizacional medió el impacto negativo del liderazgo de servicio en las intenciones de rotación de los empleados en el sector de la salud.81
El cumplimiento del contrato psicológico y la propiedad psicológica mediaron secuencialmente la relación entre el liderazgo de servicio y la integración laboral.Citación52 Además, los factores estresantes, el agotamiento y la satisfacción laboral mediaron la relación entre el liderazgo de servicio y el desempeño y la rotación.Citación87 El liderazgo de servicio influye positivamente en los resultados en el lugar de trabajo (desempeño de tareas, comportamiento laboral innovador y compromiso laboral), en parte a través del bienestar eudaimónico, y esta mediación varía según los diferentes niveles del clima de civilidad en el lugar de trabajo.Citación83
Finalmente, el liderazgo de servicio medió la relación entre la gestión ecológica de los recursos humanos y la conciencia ambiental al promover el aprendizaje de los empleados y su compromiso con conductas proambientales. El liderazgo de servicio también mediaba parcialmente la relación entre la RSE-E y el comportamiento innovador de los empleados en tiempos de crisis.77
liderazgo de servicio en la investigación sanitaria
Los moderadores relacionados con los empleados del empoderamiento psicológico y la motivación prosocial influyen en la eficacia del liderazgo de servicio. Se encontró que la relación entre el liderazgo de servicio y la voz ascendente de las enfermeras era más fuerte para aquellas con menor motivación prosocial que para aquellas con mayor motivación prosocial.Se ha descubierto que la relación entre la confianza de los seguidores en el líder y el desempeño de la organización hospitalaria es más fuerte cuando el empoderamiento psicológico de los seguidores es alto .76 Además, el liderazgo de servicio tenía una relación más fuerte con el bienestar eudaimónico cuando el clima de civilidad en el lugar de trabajo era alto.83
Además, Kul y Sonmez71 demostraron que las conductas de liderazgo de servicio de los gerentes de enfermería fortalecen la relación positiva entre las conductas innovadoras de los enfermeros y su desempeño laboral. Sin embargo, el liderazgo de servicio no tuvo un papel moderador entre los programas de equilibrio entre el trabajo y la vida personal y el bienestar psicológico.50
El liderazgo de servicio puede fomentar con éxito el compromiso de los empleados,70 ,88 ,89 inserción laboral,52 motivación del sirviente,40 bienestar psicológico,50 comportamiento de voz69 personas-organización en forma,70 comportamiento proactivo,48 y satisfacción en el trabajo.70 ,86 ,87 ,90 Además, el liderazgo de servicio se asocia positivamente con el comportamiento innovador,71 desempeño laboral,53 ,71 ,86 y comportamiento proambiental.49 Los hallazgos también mostraron que el liderazgo de servicio reduce la desviación en el lugar de trabajo,86 agotamiento,51 ,86 y las intenciones de rotación.81 ,86
Hanse y otros18 demostraron la presencia de correlaciones significativas entre las dimensiones del liderazgo de servicio y el intercambio líder-miembro entre profesionales de la salud. De manera similar, Irving y Berndt70 mostraron el efecto de la intencionalidad del líder dentro del liderazgo de servicio (perspectivas de los seguidores sobre el liderazgo de servicio, enfoque del líder en el seguidor, orientación del líder hacia las metas y intencionalidad del líder) sobre los resultados relacionados con el trabajo (satisfacción laboral, compromiso organizacional, ajuste persona-organización y percepción de la efectividad del liderazgo).
Además, el liderazgo de servicio está vinculado con el desempeño organizacional,76 ,91 desempeño del mercado92 y el sistema de gestión de recursos humanos93 de los centros de salud. Además, se ha descubierto que el liderazgo de servicio aumenta la espiritualidad.39 ,94 y apoyo organizativo de enfermeras,39 que a su vez mejoran la eficacia de la atención sanitaria.
El liderazgo de servicio también se estudia junto con el liderazgo transformacional,58 liderazgo ético,54 liderazgo verde y liderazgo digital,55 y prácticas de responsabilidad social corporativa.60 Los hallazgos revelaron la contribución única del liderazgo de servicio al desempeño organizacional y la satisfacción laboral,58 desempeño del mercado,55 y la intención de los empleados de permanecer en la organización.60 Sin embargo, el estilo de liderazgo de servicio no tuvo ningún papel en la relación entre la inteligencia cultural y el comportamiento de la voz.54
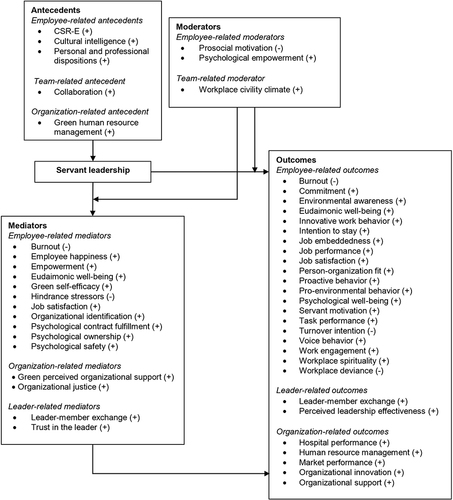
Discusión
La presente revisión sistemática exhaustiva contribuye a la literatura sobre liderazgo mediante la síntesis de estudios conceptuales y empíricos sobre liderazgo de servicio específicos del sector en el ámbito de la atención de la salud. Nuestro análisis a continuación aborda el diseño de la investigación, las conceptualizaciones sobre liderazgo de servicio, las herramientas de medición, los mecanismos teóricos y las redes nomológicas en estudios previos sobre liderazgo de servicio específicos del sector de la atención de la salud.
Los estudios conceptuales y empíricos en el ámbito de la atención sanitaria nos han permitido obtener una comprensión más profunda del concepto de liderazgo de servicio. Nuestra revisión muestra la aparición de investigaciones empíricas en los diversos contextos sanitarios de dieciséis países diferentes, lo que contribuye a la validez transcultural de la teoría del liderazgo de servicio.8 Sin embargo, muchos de los estudios empíricos en el ámbito de la atención sanitaria utilizan un diseño transversal, con mayor probabilidad de sesgo de método común y de falta de claridad en la direccionalidad causal.95 ,96
La revisión revela la variedad de conceptualizaciones del liderazgo de servicio en el ámbito de la atención médica, que acompañan la utilización de diferentes medidas. Esto limita las comparaciones entre estudios. Los temas emergentes del liderazgo de servicio (es decir, promover la equidad, fomentar las relaciones, dar reconocimiento, desarrollar a los empleados y participar en la toma de decisiones) comparten similitudes con las conceptualizaciones del liderazgo inclusivo.Los temas superpuestos identificados aquí ofrecen oportunidades para futuras investigaciones y aplicaciones.
La teoría del intercambio social domina la contribución a la explicación de la relación entre el liderazgo de servicio y otras variables en la literatura sobre atención médica. Además, solo unos pocos estudios integraron múltiples perspectivas teóricas. La teoría de la autodeterminación nos ayuda a explicar el efecto del liderazgo de servicio sobre variables específicas de interés basadas en factores de motivación intrínsecos relacionados con los empleados. La autodeterminación postula que la satisfacción de las necesidades psicológicas innatas de competencia, autonomía y relación determinan las condiciones para que los individuos realicen plenamente su potencial humano.78 Además, las teorías orientadas a los recursos, como la teoría de la conservación de los recursos, ayudan a explicar la influencia del liderazgo de servicio basado en las características personales o las condiciones valoradas por el empleado individual. La teoría de la conservación de los recursos supone que los empleados intentan obtener recursos valiosos (por ejemplo, colegas que los apoyan) para defenderse de la pérdida de recursos.5 ,82
La red nomológica de esta revisión sistemática identificó que las variables relacionadas con los empleados individuales (por ejemplo, el comportamiento de la voz) son dominantes en la investigación de la atención médica, seguidas por las variables relacionadas con la organización (por ejemplo, el desempeño del hospital). No obstante, los académicos dieron menos énfasis a la investigación de la dinámica de equipo, que brindaría nuevas vías para el contexto cada vez más interpersonal de la atención médica. Los antecedentes y las condiciones límite del liderazgo de servicio también siguen siendo menos explorados, lo que deja una brecha de conocimiento en relación con el establecimiento de terrenos fértiles para el desarrollo de comportamientos de liderazgo de servicio en la atención médica.
El liderazgo de servicio se considera predominantemente como una variable exógena que predice múltiples resultados de interés en el contexto de la atención sanitaria. Los resultados de la presente revisión son coherentes con la teoría y los resultados de la investigación sobre el liderazgo de servicio en varios sectores.5 ,98 ,99
Además, los resultados positivos en materia de seguidores y organizaciones demostrados en los estudios sectoriales específicos analizados dan testimonio de que el liderazgo de servicio es particularmente prometedor en el ámbito de la atención de salud, donde la adhesión a los códigos de conducta moral es esencial para brindar servicios de atención de salud profesionales.20 ,21
El liderazgo de servicio facilita el proceso de dar forma al buen funcionamiento psicológico en los ámbitos individual, organizacional y social en el territorio de la atención médica.47 ,83
Conclusión
La revisión ha demostrado que la investigación sobre el liderazgo de servicio ha logrado un progreso considerable en la literatura de atención médica. De manera consistente en otros dominios no relacionados con la atención médica, los académicos abordan predominantemente el liderazgo de servicio como una variable exógena que influye directa e indirectamente en varios resultados individuales y organizacionales en la atención médica. La teoría del intercambio social es el mecanismo subyacente dominante; con pocos estudios sobre el liderazgo de servicio en la atención médica que integraran múltiples lentes teóricos. Los hallazgos llaman la atención sobre la importancia de adoptar el liderazgo de servicio en la atención médica, ya que promete un trabajo por encima de la norma en el desarrollo de una fuerza laboral comprometida que contribuya al logro de la excelencia en el desempeño. Por lo tanto, la implementación efectiva del liderazgo de servicio en la atención médica puede ser un requisito esencial para obtener resultados positivos para los empleados y los pacientes.
Importancia de las Habilidades Blandas en Gerencia Hospitalaria
Habilidades Blandas de los Gerentes de Hospitales. Primer entrega.
Dr. Carlos Alberto Díaz . Profesor Titular Universidad ISALUD. Buenos Aires. Argentina.
En el contexto de la salud, las habilidades técnicas y los conocimientos médicos son esenciales; sin embargo, resulta igualmente crucial el desarrollo de habilidades interpersonales. Estas últimas permiten a los profesionales en el ámbito de la salud comunicarse de manera efectiva, empatizar con los pacientes, colaborar eficientemente, resolver problemas y ejercer un liderazgo confiado. Se podrían identificar unas veinte habilidades blandas, pero también en esto se debe priorizar en unas cinco o siete, y empezar por el liderazgo, la comunicación, el trabajo en equipo, ser coach y colaborar, resolución de conflictos, tomar decisiones y tener un pensamiento estratégico y sistémico. Surge de las experiencias exitosas de gestión que una parte fundamental de las ventajas competitivas son las habilidades blandas de los lideres en los equipos de trabajo, de los servicios hospitalarios, como sus propósitos están identificados y alineados con los objetivos institucionales, o generales de la institución. Se deben desarrollar en un programa adecuado de formación, especialmente los flujos cliente proveedor interno, la pertenencia y el compromiso. Su importancia no es valorada suficientemente, por lo tanto no forma parte de los objetivos estratégicos de muchas instituciones, los profesionales tampoco se muestran interesados, pero algunos de estos aspectos debieran formar parte del perfil de puesto y ser obligatorios.
Las tres prioridades centrales para los líderes de hospitales:
(1) mejorar la experiencia del personal (incluida la satisfacción y retención laboral);
(2) cerrar la brecha entre la promesa de análisis predictivos y el uso actual (como una oportunidad para mejorar la calidad de la atención, reducir costos y acelerar la prestación de atención médica);
(3) abordar las amenazas a la seguridad de los datos de atención médica

El perfeccionamiento de estas habilidades no solo contribuye a una atención integral, sino que también aborda las necesidades tanto físicas como emocionales de los pacientes, lo que, a su vez, se traduce en mejores resultados de salud y en una experiencia más positiva durante la atención médica. Introducción Los hospitales son componentes fundamentales del sistema de atención de salud en cualquier nación. Sin embargo, modificar y mejorar este sistema es imposible sin prestar atención a estos centros y optimizar su desempeño. Estas instituciones, en su rol como proveedores de servicios de salud en el tercer nivel, juegan un papel crucial en la mejora del estado de salud de la población y en la prestación de servicios adecuados. En la actualidad, los gerentes de hospitales desempeñan un papel vital en la supervivencia, eficiencia y productividad de estas instituciones, siendo responsables éticamente y legalmente de su operación. Estos profesionales son clave en la promoción de los objetivos del sistema de salud, supervisando y dirigiendo los recursos humanos, y asegurando la calidad de la atención y la seguridad dentro de los hospitales.
Habilidades Gerenciales en el Ámbito de la Salud
La calificación de los gerentes en habilidades de gestión es un determinante crucial en el éxito continuo de cualquier organización de salud. Estas competencias pueden contribuir significativamente a la efectividad organizacional y al rendimiento del personal, alineándose con los objetivos y metas institucionales. La falta de un conocimiento adecuado por parte de los gerentes sobre estas habilidades puede ser un factor limitante, obstaculizando el éxito general de la organización. Las calificaciones gerenciales abarcan el conocimiento y las habilidades necesarias para llevar a cabo las responsabilidades de un gerente. En este sentido, se pueden definir como el comportamiento de un gerente al desempeñar sus funciones y alcanzar un rendimiento laboral positivo, evidenciado en su motivación, características personales, habilidades, autoimagen, rol social, conocimiento y responsabilidad. Varios estudios, como los realizados por Lin, Battilana, Dignam y Müller, han evidenciado la influencia positiva de las habilidades y cualificaciones gerenciales en el liderazgo efectivo, el rendimiento personal y organizacional, el espíritu organizacional y la efectividad de los gerentes. Investigaciones adicionales, como las de Sarabi Asiabar y Saleh Ardestani, clasifican los factores que inciden en el liderazgo hospitalario en habilidades de gestión interpersonales, autogestión, gestión nuclear y habilidades en la prestación de servicios de salud.
Desafíos y Consideraciones
A fines de abordar los desafíos actuales, es fundamental reconocer que un alto porcentaje de gerentes de hospitales, aproximadamente el 90% en contextos como Irán, carece de experiencia en el ámbito de la gestión sanitaria, lo que reduce notablemente la productividad hospitalaria. Las organizaciones de atención médica, particularmente los hospitales, enfrentan desafíos constantes derivados de variables internas y externas, como cambios en la tecnología, el mercado de atención médica, las condiciones económicas y la modificación de los sistemas de salud. Estos cambios generan la necesidad de adaptar y reevaluar las habilidades y competencias necesarias para los gerentes.
En resumen, es imperativo fomentar un enfoque integral en la capacitación de gerentes de hospitales que contemple tanto habilidades técnicas como blandas, garantizando así una atención de salud más eficiente y de calidad que responda a las necesidades de la comunidad.
LOS GERENTES DE LOS MODERNOS HOSPITALES SE DEBEN CAPACITAR EN HABILIDADES BLANDAS COMO:
Liderazgo, trabajo en equipo, comunicación, capacidad de negociación, resolución de conflictos, utilización eficaz del tiempo, programación de reuniones efectivas, capacidad para motivar, generar confianza, toma de decisiones, estar organizado, escucha activa, colaborar con otros integrantes, centrar correctamente los objetivos, agilidad mental para un entorno VUCA, interesarse por los demás liderar el cambio, inteligencia intuitiva, retroalimentar lo realizado-premiar el esfuerzo, pensamiento crítico y empatía.

Estas habilidades las he seleccionado en función de la bibliografía y la experiencia. Su importancia es diferente en cada circunstancia y cada hospital, existen algunas que potencian a otras, y por ejemplo, la toma de decisiones requiere un sistema de información seguro y confiable como prerequisito. Colaborar, coach-ear es fundamental para fortalecer al equipo que te rodea, y si ellos crecen una lo hará también. Tomar decisiones, no procrastinar, pero no apresurarse, y tener pensamiento estratégico, (yo agregaría también sistémico). La comunicación ayuda a la motivación y al coach, explicar correctamente lo que se quiere y las personas del equipo tengan confianza, también centrar correctamente los objetivos, para ir generando ilusión de acercase y encontrar el propósito. Saber escuchar, no apresurarse, dejar expresarse, de codificar y repreguntar. Organizar reuniones donde el ego se deje afuera y poder acercar posiciones. Buscar innovación y soluciones distintas. Si siempre hacemos lo mismo, los resultados no se modificarán. Motivar a las personas dándole responsabilidad y encontrando sus habilidades. Los gerentes que son mentalmente ágiles pueden captar conceptos complejos rápidamente, analizar y resolver problemas sobre la marcha y tomar decisiones acertadas en el momento oportuno. No forzar innecesariamente a los equipos que responden. porque se sobrecargará y agotarán mental y físicamente. Existirán habilidades que deben ejercitar los gerentes medios específicas para hacer crecer al establecimiento homogéneamente, saber transmitir los objetivos estratégicos como objetivos específicos del centro de responsabilidad, desarrollando esas ventajas competitivas que no se compran, que son las habilidades blandas.
Conclusión
Para alcanzar la satisfacción de los pacientes y mejorar el bienestar de la comunidad, así como garantizar la eficiencia y productividad de los recursos, las autoridades deben evaluar cuidadosamente a los gerentes de hospitales en base a las competencias necesarias para una gestión efectiva y humanizada. Esto resulta clave en la toma de decisiones y en la formulación de políticas relacionadas con la atención de la salud
El desarrollo de estas capacidades es necesario para una gestión eficaz de los recursos humanos (incluida la motivación del personal, la protección del bienestar y la salud mental de los empleados, la formación de equipos y la gestión de equipos interprofesionales y de personas con diversidad de edades).
Las habilidades blandas deben ser consideradas como las verdaderas ventajas competitivas para una organización moderna, gestionada por procesos, matricial, ágil, segura y eficiente.
Impacto del Proyecto 2025 Republicano en la Comunidad LGBTQ+ y su relación con el discurso anti woke del presidente.
Siguiendo una corriente vinculada a los Republicanos en EE.UU. (antes que fuera consagrado Donald Trump como candidato a presidente) el presidente Javier Milei, toma esa corriente del progresismo de los demócratas para continuar el alineamiento sin restricciones, ni miramientos con el presidente actual del país del norte, y utiliza en el discurso que dio en Davos, unos episodios sin ninguna rigurosidad, ni constituyen arquetipos. En Argentina esta política fue impulsada por el Kirchnerismo y la izquierda que colocaron en relieve los derechos de las minorías, satisfaciendo los reclamos de esos sectores, que fue refrendada en el poder legislativo, en lo que se llama discriminación dispositiva para proteger los derechos de las minorías. Estas propuestas para transformar las sociedades no lo estaría logrando. Es imperioso informarse y tener argumentos para actuar con responsabilidad, para ello entrego en este blog un artículo que seleccione y espero que sea tomado para la lectura crítica y la información para el grupo importante de lectores que tengo, no es una toma de posición porque no corresponde a este espacio, pero si esto afectará a la salud de estas minorías, especialmente de los grupos trans y queer para tratamientos ya iniciados, no porque no haya que revisar algunos de los excesos cometidos en las gestiones políticas anteriores, como imposición y en extender la cobertura a estos grupos para consagrar derechos sociales por la igualdad avanzada, mientras nos olvidábamos de otros principios de la economía, el gasto público y la inflación afectando a la sociedad generando más y más pobres y excluidos.
Woke ha evolucionado para significar conciencia de la discriminación y de ideas sociales y políticas progresistas que promueven la diversidad, la inclusión y los valores liberales.
El término anti-woke hace referencia a un movimiento que se opone a las ideas sociales y políticas progresistas, especialmente aquellas que promueven la diversidad, la inclusión y los valores liberales. Los defensores del movimiento anti-woke afirman que conocer o ver a los grupos marginados tendrá un impacto negativo en la sociedad.
En este blog hay unos artículos publicados hace cinco años sobre las personas de estos grupos desde la inclusión de la afirmación de genero en el PMO, realizamos una experiencia al respecto y otro posteo sobre los aspectos sociales, del lenguaje inclusivo, de la forma de transmitirlo, instalando muchos conceptos forzadamente en la salud, generando una prioridad en la sociedad, pensando que ante la falta de recursos produce costo de oportunidad con otras prestaciones, solo en modo comparativo un cambio de sexo es un costo similar a un trasplante renal.
Se esta impulsando un proyecto de ley para eliminar el concepto de femicidio como agravante penal, los cupos trans y los documentos binarios, como parte de esta agenda. El proyecto se denominará «igualdad ante la ley», por lo que llaman «discriminación positiva»
De la criminalización al borrado: el Proyecto 2025 y la legislación antitrans en Estados Unidos

Abstract
Los medios de comunicación dominantes han caracterizado en gran medida las dos últimas décadas como emancipadoras de las comunidades LGBTQ; de hecho, las personas queer y trans han logrado muchas victorias legales. Pero a pesar de lo que ha parecido ser una marcha lenta hacia la aceptación y la inclusión, la era de la igualdad posterior al matrimonio ha dado paso a una forma virulenta de reacción en la que las comunidades trans son demonizadas y criminalizadas a través de una abundancia de leyes y políticas antitrust, muchas de las cuales apuntan a la juventud trans y al acceso a la atención médica, las escuelas y los deportes. Después de esbozar el panorama más amplio de la criminalización trans, este artículo pasa a un análisis de la iniciativa conservadora denominada Proyecto 2025 y su texto insignia Mandate for Leadership: The Conservative Promise (2023). Este plan integral describe una serie de políticas de gran alcance dirigidas a las poblaciones marginadas, con las personas trans en el centro mismo. Basándose en la criminología queer y la teoría trans, este artículo sostiene que el Proyecto 2025 y la legislación antitrans emergente pasan del castigo y la criminalización de las personas de género diverso al borrado y la deshumanización de la vida trans en todas sus formas. En el contexto de tendencias más amplias de política anti-trans y agendas conservadoras que buscan erosionar el progreso logrado en el avance de los derechos y la igualdad de las personas trans, este artículo también es un llamado a construir sobre la criminología queer para establecer un cuerpo de trabajo más sólido en criminología trans.
“Las personas trans son criminalizadas y discriminadas simplemente por ser trans”
– Iniciativa de política penitenciaria, citada en Herring y Widra (2022)
“En el pasado, la palabra ‘género’ era una alternativa educada a la palabra ‘sexo’ o al término ‘sexo biológico’. La izquierda ha requisado el término ‘género’, que solía significar ‘masculino’ o ‘femenino’, para incluir a un espectro de otros que buscan alterar las normas sexuales biológicas y sociales. La promoción del radicalismo de género es un anatema para las normas tradicionales de muchas sociedades […] y produce consternación y confusión innecesarias entre los hombres, e incluso prejuicios abiertos contra ellos”.
– Max Primorac ( 2023 ), Mandato de liderazgo: la promesa conservadora (p. 259)
Introducción
Los jóvenes trans parecen estar recibiendo toda la atención. Es difícil evitar los debates en las noticias sobre los baños públicos, las políticas escolares, los deportes segregados por sexo y los bloqueadores de la pubertad. Los jóvenes trans también se convirtieron en un tema de conversación importante para los conservadores en las elecciones presidenciales de Estados Unidos de 2024, cuando el presidente Donald Trump soltó afirmaciones infundadas de que los maestros están realizando en secreto cirugías de afirmación de género a los niños en la escuela. Y como dejan claro los epígrafes anteriores, la diversidad de género ha atraído la atención legislativa de los responsables de políticas conservadoras en todo Estados Unidos, y los jóvenes trans se han convertido en chivos expiatorios de la promoción de una agenda nacionalista cristiana radical centrada en los «valores familiares tradicionales». Y aunque la expansión de las identidades trans (y su consiguiente regulación y vigilancia a través de la legislación antitrans) puede parecer un fenómeno nuevo, si se analiza más de cerca, parece que, como sostiene el historiador trans Jules Gill-Peterson (2018) , la novedad de tales políticas transfóbicas “tiene mucho menos que ver con que los niños trans no tengan precedentes que con una forma muy contemporánea de reacción antitrans que ha tomado la convergencia de la visibilidad y la vulnerabilidad trans como una oportunidad” (p. 196). Esta tensión entre visibilidad y vulnerabilidad ha creado la tormenta perfecta no solo para criminalizar la atención que afirma el género y rescindir derechos, sino también para vigilar y disciplinar a las comunidades trans. Siguiendo a Foucault, el académico de estudios trans Toby Beauchamp ilustra cómo, incluso si las iniciativas de visibilidad a menudo se consideran pasos hacia un cambio social positivo, no son inocentes ni benignas. La visibilidad es una trampa, en particular porque “la visibilidad de uno ante los mecanismos de vigilancia puede permitir que esos mecanismos funcionen de manera más efectiva” ( Beauchamp, 2019 : 16). La visibilidad es, por lo tanto, un arma de doble filo: la visibilidad y la representación trans se correlacionan con una mayor violencia hacia las personas trans ( Currah, 2022 ; Fischer, 2019 ; Gossett et al., 2017 ; Stanley, 2017 , 2021 ). Esto puede incluir violencia física, pero también adopta la forma de violencia simbólica ( Bourdieu, 1990 ) y violencia administrativa ( Spade, 2015 ), que puede manifestarse en medidas legislativas y de políticas que privilegian la cisnormatividad y restringen la subsistencia trans.
Aunque las comunidades LGBTQ habían experimentado cambios sin precedentes a partir de los años 2000 y 2010 (por ejemplo, leyes de igualdad matrimonial, leyes contra la discriminación, leyes de reconocimiento de género), ahora hemos entrado en un punto de inflexión crítico. Los niños trans y los que cuestionan su género han sido colocados en el centro de este punto álgido cultural marcado por la transfobia y la misoginia trans. A pesar del número relativamente pequeño de personas trans (la población de niños trans en los EE. UU. asciende a entre 150.000 y 300.000, mientras que los adultos trans se estiman en 1,3 millones), la legislación antitrans ha aumentado a un ritmo sin precedentes, lo que ha dado como resultado que este grupo minoritario reciba una atención desproporcionada y la ira de los legisladores conservadores. Y aunque las personas trans han sido víctimas de la regulación y el control durante mucho tiempo, esta última iteración de las guerras culturales es mucho más nefasta, distópica y de amplio alcance que nunca.
Este artículo se centra en el Proyecto 2025, una iniciativa conservadora con sede en Estados Unidos que ofrecería al próximo presidente republicano (el presidente electo Donald Trump) una serie de propuestas políticas que podrían hacerse oficiales mediante una orden ejecutiva. Aunque no se menciona a Trump (todavía no había recibido la nominación republicana cuando se lanzó), muchos de sus aliados están vinculados al Proyecto 2025. Y aunque Trump se distanció de esta controvertida iniciativa durante su campaña, ya ha nominado a más de media docena de arquitectos del Proyecto 2025 para que presten servicios en su administración. Su guía de políticas de más de 900 páginas es un modelo para hacer realidad las agendas conservadoras radicales; es un manual para implementar una serie de políticas de amplio alcance dirigidas a las poblaciones marginadas, con las personas trans, como mostraré a continuación, en el centro mismo. Al hacer referencia al tenor general y los objetivos del Proyecto 2025, la investigadora de asuntos internacionales Emma Shortis (2024 : np) reconoce que esto no es algo habitual: “Desarrollar planes de transición para un candidato presidencial es una práctica normal en los EE. UU. Lo que no es normal en el Proyecto 2025, con su agenda nacional e internacional entrelazada, son los planes en sí mismos [que] apuntan nada menos que al desmantelamiento y reestructuración totales tanto de la vida estadounidense como del mundo tal como lo conocemos”. A través de un análisis tanto del Proyecto 2025 como de la abundancia de legislación antitrans en los EE. UU. (una tendencia que se ha vuelto de alcance global), este artículo sostiene que esta agenda conservadora está marcada por una intensificación de tácticas que pasan de castigar y criminalizar la diversidad de género y la no normatividad a borrar y extinguir activamente la vida trans en todas sus formas nacientes.
La visión conservadora contemporánea propuesta por el Proyecto 2025, basada en el alarmismo, las tácticas engañosas y la desconfianza en la ciencia, parte de la premisa de que “la familia estadounidense está en crisis” ( Roberts, 2023 : 4). Este tropo no es especialmente nuevo ni único: hemos visto muchas versiones de esto antes. 1 Y si bien la Heritage Foundation ha producido otras biblias conservadoras en el período previo a las elecciones presidenciales, esta es diferente, específicamente por su enfoque láser en las cuestiones de género. Su plan abierto y encubierto apunta a atacar lo que ellos llaman “ideología de género consciente” y rescindir el apoyo estructural a las personas trans, las poblaciones racializadas y otros grupos minoritarios. Esto se haría, en parte, a través de la criminalización draconiana de los actos cotidianos y la eliminación de iniciativas, lenguaje y políticas relacionadas con el género. En este contexto, los jóvenes trans se han convertido en un peón de políticas impulsadas política e ideológicamente en torno a las cuales se han cristalizado las ansiedades sociales y culturales sobre el futuro y la familia ( Butler, 2024 ).
Este artículo se centra en la legislación y las políticas actuales precisamente porque son los vehículos a través de los cuales se naturaliza el poder ( Uhlman, 2024 : 1083). Después de esbozar el panorama de la criminalización y el borrado de las personas trans a través de leyes y proyectos de ley estatales recientes en Estados Unidos, paso a una lectura y análisis minuciosos del texto insignia del Proyecto 2025, Mandato para el liderazgo: la promesa conservadora (2023). Este documento integral retrata una visión conservadora de largo alcance y socialmente distópica que incluye los siguientes pasos para la intervención gubernamental en las vidas trans:
(1) definir el «género» como el sexo asignado al nacer y revertir las interpretaciones de «sexo» para que ya no incluyan la identidad de género ni la orientación sexual,
(2) poner fin a la recopilación de datos sobre identidad de género de los Centros para el Control y la Prevención de Enfermedades (CDC),
(3) prohibir la atención de afirmación de género,
(4) detener la investigación de los Institutos Nacionales de Salud (NIH) sobre la identidad de género (lo que llaman «ciencia de género basura») pero financiar la investigación sobre los «efectos negativos de las intervenciones cruzadas, incluida la ‘afirmación’, los bloqueadores de la pubertad, las hormonas cruzadas y las cirugías» ( Severino, 2023 : 462),
(5) prohibir el uso de términos relacionados con la identidad de género y la sexualidad,
(6) restringir el alcance de la legislación existente sobre «discriminación sexual» para permitir la discriminación contra las personas trans,
(7) rescindir el uso de marcadores de género no binarios y
(8) prohibir que los niños utilicen pronombres o nombres de su elección.
En conjunto, estas propuestas políticas y cambios legislativos cultivan activamente lo que el especialista en estudios trans Eric A. Stanley (2021) llama atmósferas de violencia. Stanley yuxtapone los llamados avances en los derechos LGBTQ con el aumento de la violencia anti-trans/queer (extraño o poco usual) «queer» es «un adjetivo utilizado por algunas personas cuya orientación sexual no es exclusivamente heterosexual» ( Stanley, 2021 : 5). En lugar de ver la violencia únicamente como incidentes aislados o actos físicos, existe como una red compleja de fuerzas sociales, culturales y políticas que crean un entorno en el que la violencia es omnipresente y normalizada. Este marco deja al descubierto la naturaleza omnipresente e interconectada de la violencia, incluido el modo en que las identidades, expresiones y encarnaciones trans son víctimas de los intentos legislativos de borrar la transidad de la vida pública. Un análisis de las desigualdades estructurales, la discriminación sistémica y la violencia simbólica que afectan a las comunidades marginadas, incluidas las personas trans y queer y las poblaciones negras, morenas e indígenas, también revela cómo las normas sociales y las instituciones democráticas perpetúan aún más el daño y la opresión.
El teórico queer Lee Edelman (2004) nos recuerda que la obsesión de la sociedad con el futuro, en particular a través de un énfasis en la reproducción heterosexual y la “protección” de los niños, ha servido históricamente como un mecanismo de control social que excluye y margina las sexualidades y géneros no normativos. Si bien la investigación académica ha examinado cada vez más las formas en que las personas trans se ven afectadas por el sistema legal penal, en particular en términos de encarcelamiento y vigilancia policial, se ha prestado menos atención académica interdisciplinaria al retroceso de los derechos LGBTQ y la criminalización intensificada de las personas trans, en particular los jóvenes. Y si bien la teoría queer y los estudios trans han proporcionado marcos útiles para analizar cómo la figura del niño se ha utilizado durante mucho tiempo en batallas ideológicas y discursos políticos en torno al futuro reproductivo y las normas sociales, la investigación apenas está comenzando a examinar las formas en que los niños trans están siendo chivos expiatorios ( Gill-Peterson, 2018 ; Meadow, 2018 ; Mitchell, 2023 ). Basándose en la criminología queer y la teoría trans, este artículo sostiene que, a través de la formulación de políticas y la legislación preventivas, el Proyecto 2025 —junto con el momento más amplio de mayor sentimiento antitrans— no solo plantea amenazas a la salud, el bienestar y los derechos de las personas trans, sino que también socava activamente su dignidad y autonomía. El Proyecto 2025 se lograría en gran medida mediante una combinación de tácticas novedosas y herramientas probadas que son parte integral de los regímenes autoritarios, que tienden a utilizar esa retórica y acciones antitrans “para preservar o afianzar las jerarquías sociales existentes mediante la producción de una amenaza imaginaria de aquellos con el poder menos demostrado, exigiendo violencia para acabar con ellos” ( Gill-Peterson, 2024 : 8). Aunque su documento de políticas es de libre acceso en línea, los medios de comunicación (aparte del periodismo crítico seleccionado en el que me baso) ignoraron en gran medida el Proyecto 2025 hasta bien entrada la temporada de campaña de 2024. El hecho de que las personas trans (que representan aproximadamente el 1% de la población estadounidense) hayan sido puestas en el centro de un plan para lograr un gobierno autoritario debería asustarnos a todos, independientemente de nuestro género o alineamiento político. En estas páginas se esconde, a simple vista, un plan para erradicar por completo la vida trans.
Criminología queer y trans: el “nexo jurídico penal transgénero”
Como han descubierto tanto los historiadores de los estudios trans como los criminólogos queer ( Asquith et al., 2017 ; Awkward-Rich, 2022 ; Jenness y Rowland, 2024 ; Sears, 2014 ; Stryker, 2008 ; Uhlman, 2024 ; Walker et al., 2022 ), la no conformidad con el género y las expresiones transgresoras de género han sido criminalizadas históricamente en los EE. UU. A fines del siglo XIX y principios del XX, las leyes sobre el travestismo eran, como ha argumentado Clare Sears (2014) , parte de una estrategia de gubernamentalidad espacial que servía para imponer normas de género y disciplinar a las comunidades marginadas. Las leyes que prohibían el travestismo también aplicaban una lógica de “rehabilitación”, que buscaba producir una identidad social “fija, legible y categorizable” eliminando del público las representaciones no conformes con el género ( Awkward-Rich, 2022 : 38). Este tipo de regulaciones basadas en el género se entrecruzaban con ansiedades sociales más amplias sobre el género, la sexualidad, la raza y la clase, reforzando de manera efectiva las estructuras jerárquicas de poder y las nociones dominantes de masculinidad y feminidad.
La criminología queer, como “un enfoque teórico y práctico que busca resaltar y llamar la atención sobre la estigmatización, la criminalización y, en muchos sentidos, el rechazo de la comunidad queer” ( Buist y Lenning, 2016 : 1), ha intentado abordar los resultados equitativos y la invisibilidad de las personas LGBTQ tanto en los entornos legales penales como en la investigación académica ( Panfil, 2022 : 270). Sin embargo, el privilegio de la sexualidad en la criminología queer puede no ser el más adecuado para las comunidades que son objeto de ataques específicamente debido a la identidad de género. De hecho, las personas trans y de género diverso a menudo son solo notas secundarias en los estudios de criminología queer. Y si bien Buist y Stone (2014) sostienen que la criminología queer es necesaria para abordar y rectificar los desafíos que enfrentan las personas trans en términos de “igualdad de derechos y protección bajo la ley y dentro de las normas culturales” (p. 36), estos enfoques también tienden a pasar por alto una paradoja central: las intervenciones legislativas que apuntan a abordar y frenar la violencia pueden en realidad provocar más daño. Por ejemplo, las estrategias de inclusión legal a menudo crean nuevas formas de exclusión a medida que refuerzan las estructuras violentas ( Spade, 2015 ). Además, debido a que las comunidades trans continúan teniendo relaciones complicadas con la policía (estando simultáneamente sobrerrepresentadas en el sistema penal-legal y subrepresentadas tanto en las medidas de prevención como en los estudios de investigación), estas experiencias de vida únicas justifican un enfoque diferente. Este artículo también se basa en el llamado de Musto (2019) a que “trans” criminología para “desestabilizar las cuentas binarias de género, daño, justicia y castigo, y para replantear la praxis abolicionista en direcciones feministas anticarcelarias innovadoras” (p. 37). Sin embargo, mi enfoque es algo diferente al de Musto (2019) , quien considera que lo trans es más bien un punto de partida conceptual que puede llevar a transformar el campo de la criminología crítica (p. 50), ya que priorizo las consecuencias materiales y los impactos biopolíticos y necro políticos de la legislación antitrans en las vidas de las personas trans. Reconociendo el trabajo pionero que ha realizado la criminología queer, este artículo es también un llamado a aprovechar esta investigación existente para desarrollar una criminología trans más sólida que dé cuenta de cómo las personas trans y de género diverso se vuelven cada vez más criminales —y, por extensión, prescindibles— dentro de la ley y la política.
De hecho, las personas trans enfrentan muchos desafíos que las atrapan dentro del sistema legal penal, lo que Jenness y Rowland (2024) ilustran astutamente a través de su articulación del «nexo legal penal transgénero». Este concepto describe los sistemas interconectados de aplicación de la ley, justicia penal y encarcelamiento que se cruzan con las vidas trans. Al destacar cómo las personas trans son criminalizadas tanto directa como indirectamente y se ven desproporcionadamente afectadas por el sistema legal penal debido a injusticias sistémicas (por ejemplo, discriminación, estigma, desigualdades estructurales), el concepto también ilustra cómo las personas trans (particularmente las personas trans de color) están sobrerrepresentadas dentro del complejo industrial penitenciario. Este nexo también subraya cómo el acceso inadecuado a la atención médica que afirma el género, los mayores riesgos de violencia y la identificación errónea con el género y el maltrato se cruzan para producir resultados perjudiciales para las personas trans. 2
Los niños trans como chivos expiatorios
En abril de 2021, Arkansas fue noticia al aprobar la Ley 626, denominada “Ley de Arkansas para Salvar a los Adolescentes de la Experimentación (SAFE)”, y convertirse en el primer estado en prohibir la atención de afirmación de género. Si bien más tarde un juez federal la consideró inconstitucional, ha tenido una prolífica repercusión al impulsar una serie de leyes similares dirigidas al acceso a la atención médica y criminalizar a los profesionales médicos que brindan atención. Esta tendencia continúa, y Florida llegó al punto de prohibir o restringir la atención de afirmación de género tanto para niños como para adultos en 2023. Este impulso legislativo es parte de un patrón más amplio de ataques crecientes a los derechos de las personas queer y trans que comenzó en 2015, irónicamente solo un año después de que la revista Time anunciara infamemente la llegada del “Punto de inflexión transgénero”, una era que anunció el siguiente paso en la igualdad de derechos para todos los géneros. Inicialmente centradas en cuestiones como los baños públicos y la participación en deportes, las iniciativas legislativas recientes se han centrado cada vez más en los jóvenes trans y el acceso a la atención médica, las escuelas y el atletismo.
Como detallan Jenness y Rowland (2024) , el aumento de los proyectos de ley antitrans se ha logrado demonizando la no conformidad de género a través de campañas publicitarias y una retórica política divisiva. Yuxtapuestas a una imagen de la fragilidad femenina blanca, estas campañas han retratado a las personas trans como sexualmente depredadoras, mentalmente inestables, engañosas y socialmente disruptivas. Poniendo énfasis en los impactos sociales de larga data de este tipo de mensajes, la filósofa trans Talia Mae Bettcher (2007) ha demostrado cómo el encuadre estereotipado de las personas trans como engañosas refuerza la idea de que su identidad de género es de alguna manera fraudulenta o ilegítima, lo que conduce a una mayor estigmatización y dificultades para acceder a recursos vitales y derechos humanos. A pesar de una amplia investigación que muestra que ni los baños inclusivos de género conducen a un aumento de la delincuencia ni las niñas y mujeres trans que toman bloqueadores de la pubertad o terapia de reemplazo hormonal tienen «ventajas injustas», los activistas antitrans y los responsables políticos siguen utilizando este tipo de tácticas de miedo para hacer retroceder las medidas de igualdad de género inclusivas para las personas trans.
El enfoque en los niños trans es, en cierto modo, accidental. En “Cómo una campaña contra los derechos de los transgéneros movilizó a los conservadores”, los periodistas de investigación del New York Times Adam Nagourney y Jeremy W. Peters descubrieron la historia detrás de este intenso enfoque político. Después de que la Corte Suprema afirmó el derecho constitucional al matrimonio entre personas del mismo sexo en 2015, los conservadores se encontraron sin un tema clave en torno al cual pudieran movilizar partidarios y donantes. Después de buscar una nueva causa capaz de unir a su base y atraer la atención nacional, el tema de la identidad trans, especialmente entre los niños, ganó un impulso significativo. Este impulso legislativo comenzó con un enfoque en lo que desde entonces se ha convertido en una causa célebre para los políticos conservadores: la participación de las niñas trans en los deportes juveniles. En un contexto de medios de comunicación de derecha que parecían obsesionados con los niños trans (o más bien con el temor de que los niños estuvieran expuestos a la inestabilidad de las categorías de género), dirigieron su atención a la presentación ferviente de proyectos de ley estatales que prohibieran el acceso a la atención que afirmara el género, incluidos los bloqueadores de la pubertad ( Nagourney y Peters, 2023 ).
Aunque puede que haya sido un accidente que este sea el grito de guerra en torno al cual se han unido los republicanos, también es el resultado de una planificación cuidadosa por parte de las organizaciones conservadoras “para aprovechar la emoción en torno a la política de género” ( Nagourney y Peters, 2023 ). Y como han demostrado ahora los resultados de las elecciones de 2024, fue una estrategia exitosa que ayudó a las victorias republicanas en todo el país. Este cambio ha revitalizado las redes conservadoras e influido en las agendas de las juntas escolares locales y las legislaturas estatales. Matt Sharp, asesor principal de Alliance Defending Freedom, que brinda asesoramiento a los legisladores estatales que intentan aprobar una legislación antitrans, enfatizó que todas las medidas actuales vuelven a la pregunta “¿qué podemos hacer para proteger a los niños?” (citado en Nagourney y Peters, 2023 ). Si bien muchos conservadores afirman que las prohibiciones deportivas surgen de un deseo de proteger a los niños y asegurar los derechos de los padres, otros reconocen que los niños trans son chivos expiatorios. Nadine Smith, directora ejecutiva de Equality Florida, afirma que esto se convirtió en un caso de prueba en la mensajería: “Una vez que abrieron ese marco de los derechos de los padres, comenzaron a usarlo en todas partes” (citado en Nagourney y Peters, 2023 ).
Aunque hace no mucho los conservadores sociales y los grupos religiosos pueden haber tratado a las personas trans con confusión o desinterés, ahora utilizan el poder de la ley para atacar a las comunidades trans y a cualquiera que pueda brindarles atención médica. Esta negación sistemática de derechos a las personas que no se ajustan ni pueden ajustarse a las normas legales y burocráticas ya se repite compulsivamente a través de lo que Dean Spade (2015) llama “violencia administrativa”, o el daño sistémico y la privación de derechos infligidos a las comunidades trans a través de los procesos burocráticos y administrativos cotidianos. A diferencia de la violencia física manifiesta, la violencia administrativa opera a través de políticas, regulaciones y prácticas institucionales que apuntan y oprimen desproporcionadamente a las personas trans y no conformes con su género. A menudo incrustada en sistemas supuestamente objetivos y neutrales como la aplicación de la ley, la inmigración, la atención médica y los servicios sociales, esta forma de violencia es particularmente insidiosa porque a menudo se pasa por alto o se normaliza, pero tiene profundas consecuencias para la vida y el bienestar de las personas trans.
Los esfuerzos por limitar los derechos de los jóvenes y adultos trans (e incluso criminalizarlos) se agrupan en gran medida en torno a cuatro temas: baños, atención médica, deportes y lenguaje. Carolina del Norte inició esta agenda legislativa conservadora en 2016, cuando presentó el primer proyecto de ley del país que prohibía a las personas trans usar baños públicos que se alinearan con su identidad de género. En ese momento, esta medida provocó una reacción generalizada y la ley finalmente fue derogada en 2017. Sin embargo, los llamados «proyectos de ley de baños» han resurgido con venganza en todo el país. Aunque muchos no se han aprobado, desde 2017 se han introducido aproximadamente 100 medidas para restringir el uso de baños públicos para personas trans. La politóloga Susan Gluck Mezey (2020) enfatiza las consecuencias discriminatorias de dichos proyectos de ley, incluidos los problemas de salud que enfrentan los niños trans que a menudo evitan usar los baños por completo cuando se ven obligados a usar instalaciones que no se alinean con su identidad de género.
La legislación que restringe el acceso a la atención de afirmación de género ha aumentado drásticamente, con 185 proyectos de ley de este tipo presentados en 2023 (esto suma un total de más que los cinco años anteriores juntos). 3 De manera similar a las tácticas observadas en las restricciones a los proveedores de abortos (por ejemplo, las leyes TRAP), estos proyectos de ley a menudo implican la imposición de sanciones a los proveedores de atención médica, con castigos que van desde multas y suspensiones de licencias médicas hasta sentencias por delitos graves de hasta 99 años de prisión y acusaciones de abuso infantil. Park et al. (2021) advierten que esta amplia criminalización política de la atención médica trans podría sentar un precedente peligroso para futuras restricciones politizadas a la atención para diversas poblaciones. A pesar de la oposición de importantes organizaciones de libertades civiles y grupos de defensa como la Asociación Médica Estadounidense, estos proyectos de ley siguen surgiendo en varias jurisdicciones. A nivel federal, también se presentó al Senado de Estados Unidos la “Ley de Protección de los Niños frente a la Experimentación” y, de aprobarse, establecería un nuevo delito penal federal para los profesionales de la salud que brinden atención de afirmación de género a menores: “Un profesional de la salud física o mental que realice o proporcione una derivación para un procedimiento de transición de género en un menor está sujeto a sanciones penales: una multa, una pena de prisión de hasta cinco años o ambas”. 4
En cuanto a los deportes, Idaho se convirtió en el primer estado en prohibir a las niñas trans competir en atletismo femenino y femenino en 2020, y desde entonces al menos 24 estados han aprobado leyes que limitan la participación de los niños trans ( Strangio, 2024 ). Si bien la mayoría de estos proyectos de ley se centran en las niñas y mujeres trans, cinco estados también han extendido estas prohibiciones a los niños trans. Las escuelas secundarias han sido el foco principal, pero estas regulaciones se están introduciendo cada vez más en el nivel universitario. Estas prohibiciones también han intentado utilizar medidas intrusivas, incluidos los requisitos de un examen físico médico en casos de «sexo en disputa», como es el caso de las versiones iniciales de la prohibición deportiva de Ohio actualmente en discusión legislativa.
Por último, en lo que respecta a la vigilancia del lenguaje, nueve estados han promulgado recientemente leyes que abordan ampliamente la terminología y el lenguaje relacionados con el género, incluidos los pronombres y los nombres. En consonancia con los infames proyectos de ley estatales de “No digas gay”, Florida llega al extremo de prohibir a los profesores y a los estudiantes hablar o compartir sus pronombres personales. En Kentucky, los profesores no están obligados a utilizar pronombres para los estudiantes que no sean de su sexo biológico; mientras tanto, Indiana y otros estados han introducido políticas de “derechos de los padres” (sobre las que volveré más adelante), que obligan a notificar a los padres cuando los niños solicitan utilizar nombres o pronombres que no se correspondan con el sexo que se les asignó al nacer. En Arizona, también se han presentado varios proyectos de ley antitrans, incluido uno que exige que tanto el tutor como el profesor aprueben los pronombres de un estudiante y otro que prohíbe los libros que “promuevan la fluidez de género o los pronombres de género”. 5
La proliferación de estos proyectos de ley es asombrosa. De hecho, en 2024, 669 proyectos de ley que buscan atacar a las comunidades trans están siendo considerados actualmente en 43 legislaturas estatales diferentes. 6 Esto marca un aumento significativo, totalizando más que cualquier otro año registrado. Según el Trans Legislation Tracker Project, 48 proyectos de ley anti-trans habían sido aprobados en 2024 al momento de escribir este artículo, y 139 más estaban siendo considerados. Si bien aproximadamente 482 proyectos de ley ya han sido rechazados, el gran volumen de legislación anti-trans que se presenta constantemente debería ser motivo de alarma. Sin duda, esta cifra aumentará, particularmente a nivel federal dadas las victorias del Partido Republicano en 2024 al asegurar la presidencia y una mayoría tanto en el Senado como en la Cámara de Representantes. Como ejemplo, en el mes posterior a las elecciones de noviembre de 2024, se aprobaron tres proyectos de ley adicionales y se presentaron 14 más.
El Proyecto 2025 y la Promesa Conservadora
Muchos de los proyectos de ley mencionados anteriormente se redactaron como casos de prueba en preparación para su rápida implementación a nivel federal mediante una orden ejecutiva presidencial. Si tiene éxito, la agenda conservadora de largo alcance denominada Proyecto de Transición Presidencial 2025, más comúnmente conocido como Proyecto 2025, desmantelaría todos y cada uno de los avances logrados en el avance de los derechos, la dignidad y la aceptación de las personas trans. El Proyecto 2025 es una iniciativa de la Heritage Foundation, un grupo de expertos de extrema derecha dedicado a desarrollar y promover políticas públicas conservadoras. Según su sitio web, el Proyecto tiene cuatro pilares:
(1) una agenda política integral,
(2) un manual de 180 días, que tiene como objetivo «brindar un alivio rápido a los estadounidenses que sufren las políticas devastadoras de la izquierda», 7
(3) una base de datos de personal presidencial que contiene los currículos de conservadores examinados para colocarlos en roles gubernamentales históricamente no partidistas, y
(4) una Academia de Administración Presidencial para capacitar a futuros designados políticos. Tanto la base de datos de personal como el programa de capacitación están vinculados al “Anexo F”, un plan de extrema derecha para reemplazar a miles de empleados federales no partidistas por leales (el entonces presidente Trump instituyó algunas variantes de este plan en 2018). Este enfoque de cuatro frentes sentaría las bases para la introducción e implementación rápida y sin problemas de los objetivos principales del Proyecto 2025, lo que probablemente tomaría por sorpresa a muchos estadounidenses.
Aunque los cuatro pilares son fundamentales para el éxito del Proyecto 2025, me centro aquí principalmente en el componente de políticas, que toma la forma de Mandato para el liderazgo: la promesa conservadora (comúnmente conocida como La promesa conservadora ), un documento de 920 páginas que describe una serie de cambios de políticas y agendas legislativas que puede promulgar el próximo presidente conservador de los Estados Unidos. Montgomery (2024 : np) describe esta iteración de la planificación conservadora como «un cambio ideológico a nivel de movimiento que se aleja de una desconfianza libertaria del poder gubernamental y se acerca a una visión autoritaria del poder gubernamental que se utiliza sin piedad, ya sea como una fuerza justa ejercida para promover una ‘cosmovisión bíblica’ o contra un ‘estado administrativo’ supuestamente capturado por una izquierda marxista radical». Editado por Paul Dans y Steven Groves, The Conservative Promise cubre una serie de temas clave y cuestiones sociales en torno a las cuales la derecha ha dedicado una atención significativa en los últimos años: la rescisión de los derechos LGBTQ, el desmantelamiento de los derechos reproductivos, el negacionismo climático, la fortificación de fronteras, los derechos de los padres y la reestructuración masiva o eliminación de departamentos federales (incluido el Departamento de Educación). Pero en su centro, el Proyecto 2025 apunta a las comunidades trans. Aquí se presenta, como describe la periodista Melissa Gira Grant (2023: np), un futuro en el que “la heterosexualidad conyugal es la única forma válida de expresión e identidad sexual; todos los embarazos se llevarían a término, incluso si eso requiere coerción o muerte; y las personas transgénero y no conformes con el género no existen”.
El primer principio en torno al cual se estructura la agenda es un plan para “restaurar la familia como la pieza central de la vida estadounidense y proteger a nuestros hijos” ( Roberts, 2023 : 3), lo que pretenden lograr, en parte, mediante la rescisión de las protecciones legales para las personas LGBTQ. Al igual que los proyectos de ley estatales analizados anteriormente, el proyecto busca promulgar leyes y políticas que criminalicen o restrinjan de otro modo los derechos de las personas trans en varios aspectos de la vida, incluidas las políticas escolares, la atención médica, el atletismo y los documentos de identidad. La “ideología transgénero” y el “transgenerismo” se presentan como las principales amenazas para la nación y la familia, una construcción construida sobre marcos de larga data de las personas trans como fraudulentas, sospechosas y engañosas. Pero, como ilustra el concepto de violencia administrativa de Spade, esto también es una trampa 22. Debido a que las personas trans deben navegar por sistemas que no están diseñados para ellas, a menudo se las retrata preventivamente como engañosas, un marco que se convierte en la justificación misma del castigo. Jenness y Rowland (2024) enfatizan la “naturaleza cíclica y de refuerzo mutuo de la criminalización cultural y la criminalización legal”: las leyes anti-trans no solo excluyen a las personas trans y las exponen a la vigilancia y el acoso, sino que también hacen que un mayor número de personas trans entren en un contacto más sostenido con el sistema legal penal, “reforzando así los significados no fundamentados y dados por sentados asociados con lo que significa ser transgénero y, por lo tanto, posibilitan su criminalización” (p. 288).
En The Conservative Promise , el cambio social en torno a las normas de género y el auge de las identidades trans se enmarcan como un peligro para la familia nuclear heteronormativa. En la Introducción, el presidente de la Heritage Foundation, Kevin Roberts (2023), presenta una realidad alternativa que a muchos de nosotros nos resultaría difícil identificar. Desde su perspectiva, los niños viven en un mundo en el que “sufren la normalización tóxica del transgenerismo con drag queens y pornografía que invaden sus bibliotecas escolares” (p. 1). Este espectro de demonización trans se invoca inmediatamente como peligroso y dañino para sus principios ideológicos fundamentales. La pornografía, escribe: [se] manifiesta hoy en día en la propagación omnipresente de la ideología transgénero y la sexualización de los niños […] No tiene derecho a la protección de la Primera Enmienda. Sus proveedores son depredadores de niños y explotadores misóginos de mujeres. Su producto es tan adictivo como cualquier droga ilícita y tan psicológicamente destructivo como cualquier delito. La pornografía debería ser ilegalizada ( Roberts, 2023 : 5).
Esta invocación de la pornografía es intencionadamente amplia, vaga y amorfa. Al equiparar las cuestiones trans (“transgenerismo” e “ideología transgénero”) con la pornografía, el abuso infantil y la misoginia, esta visión da un paso hacia la ilegalización total de las personas trans. Roberts (2023) continúa detallando los mecanismos draconianos y restrictivos necesarios para erradicar la pornografía y todo lo que conlleva: “Las personas que la producen y distribuyen deberían ser encarceladas. Los educadores y bibliotecarios públicos que la ofrecen deberían ser clasificados como delincuentes sexuales registrados. Y las empresas de telecomunicaciones y tecnología que facilitan su difusión deberían ser clausuradas” (p. 5). Esta retórica extrema señala un enfoque sin restricciones para regular el género, la sexualidad y la privacidad. Consciente de que es poco probable que estados con mayor tendencia izquierdista arresten a personas trans por tales cargos, el documento detalla más adelante un plan más amplio a través del cual el Departamento de Justicia intervendría y procesaría a cualquier funcionario local que no estuviera dispuesto a emprender acciones penales contra las personas LGBTQ ( Hamilton, 2023 : 553).
La Promesa Conservadora también describe cómo se debe criminalizar tanto a las personas trans como a cualquiera que les brinde atención, incluidos terapeutas y médicos. Como advierte el periodista Bryan Tannehill (2023 : np) en “El Partido Republicano tiene un plan maestro para criminalizar el hecho de ser trans”, el Proyecto 2025 aboga por la prohibición a nivel nacional de la atención que reafirme el género para los jóvenes trans, pero también sugiere “que las personas que son visiblemente trans en público son pornográficas u obscenas, porque podrían ser vistas por un menor”. Estas propuestas planteadas por el Proyecto 2025 no se limitan a regular los espacios públicos, sino que son mecanismos de control social que refuerzan las ideologías de género dominantes y criminalizan a quienes se desvían de ellas.
En línea con la retórica actual en torno al atletismo, Roberts también apunta en particular a lo que la derecha ha llamado en gran medida “los hombres biológicos que dominan los deportes femeninos”. Si bien la afirmación no tiene fundamento, este tipo de lenguaje funciona como un mensaje secreto para los políticos y civiles antitrans (incluidas las feministas radicales que excluyen a las personas trans) y, como indican las crecientes preocupaciones legislativas, parece ser un mensaje efectivo. A pesar de su reducido número, los atletas trans han sido víctimas de una proporción desmesurada de interés, debate y legislación de los medios de comunicación. A menudo adoptado como una lucha para “proteger” a las niñas y mujeres, este enfoque ha tenido éxito a la hora de unir a los conservadores, muchos de los cuales tienen antecedentes cuestionables en lo que respecta a la promoción de los derechos de las niñas y las mujeres. Los derechos de las niñas y la paridad de género, por lo tanto, se convierten en una cobertura conveniente para la retórica y las políticas antitrans.
Protegiendo a los niños
El tema de “proteger a los niños” está presente en todo el trabajo del Proyecto 2025. Esta no es la primera vez que los niños (o los niños simbólicos) han sido utilizados por campañas políticas anti-LGBTQ para promover agendas conservadoras. De hecho, la figura del niño ha sido manipulada para atraer a los votantes durante décadas. Una de las campañas más exitosas tuvo lugar en 1977, cuando la cantante estadounidense y activista contra los derechos de los homosexuales Anita Bryant se convirtió en el rostro de la coalición política “Save Our Children” para luchar contra una ordenanza en Florida que prohibía la discriminación basada en la orientación sexual. Apenas una década después de Stonewall, esta campaña fue un síntoma de reacción contra lo que parecía ser el comienzo de una creciente aceptación social de las personas LGBTQ. Utilizando el tropo de la “decencia” y lemas como “¡No existe ningún derecho humano a corromper a nuestros niños!”, la campaña resultó efectiva y el electorado rechazó abrumadoramente la ordenanza antidiscriminación. Su éxito también desencadenó batallas similares en todo el país, y varias jurisdicciones revocaron leyes antidiscriminación aprobadas previamente.
Una retórica similar se repite en todos los capítulos de The Conservative Promise . Sin embargo, en esta iteración actual de la batalla ideológica, los niños deben ser protegidos de la “mutilación genital” ( Severino, 2023 : 495), “la nueva ideología de género progresista” ( Vought, 2023 : 62) y “las cirugías de cambio de sexo” ( Vought, 2023 : 62). Se retrata a los niños como personas totalmente vulnerables e incapaces de tomar decisiones por sí mismos, “un producto no de su condición de niños sino más bien de la infantilización histórica que se les ha hecho soportar” ( Gill-Peterson, 2018 : 196-197). También se señala a las niñas como particularmente vulnerables al “contagio social” del “transgenerismo”, lo que se basa en narrativas culturales de larga data que infantilizan a las niñas y mujeres y eliminan cualquier capacidad de acción que puedan tener. 8 Roberts (2023) también escribe que los niños están siendo corrompidos por los “principios nocivos” de la “ideología de género”, que “deberían ser extirpados de los planes de estudio en todas las escuelas públicas del país” (p. 5). Continúa: “Estas teorías envenenan a nuestros niños, a quienes se les enseña […] a negar la condición de criaturas que es inherente al ser humano y que consiste en aceptar la condición dada de nuestra naturaleza como hombres o mujeres” ( Roberts, 2023 : 5). Al ejemplificar las ideas de Edelman (2004) sobre cómo se ha manipulado la figura del niño en la política, esta narrativa cultural posiciona a la transexualidad y a los niños trans como una amenaza para el orden simbólico, precisamente porque alteran el marco tradicional de las normas de género.
Reconociendo el poder de lo simbólico (especialmente ejemplificado a través del lenguaje), una de las principales herramientas del Proyecto 2025 para rescindir las protecciones legales para las personas trans es la eliminación explícita del lenguaje y la terminología que reconocen el género y la diversidad, lo que, según afirman, “priva a los estadounidenses de sus derechos de la Primera Enmienda”:
El próximo presidente conservador debe convertir a las instituciones de la sociedad civil estadounidense en blancos difíciles para los guerreros de la cultura progresista. Esto comienza con la eliminación de los términos orientación sexual e identidad de género (‘SOGI’), diversidad, equidad e inclusión (‘DEI’), género, igualdad de género, equidad de género, conciencia de género, sensibilidad de género, aborto, salud reproductiva, derechos reproductivos y cualquier otro término […] de todas las normas federales, regulaciones de agencias, contratos, subvenciones, reglamentos y piezas legislativas que existan. ( Roberts, 2023 : 4–5)
Las palabras tienen poder. Y si bien es ingenuo suponer que eliminar el uso de palabras relacionadas con el género realmente nos librará de nuestra existencia, sabemos que el lenguaje moldea realidades. Eliminar o prohibir términos que reflejan nuestras identidades conducirá a una disminución de los recursos sociales y económicos que mejoran las oportunidades de vida de las comunidades trans y de género diverso ( Spade, 2015 ). Además, los intentos de equiparar el género con el sexo biológico asignado al nacer y argumentar que este es inmutable y binario (y luego construir políticas en consecuencia) son actos violentos, “desplazamientos convenientes para la violencia política descarada contra la vida trans” ( Gill-Peterson, 2018 : 196 ). La investigación también nos dice que la autoafirmación y la autodeterminación, incluida la autoidentificación, son fundamentales para la salud y el bienestar, no solo para las personas trans sino para las personas de todos los géneros. Pero debemos preguntarnos, ¿cómo es posible la autodefinición cuando el gobierno proscribe las mismas estructuras de apoyo (incluyendo el lenguaje y los nombres) que nos sostienen y hacen que nuestras vidas sean más llevaderas? Si bien eliminar terminología como la anterior puede parecer un paso pequeño, es otra forma en que las personas trans están sujetas a sistemas de poder que gobiernan la vida y la muerte. Y si bien las teorías de la transnormatividad sugieren que algunas personas trans están marcadas para la protección y el futuro, otras son claramente prescindibles e incluso marcadas para la muerte, en particular aquellas que son marginadas debido a su raza, clase u otras identidades interrelacionadas. Esto es lo que Haritaworn y Snorton (2013) denominan necropolítica trans, un concepto que se basa en el trabajo de Achille Mbembe para revelar las formas en que se extrae valor político de las muertes rutinarias de personas trans de color, apuntalando así proyectos imperialistas y vitalizando proyectos antiinmigrantes y homonacionalistas. A través de los borrados lingüísticos del Proyecto 2025, las personas trans son enmarcadas como desechables y prescindibles, y se revocarán recursos que podrían salvar vidas si este tipo de frases se eliminan de las políticas e instituciones, extendiendo así la necropolítica trans a los niveles más altos del gobierno.
Aquí no hay personas trans
A pesar de la fijación del Proyecto 2025 en la diversidad de género, las personas trans apenas son mencionadas. 9 En cambio, palabras como “género” y “sexo” están por todas partes en The Conservative Promise . Los autores invocan un fantasma del “transgenerismo” mediante la repetición de frases como: “radicalismo de género”, “ideología de género”, “ideologías raciales y de género radicales”, “teoría radical de género”, “la llamada identidad de género”, “ideología racial y de género de izquierdas”, “nuevas teorías antidiscriminación (como las teorías de orientación sexual e identidad de género)” y “la nueva ideología de género progresista”. Esta ausencia de personas trans es significativa porque ensaya la no-personalidad. Hay que reconocer que las personas trans realmente existen –nombrar a las personas trans como personas– es un acto de otorgar humanidad. Por extensión, este repudio está directamente vinculado a la deshumanización y la negación de la personalidad jurídica (y todo lo que conlleva). De hecho, como lo expresa la destacada académica de estudios trans Susan Stryker, la categoría de lo humano no es universal ni ontológicamente dada, sino que se ha utilizado para deshumanizar . Stryker explica en detalle cómo esto también es una dinámica de género:
Ha sido muy difícil pensar en lo humano sin hacerlo a través del esquema binario de género. Creo que gran parte de la violencia y la discriminación que enfrentamos las personas trans se deriva de una incapacidad fundamental por parte de los demás de vernos como seres humanos completos porque se nos considera inapropiadamente asignados en género y, por lo tanto, más abajo en la jerarquía de animicidad, por lo tanto, más cercanos a la muerte y la inanimatividad, por lo tanto más prescindibles y menos valiosos que los humanos. ( Stryker y Dierkes-Thrun, 2014 : np)
El plan del Proyecto 2025 (1) de definir el género como una característica biológica e inmutable que está determinada únicamente por los genitales al nacer y (2) eliminar toda la terminología relacionada con el género invisibiliza, borra y, como expresa Stryker, hace que la vida trans sea “más prescindible y menos valiosa que la de los humanos”. 10
Gill-Peterson (2018) escribe que “el niño trans sigue siendo una figura a través de la cual las fuerzas antitrans pueden centrar sus esfuerzos para socavar cualquier futuro para las personas trans” (p. 196). El Proyecto 2025 no solo erosiona las oportunidades de un futuro trans habitable, sino que va un paso más allá al negar que las personas trans siquiera existan. En The Conservative Promise , se fomenta activamente la eliminación y la deshumanización de las personas trans en los entornos escolares. En el capítulo sobre el Departamento de Educación (al que en otra parte del documento se hace referencia como una “ventanilla única para el cártel de la educación progresista” ( Dans y Groves, 2023 : 285)), se invocan los derechos de los padres y se utilizan como justificación de este repudio:
Ningún empleado o contratista de educación pública deberá utilizar un nombre para dirigirse a un estudiante que no sea el que figura en el certificado de nacimiento del estudiante, sin el permiso por escrito de los padres o tutores del estudiante. ( Burke, 2023 : 346)
Ningún empleado o contratista de educación pública deberá utilizar un pronombre que sea diferente del sexo biológico del estudiante al dirigirse a él sin el permiso por escrito de los padres o tutores del estudiante. ( Burke, 2023 : 346)
El lenguaje de los “derechos de los padres” se convierte en una herramienta para negar la dignidad y el respeto a los niños trans y no binarios (aunque los derechos de los padres son de suma importancia, se apresuran a afirmar que permitir a los padres “’reasignar’ el sexo de un menor es abuso infantil y debe terminar” ( Roberts, 2023 : 5)). También invocan escenarios extravagantes sobre lo que podría deparar el futuro si los demócratas siguieran en la presidencia, incluido el de que las escuelas “podrían estar obligadas a ayudar a un niño con una transición de género social o médica sin el consentimiento de los padres” ( Burke, 2023 : 344). Esta manipulación de los hechos sugiere que las escuelas abogan activamente por la transición de género de los estudiantes o la ayudan; mientras tanto, el uso de “podrían” es estratégico y funciona como una táctica de miedo de que los padres ya no tendrán voz ni voto en la educación o la crianza de sus hijos. Como detalla Judith Butler (2024) en Who’s Afraid of Gender? Este tipo de exageraciones extrañas y afirmaciones engañosas sobre el género no se limitan a los EE. UU., sino que están siendo utilizadas por fuerzas conservadoras en todo el mundo.
Las escuelas ya son lugares de violencia en Estados Unidos. Es difícil evitar la cobertura mediática de las epidemias de violencia con armas de fuego y acoso escolar. Si bien los jóvenes trans y queer han sido objeto de violencia por parte de otros niños durante mucho tiempo, estos cambios de política convertirían efectivamente a las instituciones educativas, incluidos los maestros y administradores, en perpetradores de violencia. Formas de este enfoque ya están sucediendo, como lo destaca la historia de Nex Benedict, una de las pocas muertes trans que recibió cobertura mediática. Benedict era un adolescente no binario de ascendencia choctaw que fue intimidado y agredido, y finalmente fue encontrado muerto el 8 de febrero de 2024, el día después de que un grupo de estudiantes lo conmocionara. Si bien el forense local dictaminó que la muerte de Benedict fue un suicidio, las circunstancias siguen siendo un misterio. 11 Esto es en gran medida lo que Stanley (2021) quiere decir cuando escribe sobre las formas estratificadas de violencia dirigidas a los jóvenes trans, primero a través de su deshumanización rutinaria al ser «aterrorizados física y emocionalmente habitualmente en las escuelas» y luego a través de la ausencia de responsabilidad legal por la violencia dirigida a ellos (p. 119). Es probable que esta dinámica también se haya visto exacerbada por la condición indígena de Benedict (un hecho que rara vez se mencionó en la cobertura mediática de su muerte). Esto también es una necropolítica trans en funcionamiento, ya que los niños trans enfrentan no solo la amenaza de violencia física y asesinato, sino también la restricción de los recursos necesarios para sobrevivir, incluida la negación del acceso a atención médica que reafirme su género, la falta de vivienda y otras formas de violencia estructural que exacerban la vulnerabilidad y posicionan a las personas trans como prescindibles.
Sasha Buchert, directora del Proyecto de Derechos No Binarios y Transgénero de Lambda Legal, afirma de manera similar que el lenguaje utilizado en la guía del Proyecto 2025 es deshumanizante y se alinea con el enfoque más amplio de la derecha política. En lugar de reconocer a las personas queer y trans como personas, a menudo se las retrata como meras ideologías o «ismos», despojándolas de su humanidad (en Pengelly, 2023 ). Buchert advierte además que incluso si el Proyecto 2025 no tiene éxito en sus objetivos, su existencia, el respaldo de medidas severas y la deshumanización de las personas trans probablemente alimentarán más legislación anti-LGBTQ ( Pengelly, 2023 ). Esto, a su vez, reforzará un clima necropolítico trans en el que las personas de género diferente se ven obligadas a vivir vidas marcadas por el secreto para poder sobrevivir, perpetuando un ciclo de discriminación, marginación y borrado (véase también Francisco, 2021 ).
Conclusión
Muchos se apresurarán a señalar que los derechos LGBTQ han avanzado mucho en los últimos años y que las personas queer y trans han logrado muchas victorias legales. De hecho, los medios de comunicación dominantes han caracterizado en gran medida las dos últimas décadas como emancipadoras para las comunidades LGBTQ, con avances como la igualdad matrimonial, la legislación sobre crímenes de odio y la expansión de las protecciones contra la discriminación. Pero a pesar de lo que ha parecido una marcha lenta hacia la aceptación y la inclusión, la era posterior a la igualdad matrimonial ha marcado el comienzo de una reacción violenta. Este panorama cambiante se refleja en los intentos omnipresentes de demonizar y criminalizar a las comunidades trans. Y en el contexto de una atmósfera de violencia ya intensificada, el Proyecto 2025 es, se puede suponer, el primer paso de un plan más amplio. Al pintar un retrato de una sociedad que se asemeja a El cuento de la criada , Grant (2024 : np) enfatiza las implicaciones e ideologías más amplias en juego en la visión autoritaria del Proyecto 2025 para el futuro: “el género y la sexualidad no se reconocen como existentes fuera de las familias nucleares patriarcales. Todo lo que existe aquí son madres y bebés, niños y familias. Cada familia está destinada a funcionar como una extensión del estado, dedicada a controlar y confinar el sexo, el género y la sexualidad, con todo el poder coercitivo y la violencia que requeriría”. El Proyecto 2025, si tiene éxito, daría un paso monumental en la reducción de los derechos y la dignidad de las personas trans y de género diverso (entre otras poblaciones, incluidas las mujeres cis y las personas de color). Al apuntar a las comunidades trans mediante una formulación de políticas y una legislación preventivas, esta iniciativa de extrema derecha socava la autonomía y el acceso a recursos esenciales. Crea un clima de miedo, incertidumbre e inseguridad para las comunidades trans, que enfrentarán aún más riesgos de violencia, discriminación y persecución legal como resultado.
Si bien la atención de los medios tradicionales al Proyecto 2025 había sido relativamente escasa, las redes sociales y el periodismo ciudadano comenzaron a llenar ese vacío haciendo sonar las alarmas. La escritora de Substack, Andra Watkins, resume las terribles consecuencias en el blog “Cómo el Proyecto 2025 arruinará tu vida”, que cito aquí extensamente:
• A cualquier persona transgénero de cualquier edad se le podría negar la atención médica que reafirme su género. Esto incluiría el tratamiento hormonal para quienes ya hayan realizado la transición.
• Las personas podrían ser procesadas como depredadores sexuales por utilizar un baño que difiere de su género asignado al nacer.
• Las personas LGBTQIA+ o sus hijos podrían ser rechazados en escuelas, universidades, empresas, farmacias e incluso hospitales debido a su orientación sexual o identidad de género.
• Discriminación contra familias LGBTQIA+ en entornos escolares.
• La gente podría morir.
• Las personas podrían ser procesadas como depredadores sexuales por actuar en espectáculos de drag o por vestirse de drag.
• Las protecciones nacionales al matrimonio entre personas del mismo sexo podrían ser derogadas.
• Las personas podrían ser procesadas como depredadores sexuales o pornógrafos por ser homosexuales, bisexuales, no binarios, transgénero u otros.
• Las personas LGBTQIA+ podrían ser arrestadas por demostraciones públicas de afecto.
• Se podría obligar a las personas a recibir adoctrinamiento religioso financiado por los contribuyentes para evitar ir a prisión por tales delitos.
• Los estados podrían perder toda la financiación federal por negarse a aplicar las leyes federales anti-LGBTQIA+. 12
Se están sentando las bases para esta visión conservadora: las etapas embrionarias del Proyecto 2025 ya se están implementando a través de decenas de proyectos de ley y políticas antitrans que se presentan a nivel estatal todos los días. La gran cantidad de nuevos proyectos de ley ante las legislaturas estatales ilustra de manera devastadora “las infinitas formas en que nuestros momentos contemporáneos de imperio son capaces de encontrar tácticas nuevas y cada vez más insensibles para capturar, encarcelar y liquidar bajo el mismo nombre de la democracia […] [L]a violencia antitrans/queer racializada no es antagónica al estado democrático; está entre sus fundamentos” ( Stanley, 2021 : 114). En efecto, este conjunto de recomendaciones de políticas federales, como se ha argumentado en este artículo, avanza en un continuo de violencia al pasar del castigo y el borrado a la criminalización y la necropolítica.
Los campos de los estudios trans y la criminología queer revelan cómo fuerzas sociales y políticas más amplias, incluidas las prácticas institucionales, la investigación científica y las representaciones culturales, han dado forma a las comprensiones de la infancia trans. Este artículo también ha buscado hacer una contribución al creciente campo de la criminología queer al alentar su expansión hacia un compromiso más sostenido con el género. Debido a que la violencia que experimentan las personas trans es diferente de la dirigida hacia las comunidades queer, un cuerpo de trabajo más riguroso en criminología trans ayudaría a descubrir y revelar cómo la no conformidad de género está atrapada en una red de estigmatización y criminalización, y que eventualmente podría conducir al borrado y la erradicación. Reflexionando desde una perspectiva criminológica queer, Copson y Boukli (2020) escriben que “las cuestiones de delito y justicia no pueden ni deben separarse de las cuestiones sobre cómo es, o podría imaginarse, la sociedad en su conjunto. El verdadero potencial de la teoría queer radica en su capacidad de traducir el pensamiento ilusorio abstracto en políticas transformadoras concretas” (p. 519). Aunque los derechos LGBTQ han sido un tema de análisis académico desde hace mucho tiempo, han adquirido una gran urgencia a medida que este tipo de leyes y políticas han desmantelado los avances logrados por las minorías sexuales y de género a un ritmo sorprendente. Si bien la criminología queer puede ser de hecho una herramienta para traducir “ilusiones abstractas en políticas transformadoras concretas”, también debemos seguir desarrollando una criminología específicamente trans ( Musto, 2019 ). La criminología queer (y transing) significa imaginar formas alternativas de reconocimiento y visibilidad en las que se priorice la integridad y la autodeterminación. Pero también significa cuestionar y tal vez evitar por completo el reconocimiento y la visibilidad como vías para la libertad trans. En este momento, debemos imaginar y promulgar nuevas realidades que valoren y celebren la transidad en toda su belleza y complejidad. Y debemos contraatacar. Esta es una cuestión de vida o muerte, y nuestra supervivencia depende de ello.
Revisión de Chatbots en Atención Sanitaria: Tendencias y Aplicaciones
The Chatbot Applied to Health. A Bibliometric Review
José Eduardo Cortés Torres. Carol Estefanía Saldaña Moren
Nota del blog:
Un chatbot es un programa informático que simula la conversación humana con un usuario final. No todos los chatbots están equipados con inteligencia artificial (IA), pero los chatbots modernos utilizan cada vez más técnicas de IA conversacional como el procesamiento del lenguaje natural (LLM) para comprender las preguntas de los usuarios y automatizar las respuestas.
La próxima generación de chatbots con capacidades de IA generativa ofrecerá una funcionalidad aún mayor con su comprensión del lenguaje común y las consultas complejas, su capacidad para adaptarse al estilo de conversación del usuario y el uso de la empatía al responder a las preguntas de los usuarios. Los líderes empresariales ven claramente este futuro: el 85 % de los ejecutivos afirman que la IA generativa interactuará directamente con los clientes en los próximos dos años, según se recoge en el estudio The CEO’s guide to generative AI, del IBV.Una solución de inteligencia artificial de nivel empresarial puede permitir a las empresas automatizar el autoservicio y acelerar el desarrollo de experiencias de usuario excepcionales.
- Los chatbots contemporáneos aprovechan los LLM que procesan y generan texto, generalmente con arquitecturas de modelos de transformadores.
- Las “dispersiones” de LLM se pueden mitigar con datos de entrenamiento de alta calidad, recuperación de generación aumentada y detección y reescritura de resultados incorrectos. Cuando los LLM logran una alta precisión y evitan las alucinaciones, tienen el potencial de abordar las disparidades en materia de salud al anclar las operaciones de investigación y atención médica en la objetividad, como un baluarte contra la subjetividad, el sesgo y el error concomitante en el proceso de razonamiento hipotético-deductivo que domina la toma de decisiones clínicas.
- Los miles de millones de tokens (generalmente palabras) y parámetros (expresiones matemáticas de lo que aprenden los modelos) utilizados para entrenar LLM requieren una potencia computacional sustancial.
- Los mensajes del LLM deben incluir contexto, instrucciones con restricciones y estimaciones de incertidumbre, omitiendo información extraña.
- Los datos de entrenamiento deben representar todas las poblaciones de pacientes y entornos para los que se puede aplicar el LLM.
- Los LLM tienen el potencial de anclar las decisiones clínicas en la objetividad, como baluarte contra el sesgo y el error inherentes al razonamiento hipotético-deductivo.
INTRODUCCIÓN:
La rápida evolución de la inteligencia artificial está provocando profundas transformaciones en diversos ámbitos de la sociedad actual. Uno de los campos donde se vislumbra un gran potencial para la aplicación de estas tecnologías emergentes es la provisión de servicios de salud. En particular, en los últimos años ha surgido un creciente interés por estudiar la implementación de chatbots o agentes conversacionales inteligentes con fines relacionados a la atención sanitaria.
Si bien existen algunas investigaciones preliminares en esta área, hasta el momento no se contaba con una caracterización integral del estado del conocimiento sobre el desarrollo y aplicación de chatbots en el ámbito de la salud. Ante esta necesidad, la presente investigación tiene por objetivo mapear de forma sistemática los principales focos temáticos, tendencias, diseños metodológicos y conclusiones obtenidas en los estudios realizados en torno a esta temática en los últimos años El creciente desarrollo de aplicaciones basadas en inteligencia artificial está transformando muchos ámbitos de la sociedad Ortega (2023). Uno de los campos donde se visualiza un gran potencial de mejora mediante estas tecnologías emergentes es la provisión de servicios de salud. En particular, en los últimos años ha surgido un marcado interés en estudiar la implementación de chatbots o agentes conversacionales para diversos fines en contextos de atención sanitaria. Si bien existen ya algunas investigaciones preliminares al respecto, no se contaba hasta el momento con una caracterización integral del estado del conocimiento en este novedoso campo de estudio.
Surge entonces la necesidad de mapear de forma sistemática los principales focos y tendencias temáticas en la investigación dedicada al desarrollo de aplicaciones de chatbots en el área de la salud Arias et al. (2022). Asimismo, y tal como lo afirma Gamarra et al. (2022) resulta clave analizar con mayor profundidad los diseños metodológicos empleados y las conclusiones obtenidas en los estudios realizados hasta el momento, para determinar la solidez de la evidencia y fundamentar adecuadamente futuras aplicaciones. Para abordar este vacío, se llevó a cabo una revisión bibliométrica cualitativa de 50 artículos científicos indexados entre 2018 y 2023, extraídos de principales bases de datos biomédicas y multidisciplinarias. A través de un análisis temático y de contenido, se clasificaron las investigaciones examinadas con relación a sus objetivos, metodologías utilizadas, principales hallazgos y áreas de aplicación estudiadas. De esta forma se obtuvieron resultados integrales sobre el estado actual y las perspectivas de este creciente campo de estudio.
Los hallazgos permiten determinar las áreas y aplicaciones específicas de chatbots en salud que
- están recibiendo mayor atención investigativa en la actualidad. Asimismo, posibilitan evaluar la
- solidez de las evidencias obtenidas hasta el momento en cuanto al real potencial y efectividad del
- uso de chatbots en contextos sanitarios (Camelo et al., 2019; Palacios et al., 2019; Auqui, 2021).
- Sobre esta base se pueden orientar de investigación a futuro y sentar las bases para una aplicación
- clínica rigurosamente fundamentada cuando se considere apropiado.
- En síntesis, el presente estudio permitirá obtener una visión integral sobre el estado de avance, tendencias temáticas, principales conclusiones y desafíos pendientes en la investigación dedicada al estudio e implementación de chatbots en el amplio campo de la salud. Los resultados servirán para orientar nuevos esfuerzos investigativos y aplicaciones prácticas optimizando recursos y esfuerzos sobre la base del conocimiento existente.
La revisión bibliométrica se basa en los 50 artículos tomados en la Base de Datos recopilada por medio de los estándares del Diagrama Prisma siendo estos publicados entre los años 2018 al 2023, a continuación, se presentarán estos artículos tomados de las Bases de Datos como Scopus, ScienceDirect, Scielo, PubMed y Web of Science. En la Tabla 4 se resaltará su autor, objetivo principal de investigación y las conclusiones, todos los artículos son afines y aportan o informan sobre proyectos realizados con Chatbots enfocados en el campo de la salud, académicos o terapéuticos teniendo en cuenta el Chatbot como factor central de estudio.
La revisión bibliométrica efectuada permite identificar diversas áreas y aplicaciones donde se están implementando chatbots en el contexto de la salud. Un claro énfasis se sitúa en el uso de estos agentes conversacionales para brindar apoyo y seguimiento en salud mental, así como para el tratamiento de diferentes tipos de trastornos. En esta línea, se encuentran estudios como los de Guerrero et al. (2019), Abd-Alrazaq et al. (2019) y Koulouri et al. (2022) quienes analizan específicamente las posibilidades de los chatbots en intervenciones para mejorar la resiliencia, la salud mental de jóvenes universitarios y en general como herramienta de apoyo psicológico.
Otra área de marcado interés es la educación y formación médica con chatbots. Aquí se ubican investigaciones como las de Castillo y Soto (2020), Vásquez (2021), Viñas (2022) y López García de Albizu (2019), cuyos chatbots buscan mejorar la educación sobre prevención de enfermedades infecciosas, el aprendizaje del sistema bucal humano, la realización de pruebas PCR y la concientización sobre la gripe respectivamente. En todos los casos se encuentran resultados prometedores sobre el potencial pedagógico y motivador de estas tecnologías conversacionales aplicadas a la capacitación en salud.
La era digital ha marcado un cambio significativo en la forma en que abordamos la salud y la atención médica. En este contexto, los chatbots han emergido como herramientas innovadoras que ofrecen un potencial transformador en diversos aspectos de la salud, desde la atención médica hasta la promoción de la salud mental. El análisis bibliométrico realizado revela una amplia gama de aplicaciones de los chatbots en diferentes áreas, destacando su capacidad para proporcionar apoyo personalizado, seguimiento continuo y comunicación eficiente. A través de esta visión general, exploraremos cómo los chatbots están siendo utilizados en la actualidad para mejorar la calidad de vida de las personas, facilitar el acceso a la información médica y contribuir al avance de la atención médica moderna. De lo anterior que a continuación se presenta un análisis de tallado de cada uno de los temas identificados destacando objetivos y principales aportes de las investigaciones.
ChatBot de rehabilitación
Los estudios citados abarcan un amplio espectro de aplicaciones de los chatbots en el ámbito de la salud y la atención médica. Ejemplo de ello, Zobenco y Vacileev (2020) analizan el uso de chatbots en odontología para mejorar la atención y conciencia en pacientes con anomalías faciales congénitas. En contraste, Bacilio (2021) evalúa la usabilidad de un chatbot en pacientes con COVID-19 y sus posibles reacciones adversas. Además, Pino (2021) busca hacer accesible la ciencia a personas con discapacidad visual mediante un chatbot que permita conversaciones en
lenguaje natural.
En otra vertiente, Morone et al. (2021) se enfocan en la rehabilitación asistida por robots para personas con discapacidad neurológica, resaltando la necesidad de investigar y estandarizar la eficacia de esta tecnología. Por otro lado, Calvaresi et al. (2019) y Segrelles-Calvo et al. (2021) centran sus estudios en la cesación del hábito de fumar mediante chatbots, subrayando su apoyo personalizado. Mientras tanto, Seitz et al. (2022) investigan el uso de agentes de conversación en atención médica, poniendo en relieve la importancia de la confianza generada en los usuarios.
Ahora bien, propuestas como la de Ávila-Tomás et al. (2020) y Fadhil y Schiavo (2019) también abordan el desarrollo de chatbots de alta calidad para ayudar a fumadores. La utilidad de estas investigaciones radica en su potencial para mejorar la calidad de la atención médica y la accesibilidad a los servicios de salud. Los chatbots pueden proporcionar apoyo personalizado, seguimiento continuo y comunicación eficiente, lo que contribuye a la innovación y la mejora de la calidad de vida de los pacientes. Además, su capacidad para ahorrar tiempo y recursos en la gestión de casos clínicos y su adaptabilidad para atender diferentes necesidades de salud, hacen que sean herramientas valiosas en el campo de la salud y la atención médica.
ChatBot educativo
En el ámbito educativo, Zobenco y Vacileev (2020) analizan el uso de chatbots en odontología para mejorar la atención en pacientes con anomalías faciales congénitas, mientras que Bacilio (2021) se enfoca en evaluar la usabilidad de un chatbot en el seguimiento de pacientes con COVID19. Por su parte, Arias-Navarrete et al. (2020) buscan implementar un chatbot para asesorar a estudiantes y mejorar su gestión de aprendizaje personalizado, haciendo énfasis en la adaptación del chatbot a las necesidades individuales.
Además, C.-Y. Huang et al. (2018) desarrollan un sistema llamado «SWITCHes» que facilita la comunicación en tiempo real con un chatbot de salud para apoyar el seguimiento del peso y la actividad física de los usuarios. En el ámbito de la educación sexual, Fernández-Saborío (2018) diseñó una interfaz de usuario para un chatbot destinado a educar a adolescentes sobre salud sexual.
De manera similar, Guerra y Rojas (2020) investigaron el efecto del aprendizaje a través de un chatbot sobre la prevención y tratamiento de la COVID-19, demostrando un aumento significativo en el conocimiento y la satisfacción de los usuarios.
Estos estudios, en conjunto con los ya mencionados, tienen como objetivo principal explorar y evaluar el uso de chatbots en contextos educativos y de salud. La utilidad de estas investigaciones radica en su capacidad para proporcionar información, apoyo, retroalimentación y motivación de manera eficiente y personalizada, contribuyendo así al aprendizaje efectivo y la promoción de conductas saludables. Además, facilitan el acceso a la información y la interacción en entornos educativos y de salud, ofreciendo nuevas oportunidades para mejorar el bienestar y la calidad de
vida de las personas.
ChatBot para el apoyo y seguimiento de la salud mental.
Las investigaciones mencionadas tienen como objetivo principal el desarrollo, evaluación y aplicación de chatbots para el apoyo y seguimiento de la salud mental en diversas áreas y poblaciones. Noble et al. (2021) evalúan la efectividad del Asistente de recursos de información inteligente de salud mental para apoyar a trabajadores de la salud y sus familias en provincias
canadienses, destacando su potencial como un punto adicional de acceso a servicios de salud mental cuando se necesitan.
Chung et al. (2021) desarrollan un chatbot para la atención obstétrica y salud mental perinatal, enfocándose en mejorar su usabilidad y motivar su uso continuo mediante la actualización periódica de su base de datos. Cameron et al. (2018) esbozan el diseño y desarrollo de iHelpr, un chatbot para cuidado de la salud mental, resaltando las mejores prácticas en su diseño, desarrollo y ética. Morales Quintero et al. (2021) se centran en el desarrollo de un chatbot para la autogestión emocional de personas jóvenes, reflexionando sobre el proceso de investigación en este campo emergente.
Por su parte, Romero et al. (2020) discuten la creciente presencia y potencial de los chatbots en psicología, resaltando la necesidad de más evidencia sobre su eficacia y eficiencia. Cueva y Medina (2020) validan el uso de un chatbot para el diagnóstico inicial de trastornos de ansiedad y depresión, enfocándose en su utilidad como herramienta de autodiagnóstico accesible. Espinosa Rodríguez etal. (2018) diseñan un chatbot para aplicar un cuestionario de TDAH, buscando mejorar la atención y apoyo a estudiantes con este trastorno.
Estas investigaciones demuestran el potencial de los chatbots en la salud mental, proporcionando apoyo, información, consejería y seguimiento personalizado a través de plataformas tecnológicas accesibles y eficientes. Los chatbots pueden facilitar la detección temprana de trastornos, ofrecer recursos de autoayuda y mejorar la comunicación entre usuarios y profesionales de la salud, contribuyendo así a la promoción de la salud mental y el autocuidado en la población.
ChatBot para tratamiento de trastornos mentales
Ahora bien, las propuestas investigativas mencionadas tienen como objetivo principal el desarrollo, evaluación y aplicación de chatbots para el tratamiento de trastornos mentales en diferentes contextos y poblaciones. DiPietro et al. (2019) se centran en la integración de terapias asistidas por computadora para enseñar habilidades sociales, mientras que Espinosa et al. (2018) buscan mejorar la calidad educativa mediante un chatbot para identificar síntomas de TDAH en estudiantes universitarios. Por su parte, Narynov et al. (2021) y Merino (2021) desarrollan chatbots para
satisfacer necesidades de salud mental y detectar trastornos cognitivos a través de dinámicas conversacionales.
La utilidad de estas investigaciones radica en su capacidad para brindar apoyo, detección temprana y seguimiento en el tratamiento de trastornos mentales a través de plataformas tecnológicas accesibles y eficientes. Mazera y González (2018) destacan cómo una aplicación puede ofrecer información y apoyo continuo para enfermedades crónicas como la insuficiencia renal, mientras que Arrabales (2020) y Hernández y Barrera (2021) exploran el uso de chatbots para la detección y apoyo en trastornos emocionales como la depresión y la ansiedad.
Los estudios de Lotero et al. (2022), Muñoz et al. (2021), Bermejo et al. (2020), Castro y Arias (2021) y Hernández y Barrera (2021) enfatizan cómo estas herramientas digitales pueden mejorar la detección temprana, el acceso a información, el apoyo emocional y el tratamiento personalizado para una variedad de trastornos mentales. Esto puede tener un impacto significativo en la promoción de la salud mental, la prevención de trastornos y la mejora de la calidad de vida de las personas afectadas.
ChatBot para tratar enfermedades
Las investigaciones mencionadas tienen como objetivo principal el desarrollo y la evaluación de chatbots para tratar enfermedades generales en diferentes contextos y poblaciones. Valencia Mesías (2020) se centran en el diseño de un sistema mecatrónico para adaptar robots en el ámbito hospitalario, enfocándose en la clasificación y traslado de material quirúrgico. Álvarez et al. (2022) buscan crear una herramienta para evaluar y gestionar el dolor oncológico pediátrico, mientras que Arimov et al. (2021) utilizan tecnologías de telemedicina para evaluar la efectividad de un bot en el monitoreo de asma y la adherencia de los pacientes al uso de herramientas de autocontrol.
La utilidad de estas investigaciones radica en su capacidad para mejorar la atención médica y la gestión de enfermedades a través de la tecnología. Martínez (2021) destaca la optimización de chatbots para brindar información precisa sobre enfermedades como el melanoma y la ELA, con acceso a una base de datos en la nube y capacidad de trabajar con servidores en línea. Viñas (2022) evalúa la utilidad de un chatbot como asistente durante la atención de una PCR, lo que puede ser fundamental para personas sin entrenamiento médico.
Además, Mazera y González (2018) enfatizan la importancia de comprender y compartir
información sobre enfermedades crónicas como la insuficiencia renal crónica, proporcionando acceso a información personalizada para pacientes, familiares y profesionales de la salud. Esto contribuye significativamente al empoderamiento de los pacientes y al fortalecimiento de la comunicación y el conocimiento en el ámbito médico. En resumen, estas investigaciones demuestran cómo la tecnología de chatbots puede ser una herramienta valiosa para mejorar la atención médica, la gestión de enfermedades y el acceso a información relevante para pacientes, cuidadores y profesionales de la salud.
En términos de las principales conclusiones, se encontró que la aplicación de chatbots en el ámbito de la salud es un área muy activa y en constante expansión. La mayoría de las investigaciones se centran en la implementación de estos en aplicaciones relacionadas con la salud mental, seguidas de su aplicación en contextos de educación y aprendizaje. Esto sugiere que los chatbots tienen un
gran potencial para apoyar y dar seguimiento a condiciones de salud mental, así como para el tratamiento de diversos trastornos.
Además, se identificaron diversas áreas temáticas en las que se están aplicando chatbots, como la atención a pacientes con TEA, la navegación quirúrgica, la rehabilitación de personas con discapacidad neurológica y la educación en el ámbito de la salud. Cada una de estas áreas ofrece un enfoque único para la implementación de chatbots con beneficios específicos para pacientes y profesionales de la salud.
En resumen, la revisión bibliométrica realizada en este estudio destaca la creciente importancia de los chatbots en el campo de la salud. Los resultados sugieren que los chatbots tienen un gran potencial para mejorar la atención médica, brindar apoyo en salud mental y en educación en salud.
Sin embargo, también se reconoce la necesidad de seguir investigando y evaluando la eficacia de estos sistemas para garantizar su utilidad y relevancia en el ámbito de la salud.
- CONCLUSIONES
El presente estudio tuvo como propósito caracterizar las publicaciones científicas sobre la implementación de chatbots en el campo de la salud. Si bien la revisión bibliométrica cualitativa de 50 artículos indexados entre 2018 y 2023 permitió alcanzar este objetivo de manera satisfactoria, es importante reconocer algunas limitaciones del estudio. En primer lugar, al tratarse de un análisis documental, los hallazgos se circunscriben a la literatura publicada en las bases de datos
consultadas durante el periodo establecido, por lo que pueden existir otros trabajos relevantes no contemplados. Asimismo, el enfoque cualitativo aplicado, si bien posibilita una comprensión en profundidad, no permite realizar generalizaciones estadísticas. No obstante, los hallazgos obtenidos sientan un precedente valioso al caracterizar integralmente el estado actual de la investigación sobre chatbots en salud, identificando tendencias, enfoques metodológicos predominantes y áreas
de aplicación prioritarias. Esto abre un margen positivo para que futuras investigaciones puedan profundizar en esta línea, ampliando el alcance, incorporando otras perspectivas y explorando nuevas aristas en torno a esta tecnología emergente en el ámbito sanitario.
Los análisis de concurrencia de palabras clave efectuados revelaron la existencia de cuatro ejes o focos principales en las investigaciones examinadas: estudios sobre comunicación académica y científica en humanos, con especial énfasis en explorar diferencias de género; aplicaciones de chatbots e inteligencia artificial específicamente en el contexto de la salud mental; investigaciones referidas al impacto de la pandemia de COVID-19 en múltiples dimensiones de la salud pública; y estudios sobre tecnologías y plataformas digitales emergentes para la prestación de diversos servicios de salud. Estos hallazgos denotan un marcado interés contemporáneo en analizar, desde un enfoque integrador, el potencial de las tecnologías para estudiar problemas complejos vinculados a la salud y la comunicación en este campo.
En lo que respecta a la clasificación por áreas temáticas, se encontró que el énfasis principal se sitúa en la implementación de chatbots para diversas aplicaciones relacionadas con la salud mental, seguido por su aplicación en contextos de educación y aprendizaje. Asimismo, entre los temas investigativos abordados destacan principalmente el apoyo y seguimiento de condiciones de salud mental y el tratamiento de diferentes tipos de trastornos mediante chatbots. Por otra parte, en cuanto a las metodologías empleadas, predominan los estudios con enfoques descriptivos, experimentales y cuantitativos.
En síntesis, el análisis bibliométrico efectuado en este estudio permite arribar a la conclusión de que la investigación sobre chatbots en el amplio campo de la salud constituye actualmente un área muy activa y en franca expansión, con prometedores beneficios tanto para la atención directa de pacientes como para la educación médica. No obstante, se requiere todavía de más investigaciones controladas, que evalúen con mayor rigurosidad la efectividad real de estas aplicaciones de inteligencia artificial, antes de proceder a una implementación a gran escala.
Desafíos y Avances en la Historia Clínica Electrónica
Dr. Carlos Alberto Díaz. Profesor Titular universidad ISALUD
Las principales innovaciones tecnológicas que podrían transformar el sistema de salud en Argentina, incluyen:
Historia Clínica Electrónica (HCE): La implementación de historias clínicas electrónicas permite un acceso más eficiente a la información de los pacientes, mejorando la trazabilidad en la prescripción y suministro de medicamentos.
Digitalización de Procesos: La adopción de sistemas electrónicos para la prescripción, gestión de turnos y telemedicina agiliza la atención al paciente y mejora su experiencia.
Inteligencia Artificial (IA): La IA se utiliza para el análisis de grandes volúmenes de datos, lo que permite identificar patrones, predecir riesgos y personalizar tratamientos, mejorando así la eficiencia y efectividad de la atención.
Telemedicina: Facilita la atención remota, superando barreras geográficas y aumentando el acceso a los servicios de salud, especialmente en zonas rurales o de difícil acceso.
Dispositivos de Diagnóstico de Precisión: Incorporación de tecnologías avanzadas como imágenes radiológicas, tomográficas y resonancias magnéticas que permiten diagnósticos más precisos y una gestión más efectiva de las condiciones de salud.
Wearables y Monitoreo Continuo: Dispositivos portátiles que permiten el monitoreo constante de los signos vitales, lo que facilita una atención más proactiva y la intervención temprana en situaciones críticas.
Sistemas Avanzados de Información y Analítica Predictiva: Ayudan en la toma de decisiones a través de la integración de datos y la analítica avanzada para optimizar los procesos de atención.
Plataformas Digitales para la Participación del Paciente: Estas plataformas permiten a los pacientes tener un rol activo en la gestión de su salud, facilitando la comunicación con los profesionales de salud y el acceso a su información médica.
Robots y Automatización de Procesos: Dispositivos robóticos para tareas quirúrgicas y logísticas, que pueden mejorar la eficiencia en la atención y reducir errores humanos.
Interoperabilidad de Sistemas: Integración de diferentes sistemas informáticos para asegurar un flujo de información más eficaz entre las distintas áreas del sistema de salud.
Estas innovaciones tienen el potencial de aumentar la calidad de la atención, mejorar la accesibilidad y la eficiencia del sistema de salud argentino, así como empoderar a los pacientes en el manejo de su propia salud.
Sin embargo, su implementación exitosa requerirá inversión, capacitación y un enfoque coordinado entre todos los actores involucrados.
Los desafíos más importantes para la implementación de la Historia Clínica Electrónica (HCE) en Argentina son:
Interoperabilidad entre Sistemas: Es crucial que la HCE pueda comunicarse y compartir datos con otros sistemas de información del hospital, como farmacia, laboratorio e imágenes. La falta de interoperabilidad puede limitar la efectividad de la HCE.
Calidad de los Datos: Asegurar que los datos que se ingresan en la HCE sean precisos, completos y actualizados en tiempo real es fundamental para su correcta utilización y para evitar errores médicos.
Alfabetización Digital del Personal: Es necesario que todos los colaboradores de salud, médicos y enfermeros, estén capacitados para utilizar la HCE y otros sistemas digitales, lo que requiere una inversión en formación y entrenamiento.
Protección de Datos y Seguridad de la Información: La naturaleza sensible de los datos de salud implica que la privacidad y la seguridad deben ser una prioridad en el diseño de los sistemas de HCE.
Resistencia al Cambio: La implementación de nuevas tecnologías a menudo genera resistencia por parte de los profesionales de salud que están acostumbrados a los métodos tradicionales. Superar esta resistencia es un desafío clave.
Costos de Implementación y Mantenimiento: La inversión necesaria para adquirir, implementar y mantener la HCE puede ser significativa, lo que puede ser un obstáculo, especialmente para instituciones más pequeñas o con menos recursos.
Estrategias de Cambio Organizacional: Implementar la HCE no es solo un cambio técnico, sino también cultural. Se necesita una gestión del cambio adecuada para facilitar la adaptación de todo el personal involucrado.
Acceso Equitativo: Asegurar que tanto profesionales como pacientes tengan acceso equitativo a la HCE, superando barreras geográficas y tecnológicas.
Estos desafíos necesitan ser abordados de manera sistemática para garantizar el éxito de la HCE y, en consecuencia, mejorar la calidad de atención en el sistema de salud argentino.
las mejores prácticas para mejorar la interoperabilidad de la Historia Clínica Electrónica (HCE) en hospitales incluyen:
Estándares Comunes: Adoptar estándares internacionales y nacionales para el intercambio de datos de salud, como HL7, FHIR y DICOM, para garantizar que todos los sistemas puedan comunicarse entre sí de manera efectiva.
Capacitación del Personal: Proporcionar formación continua al personal sanitario sobre la importancia de la interoperabilidad y cómo utilizar eficazmente los sistemas de HCE.
Integración de Sistemas: Implementar soluciones tecnológicas que permitan la integración de sistemas de información existentes, como farmacias, laboratorios e imágenes, facilitando un flujo continuo de datos.
Interoperabilidad de Datos: Asegurar que los datos sean codificados de manera comprensible y estandarizada, utilizando terminologías médicas consistentes que faciliten el intercambio de información entre profesionales y sistemas.
Políticas de Seguridad y Privacidad: Desarrollar políticas claras que protejan la privacidad de los datos del paciente al tiempo que permiten un intercambio seguro de información entre diferentes sistemas y profesionales.
Plataformas de Intercambio: Establecer plataformas o redes de intercambio de datos que faciliten la colaboración y el acceso a información entre diferentes entidades de salud.
Feedback Continuo: Implementar procesos de retroalimentación que permitan a los usuarios del sistema reportar problemas de interoperabilidad, facilitando así mejoras continuas en el diseño y funcionamiento del sistema.
Participación de los Pacientes: Involucrar a los pacientes en la gestión de su HCE, permitiéndoles acceder a sus datos y contribuir a la información que se almacena, lo que puede mejorar la calidad de los registros.
Evaluación y Mejora de Procesos: Evaluar regularmente la interoperabilidad de los sistemas de HCE y ajustar los procesos y tecnologías según sea necesario para abordar las limitaciones identificadas.
Fomento de un Enfoque Colaborativo: Promover la colaboración entre diferentes actores del sistema de salud (hospitales, clínicas, laboratorios y proveedores de tecnología) para alinearse en el objetivo de lograr una interoperabilidad efectiva. Estas prácticas ayudarán a crear un entorno más conectado y eficiente en cuanto al manejo de información sanitaria, mejorando la atención al paciente y la coordinación de servicios médicos.
La adopción de estándares como HL7 y FHIR en la Historia Clínica Electrónica (HCE) brinda numerosos beneficios, que incluyen:
Interoperabilidad: Estos estándares permiten que diferentes sistemas de información de salud se comuniquen entre sí de manera eficaz. Eso significa que los datos pueden ser compartidos y utilizados por varios proveedores de atención médica, independientemente de las plataformas que utilicen.
Consistencia en los Datos: Al utilizar formatos estandarizados, se asegura que la información sea estructurada y uniforme, lo que facilita la integración y el análisis de datos.
Mejora de la Calidad de la Atención: La interoperabilidad resultante permite un acceso rápido y preciso a la información clave de los pacientes, lo que puede disminuir errores en la atención sanitaria y mejorar la continuidad del cuidado.
Facilitación de la Innovación: Con un marco estandarizado, el desarrollo de nuevas aplicaciones y tecnologías que se integran fácilmente en el sistema existente se vuelve más accesible.
Reducción de Costos: La implementación de estándares puede disminuir los costos asociados con la integración de sistemas y la gestión de datos, al reducir la necesidad de soluciones personalizadas y facilitar el uso eficiente de recursos.
Acceso Eficiente a la Información: Al estandarizar la manera en que se recopila y almacena la información, se simplifica la extracción y el uso de datos para informes, análisis y toma de decisiones, mejorando así la rendición de cuentas y el control de calidad.
Facilitación de la Telemedicina y Atención Remota: Una HCE interoperable basada en estándares puede integrarse mejor con aplicaciones de telemedicina, permitiendo a los proveedores ofrecer atención remota de manera más efectiva.
La adopción de estándares como HL7 y FHIR es fundamental para construir un sistema de salud más conectado y eficiente, que respalde la calidad de atención y el bienestar del paciente.
La interoperabilidad en la atención médica tiene un impacto significativo en la experiencia del paciente.
Aquí hay algunas formas en que afecta esta experiencia:
Acceso Rápido a Información: La interoperabilidad permite que los profesionales de la salud accedan rápidamente a la información crítica del paciente, como su historial médico, resultados de laboratorio y medicamentos actuales. Esto reduce el tiempo de espera y mejora la eficiencia en la atención.
Continuidad del Cuidado: Cuando los diferentes sistemas de información pueden comunicarse entre sí, se asegura que todos los proveedores de atención médica tengan acceso a la misma información sobre un paciente, lo que facilita la continuidad del cuidado y evita la repetición de pruebas o exámenes innecesarios.
Menos Errores Médicos: Una mejor comunicación entre sistemas reduce el riesgo de errores médicos. Por ejemplo, tener información actualizada sobre alergias y medicamentos puede prevenir interacciones peligrosas y garantizar que el paciente reciba el tratamiento adecuado.
Experiencia del Paciente Mejorada: Un sistema interoperable permite que la atención sea más fluida y coordinada, lo que mejora la experiencia general del paciente. Los pacientes pueden sentirse más seguros al saber que su información está disponible para todos los proveedores implicados en su cuidado.
Participación Activa del Paciente: La interoperabilidad también puede facilitar que los pacientes accedan a su propia información médica, fomentando su participación activa en su cuidado. Esto les permite estar más informados y tomar decisiones conscientes sobre su salud.
Análisis y Mejora de Resultados: Los sistemas interoperables pueden recopilar datos que permiten el análisis de resultados de salud, lo que a su vez puede llevar a mejoras continuas en la calidad de atención y satisfacción del paciente.
Optimización de Respuestas a Emergencias Usando Aprendizaje Automático
Análisis automático de prioridades de sistemas de respuesta a emergencias mediante Internet de las cosas (IoT) y aprendizaje automático (ML)
Abu S.M. Mohsin 1, Shadab H. Choudhury 1, Munyem Ahammad Muyeed 1
Nota del blog: Este trabajo es muy interesante, para aumentar la capacidad de respuesta ante emergencias, su complementación con bomberos y defensa civil. La Ciudad autónoma de Buenos Aires tiene uno de los mejores servicios de emergencia en América Latina, con una importante inversión y continuidad como política de estado, que ha trasladado su modalidad de gestión y servicios a otras localidades. Entendiendo que para las emergencias los sistemas públicos son las empresas más eficientes, como ocurre en las principales urbes, como Paris, Ginebra, Roma, Madrid, etc. No tantas emergencias privadas, que no tienen médicos y dotaciones con ese grado de formación. Es imposible, porque no hay emergentólogos en cantidad suficiente. Además hay que continuar difundiendo la asistencia por testigos para reanimaciones dentro de los primeros minutos, que mejora la recuperación de latidos cardíacos. La importancia al decidir por aplicar inteligencia artificial también de utilizar para desarrollos algoritmos genéricos que acortan tiempo de desarrollo, que hace que el proyecto se pueda implementar y comparar. Blangadesh es un país pobre cuya urbanización es creciente, caótica y con una mala estructura, como muchas de nuestras ciudades por ello puede ser un buen ejemplo para aprender algunas de las aplicaciones. Somos testigos de un tiempo de cambio. Los que venden esta tecnología del conocimiento apuran la difusión de buenos resultados parciales para que otros apliquen la misma, siga aprendiendo y consolidando el modelo de comparación, y fortalecer el sistema técnico de toma de decisiones. Por otra parte, nuestro país tiene en la ciudad autónoma de Buenos aires, un sistema de emergencia consolidado, con mucha inversión. Hasta donde está publicado nuestro SAME, no tiene incorporado ningún sistema de Machine Learning que debiera ser por la jerarquía del servicio que se habla. Además el trabajo integra la emergencia a lo socio sanitario y la seguridad urbana, pudiendo integrar y modular los dispositivos, pero lo interesante es que se puedan transmitir señales que determinen las respuestas más adecuadas y combinadas entre ambulancias, bomberos y defensa civil.
Resúmenes
- •En este documento presentamos un marco integral para implementar un sistema de respuesta a emergencias (ERS) impulsado por IoT y ML que aprovecha el análisis de datos en tiempo real y el modelado predictivo.
- El sistema está diseñado para procesar y analizar diversos flujos de datos de múltiples fuentes, como sensores IoT, lo que permite respuestas rápidas e informadas a las emergencias dando prioridad a la respuesta a emergencias (policía, bomberos, hospitales o contactos de emergencia, etc.).
- Para priorizar las emergencias hemos utilizado el modelo XGBoost (es uno de los algoritmos elegidos por una gran cantidad de equipos que quieren utilizar aprendizaje automático). La exactitud, la precisión, el recuerdo promedio y la puntuación F-1 promedio fueron 96.1%, -99.8%, 0.972-0.999, 0.960-0.976 y 0.990-0.960 respectivamente para dispositivos médicos, vehiculares y domésticos.
- Nuestro marco propuesto basado en Machine Learning mejora el procesamiento de datos en tiempo real, la detección rápida de anomalías y el análisis predictivo, proporcionando respuestas oportunas y precisas a las emergencias.
- Además, la implementación web garantiza la escalabilidad y una amplia accesibilidad, lo que facilita la interacción dinámica y el monitoreo en tiempo real a través de interfaces fáciles de usar.
- Este marco no solo mejora las capacidades de respuesta inmediata, sino que también ayuda en la planificación estratégica al proporcionar información procesable sobre posibles eventos futuros hacia una gestión de emergencias más inteligente y basada en datos, mejorando la seguridad y la preparación tanto a nivel comunitario como organizacional.
El despliegue eficaz y oportuno de los recursos es esencial durante las emergencias. Al integrar el aprendizaje automático (ML) y el Internet de las cosas (IoT), el análisis automático de prioridades de los sistemas de respuesta a emergencias podría revolucionar este proceso vital, salvar vidas y minimizar los daños.
Este documento presenta un marco integral para la implementación de un sistema de respuesta a emergencias (ERS) impulsado por IoT y ML, que utiliza el análisis de datos en tiempo real y el modelado predictivo para identificar patrones y priorizar las respuestas en función de su impacto esperado, urgencia, distancia y recursos disponibles.
El sistema está diseñado para procesar y analizar diversos flujos de datos de múltiples fuentes, como sensores IoT, lo que permite respuestas rápidas e informadas a las emergencias dando prioridad a la respuesta a emergencias (policía, bomberos, hospitales o contactos de emergencia, etc.).
Se utilizó el modelo XG Boost para priorizar las emergencias, y su rendimiento se examinó utilizando la exactitud, la precisión, la memoria media y la puntuación F-1 media.
Además, se desplegó un cuadro de mando web para visualizar los datos de los sensores y los proyectados en tiempo real, lo que garantiza la accesibilidad y la escalabilidad. Esto permitió a los usuarios interactuar con el sistema a través de una interfaz intuitiva y obtener alertas e información oportunas.
El sistema proporciona visualización dinámica y seguimiento en tiempo real de escenarios de emergencia a través de la integración de sistemas de información geográfica (SIG) y la utilización de recursos de computación en la nube. Este marco no solo mejora las capacidades de respuesta inmediata, sino que también ayuda en la planificación estratégica al proporcionar información procesable sobre posibles eventos futuros.
El despliegue de este tipo de ERS marca un paso significativo hacia una gestión de emergencias más inteligente y basada en datos, mejorando la seguridad y la preparación tanto a nivel comunitario como organizativo.
Esta innovadora integración de IoT y ML tiene el potencial de transformar los sistemas de respuesta a emergencias, optimizando la asignación de recursos, reduciendo los tiempos de respuesta y, en última instancia, salvando más vidas en situaciones críticas.
1. INTRODUCCIÓN
El sistema de respuesta a emergencias (ERS) se denomina a los esfuerzos y acciones para abordar incidentes como accidentes, desastres naturales o crisis médicas, con el objetivo de minimizar las víctimas y prevenir daños mayores. Una respuesta de emergencia rápida es crucial para su capacidad de salvar vidas, reducir las lesiones y brindar asistencia médica oportuna. Cuando se trata de respuestas oportunas, a menudo hay una diferencia entre la vida y la muerte. Cada minuto cuenta en las emergencias, ya que los retrasos pueden aumentar el riesgo de mortalidad y complicaciones a nivel mundial. Como resultado, alrededor de 1,19 millones de personas han muerto [1].
En Bangladesh, la demanda de sistemas eficaces de respuesta a emergencias es cada día más necesaria debido a la rápida urbanización y el crecimiento de la población. La población de Bangladesh refleja un aumento del 1,01% con respecto al año anterior [2]. La población urbana está creciendo a una tasa anual del 3,5% en Bangladesh, lo que ha ejercido presión sobre los servicios de emergencia [3]. El avance de la sociedad y el bienestar general dependen de garantizar la seguridad individual, así como de tiempos de respuesta más cortos a emergencias como accidentes e instalaciones médicas.
Hoy en día, la respuesta de emergencia en Bangladesh es el tema más preocupante. Aunque la línea de ayuda nacional de emergencia (999) promete un tiempo de respuesta de 10 minutos, el tiempo promedio de respuesta es de aproximadamente 30 minutos [4]. Los accidentes de tráfico provocan más de 21.000 muertes al año, siendo los retrasos en los tiempos de respuesta un factor importante [5], del mismo modo, alrededor de 19.642 incendios en 2020, que resultaron en lesiones y muertes significativas [6]. Estos datos ponen de relieve la necesidad urgente de mejorar el sistema de respuesta a las emergencias.
Además, las emergencias sanitarias también son un tema preocupante, al igual que el número de muertes debidas a ENT (enfermedades no transmisibles) como las cardiopatías, los accidentes cerebrovasculares y la diabetes. Según [7], alrededor del 67% de las muertes en Bangladesh se deben a enfermedades no transmisibles. La evaluación profesional de los pacientes puede reducir las tasas de supervivencia, y los sistemas básicos de respuesta gubernamental son insuficientes para responder eficazmente al aumento de las emergencias. Para reducir las tasas de mortalidad y mejorar la salud de los pacientes, se necesitan instalaciones de respuesta y seguimiento rápidas.
Mediante el uso de dispositivos como los teléfonos inteligentes, los sistemas de automatización del hogar permiten el monitoreo y la administración de los equipos del hogar, lo que los convierte en algo más que comodidades. Aunque fomenta la conservación de energía y los estilos de vida modernos, la automatización del hogar inteligente es costosa, compleja y requiere mucho tiempo de instalar y configurar. [8]. Para superar estos obstáculos, son esenciales soluciones creativas y a precios razonables que hagan que esta tecnología esté fácilmente disponible para todos, incluidos los ancianos y los discapacitados. Además, al integrar los sistemas de automatización del hogar en los planes de respuesta a emergencias, que son soluciones esenciales para la mayoría de los problemas de seguridad, se fomenta el uso cada vez mayor de estos sistemas. Desafortunadamente, los sistemas domésticos actuales se quedan muy cortos al anteponer la comodidad a la seguridad, lo que resulta en serias brechas en la detección y respuesta a emergencias como incendios, fugas de gas e intrusiones de seguridad [9].
Teniendo en cuenta los desafíos actuales en los sistemas de respuesta a emergencias, como los retrasos en la asignación de recursos, la priorización ineficiente de incidentes y la falta de integración de datos en tiempo real, existe una necesidad apremiante de soluciones innovadoras para abordar estas limitaciones. Para superar estos desafíos, proponemos un sistema integral de asistencia de emergencia basado en IoT que integre dispositivos de monitoreo en hogares, vehículos y salud individual. Nuestra solución aprovecha la recopilación y el procesamiento de datos en tiempo real y las técnicas de aprendizaje automático como XGBoost para analizar los datos de los sensores, predecir los niveles de riesgo y priorizar las respuestas en consecuencia. Este sistema se mejora aún más con la administración de datos escalable con Firebase, el seguimiento preciso de la ubicación con la API de Google Maps y el modelado predictivo para optimizar la asignación de recursos de emergencia. Al abordar emergencias relacionadas con la salud, el hogar y los vehículos, nuestro sistema tiene como objetivo mejorar la seguridad pública, reducir las muertes y mitigar los riesgos asociados de manera efectiva.
Este documento está organizado de la siguiente manera: En la sección 2 se revisan las limitaciones de los sistemas de respuesta a emergencias existentes y se destacan las brechas abordadas por nuestro trabajo. En la sección 3 se analiza la importancia de la seguridad de IoT para garantizar la fiabilidad y la seguridad del sistema propuesto. La sección 4 describe la metodología, que abarca la recopilación de datos, las especificaciones de los sensores, la configuración del servidor central en la nube, el procesamiento y el análisis de datos, la integración de la API de Google Maps para la respuesta a emergencias, el diseño de la interfaz web y el modelo de aprendizaje automático empleado. En la sección 5 se presenta el análisis de datos realizado mediante técnicas de aprendizaje automático, mientras que en la sección 6 se detalla el despliegue web del sistema. En la sección 7 se examinan los aspectos de seguridad y privacidad del sistema propuesto. En la sección 8 se ofrece un análisis exhaustivo del rendimiento del sistema. En la sección 9 se analizan los desafíos encontrados durante el desarrollo y se esbozan los posibles trabajos futuros. Finalmente, la sección 10 concluye con un resumen de las contribuciones y las implicaciones más amplias de este trabajo.
2. REVISIÓN DE LA LITERATURA
En las últimas décadas, la implementación de IoT en el sistema de respuesta a emergencias ha florecido excesivamente en diversos dominios como el transporte, la salud y la seguridad del hogar. El objetivo principal de diferentes estudios ha sido aumentar la efectividad en grandes áreas.
Yuan et al. [10] proporcionan una revisión en profundidad de las tecnologías de aprendizaje automático en los sistemas de transporte inteligentes, insistiendo en el potencial de dichas tecnologías para mejorar la seguridad vial y la eficiencia del transporte. De manera similar, Radi et al. [11] introdujeron un sistema de redes de vehículos inteligentes y sostenibles (ISVN) que utiliza el aprendizaje automático, la comunicación de vehículo a vehículo (V2V) y de vehículo a infraestructura (V2I) para gestionar accidentes de tráfico. En otro estudio, Megnidio-Tchoukouegno y Adedeji [12] analizan la precisión del algoritmo del Árbol de Decisión en la predicción y análisis de la gravedad de los accidentes de tráfico mediante el aprendizaje automático. Un estudio notable presenta el avance de la seguridad en la conducción en el mundo real mediante un marco de aprendizaje automático para la detección automatizada de accidentes basada en sensores en el automóvil [13]. Con el fin de resolver los problemas de retrasos en las llegadas y la falta de información crítica para una respuesta de emergencia eficiente, Aslam et al. [14] presentan un sistema automático de detección de accidentes de vehículos y notificación visual de situaciones basado en el Internet de las cosas. Assi et al. [15] sugieren un método para predecir la gravedad de los accidentes mediante la combinación de enfoques y algoritmos de aprendizaje automático. En su comparación de métodos de aprendizaje automático para estimar la gravedad de los accidentes de tráfico, Akour et al.[16] y Chougule et al. [17] muestran que algunos modelos son mejores para determinar la gravedad de las lesiones y evaluar las implicaciones legales y morales de la conducción autónoma, así como sus límites. Al-Mayouf et al.[18] abordan los problemas críticos que afectan a los países en desarrollo: la congestión vial, los accidentes y la contaminación causada por el número de vehículos en las carreteras urbanas. Propone un sistema completo para la gestión de accidentes, que integra la comunicación eficiente y en tiempo real entre vehículos, ambulancias, hospitales, unidades de carretera y servidores centrales mediante redes ad hoc vehiculares (VANETs) y tecnologías de celulares públicas. El sistema utiliza un algoritmo de reenvío óptimo de múltiples saltos para reducir el tiempo de despacho de ambulancias a los lugares de accidentes y también presenta un algoritmo de planificación de rutas óptimas (ORPA) para la reducción de la congestión y la minimización de los costos de viaje.
Varios estudios realizados en el sector de la salud como respuesta de emergencia es muy crucial para la salud. Shaik et al. [19] ofrecen una revisión de los sistemas de monitorización remota de pacientes (RPM), con especial énfasis en la aplicación de la inteligencia artificial (IA) en la atención sanitaria. Mediante el uso de técnicas de ML para identificar irregularidades en el tráfico de la red, Khan y Alkhathami [20] abordan los problemas de seguridad en la atención médica basada en IoT. Wu et al. [21] desarrollan un sistema de monitoreo de la salud en tiempo real basado en el aprendizaje profundo para mejorar la seguridad de los atletas. Tahat et al. [22] desarrollaron un sistema experimental de monitoreo de salud estructural (SHM) que combina algoritmos de aprendizaje automático con conectividad LoRa IoT para identificar daños o errores. Rahman et al. [23] cubren el DL y el ML en la atención médica inteligente con gran detalle. Además, abordan los desarrollos recientes, las aplicaciones y los beneficios de integración. Los desarrollos únicos de Iranpak et al.[24] incluyen el uso de redes neuronales profundas LSTM para monitorear de forma remota la condición de los pacientes y priorizar los datos confidenciales en el IoT. Hiyama et al. [25] proponen un dispositivo portátil basado en sensores para las futuras madres para mejorar la calidad de vida materna y fetal durante todo el embarazo. Además, Gayathri S. et al. [26] diseñaron un sistema de monitorización de la salud de las mujeres embarazadas basado en IoT para la monitorización de la atención sanitaria después del parto, mientras que Banerjee et al. [27] propusieron un sistema de detección de la frecuencia del pulso basado en una técnica no invasiva. Además, Ajagbe et al. [28] proporcionan una revisión exhaustiva de las técnicas de IoT-DL para la detección de pandemias, destacando su aplicación en el monitoreo, la detección y el diagnóstico durante la pandemia de COVID-19. Identifica las brechas en la investigación existente, incluidos los modelos discriminativos de DL poco explorados y la ausencia de algoritmos metaheurísticos, lo que ofrece información para futuros avances.
Debido a la creciente amenaza de intrusiones y emergencias como incendios, la automatización del hogar y los sistemas de seguridad se están volviendo populares hoy en día. Un sistema que puede controlar el sonido, los sistemas de iluminación y varios dispositivos en respuesta a la actitud y el afecto del usuario se conoce como automatización del hogar [29]. Kulbuzhev et al [30] trabajaron para mejorar la seguridad y también reducir la pérdida de energía mediante la implementación de sistemas basados en ML e IA.
Irugalbandara et al. [31] han creado un sistema de automatización del hogar seguro y fuera de línea con reconocimiento de voz y capacidades de medición de energía para resolver los problemas de dependencia de Internet y los riesgos de ciberseguridad en los países en desarrollo.
Empleando la aplicación para teléfonos inteligentes qToggle, el usuario puede operar varios dispositivos domésticos y detectores [32]. Umer et al. [33] introdujeron un extenso sistema de automatización del hogar inteligente de Internet de las Cosas (IoT) que utiliza blockchain y aprendizaje profundo.
Reddy et al. [34] presentan un sistema de automatización del hogar que integra la inteligencia artificial (IA) con el Internet de las Cosas (IoT) para el control automatizado de electrodomésticos para aumentar la eficiencia y la seguridad. Park [35] demuestra cómo se pueden utilizar los algoritmos de aprendizaje automático para pronosticar el consumo de energía, mejorando no solo la eficiencia energética sino también la seguridad al detectar patrones de consumo anormales que pueden indicar una emergencia. Además, Cleland et al. [36] revisaron la automatización del hogar para aquellos con discapacidades, los beneficios incluyen una mayor autonomía, independencia, seguridad y bienestar psicológico.
Las tecnologías de aprendizaje automático (ML) y aprendizaje profundo (DL) están demostrando avances significativos en diversos dominios, respaldados por evidencia cuantitativa de su efectividad.
En el sector agrícola, Taiwo et al. [37], en el que participaron 145 partes interesadas de Shonga Farms, Nigeria, informaron que el 78% expresó un apoyo positivo a la adopción de tecnologías de IA/ML en áreas como la formación, el desarrollo de infraestructuras y los resultados económicos. Sin embargo, también se identificaron desafíos relacionados con los marcos de políticas y la asignación de recursos. De manera similar, en el dominio de la predicción del crimen, los modelos de ML que utilizan datos de sentimiento de Twitter por hora lograron una precisión predictiva del 81% y una puntuación AUC de 0.7079 mediante la aplicación del algoritmo XGBoost [38]. Estos hallazgos ilustran el potencial de las tecnologías de ML/DL para abordar problemas complejos del mundo real, destacando su aplicabilidad y éxito en diversos campos.
En todos los sectores, la implementación de sistemas IoT se centra en la seguridad. En este momento, la comunicación segura entre los vehículos y entre los vehículos y la infraestructura es de suma importancia para garantizar respuestas de emergencia rápidas y confiables. Mohsin et al. [39] identificaron la necesidad de un enfoque unificado que combine datos en tiempo real de los dominios de transporte, salud y seguridad del hogar para ofrecer un sistema de respuesta a emergencias más completo y abordaron el sistema unificado, que es una solución destacada para la gestión de emergencias.
El cuerpo de investigación existente destaca avances significativos en el uso de IoT para sistemas de respuesta a emergencias. Sin embargo, muchos de estos sistemas a menudo se limitan a tipos específicos de emergencias o carecen de una integración completa de múltiples flujos de datos de sensores.
En la Tabla I, exponemos el algoritmo basado en ML disponible para el análisis predictivo y los desafíos de este trabajo. Nuestro estudio busca aprovechar estos hallazgos mediante el desarrollo de una plataforma basada en IoT que combina análisis de datos en tiempo real, modelado predictivo y una interfaz fácil de usar para mejorar la respuesta a emergencias en múltiples escenarios, incluidos médicos, incendios y emergencias.
Tabla I. Algoritmo basado en ML disponible para análisis predictivos y desafíos.
| Ref | Algoritmo de ML | Métricas de rendimiento | Propósito | Desafíos |
|---|---|---|---|---|
| [12] | Árbol de decisión, LightGBM y XGBoost | Se predijo un 20% de los datos de accidentes de 2020, ligeramente superior a los datos reales, pero excluyendo los desequilibrios y errores. | Prediga la gravedad de los accidentes de tráfico en función de los factores contribuyentes. | Conjuntos de datos desequilibrados, el impacto de la COVID-19 en los patrones de tráfico, la necesidad de variables adicionales relacionadas con los conductores. |
| [21] | DNN, PCA, GD | Estándar medio de 8,73, con una longitud media de 35,95 desviaciones y un recuento de palabras de 3,40. | Seguimiento de la salud de los atletas en tiempo real; Diagnosticar afecciones graves como tumores cerebrales, enfermedades cardíacas y cáncer. | Sensibilidad al número de neuronas que causan un subajuste o sobreajuste; Abordar los problemas de gradiente que se desvanecen. |
| [22] | SVM, SGD, df, rf, KNN, LR | Los modelos de clasificación SVM y SGD lograron una precisión máxima (CA) del 96,9 % cuando se utilizaron un 10 % de datos de entrenamiento y un 90 % de instancias de datos de prueba. | Predecir fallos o variaciones en la salud estructural. | Gestione la agregación y el análisis de datos desde el servidor en la nube, lo que garantiza una predicción precisa de fallos. |
| [29] | CNN, SVM, enfoque del clasificador de rostros de Fisher. | Del 82% al 91% cuando el tamaño de las clases se reduce de 8 a 5, y las reducciones adicionales de 5 a 3 dan como resultado una mayor precisión. | Automatiza los sistemas domésticos en función de las acciones del usuario, las emociones y el entorno. | Complejidad en la integración de sistemas, garantizando la privacidad y seguridad de los datos, equilibrando la eficiencia energética y el rendimiento. |
| [34] | Algoritmos de IA (por ejemplo, reconocimiento facial, control climático) | Precisión en la detección de temperatura, humo y nivel de agua | Los electrodomésticos automatizados basados en datos de sensores reconocen rostros por seguridad y proporcionan un control inteligente de los dispositivos. | Complejidad en la integración con dispositivos IoT, calibración de sensores, posibles falsas alertas. |
| [35] | dt, rf, et, gb, hgb, DNN | RMSE: 22.29 | Prediga el consumo de energía de los sistemas HVAC en hogares inteligentes. | Los datos innecesarios eran entradas incorrectas del modelo que hacían que el modelo tuviera un rendimiento inferior. |
3. IMPORTANCIA DE LA SEGURIDAD DE IOT
El Internet de las cosas (IoT) permite la interacción inteligente y automatizada de dispositivos cuando se integra con el entorno externo. No obstante, es necesario un análisis en profundidad de las características y comportamientos de los dispositivos IoT tanto en circunstancias virtuales como reales para su seguridad [40]. Es difícil diseñar una arquitectura de seguridad robusta para el Internet de las Cosas que pueda detectar ciberataques, especialmente para las redes inalámbricas. Debido a su alto consumo de recursos y su limitada potencia de procesamiento, los dispositivos de Internet de las cosas tienen más probabilidades de ser objetivos de posibles amenazas.
Las amenazas activas y pasivas, como el análisis de virus, la suplantación de dispositivos, los ataques de denegación de servicio (DoS), los ataques Sybil y los ataques de intermediario son comunes en los sistemas de IoT. El análisis de malware, la suplantación de dispositivos, los ataques de denegación de servicio (DoS), los ataques Sybil y los ataques de intermediario son ejemplos de amenazas activas. El phishing y el espionaje son ejemplos de amenazas pasivas que pueden socavar seriamente la fiabilidad y la eficacia de los sistemas del Internet de las Cosas [41].
La confidencialidad, la integridad, la autenticación, la autorización, la disponibilidad y el no repudio son cualidades de seguridad que se priorizan en los marcos de seguridad del Internet de las cosas. Si bien la integridad aumenta la seguridad del sistema al permitir solo el acceso autorizado a los datos, la confidencialidad garantiza que la información confidencial contenida en los dispositivos IoT no sea accesible por partes no autorizadas. Los datos confidenciales deben protegerse en los sistemas de IoT utilizando métodos de autorización como diseños basados en políticas y tokens [43].
Las técnicas de aprendizaje automático y aprendizaje profundo basadas en inteligencia artificial son esenciales para identificar el malware y el tráfico de red malicioso en los sistemas de Internet de las cosas. Los sistemas convencionales de detección de ataques se basan en tácticas preestablecidas que son incapaces de reconocer nuevos tipos de ataques [44]. La detección temprana de diferentes tipos de ataques es posible gracias a los algoritmos de aprendizaje automático (ML) que pueden manejar el comportamiento dinámico del sistema IoT sin la necesidad de la participación humana [45]. En la Figura 1 se ilustran los ataques por capas y las soluciones de ML para estos ataques.
Arquitectura IoT de tres capas de nuestro sistema: La arquitectura de nuestro sistema tiene tres capas principales: la capa física, que detecta los datos utilizando muchos dispositivos IoT diferentes, la capa de red, que proporciona una transferencia de datos segura, y la capa de aplicación, donde los datos se procesan, analizan y presentan en interfaces web a los usuarios. Monitorear en tiempo real la contribución de cada capa es crucial para optimizar el rendimiento.
La figura 2 muestra la arquitectura detallada de nuestro proyecto.
4. METODOLOGÍA
La plataforma de Servicios de Asistencia de Emergencia utiliza un enfoque estructurado para garantizar una respuesta rápida y eficiente a las emergencias mediante la integración de diversas tecnologías. La metodología que se ilustra en la Figura 3 se centra en la recopilación, el análisis y la difusión sin interrupciones de datos de múltiples sensores a los servicios de emergencia, abarcando varios componentes y procesos básicos.

Recogida de datos: El sistema integral comienza con los datos recopilados del vehículo, el hogar y los dispositivos de salud. Los dispositivos de los vehículos garantizan parámetros relacionados con la seguridad, como la temperatura, la llama, el GLP, el humo y los niveles de monóxido de carbono y dióxido de carbono. Los equipos domésticos rastrean factores ambientales similares, como la temperatura, el humo, el GLP, la llama, el monóxido de carbono y el metano (MQ4). Además, los dispositivos de salud enfatizan las características de salud individuales, incluida la temperatura, la humedad y la reacción galvánica de la piel (GSR) para la detección del estrés.
Especificaciones del sensor: Nuestros dispositivos para el hogar, el vehículo y la salud utilizan una variedad de sensores, por ejemplo, detección de gases, medición de temperatura y humedad, detección de llamas, detección de movimiento y orientación, seguimiento de ubicación y monitoreo de la salud. Para la detección del nivel del sensor de gas, utilizamos MQ-2 (200-1000 ppm), MQ-4 (300-10000 ppm) y MQ-135 (resistencia de detección de 30 kΩ-200 kΩ) para detectar diferentes gases. Para la medición de la temperatura y la humedad utilizamos DHT11 y DHT 22, que son capaces de detectar la temperatura de -40 °C a 80 °C y la humedad (0-100%). Además, para la seguridad contra incendios, se implementa un sensor basado en infrarrojos que detecta las llamas dentro de un rango específico (por ejemplo, 100 cm). Además, la orientación y la aceleración de los vehículos se miden mediante MPU6050 que ofrece la medición de la orientación, la aceleración (±2 a ±16 g) y la velocidad angular (±250 a 2000 ° / s). Para controlar las colisiones y las vibraciones de los vehículos, los elementos piezoeléctricos detectan la presión y la vibración. Además, los módulos GPS Quectel L80-R proporcionan seguimiento de ubicación en tiempo real con soporte AGPS, lo que garantiza la precisión de la navegación. En consecuencia, el sensor de ECG AD8232 mide la frecuencia cardíaca, el sensor GSR detecta la actividad nerviosa autónoma. Por último, MAX30100 mide tanto la frecuencia cardíaca como la saturación de oxígeno (SpO2), que es fundamental para el seguimiento de los signos vitales en los sistemas de monitorización de la salud. La configuración de hardware para nuestros dispositivos se muestra en la Figura 4.
Servidor central en la nube: Firebase se usa para almacenar los datos recopilados en una base de datos NoSQL cuando se transmiten a un servidor central en la nube. Esta base de datos central permite una gestión de datos eficaz y adaptable mediante el almacenamiento de datos de usuarios, sensores y alarmas en formato de documento. Esta arquitectura permite gestionar grandes cantidades de datos generados por los dispositivos sensores de forma fiable y escalable.
Procesamiento y análisis de datos: Esta fase implica muchos pasos cruciales. La información recopilada se envía a los módulos correspondientes para su análisis inmediato y predicción del futuro utilizando los frameworks NodeRed y Laravel. Los datos entrantes de los sensores son evaluados inmediatamente por el módulo de análisis de datos en tiempo real para buscar irregularidades o niveles potencialmente dañinos. Si se supera algún umbral, se envía una alerta. Para mejorar las capacidades proactivas del sistema, el módulo de predicción futura también utiliza algoritmos de aprendizaje automático para predecir problemas potenciales en función de las tendencias de datos pasadas y presentes.
API de Google Maps: Cuando se detecta una emergencia, el sistema envía una alerta con detalles completos sobre el suceso, incluido el tipo de emergencia, su ubicación (que incluye su dirección física y coordenadas geográficas) y su hora. Con el fin de proporcionar a los servicios de emergencia un seguimiento preciso de la posición, esta alerta se procesa mediante la conversión de direcciones físicas a coordenadas geográficas y viceversa utilizando la API de Google Maps.
Respuesta a emergencias: De acuerdo con la naturaleza de la alerta, el mecanismo de respuesta de emergencia notifica a los respondedores adecuados. A los servicios de emergencia más cercanos y cruciales, como hospitales, comisarías de policía, bomberos y contactos de emergencia, el módulo de enrutamiento de datos transmite la información de alerta. Utiliza la integración de Google Maps para brindar a estos respondedores el enfoque más simple para la ubicación de la emergencia, lo que permite tiempos de respuesta rápidos y efectivos.
Interfaz web: A través de la interfaz de usuario, los usuarios administran eficientemente los recursos, ven los datos de los sensores y supervisan las alertas. La página de inicio del portal ofrece enlaces a los portales específicos de diferentes servicios de emergencia, como los departamentos de policía, bomberos y hospitales, y proporciona a los usuarios acceso instantáneo a las alertas actuales de todas las categorías. Los servicios de emergencia también pueden ver los datos de los sensores en una página de datos de sensores, lo que les permite filtrar los datos en función de la hora y el usuario, en forma de tablas y gráficos.
Modelo de aprendizaje automático: Nuestro sistema enfatiza las respuestas de manera adecuada mediante el uso de un modelo de aprendizaje automático desarrollado para emergencias. Por ejemplo, se recopilan datos de temperatura, humedad y GSR para entrenar el modelo en caso de una emergencia médica. Los parámetros se separan en rangos de umbrales de riesgo, desde un riesgo muy bajo hasta ningún riesgo. En el modelo se utilizó el algoritmo XGBoost, que tiene una alta tasa de precisión en la identificación de diferentes niveles de riesgo.
En resumen, la metodología de la plataforma de Sistemas de Respuesta a Emergencias garantiza una respuesta precisa y oportuna a las situaciones. El sistema tiene como objetivo reducir los tiempos de respuesta y aumentar la eficiencia del servicio de emergencia mediante el modelado predictivo y el procesamiento de datos en tiempo real. Los socorristas pueden reducir los riesgos y salvar vidas con más éxito cuando se integra una interfaz intuitiva.
5. ANÁLISIS DE DATOS MEDIANTE MACHINE LEARNING
Optimización de los tiempos de respuesta en función de la prioridad: En un momento dado, pueden ocurrir múltiples emergencias simultáneamente. No es posible que los servicios de emergencia, ya sean médicos, bomberos o policías, respondan a cada emergencia de inmediato debido a los recursos o la mano de obra limitados. Por lo tanto, es necesario un método para priorizar las emergencias.Hemos desarrollado algoritmos de aprendizaje automático para cada una de las tres categorías de respuestas en función de los datos recopilados por cada tipo de sensor y los umbrales generales adecuados. Las tres categorías utilizan un enfoque similar. Para cada conjunto de datos, utilizamos una división de prueba de entrenamiento de 80:20. Después del entrenamiento, evaluamos cada modelo utilizando la exactitud, la precisión, el recuerdo y la puntuación F-1. Las ecuaciones para cada uno de estos se dan aquí. TP se refiere a True Positive, es decir, el modelo predijo el mismo valor que la verdadera clase i. TN es True Negative, donde el modelo predijo correctamente que el valor no es i. FP es Falso positivo, donde el modelo predijo erróneamente la clase i, mientras que FN es Falso negativo, donde tanto la predicción como el valor verdadero eran de una clase diferente a i.
(1)Unccuruncy=1n∑Yo=0n−1TPYo+TPYoTPYo+FPYo+TNYo+FNYo(2)PrecYosYoon=1n∑Yo=0n−1TPYoTPYo+FPYo(3)Recunll=1n∑Yo=0n−1TPYoTPYo+FNYo(4)F1Score=2(Recunll×PrecYosYoon)Recunll+PrecYosYoon
En este caso, nuestra clase i es un valor de prioridad que va de 1 a 5. Se describen más adelante. Los resultados se dan como la media de cada métrica en todas las clases.
5.1. Emergencia médica
Para desarrollar un modelo para clasificar la gravedad del peligro y la prioridad de la respuesta a la emergencia, recopilamos una serie de puntos de datos de nuestro dispositivo sensor médico. Los datos registrados incluían tres parámetros: temperatura, humedad y GSR (estrés).
Cada parámetro se dividió en umbrales para el nivel de riesgo. Por ejemplo, una temperatura superior a 40 °C representa un alto riesgo para la mayoría de las personas. Del mismo modo, un GSR por encima de 500 indica un alto nivel de estrés. Una combinación de estos factores podría conducir a un escenario más crítico en comparación con un solo factor que sea alto [46]. Anotamos manualmente los valores en función de la información existente sobre los riesgos para la salud. En lugar de utilizar un simple sistema basado en reglas, elegimos construir un modelo que pudiera tener en cuenta estos factores y también escenarios más complejos.
Dividimos nuestros resultados en cinco niveles de prioridad: sin riesgo, riesgo bajo, riesgo moderado, riesgo alto, riesgo muy alto, en función de factores compuestos.
Con el fin de clasificar el riesgo, utilizamos un modelo XGBoost [47], que determina automáticamente las mejores características y construye un árbol basado en él. Los hiperparámetros del modelo se muestran en la Tabla II. Utilizamos la búsqueda en cuadrícula en un rango de hiperparámetros, variando la profundidad máxima de 1 a 20 a intervalos de 2, la tasa de aprendizaje de 0,1 a 0,01 a intervalos de 0,01 y el número de estimadores de 100 a 300 a intervalos de 50 antes de determinar que estos eran los mejores.
Cuadro II. Hiperparámetros para el Modelo de Emergencia Médica.
| Hiperparámetro | Valor |
|---|---|
| Profundidad máxima del árbol | 3 |
| Tasa de aprendizaje | 0.3 |
| Número de estimadores | 100 |
La precisión del modelo fue del 96,1%, lo cual es muy preciso y más que efectivo para nuestros propósitos. La precisión promedio fue de 0.972, el recuerdo promedio fue de 0.976 y el puntaje F-1 promedio fue de 0.974. Los resultados por clase se dan en la matriz de confusión de la Fig. 5 a continuación.

También analizamos los pesos de cada una de las tres características de nuestro modelo final. Como se observa en la Figura 5, las tres variables tienen niveles similares de importancia. Por lo tanto, todos ellos influyen en el proceso de toma de decisiones del modelo y deben registrarse.
5.2. Emergencia del vehículo
Para emergencias vehiculares, utilizamos un modelo similar basado en la prioridad determinada por los valores provenientes del sensor. Separamos los parámetros en diferentes niveles de umbral y les asignamos prioridades que van de uno a cinco, anotando los datos manualmente. Para este modelo, utilizamos la temperatura, la lectura de GNC, la lectura de CO, el humo, la lectura MQ4, la lectura MQ135 y la lectura de llama como características.
Después de usar una búsqueda de cuadrícula similar a la descrita en la sección anterior, llegamos a los siguientes hiperparámetros para nuestro modelo. Para este modelo, un árbol un poco más profundo funcionó mejor. Los hiperparámetros del modelo se muestran en la Tabla III
Tabla III. Hiperparámetros para el modelo de emergencia del vehículo.
| Hiperparámetro | Valor |
|---|---|
| Profundidad máxima del árbol | 5 |
| Tasa de aprendizaje | 0.3 |
| Número de estimadores | 100 |
La precisión del modelo fue del 99,8%. La precisión promedio fue de 0.999, el recuerdo promedio fue de 0.970 y el puntaje F-1 promedio fue de 0.990. Los resultados por clase se dan en la matriz de confusión de la Figura 6 a continuación.

5.3. Emergencia en el hogar
Para emergencias en el hogar, el sensor y los puntos de datos son similares a los de las emergencias de vehículos. Utilizamos la temperatura, la concentración de gas GLP, la concentración de CO, el humo, la lectura de MQ4, la lectura de CO2 y la lectura de llama como características.
Siguiendo un proceso similar al de los dos modelos anteriores, obtenemos los siguientes hiperparámetros en la Tabla IV.
Cuadro IV. Hiperparámetros para el modelo de emergencia domiciliaria.
| Hiperparámetro | Valor |
|---|---|
| Profundidad máxima del árbol | 15 |
| Tasa de aprendizaje | 0.2 |
| Número de estimadores | 100 |
La precisión del modelo fue del 96,1%. La precisión promedio fue de 0.950, el recuerdo promedio fue de 0.960 y el puntaje promedio F-1 fue de 0.960. Los resultados por clase se dan en la matriz de confusión de la Figura 7 a continuación.

En esta etapa, observamos que, si bien nuestros modelos son muy precisos para predecir un nivel de prioridad determinado a partir de los datos de entrada de los sensores, los niveles de prioridad en sí mismos pueden no ser exactamente correctos. Por ejemplo, una lectura alta del sensor de GLP y humo no siempre indica que hay un incendio o algún otro tipo de emergencia. Más bien, utilizamos estos métodos para demostrar que podemos modelar eficazmente la prioridad de las respuestas a emergencias. Los datos y anotaciones adicionales pueden ayudar a acercar estos modelos a lo que sucede en emergencias reales.
6. IMPLEMENTACIÓN WEB
Interfaz de usuario: La interfaz de usuario de la plataforma de Servicios de Asistencia de Emergencia está diseñada como un sitio web adecuado para su uso tanto en dispositivos de escritorio como móviles. El sitio web está diseñado principalmente para que los proveedores de servicios de emergencia realicen un seguimiento de las emergencias entrantes, administren los recursos para responder y monitoreen el estado de las personas potencialmente en peligro.
Características principales: Las características principales de la plataforma web se dan en la Tabla V a continuación. Todas las características enumeradas están completas y disponibles para los usuarios y el personal de los servicios de emergencia.
Cuadro V. Características y categorías.
| Categoría | Característica |
|---|---|
| Gestión y Administración de Usuarios | Los usuarios pueden registrarse, iniciar sesión, verificar mediante correo electrónico y SMS, etc. Los usuarios normales, el personal del servicio de emergencia y los administradores están separados. |
| Base de datos | Base de datos NoSQL en Firebase con monitoreo de datos de usuarios, datos de sensores y alertas. Los puntos de conexión CRUD y API para obtener datos están disponibles. |
| Aprendizaje automático | Algoritmos predictivos para detectar incidentes peligrosos a partir de datos de sensores. |
| Mapeo y enrutamiento | Google Maps se utiliza para dirigir a los proveedores de servicios de emergencia al lugar de un incidente. Los mapas muestran la ubicación de un incidente y la ruta más rápida. |
La base de datos está estructurada de la siguiente manera. Al tratarse de una base de datos NoSQL, los datos se almacenan como documentos en lugar de en formato tabular. En la siguiente Tabla VI se enumeran las colecciones y se ofrece una muestra de cada documento.
Cuadro VI. Colecciones de bases de datos y campos.
| Colección | Campos en documentos |
|---|---|
| Usuarios | Nombre, correo electrónico, teléfono, ubicación de la dirección, dirección particular como texto, tipo de usuario |
| Home Sensor (subcolección para cada usuario) | Monóxido de carbono, Dióxido de carbono, Llama, GLP, MQ4, Humo, Temperatura, Tiempo |
| Sensor del vehículo (subcolección para cada usuario) | Monóxido de carbono, dióxido de carbono, llama, GLP, humo, temperatura, MQ4, tiempo. |
| Alertas | Dirección, ubicación de la dirección, fecha y hora, tipo de alerta. |
| Servicio de Urgencias | Dirección, ubicación de la dirección, tipo de respuesta (hospital, bomberos, policía) |
Al almacenar los datos en nuestra base de datos, utilizamos la API de mapas de Google para convertir la ubicación de una dirección física en una coordenada geográfica. Esto se hace en el caso de un usuario que registra su sensor doméstico. A la inversa, convertimos una coordenada geográfica en una ubicación física en el caso de una alerta, utilizando de nuevo la misma API. Al almacenar ambos en la base de datos siempre que sea posible, minimizamos la cantidad de cálculos y nos aseguramos de que toda la información necesaria para dirigir los servicios de emergencia a una emergencia esté disponible.
El sensor activa una alerta cuando los datos registrados de un sensor superan los umbrales seguros, lo que indica una posible amenaza para la vida. La alerta se registra en la base de datos y el mapa en la plataforma web se actualiza simultáneamente para reflejar la ruta desde la ubicación del Respondedor más cercana hasta la ubicación de la Emergencia.
La página de inicio del sitio web muestra las alertas más recientes de todos los tipos, como se muestra en la figura 8. Los botones en la parte inferior conducen al portal específico para diferentes tipos de servicios de emergencia. El ejemplo del Portal de Hospitales se muestra en la Figura 9. Los portales de Policía y Bomberos están dispuestos de manera similar.


Los usuarios individuales no pueden ver estas alertas. Sin embargo, pueden ver los datos recopilados por los sensores en sus hogares y automóviles. El personal de los servicios de emergencia también puede ver estos datos. Los datos del sensor también se muestran como una tabla en forma gráfica, como se ve en la Figura 10.

La efectividad de esta interfaz se probó consultándola al personal de emergencia. La acogida general fue positiva. Durante este proceso se destacaron características como la capacidad de obtener la ruta a una emergencia con solo presionar un botón.
7. ANÁLISIS DE SEGURIDAD Y PRIVACIDAD
Nuestro sistema de respuesta a emergencias basado en IoT desarrollado consta de tres componentes: botiquines para el hogar, el vehículo y la salud, cada uno responsable de recopilar datos críticos de sensores para el análisis y la toma de decisiones en tiempo real. Para el análisis en tiempo real, los datos se transfieren utilizando protocolos seguros como TCP y MQTT y se almacenan en una base de datos MySQL. En los niveles de almacenamiento y transmisión, el sistema utiliza sofisticados algoritmos de cifrado para mantener la integridad y confidencialidad de los datos. La protección con contraseña añade un grado adicional de seguridad al intercambio y almacenamiento de datos para la base de datos MySQL y el broker MQTT «Mosquitto». Al limitar el acceso del sistema a direcciones IP particulares, los mecanismos de seguridad se fortalecen aún más.
Para proteger la privacidad del usuario y proporcionar a los respondedores información precisa y oportuna, solo los datos necesarios del usuario se comparten con los servicios de emergencia en una situación de emergencia. En el futuro, hay planes para integrar el servicio de firewall de Google para mejorar el control de acceso basado en roles tanto para los administradores como para los usuarios del sistema, así como fortalecer los procedimientos de autenticación de usuarios mediante la autenticación de dos factores (2FA). El panel de control de ThingSpeak proporciona visualización de datos en tiempo real para la supervisión del estado, lo que también garantiza una supervisión continua y comprobaciones de la integridad de los datos, al tiempo que mejora la experiencia del usuario.
La detección temprana de ataques, como la denegación de servicio distribuido (DDoS) y la actividad de botnets, es posible gracias al uso de algoritmos de aprendizaje automático (ML) para identificar patrones anormales en la actividad de dispositivos y redes. El sistema pronostica los niveles de riesgo en escenarios de emergencia, como incidentes médicos o peligros del entorno, utilizando un algoritmo de aprendizaje automático basado en regresión. Para clasificar los niveles de riesgo, utiliza datos de sensores como la temperatura, la humedad y la respuesta galvánica de la piel. Al analizar grandes conjuntos de datos, se utiliza el algoritmo XGBoost por su gran precisión y eficiencia. El modelo pronostica la posibilidad de una emergencia, así como su intensidad. Su rendimiento mejora gradualmente como resultado de su aprendizaje continuo de nuevos datos. El sistema combina métodos de seguridad avanzados con sistemas de detección basados en el aprendizaje automático para garantizar una respuesta de emergencia rápida y precisa. Estas medidas de seguridad y privacidad garantizan la protección contra amenazas convencionales y emergentes, salvaguardando los datos de los usuarios y manteniendo la privacidad en escenarios de emergencia.
8. ANÁLISIS EXHAUSTIVO
En la Tabla VII se presenta un resumen del sistema integral propuesto, en comparación con trabajos anteriores. Muestra las características de nuestro sistema que mejoran los sistemas existentes en múltiples dominios: escalabilidad, rentabilidad, capacidades predictivas, procesamiento de datos en tiempo real, integración de datos, interfaz de usuario, mapeo y enrutamiento, priorización de respuestas a emergencias y seguridad.
Cuadro VII. Comparación de nuestro sistema con obras existentes.
| Parámetros | NUESTRO DISEÑO | Otras obras |
|---|---|---|
| Escalabilidad | Utiliza Firebase NoSQL para el almacenamiento de datos escalable Maneja grandes volúmenes de datos de sensores diversos de manera efectiva | El enfoque de gestión de tráfico de Radi et al. [11] utiliza la comunicación V2V y V2I, que puede ser escalable, pero se limita a las aplicaciones de tráfico. |
| Tecno-económico | Sensores rentables para vehículos, hogares y salud. Aprovecha la infraestructura existente (API de Google Maps) | Kulbuzhev y Dhakshyani proponen un sistema de hogar inteligente IoT de bajo costo con monitoreo de IA que se centra en la automatización del hogar [20]. Park [35] falla en la gestión de diferentes dominios; En su lugar, emplea el aprendizaje automático para las previsiones de consumo de energía en el hogar inteligente. |
| Predicción futura | Modelo XGBoost con ajuste de hiperparámetros (Profundidad máxima: 3, Tasa de aprendizaje: 0,1, Estimadores: 100). Precisión del 96,1 % | Megnidio-Tchoukouegno y Adedeji [10] utilizan un algoritmo de árbol de decisión para la predicción de la gravedad de los accidentes de tráfico, limitada a contextos de tráfico. |
| Procesamiento de datos en tiempo real | NodeRed y Laravel para el enrutamiento y procesamiento de datos. Detección de anomalías en tiempo real y generación de alertas | Wu et al.[12] implementan el aprendizaje profundo para el monitoreo de la salud en tiempo real de IoT, con un enfoque solo en la atención médica. Tahat et al. [22] utilizan LoRa IoT para el monitoreo de la salud estructural en tiempo real, aplicable a la infraestructura pero no integrado con otros dominios. |
| Integración de datos | Integra los datos de los sensores del vehículo, del hogar y de la salud. Servidor central en la nube para la agregación y el análisis de datos | Jaihar et al.[34] desarrollaron un sistema de IoT que responde a las emociones y comportamientos de los usuarios para la automatización del hogar, que no cubre múltiples dominios. Reddy et al. [32] se centran en la IA y la automatización del hogar integrada en IoT, sin integración de datos de vehículos y salud. |
| Interfaz de usuario | Interfaz web para el personal de emergencias. Muestra alertas, datos de sensores y rutas en tiempo real | Stolojescu-Crisan et al. [32] crearon una aplicación de teléfono inteligente para el control de electrodomésticos, que carecía de una integración completa de datos de emergencia. |
| Mapeo y enrutamiento | API de Google Maps para convertir direcciones y coordenadas. Proporciona la ruta más rápida al lugar de emergencia | Assi et al.[15] utilizan tecnologías de mapeo para predecir la gravedad de las lesiones por choques, no integradas con una respuesta integral a emergencias. |
| Seguridad y privacidad | Transmisión segura de datos al servidor central. Datos de usuario almacenados en base de datos NoSQL con control de acceso | Umer et al.[33] utilizan blockchain para la identificación segura y descentralizada de dispositivos IoT, lo que añade complejidad al sistema. |
9. Retos y trabajo futuro
Desafíos: A continuación se muestra la lista de las dificultades que encontramos al desarrollar la Plataforma de Servicios de Asistencia de Emergencia basada en IoT.
- •Complejidad de la integración: Hacer un sistema integral con muchos problemas de integración. La integración de los datos de los sensores de los dispositivos sanitarios, del vehículo y del hogar se interrumpe a veces, pero es necesaria para garantizar una conexión ininterrumpida y la interoperabilidad entre varios dispositivos.
- •Privacidad y seguridad de los datos: Cuando se manejan datos confidenciales de tres dispositivos diferentes, surgen riesgos significativos para la privacidad del hogar, el vehículo y la salud. Proteger los datos contra el acceso no autorizado y las violaciones es necesario durante la transmisión y el almacenamiento, pero es un desafío.
- •Rendimiento del modelo predictivo: En la detección de errores en tiempo real y el análisis predictivo, es un desafío desarrollar modelos de aprendizaje automático altamente precisos y confiables. Mantener una alta precisión y bajos retrasos conlleva una serie de desafíos, como el sobreajuste, la diversidad de datos y los gastos informáticos.
- •Procesamiento en tiempo real: Los requisitos técnicos incluyen el procesamiento de datos en tiempo real para el análisis con el fin de lograr una detección y respuesta rápidas a emergencias. Se requiere una optimización completa para el procesamiento y la comunicación de baja latencia en contextos con recursos limitados.
- •Adopción por parte de los usuarios: Su capacidad para servir tanto a los consumidores como al personal de emergencia es uno de los criterios que deben cumplirse para una integración exitosa. Su usabilidad mejorará si los problemas de una persona han sido resueltos y se le ofrece seguridad antes de que la acepte.
Trabajo futuro: Nos encontramos con dificultades, aunque nuestro proyecto Estamos decididos a utilizar las iniciativas futuras para abordar a fondo los problemas a medida que avanzamos.
- •Integración de sensores adicionales: La capacidad del sistema para rastrear diferentes variables se mejorará a través de una gama más amplia de dispositivos sensores si se amplía el sistema. Esto incluye la creación de estándares de interfaz y API para permitir la transferencia de datos y la compatibilidad.
- •Blockchain para la seguridad: La implementación de la tecnología blockchain puede mejorar la seguridad porque permite un seguimiento transparente de todas las transacciones de datos y preserva la originalidad de los datos, al tiempo que protege la información confidencial del malware o el acceso externo. Como resultado, el sistema se vuelve más confiable.
- •Mejoras en el procesamiento de datos en tiempo real: La arquitectura de procesamiento de datos en tiempo real mejoraría los tiempos de detección y respuesta a emergencias, así como la precisión, al tiempo que reduciría la latencia. Para reducir la dependencia de los servidores centrales y mejorar el rendimiento en contextos con recursos limitados, se podrían emplear enfoques de computación periférica para acercar el procesamiento a la fuente de datos.
- •Pruebas de campo e implementación exhaustivas: Después de realizar pruebas de campo exhaustivas e implementación en el mundo real, evaluamos el sistema Antes de que podamos comenzar a implementar nuestro modelo, deberemos determinar si es lo suficientemente preciso. Estos datos nos proporcionarán la información que necesitamos para refinar aún más el área especificada.
10. CONCLUSIÓN
La integración de las tecnologías IoT, machine learning y web en los sistemas de respuesta a emergencias significa un enfoque transformador para la gestión de crisis. Para priorizar las emergencias hemos utilizado el modelo XG Boost. La exactitud, la precisión, el recuerdo promedio y la puntuación F-1 promedio fueron 96.1%, -99.8%, 0.972-0.999, 0.960-0.976 y 0.990-0.960 respectivamente para dispositivos médicos, vehiculares y domésticos. Nuestro marco propuesto basado en ML mejora el procesamiento de datos en tiempo real, la detección rápida de anomalías y el análisis predictivo, proporcionando respuestas oportunas y precisas a las emergencias. La implementación web garantiza la escalabilidad y una amplia accesibilidad, lo que facilita la interacción dinámica y el monitoreo en tiempo real a través de interfaces fáciles de usar. Al permitir tanto la reacción inmediata como la previsión de eventos futuros, este sistema fortalece la planificación estratégica y la resiliencia de la comunidad. La adopción de este enfoque avanzado marca un avance crítico hacia un paradigma proactivo y basado en datos en la preparación y respuesta ante emergencias.
Nuevas tecnologías y su impacto en el sistema de salud
Dr. Carlos Alberto Díaz
Profesor Asociado en la Universidad ISALUD.
El futuro del sistema de salud argentino enfrenta un proceso de transformación en múltiples dimensiones: económica, política, social y sanitaria. Aunque la dirección de este cambio no está completamente clara, lo que sí es evidente es que nada será como antes. En la gestión actual de la salud, se observan tendencias que, en un contexto de estabilidad económica y crecimiento sostenido, podrían llevar al fortalecimiento de sectores como el extractivo y financiero, emulando ejemplos de países en vías de desarrollo avanzado como Australia.
Estas tendencias, predominantes en el mundo occidental, plantean preocupaciones relacionadas con la solidez de las políticas estatales y la fortaleza de las democracias y sus instituciones. En la era del conocimiento, el acceso a datos e información adquiere un valor estratégico, generando disputas y conflictos por hegemonía global, especialmente en el contexto de la transición energética y el agotamiento de los combustibles fósiles.
Hacia un modelo de excelencia en salud
Las tendencias en salud deben orientarse hacia la excelencia en la atención, mejorando la accesibilidad, la medicina basada en el valor y la centralidad del paciente, con el objetivo de mejorar la calidad de vida y extender los años saludables. Las soluciones tecnológicas, como los sistemas de información, los dispositivos de diagnóstico de precisión, y los algoritmos de análisis de datos, permitirán tratamientos personalizados adaptados a las necesidades individuales.
Estos avances, impulsados por tecnologías disruptivas, están transformando los modelos de atención, optimizando la eficiencia, efectividad, calidad y sostenibilidad del sistema de salud. Empresas líderes como Microsoft, Google, Amazon y Meta están entrando en este sector debido al alto valor estratégico de los datos generados por los sistemas de salud, marcando una nueva era de competencias y negocios.
Retos y oportunidades
A pesar del optimismo, existen riesgos inherentes si no se implementan políticas que mejoren la calidad de los servicios, la eficiencia y el acceso equitativo. La transformación requiere adoptar avances en digitalización, robótica, inteligencia artificial y aprendizaje profundo. Además, es fundamental rediseñar paradigmas de gestión para enfocarse en modelos de atención continua, regionalización y fortalecimiento de la atención primaria.
La evolución debe comenzar en el sistema político, con liderazgo y financiamiento adecuados, fortaleciendo la gestión de las instituciones y mejorando la experiencia del paciente en cada etapa de su recorrido por el sistema de salud. Es imperativo abandonar la actitud pasiva y adoptar un enfoque proactivo en áreas clave como la detección temprana de enfermedades crónicas, la promoción de hábitos saludables y la gestión efectiva de patologías prevalentes.
Gestión y planificación estratégica
La gestión de la salud es un ciclo recursivo que abarca planificación, ejecución, comunicación, coordinación, control, evaluación y participación. La implementación de sistemas de información avanzados, junto con el uso de evidencia científica y conocimientos independientes, resulta indispensable. Los gestores de salud deben poseer habilidades para liderar y tomar decisiones basadas en datos confiables, entendiendo que toda acción en el presente tiene un impacto en el futuro.
La colaboración entre los niveles macro, meso y micro es esencial para garantizar que los ciudadanos reciban atención segura, efectiva y centrada en sus necesidades. Modelos de gestión deben incluir componentes como recolección y análisis de datos, presupuestación, estrategias de financiamiento y cobertura, así como digitalización y mejora continua de los procesos de atención.
Financiamiento y equidad
En Argentina, coexisten varios modelos de financiamiento: el modelo Bismarck, basado en contribuciones de trabajadores y empleadores; el modelo Beveridge, que asegura cobertura universal financiada por impuestos; y un modelo liberal que atiende a un pequeño segmento a través de contratos privados. Sin embargo, esta coexistencia genera superposiciones, inequidades y anarquía organizativa, exacerbadas por la inflación y la desigualdad en el acceso a servicios.
Es necesario redefinir la «universalidad» del sistema, abordando las desigualdades y asegurando un acceso equitativo basado en principios de solidaridad y regionalización. Esto implica no solo garantizar financiamiento adecuado, sino también definir estructuras claras para la distribución de recursos, establecer prioridades y diseñar planes estratégicos que involucren tanto al sector público como al privado.
Conclusión
El sistema de salud argentino enfrenta desafíos complejos que requieren un enfoque integral y transformador. La incorporación de tecnologías innovadoras, junto con una gestión estratégica orientada a la equidad y sostenibilidad, es esencial para construir un sistema más eficiente y centrado en las personas. Solo a través de un liderazgo comprometido y una colaboración efectiva entre todos los actores, será posible avanzar hacia un sistema de salud que responda a las necesidades del siglo XXI.
Grandes modelos de Lenguaje y la historia clínica electrónica

Introducción
En los últimos años, ha crecido el interés por desarrollar sistemas de inteligencia artificial (IA) que mejoren la prestación de servicios de salud y los resultados médicos mediante el uso de registros médicos electrónicos (EHR). Un paso clave en este proceso es la extracción y captura de las características de los pacientes a partir de EHR longitudinales. Cuanta más información tengamos sobre los pacientes, más efectivos serán los sistemas de IA médica que podamos diseñar.
En las últimas décadas, los hospitales y centros médicos de Estados Unidos han adoptado rápidamente los sistemas EHR, lo que ha generado enormes almacenes de datos electrónicos de pacientes. Estos datos incluyen tanto información estructurada (como códigos de enfermedades y medicamentos) como no estructurada (por ejemplo, narrativas clínicas en notas de progreso). Aunque la documentación clínica basada en datos estructurados ofrece ventajas importantes, su adopción se enfrenta a barreras como la carga adicional para los médicos. Por esta razón, las narrativas clínicas siguen siendo ampliamente utilizadas por los profesionales de la salud como una forma práctica de registrar información detallada sobre los pacientes, desde antecedentes familiares hasta determinantes sociales de la salud.
El creciente interés en aprovechar la información detallada contenida en las narrativas clínicas ha impulsado el desarrollo de sistemas de IA médica que mejoran los modelos de diagnóstico y pronóstico. Sin embargo, las narrativas en texto libre presentan desafíos, ya que no pueden integrarse fácilmente en modelos computacionales que requieren datos estructurados. Para abordar este problema, los investigadores han recurrido al procesamiento del lenguaje natural (PLN) como una tecnología esencial para interpretar el lenguaje clínico utilizado en la atención médica.
Actualmente, las soluciones de PLN se basan principalmente en modelos de aprendizaje profundo, que emplean arquitecturas de redes neuronales. Inicialmente, las redes neuronales convolucionales (CNN) y las redes neuronales recurrentes (RNN) se aplicaron en este ámbito. Más recientemente, las arquitecturas basadas en transformadores, como BERT (Bidirectional Encoder Representations from Transformers), han establecido un nuevo estándar en el procesamiento del lenguaje natural. Estos modelos, implementados con mecanismos de autoatención, han alcanzado un rendimiento sobresaliente en tareas como reconocimiento de entidades nombradas, extracción de relaciones, inferencia de lenguaje natural y respuesta a preguntas.
El entrenamiento de modelos de transformadores suele dividirse en dos etapas: preentrenamiento del modelo de lenguaje (utilizando grandes corpus de texto sin etiquetar) y ajuste fino (aplicando el modelo preentrenado a tareas específicas con datos etiquetados). Esta estrategia de aprendizaje por transferencia permite resolver múltiples tareas de PLN a partir de un modelo base. Estudios recientes han demostrado que los transformadores grandes entrenados con datos masivos superan a los modelos anteriores en términos de precisión y versatilidad, lo que ha generado un interés creciente en desarrollar modelos más robustos y escalables.
En el ámbito biomédico, se han desarrollado modelos como BioBERT y PubMedBERT utilizando literatura científica, mientras que ClinicalBERT ha sido entrenado con narrativas clínicas. Sin embargo, la escalabilidad de los modelos en este dominio sigue siendo limitada debido a la sensibilidad de los datos clínicos y los altos requerimientos computacionales. En este contexto, surge GatorTron, un modelo de lenguaje clínico desarrollado utilizando más de 90 mil millones de palabras provenientes de notas clínicas anonimizadas, artículos de PubMed y Wikipedia.
En este estudio, entrenamos a GatorTron desde cero y evaluamos el impacto de aumentar la cantidad de parámetros y datos en su desempeño en tareas de PLN. Probamos tres versiones del modelo: uno base con 345 millones de parámetros, otro mediano con 3.9 mil millones y un modelo grande con 8.9 mil millones. Además, comparamos estos modelos con transformadores existentes en tareas clínicas como reconocimiento de entidades nombradas, extracción de relaciones médicas, inferencia de lenguaje natural y respuesta a preguntas médicas. Nuestros resultados muestran que GatorTron supera consistentemente a otros modelos en estas tareas, demostrando el potencial de los transformadores grandes en el ámbito clínico.
Resultados
Analizamos más de 290 millones de notas clínicas de aproximadamente 2.5 millones de pacientes provenientes del Repositorio de Datos Integrados de UF Health, acumuladas entre 2011 y 2021. Tras la desidentificación y el preprocesamiento, el corpus final incluyó más de 82 mil millones de palabras médicas.
El entrenamiento del modelo GatorTron-large requirió seis días en 992 GPU A100, empleando la arquitectura de clúster NVIDIA SuperPOD. Observamos que los modelos más grandes convergieron más rápidamente, consistente con investigaciones previas. Además, nuestros experimentos revelaron mejoras notables en tareas como extracción de conceptos clínicos, inferencia del lenguaje natural y respuesta a preguntas al incrementar el tamaño de los modelos.
Discusión
Los resultados de este estudio demuestran las ventajas de los modelos de transformadores grandes en el ámbito clínico. GatorTron no solo supera a los modelos existentes, sino que también ofrece un mejor desempeño en tareas complejas que requieren comprender y analizar narrativas clínicas detalladas. Estas capacidades pueden integrarse en sistemas de IA médica para mejorar la atención al paciente, la toma de decisiones clínicas y la farmacovigilancia.
En trabajos futuros, planeamos optimizar GatorTron para manejar fragmentos largos de texto y abordar las limitaciones observadas en tareas complejas. Creemos que este modelo representa un paso significativo hacia el desarrollo de sistemas de IA médica más avanzados y efectivos.
Las nuevas tecnologías deberían transformar el sistema de salud.
Dr. Carlos Alberto Díaz. Profesor Titular Universidad ISALUD. [1]
No sabemos claramente cuál será la dirección del proceso de transformación de la argentina en materia económica, política, social y de salud, son un conjunto de interrogantes, pero nada, será como antes. En la gestión de salud actual, existen algunas tendencias que por un lado si el país se estabiliza económicamente y crece durante varios años se producirá un crecimiento del sector extractivo y financiero, siguiendo la corriente que acontece en los países serios en la búsqueda del desarrollo como Australia u otros.
Estas tendencias son hegemónicas en el mundo occidental, pero con preocupantes acciones vinculadas a la solidez de las políticas de estado y a la fortaleza de las democracias y sus instituciones.
El posicionamiento en esta era del conocimiento produce un interés por el acceso a los datos, la información, para su utilización con cualquier fin, que llevará a nuevas disputas y guerras por la hegemonía expansionista en el planeta, y por los últimos estertores de los combustibles fósiles como el gas y el petróleo, que no encuentran un verdadero sustituto.
Estas tendencias sanitarias radicarán también en la excelencia en la atención, la mejora en la accesibilidad, la medicina basada en el valor, y centrada en el paciente, para darle más vida a los años.
La transformación tecnológica estará basada en los nuevos sistemas de información, de monitoreo, seguimiento, los dispositivos de diagnóstico de precisión, la interpretación y algoritmos de los datos que provengan de las personas en su contacto con el sistema de salud y nuevas formas tratamiento personalizado, no de talla única, como la creación de soluciones basadas en el conocimiento, la aplicación de los datos, su interpretación, el aprendizaje constante, serán claramente superiores en cuanto a resultados y a los pacientes, y una adaptación activa a las exigencias del entorno, a la mayor longevidad de la población. Estos cambios se aceleran por la adopción de nuevas tecnologías, procesos y modelos de atención, para mejorar la eficiencia, la efectividad, calidad y sostenibilidad del sistema de salud.
No es algo que ocurrirá solo en un instante, en el próximo año, pero si será vertiginoso y sin acostumbramientos, por un descubrimiento, o una tendencia macroeconómica solamente, es una competencia con inversiones sustantivas de los grandes jugadores del mercado. Porque muchos de estos avances están bajo el influjo de los intereses de las Megaempresas, como Microsoft, Google, Amazon, Baidu, Nvidia, Salesforce CRM, Meta e IBM que también se están introduciendo en los sistemas de salud, ya que la minería de sus datos es muy valioso y valorado, un nuevo y jugoso negocio para quién lo posea, almacene y lo revenda.
Sin embargo, a pesar del optimismo con estas alternativas siempre se puede estar peor, Especialmente si los que caen el pozo no dejan de excavar y empeorar las cosas, esos somos nosotros, añorando un pasado que no fue mejor. Tambien se puede estar mejor, pero para ello hay que realizar políticas para lograr la mejora en la calidad prestacional, la eficiencia, el acceso a la salud, la desinversión, una medicina o gestión sanitaria de las seis P, e incorporar los avances en la digitalización, en el manejo de la información, la robótica y el aprendizaje profundo.
Se debe avanzar en mejorar la salud de la población en forma sostenible y cambiar varios de los paradigmas que han trazado la gestión hasta el momento, del modelo episódico de atención solo de la patología aguda por otro de gestión de la enfermedad, de red, de regionalización, de acceso a la atención primaria, de contención de la inflación en salud, de cambios en la política tributaria del sector, de formar el recurso humano necesario y distribuirlo mejor, de no usarlo como variable de ajuste, de la continuidad de atención. En la micro con el desarrollo de las áreas específicas de microsistemas de atención en todos los niveles.
La evolución tiene que empezar en el sistema político con la rectoría, el presupuesto y la financiación, en la meso, con el fortalecimiento de la gestión de los establecimientos y la evolución en las transiciones de los recorridos de los pacientes en el sistema, que se abandone la actitud pasiva de esperar la demanda para avanzar en un concepto más proactivo de cubrir las brechas en la detección y tamizaje del cáncer de cuello uterino, en la detección y manejo no farmacológico del paciente diabético, en los cambios de hábitos de vida saludables en relación al sedentarismo, la hipercolesterolemia y control de la hipertensión arterial.
La gestión sanitaria es un ciclo recursivo compuesto por la planificación, la ejecución, la comunicación, la coordinación, el control, la evaluación, la dirección participativa, todos sus aspectos se potencian, dejan mejoras que van haciendo subir algunos peldaños.
Es imperioso el uso de sistemas de información, las nuevas tecnologías de análisis de los datos y la comunicación efectiva, asertiva, del conocimiento independiente, de la evidencia científica.
Los que realizan gestión sanitaria deben entender que es una disciplina crítica en la actualidad, que se ocupa de dirigir y coordinar los recursos, la instalación adecuada de habilidades y competencias para asegurar la mejor relación de agencia posible. Implica una variedad de funciones gerenciales y acciones, con el concepto central que la gestión no se stockea, que siempre hay que ejercer presencia, liderazgo, caminar, tener información confiable para tomar decisiones en el corto plazo para lograr el futuro deseado, entendiendo que no hay decisiones de corto plazo, todo lo que hacemos impacta en el futuro que queremos, pero que tendremos que construir. Los tres niveles de la gestión son muy importantes, complementarios, sinérgicos y hacen que al final la evolución llegue a los ciudadanos. Los gestores deben asegurar que los pacientes reciban una atención segura, eficaz, y centrada en las necesidades.
Los tres niveles Macro-Meso- Micro, deben colaborar y trabajar para un objetivo común. Con una colaboración entre las diferentes entidades y profesionales de la salud.
Modelos de gestión sanitaria:
Existen varios modelos de gestión sanitaria, que se deben caracterizar por abordar los siguientes componentes: la recaudación, la presupuestación, la financiación y la cobertura. Los sistemas de pago como incentivos apropiados. Los salarios como reconocimiento de los colaboradores. Las estrategias de atención integradas. La planificación, la organización y la estructura. Los procesos de atención. La gestión de los pacientes, los accesos, la gestión de los recursos de diagnóstico y tratamiento. La digitalización. El análisis de la información, la gestión de la calidad, la seguridad, las guías clínicas y la mejora continua. También se debe establecer el enfoque o la dirección principal de las decisiones y las acciones.
En esa pormenorización define los valores (solidaridad, universalidad, equidad, integración, regionalización y fortalecimiento del recurso humano), las prioridades (asegurar el acceso, basado en la atención primaria), las metas para abordar los desafíos y como lograremos los objetivos (ejecución, conveniencias de pago y formas de ejecución). Estos componentes de la gestión, tanto en el financiamiento, la organización y la estructura, mejora en los procesos de atención, de la calidad, entre otros, interactúan y se combinan en los diferentes niveles de gestión.
La financiación sola se demuestra que no alcanza, hay que recaudar lo suficiente para prestar lo que se señala como canasta de prestaciones, fijar un presupuesto, establecer que se cubre, como se lo hace, a quién, cómo, con que estructuras.
En suma, la financiación no solo es juntar dinero, sino la forma que se recaudan y se distribuyen los recursos económicos y que tenemos que lograr con ellos. Que hay que hacer, que resultados se esperan, en que tiempo, con que estructura. Que nos proponemos como viable. Definir si se va a modificar algo en los sistemas de presupuestación de los hospitales y de compras. Cuales quedarán como establecimientos nacionales y cuales provinciales en primer lugar. Luego que le pediremos en cuanto a su área de influencia y programática. Que incentivaremos para que logren en función de factores de la producción, la utilización y la calidad, también involucrar en los sistemas de información al ámbito privado y de las entidades sin fines de lucro. Que se les pedirá a los integrantes de las empresas prestadores de salud, en cuanto a vacunación, listas de espera, cobertura de la prevención, del manejo de los hipertensos, diabéticos, con insuficiencia renal incipiente, en pacientes con EPOC, en el screening de los principales cánceres, la mayor libertad de los individuos se logra cuando tienen salud, será un factor fundamental para el logro del incremento del producto bruto interno. Disminuir la burocracia, como se organiza la atención, la asignación de roles y responsabilidades. Generar un marco para el desarrollo de los planes estratégicos.
En Argentina, coexisten varios modelos de gestión, en cuanto a la financiación existe el modelo bismarkiano, donde los fondos para la atención de los pacientes están basados en la contribución de los trabajadores y los aportes de los empleadores, instancia que claramente esta relacionada con el poder adquisitivo de los salarios, con dos factores que afectan esta fuente de financiamiento que son por un lado la perdida de los salarios con respecto a la inflación que anualizado es cercana a los siete puntos porcentuales. Que además hay una inflación en la salud cuya causalidad es múltiple, pero que existen varios factores causales. Algunos se pueden gestionar. Otros No. O que son por el momento complejos de gestionar. Pero todos, todos podemos mejorar. Este análisis de la inflación en salud afecta al sector de obras sociales, a las prepagas y a los Ministerios de salud.
El segundo modelo el Beveridge, vigente en Argentina de la cobertura universal basada en impuestos parcialmente transferida a las autonomías provinciales, pero que asegura que todos los ciudadanos pueden atenderse en cualquier hospital de la República.
Finalmente, modelo liberal o modelo de libre mercado con un pequeño grupo de contratos privados en el ámbito de la salud que es de un millón setecientos mil personas que corresponden a contratos privados atendidos por las prepagas. Los otros afiliados a los sistemas de salud prepagos que tienen los ingresos más elevados y que realizaron la opción por alguna de estas entidades privadas derivando como parte de pago de su cuota de beneficiario, los aportes y contribuciones, que afecta a los salarios más alto produciéndose un descreme al sistema solidario de la seguridad social.
Como se observa y conocemos existe superposición de coberturas, anarquía organizativa, falta de planificación estratégica tradicional, con una eminente cuestión aspiracional de los ciudadanos por mejorar su estatus social de pasarse a un prepago.
No tendremos un sistema hasta no decidir como haremos para mejorar la “universalidad” tan fatalmente desigual e inequitativa, cristalizada por el poder de pago y el código postal.
[1] Médico Especialista en Medicina Interna, Terapia Intensiva, Nefrología y Salud Pública. Director de la Especialidad en Economía y Gestión de la Salud.
Future of Healthcare in Argentina: Innovations and Challenges
Dr. Carlos Alberto Díaz. Associate Professor at ISALUD University. [1]
We do not know clearly what the direction of the process of transformation of Argentina will be in economic, political, social and health matters, they are a set of questions, but nothing, it will be as before. In current health management, there are some trends that on the one hand if the country stabilizes economically and grows for several years, there will be a growth of the extractive and financial sector, following the current that occurs in serious countries in the search for development such as Australia or others.
These trends are hegemonic in the Western world, but with worrying actions linked to the soundness of state policies and the strength of democracies and their institutions.
Positioning in this age of knowledge produces an interest in access to data, information, for use for any purpose, which will lead to new disputes and wars for expansionist hegemony on the planet, and for the last throes of fossil fuels like gas and oil, which do not find a real substitute.
These health trends will also be based on excellence in care, improved accessibility, value-based medicine, and patient-centered, to give more life to the years.
The technological solutions, Theses on new information systems, monitoring, follow-up, precision diagnostic devices, the interpretation and algorithms of the data that come from people in their contact with the health system and new forms of personalized treatment, not one-size-fits-all, like the creation of knowledge-based solutions, The application of data, its interpretation, constant learning, will be clearly superior in terms of results and patients, and an active adaptation to the demands of the environment, to the greater longevity of the population. These changes are accelerated by the adoption of new technologies, processes, and care models to improve the efficiency, effectiveness, quality, and sustainability of the health system.
It is not something that will happen only in an instant, in the next year, but if it will be dizzying and unaccustomed, due to a discovery, or a macroeconomic trend only, it is a competition with substantial investments from the big players in the market. Because many of these advances are under the influence of the interests of Mega companies, such as Microsoft, Google, Amazon, Baidu, Nvidia, Salesforce CRM, Meta and IBM that are also being introduced into health systems, since the mining of their data is very valuable and valued, a new and juicy business for those who own it. store and resell it.
However, despite the optimism with these alternatives you can always be worse, especially if those who fall into the well do not stop digging and making things worse, that is us, longing for a past that was not better. You can also be better, but to do so you must make policies to achieve improvement in the quality of services, efficiency, access to health, divestment, medicine or health management of the six Ps, and incorporate advances in digitalization, information management, robotics and deep learning.
Progress must be made in improving the health of the population in a sustainable way and changing several of the paradigms that have been drawn up by the management so far, from the episodic model of care only for acute pathology to another of disease management, network, regionalization, access to primary care, containment of inflation in health, of changes in the sector’s tax policy, of training the necessary human resources and distributing them better, of not using them as an adjustment variable, of continuity of care. In the micro with the development of specific areas of microsystems of care at all levels.
The evolution has to start in the political system with stewardship, budget and financing, in the mismanagement, with the strengthening of the management of the facilities and the evolution in the transitions of the patients’ journeys in the system, that the passive attitude of waiting for demand to advance in a more proactive concept of covering the gaps in the detection and screening of cervical cancer is abandoned, in the detection and non-pharmacological management of diabetic patients, in changes in healthy lifestyle habits in relation to sedentary lifestyle, hypercholesterolemia and control of arterial hypertension.
Health management is a recursive cycle made up of planning, execution, communication, coordination, control, evaluation, participatory management, all its aspects are enhanced, leaving improvements that make you climb some steps.
The use of information systems, new technologies for data analysis and effective, assertive communication, independent knowledge and scientific evidence are imperative.
Those who perform health management must understand that it is a critical discipline today, which deals with directing and coordinating resources, the appropriate installation of skills and competencies to ensure the best possible agency relationship. It involves a variety of managerial functions and actions, with the central concept that management is not stocked, that it is always necessary to exercise presence, leadership, walk, have reliable information to make decisions in the short term to achieve the desired future, understanding that there are no short-term decisions, everything we do impacts the future we want, but that we will have to build. The three levels of management are very important, complementary, synergistic and in the end make the evolution reach the citizens. Managers must ensure that patients receive safe, effective, and needs-centered care.
The three levels, Macro-Meso-Micro, must collaborate and work towards a common goal. With a collaboration between the different entities and health professionals.
There are several models of health management, which must be characterized by addressing the following components: collection, budgeting, financing and coverage. Payment systems as appropriate incentives. Salaries as recognition of employees. Integrated care strategies. Planning, organization and structure. The processes of care. Patient management, access, management of diagnostic and treatment resources. Digitalization. Information analysis, quality management, safety, clinical guidelines and continuous improvement. The main focus or direction of decisions and actions must also be established.
In this detail, it defines the values (solidarity, universality, equity, integration, regionalization and strengthening of human resources), the priorities (ensuring access, based on primary care), the goals to address the challenges and how we will achieve the objectives (execution, payment conveniences and forms of execution). These components of management, both in financing, organization and structure, improvement in care processes, quality, among others, interact and combine at the different levels of management.
Financing alone is shown to be not enough, it is necessary to collect enough to provide what is indicated as a basket of benefits, set a budget, establish what is covered, how it is done, to whom, how, with what structures. In short, financing is not only about raising money, but also about the way in which economic resources are collected and distributed and what we have to achieve with them. What needs to be done, what results are expected, in what time, with what structure. That we propose as viable. Define if anything is going to be modified in the budgeting systems of hospitals and purchasing. Which will remain as national establishments and which provincial in the first place. Then we will ask you about your area of influence and programmatic. That we will encourage them to achieve based on factors of production, use and quality, also involve the private sector and non-profit entities in the information systems. That the members of the health provider companies will be asked to provide information about vaccination, waiting lists, prevention coverage, and the management of hypertensive patients, diabetics, those with incipient renal failure, in patients with COPD, in the screening of the main cancers, the greatest freedom of individuals is achieved when they are healthy, will be a fundamental factor in achieving an increase in the gross domestic product. Reduce bureaucracy, how care is organized, the assignment of roles and responsibilities. Generate a framework for the development of strategic plans.
In Argentina, several management models coexist, in terms of financing there is the Bismarck model, where funds for patient care are based on the contribution of workers and the contributions of employers, an instance that is clearly related to the purchasing power of wages, with two factors that affect this source of financing that are on the one hand the loss of wages with respect to inflation which annualized is close to seven percentage points. That there is also an inflation in health whose causality is multiple, but that there are several causal factors. Some can be managed. Others do not. Or that they are for the moment complex to manage. But we can all improve. This analysis of inflation in health affects the health insurance sector, the prepaid and the Ministries of Health.
The second model is the Beveridge, in force in Argentina of universal coverage based on taxes partially transferred to the provincial autonomies, but which ensures that all citizens can be treated in any hospital in the Republic.
Finally, the liberal model or free market model with a small group of private contracts in the field of health that is one million seven hundred thousand people that correspond to private contracts attended by the prepaid. The other affiliates of the prepaid health systems who have the highest incomes and who made the option for one of these private entities deriving as part of the payment of their beneficiary quota, the contributions and contributions, which affects the highest salaries, producing a skim to the solidarity system of social security.
As can be seen and known, there is overlapping coverage, organizational anarchy, lack of traditional strategic planning, with an eminent aspirational issue of citizens to improve their social status by switching to a prepaid plan.
We will not have a system until we decide how we will improve the «universality» so fatally unequal and inequitable, crystallized by the power of payment and the postal code.
[1] Specialist in Internal Medicine, Intensive Care, Nephrology and Public Health. Director of the Specialty in Economics and Health Management.
Crisis Médica en Argentina: Medidas y Lecciones de Huelgas Globales
Autores : Tarun Ramesh , BS , Carmel Shachar , JD, MPH, y Hao Yu , Ph.D.
La república Argentina, esta viviendo una crisis profunda en su sistema de salud, uno de los problemas más acuciantes es la crisis de recursos humanos, la falta de reconocimiento, los problemas de pauperización en la profesión, el desprestigio y la calidad médica, sin respuesta por parte de las autoridades, porque «no hay plata». Que afecta al elemento más diferenciador en un modelo de atención basado en el valor. Por ello traigo este artículo de New England de esta semana, en como los médicos en otros países están defendiendo sus derechos. El problema con la prestación de salud es también económico, de falta de carrera profesional, de reconocimiento y de organización, pero fundamentalmente de remuneración y de un sistema previsional que le permita al médico vivir y no como en la actualidad un menesteroso, porque esto lleva al multiempleo y a edades inadecuadas, y a un costo de oportunidad de no poder mantenerse actualizado, de trabajar en lugares donde se formen en educación continua, de atención centrada en el paciente y el pago basado en el valor: de controlar la hipertensión, bajar la hipercolesterolemia, diagnostico precoz del cáncer, manejo adecuado del dolor, de la depresión, de los problemas ventilatorios, de la insuficiencia cardíaca crónica congestiva, de la diabetes, de la gestión de la enfermedad crónica de disminuir las internaciones, aumentar la prevención y personalizar la atención.

Desde febrero de 2024, más de 12.000 médicos residentes de Corea del Sur (el 80% de todos los residentes) han estado en huelga en protesta por una nueva política gubernamental diseñada para aumentar las admisiones a las escuelas de medicina, que según afirman no aborda sus preocupaciones sobre los bajos salarios y las malas condiciones de trabajo. A los residentes finalmente se les unieron médicos asistentes y estudiantes de medicina. La huelga, una de las huelgas médicas más grandes y prolongadas en la historia del país, ha provocado retrasos sustanciales en las cirugías, otros procedimientos médicos y admisiones hospitalarias.De manera similar, en enero de 2024, los médicos residentes del Reino Unido se declararon en huelga durante seis días debido a las escasas remuneraciones; la huelga fue la más grande en la historia del Servicio Nacional de Salud. En octubre de 2023, los médicos de atención primaria de Francia iniciaron una huelga para exigir tarifas más altas por las consultas médicas generales. En Estados Unidos, los médicos de urgencias de Detroit se declararon en huelga en abril de 2024 debido a los largos tiempos de espera y la escasa dotación de personal; en septiembre de 2024, más de 800 residentes y becarios de la Universidad de Buffalo iniciaron una huelga de cuatro días para exigir mejores remuneraciones y condiciones de trabajo, los mismos objetivos que perseguían en una huelga en mayo de 2023 de más de 150 residentes de un hospital de Nueva York afiliado a la Escuela de Medicina Icahn en el Monte Sinaí.
Entre los países de la Organización para la Cooperación y el Desarrollo Económicos, Corea del Sur y los Estados Unidos tienen algunos de los números más bajos de médicos por cada 1.000 habitantes. Por lo tanto, la negociación colectiva y las huelgas podrían tener mayores efectos en estos países que en otros. En medio de la reciente actividad huelguística, los responsables de las políticas estadounidenses podrían incorporar las lecciones de otros países para equilibrar mejor los derechos de negociación colectiva de los médicos y las protecciones de los pacientes. El tratamiento de los empleados de hospitales bajo la ley laboral estadounidense ha sido complejo e inconsistente.
La Ley Nacional de Relaciones Laborales (NLRA, por sus siglas en inglés) de 1935 originalmente cubría a los empleados de todos los hospitales no gubernamentales; fue enmendada por la Ley Taft-Hartley en 1947 para excluir a los empleados de hospitales sin fines de lucro. Las Enmiendas de Atención Médica de 1974 a la NLRA restablecieron la cobertura de la ley laboral a los empleados de hospitales sin fines de lucro. También consagraron el derecho de huelga para algunos trabajadores de la salud de Estados Unidos y exigieron que los sindicatos avisaran con 10 días de anticipación antes de una huelga en cualquier institución de atención médica. 1
Posteriormente, la Junta Nacional de Relaciones Laborales (NLRB, por sus siglas en inglés) determinó que los residentes médicos pueden formar sindicatos, pero los médicos asistentes están excluidos de las protecciones legales relacionadas con los sindicatos si son contratistas independientes en lugar de empleados, si ejercen la profesión privada, si son profesores titulares o en vías de permanencia, o si supervisan a otros empleados (la supervisión médica de enfermeras no califica para este propósito). 1,2La legislación antimonopolio se ha aplicado a la organización laboral de los médicos desde que la Comisión Federal de Comercio emprendió acciones coercitivas contra la Asociación Médica Estadounidense (AMA) en 1979, basándose en las teorías de que todos los médicos independientes compiten entre sí y que la organización laboral podría dar lugar a un comportamiento anticompetitivo. Algunas leyes estatales pueden proporcionar protecciones adicionales a las establecidas por las políticas federales para los empleados que recurren a la negociación colectiva o participan en huelgas. Históricamente, los médicos estadounidenses —especialmente en comparación con las enfermeras— no han hecho huelgas, pero las normas pueden cambiar considerablemente en los próximos años, debido al aumento de la insatisfacción laboral entre los médicos y al auge de los sindicatos de médicos en formación. En las últimas dos décadas, los médicos han expresado una creciente frustración por las elevadas cargas de trabajo, las remuneraciones relativamente bajas y el deterioro de las condiciones laborales, así como su malestar por la financiarización del sector de la salud estadounidense, incluida la priorización de las ganancias por sobre la calidad de la atención clínica. 1La sindicalización y la consiguiente autoridad para la negociación colectiva entre los médicos residentes ofrecen a los residentes y becarios una vía legal para contrarrestar las prioridades distorsionadas y abogar por mejores condiciones de trabajo y mayores remuneraciones. La sindicalización también ofrece otra vía para ejercer el poder durante las negociaciones de los contratos: la acción industrial, incluidas las huelgas. Por otra parte, la sindicalización puede estar asociada a posibles desventajas, como mayores costos sociales de la atención médica, pérdida de autonomía para los médicos individuales y la creación de desigualdades entre los médicos empleados y los independientes. Las alternativas a los sindicatos de médicos, incluidos los comités de personal médico, que están compuestos por líderes clínicos que apoyan el bienestar del personal y plantean cuestiones a la dirección del hospital, pueden permitir que los médicos empleados tengan una voz colectiva en ausencia de sindicalización. Los médicos en formación de más de 60 programas de Estados Unidos se han sindicalizado. 3 Con el creciente interés en la sindicalización entre otros médicos, aumentará el potencial de acciones sindicales en el sistema de salud de Estados Unidos. Se podrían actualizar las leyes y regulaciones para reflejar mejor las realidades de la atención médica moderna e incorporar las mejores prácticas de otros países. Aunque las huelgas de médicos plantean importantes preocupaciones éticas sobre el potencial daño a los pacientes, especialmente en zonas donde escasean los médicos, pocos estudios han examinado esos efectos. Una revisión sistemática y un metaanálisis de 14 estudios de 10 países no encontraron diferencias significativas en la mortalidad hospitalaria entre los períodos de huelga y los de no huelga. 4 Una revisión exploratoria encontró una disminución de las cirugías electivas y un aumento de las cancelaciones de citas ambulatorias durante las huelgas. 5Para hacer frente a las preocupaciones sobre los posibles daños asociados a las huelgas de médicos, los responsables de las políticas de muchos países han tomado medidas para proteger a los pacientes. Aunque los sistemas de atención de la salud de estos países difieren del de los Estados Unidos, sus experiencias podrían ofrecer lecciones útiles. Por ejemplo, Francia, Italia, Irlanda y España han aplicado políticas que exigen a los empleadores y empleados establecer un nivel mínimo de personal antes de una huelga de atención de la salud, y el Reino Unido ha considerado recientemente la posibilidad de introducir niveles mínimos de personal. Esas políticas están en consonancia con las de la Organización Internacional del Trabajo (OIT), un organismo de las Naciones Unidas que ayuda a establecer normas laborales. La OIT apoya el uso de niveles mínimos de servicio cuando las huelgas puedan interrumpir los servicios de manera que “pongan en peligro la vida, la seguridad personal o la salud… de la población”.
El aviso legal de 10 días para las huelgas contra instituciones de atención médica en los Estados Unidos tiene por objeto proporcionar un período de “reflexión” y dar a la institución tiempo para tomar medidas para salvaguardar la atención al paciente. Añadir un nivel mínimo de servicio requerido por ley podría proteger aún más a los pacientes, abordar las preocupaciones de algunos médicos de que la huelga entra en conflicto con su deber ético de brindar atención y proteger contra posibles acusaciones de abandono de pacientes por parte de las juntas médicas estatales.
También se podrían tomar medidas proactivas para evitar acciones punitivas contra los médicos asistentes o en formación que estén en huelga. La ley de Corea del Sur permite penalizar (mediante la suspensión de la licencia médica, multas o incluso el encarcelamiento) a los médicos que se nieguen a cumplir las órdenes gubernamentales de volver al trabajo. Durante la huelga de residentes, el gobierno de Corea del Sur comenzó a suspender las licencias de los médicos en formación que estaban en huelga, pero dio marcha atrás tras la protesta pública. Esas acciones punitivas pueden dañar las relaciones entre empleados y empleadores, socavar la confianza pública en el sistema médico y comprometer las condiciones de trabajo de los médicos, lo que exacerba el agotamiento y la insatisfacción laboral. Según los códigos laborales de la OIT, los trabajadores “no deben ser despedidos por participar en una huelga”, y una huelga legal no termina un contrato existente, sino que lo suspende hasta que se proceda a la negociación.Aunque la discriminación contra los empleados debido a actividades o simpatías sindicales se considera una práctica laboral injusta según la NLRA, los médicos en formación que participan en tales actividades son más vulnerables que otros médicos a sufrir daños relacionados con su carrera porque están en proceso de obtener la licencia y la certificación del colegio. Los colegios médicos estatales podrían garantizar que los cargos legales asociados con las actividades sindicales no afecten las decisiones sobre la concesión de la licencia. De manera similar, las sociedades profesionales podrían garantizar que las actividades relacionadas con los sindicatos no pongan en peligro la elegibilidad o la certificación del colegio. La AMA, que apoya el derecho de los médicos a sindicalizarse pero desalienta las huelgas de médicos, 2 podría proporcionar orientación actualizada y más específica a los médicos en formación sobre los beneficios y riesgos asociados con la huelga. Por último, el Congreso y la NLRB podrían revisar la elegibilidad de los profesores de medicina y los médicos supervisores para sindicalizarse. En una era de creciente corporativización y consolidación de hospitales, los médicos asistentes tienen menos control sobre sus horarios y su práctica. 1
En los grandes sistemas de atención médica, donde los administradores pueden impulsar la toma de decisiones, los sindicatos pueden ser un contrapeso importante que proteja los intereses de los empleados. Las políticas laborales podrían actualizarse para reflejar mejor las tendencias actuales y alinearse más estrechamente con las políticas de España, Francia y el Reino Unido que permiten a los médicos supervisores hacer huelga. Al modernizar las leyes laborales y las regulaciones de huelga, en parte aprendiendo de otros países, los responsables de las políticas estadounidenses podrían apoyar mejor a los médicos, los pacientes y los hospitales en tiempos de agitación.
La salud en la era de la desinformación
La desinformación sanitaria (datos falsos o engañosos compartidos involuntariamente) y la desinformación (información deliberadamente engañosa) no son nuevas, pero la pandemia de COVID-19 marcó un punto de inflexión. La sensación de ansiedad y urgencia, junto con el aumento del uso de las redes sociales y las interpretaciones políticamente cargadas de la pandemia, fomentaron la difusión de una serie de afirmaciones engañosas sobre el virus y las contramedidas médicas. La desinformación sanitaria se utilizó como propaganda, explotando el miedo, socavando la confianza pública y obstaculizando la acción colectiva en momentos críticos. Hoy en día, el contenido engañoso de las redes sociales impregna la información sobre la prevención y el tratamiento del cáncer; puede llevar a los pacientes a abandonar los tratamientos basados en la evidencia en favor de alternativas respaldadas por personas influyentes; minimiza la gravedad de las condiciones de salud mental; y promueve suplementos no regulados que afirman funcionar para todo, desde la pérdida de peso hasta la reversión del envejecimiento. La desinformación se ha convertido en un instrumento deliberado para atacar y desacreditar a científicos y profesionales de la salud con fines políticos. Los efectos son destructivos y perjudiciales para la salud pública.
La sensación de que las empresas tecnológicas no se están tomando suficientemente en serio esta amenaza se ejemplifica con la reciente decisión de Meta de poner fin a la verificación de hechos. Facebook (al igual que otras redes sociales) ya era una fuente importante de desinformación sobre la salud, pero aunque la verificación de datos no puede eliminar por completo el material inexacto, marca la diferencia, y su eliminación abre las compuertas para el contenido dañino. Debido a que la desinformación a menudo se propaga más rápido que los hechos, es esencial que los hechos se transmitan de una manera que no deje espacio para malas interpretaciones. El anuncio de Mark Zuckerberg es parte de una tendencia de revertir la supervisión que puede dejar la impresión de que la batalla sobre los hechos se está perdiendo. Xavier Becerra, quien dirigió el Departamento de Salud y Servicios Humanos de Estados Unidos, dice que las agencias federales se ven superadas por la «información y desinformación instantáneas».
Sin embargo, también ha habido esfuerzos positivos. Australia tiene la intención de introducir fuertes multas para las plataformas que no impidan la difusión de información errónea. La Comisión Europea ha publicado recomendaciones para abordar la desinformación sobre la COVID-19 a través de intervenciones conductuales específicas. La OMS ha tomado medidas para fomentar la comunicación responsable de la información sanitaria y señalar los contenidos engañosos. Las redes sociales pueden ser una fuerza para el bien, y hay personas que trabajan para educar al público de manera creativa y efectiva.
Luchar contra la desinformación no es tan simple como corregir los hechos; También implica abordar la manipulación intencionada y la forma en que los algoritmos dirigen la atención de las personas, dejando que las personas naveguen solas por una compleja mezcla de ciencia y ficción. El contenido generado por inteligencia artificial (IA) presenta desafíos cada vez mayores, pero la IA también puede ayudar a señalar el contenido sin base científica, aunque no puede reemplazar enseñar a las personas cómo verificar los hechos e identificar fuentes creíbles. La lucha contra la desinformación requiere un enfoque sistemático similar a frenar la propagación de agentes infecciosos: encontrar y contener la fuente; identificar de manera proactiva a los más vulnerables a sus efectos; e inmunizar a la población contra las falsas afirmaciones proporcionando recursos educativos claros. No puede dejarse a esfuerzos voluntarios e individuales.
La Investigación COVID-19 del Reino Unido ha publicado esta semana su registro Every Story Matters sobre las experiencias del público con el desarrollo y la implementación de vacunas y terapias contra la COVID-19. En conjunto, los testimonios subrayan no solo el valor de la información precisa, sino también la importancia central de la confianza y las respuestas emocionales, desde la esperanza y el alivio hasta el escepticismo y la ansiedad, durante las crisis de salud pública. Es esencial comprender y cambiar las narrativas que influyen negativamente en las decisiones de salud como determinantes emocionales de la salud. En lugar de limitarse a simplificar hechos complejos, los gobiernos y los comunicadores científicos deben esforzarse por garantizar que los mensajes de salud pública sean pertinentes para el individuo; no solo para proporcionar información precisa, sino también para fomentar un ambiente de confianza y comprensión, y para reconocer las áreas de incertidumbre e incógnitas. La comunidad médica también tiene un papel clave, a través de los comentarios, la investigación y la defensa. The Lancet se compromete a apoyar estos esfuerzos abordando de manera proactiva y, si es posible, previniendo la información errónea y la desinformación que se deriva de nuestras publicaciones.
La información errónea y la desinformación ya no pueden verse simplemente como una molestia académica, sino como una amenaza social. Solo si reconocemos esa amenaza y actuamos de manera proporcionada, podremos responder al peligro y combatir la marea de información errónea y desinformación que tiene el potencial de socavar gravemente la salud pública.
Trump y la Industria de Seguros de Salud: Un Momento de Ajuste de Cuentas
Citar esto como: BMJ 2025; 388:R87 Rebecca Coombes, rcoombes@bmj.com
La próxima semana el presidente electo de Estados Unidos, Donald Trump, asumirá el cargo con el mandato de realizar cambios radicales en el enfoque del gobierno hacia la medicina y la salud pública.

La cobertura del seguro de salud, en particular, se enfrenta a una reforma masiva y potencialmente dañina (doi:10.1136/bmj.q2801). Los republicanos en Washington planean reducir Medicaid, el programa para personas de bajos ingresos, lo que podría dejar a millones de estadounidenses sin seguro. El Medicare tradicional (para personas mayores de 65 años y personas con discapacidades) también podría reducirse hasta el punto de cubrir solo a una pequeña fracción de la población actual de Medicare.
Mientras tanto, la frustración pública con las aseguradoras ha sido evidente tras el asesinato de Brian Thompson, director ejecutivo de UnitedHealthcare (UHC) (doi:10.1136/bmj.q2879). 2 Ha expuesto la alta tasa de denegación de cobertura de seguro del gigante de la salud y la miseria que esto ha causado. El hecho de que Luigi Mangione, acusado del asesinato, dejara una nota en la que acusaba al sistema sanitario estadounidense de corrupción y codicia ha sido ampliamente difundido y reflejado en las redes sociales. La puesta en la picota de la UHC en el mes transcurrido desde el asesinato de Thompson, y la asombrosa falta de simpatía pública por el asesinato (en una encuesta reciente, el 41% de los jóvenes de 18 a 29 años consideraron que el asesinato era aceptable), es un momento de ajuste de cuentas para la industria.
El foco de esta falta de simpatía es la industria de los seguros, con UHC, la cuarta compañía más grande de los EE. UU., siendo un ejemplo particularmente atroz. Un cirujano, por ejemplo, fue retirado de una cirugía de cáncer por UHC para que se le preguntara si era médicamente necesario hospitalizarse. Ahora, los accionistas de UHC exigen conocer el costo humano de sus políticas (doi:10.1136/bmj.r64). 3 La pregunta clave es: ¿las prácticas de la empresa condujeron a la demora o el abandono del tratamiento médico y a eventos adversos graves para los pacientes?
Algunas de las opciones más radicales de Trump para puestos de alto rango en la salud estarán, si se confirman, al frente de las reformas (doi:10.1136/bmj.q2485). 4 Un pequeño ejército de 18.000 médicos hizo oír esta semana su oposición contra uno de esos elegidos por el gabinete (doi:10.1136/bmj.r60),5 Robert F. Kennedy Jr., que está previsto como nuevo secretario de Sanidad. Pidieron al Senado que rechazara la nominación, calificándola de «bofetada en la cara» para todos los profesionales de la salud. En el corazón de esto está el largo historial de Kennedy de difundir información errónea sobre la seguridad establecida de las vacunas, incluida la afirmación de que las vacunas causan autismo. También ha relacionado la violencia con armas de fuego en las escuelas con el uso de antidepresivos y ha promovido tratamientos desacreditados para el covid-19, como la hidroxicloroquina (doi:10.1136/bmj.q2791). 6
Por supuesto, los médicos tienen razón al pedir a la nueva administración estadounidense que priorice la ciencia y la medicina basada en la evidencia, pero no hay duda de que Trump heredará un sistema que puede permitir tratamientos caros pero de bajo valor, a menudo ineficaces (doi:10.1136/bmj.q2402). 7
Los recientes «premios Shkreli» ponen de relieve los peores ejemplos de especulación y disfunción en la sanidad estadounidense (doi:10.1136/bmj.r57). 8 Un ganador (o perdedor, según sea el caso) fue la compañía farmacéutica Amgen, que está vendiendo su medicamento contra el cáncer Lumakras en una formulación de dosis alta a pesar de un ensayo que muestra un beneficio similar con menos toxicidad a una dosis mucho más pequeña. Amgen, que perdería 180.000 dólares por paciente al año si cambiara a la dosis más baja, ha argumentado que la Administración de Alimentos y Medicamentos de Estados Unidos ya aprobó la dosis más alta. Los 10 ganadores de los premios Shkreli 2024, que se otorgan anualmente a los peores ejemplos de especulación y disfunción en la atención médica de EE. UU., han sido anunciados por el Instituto Lown, un grupo de expertos estadounidense sin fines de lucro.
Hay noticias más esperanzadoras para la salud pública: la última medida del cirujano general de los Estados Unidos de poner una advertencia sanitaria sobre las bebidas alcohólicas (doi:10.1136/bmj.r15),9 por ejemplo, y la propuesta de la FDA de etiquetar los oxímetros de pulso para todos los colores de piel (doi:10.1136/bmj.r59). 10 Las investigaciones demuestran que estos dispositivos pueden pasar por alto tres veces más casos de hipoxemia oculta en pacientes de raza negra. ¿Podemos esperar que se tomen medidas igualmente positivas bajo el nuevo régimen?
Esta semana, Vikas Saini, presidente del grupo de expertos en salud Lown Institute, dijo sobre los premios Shkreli, que dirige el instituto: «Todas estas historias pintan una imagen de una industria de la salud que necesita desesperadamente una transformación». A medida que el sol se pone sobre otra administración estadounidense, el cambio inminente es lo único de lo que podemos estar seguros.
Controversia del ticagrelor: ¿Beneficio real o engaño? Cuantos pacientes pudieron perder oportunidad.
Este artículo me hace afirmar cada día que debemos ser más ni Bayesianos ni Nihilistas, sino críticos de lo que estudiamos y que debemos buscar permanentemente conocimientos independientes, verdaderamente alejados de los intereses.
Dudas sobre un ensayo histórico de un fármaco cardíaco: el estudio ticagrelor PLATO
Peter Doshi. Editor en Jefe British Medical Journal.
BMJ 2024; 387:Q2550
Un medicamento antiplaquetario de gran venta nunca se ha librado de las dudas sobre su ventaja sobre rivales más baratos. Con las versiones genéricas de ticagrelor a punto de lanzarse, Peter Doshi echa un nuevo vistazo a la evidencia
En la última década, el fármaco antiplaquetario ticagrelor (Brilinta en Estados Unidos y Brilique en Europa) se ha consolidado en el tratamiento del síndrome coronario agudo, recomendado en las guías de las sociedades de cardiología de todo el mundo. 123 Al ser el único inhibidor de P2Y12 que sigue bajo patente en los Estados Unidos, el gasto público es sustancial, ya que representa alrededor de dos tercios del coste total de los inhibidores de P2Y12, a pesar de que menos del 10% de las prescripciones totales. 4 En 2022, el gobierno federal de EE. UU. gastó más de 750 millones de dólares (593 millones de libras esterlinas; 712 millones de euros) en ticagrelor.
Pero desde su aprobación en 2011 por parte de la Administración de Alimentos y Medicamentos de EE.UU. (FDA, por sus siglas en inglés), han aumentado las dudas sobre su aparente ventaja sobre los inhibidores de P2Y12 más baratos y sin patente, como el clopidogrel y el prasugrel. Si bien AstraZeneca, el fabricante de ticagrelor, informó de una eficacia superior al clopidogrel en el ensayo de fase 3 que llevó el fármaco al mercado, los estudios realizados en el período posterior a la autorización han informado repetidamente de resultados decepcionantes 5 6 789101112 1314 que muestran una eficacia similar al clopidogrel, pero con un aumento del sangrado y la disnea, lo que ha provocado llamamientos para una reevaluación de las directrices. 15 16
Con las versiones genéricas de ticagrelor esperadas pronto en los EE. UU., The BMJ echó un nuevo vistazo a la evidencia. Nuestra investigación encontró que el medicamento de AstraZeneca fue aprobado a pesar de las enfáticas objeciones del personal de revisión científica de la FDA, y que el principal ensayo clínico de ticagrelor, llamado PLATO, fue el foco de una larga y rencorosa disputa sobre su confiabilidad básica. El BMJ también puede revelar nuevos detalles sobre la controversia después de obtener los registros primarios del ensayo PLATO y los datos no publicados a través de una solicitud de libertad de información que muestra más problemas en la presentación de datos.
La paradoja de Estados Unidos
Cuando AstraZeneca desarrolló ticagrelor a mediados y finales de la década de 2000, necesitaba demostrar una clara ventaja sobre el clopidogrel (Plavix), entonces uno de los medicamentos recetados más vendidos del mundo que estaba a punto de expirar su patente. Los resultados de PLATO, un ensayo aleatorizado de 18.624 pacientes realizado en 43 países, parecían destinados a hacer realidad esas esperanzas. Los investigadores de PLATO, en un artículo publicado en 2009 en el New England Journal of Medicine (NEJM), informaron que a los 12 meses, los pacientes asignados a ticagrelor en comparación con clopidogrel vieron una reducción en el riesgo del criterio de valoración primario (muerte por causas vasculares, infarto de miocardio o accidente cerebrovascular) del 11,7% al 9,8%, una disminución del 16% en el riesgo relativo. 17
Sin embargo, a pesar de los resultados, el primer intento de la empresa de obtener la aprobación de la FDA fracasó. Un análisis de subgrupos encontró que, en los EE. UU., los pacientes con ticagrelor tuvieron peores resultados que los aleatorizados a clopidogrel, un 27% más de riesgo del objetivo primario (fig. 1). 18

Figura 1
Diapositiva de presentación de la FDA de julio de 2010 que muestra los resultados de los criterios de valoración primarios de PLATO: en general y comparando los sitios de ensayo de EE. UU. y no EE. UU.18
AstraZeneca se esforzó por explicar que los resultados desfavorables se debían a una dosis inusualmente alta de aspirina que se observa casi exclusivamente en Estados Unidos. Pero los científicos de la FDA no estaban convencidos.
Los asesores externos de la FDA estaban igualmente preocupados. En una reunión de un día en 2010, organizada por la FDA para discutir la solicitud de AstraZeneca, los miembros del comité asesor votaron 7-1 recomendando la aprobación de ticagrelor, pero instaron a la FDA a exigir un ensayo posterior a la aprobación en la población de EE.UU. 19 En lugar de aprobar y exigir dicho estudio, una opción bajo una ley estadounidense de 2007, la FDA invitó a AstraZeneca a volver a presentar su solicitud con un análisis más detallado de la hipótesis de la aspirina.
La FDA aprueba el ticagrelor a pesar de las dudas cada vez más profundas
Thomas Marciniak, un funcionario médico de la FDA con una reputación atípica por sus revisiones exhaustivas de las solicitudes de las compañías farmacéuticas,2021 fue asignado para evaluar la nueva presentación de AstraZeneca. Meses más tarde, Marciniak no solo no estaba convencido de la hipótesis de la aspirina de AstraZeneca, sino que estaba profundamente preocupado por la fiabilidad básica de los datos del ensayo PLATO.
«Ahora concluyo que hay suficientes problemas con la calidad de los datos de PLATO como para que, en el mejor de los casos, los resultados de EE.UU. sean representativos de la eficacia del ticagrelor, es decir, el ticagrelor es inferior al clopidogrel en eficacia y seguridad», escribió en 2011 en un memorándum de revisión de 47 páginas, recomendando no aprobarlo. 22
Marciniak calificó la solicitud de AstraZeneca como «la peor en mi experiencia en cuanto a la integridad de las presentaciones y la respuesta completa y precisa del patrocinador a las solicitudes». 22 Pero el liderazgo de la FDA se negó a respaldar las extensas reservas de Marciniak. Ya sea que los resultados de EE.UU. fueran simplemente un juego de azar o la consecuencia de diferencias en la dosis de aspirina, un alto administrador de la agencia razonó que «el ticagrelor debería ser aprobado». 23
Lloyd Klein, profesor clínico de medicina en la Universidad de California en San Francisco y experto en el valor clínico de los inhibidores de P2Y12, dijo a The BMJ: «En ese momento se entendía ampliamente que el problema de la dosis de aspirina era el método que la compañía captó como una forma de avanzar con la aprobación de la FDA, reconociendo que los datos de resultados en los EE. UU. eran diferentes a los de los centros europeos. Pero no había ensayos prospectivos existentes para probar si esa hipótesis era precisa». 24
Una saga que se intensifica
La aprobación de Ticagrelor provocó un flujo constante de críticas por parte de aquellos que sostenían que no se podía confiar en los resultados publicados del ensayo PLATO. 2526 Los críticos dijeron que era digno de mención que el ticagrelor fracasara en los EE.UU., el único país con un alto número de inscripciones donde los sitios no fueron monitoreados por el propio patrocinador.
Los copresidentes del comité ejecutivo del ensayo, Robert Harrington, entonces en el Instituto de Investigación Clínica de Duke, y Lars Wallentin, del Centro de Investigación Clínica de Uppsala en Suecia, han sido coautores de docenas de respuestas en defensa de PLATO. Han acusado a sus críticos de «mala ciencia» —selección selectiva, autocitación y «desprecio [por] los conceptos convencionales de probabilidad estadística»— y han cuestionado sus motivos. 272829
La saga se ha desarrollado en varias revistas de cardiología y continúa hasta el día de hoy. Pero la controversia alcanzó su punto álgido en 2013 cuando el Departamento de Justicia de EE.UU. abrió una investigación formal sobre PLATO el 30 y 31 de octubre, seguida al mes siguiente por preguntas de la Agencia Europea de Medicamentos, lo que llamó la atención de los medios de comunicación y los inversores. 32
La investigación civil del Departamento de Justicia de EE.UU. fue guiada por Victor Serebruany, un miembro adjunto de la facultad de la Universidad Johns Hopkins y posiblemente el crítico más temprano y persistente de PLATO, a quien la FDA acudió en busca de ayuda durante sus deliberaciones previas a la aprobación. Serebruany quedó inicialmente impresionado por los resultados del ensayo, pero se volvió escéptico después de notar inconsistencias y anomalías en los datos. En septiembre de 2012 demandó a AstraZeneca en una demanda presentada en nombre del gobierno, por presentar «datos falsos y fraudulentos a Estados Unidos».
Pero el Departamento de Justicia puso fin a su investigación en agosto de 2014, y los investigadores de PLATO expresaron su reivindicación. «Esta decisión debería eliminar cualquier duda restante sobre la fiabilidad de los resultados del ensayo», escribieron Wallentin, Harrington y sus colegas en una rápida respuesta a bmj.com. 34 «Ahora podemos centrarnos aún más en proporcionar nuevos conocimientos sobre la mejor manera de administrar este tratamiento que salva vidas a nuestros pacientes con ataques cardíacos». Sin embargo, al negarse a presentar la demanda por denuncia de irregularidades con Serebruany, el Departamento de Justicia escribió en una presentación judicial que el gobierno de Estados Unidos «se reserva el derecho» de revisar su decisión.
Cuando se le preguntó por qué el departamento cerró su investigación, un portavoz de la Oficina del Fiscal de los Estados Unidos para el Distrito de Columbia le dijo a The BMJ: «Después de una investigación extensa. . . determinamos que las acusaciones carecían de mérito suficiente, de modo que no era en el mejor interés de los Estados Unidos intervenir en la demanda».
La paradoja de PLATO
En los años posteriores a la investigación del Departamento de Justicia, una gran cantidad de estudios observacionales y aleatorios no han logrado replicar los resultados de PLATO,567891011121314, lo que ha llevado a algunos cardiólogos a cuestionar el lugar del ticagrelor en la práctica clínica. 1516
Eric Bates, profesor de medicina interna en la Universidad de Michigan, es coautor de las guías de cardiología de EE. UU. que recomiendan el ticagrelor. 3 Está pidiendo abiertamente una reevaluación.
Después de PLATO, «estaba cada vez más perturbado por cómo un juicio tras otro resultó no ser dramáticamente positivo de ninguna manera», dijo Bates en una entrevista con The BMJ. En un ensayo financiado por AstraZeneca en pacientes principalmente japoneses, por ejemplo, a los pacientes con ticagrelor les fue peor que a los que tomaban clopidogrel, con un 9,0% que experimentaba el criterio principal de valoración frente al 6,3% que recibía clopidogrel. 11
«Cada vez que salía uno de esos ensayos negativos, las revistas de noticias citaban a uno de los investigadores, que tenía un sesgo intelectual [y] financiero, descartándolo. Y le dije: ‘Espera un segundo, vamos a sumar los esqueletos aquí'».
Bates hizo precisamente eso en un artículo de revisión reciente,15 catalogando todos los ensayos que no confirmaron el beneficio. Dice que el ensayo atípico PLATO «no tiene razón para ser cuestionado», pero argumenta que los ensayos posteriores no lograron replicar PLATO porque los pacientes enfrentan un menor riesgo de eventos isquémicos debido a las mejoras en la prevención secundaria y al mayor uso de tratamientos con balón y stents.
Klein también razona que, en los años transcurridos, la mejora de la atención al paciente y de los dispositivos ha desempeñado un papel importante. «Había mucha gente, como yo, que era escéptica», dijo en una entrevista, «pero los datos del ensayo aleatorio fueron el resultado formal del estudio; y aunque juzgue solo por la experiencia clínica, tendría que decir que nadie pudo realmente discernir una gran diferencia, pero ninguno de nosotros está haciendo 10 000 ensayos con pacientes en nuestra práctica».
Los resultados de EE.UU.: ¿pista falsa o canario de las minas de carbón?
Otros apuntan a una posibilidad más preocupante: que los resultados de PLATO no fueron creíbles desde el principio. Estos críticos sostienen que los datos de EE.UU. no eran una aberración, sino que en realidad eran más fiables que los de otros países como Hungría y Polonia.
Destacan que la propia AstraZeneca llevó a cabo el seguimiento de los datos de PLATO, excepto en el caso de los sitios que fueron supervisados por organizaciones de investigación por contrato (CRO) de terceros. 2535 En los cuatro países supervisados exclusivamente por personal no patrocinador —Georgia, Israel, Rusia y Estados Unidos— al ticagrelor le fue peor.
Un investigador principal del sitio PLATO de Europa del Este que habló con The BMJ dijo que se volvió escéptico de los resultados generales después de ver resultados muy divergentes entre Georgia y Rusia, por un lado, y Hungría y Polonia, por el otro (ver fig. 2). En Georgia y Rusia, los resultados favorecieron numéricamente al clopidogrel. En Hungría y Polonia, ambos monitoreados por AstraZeneca, el beneficio del ticagrelor sobre el clopidogrel fue dramático. «Recuerdo este análisis regional… No hay razón para esta diferencia», dijo.
El liderazgo de PLATO ha intentado disipar el argumento, diciendo que el asunto fue abordado en un análisis por «dos estadísticos académicos de alto nivel». Los copresidentes del estudio, Wallentin y Harrington, escribieron que «si bien no es posible sacar conclusiones firmes» del análisis estadístico, «no hay razón para sospechar una influencia de la organización de monitoreo en los resultados del estudio». 36
Sin embargo, los autores del artículo estadístico no llevaron a cabo el análisis más sencillo: resultados generales del criterio de valoración primario para los pacientes en los centros supervisados por las CRO en comparación con los centros supervisados por el patrocinador. 37
El BMJ también ha descubierto que uno de los dos «estadísticos académicos senior» autores del análisis, Kevin Carroll, el autor principal del artículo, era el ex estadístico jefe de AstraZeneca, después de haber trabajado en la compañía durante más de 20 años. Fue Carroll quien presentó los resultados de PLATO en nombre de AstraZeneca en la reunión del comité asesor de la FDA de 2010. El documento enumera a Carroll como un «consultor estadístico independiente» y fue presentado para su publicación el mismo año en que dejó AstraZeneca, pero no revela su empleo anterior.
Carroll le dijo a The BMJ que «[con respecto a] CRO, esto se investigó cuidadosamente», pero continuó diciendo que «un análisis de CRO vs AstraZeneca no tiene absolutamente ningún sentido» y «no informamos un análisis de los resultados de CRO vs AstraZeneca». Defendió su declaración a Statistics in Biopharmaceutical Research de que no tenía afiliaciones o involucraciones financieras que pudieran constituir un conflicto de intereses o un aparente conflicto de intereses, y le dijo a The BMJ que «todos los intereses financieros en AstraZeneca fueron eliminados» en junio de 2012, antes de presentar el artículo. El artículo fue enviado para su publicación en agosto de ese año.
Patrones inesperados en la adjudicación de puntos de conexión
La evaluación de la eficacia de un fármaco se basa en un recuento preciso de los eventos que cumplen con la definición principal del criterio de valoración: en el caso de PLATO, muertes por causas vasculares (incluida la hemorragia mortal), infarto de miocardio (IM) o accidente cerebrovascular. Un comité central de adjudicación independiente de 51 miembros, ciego al grupo de tratamiento, revisó más de 10 000 eventos.
Pero ha habido acusaciones de parcialidad. En su denuncia legal de 2012, Victor Serebruany alegó que los adjudicadores de PLATO agregaron 45 MI al grupo de clopidogrel, «y precisamente cero MI adicionales para . . . ticagrelor.
El BMJ pudo confirmar los números de Serebruany. Los registros de la FDA muestran que, según los informes del sitio, había 504 sujetos con infarto de miocardio en comparación con 548 con clopidogrel. Después de la adjudicación, el conteo aumentó solo para el clopidogrel, a 593.
Utilizando conjuntos de datos de ensayos obtenidos por primera vez de la FDA por Serebruany y posteriormente verificados a través de una solicitud de libertad de información por parte de The BMJ, que contiene sentencias previas y posteriores a la adjudicación, también encontramos un desequilibrio entre 20 decisiones de categorías de muerte sobre las que el comité de adjudicación estaba en «importante» desacuerdo y, en última instancia, no pudo resolver: 17 estaban en el brazo de clopidogrel mientras que solo 3 estaban en ticagrelor. La disparidad plantea interrogantes sobre la posibilidad de desenmascarar.
A pesar de los desacuerdos no resueltos sobre las 20 muertes, se registró una clasificación final de la causa de muerte posterior a la adjudicación. Pero en seis casos, cambió si el evento cumplía o no con la definición de criterio de valoración primario en comparación con la atribución de la causa de muerte proporcionada por los investigadores del sitio. En todos los casos, The BMJ encontró que el cambio en la atribución favorecía al ticagrelor.
Ni los copresidentes del comité de adjudicación, Kenneth Mahaffey y Claes Held, ni los copresidentes del juicio, Harrington y Wallentin, respondieron a las solicitudes de comentarios por correo electrónico de The BMJ.
A AstraZeneca también se le presentó un resumen de los hallazgos en este artículo, pero no solicitó más detalles y se negó a ser entrevistada. Un portavoz dijo por correo electrónico que la compañía no tiene «nada que agregar», y dirigió a The BMJ asu declaración pública de 2014 después de la investigación del Departamento de Justicia de EE. UU. sobre PLATO.
Cuestionamientos sobre la exactitud de los registros de defunción
Cuando se anunciaron por primera vez los resultados de PLATO, los médicos quedaron impresionados por el aparente beneficio de mortalidad del ticagrelor. La transcripción de la reunión del comité asesor de la FDA muestra cuán persuasivos fueron los datos: al menos dos asesores declararon que votaron a favor de la aprobación debido al beneficio general de mortalidad.
Al principio, Serebruany también estaba fascinada con la reducción absoluta de la mortalidad. Serebruany, experta en plaquetas, se esforzó por explicar el beneficio observado. «Afirmar que se anticipó un resultado tan notable no está de acuerdo con los hechos», escribió en 2010, señalando que los datos de mortalidad de la fase 2 «en realidad se veían mejor para el clopidogrel». 33
A medida que el optimismo inicial de Serebruany se transformó en una profunda sospecha sobre la integridad de los datos del ensayo, comenzó a ponerse en contacto con los investigadores del sitio PLATO en todo el mundo, solicitando su ayuda para verificar los datos de muerte. Muchos cooperaron, algunos, como en México y Canadá, incluso compartieron documentos originales del juicio. Pero los récords no siempre coincidían. 38
En un sitio en el sudeste asiático, un investigador de PLATO escribió a Serebruany, en un correo electrónico visto por The BMJ, diciendo: «No hubo muertes de nuestros pacientes de PLATO. Eso es casi seguro». Pero según los datos presentados a la FDA y revisados por The BMJ, ocurrieron cuatro muertes en este sitio (tres en el grupo del clopidogrel), lo que plantea dudas sobre la exactitud de los informes a la FDA. El BMJ también vio registros a nivel de sitio donde la fecha de muerte del paciente no coincidía con la fecha en el conjunto de datos de la FDA.
En Canadá, The BMJ habló con Jean-François Tanguay, profesor de medicina en la Universidad de Montreal, quien no participó en PLATO, pero dice que lo que se informó a la FDA es inexacto. Tanguay obtuvo registros de ensayos, vistos por The BMJ, que describen la muerte de un paciente de PLATO que fue «claramente una muerte vascular». Pero según la base de datos que AstraZeneca proporcionó a la FDA, los investigadores del lugar lo clasificaron como una muerte por cáncer. Tanguay dijo que no se asemeja a una muerte por cáncer en etapa tardía. La idea de que los investigadores del lugar hubieran etiquetado la muerte como si fuera por cáncer, dijo, era «bastante exagerada».
El análisis del BMJ también encontró omisiones en la publicación histórica de PLATO. El artículo, publicado en NEJM y reportado como un análisis por intención de tratar, reporta 905 muertes totales por cualquier causa entre todos los pacientes aleatorizados. 17 Sin embargo, un informe interno de la compañía afirma que 983 pacientes habían muerto en ese momento. Si bien ocurrieron 33 muertes después del período de seguimiento, el recuento de NEJM aún deja fuera 45 muertes «descubiertas después de la retirada del consentimiento». El BMJ obtuvo algunos registros de pacientes cuyas muertes no se informaron en NEJM (ver tabla 1) y solicitó una respuesta a la revista.
El NEJM no cuestionó el error, pero dijo que no estaba seguro de publicar una corrección. Citando las nuevas directrices (pero aún no públicas) del Comité Internacional de Editores de Revistas Médicas (ICMJE), el editor en jefe de NEJM, Eric Rubin, dijo a The BMJ que «para los manuscritos más antiguos, la corrección no es necesariamente apropiada a menos que haya un efecto en la práctica clínica», concluyendo que «no parece que la corrección de este artículo de hace 15 años vaya a tener ningún impacto». (La guía actual del ICMJE dice: «Se necesitan correcciones por errores de hecho»). Rubin añadió que «de hecho, la FDA, usando los datos que usted [BMJ] proporciona, aprobó el medicamento».
No obstante, Rubin dijo que intentaría ponerse en contacto con los autores. «Pero, si no podemos comunicarnos con ellos o no pueden acceder a los datos, lo más probable es que no procedamos con las correcciones.
«Hemos escrito al Dr. Harrington [copresidente del ensayo PLATO] y esperamos una respuesta. Luego decidiremos cómo avanzar».
Resolución
Quince años después de PLATÓN, Serebruany sigue publicando críticas. Desde 2016, muchos de ellos han sido coescritos por Marciniak, ahora retirado de la FDA. Los investigadores de PLATO, sin embargo, parecen haber dejado de responder en gran medida.
En una entrevista con The BMJ, Serebruany expresó pocas esperanzas de que las palancas científicas resuelvan las preguntas sobre la integridad de los datos en PLATO. La única forma de avanzar, en su opinión, es la reincorporación del Departamento de Justicia.
«Hay muchas personas buenas en el Departamento de Justicia y tenemos que darles otra oportunidad para examinar el caso, emitir nuevas demandas de investigación civil y dejar de coquetear, negociar y dar vueltas a cambio de futuros trabajos de alto perfil en las grandes farmacéuticas. Entonces el pueblo estadounidense recibirá justicia».Tabla 1
Muertes incluidas y excluidas de los análisis en NEJM

Figura 2
Resultados de criterios de valoración primarios por país (Fuente: Memorándum de revisión de la FDA de junio de 2010)39
Productos químicos manufacturados y salud infantil: la necesidad de una nueva ley
Este trabajo recientemente publicado en el New England Journal of Medicine nos alerta con toda crudeza el daño que podríamos estar ocasionando a la especie humana desde la industria química y su manufactura, especialmente a los niños, con malformaciones y disminuyendo afectando su capacidad reproductiva, el aumento de la incidencia de obesidad, cáncer infantil entre otros aspectos, es interesante leerlo, informarse y estar atentos, Recordemos que estamos en la era neovesaliana de la medicina de las 6 P: Personalizada, predictiva, de precisión, promoción, prevención y poblacional. Suponer, pensar o proponer una ley en Argentina estos tiempos de auge libertario, sería imposible, donde lo que importa son los superávits gemelos del presente, el combate a la inflación como prioridad, las cuentas fiscales equilibradas, no emitir dinero, pero quienes valoramos eso como el bien necesario, no suficiente, no tenemos que olvidar que la verdadera libertad de los hombres se vive y disfruta cuando tienen salud, con acceso y equidad.

8 de enero de 2025
Las enfermedades no transmisibles (ENT) son las principales causas de enfermedad y muerte en los niños en la actualidad. Su incidencia y prevalencia están aumentando. Y las investigaciones más recientes vinculan múltiples ENT en los niños con productos químicos sintéticos manufacturados. 1,2
Se estima que en la actualidad hay en los inventarios mundiales unas 350.000 sustancias químicas manufacturadas, mezclas químicas y plásticos. 3 La mayoría se producen a partir de combustibles fósiles (gas, petróleo y carbón).
La producción se ha multiplicado por 50 desde 1950, actualmente aumenta alrededor de un 3% al año y se prevé que se triplique para 2050. 4 La contaminación ambiental 5,6 y la exposición humana 7 están muy extendidas. Sin embargo, la fabricación de productos químicos y plásticos sintéticos está sujeta a pocas restricciones legales o normativas. 8,9
A diferencia de los productos farmacéuticos, los productos químicos sintéticos se comercializan sin apenas evaluación previa de sus riesgos y prácticamente sin vigilancia posterior a la comercialización para detectar efectos adversos a largo plazo para la salud. Menos del 20% se ha sometido a pruebas de toxicidad y menos aún a pruebas de efectos tóxicos en lactantes y niños. 8 Se siguen descubriendo con una frecuencia alarmante asociaciones entre productos químicos de uso generalizado y enfermedades en niños, y es probable que existan otros vínculos aún desconocidos. Proteger a los niños de los peligros de los productos químicos requerirá una reforma fundamental de la legislación actual y una reestructuración de la industria química para dar prioridad a la salud infantil.
Enfermedades No Transmisibles en niños y productos químicos sintéticos
En el último medio siglo, las tasas de ENT en niños han aumentado marcadamente. 1 La incidencia de cánceres infantiles ha aumentado un 35%. 10 Los defectos congénitos reproductivos masculinos se han duplicado en frecuencia. 11 Los trastornos del desarrollo neurológico afectan ahora a 1 de cada 6 niños, y el trastorno del espectro autista se diagnostica en 1 de cada 36. 12 El asma pediátrica se ha triplicado en prevalencia. 13 La obesidad pediátrica casi se ha cuadriplicado en prevalencia y ha impulsado un marcado aumento de la diabetes tipo 2 entre niños y adolescentes. 14 En los adultos, por el contrario, la enfermedad, la discapacidad y la muerte debido a enfermedades cardiovasculares, accidentes cerebrovasculares y muchos tipos de cáncer han disminuido. 15,16
Existe una gran cantidad de evidencia que vincula múltiples ENT pediátricas con sustancias químicas sintéticas (véase el Apéndice complementario , disponible con el texto completo de este artículo en NEJM.org). 1 Esta investigación fue estimulada por estudios que involucraron a niños que tenían lesiones obvias por exposición a sustancias químicas: una epidemia de más de 10.000 bebés nacidos con focomelia después de que sus madres ingirieran al principio del embarazo el sedante talidomida 17 ; la tragedia de Minamata, en la que los bebés nacieron con un profundo deterioro neurológico debido al consumo involuntario por parte de sus madres de pescado contaminado con metilmercurio 18 ; y casos de adenocarcinoma de la vagina en mujeres jóvenes cuyas madres habían tomado dietilestilbestrol (DES) para prevenir abortos espontáneos. 19 En todos estos episodios, las madres resultaron físicamente ilesas. De estos casos se desprenden dos lecciones fundamentales: las sustancias químicas tóxicas pueden atravesar la placenta y los niños son mucho más vulnerables a ellas que los adultos. Estos hallazgos sentaron las bases intelectuales para el campo de la pediatría ambiental, también conocida como salud ambiental infantil. 1Una consecuencia adicional del desastre de la talidomida 17 fue la aprobación en 1962 de las Enmiendas Kefauver-Harris a la Ley Federal de Alimentos, Medicamentos y Cosméticos. Estas enmiendas ampliaron la autoridad de supervisión de la Administración de Alimentos y Medicamentos (FDA) para las sustancias químicas destinadas a usarse como productos farmacéuticos y crearon requisitos para que los fabricantes realizaran pruebas de seguridad y eficacia previas a la comercialización de los nuevos medicamentos y vigilancia posterior a la comercialización para detectar efectos adversos para la salud a largo plazo. A raíz de estas enmiendas, el número de medicamentos aprobados por la FDA por año se redujo en dos tercios. 20
Crecimiento de la investigación en pediatría ambiental
La investigación en pediatría ambiental ha florecido en los últimos 25 años ( Figura 1 ). Dos catalizadores clave de este crecimiento fueron la publicación en 1993 del informe del Consejo Nacional de Investigación, Pesticides in the Diets of Infants and Children 21 que dilucidó las bases biológicas de la mayor susceptibilidad de los niños a las sustancias químicas tóxicas, y la aprobación en 1996 de la Ley de Protección de la Calidad de los Alimentos (FQPA), la ley estadounidense sobre pesticidas. La FQPA convirtió la protección de la salud ambiental de los niños en una prioridad nacional y exigió la generación de datos sobre los peligros químicos para los niños, estimulando una expansión sustancial de la investigación financiada por el gobierno federal en pediatría ambiental.Figura 1

Desde entonces, esta investigación ha documentado en repetidas ocasiones que incluso las exposiciones breves y de bajo nivel a sustancias químicas tóxicas durante los primeros períodos vulnerables están vinculadas a un mayor riesgo de enfermedades y discapacidades en los niños que pueden persistir a lo largo de la vida. 22-25 Las exposiciones prenatales son particularmente peligrosas. Aunque “la dosis hace el veneno” sigue siendo una máxima probada, el momento de la exposición es claramente al menos tan importante como la dosis durante el desarrollo humano temprano. Las investigaciones también han revelado que las sustancias químicas tóxicas pueden producir un espectro de lesiones dependiente de la dosis en los niños. Algunos efectos son clínicamente evidentes, pero otros sólo pueden detectarse con una evaluación detallada. La lesión cerebral silenciosa con pérdida de coeficiente intelectual en niños expuestos a niveles bajos de plomo es un ejemplo bien estudiado. 26Un tercer descubrimiento es que las enfermedades asociadas con la exposición temprana pueden manifestarse en cualquier momento de la vida. 23 Algunas, como los defectos anatómicos congénitos, son evidentes en el momento del nacimiento o cerca de él; otras no se hacen evidentes hasta más tarde en la infancia, la adolescencia o la edad adulta. Los efectos retardados incluyen alteración del desarrollo sexual, 14,27 reducción de la fertilidad, 14,27 y un mayor riesgo a lo largo de la vida de asma, obesidad, diabetes, enfermedades cardiovasculares, deterioro neurológico y cáncer. 1,22–25
Debido a que no es ético realizar ensayos clínicos aleatorios de exposiciones a sustancias químicas tóxicas, la evidencia que vincula las sustancias químicas fabricadas con las ENT en los niños se deriva en gran medida de estudios epidemiológicos, con evidencia adicional proveniente de estudios experimentales en animales y estudios mecanicistas.
Los estudios epidemiológicos prospectivos de cohortes de nacimiento que miden las exposiciones a sustancias químicas en personas embarazadas y fetos y siguen a los niños longitudinalmente durante muchos años son plataformas particularmente poderosas para descubrir asociaciones entre sustancias químicas sintéticas y enfermedades porque vinculan las exposiciones a los resultados en niños individuales y eliminan el sesgo de memoria. Dichos estudios han revelado vínculos entre las exposiciones prenatales a ftalatos ( grupo de sustancias químicas sintéticas que se utilizan como plastificantes, disolventes o fijadores en muchos productos) y trastornos del desarrollo reproductivo masculino 28 ; entre la exposición temprana al diclorodifeniltricloroetano y el cáncer de mama en mujeres 25 ; entre la exposición en el útero a retardantes de llama bromados, ftalatos y organofosforados y disminuciones de por vida en la función cognitiva 29 ; y entre la exposición temprana a sustancias perfluoroalquiladas y polifluoroalquiladas (PFAS) y la disfunción inmunológica, la dislipidemia y los trastornos tiroideos 30 (véase el Apéndice complementario ). La evidencia de tales asociaciones es especialmente convincente cuando múltiples estudios epidemiológicos en diferentes poblaciones y ubicaciones geográficas arrojan resultados consistentes. 26,31
La exposición generalizada de los niños a una sustancia química tóxica puede dañar la salud, la viabilidad económica y la seguridad de toda una sociedad. Por ejemplo, cada año, desde la década de 1950 hasta la de 1970, se añadieron alrededor de 100.000 toneladas de tetraetilo de plomo a la gasolina en los Estados Unidos para mejorar el rendimiento de los automóviles, lo que provocó una enorme contaminación ambiental por plomo y una amplia exposición humana: el nivel medio de plomo en sangre de la población era de 16 a 17 μg por decilitro. El coeficiente intelectual medio entre los niños estadounidenses se redujo en un estimado de 2 a 5 puntos, 32 el número de niños con un coeficiente intelectual superior a 130 disminuyó en más del 50%, y el número con un coeficiente intelectual inferior a 70 (el criterio utilizado en la Clasificación Internacional de Enfermedades para definir la discapacidad intelectual) aumentó en más del 50% ( Figura 2 ). 33

Las enfermedades causadas por la exposición a sustancias químicas tóxicas durante la infancia pueden provocar enormes pérdidas económicas, 34,35 incluidos gastos de atención sanitaria y pérdidas de productividad a lo largo de la vida como consecuencia de la reducción de la función cognitiva, discapacidades físicas y muerte prematura. La industria química externaliza en gran medida estos costos y los impone a los gobiernos y a los contribuyentes. El reconocimiento de su magnitud ha dado lugar a sentencias judiciales multimillonarias en las que se ha declarado responsables a fabricantes y marcas de los daños causados por sus productos. 36,37
Por el contrario, la reducción de la exposición a sustancias químicas tóxicas puede producir importantes beneficios económicos. En la década posterior a la eliminación del plomo de la gasolina en los Estados Unidos, el nivel medio de plomo en la sangre de los niños se redujo en más del 95% y, a partir de 1980, el coeficiente intelectual medio de la cohorte de nacimiento de cada año era de 2 a 5 puntos superior al de las cohortes anteriores a 1980. Como cada punto adicional de coeficiente intelectual se asocia a un aumento del 1,8 al 2,4% del potencial de ingresos a lo largo de la vida, el beneficio económico estimado para cada cohorte de nacimiento es de unos 200.000 millones de dólares, un beneficio acumulado desde 1980 de más de 8 billones de dólares. 32 La reducción de la frecuencia de las enfermedades tras la reducción de la exposición es una prueba contundente de la causalidad química.
Ley química fallida
La legislación estadounidense sobre sustancias químicas —la Ley de Control de Sustancias Tóxicas (TSCA, por sus siglas en inglés) de 1977 y sus modificaciones posteriores— se basa en una promesa legal de “proteger la salud pública y el medio ambiente” de los “riesgos irrazonables” que plantean las sustancias químicas. 38 Sin embargo, en realidad, la TSCA no proporcionó a la Agencia de Protección Ambiental (EPA, por sus siglas en inglés) la autoridad necesaria para cumplir esta promesa. 39 De este modo, la ley alienta efectivamente la producción química sin restricciones a expensas de la salud de los niños. 9 Es una legislación que no cumple con su cometido. Las fallas de la TSCA significan que la industria de fabricación de productos químicos está en gran medida exenta de la responsabilidad de realizar pruebas de toxicidad previas a la comercialización de nuevos productos químicos o de vigilancia posterior a la comercialización para detectar eventos adversos a largo plazo. 8,9 El supuesto fundamental de la TSCA es que todos los productos químicos fabricados son inofensivos y beneficiosos, y sólo en raras ocasiones se exige a los fabricantes que examinen los posibles riesgos para la salud de los productos químicos nuevos o existentes. En cambio, la TSCA impone a los reguladores gubernamentales la carga de identificar los productos químicos potencialmente peligrosos, realizar búsquedas bibliográficas, realizar evaluaciones de riesgos y justificar cualquier restricción propuesta mediante análisis de costo-beneficio. Como resultado, pocas asociaciones entre los productos químicos fabricados y las enfermedades en los niños han sido abordadas por medidas regulatorias. Los peligros que se han reconocido generalmente se han ignorado o minimizado, y se ha permitido que los productos químicos responsables sigan utilizándose sin restricciones o con restricciones limitadas. 40,41 En los casi 50 años transcurridos desde la aprobación de la TSCA, sólo un puñado de productos químicos han sido prohibidos o restringidos en los mercados estadounidenses. 9Para inclinar aún más la balanza hacia una producción sin restricciones, el gobierno ofrece subsidios multimillonarios a los fabricantes de productos químicos y plásticos de Estados Unidos. 42 Además, los fabricantes reciben protecciones de secreto comercial que les permiten afirmar que prácticamente toda la información relativa a un producto químico o plástico es secreta. 9 Los fabricantes han aprovechado al máximo este privilegio, incluso cuando el secreto no está justificado legalmente. Por lo tanto, hoy en día prácticamente no se sabe nada sobre la toxicidad o incluso la composición química de muchos productos químicos que se venden en los mercados estadounidenses. 9
En la Unión Europea, la legislación sobre sustancias químicas es aparentemente más rigurosa. 43 La ley de gestión de sustancias químicas de la UE —Registro, Evaluación, Autorización y Restricción de Sustancias Químicas (REACH)— establece que funciona según el principio de “sin datos no hay mercado”. Exige al menos un cierto grado de análisis de toxicidad previo a la comercialización de las nuevas sustancias químicas, así como análisis basados en evidencias de las sustancias químicas consideradas particularmente peligrosas. Sin embargo, en la práctica, REACH no limita la producción de sustancias químicas. El análisis previo a la comercialización en la Unión Europea depende en gran medida de los datos de pruebas de toxicidad proporcionados por la industria química, que se aceptan con pocos controles de calidad. Además, REACH contiene múltiples exenciones y coloca una pesada carga sobre los reguladores gubernamentales para demostrar los daños. Las agresivas leyes de secreto comercial proporcionan aún más protección. 44 El efecto neto es que sólo 73 sustancias químicas y grupos de sustancias químicas han sido restringidos o prohibidos en los mercados de la UE.
Las políticas de gestión de sustancias químicas tanto en los Estados Unidos como en la Unión Europea tienen dos deficiencias adicionales. En primer lugar, sólo tienen en cuenta los peligros de una sustancia química a la vez, lo que ignora la realidad de que los niños están expuestos diariamente a mezclas de múltiples sustancias químicas fabricadas que pueden tener efectos acumulativos o sinérgicos. 45 En segundo lugar, aparte del requisito limitado de la FQPA de que la EPA tenga en cuenta las vulnerabilidades de los niños al establecer los niveles de tolerancia de los plaguicidas, las leyes químicas de la mayoría de los países no suelen tener en cuenta las sensibilidades particulares de los niños.Así, la industria química, que enfrenta pocas cargas regulatorias y un régimen legal que ofrece protección de bajo costo para sus descubrimientos, ha florecido. Hoy es la segunda industria manufacturera más grande del mundo y representa alrededor del 25% del producto interno bruto (PIB) de Estados Unidos. 46 Con la legislación actual, tiene pocos motivos para alterar su modelo de negocios o invertir en innovación sustentable.
Una receta para el cambio
Para proteger la salud de los niños frente a las sustancias químicas sintéticas fabricadas será necesario adoptar un enfoque más precautorio en la legislación sobre sustancias químicas, que dé prioridad a la protección de la salud frente a la producción sin restricciones de sustancias químicas y plásticos. En virtud de esas nuevas leyes, ya no se debería presumir que las sustancias químicas son inocuas hasta que se demuestre lo contrario. En cambio, se debería permitir que las sustancias químicas y los productos a base de sustancias químicas entren y permanezcan en los mercados sólo si sus fabricantes pueden demostrar, mediante pruebas rigurosas e independientes, que no son tóxicas a los niveles de exposición previstos. Además, se debería exigir a los fabricantes de sustancias químicas y a las marcas que comercializan productos químicos que realicen una vigilancia posterior a la comercialización para detectar efectos adversos a largo plazo, especialmente en las poblaciones pediátricas.Un paradigma jurídico de este tipo estaría en consonancia con el derecho farmacéutico, el derecho internacional que reconoce el derecho universal a un medio ambiente limpio y saludable, 47 y la orientación adoptada por el Comité de los Derechos del Niño de las Naciones Unidas que afirma que el derecho a un medio ambiente saludable se extiende con particular relevancia a los niños48
Políticas químicas nacionales
La piedra angular de un nuevo paradigma jurídico para la gestión de las sustancias químicas sería un proceso integral de aprobación a nivel nacional para todas las sustancias químicas (existentes y nuevas) y los plásticos y todos los usos químicos, similar al que se aplica a los productos farmacéuticos. Las sustancias químicas, los plásticos y los productos a base de sustancias químicas podrían entrar y permanecer en los mercados sólo si una evaluación científica rigurosa e independiente demostraba que no eran tóxicos para personas de ninguna edad, especialmente niños, en los niveles de exposición previstos. Para garantizar que dicha información sea fidedigna, todas las pruebas de toxicidad deberían realizarse en laboratorios libres de conflictos de intereses financieros y que no estén sujetos a controles contractuales o de otro tipo por parte de los patrocinadores de la industria. Los fabricantes deberían estar obligados a asumir el costo de las pruebas independientes, pero no deberían estar autorizados a realizarlas ellos mismos. Las políticas nacionales en materia de sustancias químicas deben tener en cuenta los resultados de los estudios toxicológicos en animales y en sus mecanismos, que permiten predecir con gran precisión los riesgos para la salud humana, incluidos los riesgos para los niños. 49 Para poder detectar una amplia gama de efectos sobre la salud, los estudios toxicológicos deben superar los estándares mínimos de las Buenas Prácticas de Laboratorio y ampliar los diseños de los estudios para incluir evaluaciones de los mecanismos de toxicidad reconocidos más recientemente, como la alteración endocrina. Para mejorar el reconocimiento de las consecuencias tardías de las exposiciones en los primeros años de vida, deben incluir un seguimiento a largo plazo de los animales expuestos en el útero.
Tratado mundial sobre sustancias químicas
Para hacer frente a la creciente crisis mundial de contaminación química y sus efectos cada vez más graves sobre la salud de los niños, será esencial intensificar los esfuerzos internacionales. Una estrategia clave podría ser un tratado mundial jurídicamente vinculante sobre productos químicos elaborado y aplicado bajo los auspicios de las Naciones Unidas. El tratado mundial de las Naciones Unidas sobre los plásticos que se está negociando actualmente puede servir de modelo. Los intentos de establecer un tratado mundial sobre productos químicos hasta ahora sólo han dado como resultado un marco de políticas voluntario y de múltiples partes interesadas, el Enfoque estratégico para la gestión de los productos químicos a nivel internacional, adoptado en 2006, y una iniciativa de seguimiento, el Marco mundial sobre los productos químicos, adoptado en 2023.Para elaborar y aplicar un tratado será necesario un órgano científico-normativo permanente e independiente que proporcione asesoramiento especializado. Este órgano debería estar integrado por científicos destacados, incluidos médicos, sin conflictos de intereses financieros. 50
Podría basarse en el modelo del Grupo Intergubernamental de Expertos sobre el Cambio Climático o el Comité Científico Asesor sobre Productos de Tabaco de la FDA, o podría estar adscrito al Programa Interinstitucional para la Gestión Racional de las Sustancias Químicas. Habría que establecer mecanismos institucionales para garantizar que el organismo o la secretaría de las Naciones Unidas pertinente responda a las recomendaciones del órgano asesor y actúe en consecuencia.
Informe de la huella química
La presentación de informes sobre la huella química es la estrategia del sector empresarial para documentar y reducir los peligros químicos 51 : los fabricantes de productos químicos y las marcas de consumo divulgan información sobre los riesgos potenciales que plantean los productos químicos y plásticos a lo largo de su ciclo de vida, inventarían sus productos para identificar los productos químicos de gran preocupación, restringen el uso de esos productos, monitorean la reducción del uso e informan de los resultados de manera transparente. 51 Estos informes pueden aclarar a los posibles inversores los riesgos financieros y legales asociados con sus inversiones. Pueden ser requeridos por los gobiernos, impulsados por resoluciones de los accionistas o ordenados por una combinación de los dos.
Reinvención de la industria química
En última instancia, proteger la salud de los niños frente a los productos químicos manufacturados requerirá una transformación fundamental de la estructura y el modelo de negocios de la industria química. 52
La infraestructura rígida, no innovadora y vulnerable de la industria actual basada en carbono fósil debe reemplazarse por un modelo más flexible y sostenible que permita una menor dependencia de las materias primas y la energía fósil; el desarrollo de moléculas y procesos de fabricación más seguros y sostenibles; y un diseño, una entrega y unas cadenas de valor reinventados para productos con menos efectos adversos y con el potencial de convertirse en materias primas para nuevos productos al final de su vida útil. La contaminación por productos químicos sintéticos y plásticos es un problema planetario de gran envergadura que se agrava rápidamente. El aumento continuo y descontrolado de la producción de productos químicos basados en carbono fósil pone en peligro a los niños del mundo y amenaza la capacidad de reproducción de la humanidad. 11,27
Aunque un cambio de paradigma en la gestión de los productos químicos para priorizar la salud humana exigirá un profundo realineamiento de la legislación actual, una reestructuración profunda de la industria química y una reorientación de la inversión financiera a una escala similar a la de la transición mundial a la energía limpia, es esencial preservar nuestra “casa común” y salvaguardar el futuro de nuestros hijos. 53 La inacción en materia de productos químicos ya no es una opción.
Gobernanza Clínica en UCI: Mejora de la Seguridad del Paciente
- 24 de septiembre de 2024 Volumen 50 , páginas 2154–2157, ( 2024 )
La seguridad del paciente se ha convertido en un objetivo primordial para la mejora de la atención sanitaria, en particular en las unidades de cuidados intensivos (UCI), donde la complejidad aumenta el riesgo de errores médicos en comparación con otros entornos hospitalarios [ 1 ]. Por lo tanto, garantizar una atención segura es crucial y debe perseguirse activamente como un valor fundamental [ 2 ].
La gobernanza clínica (GC) es la forma en que las organizaciones sanitarias (incluidas las UCI) se responsabilizan de mejorar constantemente sus servicios y brindar una atención segura, eficaz y compasiva.
Este artículo tiene como objetivo presentar al lector el concepto amplio de gobernanza clínica y demostrar algunas de sus aplicaciones prácticas en el campo de la medicina de cuidados intensivos.
Componentes de la gobernanza clínica
El modelo histórico de la CG se describe como un templo, con una base construida sobre cinco componentes culturales: conciencia de sistemas, trabajo en equipo, comunicación, propiedad y liderazgo. Estos componentes son esenciales para fomentar una cultura que respalde la mejora sostenible de la calidad. Los pilares del templo (eficacia clínica, auditoría clínica, gestión de riesgos, participación del paciente y del público, gestión del personal, educación y formación, y apertura) respaldan la asociación central entre pacientes y profesionales [ 3 ]. Desde una perspectiva práctica, cada dominio de la CG utiliza herramientas como auditorías clínicas, sistemas de notificación de incidentes, evaluaciones de riesgos, programas de formación del personal, mecanismos de retroalimentación de los pacientes y protocolos de atención estandarizados para supervisar, mejorar y garantizar continuamente una atención al paciente de alta calidad.
La Figura 1 proporciona una descripción general simplificada de los dominios de la CG y destaca las herramientas seleccionadas que se analizan en esta breve revisión. Si bien falta evidencia definitiva, la literatura sugiere que la integración de los componentes de gobernanza clínica puede crear un efecto sinérgico, mejorando potencialmente los resultados de los pacientes de manera más efectiva que cualquier componente individual. El estudio de Pronovost et al., por ejemplo, destaca esto al mostrar que la combinación de listas de verificación, educación del personal y retroalimentación regular redujo significativamente las infecciones del torrente sanguíneo relacionadas con el catéter en las UCI [ 4 ].
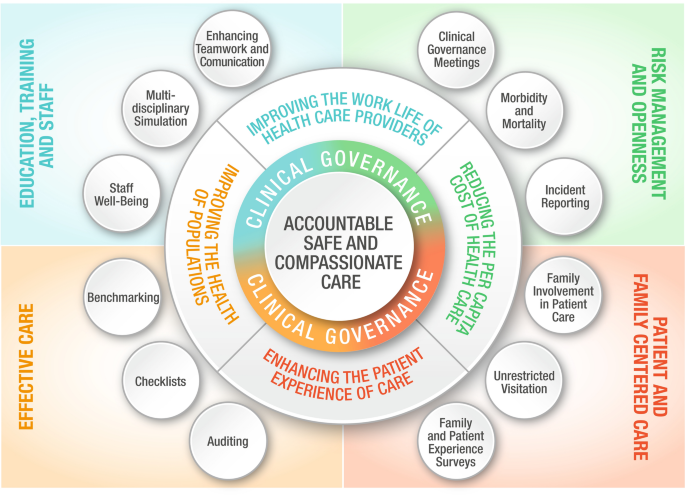
Atención centrada en el paciente y la familia
La atención centrada en el paciente y la familia (PFCC) en la medicina de cuidados intensivos es un enfoque que centra la atención en las necesidades, valores y preferencias tanto de los pacientes como de sus familias, involucrándolos activamente en la toma de decisiones y el proceso de atención, especialmente cuando los pacientes no pueden comunicarse por sí mismos [ 5 ]. La PFCC eficaz puede incluir intervenciones como alentar la presencia de la familia a través de visitas sin restricciones, involucrarlos en las rutinas de atención diaria y las rondas médicas, y apoyar su bienestar psicológico a través de herramientas como diarios de la UCI y mejoras de la comunicación. Estas prácticas se asocian con una menor ansiedad, una mayor satisfacción del paciente y la familia y un menor riesgo tanto de delirio como de trastorno de estrés postraumático. La implementación de la PFCC presenta desafíos como garantizar la capacitación del personal y los recursos para una participación significativa de la familia mientras se maneja la tensión del proveedor de atención médica. Una encuesta internacional reciente mostró que priorizar la PFCC también puede reducir el agotamiento del personal de la UCI, lo que lleva a mejores experiencias tanto para los pacientes como para el personal [ 6 ].
Trabajo en equipo y comunicación eficaces
La comunicación y el trabajo en equipo eficaces se facilitan mediante rondas interprofesionales por las salas, traspasos estructurados y reuniones de seguridad. En estas rondas por las salas, varios profesionales sanitarios trabajan juntos para tomar decisiones integrales, lo que mejora la seguridad del paciente y reduce los errores. Los traspasos son cruciales para transferir información y responsabilidad entre los médicos, y las estrategias como las ayudas para la memoria y los protocolos estandarizados ayudan a minimizar los errores. Las reuniones de seguridad, breves reuniones interprofesionales al comienzo de un turno, se centran en identificar los riesgos potenciales y garantizar que todos los miembros del equipo estén actualizados sobre la información crítica de seguridad del paciente [ 7 ].
Gestión y bienestar del personal
La gestión del personal desempeña un papel crucial en la CG al garantizar que los equipos de atención médica sean reclutados, capacitados y apoyados de manera efectiva para brindar atención al paciente de alta calidad. Esto incluye fomentar un entorno de trabajo positivo, abordar las necesidades de desarrollo del personal y garantizar que existan políticas y prácticas para promover la seguridad del paciente, la eficacia clínica y una experiencia positiva para el paciente. Una buena gestión del personal es esencial para mantener los estándares, mejorar los resultados y responder a los desafíos de la atención médica moderna, como la escasez de personal y el agotamiento. El estudio Iatroref encontró que los síntomas de depresión en el personal de la UCI están significativamente asociados con un mayor riesgo de errores médicos [ 8 ]. Actualmente se están investigando intervenciones de CG efectivas para fomentar el bienestar del personal y reducir las tasas de agotamiento y depresión.
Listas de verificación
Las listas de verificación y las pautas son fundamentales para mejorar la eficacia clínica y la gobernanza en la medicina de cuidados intensivos. Actúan como ayudas cognitivas, asegurando que los proveedores de atención médica se adhieran a las mejores prácticas y completen tareas complejas con precisión. Al igual que la aviación, las listas de verificación estandarizan los procesos, mejoran el rendimiento del equipo y reducen los errores en la UCI. La implementación de listas de verificación para la detección del delirio, la prevención de CLABSI y el manejo de las vías respiratorias se asocia con impactos positivos en los resultados clínicos y del proceso de atención [ 9 ]. La Sociedad de Cuidados Intensivos ofrece listas de verificación para varios procedimientos de la UCI, incluida la inserción de catéteres venosos centrales, la inserción de sondas nasogástricas, drenajes torácicos, broncoscopias, intubaciones y traqueotomías, entre otros.
Auditoría y benchmarking como herramienta de efectividad clínica en UCI
La auditoría es la revisión sistemática de las prácticas clínicas para asegurar el cumplimiento de los estándares establecidos. Las áreas clave de auditoría incluyen ventilación, neumonía asociada al respirador, intubación, atención de traqueotomía, cumplimiento de los paquetes de acceso venoso y terapia de reemplazo renal. El Compendio de Mejora de la Calidad del Royal College of Anesthetists ofrece orientación para las auditorías de la UCI. Las auditorías no deben percibirse como evaluaciones críticas, sino como oportunidades de crecimiento que brindan retroalimentación para reforzar el cumplimiento de las pautas y facilitar el cambio. El proceso de auditoría es cíclico: los datos se recopilan, evalúan y vuelven a recopilar para medir las mejoras. Los resultados se comparten en las reuniones del CG para promover la transparencia, la responsabilidad y la colaboración para abordar los problemas y mantener las mejoras. Una revisión Cochrane encontró que la auditoría y la retroalimentación conducen a mejoras pequeñas pero significativas en la práctica [ 10 ]. La evaluación comparativa complementa la auditoría al permitir que las UCI comparen el desempeño utilizando métricas estandarizadas, como tasas de mortalidad, duraciones de la estadía, tasas de readmisión, adherencia a los protocolos de atención y satisfacción del paciente, tanto internamente como en diferentes instituciones [ 11 ].
Notificación de incidentes en la UCI
La notificación de incidentes es la práctica de divulgar y documentar abiertamente eventos adversos, errores y cuasi accidentes que ocurren durante la práctica clínica. Los sistemas de notificación de incidentes (IRS) son fundamentales no solo para recopilar eventos, sino especialmente para alimentar datos para la reflexión sobre por qué sucedieron los eventos y las formas de prevenirlos. Estos informes se pueden utilizar para informar programas de capacitación y cambios de políticas (ver a continuación), lo que conducirá a una mejor atención al paciente. Los IRS generalmente se basan en plataformas informáticas, generalmente basadas en la web (o en papel), donde los profesionales de la salud informan incidentes con confianza sin temor a represalias. Es crucial educar al personal sobre la importancia y el papel de un sistema de notificación para reducir la falta de notificación de incidentes debido al miedo a la culpa y para garantizar que se les pueda dar retroalimentación oportuna [ 12 ].
Morbilidad y mortalidad
Las conferencias sobre mortalidad y morbilidad (M&M) permiten a los médicos revisar sistemáticamente los eventos adversos y las muertes de pacientes, mejorando la seguridad del paciente y la calidad de la atención al identificar errores evitables o problemas sistémicos. Estas reuniones fomentan la participación del personal, vinculan las presentaciones de casos con debates y elementos de acción e identifican oportunidades para mejoras sistémicas. Una revisión de alcance destaca que las reuniones de M&M apoyan objetivos como la mejora de la calidad, la educación, la gestión de riesgos legales y el apoyo de pares, enfatizando la necesidad de un enfoque estandarizado, especialmente en cuidados críticos [ 13 ]. Finalmente, un estudio a gran escala que evaluó la cultura organizacional y la prevenibilidad de los eventos adversos discutidos durante M&M demostró una fuerte relación entre la evaluación de la prevenibilidad de los eventos adversos informados por los cuidadores y su cultura organizacional en la UCI. Los autores concluyen que la educación y los cambios inducidos por la comunicación de errores son el primer paso para mejorar el desempeño en la UCI [ 14 ].
Simulación multidisciplinar como herramienta de gobernanza clínica en la UCI
La simulación es una técnica, no una tecnología, para reemplazar o amplificar experiencias reales con experiencias guiadas que evocan o replican aspectos sustanciales del mundo real de una manera completamente interactiva ( David Gaba ). La simulación in situ, realizada dentro de la UCI utilizando equipo real y, a menudo, durante las actividades clínicas habituales, garantiza que la capacitación sea relevante y refleje escenarios del mundo real, mejorando tanto las habilidades técnicas como las no técnicas. Este tipo de simulación permite a los estudiantes practicar en su propio entorno, descubriendo errores del sistema local y amenazas de seguridad latentes, como equipos defectuosos o recursos inadecuados que podrían pasarse por alto en simulaciones fuera del sitio. Lo ideal es que las simulaciones utilicen casos del sistema de notificación de incidentes del hospital o casos reales de la UCI para abordar riesgos genuinos y errores pasados. Los ejemplos incluyen falla de las vías respiratorias, extubación accidental, errores de medicación y reconocimiento de sepsis. Estos escenarios realistas ayudan a evaluar la dinámica del equipo, la efectividad de los procedimientos y las vulnerabilidades del sistema, mejorando la preparación para eventos críticos. La sesión informativa eficaz desempeña un papel fundamental en la transformación de las experiencias de simulación en oportunidades de aprendizaje a través de la reflexión y la retroalimentación estructuradas. Además, los resultados de las simulaciones in situ deberían registrarse y difundirse entre las partes interesadas pertinentes, como la dirección del hospital, y compartirse mediante carteles y resúmenes, para garantizar que los aprendizajes beneficien a la comunidad sanitaria en general [ 15 ].
Poniéndolo todo junto: gestión de la información y reuniones de gobernanza clínica
La gestión de la información es un tema común en todas las herramientas de CG. La clave de la CG es que la información se comparta adecuadamente con todos los médicos, administradores, pacientes y familiares involucrados, según corresponda. La ocasión central para compartir información es la reunión de CG, conferencias multidisciplinarias periódicas en las que se discuten las pautas de la UCI, innovaciones, quejas, informes de incidentes, auditorías y casos de morbilidad y mortalidad. Estas reuniones, abiertas a todos los profesionales de la UCI, fomentan la participación y el liderazgo de proyectos. La administración del hospital, las partes interesadas externas y los representantes de los pacientes también pueden asistir. Los resultados de las reuniones deben documentarse como evidencia del proceso.
Mensajes para llevar a casa
En este artículo se destacan las herramientas que pueden utilizar las UCI en el marco de la CG para identificar riesgos y promover una cultura de transparencia, rendición de cuentas y aprendizaje colectivo. Al aplicar sistemáticamente estas herramientas, las UCI pueden afrontar mejor los desafíos de los cuidados críticos, lo que en última instancia conduce a una atención al paciente más segura y responsable.
Impacto Psicológico en Profesionales de Salud tras Eventos Adversos

Antecedentes: El fenómeno de la segunda víctima se refiere al trauma emocional que los profesionales de la salud experimentan después de los eventos adversos (EA) en la atención al paciente, lo que puede comprometer su capacidad para brindar una atención segura. Este problema tiene implicaciones significativas para la seguridad del paciente, ya que los EA generan costos humanos y económicos sustanciales.
Análisis: La evidencia actual indica que los EA suelen ser consecuencia de fallos sistémicos que afectan profundamente a los trabajadores sanitarios. Si bien existen iniciativas de seguridad para los pacientes, el impacto psicológico en los profesionales sanitarios sigue sin abordarse adecuadamente. La Red Europea de Investigadores que Trabajan sobre Segundas Víctimas (ERNST) hace hincapié en la necesidad de apoyar a estos profesionales mediante programas de apoyo entre pares, cambios sistémicos y un cambio hacia una cultura justa en los entornos sanitarios.
Opciones de política: Entre las opciones clave se encuentran la implementación de programas de apoyo entre pares, la revisión del marco legal para despenalizar los errores involuntarios y la promoción de principios de cultura de justicia. Estas iniciativas apuntan a mitigar el fenómeno de la segunda víctima, mejorar la seguridad del paciente y reducir los costos de la atención médica.
Conclusión: Abordar el fenómeno de la segunda víctima es esencial para garantizar la seguridad del paciente. Mediante la implementación de políticas de apoyo y el fomento de una cultura de justicia, los sistemas de atención de la salud pueden gestionar mejor las repercusiones de los eventos adversos y respaldar el bienestar de los profesionales de la salud.
La promoción de la seguridad del paciente sigue siendo un objetivo primordial en los sistemas de atención sanitaria mundiales. A pesar de los esfuerzos concertados para minimizar los eventos adversos (EA) tanto en los hospitales como en los centros de atención primaria, un número considerable de pacientes sigue sufriendo daños durante el curso de su tratamiento y atención [ 1 – 3 ]. Cabe destacar que el 49% de los EA evitables tienen consecuencias leves, mientras que el 12% tienen consecuencias graves, como discapacidad permanente o muerte.
En Europa, se estima que el costo económico de los EA evitables oscila entre 17 y 38 mil millones de euros anuales, junto con la pérdida de 1,5 millones de años de vida ajustados por discapacidad (AVAD) [ 4 ]. Un asombroso 15% de los gastos hospitalarios totales puede atribuirse directamente a los EA [ 5 , 6 ]. Sin embargo, el costo más profundo de los EA, el costo humano, desafía la cuantificación. En consecuencia, se ha adoptado el Plan de Acción Mundial de Seguridad del Paciente 2021-2030 de la OMS, aunque se reconoce que aún se requieren avances sustanciales [ 7 ].
Después de un EA, la atención inmediata se dirige a abordar las necesidades psicosociales, biológicas y físicas del paciente y sus familiares. Esto implica proporcionar información clara, comprensible y veraz sobre el incidente, alentar su participación en la mejora de la atención y ofrecer vías para una compensación justa [ 8 – 10 ]. Reconociendo que la mayoría de los eventos adversos se derivan de fallas sistémicas, también es importante abordar el impacto emocional en los profesionales de la salud para garantizar que estén en las mejores condiciones para brindar una atención segura y eficaz al paciente [ 11 – 13 ].
El término “segunda víctima”, acuñado por Albert Wu, describe lo que les sucede a los trabajadores de la salud cuando algo sale mal. Pueden sentirse tristes, culpables, enojados, tener recuerdos, sentirse solos, preocuparse por cómo reaccionarán los pacientes, los colegas y su lugar de trabajo y cuestionar sus habilidades [ 11 ]. Esta experiencia angustiante puede progresar hacia la desconexión, el abandono, el agotamiento, el estrés postraumático y, en casos extremos, el suicidio. El consorcio ERNST (Red Europea de Investigadores que Trabajan sobre Segundas Víctimas) recientemente perfeccionó esta definición para abarcar: “cualquier trabajador de la salud, directa o indirectamente involucrado en un evento adverso imprevisto para el paciente, un error de atención médica no intencional o una lesión al paciente, y que se convierte en víctima en el sentido de que también se ve afectado negativamente” [ 14 ]. Sin medidas proactivas para restaurar el bienestar mental y la confianza de los profesionales de la salud, el costo psicológico puede comprometer su capacidad para brindar atención de calidad y segura ( Figura 1 ).

Enfrentar el estigma asociado con los eventos adversos es crucial para mitigar los riesgos en los entornos clínicos y mejorar la seguridad general del paciente. Este documento presenta una descripción general concisa de los principios, un marco conceptual y estrategias viables destinadas a disminuir las repercusiones del fenómeno de la segunda víctima y, al mismo tiempo, reforzar la seguridad del paciente.
Análisis
El Consorcio ERNST, financiado por la Asociación COST con la referencia de acción CA19113, se estableció oficialmente el 15 de septiembre de 2020. Su objetivo principal es facilitar un diálogo abierto y completo entre las partes interesadas sobre las implicaciones del fenómeno de la segunda víctima. ERNST funciona como una plataforma de colaboración que abarca fronteras internacionales e incorpora diversas disciplinas y perspectivas, incluidas consideraciones legales, educativas, profesionales y socioeconómicas.
Se inició un proceso de construcción de consenso, coordinado por los líderes de los grupos de trabajo que constituyen el Grupo Central de esta Acción COST 19113. La participación de los miembros del Consorcio que representan a 29 países europeos y 15 países objetivo de inclusión fue fundamental para este procedimiento. Esta declaración, respaldada por los principales profesionales del Comité de Gestión de ERNST, líderes de grupos de investigación y jefes de departamento en hospitales y atención primaria, refleja los resultados de amplias deliberaciones, incluidos intercambios de experiencias, seminarios web, talleres y foros celebrados durante esta Acción. Se llevaron a cabo consultas con expertos de Europa y del exterior, y sus opiniones se tuvieron en cuenta al revisar las contribuciones y dar forma a la declaración final, lo que condujo a la formulación de las aclaraciones propuestas. Todas las reflexiones e ideas discutidas en los diversos foros organizados por ERNST, junto con las experiencias y publicaciones recientes que alimentaron los debates, se clasificaron sistemáticamente en componentes clave. Estos temas se utilizaron para extraer los principales puntos de consenso, que luego se formalizaron en propuestas viables. El Consorcio ERNST ha articulado esta declaración de política, organizada en cinco componentes distintos.
Opciones de política
Declaración de política de ERNST
1. Garantizar la seguridad del paciente es una prioridad mundial.
1.1. La complejidad de los entornos clínicos y de atención de salud requiere que las instituciones de atención de salud anticipen, gestionen y controlen los riesgos y respondan a los EA con un aprendizaje de todo el sistema [ 18 , 19 ].
1.2. La mayoría de los EA tienen un origen multifactorial y sistémico. Son el resultado de una combinación de condiciones latentes y fallas del sistema que pueden provocar daños al paciente, que pueden incluir errores clínicos [ 20 ].
1.3. La seguridad del paciente es una dimensión transversal de la calidad de la atención. Las instituciones de salud necesitan contar con un sistema de mitigación de riesgos de la atención sanitaria que conduzca a la mejora continua y a la creación de organizaciones de aprendizaje.
2. Garantizar la capacidad de los proveedores de atención sanitaria es una prioridad.
2.1. La atención sanitaria es una profesión que exige mucho desde el punto de vista emocional. Es necesario un compromiso de la Comisión Europea, que inste a los países a establecer programas nacionales de salud y seguridad en el trabajo para los trabajadores sanitarios, en línea con las recomendaciones de la OMS [ 21 ].
2.2. Tras cualquier incidente de seguridad o resultado inesperado para el paciente, es esencial priorizar la atención al paciente. Esta atención no debe pasar por alto el impacto psicológico del evento adverso. También debe abordarse el impacto en los profesionales de la salud [ 22–27 ], los estudiantes y los practicantes de ciencias de la salud [ 28 , 29 ] como segundas víctimas para garantizar una atención adecuada al paciente. Esta reacción humana ocurre de manera similar entre los cuidadores informales en el hogar [ 30 , 31 ].
2.3. En situaciones que generan angustia e incertidumbre, las personas reaccionan de forma natural y cuestionan sus acciones. Sin un entorno organizacional de apoyo y apoyo emocional, estas reacciones pueden tener consecuencias negativas duraderas para los pacientes, el equipo profesional y las propias personas [ 15 , 32–37 ]. En los casos más graves, la experiencia de la segunda víctima puede desencadenar un trastorno de estrés postraumático (prevalencia estimada que oscila entre el 5% y el 17%) [ 38 ] o incluso el suicidio [ 39 ]. Los planes y programas de seguridad del paciente y de calidad de la atención a nivel local, regional y nacional no deben diseñarse sin tener en cuenta esta realidad.
3. Asignar recursos para la atención a las segundas víctimas.
3.1 . Existen evidencias que respaldan la efectividad y aceptabilidad de los programas de apoyo entre pares con personal capacitado [ 40–44 ] . Estos programas deberían implementarse a nivel local junto con medidas preventivas e iniciativas que promuevan el autocuidado emocional y la resiliencia [ 16 ], ayudando a los profesionales de la salud a manejar las situaciones altamente estresantes inherentes a la práctica clínica. No hacerlo pone en riesgo la seguridad del paciente [ 21 ].
3.2. El apoyo entre pares es la modalidad de apoyo más deseada, aceptada, factible y asequible para las organizaciones de atención médica [ 37 , 45–47 ]. Los programas iniciales de apoyo entre pares comenzaron en los EE. UU. y han estado en funcionamiento durante aproximadamente 14 años [ 42 , 48 ]. Estos programas ofrecen asistencia emocional a las segundas víctimas a través de iniciativas diseñadas institucionalmente y, en ciertos casos, abarcan una red de hospitales para un impacto más amplio. Dependiendo de los modelos organizativos del país, estos programas podrían ser administrados por departamentos de seguridad del paciente, salud ocupacional, recursos humanos o de forma independiente. El apoyo psicosocial se ha extendido a eventos inesperados y trágicos que afectan a los profesionales de la salud, que se intensificaron durante la pandemia de COVID-19 [ 49 ].
3.3. Además, la implementación de un programa de apoyo entre pares genera ahorros monetarios netos. La evidencia sugiere un ahorro estimado de costos para instituciones de atención médica individuales de 1 millón de euros por año [ 45 , 50 ]. Este costo aumenta considerablemente si consideramos la pérdida de profesionales de la salud competentes, así como los costos inherentes a la medicina defensiva [ 51 , 52 ].
4. Repensar el marco legal y construir una cultura justa.
4.1. La promoción de principios culturales justos dentro de las organizaciones de atención de salud es esencial [ 53 ]. Un cambio regulatorio para despenalizar los errores clínicos honestos, como en la aviación civil, es esencial para pasar de una cultura reactiva a una que fomente la seguridad.
4.2. La complejidad del fenómeno de la segunda víctima requiere soluciones que vayan más allá de mejorar la resiliencia [ 16 , 54 , 55 ]. Se recomienda avanzar en el análisis y discusión de alternativas al marco legal tradicional [ 56 ]. Aprovechar las experiencias de los países que han adoptado sistemas sin culpa e instituido modificaciones en los procedimientos de reclamaciones e indemnización puede proporcionar información valiosa para avanzar en este sentido [ 57 – 60 ].
5. Compromiso de ERNST con acciones exitosas
5.1. Aumentar la concienciación de todas las partes interesadas (a nivel europeo, nacional y regional) para facilitar el debate sobre las cuestiones jurídicas, éticas, sociales y organizativas que impiden abordar el impacto del fenómeno de la segunda víctima en la seguridad del paciente.
5.2. Examinar más a fondo las consecuencias de los errores de medicación y atención entre los cuidadores informales de pacientes dependientes en el hogar y promover iniciativas a nivel local para mitigar sus efectos.
5.3. El fenómeno de la segunda víctima no debe entenderse como un problema que recaiga exclusivamente sobre las organizaciones sanitarias, sus profesionales y los pacientes, ya que su gestión eficaz implica a la sociedad en su conjunto. Esta cuestión debe ser abordada por los sistemas de salud, las instituciones sanitarias y las organizaciones que representan a los profesionales, los pacientes y los ciudadanos. Las autoridades sanitarias y los responsables políticos, tanto a nivel nacional como internacional, deben considerar estos aspectos y actuar de acuerdo con la evidencia científica.
Basándose en la colaboración y las consultas internacionales, la declaración destaca la necesidad de adoptar enfoques integrales, programas de apoyo entre pares y una reevaluación de los marcos jurídicos. Al fomentar el diálogo entre las partes interesadas y abogar por cambios sistémicos, esta declaración de política tiene por objeto cultivar un entorno de apoyo para los trabajadores sanitarios y, en última instancia, mejorar la calidad y la seguridad de la atención al paciente.
Casa de Confianza: Un Marco Para la Atención Sanitaria
The “House of Trust”. A framework for quality healthcare and leadership.
Kris Vanhaecht 1,2,a, Peter Lachman 3, Charlotte Van der Auwera 1, Deborah Seys 1, Fien Claessens 1, Massimiliano Panella 4, Dirk De Ridder 1,2;
17 de Mayo 2024

En el ámbito de la atención sanitaria, los líderes en materia de mejora se han inspirado en los marcos de la industria que se han adaptado a los sistemas de control y las certificaciones para mejorar la calidad de la atención a las personas. Para abordar el desafío de recuperar la confianza en el diseño y la prestación de servicios de atención sanitaria, proponemos un marco conceptual, es decir, la “Casa de la confianza”. Esta Casa reúne la Trilogía de Juran, el concepto emergente de coproducción en la gestión de la calidad y la definición multidimensional de la calidad, que describe los valores fundamentales como parte integral del sistema para brindar atención centrada en la persona y en los familiares.
En la “Casa de la Confianza” los pacientes, sus familiares, los proveedores de atención médica, los ejecutivos y los gerentes se sienten como en casa, con un sentido de pertenencia. Si queremos construir una organización de atención que inspire e irradie confianza a todos los interesados, es necesario resaltar las interacciones básicas entre el front-office y el back-office. Una organización con back-office y front-office bien organizados puede permitir que todos se beneficien de la confianza que cada uno de ellos necesita y merece.
Un sistema de calidad no depende de la inspección y las normas gubernamentales ni de la acreditación externa para convertirse en una institución de confianza. El éxito sólo se alcanzará si todos los implicados se cuestionan continuamente sobre las dimensiones técnicas de la calidad y sus valores fundamentales en el “momento de la verdad”.
Introducción
Los pacientes, familiares, proveedores de atención médica, ejecutivos y gerentes tienen altas expectativas en todos los aspectos de la atención. Para satisfacer estas expectativas, las personas deben confiar en el servicio de atención médica. La confianza se define como » las expectativas del público de que quienes los atienden desempeñarán sus responsabilidades de manera técnicamente competente, que asumirán la responsabilidad y no cederán indebidamente ante otros, y que harán del bienestar de sus pacientes su máxima prioridad». 1 La confianza que los pacientes tienen en los médicos está asociada no solo con la satisfacción del paciente, sino también con la continuidad de la atención, conductas de salud más beneficiosas, menos síntomas, mayor calidad de vida y adherencia al tratamiento. 1 , 2
La confianza es tan fundamental para la relación médico-paciente que es fácil suponer que existe como parte de la interacción clínica. Esto no es necesariamente así y, cuando se pierde la confianza, no hay un único enfoque que la reconstruya, mantenga o garantice. Se han definido varios factores clave para aumentar la confianza entre los pacientes, la organización y los equipos involucrados. 1 Estos incluyen la medición de la experiencia de los pacientes, el compromiso de los médicos, el compromiso de satisfacer las necesidades de los pacientes como el núcleo de la cultura organizacional, equipos clínicos eficaces e inclusión de los pacientes en todas las fases de este trabajo. 3
La confianza no sólo es importante en la relación entre el paciente y el proveedor, sino también en la confianza entre los proveedores de atención médica, los gerentes y la organización de atención médica. En un estudio basado en informes de retroalimentación de 360 grados de 87.000 líderes, Zenger y Folkman concluyeron que tres elementos pueden crear o restablecer la confianza, es decir, relaciones positivas, coherencia y buen juicio o experiencia. 4 Esto se aplica a los líderes y a sus organizaciones complejas, por ejemplo, los hospitales, donde la oficina de atención al cliente y la oficina administrativa de apoyo se encuentran en lo que se denomina el punto de «bisagra». En el punto de bisagra, las vías de atención, los programas de atención, los protocolos y los procedimientos guían a todas las partes interesadas hacia una atención de alta calidad y excelencia.
Jain señaló que, incluso antes de la pandemia de COVID-19, la confianza en la atención médica estaba disminuyendo. 5 La desinformación que acompañó a la pandemia erosionó aún más la confianza, lo que generó desafíos para la confianza en el diseño y la prestación de servicios de atención médica. En consecuencia, los ciudadanos, los proveedores de atención médica y los gerentes necesitan más confianza entre sí y en las organizaciones que visitan o en las que trabajan para coproducir los cambios necesarios. 6
Un artículo reciente de Bates et al. informó sobre los altos niveles de daño que persisten en la atención médica. Esto implica que para implementar los cambios necesarios, los modelos de liderazgo y cambio del pasado no han sido tan efectivos como deberían ser. 7 En respuesta a este hallazgo, Berwick comentó que la seguridad tiene que ser un foco central del liderazgo. 8 Mineo consideró que la confianza es el pegamento que une al líder con sus colegas y esto proporciona la capacidad para el éxito organizacional y de liderazgo. 9 El punto de éxito más importante que se debe lograr sería una alta calidad y seguridad de la atención.
En 2001, el Instituto de Medicina definió la calidad en seis dominios, a saber, seguridad, eficacia, atención centrada en el paciente, puntualidad, eficiencia y equidad. 10 Desde entonces, los marcos para mejorar la calidad y la seguridad se han basado en las teorías de Deming, Juran, Feigenbaum, Crosby y otros que desarrollaron metodologías de mejora de la calidad en otras industrias. La introducción de estas metodologías de mejora en la atención sanitaria ha estado acompañada por la introducción de sistemas de control como la acreditación, la regulación y la certificación. 11
Si bien se ha avanzado en la mejora de la calidad, la difusión y ampliación de las buenas prácticas no ha tenido el ritmo necesario. Entre los nuevos desafíos para alcanzar altos niveles de calidad y seguridad se encuentran la gestión de los recursos humanos, la crisis energética, la inflación y el cambio climático. Sostenemos que para alcanzar este objetivo se requiere un enfoque diferente. Esto requerirá coproducción y cocreación para facilitar la calidad sostenible. El modelo de cocreación considera el contexto interno y externo de una organización, crea soluciones en conjunto y se centra continuamente en cinco pilares principales. 12 Los pilares incluyen la trilogía de Juran de diseño y planificación de la calidad, control de calidad y mejora de la calidad, 13 con la adición de liderazgo de calidad y cultura de calidad.
Se podría argumentar que la literatura y la investigación sobre liderazgo no requieren otro ángulo o marco. Sin embargo, el nivel decreciente de confianza implica que los modelos actuales de calidad y liderazgo no son adecuados para enfrentar este nuevo desafío. Para restablecer la confianza, la atención médica requiere una recalibración de cómo vemos los diferentes componentes del sistema, cómo nos comunicamos con las personas en el sistema y cómo aprendemos a mejorar continuamente. Lee et al. (2019) han sugerido un marco para mejorar la confianza en la atención médica que incluye conceptos de liderazgo, medición de la confianza, transparencia, uso de datos para demostrar confianza, coproducción de atención con las personas y garantía de que los pacientes participen activamente en la atención. 3 Otro marco, el modelo multidimensional, incluye la atención centrada en la persona y en los familiares, la resiliencia, la transparencia y el liderazgo junto con los dominios de calidad técnica y los valores fundamentales de amabilidad, respeto, atención integrada y coproducción. 6
En este artículo, ofrecemos un nuevo marco conceptual que reúne los diferentes marcos de trabajo en el ámbito de la atención sanitaria y coloca a las personas en el centro para coproducir confianza y calidad de atención en la que el liderazgo sea un esfuerzo compartido. La Casa de la Confianza facilita la implementación y el desarrollo de una calidad en la que las personas (pacientes), sus familiares, los proveedores de atención sanitaria y los líderes y gerentes tengan un sentido de pertenencia mediante la cocreación de organizaciones a prueba de futuro.
El front-office, el back-office y el “momento de la verdad”
La verdadera atención y la prestación de servicios se llevan a cabo en el punto de articulación entre la oficina principal y la oficina administrativa de una organización de atención. 14 Es un mecanismo de coproducción entre el usuario del servicio y el proveedor del servicio. 15
- •En el back office se diseñan procesos, protocolos y rutas de atención, pero cobran vida en el front office. El personal sanitario y los directivos reciben formación en los modelos teóricos que incluyen las últimas evidencias para llevar sus conocimientos y habilidades a un nivel óptimo. Es similar a la cocina de un restaurante, donde la comida se prepara de forma impecable. El comensal no sabe cómo se prepara la comida y tal vez no necesite saberlo, ya que hay confianza en que el proceso es higiénico y la comida será segura para consumir.
- •La recepción en el ámbito sanitario es el lugar donde se producen los encuentros singulares entre los receptores y los proveedores de atención, una interacción humana real. Esta interacción única tiene lugar entre una persona como paciente, su ser querido o pariente y el cuidador individual como persona; o dentro del propio equipo, en su microsistema clínico. Este es un momento único, el momento de la verdad , que no se puede revertir si no es óptimo. 16 – 19 El momento de la verdad requiere una comunicación y una educación bidireccionales eficaces en una asociación dinámica, auténtica y, a veces, igualitaria. El momento de la verdad incluye el diseño del entorno, la integridad de la recopilación de conocimientos y la adaptación de las personas, los recursos y los entornos a las necesidades de ambos involucrados en la relación única. 20
Para crear una organización de atención que inspire e irradie confianza a todas las partes interesadas, debemos destacar las interacciones entre las oficinas de atención al cliente y administrativas. Sostenemos que una organización con oficinas administrativas y administrativas bien organizadas puede generar confianza y calidad para los pacientes, familiares, proveedores de atención médica, líderes y gerentes.
Construyendo una Casa de Confianza para posibilitar momentos auténticos de verdad
Hay cinco etapas para construir una Casa de Confianza que permita el momento de la verdad ( Figura 1 ).
- 1.El núcleo de la casa (cuadrados verdes en el medio de la casa en la Figura 1 ):La calidad de la atención se da en la recepción, en el momento de la verdad. Por lo tanto, el punto de partida del modelo de visión multidimensional es priorizar los cuatro valores fundamentales de dignidad y respeto, una visión holística, asociación y coproducción y atención a la compasión con amabilidad. 6 Estos valores se aplican no solo a la interacción única entre las personas en sus roles como proveedores de atención médica, pacientes o familiares, sino también entre las personas como proveedores de atención médica o con sus gerentes. 17 Los valores fundamentales se encuentran en el corazón de la Casa de la Confianza , donde la interacción, la resonancia positiva, el humor y los actos de amabilidad (por ejemplo, Mangomoments) pueden tener lugar y las personas se conocen en persona o virtualmente. 18 – 20
- 2.Los cimientos (rectángulo gris en la figura 1 ):Esta interacción sólo puede ser fluida, cálida y de alta calidad si los procesos, programas, protocolos y procedimientos de atención están bien desarrollados y gestionados. 21 Las vías y procedimientos clínicos son las tablas del suelo de la Casa y deben desarrollarse sobre una base sólida, en lugar de sobre arena suelta. Los cimientos de una Casa de Confianza se basan en las dimensiones técnicas del modelo de calidad multidimensional y son el verdadero punto de articulación entre el front-office y el back-office de la organización.
- 3.Los postes de soporte (cuadrados turquesas en la Figura 1 ):Los dominios de la calidad son los pilares de apoyo de la Casa de la Confianza. La seguridad y la eficiencia son los pilares de apoyo externos de la Casa, ya que una organización insegura o ineficiente no puede proporcionar calidad ni confianza. 22 Los otros pilares de apoyo son la equidad y la diversidad inclusivas, la eficacia, la puntualidad y la sostenibilidad ecológica. 6 Los seis pilares de apoyo forman la columna vertebral de una organización de atención sanitaria y son las dimensiones técnicas de la calidad. Estas estructuras deben estar en buen estado y, sin ellas, no puede darse una atención real.
- 4.Los pilares de soporte (rectángulos azules en la Figura 1 ):Cuatro pilares de apoyo se encuentran en la recepción y también están conectados con la oficina administrativa. Estos pilares son la transparencia, la comunicación, la resiliencia y el liderazgo. Necesitamos comunicarnos de manera transparente, tanto sobre la interacción única a nivel individual como sobre nuestros procesos comerciales que operan en segundo plano. La transparencia en los informes públicos, así como la apertura interna y la comunicación con nuestras propias partes interesadas, garantizan que haya confianza en la organización. Un enfoque continuo en el liderazgo clínico y la resiliencia es importante para garantizar que la filosofía de la atención esté alineada en todos los procesos. La pandemia puso de relieve que el liderazgo clínico auténtico, el comportamiento ejemplar y el conocimiento son importantes, así como garantizar el bienestar físico y psicológico y la resiliencia de los proveedores y gerentes de atención médica. 23 La resiliencia de la persona individual como paciente, sus familiares y las personas que brindan atención y administran la organización es esencial. Esto, a su vez, tendrá un impacto en el atractivo de la organización como empleador, la retención del personal y la creación de confianza.
- 5.El techo (triángulo naranja en la Figura 1 ):El techo se apoya en las demás estructuras y hace referencia a la atención continua a la atención centrada en la persona y en el parentesco en todo lo que hace la organización. La atención centrada en la persona tiene que ver con la experiencia y las relaciones humanas tanto de las personas conocidas como pacientes como de las personas conocidas como proveedores y administradores de atención médica, es decir, todas las partes interesadas en este ecosistema. 24 Una Casa de Confianza se puede construir paso a paso cuando todas las estructuras debajo del techo son de alta calidad y las personas confían entre sí y confían en la organización. El techo puede ser la tarjeta de visita de la organización, que se puede ver desde lejos para invitar a las personas a buscar o brindar atención.
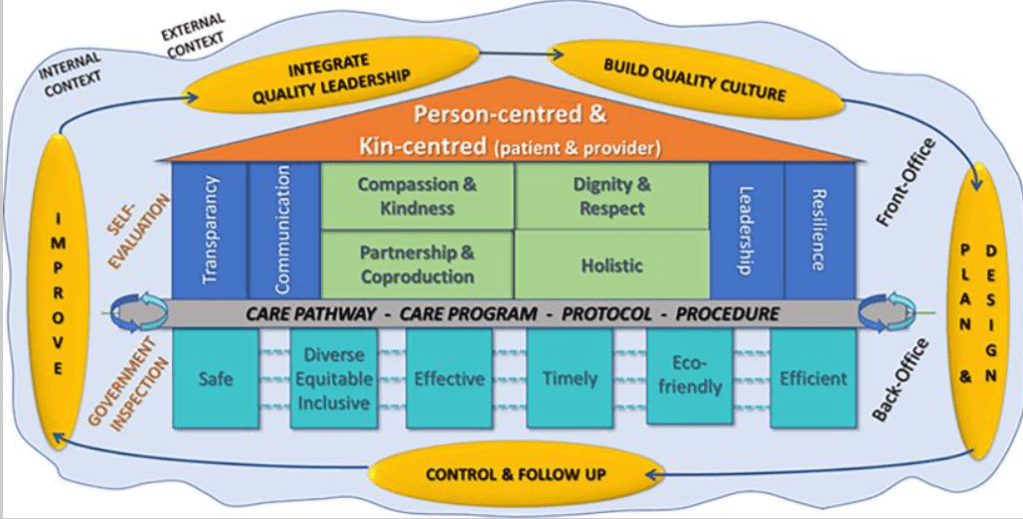
Principios para la construcción de una Casa de Confianza (óvalos amarillos en la Figura 1 ).
A la hora de construir una Casa de Confianza se deben aplicar varios principios . Así como una casa real se construye ladrillo a ladrillo, conectados entre sí, con arquitectos, topógrafos y constructores, así una Casa de Confianza se construye paso a paso, proyecto a proyecto y con una visión y misión claras. 6 , 12 , 17 De esta manera, podemos integrar la investigación de implementación con la metodología de mejora. 6 A la hora de construir la Casa tenemos que tener en cuenta el contexto interno de una organización, por ejemplo, su situación financiera o los retos de gobernanza, y el contexto externo, como la legislación o el impacto de una pandemia.
Es fundamental implicar a todos los interesados como socios en un verdadero proceso de co-creación desde el principio. Cada uno aporta su propio conocimiento único a la tarea de co-producción. 15 Por eso, el módulo de planificación y diseño está situado tanto en la oficina principal como en la oficina administrativa de la organización. El funcionamiento de la oficina principal y la oficina administrativa debe ser supervisado y controlado adecuadamente. Sin embargo, los proveedores de atención médica, los líderes, los gerentes, los pacientes y los familiares deben experimentar la menor incomodidad posible como resultado del control y la supervisión . El uso de fuentes de datos existentes será crucial y debe implementarse en la oficina administrativa tanto como sea posible, incluido el desarrollo de sistemas de control automatizados.
La evidencia científica es importante para sustentar la calidad. Si la Trilogía de la Calidad de Juran mejorada funciona bien, entonces los médicos, la gerencia y la junta directiva podrán usar su liderazgo en calidad para construir una cultura de calidad. 13 Cuando la cultura de calidad es justa y existe una red de salud de aprendizaje innovadora, será posible examinar continuamente de manera crítica el diseño actual y el nivel de calidad de la Casa, con la seguridad psicológica necesaria. 25 Los equipos deben participar de cerca en cada iniciativa de mejora y la voz del paciente y sus familiares debe contar. La estrategia de cambio e implementación es un impulsor esencial de la mejora sostenible.
Puede ser necesaria una inspección o regulación gubernamental , incluso si el núcleo, los cimientos y pilares de la Casa están en buen estado y se siguen los sistemas y procesos impuestos por los reguladores gubernamentales. Sin embargo, la autoevaluación continua por parte de los pacientes, familiares, líderes de los proveedores de atención médica y gerentes será clave para mantener la oficina principal en un alto nivel durante el momento de la verdad y desafiará a todos a mejorarla continuamente.
Observaciones finales
La Casa de la Confianza encarna los tres pilares de la confianza descritos por Zenger y Folkman, 4 es decir, relaciones positivas, experiencia y consistencia, y aborda los desafíos planteados por Jain 5 y Lee. 3 Mate 26 destacó la necesidad de reconstruir la confianza en la atención médica y recomendó que uno tiene que empoderar a las personas para desarrollar una cultura de confianza. El núcleo de la Casa de la Confianza, con sus cuatro valores centrales de atención y pilares de apoyo de transparencia, comunicación, liderazgo y resiliencia, puede satisfacer este requisito urgente y proporciona un nuevo enfoque que incorpora las lecciones de los últimos 20 años de esfuerzos de mejora. Es clave para el desarrollo de relaciones positivas que empoderen a las personas, es decir, pacientes, familiares, proveedores de atención médica, líderes y gerentes para coproducir confianza juntos. Sin estos valores, las relaciones no serán confiables ni estarán centradas en el ser humano y no se logrará la calidad y la seguridad.
La evolución de una organización hacia una Casa de Confianza sólo tendrá éxito si cuestionamos continuamente las dimensiones técnicas de la calidad y nuestros valores fundamentales en el momento de la verdad. El diseño arquitectónico y la co-construcción de una Casa de Confianza son más probables si los involucrados están personalmente involucrados en el diseño, la co-producción y la revisión continua para mejorar su funcionamiento y evaluar sus beneficios. Esto incluye la transparencia, la comunicación, el liderazgo y la resiliencia y la aplicación del modelo de co-creación en sí.
Sólo entonces la orientación personal, para las personas, es decir, los pacientes, sus familiares y el personal sanitario, irradiará verdaderamente confianza. Esto dará como resultado que las personas, los receptores y proveedores de atención sanitaria, permanezcan leales con energía positiva, compromiso y participación día tras día.
Microplásticos y nanoplásticos en ateromas y eventos cardiovasculares
Autores: Raffaele Marfella , MD,Ph.D., Francesco Prattichizzo , Ph.D. , Celestino Sardú , MD,Ph.D. , Gianluca Fulgenzi , Ph.D. , Laura Graciotti , Ph.D. , Tatiana Spadoni , Ph.D. , Nunzia D’Onofrio , Ph.D.,y Giuseppe Paolisso , MD
N Engl J Med 2024 ; 390 : 900 – 910 VOL. 390 NÚM. 10

Abstract
Los microplásticos y nanoplásticos (MNP) están surgiendo como un posible factor de riesgo de enfermedad cardiovascular en estudios preclínicos. No hay evidencia directa de que este riesgo se extienda a los humanos.
Métodos
Realizamos un estudio observacional, multicéntrico y prospectivo en pacientes sometidos a endarterectomía carotídea por enfermedad de la arteria carótida asintomática. Las muestras de placa carotídea extirpada se analizaron para detectar la presencia de nanopartículas con el uso de pirólisis-cromatografía de gases-espectrometría de masas, análisis de isótopos estables y microscopía electrónica. Los biomarcadores inflamatorios se evaluaron con un ensayo inmuno absorbente ligado a enzimas y un ensayo inmunohistoquímico. El criterio de valoración principal fue una combinación de infarto de miocardio, accidente cerebrovascular o muerte por cualquier causa entre los pacientes que tenían evidencia de nanopartículas en la placa en comparación con los pacientes con placa que no mostraba evidencia de nanopartículas.
Resultados
Se incluyeron en el estudio un total de 304 pacientes, y 257 completaron un seguimiento medio (±DE) de 33,7 ± 6,9 meses. Se detectó polietileno en la placa de la arteria carótida de 150 pacientes (58,4 %), con un nivel medio de 21,7 ± 24,5 μg por miligramo de placa; 31 pacientes (12,1 %) también tenían cantidades mensurables de cloruro de polivinilo, con un nivel medio de 5,2 ± 2,4 μg por miligramo de placa. La microscopía electrónica reveló partículas extrañas visibles de bordes irregulares entre los macrófagos de la placa y dispersas en los restos externos. El examen radiográfico mostró que algunas de estas partículas incluían cloro. Los pacientes en los que se detectaron MNP dentro del ateroma tuvieron un riesgo mayor de sufrir un evento final primario que aquellos en los que no se detectaron estas sustancias (cociente de riesgos, 4,53; intervalo de confianza del 95 %, 2,00 a 10,27; P < 0,001).
Conclusiones
En este estudio, los pacientes con placa en la arteria carótida en la que se detectaron MNP tuvieron un riesgo mayor de un compuesto de infarto de miocardio, accidente cerebrovascular o muerte por cualquier causa a los 34 meses de seguimiento que aquellos en los que no se detectaron MNP.
Estudio:
La producción de plásticos aumenta constantemente y se prevé que esta tendencia se mantenga hasta 2050. 1 Los plásticos pueden contaminar el medio ambiente a través de las corrientes oceánicas, los vientos atmosféricos y los fenómenos terrestres, lo que contribuye a su amplia distribución. 2,3 Una vez liberados en la naturaleza, los plásticos son susceptibles a la degradación, lo que lleva a la formación de microplásticos (definidos como partículas de menos de 5 mm) y nanoplásticos (partículas de menos de 1000 nanómetros). Ambos tipos de partículas desencadenan una serie de efectos toxicológicos. 4,5
Varios estudios han demostrado que los microplásticos y nanoplásticos (MNP) ingresan al cuerpo humano a través de la ingestión, inhalación y exposición cutánea, donde interactúan con tejidos y órganos. 5,6 Se han encontrado MNP en tejidos humanos seleccionados, como la placenta, 7 pulmones, 8 e hígado, 9 así como en la leche materna, 10 orina, 11 y sangre. 12 Estudios recientes realizados en modelos preclínicos han llevado a la sugerencia de que los MNP son un nuevo factor de riesgo para las enfermedades cardiovasculares. Los datos de estudios in vitro sugieren que MNP específicos promueven el estrés oxidativo, la inflamación y la apoptosis en las células endoteliales y otras células vasculares; los modelos animales respaldan un papel de los MNP en la frecuencia cardíaca alterada, el deterioro de la función cardíaca, la fibrosis miocárdica y la disfunción endotelial. 13 Sin embargo, se desconoce la relevancia clínica de estos hallazgos. Falta evidencia para demostrar que los MNP se infiltran en las lesiones vasculares en humanos o para respaldar una asociación entre la carga de MNP y la enfermedad cardiovascular.
Para explorar si las MNP son detectables dentro de la placa aterosclerótica y si la carga de MNP está asociada con la enfermedad cardiovascular, evaluamos la presencia de estas sustancias en la placa de la arteria carótida extirpada quirúrgicamente mediante pirólisis-cromatografía de gases-espectrometría de masas, análisis de isótopos estables y microscopía electrónica. Luego determinamos si la presencia de MNP estaba asociada con un punto final compuesto de infarto de miocardio, accidente cerebrovascular o muerte por cualquier causa.
Métodos
Diseño del estudio
Realizamos un estudio observacional, multicéntrico y prospectivo en el que los pacientes fueron asignados a grupos (un grupo con placa en la que se detectaron MNP y un grupo con placa en el que no se detectaron MNP) después del reclutamiento. Los pacientes fueron reclutados del Hospital Cardarelli, Ospedale del Mare y la Universidad de Salerno desde el 1 de agosto de 2019 hasta el 31 de julio de 2020. Pacientes consecutivos con estenosis asintomática de la arteria carótida (según la clasificación del North American Symptomatic Carotid Endarterectomy Trial 14 ) para quienes estaba indicada la intervención fueron examinados para este estudio. Se contactó a un total de 447 pacientes consecutivos para participar, y 312 aceptaron someterse a la evaluación. Se seleccionaron pacientes con enfermedad asintomática para participar, con el fin de maximizar las posibilidades de sobrevivir el período posterior al procedimiento y minimizar la variación interpaciente en los fenotipos de la placa. 15,16 Se realizaron exámenes clínicos basales y se evaluaron los registros médicos electrónicos para recopilar datos demográficos, clínicos y de intervención terapéutica. Se obtuvieron muestras de sangre de acuerdo con los procedimientos estándar después del ayuno nocturno para el análisis de las variables bioquímicas. Después de someterse a una endarterectomía carotídea, se realizó un seguimiento de los pacientes para controlar la incidencia de infarto de miocardio no mortal, accidente cerebrovascular no mortal y muerte por cualquier causa hasta el 1 de julio de 2023. Las visitas de seguimiento se realizaron de acuerdo con la práctica clínica común y no se programaron. Los participantes sin visitas durante el período de seguimiento se consideraron perdidos para el seguimiento. Los eventos se adjudicaron mediante la revisión de los registros médicos electrónicos por parte de investigadores que desconocían los resultados de la pirólisis-cromatografía de gases-espectrometría de masas (y, por lo tanto, las asignaciones de grupo). El protocolo fue aprobado por el comité de revisión ética local (Università Vanvitelli Caserta). Los participantes dieron su consentimiento informado por escrito y nos adherimos a la lista de verificación de las pautas STROBE (Fortalecimiento de la presentación de informes de estudios observacionales en epidemiología) para la presentación de datos. 17
Las muestras de la placa ateromatosa que se extirparon quirúrgicamente de la región de bifurcación de la arteria carótida en la aterectomía se recogieron en tubos de vidrio y luego se congelaron en nitrógeno líquido, se fijaron en formalina tamponada al 10% o se fijaron en glutaraldehído apto para microscopía electrónica al 2,5% para análisis posteriores. La abundancia de 11 MNP diferentes se midió con pirólisis-cromatografía de gases-espectrometría de masas (una técnica cuantitativa que mide las MNP en combinación y no distingue entre microplásticos y nanoplásticos), y los resultados se corroboraron con el uso de microscopía electrónica y análisis de isótopos estables. Las muestras se analizaron a medida que estuvieron disponibles para los investigadores, que desconocían los datos de los resultados. Todos los autores aceptaron enviar el manuscrito para su publicación.
Pacientes
Los pacientes fueron elegibles si tenían entre 18 y 75 años de edad, presentaban estenosis de la arteria carótida interna de alto grado (>70%) extracraneal asintomática y estaban programados para someterse a una endarterectomía carotídea. Los criterios de exclusión fueron evidencia de insuficiencia cardíaca, defectos valvulares, neoplasias malignas o causas secundarias de hipertensión. Se excluyeron del análisis los pacientes con complicaciones en el período posoperatorio antes del alta, que tenían datos incompletos o que se perdieron durante el seguimiento.
Puntos finales
El criterio de valoración principal fue una combinación de infarto de miocardio no mortal, accidente cerebrovascular no mortal o muerte por cualquier causa entre pacientes con placa que contenía MNP y pacientes con placa que no contenía esas sustancias. Los criterios de valoración secundarios incluyeron los niveles de biomarcadores tisulares interleucina-18, interleucina-1β, factor de necrosis tumoral α (TNF-α), interleucina-6, CD68, CD3 y colágeno en pacientes con evidencia de MNP en comparación con aquellos sin ellos.
Análisis estadístico
No había datos previos con los que estimar el tamaño de la muestra. Por lo tanto, se realizó un análisis intermedio que incluyó a los primeros 100 pacientes para calcular el tamaño de la muestra. Observamos que 61 pacientes tenían evidencia de MNP en la placa y que dichos pacientes tenían un riesgo mayor de un evento de punto final primario por un factor de 2,1, que los pacientes sin MNP. Considerando un alfa de 0,05, un beta de 0,2, una tasa de eventos basal de 9 eventos por 100 personas-año en el grupo sin evidencia de MNP y un seguimiento planificado de 3 años, calculamos un tamaño de muestra de 246 pacientes, con la intención de utilizar un modelo de riesgos proporcionales en el análisis de datos. Esperábamos una pérdida del 20% durante el seguimiento y ajustamos el tamaño de la muestra a 300 pacientes.
Después del análisis de la placa aterosclerótica, los pacientes fueron asignados a uno de dos grupos: pacientes con evidencia de MNP (que tenían niveles detectables de al menos una de las dos sustancias) o pacientes sin evidencia de MNP. La distribución de las variables se evaluó con el uso de la prueba de Shapiro-Wilk. Las variables continuas se compararon entre los dos grupos con una prueba t para datos distribuidos normalmente, la prueba U de Mann-Whitney para datos distribuidos no normalmente y la prueba exacta de Fisher para variables categóricas. Se realizaron análisis de regresión lineal para estimar la asociación de la carga de MNP con marcadores de placa. Se utilizó el análisis de regresión de Cox para examinar la asociación entre la presencia de MNP dentro de la placa y la incidencia del punto final primario compuesto y se ajustó por edad, sexo, índice de masa corporal, colesterol total, colesterol de lipoproteínas de alta densidad y lipoproteínas de baja densidad, triglicéridos, creatinina, diabetes, hipertensión y eventos cardiovasculares previos. Se consideró que un valor P bilateral inferior a 0,05 indicaba significación estadística. Todos los cálculos se realizaron con el software SPSS, versión 12. Las figuras se prepararon con GraphPad Prism, versión 9.1.2.
Resultados
Estudio de población y carga de plásticos
Se examinó a un total de 312 pacientes sometidos a endarterectomía carotídea. De los pacientes examinados, 8 sufrieron un accidente cerebrovascular o murieron antes del alta hospitalaria, y 47 tenían datos incompletos o se perdieron durante el seguimiento ( Figura 1A ). De los 257 pacientes que completaron una media (±DE) de seguimiento de 33,7 ± 6,9 meses, 150 pacientes (58,4%) tenían una cantidad detectable de polietileno en la placa carotídea extirpada, y 31 de ellos (12,1%) también tenían una cantidad medible de cloruro de polivinilo en la placa carotídea. Entre los pacientes con evidencia de estos MNP en la placa, el nivel medio de polietileno fue de 21,7 ± 24,5 μg por miligramo de placa, y el nivel medio de cloruro de polivinilo fue de 5,2 ± 2,4 μg por miligramo de placa ( Figura 1B ).
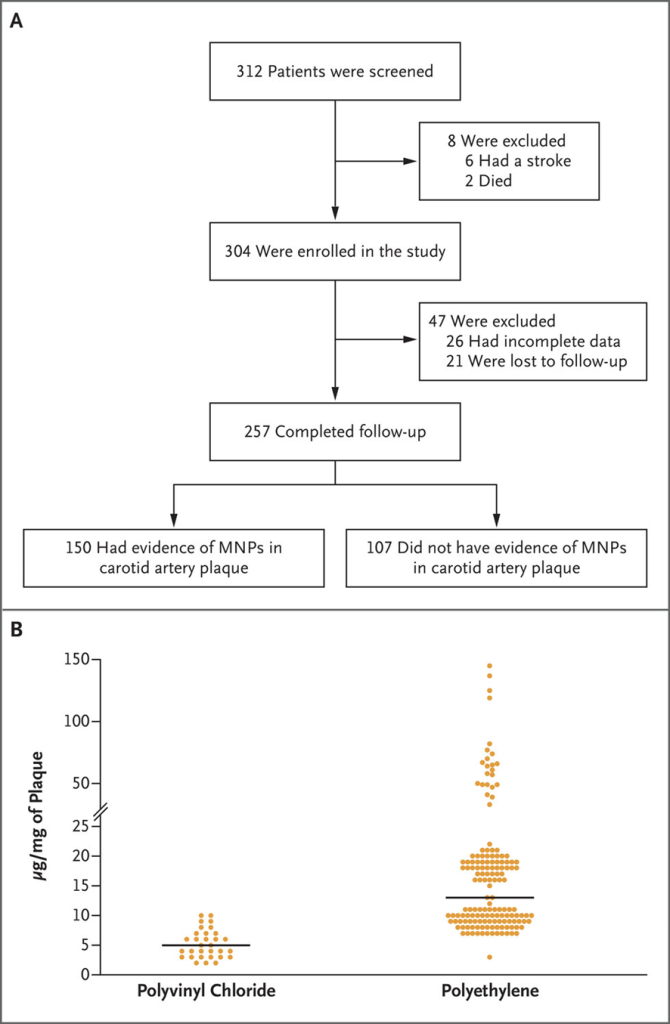
MNP en la placa de la arteria carótida.
Las características basales de los pacientes se resumen en la Tabla 1. Los pacientes con evidencia de MNP eran más jóvenes; tenían más probabilidades de ser hombres; tenían menos probabilidades de tener hipertensión; tenían más probabilidades de tener diabetes, enfermedad cardiovascular y dislipidemia; tenían más probabilidades de fumar; y tenían valores de creatinina más altos que aquellos sin evidencia de plásticos en la placa extirpada; las otras variables clínicas parecían similares en los dos grupos. No hubo diferencias aparentes en la incidencia de MNP según las áreas geográficas donde vivían los pacientes o los centros donde estaban incluidos (Fig. S2). No se encontraron diferencias sustanciales entre los pacientes que se incluyeron en el análisis y los que se excluyeron con respecto a las características clínicas de los pacientes o la prevalencia y los niveles de MNP detectados (Tabla S1).
Tabla 1

Características de los pacientes al inicio del estudio.
Microscopía electrónica y análisis con isótopos estables
Para corroborar los resultados obtenidos con la cromatografía de gases por pirólisis y la espectrometría de masas y obtener información preliminar sobre el tamaño de las partículas de MNP, evaluamos muestras de placa que fueron positivas tanto para polietileno como para cloruro de polivinilo de 10 pacientes seleccionados al azar mediante microscopía electrónica de transmisión y microscopía electrónica de barrido. La visualización con microscopía electrónica de transmisión mostró la presencia de partículas con bordes dentados que probablemente eran de origen extraño dentro de los macrófagos espumosos presentes en la placa ateromatosa y en el material amorfo de la placa ( Figura 2A y Fig. S3A). Estas partículas eran casi todas más pequeñas que 1 μm y probablemente tenían un tamaño nanométrico.
Figura 2
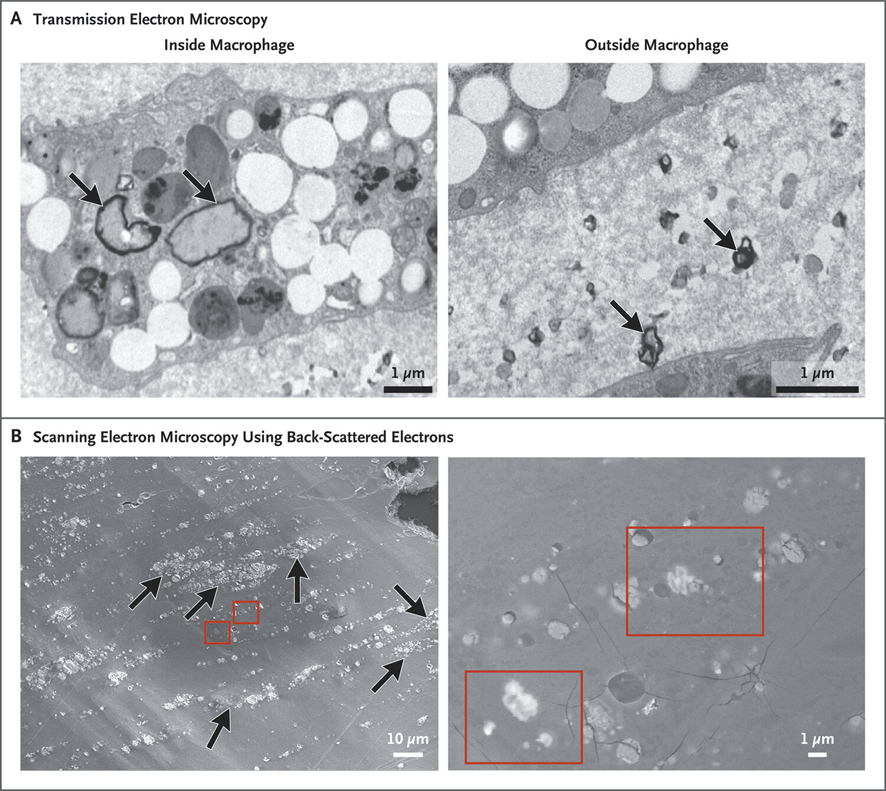
Análisis por microscopía electrónica de la placa ateromatosa.
Observando los mismos cortes utilizando los electrones retrodispersados con microscopía electrónica de barrido, hicimos mapas espectrales de rayos X de algunas partículas que se parecían a las vistas en la microscopía electrónica de transmisión con respecto al tamaño y la forma ( Figura 2B ). Estos mapas proporcionaron evidencia de una reducción en la presencia de carbono y oxígeno en las muestras de placa y una mayor presencia de cloro (Fig. S3B). Para comparar los elementos detectables en las partículas con los presentes en el fondo, obtuvimos espectros de rayos X de dos áreas idénticas y confirmamos que la concentración de cloro era mayor dentro de las partículas (Fig. S3B). Como control adicional, también comparamos el contenido de cloro en dos áreas idénticas adyacentes que estaban desprovistas de partículas y encontramos que los niveles de cloro eran similares (Fig. S3C). Dada la probable naturaleza no biológica del cloro en estado sólido, estos resultados pueden confirmar depósitos de cloruro de polivinilo. Otro ejemplo de tales partículas se muestra en la Figura S3D; muestras de 4 de los 10 pacientes evaluados tenían niveles de cloro detectables con este patrón.
Se realizó un análisis de isótopos estables en 26 muestras aleatorias de placa de pacientes porque los plásticos derivados del petróleo tienen valores de δ 13 C más bajos (la relación entre el carbono 13 y el carbono 12) que los tejidos humanos. 18 Este análisis identificó dos grupos distintos de pacientes: un grupo con valores isotópicos más altos de δ 13 C y otro con valores más bajos, que indicaron relaciones más altas y más bajas, respectivamente, de carbono 13 a carbono 12. Los valores isotópicos más bajos de δ 13 C podrían deberse a la contaminación con MNP, ya que el material derivado del petróleo tiene una señal isotópica más baja que la de los tejidos humanos. Los valores isotópicos más bajos de δ 13 C fueron más evidentes en la placa que tenía evidencia de MNP (Fig. S4).
Fenotipo de placa
Debido a que los datos previos sugirieron que las MNP pueden inducir vías proinflamatorias, 13 cuatro marcadores inflamatorios —interleucina-18, interleucina-1β, interleucina-6 y TNF-α— se midieron con el uso de un ensayo inmunoabsorbente ligado a enzimas ( Figura 3A a 3D ). El contenido de colágeno de las muestras de placa ( Figura 3E ) y los niveles de CD3 ( Figura 3F ) y CD68 ( Figura 3G ), dos marcadores de infiltración de linfocitos y macrófagos, respectivamente, se evaluaron mediante un ensayo inmunohistoquímico. El análisis de regresión lineal reveló una correlación entre la cantidad de polietileno presente y los niveles de expresión de estos marcadores (Fig. S5). Los resultados de estos análisis, estratificados según la presencia de polietileno solo o en combinación con cloruro de polivinilo, se muestran en la Figura S6.
Figura 3

Marcadores inflamatorios en muestras de placa.
Eventos cardiovasculares
Un evento de punto final primario (infarto de miocardio no fatal, accidente cerebrovascular no fatal o muerte por cualquier causa), ocurrió en 8 de 107 pacientes (7.5%) en el grupo que no tenía evidencia de MNP (2.2 eventos por 100 pacientes-año) y en 30 de 150 pacientes (20.0%) en el grupo que tenía evidencia de MNP (6.1 eventos por 100 pacientes-año) a los 33.7 ± 6.9 meses. La incidencia de componentes individuales del punto final compuesto se muestra en la Tabla S2. Los pacientes con MNP en placa tuvieron un riesgo mayor de tener un evento de punto final primario que los pacientes sin evidencia de MNP (cociente de riesgos, 4.53; intervalo de confianza del 95% [IC], 2.00 a 10.27; P < 0.001) ( Figura 4 ), como lo muestra el análisis de regresión de Cox con ajuste para factores de riesgo para enfermedad cardiovascular (Tabla S3). El cociente de riesgo no ajustado fue de 2,84 (IC del 95 %, 1,50 a 5,40; P = 0,007). Cuando se analizaron los niveles de MNP como una variable continua, los resultados mostraron una asociación con el punto final primario (Tabla S4).
Figura 4
Asociaciones entre la presencia de MNP y eventos cardiovasculares.
Discusión
Entre los pacientes con estenosis de la arteria carótida de alto grado asintomática (>70%) que se sometieron a una endarterectomía carotídea, aquellos con evidencia de MNP dentro de la placa carotídea tuvieron una mayor incidencia de un compuesto de infarto de miocardio, accidente cerebrovascular o muerte por cualquier causa que los pacientes que no tenían evidencia de MNP dentro del ateroma. Los datos observacionales de los estudios de exposición ocupacional sugieren un mayor riesgo de enfermedad cardiovascular entre las personas expuestas a la contaminación relacionada con los plásticos, incluido el cloruro de polivinilo, que el observado en la población general. 19-21 Los datos mecanicistas de los modelos preclínicos han propuesto tanto la translocación directa de MNP a la circulación como los mecanismos indirectos como posibles fundamentos de los efectos tóxicos cardiovasculares observados con MNP, como se ha observado con otras nanopartículas como las nanopartículas de oro inhaladas de tamaño similar a las MNP. 22 Una serie de estudios en ratones y ratas mostraron una amplia distribución de MNP después de la inhalación y la ingestión, con acumulaciones constantes en órganos altamente vascularizados y el corazón. 23,24 El tamaño de partícula influye en la capacidad de las MNP para llegar a múltiples tejidos. Según una declaración de la Organización Mundial de la Salud, las MNP mayores de 150 μm o 10 μm de diámetro, respectivamente, no se absorben en la sangre y no penetran en los vasos sanguíneos. 25 Nuestros hallazgos sugieren que los nanoplásticos, en lugar de los microplásticos, podrían acumularse en sitios de aterosclerosis. De hecho, la gran mayoría de las partículas detectadas en el estudio actual también estaban por debajo del umbral de 200 nm sugerido para el intestino y otras barreras y eran visibles en el espacio extracelular como desechos dispersos, lo que se alinea con la noción de que la absorción y distribución de MNP aumentan a medida que disminuye el tamaño de partícula. 26 Los datos de estudios en humanos han demostrado que se han detectado MNP de hasta 30 μm de tamaño en muestras de hígado, hasta 10 μm en muestras de placenta, hasta 88 μm en muestras de pulmón, hasta 12 a 15 μm en leche materna y orina, y más de 700 nm en sangre completa. 7-12
En términos cualitativos, el análisis por pirólisis, cromatografía de gases y espectrometría de masas indicó que, entre las 11 MNP analizadas, se detectaron polietileno y cloruro de polivinilo en la placa carotídea en cantidades de microgramos (μg por miligramo de placa). Estudios previos que utilizaron la misma tecnología mostraron que se encontró polietileno en aproximadamente el 25% de las muestras de sangre completa derivadas de voluntarios sanos, con una concentración máxima de 7,1 μg por mililitro. 12 Otros estudios han sugerido que el polietileno y el cloruro de polivinilo también fueron las MNP más abundantes encontradas en la leche materna y la orina humanas, 10,11 con fibras de polietileno observadas en el tejido pulmonar humano en una concentración de 1 partícula por gramo de tejido. 8 También se ha demostrado la presencia de cloruro de polivinilo en un número constante de muestras de hígado obtenidas de pacientes con enfermedad cirrótica, en el rango de unas pocas partículas por gramo de tejido. Se ha informado que los nanoplásticos de polietileno inducen una variedad de efectos nocivos en el sistema cardiovascular en embriones de pez cebra, promoviendo el desarrollo de derrames pericárdicos, la inhibición de la angiogénesis y la inducción de un estado protrombótico. 27 Hay datos similares disponibles de estudios de los efectos del cloruro de polivinilo. 28 Sin embargo, en la mayoría de los estudios preclínicos, se evalúan altos niveles de MNP, órdenes de magnitud más allá de los observados en el presente estudio, un factor que dificulta la extrapolación de la relevancia de los hallazgos preclínicos para los humanos.
El polietileno y el cloruro de polivinilo, en sus diversas formas, se utilizan en una amplia gama de aplicaciones, incluida la producción de envases de alimentos y cosméticos y tuberías de agua. Se han encontrado MNP en el agua potable, una amplia gama de alimentos, productos cosméticos y aire, también en una forma unida a partículas finas inhalables con un diámetro aerodinámico de 2,5 μm o menos (PM 2,5 ) y transportadas largas distancias por el viento. 5,6,29,30 Dada la amplia distribución y disponibilidad de MNP, la atribución de todas las fuentes potenciales en humanos es casi imposible. Nuestro estudio no fue diseñado específicamente para explorar las posibles fuentes de plásticos subyacentes a la presencia de MNP dentro de la placa carotídea. La comparación de datos sobre la base de las ubicaciones de los hogares de los pacientes y de los centros de reclutamiento no reveló diferencias obvias. De manera similar, no podemos establecer por qué solo se detectaron polietileno y cloruro de polivinilo, entre los 11 tipos de plásticos evaluados. Los estudios en modelos animales sugieren que las características fisicoquímicas de diferentes MNP influyen en si alcanzan órganos distantes. 30,31 Se necesitan estudios adicionales para evaluar si el polietileno y el cloruro de polivinilo se acumulan preferentemente dentro de la placa y si son más patógenos que otros tipos de MNP en este sentido.
Es importante señalar que nuestros resultados no prueban causalidad. La asociación entre la presencia de MNP dentro de la placa y la incidencia de un compuesto de resultados de enfermedad cardiovascular o muerte también puede implicar el riesgo de exposición a otras variables de confusión residuales no medidas, como exposiciones desconocidas durante el curso de la vida del paciente o, más ampliamente, el estado de salud y los comportamientos de los pacientes. Además, no consideramos los niveles de exposición a PM 2.5 y PM 10 , que es un factor de riesgo emergente para la enfermedad cardiovascular. 31
Nuestro estudio tiene limitaciones. A pesar de las medidas preventivas adoptadas, no se puede descartar firmemente la contaminación del laboratorio. Aunque aplicamos procedimientos actualizados para recolectar y analizar muestras de placa, podría existir el riesgo residual de contaminación. Estudios futuros realizados con el uso de salas limpias, donde no hay plástico en ninguna forma excepto el material en estudio, podrían corroborar nuestras observaciones. No teníamos datos socioeconómicos disponibles para nuestra población de estudio. Los ingresos y la educación, entre otras condiciones, están vinculados a una amplia gama de resultados y podrían ser particularmente relevantes. 32 Nuestros hallazgos pertenecen solo a una población de pacientes asintomáticos sometidos a endarterectomía carotídea, que pueden no ser representativos de la población general. 14 Por lo tanto, nuestros hallazgos pueden no ser generalizables. La representatividad de los pacientes que participaron en el estudio se muestra en la Tabla S5. No exploramos las variables de alimentos y agua potable, que pueden estar vinculadas a la acumulación de MNP en humanos. 25,33,34 Por lo tanto, es posible que el papel putativo de las MNP en el impulso de la enfermedad cardiovascular pueda ser limitado si se compara con los factores de riesgo canónicos, dado que durante un período de décadas en el que la exposición a los plásticos presumiblemente ha ido aumentando, la tasa de enfermedad cardiovascular ha ido disminuyendo. 35
Sin embargo, los resultados de nuestro estudio muestran que los pacientes con MNP que se detectaron en la placa de la arteria carótida tienen un mayor riesgo de un punto final compuesto de infarto de miocardio, accidente cerebrovascular o muerte por cualquier causa a los 34 meses de seguimiento.
Eficiencia en Triage Virtual: Inteligencia Artificial en Salud
Medicina Digital volume 7, 381 (2024)
Nota del Blog: El triage para el ordenamiento de las prioridades de ingreso a los sistemas de salud, de acuerdo a la gravedad, hace varias décadas se viene aplicando, el agregado a este sistema reglado y probado de Machine Learning permite hacer más eficiente el sistema y muestra una aplicación de inteligencia artificial que promete mejora, eficiencia y equidad en la organización de la atención. Por ello, se incluye en este capítulo creado el año 2024 de estudio y actualización de la AI que cambiará los esquemas, los flujos de pacientes, el seguimiento y la coparticipación. Para bien, faltará ver algunos otros aspectos ya que esto es un servicio que tiene su costo de inversión, por lo tanto es para sistemas que estén integrados, porque no habría forma de remunerarlos. Hace un tiempo, nuestro sistema de atención desarrollo un bot que da prioridad a algunos pacientes en los lugares donde pueden ser con mayor celeridad.
Resumen:
Los sistemas de acceso inteligente y autotriage para pacientes en servicios de emergencia han estado en desarrollo durante décadas. Hasta el momento, los sistemas de salud no han publicado ningún LLM para el procesamiento de datos de pacientes auto informados. Muchos sistemas expertos y modelos computacionales se han lanzado a millones de personas y países. Esta revisión es la primera en resumir el progreso en el campo, incluyendo un análisis de las soluciones exactas de autotriage disponibles en los sitios web de 647 sistemas de salud en los Estados Unidos.
Introducción
Hoy en día, los pacientes se benefician de los sistemas de autotriage digital, admisión automatizada, diagnóstico diferencial y caracterización de enfermedades1,2,3,4,5,6,7,8,9,10,11,12. Antes de estos sistemas automatizados, los pacientes han tenido que navegar por la toma de decisiones sanitarias apoyada en los límites de su propio conocimiento, los navegadores de búsqueda en Internet y de las personas con las que contactan, en particular los profesionales médicos. Los centros de llamadas de enfermería han existido durante décadas (Fig. 1). Estos servicios permitieron a los pacientes llamar a un número, informar sobre sus síntomas/afecciones y recibir información para respaldar sus decisiones de atención médica (es decir, Apoyo para la Decisión del Paciente (PDS)). Los protocolos de triage telefónico más ampliamente adoptados son los protocolos de triage telefónico (STP) de Schmitt-Thompson, que hoy en día alimentan el 95% de los centros de llamadas de enfermería en todo el país y se utilizan en >200 millones de encuentros13,14,15.
Los STP son un conjunto de reglas de triage que ayudan a determinar si se necesita atención y, de ser así, específicamente qué tipo de atención. Resuelven entre los servicios médicos de emergencia (911), las salas de emergencia, los centros de atención de urgencia y los PCP. ¿Cuántos de nosotros hemos dudado de qué cuidado buscar o si buscarlo en absoluto cuando estamos enfermos?
El propósito de estos STP es estandarizar y mejorar la precisión de la orientación que los profesionales médicos dan por teléfono en un libro de texto publicado por la Academia Americana de Pediatría que se sigue manteniendo14,15. A medida que las líneas de enfermería se convirtieron en una oferta omnipresente en todas las aseguradoras y sistemas de salud, el PDS se convirtió en sólido16,17. A medida que mejoraron las capacidades tecnológicas, la automatización de estas reglas se convirtió en una opción y un medio más sencillo para que los pacientes se autoapoyaran18,19.
Fig. 1: Cronología para el desarrollo de sistemas de inteligencia artificial que utilizan datos autoinformados por los pacientes.
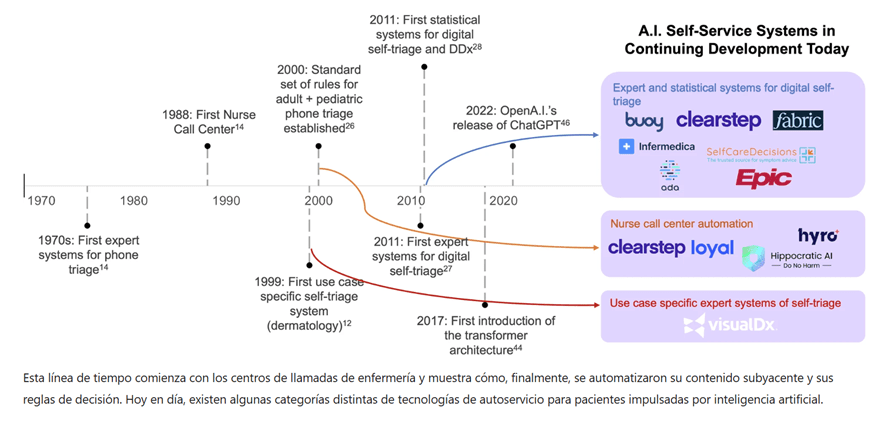
Esta línea de tiempo comienza con los centros de llamadas de enfermería y muestra cómo, finalmente, se automatizaron su contenido subyacente y sus reglas de decisión. Hoy en día, existen algunas categorías distintas de tecnologías de autoservicio para pacientes impulsadas por inteligencia artificial.
Estos sistemas de «triage virtual», que inicialmente ayudaban con la admisión y el triage, estuvieron entre los primeros mecanismos para que los pacientes informaran por sí mismos sus síntomas y recibieran PDS. Sin embargo, la automatización tuvo una contrapartida. El aumento de la velocidad, el anonimato y la comodidad se produjo a costa de una menor capacidad para aclarar e interpretar las respuestas a través de un profesional médico por teléfono 4,9,10,19,20. Por otro lado, el sistema de salud también podría ahorrar dinero optimizando mejor el uso de sus centros de llamadas10.
A medida que la disponibilidad de datos y la capacidad tecnológica mejoraron, también lo hicieron los métodos estadísticos computacionales. Las computadoras fueron programadas para realizar tareas típicamente reservadas a la inteligencia humana (Inteligencia Artificial, IA)21. Eventualmente, se crearon métodos que permitieron a las computadoras aprender de grandes cantidades de datos y generalizar dichos aprendizajes para completar tareas (Machine Learning—ML)22. Si se combina esto con la capacidad de las computadoras para procesar la entrada de lenguaje natural por parte de los usuarios (Procesamiento del Lenguaje Natural, PLN), se establecieron los componentes básicos para motores de diagnóstico diferencial más potentes y capacidades de caracterización de enfermedades 23,24. Finalmente, se desarrollaron el transformador y los grandes modelos de lenguaje (LLM), lo que llevó a otro punto de inflexión 25,26,27. El procesamiento y la generación del lenguaje natural alcanzaron nuevas alturas con la «IA generativa» y la automatización ya no requería una compensación en la capacidad de aclarar o interpretar el lenguaje ingresado por el paciente. Sin embargo, aún existen brechas relacionadas con la alucinación, la interpretabilidad, la validación y la precisión21,29.
La ingesta automatizada, el triage virtual y la predicción diagnóstica diferencial florecieron en la industria y en el mundo de las empresas emergentes 30,31,32,33,34 gracias al hecho de que la FDA ha pasado por múltiples períodos de revisión de borradores de directrices, pero aún no tiene una guía obligatoria sobre los sistemas PDS 35,36. Este artículo de perspectivas profundizará en los matices de los sistemas de triage virtual y diagnóstico diferencial auto informados. Se discutirán varios enfoques para construir, validar y mejorar ambos. Se detallarán las ventajas y desventajas de los sistemas basados en reglas frente a los basados en ML (Tabla 1). Por último, se analizará el panorama regulatorio y las direcciones futuras.
Tabla 1 Ventajas y desventajas de los sistemas expertos y los métodos de aprendizaje estadístico para el autotriaje por parte de los sistemas de salud
| Sistemas basados en expertos | Aprendizaje automático estadístico | ||||
| Ventajas | Desventajas | Ventajas | Desventajas | ||
| Consideraciones importantes sobre las soluciones de autotriage para los sistemas de salud | Validación | Los STP han sido probados en >200 millones de encuentros de enfermería durante 20+ años12,83. | Requiere que un panel de médicos repita la determinación de las reglas exactas. No existe un estándar de oro para el auto-triaje. Lo más parecido es el triaje telefónico84. | Los sistemas de clasificación estadística utilizan grandes conjuntos de datos para entrenar modelos (a menudo una red neuronal) para calcular un nivel de clasificación. El origen de estos conjuntos de datos es desconocido en la literatura85,86. | Los sistemas de triaje estadístico han existido durante ~ 10 años en contraste con los 20+ años de los sistemas de triaje expertos. Naturalmente, están menos validados63,83. |
| Sigue las pautas de mejores prácticas clínicas | El campo de la Medicina de Urgencias y Emergencias se centra en el triaje. Capaz de codificar el conocimiento experiencial adquirido en el campo18,87. | Es posible que haya patrones de clasificación que aún no han sido descubiertos por los humanos para la codificación88. | Potencial para identificar patrones de clasificación que optimicen la utilización mínima de recursos y la máxima probabilidad de resolución de síntomas18,89,90,91,92. | El triaje no tiene un «estándar de oro». Por lo tanto, no hay una «respuesta correcta» con la que etiquetar los datos de entrenamiento93. | |
| Mejora a lo largo del tiempo | Los sistemas pueden tener sus propias reglas para el triaje que varían según los recursos disponibles en las instalaciones. Los sistemas expertos permiten esta configurabilidad94. | La mejora a lo largo del tiempo requiere un muestreo aleatorio de encuentros reales de triaje y refuerzo humano. También requiere prestar atención a las distribuciones de triaje a nivel poblacional y ajustarlas según sea necesario95. | Si se proporciona retroalimentación sobre la corrección del triaje de un paciente individual, los sistemas basados en el aprendizaje automático pueden permitir una mejora más automatizada con el tiempo96,97. | No existe un conjunto estándar de datos «específicos de triaje» en el EMR. El hecho de que un paciente individual haya ido a X ubicación, no significa que fuera la ubicación «correcta» para su atención. El EMR no contiene información directa sobre si ese sitio de atención era o no «correcto» o si otro habría sido más apropiado98,99,100,101,102,103,104,105,106,107,108,109. | |
| Explicabilidad | Cualquier predicción puede ser examinada para determinar las reglas exactas que condujeron a ella y ajustarse según sea necesario110. | Si se encuentra un problema con el triaje, es difícil entender exactamente por qué se proporcionó esa recomendación y ajustar esa vía específica111. | |||
| Largura | Hace menos preguntas en general (promedio: 17.5)63. | Hace más preguntas (promedio: 29.2)63. | |||
Clasificación
Definición
El término médico para triaje proviene del verbo francés trier, que significa clasificar o separar37,38. En consecuencia, el triaje es un proceso de asignación de prioridad a los tratamientos de un paciente en función de la gravedad de su afección. Este proceso ayuda a asignar recursos médicos limitados y se utiliza en una variedad de entornos37. Después de su desarrollo y uso en tiempos de guerra, el triaje se generalizó para entornos de emergencia en la vida civil39. El triaje se utiliza habitualmente en los servicios de urgencias para determinar el orden en que se atiende a los pacientes40. De manera más general, los proveedores de atención primaria (PCP, por sus siglas en inglés) deben clasificar qué pacientes pueden ser tratados por ellos y cuáles pacientes deben ser tratados por especialistas. Si bien los hospitales o sistemas individuales pueden desarrollar sus propias reglas para apoyar la toma de decisiones de los médicos de atención primaria, no existe un conjunto estandarizado de pautas clínicas que determinen exactamente qué pacientes deben ser remitidos a especialistas41. Hoy en día, los pacientes deben decidir acceder a la atención entre una lista cada vez mayor de servicios de emergencia, salas de emergencia, centros de atención de urgencia, clínicas ambulatorias/minoristas, proveedores de telemedicina, consultorios de atención primaria, consultorios especializados y más. Como resultado, entre el 20 y el 40% del gasto sanitario se desperdicia cada año en una utilización innecesaria de la asistencia sanitaria42. Para minimizar el uso de recursos, es necesario permitir que los pacientes se autoclasifiquen mejor. La tecnología digital orientada al paciente ha hecho posible que el PDS se proporcione en formatos fáciles de usar para el paciente. Por lo general, hay dos clases de sistemas de clasificación virtual: (1) sistemas basados en reglas y (2) sistemas basados en aprendizaje automático. Cada una de estas dos clases ofrece ciertas ventajas y desventajas que se analizarán en las siguientes subsecciones.
Sistemas de autoclasificación basados en reglas
Los sistemas de triaje virtual basados en reglas emplean un conjunto de reglas empíricas, diseñadas por profesionales médicos, para guiar a los pacientes con un conjunto específico de signos, síntomas y afecciones al sitio de atención más apropiado dentro del período de tiempo más apropiado. Los hospitales o sistemas de salud individuales pueden diseñar sus propias reglas para ayudar a los médicos de atención primaria a determinar qué pacientes deben ser derivados a qué especialistas41,43. Sin embargo, el primer conjunto de reglas de triaje adoptado a nivel nacional fue para el triaje telefónico44. La mayoría de los sistemas de salud en los EE.UU. confían en los protocolos basados en reglas desarrollados por los Dres. Barton Schmitt y David Thompson para el triaje telefónico de pacientes (STPs)45. Los sistemas basados en reglas sirven para codificar el conocimiento médico y la experiencia acumulada a lo largo de la vida útil de la medicina clínica y permiten una completa configurabilidad y explicabilidad de cualquier triaje. Los STP se han utilizado en >200 millones de encuentros con centros de llamadas de enfermería45. Las desventajas de los sistemas basados en reglas son que son laboriosos de crear, requieren un proceso de reconciliación entre varios médicos, complicado por el hecho de que no existe un estándar de oro de triaje y existe una variación inherente entre la forma en que los diferentes profesionales médicos podrían clasificar a los pacientes, y que la precisión del triaje se limitaría a la precisión de los humanos que desarrollan las reglas.. Algunas soluciones han llevado a cabo este proceso de conciliación para estandarizar mejor las reglas exactas que indicarían qué pacientes deben ver a un especialista en comparación con un médico de atención primaria (Tabla 2). Estas soluciones utilizan árboles de decisión o gráficos de conocimiento para impulsar las experiencias de autoclasificación que están codificadas con las pautas de mejores prácticas clínicas tal como se han desarrollado y validado hasta la fecha (por ejemplo, STP).
Sistemas de autoclasificación basados en aprendizaje automático (ML)
A diferencia de los sistemas basados en reglas que utilizan reglas de decisión empíricas, un enfoque basado en ML para el triaje virtual depende de entrenar un modelo con un gran conjunto de datos de pacientes para predecir el sitio de atención más apropiado para que esa persona acuda. Con muchos de los enfoques estadísticos, a menudo es difícil proporcionar las respuestas exactas de los pacientes que condujeron a su resultado de triaje (por ejemplo, redes neuronales, aprendizaje profundo, basado en transformadores)47. Esto afecta a la explicabilidad e interpretabilidad de los enfoques estadísticos de aprendizaje automático (ML). Ciertos enfoques estadísticos pueden permitir cierta explicabilidad (por ejemplo, enfoques de redes no neuronales como los modelos de regresión y la importancia de las características basadas en árboles)48,49. Estas son limitaciones típicas de los enfoques basados en ML en general.
Uno de los desafíos al etiquetar conjuntos de datos para el aprendizaje supervisado es que puede ser difícil establecer una «respuesta correcta» para la clasificación. Esto se debe a que diferentes proveedores de atención médica (HCP, por sus siglas en inglés) clasificarían a ciertos pacientes de manera diferente46. Como resultado, los datos de entrenamiento disponibles están sujetos a variabilidad. Además, no hay consenso sobre la base para concluir que un paciente fue clasificado «con éxito». Numerosos centros de prestación de servicios de salud podrían resolver el problema de un paciente (Recuadro 1). Teóricamente, el autotriaje perfectamente preciso siempre indicaría al paciente el sitio óptimo de atención al menor costo. Por el contrario, una autoclasificación inexacta daría lugar a más puntos de contacto innecesarios y a un mayor coste. La mejor práctica actual en este campo del triaje son las reglas en las que se ha confiado en los centros de llamadas de enfermería durante las últimas décadas (STP). Las métricas de éxito podrían incluir el número de visitas necesarias para resolver/manejar el problema médico de un paciente o el costo de la atención brindada a los pacientes (Recuadro 1). Estas dos métricas podrían combinarse en una proporción. Sugerimos esta proporción con la idea de que una atención médica «exitosa» resolvería idealmente la inquietud médica de un paciente utilizando los recursos mínimos de atención médica para hacerlo. Usando alguna medida definida de éxito, los modelos de aprendizaje automático podrían entrenarse para recomendar ciertos niveles y tiempos de atención. A modo de ejemplo, podríamos crear un modelo que minimice las derivaciones a otros cuidados y la utilización de los recursos sanitarios.
Mostrar menos
El uso de modelos de lenguaje de gran tamaño para la autoclasificación
Noviembre de 2022 marcó un punto de inflexión en lo que era posible con la IA con el lanzamiento de ChatGPT y la posterior ola de proliferación de LLM en todas las industrias. La capacidad de los LLM para procesar y convertir entradas en salidas atractivas y similares a las humanas marcó un punto de inflexión en lo que era posible con las experiencias conversacionales automatizadas con pacientes que informaron el deseo de usar LLM para consultas relacionadas con la atención médica50.
Hasta ahora, los LLM han sido evaluados por su relación con los pacientes, su triaje y precisión DDx en general, y su utilidad para la autoeducación y el autodiagnóstico del paciente en una colección de casos de uso específicos (p. ej., COVID51, oftalmología52, apnea obstructiva del sueño53, sialendoscopia54). Sin embargo, el uso comercial de los LLM en la atención médica se ha limitado en gran medida a la documentación clínica y otras funciones administrativas del lado del proveedor. El lado de cara al paciente aún no ha demostrado el mismo nivel de adopción.
Gran parte de la lentitud en la adopción por parte del paciente se ha debido a una serie de preocupaciones con los LLM, que incluyen, entre otros, las tasas de alucinación, la consistencia de la respuesta, la interpretabilidad, la regulación y los derechos de autor55. Se descubrió que ChatGPT tenía una precisión del 63% en promedio en 10 categorías de razonamiento diferentes56. En la atención médica, el riesgo de una recomendación incorrecta tiene un costo para la salud del paciente. Por lo tanto, es imperativo que los pacientes y los profesionales de la salud tengan la capacidad de interpretar las razones exactas de la predicción/recomendación de un modelo. En general, este es un inconveniente de los enfoques de ML para el triaje o diagnóstico autoinformado por el paciente57.
Considerable work is being done to evaluate the full scope of LLMs’ viability in healthcare. Levine et al. compararon la precisión del triaje y el diagnóstico de GPT-3 con un conjunto estandarizado de viñetas utilizadas históricamente para evaluar la precisión de los sistemas de autotriaje. GPT-3 realizó diagnósticos a niveles cercanos, pero inferiores a los de los médicos y mejores que los de los profanos. El modelo tuvo un desempeño menos bueno en el triaje, donde su desempeño estuvo más cerca del de los legos y por debajo del de los clínicos58. Hirosawa et al. evaluaron la precisión diagnóstica de los diagnósticos diferenciales generados por GPT-3 en una colección de quejas principales comúnmente reportadas y encontraron que GPT-3 es un 40% menos preciso en promedio en comparación con el juicio de los médicos59. Chiesa-Estomba et al. evaluaron el potencial de GPT-3 como herramienta de apoyo para la toma de decisiones clínicas en sialendoscopia y el apoyo a la información al paciente. Se encontró que GPT-3 tiene una fuerte concordancia con los especialistas en otorrinolaringología54. Cuando se compararon las respuestas a las preguntas de los pacientes de GPT-3 con las de los médicos, los pacientes informaron que las respuestas del LLM fueron un 10× más empáticas que las de los médicos60. Además, los pacientes encuestados indicaron el deseo de utilizar los LLM para consultas relacionadas con la atención sanitaria50. Con todo, los LLM tienen un progreso significativo que hacer para lograr una precisión comparable a la de los médicos en casos de uso de autotriaje y autodiagnóstico, han demostrado una clara demanda de los pacientes y han superado a los médicos en la empatía de sus respuestas. Dejando a un lado la regulación, existe un claro potencial para el uso de LLM en los espacios de autotriaje y autodiagnóstico.
Panorama regulatorio de la FDA
Actualmente, los sistemas de apoyo a la toma de decisiones que hacen uso de los datos autoinformados por los pacientes no están regulados por la FDA. Sin embargo, la FDA ha publicado varias iteraciones de borradores de directrices que han estado abiertas a comentarios públicos 36. A través de estas iteraciones ha habido varios desarrollos. Inicialmente, el borrador de las directrices separaba el SPD y los sistemas de apoyo a la decisión clínica (CDS) como dos categorías diferentes61. Sin embargo, estas dos categorías se han fusionado ahora en una categoría más amplia de CDS36. Los CDS son aquellos que cumplen con los siguientes cuatro criterios: El sistema «(1) no está destinado a adquirir, procesar o analizar una imagen médica o una señal de un dispositivo de diagnóstico in vitro o un patrón o señal de un sistema de adquisición de señales (2) está destinado a mostrar, analizar o imprimir información médica sobre un paciente u otra información médica (3) está destinado a apoyar o proporcionar recomendaciones a un profesional de la salud sobre la prevención, el diagnóstico o el tratamiento de una enfermedad o afección y (4) tiene el propósito de permitir que un profesional de la salud revise de forma independiente la base de las recomendaciones que presenta dicho software, de modo que no sea la intención que el profesional de la salud se base principalmente en cualquiera de dichas recomendaciones para hacer un diagnóstico clínico o una decisión de tratamiento con respecto a un paciente individual36.
Los sistemas que se ajustan a estos cuatro criterios están exentos de la regulación de la FDA. Tenga en cuenta que el último de estos criterios tiene implicaciones importantes en la arquitectura de los sistemas de clasificación y DDx exitosos. Permitir que los pacientes vean la base por la cual se les recomienda la información es más difícil para los sistemas que operan con un enfoque de ML en comparación con los que se basan en reglas. Si el enfoque específico de ML no puede ajustarse a este cuarto criterio, entonces no estaría exento de la regulación de la FDA y estaría sujeto a un mayor escrutinio. Esto requeriría mayores recursos para llevar con éxito los sistemas basados en ML para su uso generalizado con los pacientes. En caso de que el borrador de las directrices de apoyo a las decisiones clínicas de la FDA se convierta en ley, los sistemas híbridos o basados en normas pueden tener una ventaja desde el punto de vista regulatorio. Una limitación de esta revisión es su enfoque en el sistema de salud de los Estados Unidos. No incluye una visión general de la reglamentación de otras regiones del mundo que pueda ser objeto de trabajos futuros.
Desafíos y rumbos futuros
La generalización de la IA a la práctica clínica sigue siendo una incógnita62. En la literatura se han reportado muchos modelos diferentes de ML por su capacidad para superar a los humanos en entornos médicos, sin embargo, pocos se han generalizado para un uso clínico amplio62. A menudo, estos modelos no funcionan tan bien cuando se generalizan a la población en general. Nuestra hipótesis es que los enfoques más exitosos emplearán una metodología híbrida de conocimiento empírico y métodos estadísticos. En pocas palabras, el uso de los siglos de experiencia médica humana para codificar reglas que generalmente son aceptadas por la mayoría de los expertos médicos probablemente permitiría que los sistemas alcancen niveles de precisión comparables a los clínicos humanos. Luego, la construcción de capas estadísticas sobre estas reglas empíricas permitiría a los sistemas avanzar en la precisión más allá de la capacidad humana y, al mismo tiempo, permitir más experiencias conversacionales.
Los datos publicados sobre el rendimiento de los sistemas de autoclasificación son limitados. El artículo seminal que comparó la precisión de varios sistemas de diagnóstico y triaje estadísticos y basados en el conocimiento encontró que, entre 23 verificadores de síntomas, el diagnóstico correcto se proporcionó primero en el 34% (IC: 3%) de un conjunto de viñetas de pacientes estandarizadas, en los 20 diagnósticos principales en el 58% (IC: 3%) de las viñetas, y el triaje apropiado en el 57% (IC: 5%) de viñetas63. Un estudio posterior que comparó 37 sistemas reportó resultados similares64. El rendimiento del triaje disminuyó con la urgencia decreciente de la condición63. La precisión de los sistemas de triaje para escenarios emergentes fue de 2 a 3× mayor que en escenarios de autocuidado63. Por otra parte, la precisión varió ampliamente como El rendimiento en los consejos de triaje adecuados de 24 verificadores de síntomas varió del 33 al 90%63,64,65.
Esta amplia variación en la precisión de los sistemas de auto-triaje revela una de sus limitaciones. Es posible que la autoevaluación inexacta aumente los puntos de contacto totales y el costo. Para ilustrar este punto, se puede llevar a cabo un experimento mental con los siguientes grupos: (a) usuarios de un sistema de auto-triaje «ficticio» que asigna aleatoriamente un triaje a cada paciente y (b) usuarios de un sistema de auto-triaje «perfecto» que es capaz de optimizar perfectamente todos los factores de precisión clínica, seguro, preferencias del paciente, preferencias del proveedor y preferencias de la red. Una hipótesis es que los usuarios de (a) son rebotados en el sistema con más frecuencia. Posiblemente hasta que tengan la suerte de estar con el proveedor adecuado para su necesidad. Por el contrario, a los usuarios de (b) siempre se les presentaría el proveedor exacto para su necesidad clínica inmediata, minimizando así el número de puntos de contacto, el costo y el tiempo invertido para recibir esa atención óptima. Aún no se ha informado sobre el efecto de los sistemas de auto-triaje en el promedio # de puntos de contacto con el paciente en el sistema de salud, el costo promedio de la atención general o en los resultados clínicos. En cualquier caso, cualquier estudio que examine estos resultados del autotriaje también tendrá que tener en cuenta la variación en la precisión en función del sistema de triaje individual utilizado.
Un estándar de oro de la precisión del triaje es el juicio de los médicos humanos. Existen estudios que evalúan la concordancia de los sistemas de auto-triaje y diagnóstico con los profesionales médicos. Se ha encontrado que varios sistemas con capas basadas en reglas y ML funcionan al menos tan bien como los médicos46,66. A medida que se prueban más métodos estadísticos, los sistemas de auto-triaje y diagnóstico continúan mejorando. Un grupo planteó la hipótesis de que los médicos pasan más tiempo descartando que dentro. Así, se encontró que un sistema contrafáctico es más preciso que uno inferencial67. Además, a medida que se cree una mayor conectividad entre estos sistemas y la historia clínica electrónica (EMR), aumentará la retroalimentación. Los sistemas de auto-triaje pueden comenzar a optimizarse para obtener referencias y costos mínimos, al tiempo que maximizan la resolución y la satisfacción. Están surgiendo sistemas híbridos basados en reglas y ML46. Eventualmente, la integración con la tecnología portátil y de sensores facilitará la incorporación de información objetiva sobre el estado de salud de una persona, mejorando aún más la precisión. Comprender las compensaciones entre varios métodos basados en reglas y ML será fundamental para diseñar sistemas PDS autoguiados exitosos. Además, navegar por el panorama regulatorio emergente también determinará el éxito. La investigación y el diseño de la experiencia del usuario (UX) para optimizar la forma en que los usuarios pacientes interactúan con los sistemas de auto-triaje serán críticos. Teniendo en cuenta que los sistemas de auto-triaje requieren cantidades significativas de información (decenas de preguntas) para ser respondida por los pacientes usuarios, hay un alto porcentaje de abandono. La optimización de la experiencia de usuario para facilitar y maximizar la finalización representa un cuerpo emergente de literatura.
Una de las modalidades más comunes para administrar sistemas de auto-triaje es a través de un chatbot 6,9,63,68. La investigación sobre el diseño y la optimización de los chatbots de atención médica ha identificado varias ideas clave para mejorar la participación de los usuarios y minimizar las tasas de abandono. En los entornos sanitarios, la percepción de empatía y comprensión de un chatbot puede hacer que los usuarios se sientan más cómodos69. Además, las investigaciones destacan la importancia de la equidad en las respuestas de los chatbots. Un estudio indica que los usuarios son sensibles a los sesgos percibidos o a la injusticia en las interacciones de los chatbots70. Garantizar la transparencia y la equidad en el comportamiento de los chatbots se correlaciona directamente con una mayor satisfacción y confianza, lo que subraya la necesidad de principios de diseño éticos en el desarrollo de UX para los sistemas de atención médica71. Además, la presentación visual y el estilo conversacional de los chatbots también pueden influir en la forma en que los usuarios perciben e interactúan con el sistema, aunque estos factores no siempre pueden mejorar directamente la experiencia del usuario sin una integración reflexiva.
Para reducir las tasas de abandono en los sistemas de autoevaluación, las mejores prácticas de la investigación sobre chatbots sugieren centrarse en la creación de interacciones fluidas e intuitivas que reduzcan la carga cognitiva sin dejar de recopilar información esencial72. Esto incluye la optimización de la longitud y la complejidad de las preguntas y el diseño de agentes conversacionales que puedan adaptarse a las respuestas de los usuarios de forma dinámica, manteniendo la interacción atractiva y eficiente70. El potencial de diseños más efectivos y centrados en el ser humano radica en equilibrar estos factores tecnológicos y psicológicos para crear una experiencia que se sienta personalizada y receptiva.
Para garantizar que la experiencia también sea segura, hay que tener en cuenta una serie de cuestiones éticas y de privacidad. En primer lugar, la protección de la privacidad del paciente es primordial. Estos sistemas recopilan y analizan datos de salud confidenciales y, por lo tanto, deben cumplir con estrictos estándares de seguridad de datos. Estos incluyen la prevención del almacenamiento de información de salud identificable, el borrado automatizado de datos, la auditoría de los procesos y datos de la organización y la certificación de mantener estrictos estándares de seguridad (por ejemplo, HIPAA, SOCII o HITRUST). Además, los usuarios deben tener control sobre cómo se recopila y utiliza su información, garantizando el consentimiento informado y la autonomía en las decisiones sanitarias73. Igualmente importante es la necesidad de garantizar que los sistemas de autoclasificación funcionen de manera equitativa. Estas herramientas deben diseñarse para tener en cuenta las desigualdades sistémicas, como las que enfrentan las personas con discapacidad o las que no lo son.Entornos socioeconómicos desfavorecidos. La incorporación de ajustes de equidad, como reservar la atención para grupos marginados, ayuda a mitigar los sesgos en la toma de decisiones algorítmicas74,75.
La transparencia es otra consideración ética crítica. Proporcionar a los pacientes usuarios y a los profesionales de la salud la capacidad de comprender la lógica que subyace a las decisiones tomadas por los algoritmos de autoclasificación genera confianza y garantiza un uso adecuado76. Hacerlo también se alinea con el borrador de la guía de la FDA36. Sin información clara y accesible sobre el funcionamiento de estos sistemas, existe el riesgo de desconfianza o uso indebido, lo que puede conducir a resultados perjudiciales para los pacientes77. Por último, si bien los sistemas de autotriaje pueden mejorar la eficiencia, los profesionales de la salud deben ser capaces de intervenir cuando sea necesario para corregir errores algorítmicos o sesgos, asegurando que las decisiones críticas de salud no se dejen completamente en manos de sistemas automatizados74,78.
Abordar estas cuestiones éticas (privacidad, equidad, transparencia y supervisión humana) permitirá que los sistemas de autoclasificación contribuyan positivamente a la prestación de atención médica, sin exacerbar las desigualdades existentes ni socavar la confianza de los usuarios. La intersección de los datos autoinformados de los pacientes, la inteligencia artificial y la investigación de la experiencia del usuario en forma de sistemas de autotriaje representa un paso importante hacia una prestación de atención sanitaria más proactiva, automatizada, optimizada y autoguiada.
Pero para lograr este futuro, es probable que se requiera una colaboración más profunda entre los socios de la industria, incluidas las compañías de registros médicos electrónicos, los sistemas de salud comunitarios, los pagadores y las empresas de tecnología. Esto se debe a que la precisión de los sistemas de auto-clasificación es limitada sin una «respuesta correcta» para afirmar o negar la validez de una recomendación. Sin embargo, sin acceso a los datos que se encuentran en el EMR o en las declaraciones, no hay forma de «cerrar el ciclo» con fines de validación. Esta necesidad insatisfecha en el campo da como resultado un progreso más lento para mejorar la experiencia de navegación del paciente en la atención médica. Las colaboraciones entre estos socios resolverían esto. Si bien los centros médicos albergan la mayoría de los datos que se requerirían para validar dichos sistemas, la mayor parte de la innovación en los sistemas de autotriage de IA se ha producido en la industria privada (Tabla 3).
Adopción de sistemas de autotriage por parte del sistema de salud
Como parte de esta revisión, se midió la adopción del auto-triage por parte de los sistemas de salud en los EE. UU. (Tabla 3 y 4). Se examinaron los sitios web de 647 sistemas de salud aplicando los siguientes criterios de inclusión de una lista completa de hospitales y sistemas de salud de EE. UU79: (a) el sistema posee al menos 3 hospitales y genera al menos 250 millones de dólares en ingresos netos de pacientes, (b) el sistema tiene una experiencia web distinta, y (c) la experiencia de auto-triaje está disponible para el público. De esta lista, se encontró que 50 sistemas de salud (7,72%) adoptaron 15 sistemas diferentes de autotriage, y 6 de ellos (0,93%) fueron de autotriage exclusivamente para COVID. De los 15 sistemas de autoevaluación, el proveedor más ampliamente adoptado estaba disponible en los sitios web de 13 sistemas de salud (2,01%) y el siguiente más alto estaba disponible en 10 sistemas de salud (1,55%) cada uno (Tabla 3). Dado que los sistemas de salud de EE. UU. varían en tamaño, también se incorporó al análisis el número de hospitales atendidos por cada sistema de salud. La Tabla 4 muestra que 534 hospitales (8,73% de un total de 6120 en los EE.UU.)80) tienen sitios web con auto-clasificación fácilmente disponibles. El proveedor más adoptado estuvo disponible en los sitios web que representan a 244 hospitales (3,99%). El siguiente más alto está disponible en los sitios web que representan a 91 hospitales (1,49%). Un estudio futuro podría examinar las diferencias en las necesidades de enrutamiento necesarias para que la tecnología optimice el acceso de los pacientes con la entrega de recursos de atención médica a diferentes escalas del área de servicio (por ejemplo, 100 hospitales frente a 300 hospitales). Además, en la Tabla 2 se proporcionan más detalles sobre cada sistema.
Tabla 4 Adopción hospitalaria de soluciones de triage virtual por parte del proveedor en sitios web accesibles al público (no autenticados)
Por ahora, la mayoría de los pacientes que experimentan un nuevo síntoma deben autoclasificarse en un sitio de atención adecuado. Como resultado, un estudio muestra que el 60% de las veces los pacientes se clasifican a sí mismos de manera inapropiada81. A gran escala, se estima que se desperdicia casi un billón de dólares de gasto sanitario (es decir, el 25% del gasto total en atención sanitaria)82. Los sistemas de autotriage son muy prometedores para ayudar a los pacientes a tomar decisiones más precisas desde el punto de vista clínico. De hecho, el mismo estudio mostró que entre el 15 y el 30% de los pacientes que utilizaron un sistema de autotriage digital se comprometieron con los resultados del triage para redirigirlos a una atención más adecuada desde el punto de vista clínico81.
A medida que los sistemas de salud, los pagadores, las compañías de EHR y las compañías de auto-triaje trabajan más juntos, las asociaciones entre ellos beneficiarían a los pacientes al proporcionar un «circuito cerrado» de retroalimentación a los sistemas de IA. De este modo, estos sistemas podrían validar las predicciones y aprender más rápidamente con un mayor uso; en última instancia, proporcionando capacidades de navegación más inteligentes. Como resultado, menos pacientes rebotarían en el sistema de salud y más probablemente buscarían la atención adecuada en el lugar y el momento adecuados. Además, hacerlo también beneficiaría a los pagadores, ya que una utilización más eficiente de la atención médica reduciría el costo de la atención por paciente.
Finalmente, los proveedores podrían esperar ver a más pacientes que sean apropiados para ellos. Esto es especialmente relevante en el contexto de la actual escasez de proveedores y el agotamiento. Más que nunca, el sistema sanitario necesita asegurarse de que no está desperdiciando recursos innecesarios. Permitir que los pacientes se encaucen mejor es un componente clave para controlar el gasto. Se vislumbra un futuro en el que los conocimientos necesarios para la toma de decisiones clínicamente precisas se democraticen y se hagan accesibles a los pacientes en una experiencia agradable que beneficie a la gente común, independientemente de su nivel educativo.
EL SISTEMA DE SALUD, SU REALIDAD, SUS BARRERAS Y HACIA DONDE DEBE ORIENTARSE
Mg. Sergio Rovira
La sanidad está pasando por un momento crítico, no solo financiero, sino también relacionado a la gestión del sistema de salud y a la atención del paciente.
El sistema de salud está influenciado por las dinámicas políticas, sociales, tecnológicas, epidemiológicas y económicas, lo que ha llevado a un deterioro del capital humano y físico a lo largo de los años; y aunque se destina más del 10% del Producto Bruto Interno (PBI) al sector salud, este no logra satisfacer las necesidades de la población, y los indicadores de salud están empeorando en comparación con otros países de la región.
La inequidad en el acceso a servicios de salud se ha incrementado, lo que es especialmente preocupante en un contexto de empobrecimiento económico. El sistema de salud enfrenta desafíos significativos en términos de cobertura, calidad y sostenibilidad, que requieren atención urgente y un enfoque más integral, donde la seguridad social como la salud privada, han mostrado indiferencia ante el deterioro del sistema de salud estatal. Esta situación ha llevado a que cada entidad actúe de manera independiente, con un Estado ausente, que pareciera estar más en una actitud de cómplice que de mediador y gestor. Como resultado, el sistema de salud se vuelve insostenible para todos los involucrados.
Es hora que se debata y se defina una política de salud, donde dicho debate sea ésta vez un debate más profundo y complejo y así, llegar a construir un nuevo consenso; pero esta vez, es necesario dejar de que sea un debate de algunos allegados al gobierno de turno o algunas personas y crear un consenso donde todos los colectivos, sociedades, gremios, representantes sociales y demás, participen activamente, para dejar de ser algo fragmentado y de intereses personales de algunos, para que por fin, sea representativo a todas las áreas afectadas. Es decir, es de suma importancia que todos los actores del sistema de salud trabajen de manera coordinada, definiendo objetivos y estrategias comunes, y evaluando su implementación. Esto es crucial para abordar los problemas existentes y garantizar un sistema de salud más efectivo y equitativo.
Para poder avanzar hay que debatir el cómo enfrentar e implementar las políticas públicas, programas preventivos, control de enfermedades crónicas no transmisibles, enfermedades emergentes, enfermedades transmisibles, etc.; como también cambiar la manera de gestionar la salud a nivel hospitalaria y mejorar la gestión hospitalaria, para un cambio de paradigma, centrándonos así en la calidad de atención, seguimiento del paciente y mejor gestión hospitalaria, haciéndola más eficiente y eficaz.
Es momento de comenzar a pensar en una manera diferente de gestionar también los Hospitales, para no solo ayudarles a evolucionar, sino también, salud poblacional y políticas del Estado en salud.
Pero cambiar las variables de gestión a nivel de las Políticas Públicas de Salud, de Programas Preventivos y de la gestión hospitalaria como así de atención del paciente, es una tarea muy ardua, y muy difícil de lograr, donde las barreras para llegar al cambio es un problema diario, que va desde el rechazo al mismo, hasta las barreras económicas, infraestructura, espacio, capacitaciones o específicamente, contrato de trabajo, políticas de compras, y los límites de la gestión. Es muy importante reconocerlos y analizarlos, así, nos preparamos para poder afrontarlas y sobrepasarlas:
- El desafío de implementar cambios en la gestión de la salud y llevar la evidencia a la práctica clínica radica en diversos factores complejos. Entre las razones por las que este proceso puede resultar difícil se encuentran:
- Resistencia al cambio: Muchas veces, los profesionales de la salud y las organizaciones pueden resistirse a adoptar nuevas prácticas debido a la comodidad con las prácticas existentes, el miedo a lo desconocido o la falta de motivación para cambiar.
- Barreras organizativas: Las estructuras organizativas rígidas, la burocracia, la falta de recursos y la resistencia a la innovación dentro de las instituciones de salud pueden obstaculizar la implementación de cambios efectivos.
- Falta de tiempo y recursos: La sobrecarga de trabajo, la falta de tiempo protegido para la formación y la implementación de nuevas prácticas, así como la escasez de recursos financieros, pueden dificultar la adopción de evidencia científica en la práctica clínica.
- Complejidad del sistema de salud: La naturaleza multifacética y fragmentada del sistema de salud puede dificultar la coordinación y colaboración entre los diferentes actores involucrados en la atención médica, lo que dificulta la implementación de cambios efectivos.
Para superar estos desafíos, es fundamental contar con un liderazgo comprometido, promover una cultura organizacional que fomente la innovación y el aprendizaje continuo, brindar apoyo y recursos adecuados, y fomentar la colaboración interdisciplinaria para integrar la evidencia científica en la práctica clínica de manera efectiva.
Ahora bien, vamos a analizar más detallado éstes problemas, según cada nivel de Gestión:
- En el nivel de Microgestión del núcleo operativo, se identifican varios problemas:
- Inseguridad al traspasar las funciones profesionales y salir de la zona de confort.
- Falta de comprensión sobre cómo contribuir como profesionales en su gestión día a día.
- Enfoque en la hiperespecialización con premios y incentivos, descuidando la visión holística de los pacientes.
- Presión asistencial excesiva y falta de tiempo para la atención de calidad.
- Desbalance entre la cantidad de personal designado y el trabajo efectivo, afectando la productividad en hospitales públicos.
- Falta de protección para quienes trabajan en exceso y se exponen.
- Ausencia de esquemas de participación efectivos para implementar cambios.
- Falta de reconocimiento por los esfuerzos en mejorar los procesos de implementación y carencia de horas protegidas para la gestión.
- Se identifican las siguientes problemáticas relacionadas con la gestión:
- Falta de interés por la gestión en la formación académica y profesional, debido al temor de limitar la libertad profesional.
- Ausencia de incentivos económicos por mejoras en la eficiencia y ahorros generados.
- Carencia de continuidad en la atención de los pacientes y en los roles asignados.
- El multiempleo reduce la dedicación plena en un solo lugar de trabajo.
- Falta de incentivos para la formación continua, la capacitación y la investigación.
- Rotación frecuente de cargos políticos sin escuchar a quienes están en el nivel operativo.
- Necesidad de comprender la minimización de costos, una responsabilidad compartida por diversos profesionales de la salud.
- Hay que reconocer que la gestión se realiza a través de procesos que son fundamentales en las actividades y procedimientos de atención médica.
- Falta de recertificaciones obligatorias una vez finalizada la residencia médica.
- En el nivel de Mesogestión, se identifican varios problemas:
- Falta de formación profesional y técnica en los directores para implementar innovaciones en la gestión, así como una carencia de profesionalización en los gobiernos institucionales.
- Ausencia de un sistema de información para la toma de decisiones, incluyendo la falta de un cuadro de mando integral y de datos ordenados para respaldar la toma de decisiones.
- Necesidad de formación en habilidades blandas esenciales para los gerentes modernos, como liderazgo, comunicación, trabajo en equipo, resolución de conflictos y negociación.
- Carencia de una planificación estratégica que defina claramente la dirección institucional y permita identificar los objetivos a largo plazo.
- Se identifican las siguientes problemáticas adicionales en el ámbito de la gestión:
- Escasez de personal con niveles técnicos adecuados y exceso de comisarios políticos, lo que puede llevar a la conformidad y la falta de liderazgo proactivo.
- Baja investigación y publicación en el campo de la gestión, limitando la difusión de experiencias exitosas y buenas prácticas.
- Carencia de integración de equipos multiprofesionales, como ingenieros, coaches y especialistas en factores humanos, ergonomía y resiliencia.
- Insuficiente inversión en digitalización y modernización de sistemas de información en el ámbito de la salud.
Pero no solo podemos encontrar los problemas recién observados, sino que la realidad del día a día de cada integrante de la sanidad hospitalaria o salud (Médicos, Enfermeros, Técnicos, Administrativos, Mantenimiento y demás), complejizan aún más esta realidad para dificultar el conseguir este cambio que tanto necesita la salud actual.
Ahora nos vamos a centrar en las problemáticas específicas que padecen dos de los principales actores sanitarios (los Médicos y los Enfermeros), que nos servirán de ejemplo y de representación, a lo que le ocurre a los demás profesionales y no profesionales de la salud, que son también engranajes muy importantes en esta máquina llamada Sanidad.
LA SITUACIÓN DE LA ENFERMERÍA
La complejidad de los factores que influyen en el rendimiento laboral del personal de enfermería, especialmente en el contexto de la salud y la enfermedad es compleja y variada. El personal de enfermería debe ofrecer un servicio óptimo a la comunidad, lo que requiere no solo conocimientos teóricos y prácticos, sino también un equilibrio mental y físico que les permita desempeñar su labor de manera eficiente y por eso, es importante entender que las condiciones laborales, los problemas personales, lo problemas económicos, la falta de reconocimiento, una mala carrera profesional y muchos otros factores; sumado a que las enfermeras, debido a su constante interacción con pacientes, están expuestas a una carga emocional significativa, derivada de la confrontación repetida con el sufrimiento humano y la muerte; puede llevarla a situaciones de estrés y agotamiento, lo que a su vez afecta su rendimiento laboral, bienestar general y hasta puede afectar a la vida personal de los mismos.
La literatura señala que estos profesionales enfrentan múltiples estresores inherentes a su profesión, tales como largas jornadas laborales, el manejo del dolor y el sufrimiento, así como el cuidado de pacientes en condiciones críticas; como por ejemplo en las unidades de emergencia, que son entornos de trabajo caracterizados por un alto estrés ocupacional, lo que aumenta la vulnerabilidad de los enfermeros a desarrollar problemas de salud. Estos estresores, junto con la forma en que se llevan a cabo las actividades diarias y los recursos de apoyo disponibles, subrayan la necesidad de abordar la salud y el bienestar de los profesionales de enfermería para garantizar una atención de calidad a los pacientes.
Además, se establece una conexión entre los problemas de salud y el presentismo, que se refiere a la disminución de la productividad debido a problemas de salud. Este fenómeno impacta la seguridad del paciente, contribuyendo a un aumento en los errores de medicación y a una caída en la calidad de atención, lo que genera costos significativos, estimados en alrededor de dos mil millones de dólares anuales en Estados Unidos. Por otro lado, el ausentismo, o las ausencias al trabajo, también se reconoce como un problema global que afecta la eficiencia y funcionamiento de los servicios de salud.
La complejidad de los factores que afectan el rendimiento laboral en profesiones de servicio de Enfermería aparece el síndrome del desgaste profesional (o Burnout), donde se caracteriza por una sensación de fracaso y agotamiento, resultado de la sobrecarga de recursos personales y energía del trabajador.
La definición más reconocida del síndrome de desgaste profesional es la de Christina Maslach, que lo describe como un estado que incluye despersonalización y baja realización personal, afectando a aquellos que trabajan en contacto directo con personas. Este fenómeno es particularmente relevante en el campo de la enfermería, donde los profesionales enfrentan desafíos emocionales y físicos significativos, lo que puede impactar negativamente en su rendimiento y bienestar.
Se identifican diversas fuentes que afectan el rendimiento laboral del personal de enfermería, incluyendo la recarga laboral, la falta de comunicación, un entorno laboral desfavorable, y la excesiva responsabilidad inherente a su trabajo. Además, se mencionan factores emocionales, la interacción con pacientes y familiares, así como conflictos con otros profesionales de la salud, como médicos. También se considera que la situación socioeconómica y familiar del personal puede influir en su productividad y eficacia en el trabajo.
Es fundamental implementar estrategias de apoyo y recursos que ayuden a mitigar el estrés, como así, acciones en el entorno laboral para reducir el número de lesiones y enfermedades entre los profesionales de enfermería, como así la carga emocional que enfrentan las enfermeras en su práctica diaria. Las enfermeras enfrentan una serie de presiones y responsabilidades que pueden intensificar su estrés laboral.
Se ha identificado que además de los problemas de salud mental de los enfermeros, también podemos encontrar como uno de los principales problemas a las enfermedades músculo-esqueléticas. La mayoría de los profesionales reportaron tener dos o más lesiones o enfermedades, lo que subraya la necesidad de intervenciones efectivas.
Además, se observó que aquellos con un mayor tiempo de trabajo en la unidad y en la institución, así como las víctimas de violencia laboral, presentaron un número más elevado de lesiones y enfermedades. Es fundamental que las instituciones de salud proporcionen condiciones laborales que favorezcan el mantenimiento de la salud y las habilidades de los trabajadores, lo que no solo mejorará su calidad de vida a corto y largo plazo, sino que también optimizará la calidad del cuidado que ofrecen a los pacientes.
En cuanto al horario de trabajo, se destaca que la atención en salud es un servicio continuo, que requiere turnos de mañana, tarde y noche. Esta distribución de la jornada puede tener repercusiones significativas en la salud de los profesionales, principalmente debido a la alteración de los ritmos circadianos, problemas de sueño y efectos negativos en la vida familiar y social. Estos factores pueden contribuir al desgaste emocional y físico del personal de enfermería, afectando su bienestar general y su capacidad para brindar atención de calidad.
Las condiciones ambientales durante el día, como la luz, el ruido, el calor y factores sociales, pueden dificultar que los enfermeros logren un sueño reparador. La falta de sueño tiene repercusiones directas en la salud de estos profesionales, contribuyendo a situaciones de estrés y fatiga crónica, que a su vez pueden provocar alteraciones en el sistema nervioso y digestivo.
El desgaste profesional está relacionado tanto con factores personales como ambientales, y puede llevar a conductas estresantes que afectan el desempeño laboral. La despersonalización, en particular, se traduce en actitudes frías, déspotas o cínicas hacia compañeros de trabajo y pacientes, lo que puede deteriorar la calidad de la atención brindada.
Además, se plantea la inquietud sobre por qué muchos profesionales de la salud recurren a ansiolíticos o antidepresivos, y se observa que los más jóvenes son los que parecen estar más afectados por el desgaste emocional. Es decir, es muy importante crear políticas preventivas que aborden el bienestar mental de los trabajadores de la salud para prevenir el Burnout y mejorar la calidad del servicio.
Resumamos en algunos puntos clave el Burnout en la Enfermería:
- Factores causales: Se identifican múltiples factores que contribuyen al desarrollo del burnout, como la alta responsabilidad en el proceso asistencial, la sobrecarga de trabajo, y las dificultades en las relaciones humanas y la comunicación dentro del equipo de trabajo.
- Enfrentamiento al dolor, sufrimiento y muerte: Los enfermeros a menudo están expuestos a situaciones emocionalmente difíciles que pueden impactar su bienestar psicológico.
- Riesgos biológicos: La exposición a agentes patógenos y otros riesgos biológicos en el entorno de trabajo puede afectar la salud física de los enfermeros.
- Estrés mantenido por situaciones de urgencias y emergencias: Las demandas constantes y la presión en situaciones críticas contribuyen al estrés laboral.
- Condiciones de trabajo y sobrecarga: La alta responsabilidad y la carga de trabajo, junto con problemas de comunicación y relaciones humanas dentro del equipo, generan un ambiente estresante.
- Tareas en el hogar: Las responsabilidades familiares y el cuidado de la propia salud también añaden estrés a la vida de los enfermeros, lo que puede afectar su capacidad para desempeñar su trabajo.
El burnout puede llevar a problemas de salud física y psicológica, incluyendo ansiedad, depresión, trastornos del sueño, y otros síntomas relacionados con el estrés. Por eso es muy importante implementar acciones para contrarrestarlo y así, cuidar la salud de los enfermeros, y las enfermeras.
Para ello, se sugiere varias estrategias para que el personal de enfermería practique el autocuidado, con el fin de mantener su salud y bienestar. Algunas de estas recomendaciones incluyen:
- Mecanismos de defensa y afrontamiento al estrés: Implementar técnicas para manejar el estrés.
- Establecimiento de relaciones humanas: Fomentar un ambiente de apoyo entre colegas.
- Estilo de vida saludable: Mantener hábitos saludables como una buena alimentación y ejercicio.
- Sistema de apoyo: Contar con un sistema que ofrezca apoyo emocional y psicológico.
- Fomento del bienestar bio-psico-social: Promover el bienestar integral para desarrollar una personalidad terapéutica.
- Reconocimiento de la importancia del autocuidado: Ser conscientes de la necesidad de cuidar de sí mismos para poder cuidar de los demás.
- Mejorar las Condiciones Laborales: Es fundamental abordar los factores estresantes en el entorno laboral, como la sobrecarga de trabajo, la escasez de personal y la falta de autonomía. Esto podría implicar la contratación de más personal y la implementación de horarios de trabajo más flexibles.
- Fomentar el Apoyo Social: Promover un ambiente de trabajo donde haya apoyo social entre compañeros y supervisores puede ayudar a reducir el estrés. Esto incluye el reconocimiento del trabajo realizado y la creación de espacios para la comunicación abierta sobre las dificultades que enfrentan.
- Capacitación en Manejo del Estrés: Proporcionar formación en técnicas de manejo del estrés y autocuidado puede ser beneficioso. Esto podría incluir talleres sobre mindfulness, gestión del tiempo y habilidades de comunicación para mejorar las relaciones interpersonales en el trabajo.
- Promover la Salud Mental: Implementar programas de salud mental que ofrezcan recursos y apoyo psicológico para el personal de enfermería puede ayudar a abordar problemas de salud mental antes de que se conviertan en crisis.
- Fomentar la Participación en la Toma de Decisiones: Involucrar al personal en la toma de decisiones relacionadas con su trabajo puede aumentar su sentido de control y satisfacción laboral, lo que puede contribuir a un mejor bienestar emocional.
- Crear un Entorno de Trabajo Positivo: Desarrollar una cultura organizacional que valore el bienestar del personal y que promueva un enfoque humanístico en el cuidado puede ayudar a mitigar el impacto negativo del estrés laboral.
Es decir, el autocuidado es esencial para que los enfermeros puedan manejar el estrés y las demandas de su trabajo, lo que a su vez impacta positivamente en la calidad de la atención que brindan a sus pacientes.
También, los enfermeros pueden tener otros peligros, más allá de los detallados anteriormente, ya que las enfermeras se enfrentan a varios peligros en su entorno laboral, que se pueden clasificar en diferentes categorías:
- Peligros biológicos: Exposición a virus y bacterias que pueden causar infecciones.
- Peligros químicos: Contacto con sustancias como glutaraldehído y fármacos citotóxicos que pueden ser perjudiciales para la salud.
- Peligros ergonómicos: Riesgos asociados a sobresfuerzos, caídas y levantamiento de pesos, que pueden provocar lesiones musculoesqueléticas.
- Peligros físicos: Incluyen la exposición a radiación y pinchazos accidentales con agujas u otros objetos punzantes.
Estos peligros pueden aumentar debido a la alta demanda en el sector de la salud, una mala ergonomía y una inadecuada dotación de personal y patrones de turnos.
El Consejo Internacional de Enfermeras (ICN) propone varias medidas para mejorar la salud y seguridad laboral de las enfermeras, que incluyen:
- Acceso a Equipos de Protección Individual (EPI): Garantizar que todo el personal tenga acceso a EPI sin costo alguno.
- Mecanismos de Notificación: Crear o facilitar mecanismos de notificación sencillos, confidenciales y eficaces para reportar incidentes relacionados con accidentes, lesiones y enfermedades laborales.
- Formación Continua: Proporcionar formación a los trabajadores sobre la prevención y gestión de peligros laborales, con un enfoque en la formación continuada específica según las evaluaciones de riesgo.
- Concienciación: Concienciar a las enfermeras, empleadores y ciudadanos sobre los peligros laborales en el sector de la salud, incluyendo la violencia y los abusos, así como sobre los derechos de las enfermeras a un entorno seguro.
- Cumplimiento de Legislación: Instar a los empleadores a cumplir con la legislación y directrices pertinentes sobre salud y seguridad laboral, y a formular e implementar políticas para identificar y prevenir peligros laborales.
- Colaboración Interinstitucional: Fomentar la colaboración entre ministerios de sanidad y trabajo para abordar los temas de salud y seguridad laboral en los entornos sanitarios.
Estas medidas buscan crear un entorno de trabajo más seguro y saludable para las enfermeras, lo que a su vez beneficia a los pacientes y a la comunidad en general.
El cuidar a los enfermeros y a las enfermeras impacta positivamente en la salud de los pacientes, ya que es directo la relación salud del que cuida con el trato y cuidado al paciente. Es decir, la salud laboral de las enfermeras tiene un impacto significativo en la calidad de atención a los pacientes de varias maneras, por ejemplo:
- Reducción de Lesiones y Enfermedades: Cuando las enfermeras están protegidas de lesiones y enfermedades laborales, pueden desempeñar sus funciones de manera más efectiva y con menos interrupciones, lo que se traduce en una atención más continua y de calidad para los pacientes.
- Satisfacción Laboral: Un entorno de trabajo seguro y saludable contribuye a una mayor satisfacción laboral entre las enfermeras. Esto puede resultar en una menor rotación de personal y una mayor experiencia en el cuidado, lo que beneficia a los pacientes.
- Menor Estrés y Agotamiento: La salud laboral adecuada ayuda a reducir el estrés y el agotamiento entre las enfermeras. Un personal menos estresado y más comprometido es más capaz de proporcionar atención compasiva y centrada en el paciente.
- Mejora en la Comunicación y el Trabajo en Equipo: Un entorno laboral positivo fomenta una mejor comunicación y colaboración entre el personal de salud, lo que es crucial para la atención integral del paciente.
- Prevención de Errores: La salud y el bienestar de las enfermeras son fundamentales para minimizar errores en la atención. Enfermeras sanas y bien capacitadas son menos propensas a cometer errores que pueden afectar la seguridad del paciente.
- Impacto en la Salud de los Pacientes: La protección de la salud de las enfermeras no solo beneficia a las propias enfermeras, sino que también tiene repercusiones positivas en la salud de los pacientes, las familias y las comunidades, contribuyendo a un sistema de salud más eficaz.
LA SITUACIÓN DE LA MEDICINA
Según algunos autores, las principales causas de la crisis en la profesión médica incluyen:
- Disminución del prestigio social: La profesión médica ha perdido el respeto y reconocimiento que tenía en décadas anteriores, lo que se traduce en peores condiciones laborales y menores ingresos para los médicos.
- Proletarización de la medicina: La erosión de la relación médico-paciente y la desvalorización del rol del médico, han contribuido a la crisis, afectando la percepción pública sobre la profesión.
- Violencia hacia los médicos: Ha habido un aumento en los reportes de agresiones a médicos en su lugar de trabajo, lo que refleja una falta de respeto y reconocimiento hacia su labor.
- Condiciones laborales precarias: Los médicos enfrentan jornadas laborales extensas y salarios bajos, lo que ha llevado a una disminución en la cantidad de personas que eligen carreras relacionadas con la salud.
- Los profesionales de la salud a menudo trabajan en ambientes estresantes que socavan su bienestar físico, emocional y psicológico. Esto incluye el exceso de trabajo y la presión constante para brindar atención de calidad en situaciones difíciles.
- Limitada autoridad en la planificación de horarios. La falta de control sobre sus horarios de trabajo puede llevar a un desequilibrio entre la vida laboral y personal, aumentando el estrés y el agotamiento.
- Cambio en las motivaciones: Las nuevas generaciones pueden estar menos motivadas por el altruismo y el prestigio social, y más enfocadas en la calidad de vida y la compensación económica.
- Sobrecarga administrativa: La carga de trabajo administrativo puede ser abrumadora, lo que contribuye al agotamiento. Esto incluye tareas como la documentación y el cumplimiento de requisitos burocráticos que desvían tiempo y energía de la atención al paciente.
- Falta de apoyo organizacional: Muchos profesionales sienten que no reciben el apoyo necesario de sus organizaciones, lo que puede incluir la falta de recursos, formación y reconocimiento por su trabajo.
- Desigualdades preexistentes: Factores sociales y culturales, como el racismo y la discriminación, también pueden exacerbar el agotamiento, afectando desproporcionadamente a ciertos grupos, como las mujeres y los profesionales de la salud de color.
- Impacto de la pandemia: Aunque la pandemia de COVID-19 inicialmente revalorizó el rol del personal de salud, una vez superada, los problemas estructurales de la profesión han resurgido con fuerza.
Estas causas reflejan un panorama complejo que afecta tanto a los profesionales de la salud como a la calidad de la atención médica que reciben los pacientes.
La pandemia de COVID-19 tuvo un impacto significativo en la percepción del personal de salud, que se puede resumir en los siguientes puntos:
- Revalorización del rol del personal de salud: Durante la pandemia, el trabajo de médicos, enfermeros y otros profesionales de la salud fue ampliamente reconocido y valorado por la sociedad. Se llevaron a cabo aplausos nocturnos y otras formas de agradecimiento público, lo que resaltó la importancia de su labor en momentos críticos.
- Visibilidad de los desafíos: La pandemia expuso las dificultades y riesgos que enfrentan los profesionales de la salud, lo que generó una mayor empatía y comprensión por parte del público hacia su trabajo y sacrificios.
- Efecto temporal: A pesar de la revalorización durante la pandemia, una vez que la crisis sanitaria comenzó a disminuir, los problemas estructurales de la profesión médica, como la falta de personal y las condiciones laborales precarias, volvieron a ser evidentes. Esto sugiere que la percepción positiva no se tradujo en cambios sostenibles en la valoración de la profesión a largo plazo.
- Desafíos persistentes: A pesar del reconocimiento temporal, los médicos continúan enfrentando problemas como la violencia en el lugar de trabajo, la disminución de salarios y la falta de respeto, lo que indica que la percepción positiva no ha resuelto los problemas subyacentes de la profesión.
En muchos países, incluidos Argentina y el Reino Unido, los profesionales de la salud están organizándose para exigir mejores salarios y condiciones de trabajo. Esto incluye protestas y negociaciones con los gobiernos para mejorar la situación laboral.
El agotamiento de los profesionales de la salud tiene un impacto significativo en la atención al paciente de varias maneras:
- Calidad de la atención: Los profesionales agotados pueden tener dificultades para brindar atención de calidad, lo que puede resultar en errores médicos, diagnósticos incorrectos y una atención menos personalizada. Esto se debe a que el agotamiento afecta la capacidad de concentración y la toma de decisiones.
- Empatía y conexión emocional: El agotamiento puede disminuir la capacidad de los profesionales de la salud para conectarse emocionalmente con sus pacientes. Esto puede llevar a una atención menos compasiva y a una menor satisfacción del paciente, ya que los profesionales pueden sentirse incapaces de cuidar emocionalmente a cada paciente de manera individual.
- Aumento de la rotación de personal: El agotamiento puede llevar a que los profesionales de la salud abandonen la fuerza laboral, lo que resulta en una escasez de personal. Esto puede aumentar la carga de trabajo para los que quedan, perpetuando el ciclo de agotamiento y afectando aún más la atención al paciente.
- Tiempo de atención reducido: Los profesionales agotados pueden tener menos tiempo y energía para dedicar a cada paciente, lo que puede resultar en consultas más cortas y menos oportunidades para abordar las preocupaciones de los pacientes de manera adecuada.
- Impacto en la salud pública: Si el agotamiento no se aborda, puede dificultar la capacidad del sistema de salud para prepararse para emergencias de salud pública, lo que puede afectar la atención que reciben los pacientes en situaciones críticas.
En conclusión, el agotamiento de los profesionales de la salud no solo afecta su bienestar personal, sino que también tiene repercusiones directas en la calidad de la atención que pueden ofrecer a sus pacientes, lo que puede comprometer la salud y el bienestar de la población en general.
En Argentina, se ha observado una creciente dificultad para cubrir los cargos vacantes en el sistema de salud, incluyendo los de acceso a residencias médicas. Esto indica una falta de interés o disponibilidad de candidatos para ocupar estos puestos, lo que agrava la crisis. En algunos países están implementando políticas para atraer y retener personal de salud, aunque la efectividad de estas iniciativas puede variar. Esto puede incluir incentivos económicos, programas de formación y desarrollo profesional, y mejoras en las condiciones de trabajo.
A pesar de los esfuerzos, la crisis de personal de salud es un problema complejo que requiere soluciones a largo plazo, incluyendo cambios en la formación médica, la gestión de recursos humanos en salud y la inversión en infraestructura.
CONCLUSIÓN
La frustración expresada sobre la falta de avances significativos en la gestión sanitaria es comprensible y refleja la complejidad y persistencia de los desafíos en el sistema de salud. Es fundamental reconocer la necesidad de abordar de manera integral las barreras estructurales, las deficiencias en la gestión operativa y política, y la resistencia al cambio que obstaculizan la mejora continua en el sector de la salud.
Para superar esta situación, es crucial promover un enfoque colaborativo y participativo que involucre a todos los actores relevantes, incluidos profesionales de la salud, gestores, políticos y la comunidad en general. Se requiere un compromiso firme con la transparencia, la rendición de cuentas, la innovación y la implementación efectiva de políticas basadas en evidencia y buenas prácticas.
Además, es importante aprender de las lecciones pasadas, identificar las causas subyacentes de los problemas persistentes y trabajar en soluciones sostenibles a largo plazo. La continuidad en la implementación de estrategias efectivas, el monitoreo constante de los resultados y la adaptación a las nuevas circunstancias son clave para lograr mejoras significativas en la gestión sanitaria y, en última instancia, en la calidad de la atención y la salud de la población.
Es importante fortalecer el área Médica, Enfermería, recepción, administración y personal no médico, ya que puede ser el eje de la atención en la nueva gestión y atención hospitalaria y de Políticas de Salud, haciendo que la importancia de la atención, no solo se centre en los aspectos técnicos, sino también en la relación humana y el respeto hacia los pacientes y sus familias.
Estas conclusiones resaltan la necesidad de un enfoque más humano y comprensivo en la atención de todo el personal de salud, especialmente en situaciones críticas; y principalmente, nos deja la inquietud de pensar, cómo podemos cuidar a ésta especialidad y cómo podemos apoyarlos para protegerlos y traer a más personas a estudiar y trabajar en diversas área hospitalarias.
Es importante comenzar a trabajar de otra manera el cuidado de los trabajadores de Salud; cambiando la Medicina Laboral tradicional por una nueva metodología de trabajo y de concepto del cuidado, como es la implementación de una Salud Ocupacional y del Cuidado del Medio Ambiente, donde el trabajo multiprofesional es fundamental y el eje del trabajo, para crear programas y políticas preventivas y del cuidado de todos y todas los trabajadores de la salud, desde una mirada más integral y que abarque todas las variables de la salud.
El personal sanitario, en su totalidad (no importa el cargo, función o profesión), son muy importantes para el sistema de salud y el manejo del cuidado de los pacientes en los hospitales y en las atenciones primaria de la salud, con una participación fundamental en los nuevos cambios que se vienen en el sistema de salud y en la gestión hospitalaria y políticas de salud y comenzar a reconocer que todos los puestos de trabajo dentro de un hospital es una pieza fundamental en el cuidado del paciente, mejorando su salario, carrera y principalmente, creando políticas preventivas para evitar las enfermedades que trae dicha especialidad o puestos de trabajo.
Las recomendaciones para abordar el agotamiento en el sistema de salud incluyen diversas estrategias dirigidas a diferentes actores, como organizaciones sanitarias, gobiernos, instituciones educativas y los propios profesionales de la salud. Algunas de las principales recomendaciones son:
- Organizaciones sanitarias:
- Construir un compromiso con la salud y seguridad de los profesionales de la salud en la estructura de las organizaciones.
- Reducir la sobrecarga administrativa que contribuye al agotamiento.
- Invertir en la prevención sanitaria y servicios sociales para abordar las inequidades en la salud.
- Gobiernos:
- Invertir en asociaciones y prácticas basadas en la evidencia que garanticen la salud y el bienestar de los profesionales de la salud.
- Abordar políticas que disuadan a los profesionales de la salud de buscar atención para su salud mental y el consumo de sustancias, y aumentar el acceso a atención de calidad.
- Reclutar y retener una fuerza de trabajo diversa en la atención médica para enfrentar desafíos sanitarios actuales y futuros.
- Instituciones educativas:
- Priorizar y promover el bienestar de los estudiantes en carreras de salud, así como abordar el impacto de las enseñanzas subliminales en su desarrollo.
- Fortalecer la conexión entre los residentes y las comunidades para mitigar el agotamiento y construir confianza.
- Profesionales de la salud:
- Aprender a reconocer las señales de angustia y agotamiento en sí mismos y en sus colegas, y permanecer conectados para pedir ayuda.
- Priorizar momentos de disfrute y conexión, y volver a hábitos de salud básicos.
- Investigadores:
- Solicitar más investigación para desarrollar herramientas que evalúen y respondan al agotamiento y bienestar de los profesionales de la salud.
- Estas recomendaciones buscan crear un entorno más saludable y sostenible para los profesionales de la salud, lo que a su vez beneficiará la atención que reciben los pacientes.
EL CUIDAR A LOS QUE NOS CUIDAN, DEBERÍA DE SER UN OBJETIVO FUNDAMENTAL Y PRIORITARIO PARA EL CAMBIO Y PARA LOGRAR UNA SALUD POBLACIONAL IDEAL Y MEJOR ATENCIÓN AL PACIENTE.
BIBLIOGRAFÍA
- Ariela, Micha. (año 2015). “Las condiciones de trabajo de la enfermería en Argentina: algunos determinantes políticos-institucionales”. Versión impresa ISSN 0327-5744, versión ON-line ISSN 2545-7756. Estud. Trab. No. 49.
- Benavidesa, Fernando G; Delclósa, Jordi y Serraa, Consol. (año 2018). “Estado de bienestar y salud pública: el papel de la salud laboral/Welfare State and public health: the role of occupational health”. Gaceta Sanitaria, versión impresa ISSN 0213-9111, Gac. Sanit. Vol.32, no.4. Barcelona jul/ago. 2018. https.//dx.doi.org/10.1016/j.gaceta.2017.07.007.
- Bordignon, Maiara y Monteiro, María Inés. (año 2018). “Problemas de salud entre profesionales de enfermería y factores relacionados” (Problemas de saúde entre profissionais de enfermagem e fatores relacionados Health problems among nursing professionals and related factors). Publicado en Enfermería Global. ISSN 1695-6141. Revista Electrónica Trimestral de Enfermería. N° 51.
- Diaz, Carlos. (año 2024). “Editorial. Porque cuesta tanto cambiar la gestión de salud y llevar la evidencia a la práctica clínica”. Publicado por saludbydiaz. Editorial Política Sanitaria.
- Diaz, Carlos. (año 2022). “Gestión Clínica por Cuidados Progresivos”. Editorial Isalud.
- Ferrero F. La crisis de la profesión médica. Arch Argent Pediatr 2024;122(2):e202310225
- Jean-Marteau, Place. (año 2009). “Salud y seguridad laboral de las enfermeras”. Consejo Internacional de Enfermería 3. Declaración de posición. Ginebra – Suiza.
- Lisbeth Madelayne, Andrade-Pizarro y col. (año 2023). “Retos y desafíos de enfermería en la actualidad”. Revista Arbitrada Interdisciplinaria de Ciencias de la Salud. Salud y Vida. Versión on-line ISSN 2610-8038. Vol 7 no.14 Santa Ana de Coro.
- Luengo-Martínez, Carolina y Sanhueza, Olivia. (año 2016). “Condiciones de trabajo y su relación con la calidad del cuidado y salud del profesional de enfermería/Working conditions and its relation to health care quality and nursing professional health”. Medicina y Seguridad del Trabajo. Versión On-line ISS 1989-7790versión impresa ISSN 0465-546X
Med. segur. trab. vol.62 no.245 Madrid oct./dic. 2016. - Marcia Ortega-López, Rosa; Piedad Morán-Asencio, Ruth; Jakeline Oviedo-Rodríguez y Evelyn Vanessa Apolinario-Olaya. (año 2023). “Ejes del cuidado humanizado de enfermería en las Unidades de Cuidados Intensivos”. Pol. Con. (Edición núm. 85) Vol. 8, No 12 Diciembre 2023, pp. 207-222 ISSN: 2550 – 682X DOI: 10.23857/pc.v8i12.627.
- Palma, Daniela Berón Flavia. (octubre de 2011). “Factores que influyen en el rendimiento laboral del personal de Enfermería”. Universidad Nacional de Cuyo (Facultad de Ciencias Médicas-Escuela de Enfermería, Sede Malarqüe). Estudio descriptivo de corte transversal, realizado en los servicios de maternidad, pediatría, guardia, consultorios externos y traslados, del Hospital Malargüe durante el período de julio del 2010 a julio del 2011.
- Revista de bioética y derecho. “seminario internacional de bioética unesco. La equidad y el acceso a los recursos sanitarios. ¿médicos con fronteras?. Justicia global y emigración del personal sanitario. Observatori de Bio{wtica i Dret. Publicación del Master en Bioética y Derecho. www. Bioeticayderecho.ub.edu. Revista de Biética y Derecho, num 29. Septeimbre 2013. P. 68-76.
- Silberman, Pedro; García Argibay, Sofía; López, Emiliano; Skouma, Gladys y De Socio, Daniel. (año 2022). Programa de residencia en cuidados progresivos basado en actividades profesionales confiables. Investigación en educación médica. Versión ON-Line ISSN 2007-5057. Investigación educ. médica vol.11, no.44. Ciudad de México oct./dic. 2022. Epub 06-Ene-2023.
- Torres, Rubén. (año 2024). “En el tema salud hay necesidad y urgencia” (entrevista realizada por Natalia Jorgensen). Diario La Nación (27 de enero de 2024).
NICE: Evaluación de Medicamentos y Consecuencias para la Salud en Inglaterra
En el número de Lancet de esta semana Viernes 2-1-2025 se publica una editorial escrita por la Dra Victoria Charlton y un trabajo retrospectivo de Naci H. et al sobre el efecto de las evaluaciones realizadas por el NICE cuyas recomendaciones para el uso de nuevos medicamentos son vinculantes para el National Health Service, las inferencias que hace el trabajo generarán fuertes polémicas y críticas, por los valores que toma de referencia para el AVAC, pero es muy interesante para que se entienda la difícil situación en la cual nos encontramos en el planeta y el ecosistema de la salud para definir los límites de lo que es posible financiar en relación a los valores que los productores que ponen a sus fármacos y el sacrificio que este impone a la sociedad para financiar nuevas tecnologías farmacológicas, con el matiz que agrega el empleo al final de la evolución de la enfermedad, cuando es menor la capacidad de respuesta que tienen los organismos. Lo que obliga a pensar en el concepto de apropiabilidad, como complementario a estas evaluaciones económicas. Las mismas expresan que la sociedad en el Reino Unido con el asesoramiento del NICE, en el uso de nuevos medicamentos puede estar aumentando el costo de los años de vida ganados con calidad, generando con ello una pérdida neta por restarle a otras aplicaciones «más rentables» para el nivel de salud de la población. Bueno aqui envío para la discusión y la polémica para mis Blogueros.
What price is society willing to pay for new drugs?
El propósito del Servicio Nacional de Salud de Inglaterra (NHS) es mejorar la salud y el bienestar de la nación a través de la prestación de atención médica.1 El dinero disponible para lograr este propósito es restringido y el costo de proporcionar toda la atención médica posible a todos los ciudadanos posibles excedería ampliamente el presupuesto del NHS. Por lo tanto, a medida que surgen nuevos medicamentos, se deben tomar decisiones sobre si los beneficios para la salud que ofrecen estos medicamentos son suficientes para justificar los beneficios para la salud a los que se renunciará en otras partes del NHS para liberar los recursos necesarios para pagarlos. Para llegar a estas decisiones, el NHS cuenta con el apoyo del National Institute for Health and Care Excellence (NICE), un organismo independiente pero financiado con fondos públicos que, desde 1999, ha hecho recomendaciones basadas en la evidencia sobre la adopción de nuevas tecnologías sanitarias en el NHS. Al igual que el NHS, el NICE tiene como objetivo «satisfacer las necesidades de la población mediante la identificación de una atención que sea de alta calidad, de buen valor y que proporcione los mejores resultados… dentro del presupuesto disponible».2
Sin embargo, el artículo publicado en The Lancet por Naci y sus colegas3 sugiere que, al recomendar la adopción de muchos medicamentos nuevos, el consejo de NICE ha tenido el efecto no deseado de reducir la cantidad total de salud que el NHS ha sido capaz de ofrecer.
Naci y colaboradores3 Llegaron a esta conclusión comparando los beneficios y costos acumulativos de los nuevos medicamentos recomendados por el NICE con un escenario contrafáctico en el que esos medicamentos no se recomendaron y los fondos utilizados para pagarlos se destinaron a otros usos.
Estimaron que, entre 2000 y 2020, el uso de los nuevos fármacos recomendados por el NICE generó 3,75 millones de años de vida ajustados por calidad (AVAC) para 19,82 millones de pacientes, con un coste de alrededor de 75.000 millones de libras. Sin embargo, si esos 75.000 millones de libras esterlinas se hubieran gastado en otros usos, estimaron que el NHS habría generado 5,00 millones de AVAC durante el mismo período, lo que implica que el asesoramiento del NICE le ha costado al NHS, y a los usuarios del NHS, 1,25 millones de AVAC. Este cálculo se basa en varios supuestos, uno de los cuales es que la cifra utilizada por NICE para evaluar la rentabilidad de un medicamento es inexacta. A la hora de juzgar si es probable que una nueva tecnología aporte suficientes beneficios para la salud como para justificar sus costos, el NICE ha utilizado durante mucho tiempo un umbral de rentabilidad de 20 000 a 30 000 libras esterlinas por AVAC.3 Este umbral implica que por cada 20.000-30.000 libras esterlinas gastadas en una nueva tecnología, los pacientes de otras partes del NHS renuncian a 1 QALY debido a que los fondos se asignan a otros usos. Sin embargo, la mejor evidencia disponible sugiere que este umbral potencialmente subestima lo bueno que es el NHS para convertir los recursos financieros en AVAC, y que una mejor estimación sería de 15 000 libras esterlinas por AVAC.4,5 Naci y sus colegas utilizaron la cifra más baja al estimar el efecto neto de las recomendaciones de NICE.3 El umbral apropiado a utilizar para evaluar la rentabilidad de una tecnología sigue siendo polémico, y aquellos que no están de acuerdo con la conclusión de Naci y sus colegas probablemente se centrarán en este aspecto de su metodología.6 Sin embargo, a diferencia del umbral de 20.000-30.000 libras esterlinas por AVAC utilizado por NICE, la cifra de 15.000 libras esterlinas por AVAC utilizada por Naci y sus colegas es empírica y refleja la mejor estimación disponible del coste de oportunidad del NHS. Por lo tanto, su artículo proporciona pruebas contundentes de que las recomendaciones de NICE han desplazado a más AVAC de los que han producido. Este efecto no parece ser consistente en todas las áreas de la enfermedad. Desde 2009, el NICE ha adoptado una estrategia de recomendar tratamientos al final de la vida cuyos costes superan sustancialmente las 20.000-30.000 libras esterlinas por AVAC, y el Fondo de Medicamentos contra el Cáncer del Reino Unido sigue facilitando la recomendación de fármacos cuyos beneficios son inciertos.7–9
Como era de esperar, la oncología, que representa casi la mitad de las evaluaciones de NICE, se asocia con una mayor pérdida neta de AVAC que otras áreas terapéuticas (es decir, 0,87 millones del total estimado de 1,25 millones de AVAC).
NICE argumentaría que esta pérdida se justifica por la mayor prioridad que la sociedad atribuye a las personas con cáncer y el alto valor que asignamos a las ganancias de salud relativamente pequeñas que ofrecen muchos medicamentos contra el cáncer en etapa avanzada.7
Aunque el artículo no ofrece información sobre los usos precisos que estos fondos podrían haber tenido, al menos algunos de ellos probablemente habrían beneficiado a las personas con cáncer. Por lo tanto, el argumento para priorizar deliberadamente a grupos específicos de esta manera es cuestionable.
El artículo tampoco tiene en cuenta los medicamentos altamente especializados para enfermedades muy raras, que se recomiendan habitualmente a un coste de 100.000 libras esterlinas por AVAC o más.10
La inclusión de este pequeño pero impactante grupo en el análisis habría aumentado la pérdida neta estimada del AVAC. La clara implicación de esta ambiciosa y muy necesaria investigación es que el asesoramiento de NICE no está promoviendo su supuesto objetivo de promover la salud de la población. El artículo contribuye a la evidencia existente de que las decisiones de NICE podrían no estar éticamente justificadas.11 La pregunta obvia es por qué NICE se ha encontrado en esta situación. Es probable que la respuesta sea compleja, pero NICE ha enmarcado cada vez más su función como una de promoción de la innovación y ha reconocido abiertamente su papel en «apoyar un sector próspero de las ciencias de la vida» y, por lo tanto, «contribuir al crecimiento económico del Reino Unido».12,13
La sociedad juzgará si 1,25 millones de AVAC es un precio aceptable para el NHS y sus pacientes en la búsqueda de alcanzar estos objetivos más amplios.
Impacto en la salud poblacional de los nuevos medicamentos recomendados por el National Institute for Health and Care Excellence en Inglaterra durante 2000–20: un análisis retrospectivo

Los sistemas de salud experimentan difíciles disyuntivas a la hora de pagar por nuevos medicamentos. En Inglaterra, las recomendaciones de financiación del National Institute for Health and Care Excellence (NICE) para nuevos medicamentos pueden generar beneficios para la salud, pero inevitablemente resultan en una pérdida de salud, ya que los fondos no se pueden utilizar para tratamientos y servicios alternativos. Nuestro objetivo fue evaluar el impacto en la salud poblacional de las recomendaciones del NICE para nuevos medicamentos durante el período 2000-2020.
Resultados
NICE evaluó 332 productos farmacéuticos únicos entre 2000 y 2020; 276 (83%) tuvieron recomendaciones positivas. De estos 276, 207 (75%) tuvieron una evaluación NICE dentro de los 5 años posteriores a la aprobación regulatoria. Incluimos 183 (88%) de 207 medicamentos en este análisis, después de excluir los medicamentos que no cumplían con los criterios de elegibilidad. La mediana de la ganancia del AVAC en las 339 evaluaciones fue de 0,49 (RIC 0,15-1,13), lo que equivale a medio año adicional con plena salud.
La mediana de la ICER para recomendar nuevos fármacos aumentó de 21 545 libras esterlinas (RIC 14 175-26 173) por AVAC obtenido para 14 evaluaciones publicadas entre 2000 y 2004 a 28 555 libras esterlinas (19 556-33 712) para 165 evaluaciones publicadas entre 2015 y 2020 (p=0,014). La mediana de la RCEI varió según el área terapéutica, oscilando entre 6478 libras esterlinas (3526-12 912) para 12 evaluaciones de medicamentos antiinfecciosos y 30.000 libras esterlinas (22.395-45.870) para 144 evaluaciones de medicamentos oncológicos (p<0,0001).
Se estima que los nuevos fármacos generaron 3,75 millones de AVAC adicionales en 19,82 millones de pacientes que recibieron nuevos fármacos recomendados por el NICE. El uso de nuevos medicamentos supuso un coste adicional estimado para el NHS de 75.100 millones de libras esterlinas. Si los recursos asignados a los nuevos medicamentos se hubieran gastado en los servicios existentes en el NHS, se estima que se podrían haber generado 5,00 millones de AVAC adicionales durante 2000-20. En general, el impacto acumulado de los fármacos recomendados por el NICE en la salud de la población fue negativo, con una pérdida neta de aproximadamente 1,25 millones de AVAC.
Interpretación
Durante 2000-2020, la cobertura del NHS de nuevos medicamentos desplazó la salud de la población más de la que generó. Nuestros resultados ponen de manifiesto las compensaciones inherentes entre los individuos que se benefician directamente de los nuevos fármacos y los que renuncian a la salud debido a la reasignación de recursos hacia los nuevos fármacos.
Financiación
El Fondo de la Commonwealth.
Introducción
Pocas decisiones en el ámbito de la atención sanitaria suscitan tanta controversia como las relativas a la financiación, o la falta de ella, de nuevos medicamentos. Los nuevos medicamentos suelen tener una pequeña base de pruebas que respaldan su uso tras la aprobación regulatoria en todo el mundo.1,2 A pesar de las incertidumbres en la base de evidencia, los nuevos medicamentos suelen tener precios más altos que las opciones existentes dentro de los sistemas de atención de salud.3 Esta combinación de efectividad clínica incierta y precios más altos ha resultado históricamente en una variación regional y global sustancial en las decisiones de financiamiento y el acceso de los pacientes a nuevos medicamentos.4,5
La investigación en contexto
Evidencias previas a este estudio
Investigaciones anteriores han caracterizado la evidencia clínica que respalda la aprobación regulatoria y la evaluación de tecnologías sanitarias de nuevos medicamentos en Europa y Estados Unidos, destacando deficiencias en la solidez de la evidencia que subyace a las decisiones de aprobación y financiación, y ha demostrado que los precios de los nuevos medicamentos son altos y están aumentando a nivel mundial, lo que plantea preguntas sobre su rentabilidad. Se realizaron búsquedas en MEDLINE desde el inicio de la base de datos hasta el 25 de septiembre de 2024, sin restricciones de idioma, utilizando varias combinaciones de los términos de búsqueda «fármacos», «medicamentos», «farmacoterapia», «beneficio neto para la salud», «costo de oportunidad» y «salud de la población» para identificar estudios que evaluaran los efectos netos en la salud de los nuevos fármacos en todo el mundo. Aunque algunos estudios observacionales indicaron que los nuevos medicamentos han contribuido a aumentar la esperanza de vida a nivel poblacional durante los últimos cuatro decenios, ninguna investigación ha examinado el impacto de los nuevos medicamentos en la salud de la población en general, teniendo en cuenta tanto los beneficios para la salud como la salud perdida por la asignación de recursos finitos hacia los nuevos medicamentos y alejada de las prioridades de atención de la salud alternativas.
Valor añadido de este estudio
Estimamos el número de pacientes que recibieron nuevos medicamentos recomendados por el National Institute for Health and Care Excellence (NICE) en Inglaterra durante 2000-20, documentando los impactos económicos y de salud a nivel poblacional de los nuevos medicamentos en múltiples áreas terapéuticas. También estimamos los efectos en la salud de los servicios que no pudieron ser financiados debido a la asignación de recursos a nuevos medicamentos. Estimamos que los nuevos fármacos desplazan más salud de lo que generan a nivel poblacional. Hasta donde sabemos, esta es la primera evaluación del impacto de los nuevos medicamentos en la salud de la población en general.
Implicaciones de toda la evidencia disponible
Nuestro hallazgo hace hincapié en las compensaciones y la priorización implícita de las personas que se beneficiarán directamente de los nuevos medicamentos a expensas de las personas que no lo harán. Una consideración importante de política es si el umbral de NICE debería alinearse mejor con la estimación de los costos de oportunidad de salud del gasto del Servicio Nacional de Salud del Departamento de Salud y Asistencia Social. La presentación de las recomendaciones del NICE en relación con el umbral del costo de oportunidad para la salud generaría compensaciones en las decisiones de financiamiento. Las investigaciones futuras deben explorar la implementación de las recomendaciones de financiamiento de NICE por parte de los tomadores de decisiones.El National Institute for Health and Care Excellence (NICE), establecido originalmente como el National Institute for Clinical Excellence en 1999, tenía como objetivo explícito abordar esta «prescripción de código postal» en Inglaterra.6 Una de las principales responsabilidades de NICE es proporcionar recomendaciones de financiación para el Servicio Nacional de Salud (NHS) en Inglaterra. El NICE basa sus recomendaciones en «una evaluación de los beneficios para la población y la relación calidad-precio».7 Un principio básico que guía el trabajo de NICE es la consideración del «‘costo de oportunidad’ de recomendar una intervención en lugar de otra», así como la contabilidad de los beneficios perdidos de gastar recursos finitos.7La relación calidad-precio de los nuevos medicamentos recomendados por NICE tiene consecuencias para la salud de la población. Con un presupuesto limitado, la opción de financiar un nuevo medicamento para un grupo de pacientes podría significar renunciar a la financiación de intervenciones y servicios que brindarían beneficios para otros.8 El NICE aconseja a sus comités que consideren que los nuevos medicamentos ofrecen una buena relación calidad-precio y, por lo tanto, son adecuados para la financiación dentro del NHS, si cuestan menos de 20.000-30.000 libras esterlinas por año adicional de salud completa obtenido, medido como años de vida ajustados por calidad (AVAC).9 Históricamente, no ha habido ninguna base empírica para el umbral de financiación de NICE.10 Los análisis que examinan la relación entre el gasto del NHS y los resultados de salud han sugerido que el NHS gasta aproximadamente £ 15 000 para generar un año adicional de salud completa con los servicios existentes, que es utilizado por el Departamento de Salud y Asistencia Social del Reino Unido.11,12 Por lo tanto, gastar más de esta cantidad podría perjudicar la salud de la población, ya que podría desplazar más salud de la que genera. Es esencial comprender los efectos netos de las decisiones de financiación del NICE sobre la salud de la población, teniendo en cuenta tanto la relación calidad-precio de los nuevos medicamentos como las implicaciones de la desinversión en otras áreas.
Nuestro objetivo fue evaluar el impacto en la salud poblacional de las recomendaciones del NICE para nuevos medicamentos durante el período 2000-2020. Nuestro objetivo fue caracterizar los beneficios adicionales para la salud y la relación calidad-precio que ofrecen los nuevos fármacos mediante la revisión sistemática de los informes de evaluación disponibles públicamente. A continuación, nos propusimos cuantificar los efectos netos sobre la salud por paciente en diferentes áreas terapéuticas y estimar sus efectos netos sobre la salud de la población teniendo en cuenta el número de pacientes que recibieron los fármacos recomendados por el NICE.
Métodos
Fuentes de datos
Para este análisis retrospectivo, buscamos e identificamos manualmente las evaluaciones de tecnología para nuevos medicamentos en Inglaterra publicadas desde el año 2000 en la base de datos de evaluaciones disponible públicamente de NICE.13 Para tener en cuenta la creciente frecuencia de información censurada en los documentos de NICE, incluimos evaluaciones publicadas hasta 2020.14,15 Se excluyeron los productos con valoraciones finalizadas, no recomendados o posteriormente retirados del mercado. No se incluyeron las evaluaciones en el programa de Tecnologías Altamente Especializadas del NICE y otros programas centrados en dispositivos médicos, diagnósticos o procedimientos intervencionistas. Se incluyeron medicamentos que se sometieron a la evaluación NICE dentro de los 5 años posteriores a la aprobación regulatoria inicial. Por lo tanto, se diferenció entre los fármacos nuevos, a menudo asociados con precios más altos y pruebas menos completas.2,3 y los que han estado disponibles en el mercado durante más tiempo (apéndice P 3).Para identificar todas las indicaciones aprobadas de nuevos medicamentos, revisamos el Formulario Nacional Británico y mapeamos las indicaciones correspondientes evaluadas por NICE.16 Se incluyeron todas las indicaciones evaluadas posteriormente de los medicamentos, siempre y cuando la evaluación inicial de NICE para cualquier indicación se produjera dentro de los primeros 5 años de la aprobación de la agencia reguladora. Para las indicaciones con evaluaciones actualizadas, consideramos el año de la primera evaluación positiva. Nuestro conjunto de datos final incluyó una evaluación de tecnología por indicación evaluada por NICE con una recomendación de financiación positiva.
Extracción de datos
Se recopilaron datos sobre el nombre del medicamento, la indicación evaluada y las características específicas tanto del medicamento como de su evaluación. Se estableció si la indicación del medicamento tenía una designación huérfana (es decir, una designación para el tratamiento de enfermedades raras) de la Agencia Europea de Medicamentos en el momento de la evaluación de NICE.17 si el comité de evaluación tecnológica del NICE concluyó que el medicamento era innovador,18 y si la evaluación cumplía con los criterios de fin de vida útil de NICE que habían estado vigentes desde 2009 y permanecieron vigentes durante la duración de nuestro análisis.19 El proceso de extracción de datos fue llevado a cabo de forma independiente por dos investigadores, uno de los cuales fue PM. El consenso se alcanzó a través de la discusión, y un tercer investigador (HN) verificó todos los datos extraídos.Observamos la relación calidad-precio que ofrecen los nuevos fármacos, expresada como la relación coste-efectividad incremental (ICER; panel),20,21 que se calcula dividiendo la diferencia en los costos totales (es decir, el costo incremental) por la diferencia en los beneficios para la salud (es decir, los beneficios incrementales para la salud). Este proceso genera una proporción que muestra el costo adicional por unidad adicional de salud. El NICE utiliza los AVAC como medida de los beneficios para la salud; un AVAC representa 1 año en plena salud.22 El uso de AVAC facilita la comparación de las RCIE en todas las áreas terapéuticas y con usos alternativos de los recursos del sistema de salud. Los AVAC, los costos y las RCIE suelen estimarse para toda la vida de un paciente. Dado que la evidencia de los ensayos clínicos utilizada para respaldar la aprobación de nuevos medicamentos proporciona un período de seguimiento mucho más corto, el NICE generalmente considera los resultados de por vida estimados con modelos analíticos de decisiones que combinan evidencia de una variedad de fuentes, como ensayos clínicos aleatorios, estudios observacionales y estudios de uso de recursos. Los comparadores en los análisis de coste-efectividad de NICE representan el estándar de atención del NHS.9
Relación costo-efectividad incremental
Medida resumida que representa el costo adicional requerido para lograr una unidad adicional de resultado de salud con un nuevo tratamiento, en comparación con una alternativa. Se calcula dividiendo la diferencia en los costos totales (es decir, el costo incremental) por la diferencia en los beneficios para la salud (es decir, los beneficios incrementales para la salud). Las relaciones incrementales de costo-efectividad bajas indican una mejor relación calidad-precio que las relaciones de costo-efectividad incrementales altas.
Efecto neto sobre la salud
Una medida resumida que cuantifica el impacto de un nuevo tratamiento, considerando tanto los beneficios para la salud del nuevo tratamiento como los beneficios para la salud a los que se renuncia debido a la asignación de recursos al nuevo tratamiento. Un efecto neto negativo en la salud indica que los beneficios para la salud del nuevo tratamiento no compensan suficientemente las pérdidas de salud sufridas por el desvío de recursos de los servicios de atención de la salud alternativos.
Costo de oportunidad
Beneficios para la salud a los que se renuncia debido a la implementación de un nuevo tratamiento. En un sistema de salud con un presupuesto fijo, el aumento de los costos necesarios para pagar un nuevo tratamiento podría desplazar a otros servicios de atención de la salud que ya se están prestando o que podrían prestarse si se dispusiera de fondos. En tales casos, el costo de oportunidad se refiere a los beneficios de salud perdidos debido al desplazamiento de las actividades existentes para financiar el nuevo tratamiento.
Años de vida ajustados por calidad
Medida de resultados de salud que combina los efectos de las mejoras en la cantidad y la calidad de vida asociadas con un tratamiento. A la salud completa se le asigna un valor de 1 y a la muerte se le asigna un valor de 0. Un año pasado con una calidad de vida que se considera la mitad de la de una persona con plena salud equivaldría a 0,5 años de vida ajustados por calidad.
Del documento de evaluación final se extrajo la RCIC preferida del comité de evaluación de tecnología del NICE. En caso de que no se dispusiera de la RCIE preferida por el comité, se llevó a cabo una revisión jerárquica teniendo en cuenta las diapositivas públicas del comité que resumían los datos disponibles, los informes de los grupos de revisión de la evidencia y las presentaciones de los fabricantes (apéndice p 3).
A continuación, extrajimos los AVAC incrementales y los costes correspondientes a los ICER extraídos de la documentación de NICE siguiendo el mismo enfoque jerárquico. Cuando los AVAC incrementales coincidentes no estaban disponibles en la documentación de NICE, verificamos sistemáticamente la información correspondiente de otras fuentes (apéndice p 3). Se calcularon los costos incrementales faltantes utilizando AVAC incrementales imputados y RCIE extraídos. Cuando los fabricantes ofrecieron reducciones de precios confidenciales durante el proceso de evaluación de NICE, los ICER finales reflejaron estas reducciones y se tuvieron en cuenta en los costos incrementales utilizados en nuestro análisis. Los costos y las RCIE reflejaban los precios reales en términos nominales en el momento de la evaluación, con descuentos ya aplicados. Por lo tanto, no aplicamos descuentos adicionales, ya que nuestro objetivo era evaluar la razonabilidad de las decisiones en el momento en que se tomaron.
Estimación del número de pacientes
Dado que el NHS no recopila información de forma centralizada sobre el uso de medicamentos con receta tanto en el ámbito de la atención primaria como en la secundaria,23 obtuvimos datos patentados sobre los volúmenes totales de nuevos medicamentos vendidos en Inglaterra entre el 1 de enero de 2000 y el 31 de diciembre de 2020 del Sistema Multinacional Integrado de Análisis de Datos (MIDAS) de IQVIA. MIDAS registra datos sobre el volumen de productos de marca y genéricos dispensados tanto en farmacias minoristas como hospitalarias. Las fuentes de datos son fabricantes, mayoristas y farmacias hospitalarias y minoristas. MIDAS no se limita a las ventas del NHS, ya que capta el pequeño número de recetas privadas dispensadas por los farmacéuticos comunitarios y utilizadas para pacientes tratados de forma privada en las salas del NHS (pero no en hospitales privados). Este conjunto de datos es la fuente más completa de datos sobre el volumen de ventas de productos farmacéuticos en Inglaterra y se utiliza para evaluar el uso de medicamentos por parte del Gobierno del Reino Unido.24–26Los datos de ventas estaban disponibles en unidades estándar, una medida de volumen definida por IQVIA para representar la dosis común más pequeña de una forma de producto. Para calcular el total de días de tratamiento de los pacientes, dividimos las unidades estándar de cada fármaco por las dosis diarias definidas (DDD). Las DDD representaron la dosis media de mantenimiento supuesta por día para un fármaco utilizado en su indicación aprobada. La DDD es un método desarrollado por la OMS para estandarizar medicamentos de dosis variables.27 Si la OMS no disponía de factores DDD, utilizamos los calculados por IQVIA para monitorizar el uso global de nuevos medicamentos.28
Para estimar el número de pacientes que recibieron los nuevos fármacos en sus indicaciones evaluadas, dividimos el total de días de tratamiento de los pacientes por la duración media del tratamiento. La información sobre la duración del tratamiento se obtuvo de documentos del NICE y de búsquedas bibliográficas específicas (apéndice, p 4). Se utilizó IQVIA MIDAS Disease para obtener información sobre la proporción relativa de uso en diferentes indicaciones. Este conjunto de datos estima el uso a nivel de indicación sobre la base de encuestas transversales repetidas a prescriptores en países europeos. Se asignó el total de días de paciente en función de la proporción de uso dentro de cada indicación. A continuación, dividimos el total de días de tratamiento de los pacientes por su correspondiente duración del tratamiento (apéndice p 4).
Análisis estadístico
Resumimos las ganancias incrementales de AVAC a nivel de evaluación y las RCIE utilizando datos de mediana (RIC) a lo largo del tiempo, por área terapéutica y por características del fármaco y la evaluación (es decir, criterios huérfanos, de innovación y de fin de vida). Se compararon las medianas utilizando una prueba no paramétrica de k-muestra en Stata versión 18.A continuación, calculamos el efecto neto sobre la salud por paciente para cada evaluación.29 El efecto neto sobre la salud representa la diferencia entre las ganancias incrementales del AVAC derivadas de la implementación del nuevo fármaco en el NHS y los AVAC estimados que hipotéticamente podrían obtenerse reasignando los mismos fondos a otros servicios o tratamientos del NHS. Obtuvimos los AVAC renunciados dividiendo el costo incremental del nuevo medicamento por el costo de oportunidad para la salud del gasto del NHS. Utilizamos 15 000 libras esterlinas por AVAC ganado como estimación del coste de oportunidad para la salud, en consonancia con las evaluaciones de impacto del Departamento de Salud y Asistencia Social del Reino Unido y la evidencia empírica sobre la productividad del gasto del NHS.11,12,30–32 Este proceso implica que por cada 15.000 libras esterlinas asignadas a nuevos gastos en medicamentos, los pacientes de otras partes del sistema de salud renuncian a 1 AVAC. Un efecto neto positivo sobre la salud indica que la recomendación de la evaluación mejora los resultados sanitarios, mientras que un efecto neto negativo sobre la salud sugiere que los beneficios para la salud del nuevo fármaco no compensan adecuadamente las pérdidas de salud resultantes de la reasignación de los fondos de atención sanitaria para dar cabida al nuevo fármaco.29
A continuación, estimamos el número total de AVAC obtenidos con cada fármaco a nivel poblacional multiplicando el número de pacientes por los AVAC incrementales. Del mismo modo, calculamos el gasto adicional total en cada medicamento multiplicando el número de pacientes por los costos incrementales.
Para estimar el número total de AVAC que se podrían haber obtenido si los mismos costos se hubieran asignado a otro lugar, dividimos el costo adicional total de los nuevos medicamentos por la estimación del costo de oportunidad para la salud del Departamento de Salud y Asistencia Social (es decir, 15 000 libras esterlinas por AVAC). Por último, estimamos el impacto en la salud poblacional de los nuevos fármacos recomendados por el NICE comparando el total de AVAC obtenidos y el total de AVAC que podrían haberse obtenido durante 2000-20.
Se realizaron análisis de sensibilidad múltiple (apéndice p 6). En primer lugar, limitamos nuestro análisis a los datos de 2010 a 2020, para centrarnos en el impacto en la salud de la población de los medicamentos evaluados más recientemente. En segundo lugar, evaluamos el impacto de que más o menos pacientes recibieran los nuevos fármacos cambiando la duración media del tratamiento. En tercer lugar, consideramos el impacto de la reducción de los costos incrementales de los medicamentos con alternativas genéricas o biosimilares. En cuarto lugar, consideramos cómo los umbrales alternativos de costo de oportunidad impactan los efectos netos sobre la salud. En quinto lugar, en el caso de los fármacos con múltiples indicaciones, asumimos que todo el uso se produjo en la indicación con menor o mayor ICER.
Todos los análisis se realizaron en Stata versión 18.
Papel de la fuente de financiación
El financiador del estudio no participó en el diseño del estudio, la recopilación de datos, el análisis de datos, la interpretación de datos ni la redacción del informe.
Resultados
NICE evaluó 332 productos farmacéuticos únicos entre 2000 y 2020; 276 (83%) tuvieron recomendaciones positivas. De estos 276, 207 (75%) tuvieron una evaluación NICE dentro de los 5 años posteriores a la aprobación regulatoria. Incluimos 183 (88%) de 207 medicamentos en este análisis, después de excluir los medicamentos que no cumplían con los criterios de elegibilidad (apéndice p 9).
Los 183 medicamentos incluidos tenían aprobaciones regulatorias para su uso en 385 indicaciones. 287 (75%) de las 385 indicaciones recibieron recomendaciones positivas en 339 evaluaciones separadas del NICE realizadas entre 2000 y 2020 y se incluyeron en nuestro análisis (apéndice p 9). La oncología comprendió 154 (45%) de las 339 evaluaciones, seguida de 71 (21%) evaluaciones para inmunología y 27 (8%) evaluaciones para el sistema vascular. De las 339 tasaciones, 191 (56%) se publicaron entre 2015 y 2020. Entre 2000 y 2020, 35 (19%) de los 183 nuevos medicamentos recomendados por el NICE tenían alternativas genéricas o biosimilares.
La mediana de la ganancia de AVAC en las 339 evaluaciones fue de 0,49 (RIC 0,15-1,13), lo que equivale a medio año adicional en plena salud (figura 1A). La mediana de las ganancias del AVAC fue de 0,35 (0,17–0,78) para 16 evaluaciones publicadas entre 2000 y 2004 y de 0,59 (0,17–1,30) para 191 evaluaciones publicadas entre 2015 y 2020 (p=0,046). Hubo una variación significativa entre las áreas terapéuticas, oscilando entre 0,07 (0,02-0,22) AVAC adicionales obtenidos para las 27 evaluaciones de fármacos del sistema vascular y 0,74 (0,32-2,53) para 16 evaluaciones de fármacos antiinfecciosos (p<0,0001; figura 1B).
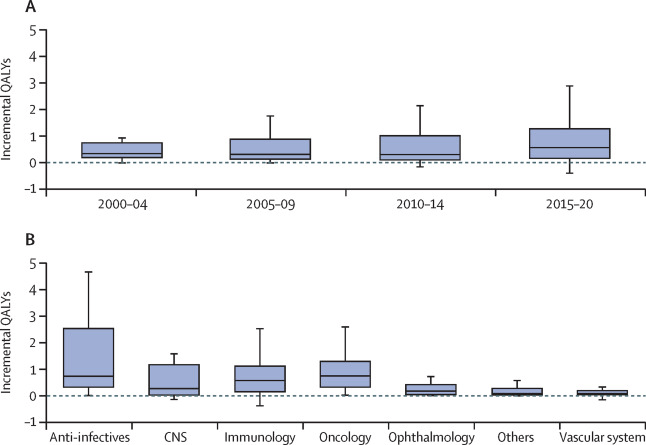
La mediana de la RCEI para recomendar nuevos fármacos aumentó de 21 545 libras esterlinas (RIC 14 175-26 173) por AVAC obtenido para 14 evaluaciones publicadas entre 2000 y 2004 a 28 555 libras esterlinas (19 556-33 712) para 165 evaluaciones publicadas entre 2015 y 2020 (p = 0,014; figura 2A). La mediana de la RCIE varió según el área terapéutica, oscilando entre 6478 libras esterlinas (IQR 3526-12 912) para 12 evaluaciones de medicamentos antiinfecciosos y 30 000 libras esterlinas (22 395-45 870) para 144 evaluaciones de medicamentos oncológicos (p<0,0001); figura 2B).
02352-3/asset/9c02f13a-4d93-4cec-a539-4b2ad5772f0f/main.assets/gr2.jpg)
Al considerar la pérdida anticipada de AVAC en otras partes del NHS debido al aumento de los costos de los nuevos medicamentos, 233 (69%) de las 339 evaluaciones resultaron en efectos netos negativos para la salud. La mediana del efecto neto sobre la salud por paciente fue de –0,06 (RIC –0,49 a 0,04) para las evaluaciones publicadas entre 2000 y 2004; –0,15 (–0,40 a 0,01) para las evaluaciones publicadas entre 2005 y 2009; –0,07 (–0,49 a 0,06) para las evaluaciones publicadas entre 2010 y 2014; y –0,30 (–1,19 a 0,01) para las tasaciones publicadas entre 2015 y 2020 (p=0,080; figura 3A). La mediana del efecto neto sobre la salud por paciente varió según el área terapéutica, oscilando entre –0,52 (RIC –1,52 a –0,18) para las evaluaciones en oncología y 0,97 (0,15 a 1,99) para las evaluaciones en antiinfecciosos (p<0,0001); figura 3B).
02352-3/asset/3eb52a6b-6c33-4ea4-b19f-c77d79d2ed54/main.assets/gr3.jpg)
Durante 2000-2020, estimamos que 19,82 millones de pacientes recibieron nuevos fármacos recomendados por el NICE. El número estimado de pacientes que recibieron estos fármacos varió según el área terapéutica, oscilando entre 0,17 millones para los antiinfecciosos y 7,53 millones para los tratamientos del sistema vascular.
El uso de nuevos medicamentos supuso un coste adicional estimado para el NHS de 75.100 millones de libras esterlinas. Las áreas terapéuticas que más contribuyeron a estos costes adicionales fueron la inmunología (25.700 millones de libras), la oncología (22.700 millones de libras) y el sistema vascular (16.000 millones de libras; figura 4A).
02352-3/asset/8d09c552-802d-42d2-abec-329854d0aecc/main.assets/gr4.jpg)
Se estima que los nuevos medicamentos generaron 3,75 millones de AVAC adicionales (figura 4B). De estos, se estima que 1,10 millones de AVAC adicionales fueron atribuibles a los nuevos fármacos utilizados en inmunología, 0,97 millones de AVAC adicionales fueron atribuibles a los utilizados para el sistema vascular y 0,64 millones de AVAC adicionales fueron atribuibles a los utilizados en oncología. Si los recursos asignados a los nuevos medicamentos se hubieran gastado en los servicios existentes en el NHS, se estima que se podrían haber generado 5,00 millones de AVAC adicionales durante 2000-20 (figura 4C). En inmunología se renunció a 1,71 millones de AVAC, en oncología se prescindió de 1,51 millones de AVAC y en el sistema vascular se prescindió de 1,07 millones de AVAC.
El efecto neto sobre la salud del uso de los nuevos fármacos recomendados por el NICE en el NHS fue positivo para los antiinfecciosos, los tratamientos oftalmológicos y los fármacos que clasificamos como otros (es decir, respiratorios, gastrointestinales, endocrinos, ortopédicos, urológicos, dermatológicos y de salud mental), lo que en conjunto dio lugar a aproximadamente 0,36 millones de AVAC adicionales a nivel poblacional (figura 4D). Sin embargo, el resto de las áreas terapéuticas tuvieron un efecto neto negativo en la salud, y el uso de fármacos oncológicos representó una pérdida de 0,87 millones de AVAC a nivel poblacional.
El efecto neto sobre la salud de los nuevos fármacos se volvió progresivamente más negativo con el tiempo (figura 5A), impulsado principalmente por el impacto neto del uso más generalizado de fármacos oncológicos e inmunológicos (figura 5B). En general, el impacto acumulado de los medicamentos recomendados por el NICE en la salud de la población fue negativo durante 2000-2020, lo que resultó en una pérdida neta de aproximadamente 1,25 millones de AVAC. Los costos incrementales habrían tenido que reducirse en una mediana del 42% (IQR 13-53) en el momento de la evaluación del NICE para garantizar que los nuevos medicamentos contribuyeran positivamente a la salud de la población durante 2000-20.
02352-3/asset/3eed69ae-d8ac-4899-bb34-cc6304efe215/main.assets/gr5.jpg)
En los análisis de sensibilidad, los únicos escenarios que arrojaron un impacto positivo en la salud fueron cuando asumimos que todo el uso de cada medicamento estaba en la indicación más costo-efectiva, con la RCIE más baja, y cuando consideramos 30 000 libras esterlinas como una medida alternativa del costo de oportunidad (figura 6).
02352-3/asset/ed3dbb78-d30b-4946-a664-0e42f6fc926d/main.assets/gr6.jpg)
Discusión
Cuantificamos el impacto en la salud poblacional de los nuevos fármacos recomendados por el NICE durante 2000-2020. Los nuevos medicamentos generaron el equivalente a 3,75 millones de años adicionales de salud plena. Sin embargo, la reasignación de los gastos adicionales en estos nuevos medicamentos a otros tratamientos y servicios del NHS podría haber generado el equivalente a 5,00 millones de años adicionales de salud plena. Aunque los nuevos medicamentos podrían haber beneficiado a los pacientes que los recibieron, su acceso tuvo un costo considerable para otros que podrían haberse perdido posibles beneficios para la salud debido a la necesaria desinversión o la falta de inversión en otras formas de atención para financiar estos medicamentos recién recomendados. El NICE recomienda cada vez más fármacos con RCIE que superan su umbral habitual de coste-efectividad.33 A través de la ponderación explícita del AVAC y otros mecanismos, el NICE da prioridad a los pacientes con mayores necesidades insatisfechas y que podrían beneficiarse de nuevos fármacos, valorando sus beneficios para la salud más que los de los pacientes cuyas necesidades pueden satisfacerse en otras partes del NHS.34,35 Sin embargo, las encuestas nacionales y los estudios cualitativos no han encontrado apoyo social para esta priorización.36–38 Además, este enfoque no tiene en cuenta que los costes de oportunidad de los medicamentos para los pacientes con necesidades sustanciales no satisfechas puedan afectar a otros con necesidades similares en el NHS, lo que socava la justificación moral de las recomendaciones de financiación.39Nuestro análisis hace una contribución importante a la literatura. No solo documentamos las ganancias incrementales de QALY y los ICER a lo largo del tiempo, ampliando así los estudios anteriores, sino que también40–43 pero también utilizaron datos sobre volúmenes de prescripción para evaluar los impactos a nivel poblacional por primera vez, hasta donde sabemos. Contrariamente a estudios anteriores que sugieren que los nuevos medicamentos se asocian con mejoras sustanciales en la salud a nivel poblacional en todo el mundo.44–47 contribuyendo a más de un tercio de los aumentos de la esperanza de vida en las últimas cuatro décadas,48 encontramos que el uso de nuevos medicamentos recomendados por el NHS en Inglaterra tuvo un impacto general negativo en la salud de la población. Nuestros resultados difieren porque los estudios anteriores solo cuantificaron los beneficios de los medicamentos, descuidando sus posibles costos de oportunidad para la salud. Consideramos los beneficios para la salud que podrían derivarse de los usos alternativos de los gastos farmacéuticos, lo que nos permitió calcular los efectos netos sobre la salud. Las investigaciones futuras deben explorar la implementación de las recomendaciones de financiamiento de NICE y documentar las compensaciones experimentadas por los tomadores de decisiones.Nuestra estimación de los beneficios para la salud perdidos asociados con la financiación de nuevos medicamentos se basa en la estimación del Departamento de Salud y Asistencia Social del Reino Unido sobre el costo de oportunidad para la salud del gasto del NHS.30 Esta es la mejor estimación actual del impacto esperado en la salud de la reducción de los gastos sanitarios disponibles en el NHS.11,12 Los medicamentos recomendados por NICE incurren en costos adicionales y reducen directamente los recursos disponibles para el resto del NHS. Por lo tanto, podemos utilizar esta cifra para estimar el impacto esperado en los resultados de salud debido al desplazamiento de otros servicios del SNS. Una amplia bibliografía ha demostrado la solidez de la estimación de 15.000 libras esterlinas por AVAC.49–52 Por el contrario, el umbral establecido de NICE (es decir, 20 000 a 30 000 libras esterlinas por AVAC) no tiene ninguna base empírica.53El acuerdo de 2024 entre el Gobierno del Reino Unido y la industria farmacéutica ha comprometido a NICE a mantener su umbral de rentabilidad hasta 2029. Una consideración política importante es si el umbral de NICE debería alinearse mejor con la estimación del Departamento de Salud y Asistencia Social del costo de oportunidad para la salud del gasto del NHS.54 Hacerlo garantizaría que el NHS no pague más por los beneficios de los nuevos medicamentos de lo que paga por los beneficios de los tratamientos y servicios existentes. Sin embargo, existe una oposición sustancial por parte de la industria, ya que la reducción del umbral daría lugar a una reducción de los precios y, por lo tanto, a una reducción de los beneficios de la industria. El NHS debe encontrar un equilibrio entre la promoción de la innovación farmacéutica y la garantía de la capacidad del sistema para prestar todas las formas de atención que ofrezcan una buena relación calidad-precio. Aunque un umbral único podría no ser el mejor enfoque para equilibrar los objetivos de salud de la población y la innovación, un nivel de precios adecuado probablemente sería equivalente o inferior al valor proporcional a un umbral de 15 000 libras esterlinas por AVAC para la mayoría de los productos.55La discrepancia entre el umbral de costo-efectividad de NICE y el umbral de costo de oportunidad del sistema de salud pone de relieve la incoherencia en el enfoque de NICE: su compromiso manifiesto con el principio de costo de oportunidad y beneficios para la población a pesar de usar un umbral que no refleja con precisión el costo de oportunidad del NHS.39 Esta discrepancia podría poner en peligro la legitimidad del NICE a la hora de apoyar el objetivo del NHS de maximizar los beneficios sanitarios con recursos escasos.56–58 El concepto de costo de oportunidad sigue siendo difícil de implementar en la práctica, y a menudo se pasa por alto en los procesos de toma de decisiones.59–63 En la actualidad, el NICE no reconoce las consecuencias para la salud de la población de las recomendaciones que superan el umbral de costo de oportunidad del sistema de salud.La presentación de las recomendaciones del comité en relación con el umbral del coste de oportunidad para la salud (es decir, 15 000 libras esterlinas por AVAC) transmitiría la compensación entre las personas que se benefician directamente y otros usuarios del NHS que podrían perder prioridad a medida que las intervenciones existentes y los servicios del NHS se desplazan para adaptarse a nuevos medicamentos.64 Por ejemplo, el NICE recomendó el trastuzumab para el tratamiento de personas con cáncer gástrico metastásico en 2010, y el comité consideró rentable una RCIE de 43.206 libras esterlinas por AVAC. Expresar este resultado como 2,88 AVAC perdidos por AVAC ganado dilucidaría mejor la importancia relativa asignada a los pacientes que se benefician del tratamiento en comparación con otros que se espera que renuncien a la salud.64 A nivel poblacional, el uso de trastuzumab en personas con cáncer gástrico provocó la pérdida de 4000 AVAC durante 2010–20. Sin embargo, presentar recomendaciones de esta manera puede ser un desafío para los responsables de la formulación de políticas debido a los compromisos históricos y actuales con el umbral de 20 000 a 30 000 libras esterlinas por AVAC.La perspectiva predominante en la política farmacéutica sugiere que el impacto negativo en la salud de los precios altos durante el período de protección de las patentes podría ser una compensación aceptable si las reducciones de precios posteriores a la expiración de las patentes mitigaran los efectos negativos en la salud de la población.65 Sin embargo, la evidencia relacionada con la disponibilidad, el uso y el precio de los genéricos y biosimilares sugiere que esta mitigación suele ser insuficiente.66 Entre 2000 y 2020, solo 35 (19%) de los 183 nuevos medicamentos recomendados por el NICE tenían alternativas genéricas o biosimilares. La contabilización de las reducciones de costos después de la entrada de genéricos o biosimilares no cambió significativamente el impacto en la salud de la población. En general, los costos incrementales habrían tenido que reducirse en una mediana del 42% (IQR 13-53) en el momento de la evaluación del NICE para garantizar que los nuevos medicamentos contribuyeran positivamente a la salud de la población durante 2000-20.Nuestros hallazgos reflejan las características del NHS inglés, que opera bajo un presupuesto limitado e intensas restricciones de recursos.67 Los indicadores de rendimiento más importantes del NHS ya no se cumplen.68 En este entorno, pagar precios elevados por los nuevos medicamentos puede afectar negativamente a la salud de la población, potencialmente más que en sistemas con mayor flexibilidad presupuestaria. Sin embargo, otros sistemas de salud tienen desafíos similares.69 A medida que surjan nuevas innovaciones con precios más altos, el costo de oportunidad será aún más importante si el objetivo es mejorar la salud de muchos, no de los pocos que se beneficiarán del nuevo medicamento. Incluso en entornos en los que se pueden disponer de fondos adicionales para pagar nuevos medicamentos, estos recursos podrían producir mayores beneficios para la salud si se asignan a otros tratamientos y servicios.70 En consecuencia, el concepto de costo de oportunidad —y nuestra metodología— es relevante para otros sistemas de salud con presupuestos más altos y flexibles.Nuestro análisis tuvo limitaciones. En primer lugar, la fiabilidad de los datos extraídos en relación con los beneficios adicionales para la salud y la relación calidad-precio de los nuevos medicamentos se vio afectada por las redacciones, que se han vuelto frecuentes en los últimos 10 años.14,15 Nuestra solicitud de libertad de información de AVAC incrementales redactados para un subconjunto de evaluaciones fue rechazada por NICE. En consecuencia, utilizamos un enfoque jerárquico sistemático para imputar la información faltante de otras fuentes. A menos que se reviertan las prácticas de redacción, no se podrán realizar análisis similares en el futuro, lo que socavará la responsabilidad de las decisiones de NICE. En segundo lugar, se excluyó un pequeño número de fármacos nuevos que se incorporaron posteriormente a las guías clínicas y para los que ya no se disponía de evaluaciones tecnológicas. Estos medicamentos podrían haber sido particularmente rentables y su exclusión podría haber llevado a una subestimación del impacto positivo de los nuevos medicamentos recomendados por el NICE en la salud de la población. En tercer lugar, debido a las limitaciones en la disponibilidad de datos, desarrollamos un enfoque novedoso para estimar el número de pacientes mediante el uso de volúmenes de ventas y la duración del tratamiento a nivel de indicación. En cuarto lugar, nuestra estimación del número de pacientes no tuvo en cuenta el desperdicio de fármacos, que podría afectar especialmente a los fármacos infundidos dosificados por peso o superficie corporal.71 Dado que las prácticas de compartir viales son comunes en el Reino Unido,72 No consideramos que este fuera un factor importante. En quinto lugar, nuestro análisis tampoco tuvo en cuenta las rebajas de las empresas farmacéuticas al Gobierno del Reino Unido. Sin embargo, dada la tasa de pago relativamente baja durante este período, es poco probable que los reembolsos influyan sustancialmente en nuestros resultados.73El impacto negativo potencial de los nuevos medicamentos en la salud de la población podría ser mayor de lo que sugieren nuestros hallazgos. En primer lugar, cuando los comités NICE no preferían una sola estimación, optamos por la ICER más baja, asumiendo así que los nuevos medicamentos ofrecían una mejor relación calidad-precio de lo que podrían ofrecer en la realidad. En segundo lugar, nuestros análisis podrían haber sobrestimado los beneficios para la salud de los nuevos fármacos. Los AVAC incrementales en los documentos de NICE se basan en suposiciones sobre el rendimiento futuro de los nuevos medicamentos, que a menudo tienen poca evidencia en el momento de la evaluación.74 Por ejemplo, la mayoría de los medicamentos contra el cáncer no tienen evidencia de sus beneficios de supervivencia cuando se someten a la evaluación NICE.75,76 Sin embargo, los modelos de coste-efectividad de NICE con frecuencia asumen ganancias clínicas a largo plazo sobre la base de criterios de valoración indirectos.77,78 La mayoría de los nuevos medicamentos contra el cáncer no generan evidencia sobre los beneficios de supervivencia durante el período posterior a la comercialización.79,80 En tercer lugar, no contabilizamos los 1.300 millones de libras esterlinas gastados en el Fondo de Medicamentos contra el Cáncer entre 2011 y 2016.81 Del mismo modo, algunos fármacos de alto coste, como lumacaftor e ivacaftor para la fibrosis quística, se excluyeron de nuestra muestra por no estar recomendados por el NICE pero, sin embargo, se han puesto a disposición en el NHS y han contribuido sustancialmente al aumento del gasto en medicamentos del NHS en los últimos 5 años. También excluimos los medicamentos considerados en el marco del programa de Tecnologías Altamente Especializadas del NICE, que establece un umbral de costo-efectividad mucho más alto para recomendar medicamentos que tratan enfermedades muy raras que su umbral de £ 20 000 a 30 000 por AVAC.En conclusión, nuestro análisis de las evaluaciones de NICE durante 2000–2020 indica que NICE no logra plenamente sus objetivos declarados de basar sus recomendaciones en «una evaluación de los beneficios para la población».7 Los beneficios derivados de los nuevos fármacos recomendados por el NICE fueron superados por los beneficios potenciales que podrían haberse generado a partir de usos alternativos de los recursos asignados a estos nuevos fármacos. Entre 2000 y 2020, el impacto en la salud de la población de los nuevos fármacos recomendados por el NICE se deterioró. Es necesario introducir cambios en el marco de evaluación del NICE para garantizar que las concesiones inherentes al sector de la salud, y la priorización implícita de algunas poblaciones de pacientes sobre otras, se alineen con las opiniones y preferencias de la sociedad.
Cómo los Factores Sistémicos Afectan la Angustia Moral
Sofia Weiss Goitiandiaa , Julia K. Axelroda , Teva D. Brendera , Jason N. Battenb y Elizabeth W. Dzenga,

INTRODUCCIÓN
En un artículo reciente, Buchbinder et al. (2024) proponen el estrés moral como complemento del concepto más familiar, aunque controvertido, de angustia moral. Les preocupa que la angustia moral no tenga en cuenta la amplitud de las tensiones morales experimentadas por los profesionales de la salud. Proponen que el estrés moral puede ayudar a dirigir la atención más allá de los casos individuales de angustia experimentados en respuesta a los encuentros clínicos y hacia los «factores sistémicos generadores de estrés» (Buchbinder et al. 2024, 8). Compartimos la preocupación de los autores sobre la claridad conceptual y el alcance de la angustia moral. En este comentario, abordamos su propuesta de distinguir entre el estrés moral y la angustia moral a partir de la opinión de que los factores sistémicos juegan un papel causal en el estrés moral, pero no en la angustia moral. A partir de nuestra investigación, ofrecemos una perspectiva alternativa, argumentando que los factores sistémicos son, de hecho, fundamentales para el desarrollo de la angustia moral. Para nuestro trabajo, hemos adaptado la definición fundamental y frecuentemente citada de Jameton, según la cual «la angustia moral ocurre cuando los individuos creen que no pueden actuar de acuerdo con sus valores éticos debido a restricciones externas, como las restricciones institucionales y jerárquicas». (Rosenwohl-Mack et al. 2021; Dzeng et al. 2016; Jameton 1984). Gran parte de nuestra investigación ha examinado cómo los factores relacionados con las instituciones (p. ej., hospitales) y el sistema sanitario en su conjunto (p. ej., leyes y políticas estatales y nacionales) influyen en las experiencias de angustia moral de los médicos (Rosenwohl-Mack et al. 2021; Dzeng et al. 2018). A partir de ahora, nos referimos a los factores institucionales y del sistema de salud como «factores sistémicos». Nuestra investigación utiliza tratamientos de soporte vital (LST, por sus siglas en inglés) potencialmente no beneficiosos y de alta intensidad como un ejemplo paradigmático de cómo los factores sistémicos podrían generar angustia moral (Dzeng et al. 2018, 2016; Rosenwohl-Mack et al. 2021). Este ejemplo es especialmente pertinente dado que, si bien el sufrimiento moral se produce en varias áreas de la atención médica, es particularmente frecuente entre los médicos en las unidades de cuidados intensivos (UCI) (Whitehead et al. 2015). Sin embargo, sostenemos que una comprensión sistémica del sufrimiento moral no se limita a la atención en la UCI y puede adaptarse a otros contextos.
COMPLICANDO LA DISTINCIÓN ENTRE ANGUSTIA MORAL Y ESTRÉS MORAL
En la distinción de Buchbinder et al. entre sufrimiento moral y estrés moral, el sufrimiento moral puede explicarse principalmente con referencia a individuos o conflictos específicos e identificables. Por el contrario, el estrés moral no puede explicarse con tanta precisión: a diferencia de la angustia moral, en la que puede ser fácil culpar a determinados responsables de la toma de decisiones o a agentes de autoridad (Dudzinski 2016), el estrés moral puede no dar lugar a objetivos fáciles de culpa, aparte de culpar al «sistema» mismo… Esto se debe a que las fuentes [de estrés moral] a menudo se encuentran fuera de los encuentros clínicos individuales y las decisiones centradas en el paciente. En cambio, [el] enfoque [del estrés moral] está en los aspectos estructurales cotidianos de la atención médica que producen estrés. (Buchbinder et al. 2024, 12)
Estamos de acuerdo con Buchbinder et al. en que la angustia moral a menudo está ligada a «encuentros clínicos individuales» y «decisiones específicas centradas en el paciente». Esta afirmación es relevante para los casos de sufrimiento moral relacionados con la administración de LST de alta intensidad potencialmente no beneficiosa, ya que existe un conflicto frecuente entre los clínicos, o entre los clínicos y los pacientes o sus sustitutos, sobre si la LST debe ser retenida o retirada. Si bien estamos de acuerdo en que los conflictos interpersonales específicos contribuyen a la angustia moral, sostenemos que son simplemente las causas próximas de la angustia moral y que, lo que es más importante, los factores sistémicos subyacen a dichas causas próximas (Rosenwohl-Mack et al. 2021; Dzeng et al. 2016, 2018).
¿Cómo crean los factores sistémicos las condiciones para encuentros clínicos moralmente angustiosos que implican la retención o retirada de LST de alta intensidad potencialmente no beneficiosos?
Utilizaremos datos empíricos de entrevistas clínicas etnográficas (Tabla 1) para avanzar en nuestra posición. Estos datos se extraen de un gran estudio cualitativo multiinstitucional de 113 encuestados en tres instituciones médicas académicas, cuyos resultados se presentan en Dzeng et al. (2023).

LOS FALLOS SISTÉMICOS EN LA ATENCIÓN CLÍNICA JUEGAN UN PAPEL EXPLICATIVO EN EL SUFRIMIENTO MORAL
Sobre la base de nuestros datos, postulamos que una ruta clave entre los factores sistémicos y los casos individuales de angustia moral radica en el papel de los factores sistémicos en el establecimiento de un entorno de práctica cotidiana donde el aumento de la intensidad del tratamiento hacia el LST de alta intensidad es el defecto práctico (lo que se hace rutinariamente) y normativo (lo que se considera «correcto» o «bueno»). Este defecto parece mantenerse incluso cuando los clínicos juzgan que el LST no es potencialmente beneficioso.
En nuestros datos, los clínicos encuestados expresaron la idea de que el «sistema» o «cultura» organiza la práctica clínica hacia un defecto de aumento de la intensidad del tratamiento (Citas 1-3, Tabla 1).
Identificaron factores sistémicos específicos que contribuyen a este defecto, como los avances tecnológicos en medicina sin claridad sobre las limitaciones en su uso (Cita 4).
Los encuestados describieron cómo los factores sistémicos que crean un incumplimiento hacia la provisión de LST de alta intensidad podrían generar conflictos interpersonales y sitios de ruptura entre los valores éticos de los clínicos y las demandas del sistema, lo que caracterizamos como la ética del sistema. Tales tensiones podrían llegar al grado en que condujeron a la angustia moral, como lo ilustra una de nuestras encuestadas, una enfermera de la UCI, en la Cita 5. La experiencia de angustia moral de esta enfermera de la UCI no parece surgir de una «situación excepcional» en la que haya un «tomador de decisiones específico o un agente de autoridad» al que culpar, como Buchbinder et al. caracterizan las causas de la angustia moral. En cambio, su angustia moral podría entenderse mejor como derivada de «aspectos estructurales cotidianos inespecíficos de la atención médica» —esos factores que, según Buchbinder et al., causan estrés moral (Buchbinder et al. 2024, 12)— que generan sistemáticamente conflictos entre los valores éticos de los clínicos y la ética del sistema (Dzeng y Wachter 2020). Por lo tanto, una comprensión sistémica de las causas de la angustia moral complica la distinción principal que Buchbinder et al. establecen entre las fuentes de la angustia moral y el estrés moral.
LOS FACTORES SISTÉMICOS LIMITAN LA CAPACIDAD DE LOS CLÍNICOS PARA ACTUAR DE ACUERDO CON SUS VALORES ÉTICOS, MOLDEÁNDOLOS CON EL TIEMPO
Además, sostenemos que el incumplimiento sistémico de proporcionar LST de alta intensidad se manifiesta en restricciones y sanciones externas impuestas a los médicos que buscan cuestionar o actuar contra ese incumplimiento (Rosenwohl-Mack et al. 2021; Dzeng et al. 2016; Barnato 2017). De esta manera, los factores sistémicos pueden restringir la capacidad percibida y real de los clínicos para actuar de acuerdo con sus valores éticos, lo que lleva a una sensación de impotencia que contribuye a las experiencias de angustia moral. Con el tiempo, creemos que la experiencia de uno mismo como impotente para actuar con integridad puede transformarse en cambios en los valores éticos, las creencias y las acciones de los médicos individuales a medida que se internalizan los factores sistémicos. Nuestro punto de vista se basa en la teoría de la estructuración de Giddens para articular el mecanismo por el cual creemos que pueden ocurrir cambios en los clínicos y retroalimentar la ética del sistema (Giddens 1984). Proponemos que los factores sistémicos dan forma a las percepciones de los médicos sobre el mundo, influyendo en sus valores éticos, creencias y acciones. Esto, a su vez, puede llevar a los clínicos a actuar de manera que refuercen la ética del sistema, creando un bucle de retroalimentación que perpetúa esta ética (Giddens 1984; Dzeng et al. 2018). La Figura 1 presenta nuestro modelo conceptual para este proceso. De acuerdo con este modelo, los clínicos que se enfrentan a un conflicto entre sus valores éticos y la ética del sistema, junto con su impotencia percibida para actuar sobre este conflicto, se encuentran con dos opciones. En primer lugar, sus valores éticos pueden adaptarse para alinearse más estrechamente con la ética del sistema. Esto puede reducir el conflicto ético y la consiguiente angustia moral que experimentan los clínicos, pero a costa de cambiar las creencias y acciones de los clínicos de tal manera que lleguen a defender la ética del sistema, como se ejemplifica en la cita 6. Por otra parte, si los médicos no son capaces de adaptarse, las experiencias repetidas de angustia moral pueden convertirse en daño moral, lo que lleva a algunos a abandonar la profesión. Nuestra teoría es que este proceso crea un ciclo que se perpetúa a sí mismo, en el que los clínicos que permanecen en la práctica ya están alineados con la ética del sistema o se ven obligados a adaptarse a esta ética. Por lo tanto, nuestra comprensión sistémica de la angustia moral combina la idea de «impotencia», que Buchbinder et al. aplican a la angustia moral, con la idea de «socavar la integridad profesional», que aplican al estrés moral (Buchbinder et al. 2024, 8).
LAS INTERVENCIONES DEBEN ACTUAR SOBRE LA ETIOLOGÍA SISTÉMICA DE LA ANGUSTIA MORAL
La definición de la angustia moral no es simplemente una preocupación semántica; La forma en que se conceptualiza la angustia moral determina la forma en que se estudia y el desarrollo de intervenciones destinadas a mitigarla. Reconocer el papel de los factores sistémicos en la generación de angustia moral es esencial para permitir el diseño de intervenciones que puedan abordar sus causas subyacentes. Además, un enfoque sistémico destaca la importancia de garantizar que los sistemas éticos sean un factor crítico en el bienestar de los clínicos, con implicaciones para el agotamiento, la insatisfacción profesional y el abandono del puesto. Si bien las intervenciones a nivel individual para mitigar la angustia moral, como los programas de bienestar clínico y las sesiones informativas emocionales, son valiosas para aliviar los impactos emocionales de los conflictos éticos, es probable que solo ofrezcan un alivio temporal. Las soluciones duraderas a la angustia moral requieren actuar sobre los factores sistémicos que la engendran y perpetúan
Agotamiento Moral en Médicos: Causas y Consecuencias
Dr. Carlos Alberto Díaz. Profesor Titular Gestión estratégica Universidad ISALUD.
El agotamiento es una constelación de síntomas que incluyen malestar, frustración, cinismo, insomnio y disminución de la productividad. Más de la mitad de los médicos informan al menos uno de estos.
«la angustia moral ocurre cuando los individuos creen que no pueden actuar de acuerdo con sus valores éticos debido a restricciones externas, como las restricciones institucionales y jerárquicas». (Rosenwohl-Mack et al. 2021; Dzeng et al. 2016; Jameton 1984).
El agotamiento moral se produce por situaciones que afectan el desempeño profesional y personal de los médicos, de variado origen y causalidad, de base existen factores de riesgo, en la comunicación, la conformación de los equipos, el liderazgo, tener carencias, controversias con el paciente y su familia, escasez de la fuerza de trabajo, falta de apoyo de las organizaciones, una remuneración que siempre se considera no valorativa del trabajo y la responsabilidad que el mismo implica. Tenemos problemas sistémicos que hacen al stress o daño moral y otros que entran en la esfera personal produciendo angustia, y agotamiento que afecta su salud, que pueden culminar en el burnout. Es diferente en aspectos particulares en el ámbito privado y público, en la práctica en establecimientos o en consultorio, en atención primaria y especializada. Tener planes inconsistentes de cuidado. Cuestionamientos en la atención. Tener que hacer acciones que hacen a la futilidad médica. Escaso manejo en situación de muerte o fracaso en la reanimación. Pero también existen factores comunes causales y de riesgo que se expresan en la tabla 1
Tabla 1
| Elementos causales | Problemas de comunicación entre el equipo de trabajo, paciente y familia. Planes inconsistentes de cuidado. Cuestionamiento sobre la atención brindada por otros trabajadores en salud. Futilidad médica. Controversia entre el equipo de salud y la familia. Poco manejo de situaciones de muerte. Jerarquías de trabajo. Sobrecarga administrativa. La limitada autoridad para planificar horarios y la falta de apoyo de las organizaciones. Escasez de fuerza de trabajo. Unidades de cuidado crítico. Unidades de reanimación. Terapias intensivas pediátricas y neonatales. Centros de atención primaria sin apoyo diagnóstico. |
| Factores de riesgo | Insatisfacción laboral. Condiciones laborales adversas. Largas horas de trabajo. Falta de recursos tangibles e intangibles. Poca experiencia. Género femenino. La medicina defensiva y la judicialización de la medicina. La auditoría restrictiva de los prepagos y las obras sociales |
| Factores protectores. | Buena relación médico paciente. Regulación y protección emocional. Distanciamiento emocional. Libertad en la toma de decisiones. Buen contacto con los pacientes. Reconocimiento de carrera y mejora de las condiciones de trabajo. |
Hay tres esferas que se relacionan el agotamiento moral, la angustia moral y el daño moral, que influyen, coparticipan, y causan el burnout.

Agotamiento:
En la profesión médica el agotamiento se inscribe en la falta de perspectiva de carrera profesional, de crecimiento, de algo de bienestar económico, de carencia en el reconocimiento social. De que médicos sobran. De no poder ordenar prioridades. De afectar las horas de descanso, ocio y esparcimiento. La imperiosa necesidad de tener multiempleo. De compensar la falta de actualización salarial en el sector público, con mejora de aranceles en el ámbito privado, pero con inseguridad e inestabilidad, informalidad y retraso en los pagos. En el sector público es poco, pero seguro y constante, con algunos espacios de placer vinculados a la posibilidad de aprender y seguir formándose. Participar en actualizaciones, y ateneos. Pero a veces es tan bajo esto, que los profesionales prefieren el riesgo del privado. Existen instituciones privadas, con o sin fines de lucro que también tienen organización hospitalaria, con servicios y que finalmente involucran los dos aspectos: seguridad y lo económico. Cada vez los profesionales deben destinar más horas al trabajo y menos a sus familias. En el trabajo hacer más actividades administrativas que estar con sus pacientes. Se observa más agresividad de los pacientes y sus familias. Más exigencias no vinculadas con su accionar, sino con perspectivas erróneas sobre los resultados que puede tener un tratamiento o la aplicación de una tecnología. Los médicos deben soportar riesgos mayores sobre su praxis médica y sobre los resultados que los tratamientos producen en los pacientes. En suma, con información distorsionada que cuentan los pacientes o minimización de los riesgos de algunos profesionales en relación con el riesgo inherente de una práctica. Riesgo patrimonial y la necesidad de tener un seguro de cobertura con la praxis médica. La medicina defensiva es otro factor causal para provocar el agotamiento además de incrementar los costos en salud a través de la futilidad en la prescripción. La judicialización también compromete a los profesionales y el tener que indicar tratamientos que no están de acuerdo.
La postergación de sus honorarios como variables de ajuste de los financiadores y los responsables públicos, tambien los compromete, siendo finalmente una puja distributiva muy desigual.
Se deben considerar que el ámbito del ejercicio profesional de sus actividades afecta su moral, porque siempre faltan insumos, medicamentos y prestaciones. Dificultades en la provisión, tiempos prolongados en los procesos de compras, falta de nombramientos y concursos para impulsar sus carreras. No se cubren los cargos porque no se presentan candidatos. No se cubren los cargos de la residencia médica.
Lo prolongado que resulta el desarrollo de una carrera profesional en años, en tiempos de formación, en inmadurez práctica del ejercicio, que son esfuerzos de paciencia, de persistencia, de tesón, mientras sus amigos de la infancia ven en otras carreras una posibilidad más abierta con mayor capacidad de elección. El tiempo que lleva son siete años de la carrera de grado y cuatro de residencia, un total de once años. Por lo tanto, llega a la edad de treinta años de no depender de su familia.
La incertidumbre que genera la rapidez con la que está evolucionando el conocimiento médico que hace muy difícil estar actualizado, seguir el ritmo de este y poder seleccionar correctamente las fuentes que permiten acceder a información confiable y formativa, independiente y real, sin ninguna entidad formal intermedia que evalúe estas nuevas tecnologías.
La presión del complejo industrial médico porque aplique una tecnología y los colegas que son proclives al uso de estas nuevas tecnologías médicas.
La necesidad de tener que recurrir cada vez más a una medicina de práctica institucionalizada por su complejidad y la posibilidad de estar respaldado ante las complicaciones.
Por el aumento de los gastos en todos los aspectos inherentes al ejercicio de su profesión tiene que trabajar más horas para pagar las cuentas. El incremento de los costos de alquileres de consultorios. De los servicios públicos. Del costo de las suscripciones. Que no se compensan con los valores de la consulta.
No tener posibilidades de jubilarse porque los aportes a la caja médica no le aseguran un pago por subsistencia, y en el ámbito público tener un techo, y muchos rubros no remunerativos que no pasan al calculo de la remuneración pasiva. No tener asegurado nada y tener que asumir que en Argentina no te podes jubilar. Salvo que no tengas salud o ahorros que te permitan poder compensar la caída de ingresos que esta situación te acarrea. Con los riesgos que implica para los pacientes y la profesión trabajar más allá de los setenta años.
La mayoría de los aspectos como intento analizar no son cuestiones económicas sino fundamentalmente de condiciones de trabajo, o como se tiene que hacer para recobrar el estímulo por ser médico, vivir dignamente de su profesión, de contar con un reconocimiento jerárquico y social, de tener contención en los lugares donde es empleado, tener contención en los momentos difíciles personales, acompañarlo en los crecimientos, ver como puede mejorar su posición con una carrera consolidada por la estabilidad y el crecimiento en base a la meritocracia, sustentada por la dedicación, el compromiso con los pacientes, y los resultados, su trabajo por la calidad y la seguridad de los pacientes, por comunicarse mejor con ellos, por lograr que cumplan los tratamientos y por una medicina basada en el valor.
Destinarle horas a la docencia implica más sacrificio, más postergación por una vocación, que implica ser profesor universitario, un gusto raro y costoso, además para formar residentes que cada vez tienen menos voluntad y capacidad de sacrificio.
Se debe mejorar el ambiente laboral, las condiciones de trabajo, la remuneración, contener los aspectos personales, porque además de la profesión, la deontología y los deberes son personas, cada vez menos valorizadas por la sociedad donde la salud no es una prioridad, hay que darle vida a los años de nuestros médicos.
Con demasiada frecuencia los administradores toman decisiones sobre organización de los procesos, horarios y flujos de trabajo sin tener en cuenta la opinión de enfermería o médico, o sea los que ejecutan el proceso.
Conclusión:
El sufrimiento moral se enmarca y acontece en un sistema de salud inhumano. Es imperioso humanizar la educación profesional de pregrado, las residencias médicas y el ejercicio de la profesión, remunerarla en forma más justa, y tener en cuenta la contención de los profesionales, desarrollarlos en habilidades blandas y protegerlos en el ejercicio de su profesión, que basen su accionar en una medicina basada en el valor para los pacientes y sus familias, para la profesión médica, y el sistema de salud. Generar espacios de reflexión y reflexión respecto a las implicancias profesionales, emocionales, morales y existenciales de la practica médica como punto de valor para nuestro liderazgo como gerentes.
Angustia Moral en el Personal de Salud: Enfoques y Estrategias
Se inicia el mes de Enero de 2025, donde comienzo con una serie de recopilación de artículos de los últimos dos años sobre un tema no abordado por nosotros los gestores la angustia moral en el personal de salud. Este tópico fue abordado en una conversación con el Dr. Sergio Wisky con quien trabajo en diferentes aspectos de su gestión en Chubut a raíz de un viaje de capacitación que el realizó a Washington donde observó en el Hospital Universitario de esa ciudad, este aspecto la angustia moral. Me quedó como un pendiente que en este espacio tiempo lo quiero proponer para el intercambio, el análisis, estudio de incidencia, la importancia que tiene para nosotros los gestores porque entrecruza aspectos generales, e individuales, que impactan sobre el propósito, trabajar con plenitud y capacidad de autoorganización, eso se traduce en cansancio, desmotivación, desatención, falta de iniciativa, no querer involucrarse más allá de las fronteras, se pierde empatía y atención centrada en la persona. No esta referido a aspectos materiales sino espirituales y vocacionales.
Navegando el estrés moral y la angustia moral en la deliberación de casos morales: un esfuerzo conjunto
Malene Vera van Schaik y Suzanne Metselaar Amsterdam

Estamos totalmente de acuerdo con Buchbinder et al. (2024) en que se presta destacada atención a la angustia moral que surge de los encuentros clínicos individuales, así como a los profesionales de la salud individuales al abordar los desafíos morales en la práctica. De hecho, se debe prestar más atención a los factores sistémicos y estructurales que generan estrés y que van más allá del individuo, y cómo mitigarlos eficazmente para promover tanto el bienestar de los profesionales de la salud como la buena atención al paciente. Distinguir la angustia moral del concepto de «estrés moral», es decir, el estrés generado por los sistemas rutinarios y complejos de atención médica, podría ayudar con esto. Sin embargo, argumentamos que, en la práctica, los factores sistémicos a menudo se manifiestan a nivel de caso individual, lo que hace difícil separar la experiencia de estrés moral de la de angustia moral.
En consecuencia, sostenemos que los profesionales de la salud reciben un apoyo más eficaz cuando exploran cómo los factores estresantes organizacionales y sistémicos se cruzan con los desafíos morales que experimentan en casos individuales (Haan et al. 2018; Rushton 2016; Morley, Sankary y Horsburgh 2022). Además, sostenemos que esta exploración, liderada por un especialista en ética clínica, debe ser un esfuerzo conjunto e interprofesional dentro de la institución de salud, incluyendo no solo a los proveedores de atención a pie de cama, sino también a los responsables de diseñar e implementar políticas y procesos organizacionales.
Si bien Buchbinder et al. enfatizan que la angustia moral y el estrés moral pueden superponerse, proponen que distinguir conceptualmente entre (las causas de) el estrés moral y la angustia moral puede ayudarnos a encontrar vías estratégicas para reducir ambos. Sin embargo, su distinción pasa por alto la intersección de la angustia moral en casos individuales y los factores estresantes sistémicos, y cómo estas causas pueden reforzarse mutuamente. Por ejemplo: los profesionales de la salud que tienen poco personal y están sobrecargados de tareas, experimentan una falta de tiempo y atención para sus pacientes. En consecuencia, esto puede ser una causa de angustia moral en casos individuales de pacientes.
Además, un caso individual puede arrojar luz sobre los factores estresantes sistémicos. Por ejemplo, el personal de enfermería puede sentir que tiene que brindar cuidados inútiles a un paciente, lo que causa angustia moral, y sentir su perspectiva y experiencia no es tenido en cuenta por los médicos. La reflexión sobre esta experiencia puede dilucidar que las perspectivas de los enfermeros generalmente se pasan por alto en la toma de decisiones sobre el cuidado y el tratamiento del paciente en la sala, lo que puede estar relacionado con factores sistémicos, como las rutinas cotidianas, el trabajo y la jerarquía.
Buchbinder et al. mencionan la necesidad de explorar vías estratégicas para lidiar con el estrés moral en la práctica diaria, pero no dan ejemplos concretos de tales intervenciones. Refiriéndose a las intervenciones que reconocen la angustia moral, los autores sostienen que «muchos de los enfoques dominantes para reducir la angustia moral se centran desproporcionadamente en la educación y la reflexión individuales porque son relativamente más fáciles de abordar». Más bien, sostienen que las intervenciones deben ser capaces de abordar los sentimientos de angustia moral, así como apoyar a los profesionales en la lucha contra los sistemas y la creación de cambios estructurales como respuesta a los factores estresantes sistémicos que causan el estrés moral.
En los Países Bajos, se tiene una larga tradición de utilizar la Deliberación Moral de Casos (MCD) para proporcionar apoyo ético en la práctica clínica. Durante un MCD, los profesionales de la salud, preferiblemente de todos los niveles relevantes de la organización, participan en un diálogo metódicamente estructurado sobre un desafío moral concreto en cuestión (Metselaar y Molewijk 2023). El aprendizaje mutuo y la toma de perspectiva son clave, lo que significa que, a menudo, los profesionales aprenden unos de otros. Este aprendizaje mutuo a menudo no se trata solo de un caso específico de paciente, sino también de cómo la política y los procesos afectan a las personas en toda la organización de manera diferente. Por lo general, un MCD comienza con la discusión de una situación concreta que se experimenta como moralmente problemática, partiendo de las dudas y preguntas morales de (un miembro de) un equipo de atención. En este punto, aún no está claro si interactúan los factores estresantes sistémicos y los aspectos de la situación individual y cómo lo hacen. El siguiente caso ilustra esto:
Un Moral Case Deliberation se organiza en una residencia geriátrica a petición del personal de enfermería.
Luchan con cómo lidiar con una situación en la que un residente con lesión cerebral adquirida sigue saliendo a caminar, generalmente por las mañanas, donde a menudo se pierde o termina en situaciones peligrosas en el tráfico. El geriatra ha aconsejado al personal de enfermería que lo encierre en su habitación, especialmente en las horas punta de la mañana cuando no pueden supervisarlo. Las enfermeras, sin embargo, consideran moralmente problemático limitar la libertad del cliente encerrándolo contra su voluntad, aunque también se sienten responsables si algo le sucediera fuera. Al mismo tiempo que explora su dilema moral en este caso individual, la deliberación conjunta también saca a la luz los factores estresantes sistémicos, que son causados por la creciente escasez de personal en relación con una población residente con necesidades de cuidados cada vez más complejas; Las enfermeras luchan regularmente por no poder prestar suficiente atención a algunos residentes, también en este caso. Además, mencionan que el guardián de la puerta fue reemplazado recientemente por un sistema digital menos efectivo, ya que la política de la organización es adoptar la tecnología para ser más rentable. Esto se suma a su sentimiento de ansiedad y responsabilidad personal por la seguridad de su cliente.
Este ejemplo de nuestra práctica como especialistas en ética clínica muestra cómo puede ser difícil separar el estrés moral de la angustia moral, así como el individuo de lo sistémico; más bien, se entrelazan en la experiencia de un desafío moral que conduce a un llamado al apoyo ético. Sin embargo, al explorar conjuntamente el caso de manera gradual en un MCD, se pueden identificar los elementos que pertenecen a los factores estresantes sistémicos y las características específicas del caso individual. Posteriormente, se puede considerar qué se debe hacer para mitigar ambos.
El MCD está orientado a la acción: busca promover la «agencia moral» de los profesionales, es decir, su capacidad para tomar decisiones bien meditadas y autónomas y para elegir qué acciones tomar cuando se enfrentan a un desafío moral. Concretamente, muchas formas de MCD terminan con un paso metódico en el que se considera qué acciones tomar en base a los valores y/o argumentos que se concluyen conjuntamente deben ser líderes en la situación en cuestión (Metselaar y Molewijk 2023; Metselaar et al. 2022). Esta orientación hacia la toma de medidas puede referirse no sólo a la acción clínica directa, sino también a las iniciativas para cambiar o influir en las políticas y los procesos. Por lo tanto, facilita a los profesionales hacer retroceder a los sistemas y fomentar el cambio sistémico.
En el caso comentado anteriormente, el MCD terminó en una conclusión conjunta de que la libertad del cliente debe ser respetada, pero no a costa de su seguridad. Por lo tanto, le pidieron al cliente que se inscribiera en un programa de actividades sociales dirigido por voluntarios durante las mañanas, para mantenerlo comprometido. Además, un miembro del equipo directivo que participó en el MCD prometió reconsiderar el sistema de seguridad digital para puertas y abordar el problema en la próxima reunión de la junta.
Como sostienen Buchbinder et al., involucrar a los profesionales de la salud en la lucha contra los sistemas a través del apoyo a la ética clínica, «no solo [efectúa] el cambio estructural, sino que también [alivia] el estrés moral en el proceso». Cada vez hay más evidencias (van Schaik et al. 2024; Haan et al. 2018; de Snoo-Trimp et al. 2020) que el MCD fomenta las competencias morales y la resiliencia moral, es decir, la capacidad de mantener y restaurar la propia integridad en respuesta a la adversidad moral (Rushton 2016), que son necesarios para abordar eficazmente los factores estresantes sistémicos y para hacer frente bien a la angustia moral (van Schaik et al. 2024). Cuando los profesionales de la salud alinean sus valores morales con sus elecciones y acciones, pueden llegar a acciones bien consideradas que brinden una buena atención al paciente en situaciones difíciles, y abordar y cambiar los factores estresantes sistémicos que se manifiestan en estas situaciones. Sin embargo, lidiar bien con el (des)estrés moral no debe ser responsabilidad exclusiva de los profesionales de la salud individuales o de aquellos que trabajan «a pie de cama». Más bien, es una responsabilidad compartida de las instituciones sanitarias y los profesionales sanitarios de toda la organización, incluidos los responsables de las políticas y los procesos organizativos. Por lo tanto, las organizaciones deben crear un clima seguro y ético que permita que todos compartan abiertamente sus dudas morales, también sobre los factores sistémicos que podrían obstaculizar la buena atención al paciente o el bienestar de los profesionales de la salud (Rushton y Sharma, 2018). Idealmente, las organizaciones de atención médica documentan los temas y los resultados de los MCD de manera sistemática. Esta es una estrategia efectiva para hacer que la gerencia sea consciente de cuáles y cómo se manifiestan los factores estresantes sistémicos en la práctica diaria y, por lo tanto, para facilitar el cambio organizacional.
Para concluir, al distinguir la angustia moral del estrés moral, como proponen Buchbinder et al., podemos pasar por alto la forma en que se refuerzan mutuamente y, a menudo, se presentan como entrelazados en la experiencia de una situación moralmente problemática. Además, proponemos que las vías efectivas para apoyar a los profesionales de la salud son intervenciones que abordan tanto los factores estresantes sistémicos como los casos individuales de pacientes que causan angustia moral. Como ejemplo, discutimos la Deliberación Moral del Caso, una intervención de apoyo a la ética clínica que fomenta un proceso compartido de indagación moral a través del diálogo entre diferentes profesionales de la salud en la organización. Esto puede generar un entendimiento mutuo y llegar a acciones compartidas para abordar los desafíos tanto a nivel sistémico como a nivel de caso individual.
Crisis Sanitaria y la Economía: Un Análisis de la Salud en Argentina.
Dr. Carlos Alberto Díaz. Profesor Titular de Gestión Estratégica. Universidad ISALUD. Maestría de Economía y gestión de la salud.
Este es un documento editorial escrito en nueve bloques buscando las complejas relaciones entre el nuevo modelo económico, el orden político diferente y el sistema de salud en crisis, comenzando con el análisis del contexto económico, social, y político, el ajuste la recesión y la salida de la misma. La orientación que llevan los cambios en la salud y los impactos que están produciéndose. La perdida de solidaridad y de inclusión. Las transformaciones que están marcando el camino, de la libertad económica. Estamos en la puerta de una gran prueba, la epidemia de dengue que se puede avecinar, y se dejó librado a las jurisdicciones, las provincias, la estrategia de vacunación, esto podrá provocar distintas formas de circulación del virus.
Los bloques son: 1) La gestión política, económica y social. Cambios en el Ministerio de Salud. 2) Logros de la gestión sanitaria. 3) Más preguntas que respuestas 4) Sensación de un final de época. 5) Minar el poder político de los sindicatos 6) El precio de los medicamentos 7) Pauperización de los trabajadores de salud 8) causas de aumento del costo en salud y 9) conclusiones
- La gestión política, económica y cambios en el Ministerio de salud. Introducción: Un año de gestión política-económica con éxitos macroeconómicos. vinculados al combate a la inflación, a la abolición del déficit en las cuentas públicas, a la cesación de la emisión monetaria sin respaldo, logrando superávit fiscal primario sin mayor presión fiscal, pero también exigiendo un sacrificio a las provincias con disminución del 70% de las transferencias, esfuerzo de los ciudadanos, en reducción de los haberes jubilatorios y del salario real, con perdida de capacidad adquisitiva, esto provocó una recesión económica que parece interrumpirse en el último trimestre. Reducción de la producción industrial que no repunta, ni el índice de la construcción. Aumento de las exportaciones de commodities y liquidación más ordenada de las mismas que estabilizó el flujo de divisas. Una lucha contra la inflación aún no consolidada, por la corrección de los subsidios, de los precios relativos y aumento de costos en dólares que es preocupante por la competitividad. Utilizando el valor del dólar oficial como un anclaje para la inflación lo que hizo perder la ventaja de la devaluación inicial y retrasarse un poco. Se terminó con los gerentes de la pobreza, con los piquetes, y con los paros salvajes. Se está realizando una construcción política nacional con identidad pura sin alianzas de partidos, sumando buenos dirigentes y gestores. Pero en un muy cerrado círculo de confianza. Gestionando sin presupuesto porque no hubo acuerdos, pero antes de ceder con algunos principios económicos se consideró preferible prorrogar el del 2023. Enfrentamiento con las Universidades públicas, sus docentes y estudiantes. No pudiendo distinguir entre unas Universidades y otras. Las otras con menor trayectoria y creadas para un fin partidario, y tener un lugar para nombrar personas. Se efectuó una reducción de la planta permanente del estado con más declamación y sin discernir, se tomó exámenes de idoneidad, que aprobaron casi todos así que no hay excusas. No se está estableciendo como sacar a la gente de la pobreza aunque se está reduciendo. Tampoco, como darles educación a los jóvenes que han dejado de concurrir a las escuelas. Que hacer con la delincuencia infantil. La falta de alojamientos carcelarios. El nombramiento de los jueces con acuerdo parlamentario. El incentivo para el incremento de la producción agropecuaria, los mercados ganaderos, con la minería, con la manufactura del litio, en cobre, en oro, en gas licuado y petróleo, que producir en la marca país, como aumentar la productividad y las inversiones. ¿Sera solo con desregular?, puede ser, pero creo, que debe haber alguna política vinculada con el desarrollo. Escuchar más a los gobernadores que han realizado el ajuste y no aumentaron los impuestos. Impulsar la obra pública con capitales privados. Relanzar el ferrocarril como medio ecológico y eficiente de transporte como en EE.UU y Europa. La apertura de la economía exige tiempo de adecuación de las empresas, menos impuestos y una legislación laboral que elimine la industria de los juicios, si se liberan las importaciones antes del alistamiento de las empresas estaremos importando bienes más económicos con dumping y generando un mayor desempleo, lo que llevará al fracaso de este proyecto de país. No sirve de nada bajar los impuestos nacionales si aumentan los provinciales.
«El gasto público fue de $83.2 billones (81,870 millones de dólares) hasta noviembre, lo que representa casi un tercio menos que los $116.9 billones (115,000 millones de dólares) de la misma administración en ese período. La contracción es en términos reales, es decir descontada la inflación acumulada. Los fondos destinados a la obra pública representan la caída más drástica, con un 78% de disminución en relación a 2023. Fueron $8 billones entre enero y noviembre de 2023, contra $1.7 billón en el mismo período de este año». «Las transferencias a las provincias bajaron un 70% interanual y son la segunda categoría más afectada por la motosierra. El fondo que otorgaba subsidios a colectivos en la ciudad de Buenos Aires y las provincias experimentó una caída del 50%. Los fondos para programas sociales son un 40% menores que hace un año.» El economista Diciembre 2024
«Las jubilaciones y pensiones conforman el reglón de mayor gasto estatal. Allí el recorte fue del 17 por ciento. En 2023, se destinaron 43.5 billones contra $36 billones de este 2024, siempre medido en términos «reales» (descontada la inflación)». El economista Diciembre 2024
La salud, y su sistema no son una prioridad. Pero el Ministerio de salud y su rango, se mantuvieron, eso es positivo y alentador. En septiembre de este primer año se produjo el relevamiento del ministro de salud de esta gestión Mario Russo, súbitamente, fue reemplazado por el Dr. Mario Lugones, Una médico cardio-angiólogo y sanitarista de trayectoria, capaz, gran gestor y capacidad de liderazgo, conocedor acabado del sistema de salud y de la prestación del mismo. Condiciones necesarias. Un cambio para mejor. Aunque no suficiente. Este cambio produjo una estela de renuncias en la estructura y reacomodamientos en el organigrama del Ministerio. Ciertos sectores del mismo están paralizados, inmovilizados, sin innovación y con austeridad como característica, aunque las reducciones en salud pública tienen evidencia muy fuerte que empeora los resultados que se publicarán en los próximos años. Se efectuó una depuración en algunas prepagas que no tenían afiliados o no daban servicios y se intervinieron obras sociales que no superaron las auditorias. No se avanzó con la mejora en la cobertura de la discapacidad, ni tampoco en solucionar los excesos en el otorgamiento de beneficios y las características de los mismos, que cada año incrementa el gasto proporcional. Es una gestión que recién comienza. También se dijo que la cartera se quería desprender de los hospitales nacionales, siendo algunos de ellos creados por leyes, y su financiamiento incluido en el presupuesto, que reciben demanda de otras jurisdicciones por sus productos hospitalarios. Los hospitales de alta complejidad, tienen áreas de influencia marcada por el producto diferencial que ofrecen sus equipos asistenciales. Que son una ventaja competitiva que se debe proteger. Porque es la tecnología del conocimiento – experiencia – sabiduría – equipos difícil de conseguir y que se construyó con inversión de años, becas, residencias, formación y rotaciones. También que hacer con las residencias médicas, con la formación de especialistas. Se debe solucionar un problema álgido, crucial, que es la falta de anestesiólogos y la distribución de especialistas. Algunos programas exitosos deben continuar, porque las políticas de estado exitosas se deben seguir. Tampoco se abordó un problema de subsidio cruzado entre los trabajadores formales y los monotributistas, cuyo aporte cubre solo un tercio del costo del PMO, y además la recaudación media del sistema esta por debajo del costo. Con lo cual ocurre una solidaridad forzada e inequitativa, que se debería corregir. La salud no se puede financiar por once dólares mensuales del monotributo, tampoco con cuarenta de los formales.
2. Los logros sanitarios. Receta electrónica, la nueva forma de distribución del subsidio de mitigación de asimetrías (por cápita) y la libre elección de las obras sociales: Se consolidó la receta electrónica, la prescripción por nombre genérico, la libre elección de cobertura de agentes del seguro de salud. Los medicamentos y los insumos, los costos en salud aumentaron más que la inflación.
Se realizó una reunión en una mesa de trabajo con obras sociales nacionales y la participación de quien lideró el proceso en el Uruguay, para mostrar una experiencia de Benchmarking.
Problemas en el financiamiento de los hospitales en los primeros seis meses de este año. Dificultades de las provincias para sostener sus sistemas de salud, adquirir medicamentos, contratar recurso humano, incremento de la demanda, déficit de obras sociales nacionales y provinciales, dificultades en la cuenta de resultados en los establecimientos privados. Hospitales congestionados, privados con números en rojo.
Las provincias en general tuvieron que ajustar sus estructuras, sus salarios, las compras, y disminuir hasta hacer desaparecer el déficit fiscal con excepción de las gestiones de la Provincia de Buenos Aires y La Rioja. Por el lado de incrementar la presión fiscal e impuestos provinciales.
La distribución del subsidio de mitigación de asimetrías se realiza por número de afiliados, para incentivar la concentración y premiar a las obras sociales que tienen más afiliados.
3. Más preguntas que respuestas:
¿Hay posibilidades de libertad económica, en salud?, evidentemente aún no y si la hubiera no sería una buena noticia para los postergados. La libertad económica aplicada a la salud, con los riesgos que esta implica es posible?. Individualmente no. aisladamente tampoco. Recurriré al análisis de sistemas comparados y aspectos de la curva en U invertida de Kuznets.
En 2022, el 8,9% (27 millones) de los estadounidenses carecía de seguro médico, la mitad de los estadounidenses afirmó tener dificultades para afrontar los costes médicos, una cuarta parte de los adultos afirmó que el coste les impedía obtener la atención necesaria y el 40% tenía deudas médicas (10, 11). Los precios de los medicamentos recetados son entre 2 y 2,5 veces más altos en Estados Unidos en comparación con países similares (12, 13). Un informe de 2021 concluyó que el acceso a la atención sanitaria necesaria en Estados Unidos dependía de los ingresos: el 50% de los adultos estadounidenses de bajos ingresos afirmaron que el coste les impedía obtener la atención que necesitaban. Países como el Reino Unido, España, Francia, Alemania, Bélgica, Suiza, Noruega, Italia, Israel, Suecia, Canadá, Nueva Zelandia, Australia entre otros, no tienen un modelo liberal en salud como EE.UU, gastan menos y con mejores resultados. Entonces que modelo adoptaremos, como lo haremos.
Otro aspecto diferente del análisis es cuanto de la libertad económica influye en el desarrollo de esos países. Pero no que los sistemas de salud dejen de tener solidaridad y sean equitativos. Por ello, con algunas acciones de desburocratización y mayor competencia, estrategia de economía de escala y disminución de los costos de transacción, se puede impulsar un sistema más dinámico, eficiente y que cubra a más población en forma efectiva.
Debo expresar que es necesario tener en cuenta la relación causal entre las desigualdades en salud relacionadas con el ingreso. Al considerar las desigualdades sanitarias, se podría centrar la atención en las «desigualdades puras» en materia de salud, que son en gran medida el resultado de determinantes socioeconómicos más amplios que a menudo quedan fuera del ámbito de acción de las políticas sanitarias (Schultz, 2003 ), o, alternativamente, se podría centrar la atención en las desigualdades relacionadas con los ingresos en materia de salud, que pueden verse influidas por los mecanismos de redistribución adoptados por los gobiernos. En las úlltimas décadas, la mayoría de los países avanzaron en el Producto Bruto Interno per cápita nominal, pero no en todos los indicadores de salud. La mortalidad infantil y la desnutrición parecen tener una tendencia descendente bien definida a medida que los países y los individuos mejoran sus ingresos. Sin embargo, otros, como las enfermedades cardiovasculares y varias enfermedades no transmisibles, no siguen patrones claros de cambio con el desarrollo económico. Los factores socioeconómicos, como los recursos económicos (por ejemplo, el ingreso), la desigualdad, las relaciones sociales, la educación y la ocupación, se utilizan comúnmente para explicar los resultados y las inversiones en salud.
Estos fundamentos quieren afirmar que solamente con el crecimiento de la riqueza puede tardar más la convergencia en la salud, y que debamos recurrir a elementos redistributivos fundamentales, por los próximos años, sino solo se beneficiará a unos pocos y eso no contribuirá al desarrollo.
¿No se debiera definir que se puede cubrir con los recursos que se tienen cual sería el Programa médico obligatorio?. El programa médico obligatorio es un piso para el máximo tribunal de la Nación, por tanto el sistema de salud, las obras sociales nacionales deben dar todo y más. el texto original decía: «Es una canasta básica de prestaciones obligatorias para todas las prepagas y obras sociales. Son las obligaciones que toda obra social o prepaga tiene que cubrir como mínimo en cualquiera de sus planes.» Pero la corte la consideró en varios fallos como mínimo y obligó a dos coberturas a cubrir endoprotesis valvulares con una expresión que deja abierta que cualquier innovación que mejore los resultados debe ser cubierta. «Cabe dejar sin efecto la sentencia que desestimó la acción de amparo deducida a fin de obtener la cobertura para una cirugía con endoprótesis en base a que no se hallaba incluida en el PMO, pues el Tribunal ha juzgado (Fallos: 325:677) que el derecho a obtener conveniente y oportuna asistencia sanitaria, se vería frustrado si se aceptara que la falta de exclusión de un tratamiento no importa su lógica inclusión en la cobertura, siendo inadmisible la referencia histórica al estado del conocimiento médico al tiempo de fijarse los términos de dicha cobertura, toda vez que se traduciría en la privación de los adelantos terapéuticos que el progreso científico incorpora al campo de las prestaciones médico asistenciales. Es imperiosa su revisión, no empezar desde cero si con los trabajos ya realizados.
¿Las provincias deben financiar establecimientos hospitalarios de alta complejidad hoy bajo el financiamiento de la nación?, la nación tiene bajo su órbita a nueve hospitales, que realizan prestaciones que no tienen equivalencia, fijan políticas nacionales de salud y que deben confluir necesariamente a una concentración de casos para mejorar resultados. Que deben hacer con los pacientes que vienen de otras provincias u otras jurisdicciones. Algunos hospitales, como oncológicos de alta complejidad y de niños también tienen que seguir tratando a los casos que así lo requieran por su complejidad. «La decisión en el Gobierno está tomada y su ejecución será “un proceso” progresivo a partir del año que viene. Según pudo conocer este medio, el único de los hospitales nacionales que retendrá el Ministerio de Salud será el Garrahan “en principio” y los restantes –ubicados en la ciudad, la provincia de Buenos Aires y Santa Cruz– seguirán perteneciendo a la jurisdicción nacional, pero con una administración privada, de acuerdo con opciones que analizan en esa cartera y conversaciones con grupos que manifestaron interés». La Nación 20 de noviembre de 2024.
¿Que se debe hacer con la formación profesional, el recurso humano, las residencias, el vínculo con las universidades que forman médicos, el financiamiento del hospital universitario?. Es necesario fomentar algunas especialidades que se necesitan para cubrir cargos indispensables y mejorar condiciones de trabajo. Son ellos la terapia intensiva, la neonatología, la cirugía infantil, la emergentología, entre otros, pero fundamental y centralmente la anestesiología, ya que está generando situaciones difíciles de sobrellevar y que está limitando prestaciones públicas y en algunos establecimientos privados, que condiciona listas de espera. Es la única especialidad que es regulada por los propios prestadores, por lo tanto su interés radica en generar un equilibrio que no facilite la negociación de precios, ni la cobertura de algunos cargos. Ninguna gestión publica se animó o si lo hizo pudo avanzar en aumentar la cantidad de anestesiólogos que se formen. Cuando se quiera corregir estos problemas de recursos humanos, recordar que formar un especialista lleva cuatro años. Las otras especialidades tienen un mercado laboral de paga insuficiente en relación a las condiciones de trabajo, entonces la solución pasa por otro lado.
¿Que se debe hacer con la cobertura de los medicamentos en la obra social de jubilados y pensionados?. Como podrán sostener sus tratamientos con la jubilación de 200 dólares. Es necesario revisar la apropiabilidad y la pertinencia de todas las indicaciones. Limitar la cobertura a lo indispensable. No seguir fomentando la medicalización de la vida.
¿La vacunación será responsabilidad de las provincias? Con la posibilidad de externalidades negativas que significan bajos niveles de cobertura en las poblaciones de niños. No se puede dejar en manos de las provincias las campañas de vacunación que deben ser nacionales, sino estaremos siempre corriendo desde atrás brotes, de enfermedades que tendrían que estar cubierta por la inmunidad colectiva, conocido como inmunidad de rebaño. Al 26 de abril de 2024, en los EE. UU.,
la incidencia de sarampión de este año supera la del año pasado , con 128 casos notificados por 20 estados y el 55 % de los pacientes que requieren hospitalización. El drástico aumento refleja varios brotes resultantes de una cobertura de vacunación inconsistente. La desinformación probablemente reduzca las tasas de cobertura de vacunación, lo que deja a las personas susceptibles a la importación del virus de países con brotes. Debemos a nuestros pacientes información precisa sobre los verdaderos riesgos asociados con la infección por sarampión, y el más importante, la alta mortalidad (se estima que es del 0,1 % en las naciones industriales y de hasta el 15 % en las regiones con pocos recursos). New Eng J Med. 2024.
¿Porqué tanta enjundia por los medicamentos de venta libre en todo el país? Esto empeora el acceso, porque no bajarán de precio y además los pacientes tendrán que abonar el 100%. No es un avance significativo a la modernización y eficiencia del sistema de salud. Sino aumento de la inseguridad farmacológica.
¿Que ocurrirá con la agencia de evaluación de tecnología? Institución indispensable en el país, para determinar la costo efectividad de muchos tratamientos. Estamos utilizando el conocimiento adecuado para su evaluación, el paradigma de la efectividad y la eficiencia, hacer las cosas mejor, hacer bien las cosas correctas correctamente, eso es lo que tenemos que hacer, y luego pagar por hacer las cosas correctas el valor que corresponda. La tecnologías es la aplicación sistemática de los conocimientos científicos para resolver problemas prácticos. La evaluación sirve para establecer evidencias para llegar a las políticas, establecer prioridades y mejorar la salud de los individuos, producir información para tomar decisiones, tiene un aspecto normativo y un aspecto pragmático para que los decisores estén incluidos, por lo tanto, los que prescriben, financian, los pacientes y la justicia. No es su función prioritaria disminuir las conflictivas judiciales de la cobertura. Si las guías clínicas y las obsolescencias tecnológicas. Es una prioridad importante. No es tampoco para bajar los costos en salud. Requerirá todo un proceso de maduración de varios años que debe empezar, se lleva una demora desde el 2016 cuando tomó estado parlamentario el primer proyecto con dictamen. No es para resolver todos los problemas del sistema de salud, es solo un aspecto más de la reforma. Las decisiones deben crecer hasta hacerse vinculantes y colaborar en fijar precios. Evaluar beneficios relativos e innovadores. También se debe acreditar prestadores para hacerle llegar tecnología a la gente en forma segura. Revisar que priorizar en evaluación primero y también las que ya se están utilizando porque hay que evaluar obsolescencia. Todo para todos no es posible. Tampoco es necesario dijo la OMS. Definir plazos para evaluación. Monitorear el cumplimiento de las decisiones tomadas. Acceso equitativo.
Es posible señalar que se abolieron las disposiciones que reglamentaban los traspasos de las obras sociales a las prepagas o «agentes del seguro privados de salud», hoy no hace falta pasar por una obra social «telonera» que tenga convenio con estas entidades para tener su cobertura. Pero ese mercado liberado tiene agentes que cubren riesgo de la población con salario formal o monotributista de ingresos bajos o medios bajos. Esa franja de trabajadores pobres no son en este momento elegibles por los seguros privados. Salvo los salarios elevados. Por lo tanto, es un incentivo franco al descreme y al debilitamiento de la solidaridad intrasistema. Esto hizo que no se produjeran efectivamente esos cambios porque la gente tiene desconfianza. Pero si, que las obras sociales, deban competir con lo que ofrecen esos prepagos.
Estas modificaciones además son parciales, en tanto, no alcanzan a las obras sociales creadas en derechos especiales, y a las obras sociales provinciales.
4. La sensación de un final de época. El final de época: La política argentina nos ha demostrado, que nunca los cambios son definitivos, tenemos un empecinamiento por el pasado, por un tiempo que no fue mejor, pero lo sentimos con una nostalgia de olvido por lo malo. Un claro desdén por la corrupción instalada, la inseguridad, la inestabilidad económica, el empleo de mala calidad, por gastar más de lo que tenemos y la irresponsabilidad fiscal. Este cambio en el Ministerio, aceleró algunas medidas que se estaban gestando en la desregulación de las obras sociales y las prepagas, de las cuales cuesta machear con las piezas del puzle, como es lógico, ya que todas las reformas del sistema de salud Argentino, no tuvieron nunca institucionalidad, ni ley, solo decretos y disposiciones, dictámenes y fallos, mucha, demasiada inseguridad jurídica, constituyendo finalmente un farrago de normas que eruditamente tratamos de interpretar, una galimatías, no encuentro la forma de expresarlo, sin dejar el sesgo interpretativo, pero todo parece como un final de época, para dejar atrás una salud en la cual el Estado Nacional tenga que ver con la salud, sino solamente los estados provinciales y la concentración de salud paga de bolsillo en entidades privadas para tres segmentos cápitas altas, medias y bajas. Nada al final de esta gestión quedará como estaba. Espero que se pueda hacer algo por mejorar el sector público, dotarlo de presupuesto y gestión profesional, que las obras sociales mejoren la gobernanza, que puedan tener un número de afiliados que les permita diluir el riesgo prestacional y en la cobertura.
Finalmente, En quienes tenemos la obligación de gestionar establecimientos soportar un aumento inusitado de los costos, que no podemos financiar, ya no nos queda que reducir, sin llevarnos por delante la calidad, importantes retrasos en las remuneraciones de los colaboradores, dificultad para poder sostener la producción y los equipos médicos, la productividad, los resultados, con ello la moral y el entusiasmo del personal en contacto, y disminuir los tiempos de espera de los pacientes. Sostener el programa de trasplantes, con cada vez más exigencias, siguiendo el son de los que quieren concentrar procedimientos. En el cuadro siguiente es posible observar como en las distintas regiones incidió el aumento del gasto en salud, llevando la delantera los productos medicinales los insumos y los productos farmacéuticos.
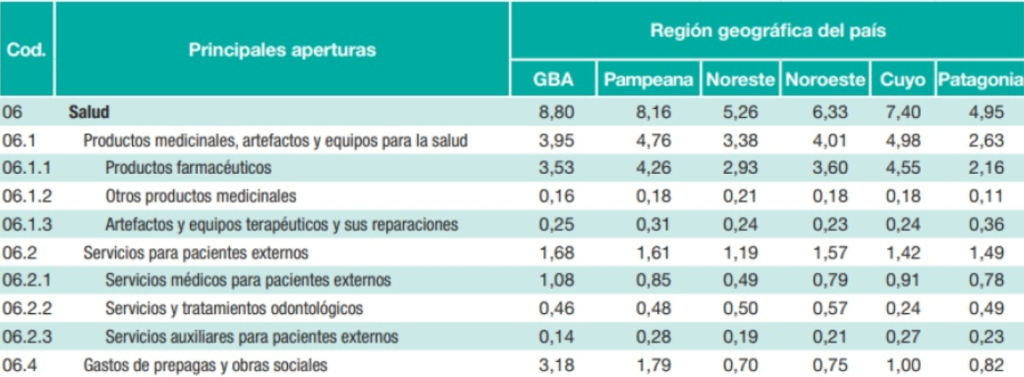
5. ¿Minar el poder político de los sindicatos?: Hace muchos años, décadas que se quiere erosionar el poder de los sindicatos. Como actor social, de una representación para moderar el poder de las empresas sobre los trabajadores, defender sus derechos y pactar las remuneraciones, pero en su crecimiento tienen áreas de intervención subsidiada de ayudas escolares, cobertura de salud y turismo, que en otro modelo de país constituyeron escalones del ascenso social. El cuestionamiento sobre el manejo de la salud con la afiliación compulsiva y falta de competencia fue una de los aspectos que se quiso combatir. Pero las reformas siempre tensan las relaciones entre el poder político democrático y los sindicatos. Inclusive se dio una paradoja, que el avance lo protagonizó parte de la oposición dialoguista, pero que no se dio quorum. Entonces que movimiento es afectar el financiamiento de las obras sociales, parece que es un gesto que quedó a medio camino. La afectación de los fondos se agrava por la inflación en salud.
La inflación en salud se produce por: los cambios epidemiológicos, envejecimiento de la población, mayor cantidad de procedimientos costosos, gastos administrativos, fraude, la pulsión innovativa de los nuevos tratamientos, la ensoñación tecnológica, la demanda inducida, la ineficiencia técnica y asignativa continúan afectando la sostenibilidad y sustentabilidad de los fondos, como también la solvencia de las obras sociales. Si no se financia esto, las obras sociales entran en déficit, las más pequeñas podrán desaparecer. No ocurrirá en lo inmediato, pero se está preparando la tierra para una sepultura, cuando se logre la reforma laboral que es el objetivo teleológico.
¿El objetivo político es debilitar el poder del sindicalismo que en sus estructuras maneja las obras sociales, dentro del marco legal de dos leyes de obras sociales?.
La recaudación del impuesto al salario no alcanza: Esto pone en duda que se pueda seguir financiando la salud por el 9% de los salarios. Tendrían que explorarse medios alternativos. Especialmente si quiere que los jubilados queden en la obra social de origen y que aumenten la cantidad de monotributistas.
Los ajustes necesarios e impuestos, la pérdida en el salario real de los trabajadores, la recaudación de la seguridad social hacia la baja, el aumento desmedido de los medicamentos, insumos y las prepagas, afectó la intención de la medida, que más personas se pasen a las prepagas.
El estado además observó un comportamiento oportunista de colusión con los aumentos al liberal la fijación de precios. Este mes de Enero, las prepagas aumentarán en el orden del 3,5 % o sea por encima de la inflación y lo que el gobierno quiere con los aumentos de salarios para que no se traslade a precios.
6. Pauperización de los trabajadores de salud. Mientras todos ajustan, los trabajadores de salud cobran salarios paupérrimos, los médicos salen expulsados de los sistemas, hoy no quieren pertenecer, porque el formarse y estar en la salud pública, los esta llevando a la mendicidad. Mientras existen algunos, grupos o sectores dentro de este mercado que no son abordables por ninguna institución. esto como salida esta generando un aumento del cobro de copagos y coseguros, y de profesionales que salen de las cartillas de los sistemas.
7. Los precios de los medicamentos: Los medicamentos cuestan más que en muchos países, con la excepción de EE.UU. Pero al ser Bienes inelásticos indispensables para pacientes que tienen enfermedades crónicas, es necesario contrastarlo contra el poder adquisitivo y las formas de financiamiento, es importante no interrumpir tratamientos porque en forma de ejemplo quiero recordar que las enfermedades cardiovasculares son responsables de más del 28 % de las muertes, y constituyen la mitad de la carga sanitaria de las enfermedades no transmisibles.
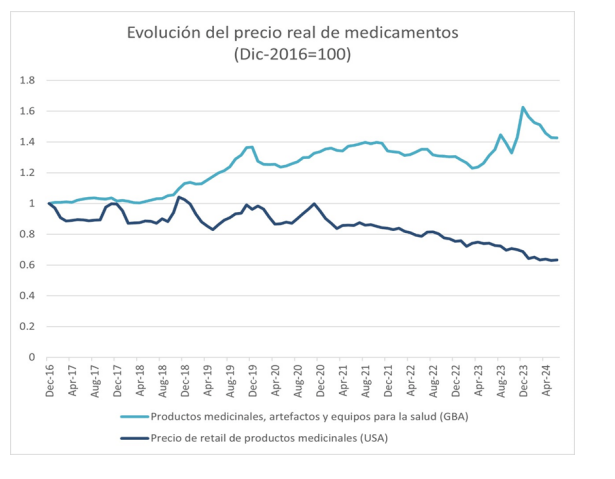
Muchos son Medicamentos que ya no tienen protección por patentes son más costosos que en Europa. Con total impunidad y nadie hace nada por ello. Allí no se aplica la libertad económica. La argentina tiene un defecto, que los genéricos se hicieron marca y por lo tanto tienen comportamientos comerciales como los originales.
¿Porque?. Los nuevos medicamentos para determinadas enfermedades están a un valor infinanciable, inaccesible. Para todos. Solventar gasto de quebranto desde 500 mil a 2 millones de dólares es imposible con una cápita media de 41 dólares, dentro de ellos, unos 2 millones de aportantes del régimen impositivo simplificado de 11 dólares. No es posible de ninguna forma.
Los que no tienen voz, están sufriendo las consecuencias. Muchos argentinos sin voz, están pagando el costo de oportunidad y la pérdida de la misma. Con años de vida y de calidad de vida perdidos. Los que trabajan en el sistema de salud están aportando sin que les pidan permiso. Se requieren introducción de precios de referencias, prescripción de genéricos y esenciales de bajo precio, prescripción por 90 días, entrega gratuita, más descuentos, más competencia, otros actores, con la misma firmeza que no se negocian el equilibrio fiscal y la emisión. Una política activa sobre los medicamentos o procedimientos de muy alto costo diferenciándolos en lo que se usan por única vez, los que corresponden a un tiempo prolongado (inmunológicas, oncológicas, HIV y genéticas), y los que están destinados a tratar enfermedades raras o poco frecuentes.
8. Causas del aumento del costo en salud: La salud es inflacionaria con respecto al crecimiento económico de los países, por una serie de causas, que se deben ponderar y estudiar adecuadamente, porque son muchos los factores que son incidentales y se relacionan mutuamente tienen una diferente ponderación de acuerdo a los países, en las diferentes segmentaciones de cobertura. La enumeración de las causas son el aumento de la edad media de la población, la transición epidemiológica de las enfermedades crónicas, el incremento del costo de los medicamentos y los insumos, el costo de los servicios de salud, la nuevas tecnologías que sustituyen o mejoran a las anteriores pero a una costo efectividad no estudiada, ni validada, también incrementa el costo por cuestiones organizativas, administración, cobertura y fraude, por la variabilidad en la prestación médica, por peores resultados a los que debiéramos tener. El 5% superior de usuarios de atención sanitaria en función del gasto total representa aproximadamente el 50% de todos los gastos de atención sanitaria.


Grafico extraído del libro del costo del PMO. Torres R y col. 2024.
9. Conclusiones:
Estamos recorriendo una ruta de reformas que no sabemos adonde nos lleva, queremos ir a un lugar por una estrategia distinta la libertad económica llevada al ámbito de la salud, pero que los principios de la libertad no pueden ser aplicados dogmáticamente porque hay una población entre el 42 y 52% por debajo de la línea de la pobreza, y se incremento el índice de desigualdad de Gini, por lo tanto los determinantes sociales de esa población se ven muy afectados. Por lo tanto, se debe mejorar el acceso a los sistema de salud, incrementar su efectividad, la calidad, la seguridad, la eficiencia, renovar la capacidad instalada, fortalecer lo más importante: al factor humano dedicado a la atención y los servicios de apoyo.
Tenemos la obligación, todos y en cada uno de nuestros niveles de reducir los costos de la no calidad, ineficiencia, variabilidad, fraude, los costos administrativos y apostar fuertemente a una medicina basada en el valor y en la efectividad clínica, en trasladar con pensamiento independiente la evidencia a la práctica asistencial, mejorar los niveles de atención primaria, el acceso a la atención, la prevención, la información, la digitalización del ecosistema sanitario, evitar que se cristalice la desigualdad vía fragmentación de capacidad de pago, y conservar un esquema de financiamiento solidario que permita acceder a prestaciones adecuadas a la población postergada, que ha quedado sin trabajo, sin educación y sin expectativas en los últimos 25 años.
Por ello necesitamos, que el área de la salud sea libertaria, pero también justa, como lo ha hecho con los planes sociales, eliminar intermediación de la pobreza, pero fortalecer el acceso a la salud, no recortar masivamente el financiamiento de los gastos variables en la salud pública, en seguir sosteniendo hospitales nacionales que capitalizan la atención de los casos más graves, sostener a las obras sociales de cápitas medias bajas, hasta que se recupere el salario, en consolidar niveles de ingresos que permitan financiar realmente un programa médico renovado y adecuado a las exigencias y a las posibilidades reales de financiamiento. Desarrollar un sistema de competencia en el mercado de insumos y medicamentos. Una agencia de evaluación de tecnologías médicas, que sean el respaldo para su cobertura. Una nueva canasta de prestaciones. No se puede dar todo a todos. Debemos procurar darle todo a quienes lo necesitan con evidencia científica y apropiabilidad.
Protecciones jurídicas diferenciales para medicamentos biológicos y de moléculas pequeñas en EE. UU.
Nota del autor del blog: Este artículo analiza la protección que reciben en forma diferencial los medicamentos biológicos y los de moléculas pequeñas y el mercado de los fármacos, que cada vez, cada año incrementa su participación relativa en el gasto en salud, convirtiendo peligrosamente a la misma, y a su financiamiento en un bien de lujo.
Dr. Olivier J. Wouters1; Matthew Vogel, MBA2; William B. Feldman,
JAMA. 2024;332(24):2101-2108.
Importancia Los productos biológicos aprobados por la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) reciben 12 años de protección garantizada contra la competencia de los biosimilares, en comparación con los 5 años de protección contra la competencia de los genéricos para los nuevos medicamentos de moléculas pequeñas. Según la Ley de Reducción de la Inflación de 2022, los productos biológicos están exentos de la selección para la negociación de precios de Medicare durante 11 años, en comparación con los 7 años para los medicamentos de moléculas pequeñas. El Congreso codificó estas diferentes protecciones legales sobre la premisa de que los productos biológicos requieren más tiempo y recursos para desarrollarse y tienen una protección de patentes más débil, lo que requiere protecciones adicionales para que los fabricantes recuperen sus costos de desarrollo y generen retornos adecuados sobre la inversión.
Objetivo Revisar la evidencia empírica de la experiencia estadounidense con productos biológicos para analizar los supuestos que subyacen a períodos más largos de exclusividad en el mercado y protección frente a la negociación de precios en comparación con los medicamentos de moléculas pequeñas.
Revisión de evidencia Se analizaron datos recientes sobre tiempos de desarrollo, tasas de éxito de ensayos clínicos, costos de investigación y desarrollo, protección de patentes, períodos de exclusividad en el mercado, ingresos y costos de tratamiento de productos biológicos frente a medicamentos de moléculas pequeñas.
Resultados La FDA aprobó 599 nuevos agentes terapéuticos entre 2009 y 2023, de los cuales 159 (27 %) eran productos biológicos y 440 (73 %) eran fármacos de moléculas pequeñas. Los tiempos de desarrollo medios fueron de 12,6 años (RIC, 10,6-15,3 años) para los productos biológicos frente a 12,7 años (RIC, 10,2-15,5 años) para los fármacos de moléculas pequeñas ( P = 0,76). Los productos biológicos tuvieron mayores tasas de éxito en los ensayos clínicos en todas las fases de desarrollo. Los costes de desarrollo medios se estimaron en 3.000 millones de dólares (RIC, 1.300 millones-5.500 millones de dólares) para los productos biológicos y 2.100 millones de dólares (RIC, 1.300 millones-3.700 millones de dólares) para los fármacos de moléculas pequeñas ( P = 0,39). Los productos biológicos estuvieron protegidos por una mediana de 14 patentes (RIC, 5-24 patentes) en comparación con 3 patentes (RIC, 2-5 patentes) para medicamentos de moléculas pequeñas ( P < .001). El tiempo medio hasta la competencia de los biosimilares fue de 20.3 años (RIC, 16.9-21.7 años) en comparación con 12.6 años (RIC, 12.5-13.5 años) para los medicamentos de moléculas pequeñas. Los productos biológicos lograron mayores ingresos máximos medios ($1.1 mil millones en el año 13; RIC, $0.5 mil millones-$2.9 mil millones) que los medicamentos de moléculas pequeñas ($0.5 mil millones en el año 8; RIC, $0.1 mil millones-$1.2 mil millones; P = .01) y tuvieron mayores ingresos medios en cada año después de la aprobación de la FDA. El costo anual medio del tratamiento fue de $92 000 (RIC: $31 000-$357 000) para los productos biológicos y de $33 000 (RIC: $4000-$177 000) para los medicamentos de moléculas pequeñas ( P = .005).
Conclusiones y relevancia Hay pocas pruebas que respalden que los productos biológicos tengan períodos más largos de exclusividad en el mercado o de protección frente a la negociación. Como resultado del trato diferenciado, la legislación estadounidense parece recompensar excesivamente el desarrollo de productos biológicos en comparación con los fármacos de moléculas pequeñas.
La atención integral al final de la vida: un enfoque necesario
Observamos a diario como instituciones de alta complejidad, acreditadas, de cuidados progresivos, a muchas personas morir y sufrir sin recibir el apoyo necesario. Entendiendo que morir es una transición natural e inevitable como el nacimiento. Recuperando la muerte, el duelo, como procesos sociales, con la desmedicalización necesaria, normalizando las conversaciones sobre la muerte, asistiendo al paciente y a sus seres queridos. Ciertamente en un mucho destrozado por los conflictos, la injusticia y la desigualdad. Personas desplazadas. Sin esperanzas. Rescatemos en cada uno de nosotros, los cuidadores, los pequeños actos de bondad, la palabra, la comprensión, la empatía, los tiempos y los afectos, el despedirse con lucidez de sus hijos, de sus parejas, de sus padres, comprendiendo que es un acto fundamental. Estas fuerzas, tan universalmente reconocidas como personales, dan forma a nuestra salud, nuestras vidas y nuestro mundo.
Afrontar la muerte de otra manera: revolucionar nuestra aproximación a la muerte y al duelo
BMJ 2024;387:q2815 Autor Selman Lucy.
A pesar del creciente interés público por la muerte, el apoyo a los cuidados al final de la vida y al duelo sigue siendo insuficiente. Necesitamos urgentemente un enfoque de salud pública centrado en la comunidad para los procesos sociales de la muerte y el duelo, respaldado por cuidados paliativos adecuadamente financiados,
En el Reino Unido, cada año mueren más de 600 000 personas, y más de seis millones de ellas siguen de luto. 2 A primera vista, las actitudes ante la muerte parecen estar cambiando: basta con observar el auge de los cafés sobre la muerte y el duelo, 3 festivales y eventos anuales de concienciación, 4 5 6 7 8 9 10 11 y la formación, en 2018, de una asociación nacional de doulas de fin de vida. 12 Proliferan los programas de televisión, las películas y los libros sobre la muerte y el duelo. Un vídeo de la BBC de la doctora en cuidados paliativos, autora y activista Kathryn Mannix, “Morir no es tan malo como crees”, ha tenido 145 000 visualizaciones. 13
Pero debajo de la superficie hay grandes lagunas en el conocimiento y la confianza del público en torno a la muerte, lo que significa que los deseos prácticos, emocionales y espirituales de las personas moribundas a menudo permanecen sin expresar ni cumplir. Mientras tanto, las intervenciones médicas inútiles al final de la vida persisten como un fracaso global. 14
La muerte es un proceso tan natural como el nacimiento, pero gran parte de la sociedad se niega a verlo así. Esta incomodidad se refleja en nuestro comportamiento: evitamos a las personas gravemente enfermas o en duelo y nos abstenemos de hablar de nuestros propios deseos sobre el final de la vida con familiares, amigos y profesionales de la salud. Estas actitudes están profundamente entrelazadas con cuestiones culturales y sistémicas, desde conceptos erróneos y perjudiciales sobre el duelo hasta la medicalización de la muerte.
Los recientes debates sobre la muerte asistida han puesto de relieve los fallos de nuestras actitudes y sistemas de atención al final de la vida y apoyo al duelo, y la diputada Rachael Maskell ha anunciado la creación de una comisión para mejorar los cuidados paliativos. Se trata de una medida oportuna y vital, pero la comisión debe abordar las cuestiones estructurales más amplias que determinan cómo mueren y sufren las personas. 15 Así como los determinantes sociales (ingresos, empleo, vivienda, educación, discapacidad y redes de apoyo social) determinan nuestra salud en vida, también determinan cómo morimos. 14 15 Sin un enfoque de salud pública de largo alcance e integrado para la atención al final de la vida y el duelo, solo estaremos haciendo pequeños retoques en los bordes de un sistema complejo.
Las personas gravemente enfermas o moribundas pasan sólo alrededor del 5% de su último año de vida bajo la atención directa de los servicios de salud, y el resto del apoyo lo proporcionan amigos, familiares y miembros de la comunidad sin formación sanitaria. 16 Entre el 75% y el 90% de la atención domiciliaria al final de la vida la proporcionan cuidadores no remunerados, a menudo miembros de la familia. 17 Es hora de cambiar el enfoque y poner a las familias y las comunidades en el centro de la gestión de la muerte, el duelo y el dolor, pero para desempeñar esta función necesitan recursos integrales, educación y apoyo. 18
Necesitamos hablar sobre la muerte…
La COVID-19 obligó a un reconocimiento global de la mortalidad, algo que para muchas personas es muy personal. Una encuesta realizada en 2021 por la empresa de funerarias Co-op Funeral Care sugirió un cambio de actitud: el 20% de los adultos se sentían más cómodos hablando del duelo, el 47% manifestó una mayor compasión hacia las personas en duelo y el 54% se sentía más consciente de su propia mortalidad. 19 Pero esta concienciación no ha llevado a la acción: solo el 14% de los adultos del Reino Unido ha hablado realmente con alguien sobre sus deseos al final de la vida. 20
A muchas personas les cuesta tomar decisiones informadas sobre los cuidados al final de la vida porque la jerga y los procesos médicos son muy opacos. Pocas personas saben qué es un plan de cuidados anticipados o una directiva anticipada o cómo y por qué se toman decisiones de “no intentar reanimación cardiopulmonar” (DNACPR, por sus siglas en inglés), 21 22 y solo el 60% de las personas son conscientes de que tienen derecho a rechazar un tratamiento que les salve la vida. 23
La desconfianza en los proveedores de atención sanitaria es otra barrera. Casi un tercio de los adultos del Reino Unido dudan de que se respeten sus preferencias al final de la vida, lo que hace que sea menos probable que expresen sus deseos. 20 Esto refleja una creciente insatisfacción con el NHS, 24 lo que indica que es necesario hacer mucho más para mejorar las experiencias del público y reconstruir la confianza.
. . . y de duelo
Las conversaciones después de una muerte también son vitales, pero el duelo es un tema que plantea desafíos particulares. El apoyo de los familiares, amigos y comunidades es fundamental para afrontar el duelo, 25 26 pero con demasiada frecuencia es insuficiente. 2 27 Muchos de nosotros tememos “decir algo incorrecto” y no sabemos cómo ofrecer apoyo; una cuarta parte de nosotros evitamos hablar con alguien que está de duelo, lo que agrava su aislamiento. 28
La vergüenza y el miedo a ofender pueden deberse a un estigma o a ideas equivocadas sobre el duelo. Por ejemplo, la idea psicoanalítica obsoleta de que el duelo se produce en “etapas” y tiene un tiempo limitado suele ser contraria a la experiencia. Las normas culturales también moldean el duelo: en los EE. UU., el “trastorno de duelo prolongado” es un diagnóstico para un duelo intenso después de 12 meses, 29 mientras que en Egipto el duelo entre lágrimas años después de una muerte se considera saludable. 30
También es una opinión común que existe una jerarquía en el duelo. Esto podría reflejar los esfuerzos sociales por controlar o compartimentar el duelo, pero aprobar algunas formas de respuesta a la pérdida mientras se priva de derechos a otras, como sucede a menudo cuando un bebé muere antes de nacer, 31 puede llevar a las personas a comparar su duelo con el de los demás y preocuparse de estar sufriendo demasiado o muy poco. Esas expectativas sociales mixtas hacen que las personas en duelo puedan creer que están fracasando, que son anormales o que no merecen apoyo, lo que les impide expresar sus sentimientos o pedir ayuda.
Medicalización . . .
La medicalización de la muerte ha desplazado el proceso de morir de los hogares y las comunidades a la atención sanitaria. 14 32 33 Morir se ha convertido en un proceso clínico, dejando de lado las dimensiones emocionales, sociales y espirituales que antes eran parte integral de las experiencias del final de la vida. La pérdida de los rituales religiosos y comunitarios en el norte global no ha hecho más que profundizar nuestra distancia con la muerte. El negocio funerario ha comercializado el duelo, y el duelo se ha profesionalizado: es competencia de los consejeros capacitados. 32 33
En el hinduismo, el sijismo y el islam, los rituales funerarios suelen incluir el lavado y la cobertura del cuerpo por parte de los miembros de la familia. En algunas partes del Reino Unido, hasta mediados del siglo XX, era común que las familias se encargaran de la muerte en casa. En los pueblos de Yorkshire, por ejemplo, las mujeres se enorgullecían de “acostar” a los muertos. 34 Los miembros de la familia se turnaban para sentarse junto al cuerpo durante la noche. Se contrataba a una mujer, la “postora”, para que llamara a todas las casas para pedir, o invitar, a los miembros de la familia a asistir al funeral. Estas tradiciones se han desvanecido; a nivel comunitario, los conocimientos y las habilidades cruciales han disminuido constantemente. Como resultado, es posible que no reconozcamos ni aceptemos cuando la muerte está cerca y que tengamos más miedo de la muerte y sus consecuencias.
Los profesionales de la salud también tienen dificultades para afrontar la muerte y los límites de lo que la ciencia médica puede lograr, sobre todo porque eso significa enfrentarse a su propia mortalidad. Pero, cuando los médicos evitan hablar de la muerte y de las preferencias de los pacientes para el final de sus vidas, los pacientes y sus familias pierden oportunidades cruciales de conectarse, prepararse y, en última instancia, tomar decisiones informadas. 35 La educación y la formación clínicas deben garantizar que los futuros médicos tengan habilidades de cuidados paliativos generalistas, sepan cuándo consultar a un especialista en cuidados paliativos y, fundamentalmente, no tengan miedo y reciban apoyo para tener conversaciones tiernas sobre la muerte, la piedra angular de la atención centrada en la persona. 36
… y despriorización
Los cuidados al final de la vida no sólo se han medicalizado, sino que se les ha quitado prioridad. Los sistemas de atención sanitaria y la educación se centran en la cura y la prolongación de la vida, a veces a expensas de la calidad de vida y la atención compasiva a las personas moribundas. 37 38
En el Reino Unido, aproximadamente el 90% de las personas que están muriendo se beneficiarían de cuidados paliativos, pero el 25% no los recibe. 39 40 41 Se prevé que la demanda aumente un 25% en los próximos 25 años a medida que aumenta la esperanza de vida y las condiciones de salud se vuelven más complejas, pero el sector ya está gravemente subfinanciado y sobrecargado. Solo un tercio de la financiación de los hospicios del Reino Unido proviene del estado, y los 1.000 millones de libras restantes se recaudan anualmente a través de tiendas benéficas, eventos de recaudación de fondos y donaciones. 42 Esta brecha de financiación envía un mensaje claro: la atención a las personas moribundas se valora menos que los tratamientos agresivos y los avances médicos de alta tecnología. (Seguramente no es coincidencia que 9 de cada 10 del personal clínico y asistencial en los hospicios del Reino Unido sean mujeres, 43 lo que refleja una larga historia de infravaloración del «trabajo de las mujeres»).
Este modelo de financiación fragmentado deja a las comunidades rurales y otras comunidades desatendidas con graves carencias en materia de atención, en particular para los niños. 44 A medida que aumenta la demanda de cuidados paliativos, se hace cada vez más urgente la necesidad de una financiación gubernamental adecuada para la prestación de cuidados al final de la vida en hogares de ancianos y en la comunidad, incluidos los hospicios. 45 46
Mientras tanto, existen marcadas desigualdades en el acceso a los servicios de cuidados paliativos, de cuidados paliativos y de duelo. Las comunidades marginadas enfrentan la mayor cantidad de obstáculos para acceder a la ayuda en un momento en que la compasión es más necesaria. 47 48 49 50 51 52 Los grupos de minorías étnicas, en particular, se enfrentan a barreras lingüísticas, una difusión inadecuada y una escasez de proveedores culturalmente competentes. 48 50 51 El 30% de las personas de grupos de minorías étnicas, pero solo el 17% de las personas blancas, dicen que no confían en los profesionales de la salud para brindar atención de alta calidad al final de la vida. 23
Para cerrar esas brechas, los servicios e intervenciones de cuidados paliativos y de hospicio deben ser coproducidos con y para las comunidades desatendidas. El acceso a la planificación anticipada de la atención, por ejemplo, puede mejorarse mediante el uso de métodos participativos basados en las artes y mediante la colaboración con organizaciones comunitarias de confianza para garantizar que la información y el apoyo sean culturalmente apropiados y accesibles en múltiples formatos e idiomas. 53 54
Integración significativa a través de un enfoque de salud pública
El acceso a los servicios y las intervenciones, aunque necesario, no es suficiente. La muerte, el morir, la atención y el duelo son eventos esencialmente comunitarios y deben recuperarse como tales. 14 Esta transformación requiere más que inversión: exige un cambio desde la evaluación de necesidades y la prestación de servicios hacia asociaciones intersectoriales genuinas con las autoridades locales, la asistencia social, el sector voluntario y comunitario y las comunidades. Debemos aprovechar y apoyar los activos comunitarios (los recursos sociales, culturales y naturales que ya están arraigados en nuestras comunidades) y priorizar los enfoques de atención basados en las relaciones. 55 56 A través de este enfoque pueden surgir nuevos sistemas en los que la resiliencia comunitaria y las redes de apoyo puedan prosperar. 57
Las alianzas entre la atención sanitaria, la asistencia social, las autoridades locales, el sector voluntario y comunitario y las comunidades no son nuevas: la atención integrada ha sido un principio central del NHS durante más de dos décadas. 58 Desde 2022, todas las juntas de atención integrada de Inglaterra tienen el deber legal de encargar servicios adecuados de cuidados paliativos y al final de la vida, incluido el apoyo al duelo, con el mandato de reducir las desigualdades sanitarias locales, proporcionando un impulso de arriba hacia abajo para el enfoque de salud pública para la atención al final de la vida y el duelo que es claramente necesario. Pero la prestación varía entre las juntas. 59 60
El debate sobre cómo debería ser una integración eficaz y qué es lo que se necesita para lograrla continúa. Los críticos de la integración sostienen que corre el riesgo de trasladar a la comunidad la responsabilidad de las desigualdades sanitarias, arraigadas en las políticas de austeridad. 61 Otros sostienen que la superación de las barreras a la integración, como la precariedad financiera a la que se enfrentan muchas organizaciones comunitarias, mejora la prestación de servicios y reduce las desigualdades sanitarias mediante la creación de resiliencia y capacidad colectiva en los sistemas vecinales. 62 En el ámbito de los cuidados paliativos y al final de la vida, los modelos comunitarios compasivos, como la Carta de Ciudades Compasivas, ofrecen un marco formalizado para apoyar los enfoques de salud pública, 63 pero puede ser un desafío cambiar un sistema hacia la participación y el desarrollo comunitarios después de un enfoque prolongado en la prestación de servicios. 64 66 Necesitamos un compromiso gubernamental a largo plazo para invertir en una integración intersectorial significativa y en la reorientación de los servicios de salud.
Alfabetización sobre la muerte y el duelo
Los medios de comunicación desempeñan un papel fundamental en la construcción colectiva de un sentido y la comprensión pública de la muerte y el duelo, pero a menudo higienizan o sensacionalizan las experiencias del final de la vida. En los dramas médicos, por ejemplo, la reanimación cardiopulmonar (RCP) suele presentarse como altamente efectiva, presentando resultados poco realistas que refuerzan conceptos erróneos. 67 68 Rara vez se muestran las experiencias de pacientes ancianos con multimorbilidad (la mayoría en entornos hospitalarios reales) cuyos resultados después de la RCP son notoriamente malos. 69 70 La cobertura de noticias, a menudo de muertes violentas o inesperadas, presenta la muerte como algo angustiante y temible, pero a distancia, como algo que les sucede a otras personas. 71 De manera similar, las vívidas descripciones del sufrimiento intratable hacia el final de la vida que se relataron en el parlamento el mes pasado durante los debates sobre la muerte asistida pueden causar un miedo innecesario a menos que también contemos historias de “muerte común”. 72 73 Las representaciones y los debates realistas sobre la muerte y el duelo pueden contrarrestar conceptos erróneos comunes, ayudando a alinear las expectativas del público con la realidad y fomentar actitudes y comportamientos sociales más compasivos.
Promover la alfabetización en la muerte y el duelo (el conocimiento y las habilidades para hablar y planificar la muerte y apoyar a otros en su duelo) es una parte clave de un enfoque de salud pública para los cuidados paliativos y al final de la vida y el duelo. Las artes y la cultura, incluidos los festivales, ofrecen puntos de entrada vitales a lo que pueden ser temas desafiantes. 7 8 La mayoría de los niños del Reino Unido estarán de luto por alguien cercano a ellos, sin embargo, el duelo, la muerte y la pérdida están en gran medida ausentes del currículo escolar. 74 Para preparar mejor a los niños para manejar su propio duelo y apoyar a otros, la educación sobre el duelo debería convertirse en una parte central del currículo nacional, una medida que actualmente se está debatiendo en el parlamento.
Los médicos también tienen un papel fundamental en la remodelación de actitudes y, por lo tanto, deben desarrollar su propia alfabetización sobre la muerte y el duelo. Al hablar abiertamente sobre los cuidados al final de la vida y cuestionar los conceptos erróneos comunes, los proveedores de atención médica pueden dar ejemplo de aceptación de la muerte, generar confianza y mostrar al público que es seguro hacer preguntas y expresar dudas y temores. La atención debe ser emocionalmente consciente, culturalmente sensible, compasiva y centrada en la persona, y esto debe reflejarse en la educación clínica y el apoyo continuo a los médicos. Los líderes clínicos deben reconocer el peso emocional de lidiar con la muerte y el duelo y apoyar a los médicos en esta tarea, alentando el intercambio, el apoyo entre pares y el recuerdo. Al hacer espacio para el duelo y la vulnerabilidad en la vida profesional, fomentamos el lado humano de ser un médico.
Para cambiar las actitudes sociales ante la muerte y el duelo se necesitan acciones audaces y multifacéticas. Necesitamos una inversión estatal adecuada en hospicios, cuidados paliativos y apoyo al duelo, y un esfuerzo decidido para eliminar las desigualdades en el acceso. Esto debe ir de la mano de un enfoque de salud pública que se base en la colaboración, la integración y el reconocimiento de las fortalezas de la comunidad. Pero nada de esto tendrá éxito sin alfabetización sobre la muerte y el duelo: los conocimientos, las habilidades y la confianza para enfrentar la mortalidad con los ojos abiertos. Tal vez la última pieza del rompecabezas, y la más difícil, sea el coraje de tender la mano a los demás cuando más importa.
Avances en IA y aprendizaje automático para la medicina predictiva

Introducción
Los recientes avances en genómica han reforzado nuestra capacidad para profundizar en las etiologías complejas de diversas enfermedades. Entre ellos, los estudios de asociación del genoma completo (GWAS, por sus siglas en inglés) son un ejemplo de los enfoques que impulsan estos avances y han mejorado enormemente nuestra comprensión de los factores genéticos que sustentan muchos rasgos y enfermedades complejos importantes. Sin embargo, esta investigación aún enfrenta muchas limitaciones que exigen soluciones innovadoras para liberar todo su potencial. Muchos de estos problemas surgen de la capacidad insuficiente de los métodos de modelado actuales para capturar el grado completo de complejidad biológica subyacente. El número de variantes genéticas es enorme y sus efectos individuales suelen ser pequeños y específicos del contexto. El mapeo completo de los mecanismos que traducen la variación genética en fenotipos requiere una fina integración del análisis genético con otros tipos de conocimiento y dominios «ómicos». Por su naturaleza, estas aspiraciones se alinean estrechamente con los problemas que se encuentran y resuelven actualmente en otros dominios de uso intensivo de datos, tanto en otras áreas de la biología como en un ámbito más amplio. En esta revisión, describiremos sinergias y soluciones prometedoras de los avances recientes en el análisis de DL y explicaremos sus posibles aplicaciones en la investigación biomédica.
Los amplios conjuntos de datos ofrecen información sobre los mecanismos moleculares que subyacen a diversas enfermedades y crean nuevas oportunidades para el modelado predictivo en la medicina de precisión, en particular en el ámbito de la predicción de la eficacia de los fármacos. Sin embargo, la complejidad y el volumen de los datos ómicos plantean desafíos importantes a la hora de extraer información significativa y descifrar el contexto biológico esencial. En el ámbito de la genómica de alto rendimiento, al igual que en otros dominios ómicos, los avances tecnológicos han traído consigo tanto los desafíos típicos asociados con la sobreabundancia de datos como también problemas únicos, como los que surgen de las particularidades metodológicas de los análisis de grupos de estudio. La interpretación significativa de dichos datos es complicada, ya que la mayoría de las estrategias de elaboración de perfiles contemporáneas capturan una visión aparentemente extensa pero funcionalmente estrecha de todo el sistema biológico. A continuación se describen brevemente algunos de los desafíos clave que afectan actualmente a la investigación genómica en el contexto de estos temas generales.
Una crítica que se recibe con frecuencia al enfoque GWAS es su enfoque en variantes genéticas comunes con efectos modestos que a menudo no explican una parte significativa de la contribución genética a los rasgos complejos [ 1 ]. Este problema surge debido a la presencia de variantes raras con contribuciones muy grandes, efectos epistáticos complejos e interacciones entre los genes y el medio ambiente. Incluso una vez que un estudio GWAS ha llevado a la identificación de variantes potencialmente relevantes, sigue siendo esencial determinar sus consecuencias funcionales y causalidad, lo que a menudo puede ser complicado y requerir experimentos específicos adicionales [ 2 ]. La tarea de distinguir las variantes causales de otros marcadores en bloques de desequilibrio de ligamiento y comprender sus efectos mecanicistas en los fenotipos observables requiere algún tipo de información adicional. Por lo tanto, este tipo de investigación se beneficiará en gran medida de la integración confiable y automatizada de la genómica funcional [ 3 ], la epigenómica [ 4 ] y la transcriptómica [ 5 ].
Intentar explicar procesos naturales cada vez más complejos requiere inevitablemente modelos de una complejidad comparable. Esto requiere el uso de algoritmos avanzados para automatizar la construcción de modelos y el proceso de ajuste, lo que da como resultado modelos de «caja negra» que, aunque son muy precisos, generalmente carecen de interpretabilidad humana. El aumento de la complejidad puede, en última instancia, limitar la utilidad de estos métodos para el descubrimiento biológico (ya que puede oscurecer pistas sobre mecanismos potenciales) y socavar la confianza en dichas herramientas para aplicaciones clínicas, un ejemplo son las puntuaciones de riesgo poligénico para enfermedades complejas [ 6 ]. Además, muchos estudios genéticos tienen que lidiar con cantidades subóptimamente pequeñas de muestras, especialmente en el caso de enfermedades raras, variantes con efectos sutiles o aquellas confinadas a subgrupos específicos de población. La inteligencia artificial (IA) y las técnicas de ML [ 7 , 8 ] ofrecen múltiples estrategias nuevas para abordar estas limitaciones y, lo que es más importante, mejorar nuestra capacidad para integrar el conocimiento y los datos en múltiples capas de organización biológica.
Los algoritmos de ML abarcan una amplia gama de métodos computacionales que permiten a las computadoras construir modelos predictivos que conducen a información procesable. En genómica médica, las técnicas de ML han encontrado diversas aplicaciones, que incluyen, entre otras, la clasificación predictiva de enfermedades, el descubrimiento de biomarcadores, la predicción de la respuesta a medicamentos y la identificación de variantes genéticas causantes de enfermedades. Las técnicas clásicas de ML, como Random Forest [ 9 ], Support Vector Machines [ 10 ] y la regresión logística [ 11 ], han sido fundamentales en el análisis de datos ómicos. Estos métodos se destacan en el manejo de datos de alta dimensión y han demostrado éxito en varios esfuerzos de investigación genómica. Para una encuesta integral sobre las aplicaciones típicas de las técnicas de ML estándar en la investigación biomédica, se remite a los lectores a los artículos de revisión existentes [ 12 , 13 , 14 , 15 , 16 , 17 ]. Sin embargo, a medida que aumentan las dimensiones y las capas de datos, también lo hacen las limitaciones de estos métodos clásicos. Un inconveniente importante es su falta de sensibilidad a las relaciones que se esconden detrás de los datos, por ejemplo, los genes, que suelen ser cruciales en la ómica, porque en su mayoría provienen de datos “tabulares”, donde las variables se representan de forma independiente entre sí. Aprovechar las posibles relaciones de los genes o elementos puede ofrecer una gran cantidad de información, como describimos en detalle a continuación.
La aparición del aprendizaje automático ha revolucionado el campo de la IA y ha transformado el panorama del análisis de datos. Esta capacidad del aprendizaje automático para aprender representaciones jerárquicas a partir de datos sin procesar ha demostrado ser inestimable para el modelado predictivo, capturando dependencias intrincadas dentro de los conjuntos de datos, incluso cuando se trata de datos ruidosos y de alta dimensión. Un avance particularmente importante en el área del aprendizaje automático es la creación de nuevos métodos para tratar con tamaños de muestra pequeños, una preocupación recurrente en la elaboración de perfiles genéticos de poblaciones pequeñas y enfermedades raras. Si bien la aplicación ideal del aprendizaje automático tiene como objetivo facilitar el aprendizaje de la representación integral de las estructuras subyacentes dentro de los datos ómicos, surgen desafíos prácticos cuando hay muy pocas muestras disponibles. En ciertas aplicaciones, esto puede incluso obstaculizar el aprendizaje de la representación adecuada y complicar el procesamiento directo de los datos ómicos dentro de los marcos de aprendizaje automático. Esta importante limitación se puede mitigar utilizando una técnica llamada aprendizaje por transferencia. A diferencia de los modelos estadísticos clásicos, las redes neuronales se ajustan secuencialmente, lo que significa que se pueden actualizar continuamente con nuevos datos. Esto abre la posibilidad de «preentrenar» un modelo en un conjunto de datos grande, pero débil o parcialmente relevante y luego finalizar el entrenamiento en uno más valioso pero más pequeño. Para los patrones que persisten entre los dos conjuntos de datos habrá un beneficio del acceso a todas las observaciones combinadas, mientras que los patrones irrelevantes simplemente se sobrescribirán con nuevos datos. El aprendizaje por transferencia puede facilitar la reutilización del conocimiento de conjuntos de datos más grandes para mejorar sustancialmente la precisión en cohortes más pequeñas. En principio, los modelos preentrenados inicializados en datos genéticos a gran escala pueden reespecializarse para nuevas tareas, lo que reduce la necesidad de recopilación de datos y al mismo tiempo mejora el rendimiento. El potencial y las limitaciones de esta estrategia se discuten en detalle en esta revisión y sus beneficios se demuestran con varios ejemplos [ 18 , 19 , 20 , 21 , 22 , 23 , 24 ].
Los modelos DL ofrecen una amplia gama de capacidades de análisis adicionales que pueden mejorar muchos tipos de análisis biomédicos de alto rendimiento. En primer lugar, las redes neuronales artificiales pueden identificar fácilmente grandes cantidades de interacciones y modelar efectos no lineales, al mismo tiempo que ofrecen una regularización muy eficaz para mitigar el riesgo de sobreajuste [ 25 ]. En segundo lugar, las redes neuronales modernas pueden utilizar tamaños de entrada muy grandes, incorporar métodos para la imputación de valores faltantes [ 26 ] y acomodar tipos muy diversos de información estructurada. Todas estas capacidades ofrecen formas adicionales de aumentar la potencia para detectar SNP raros, epistasis y modelar con mayor precisión la gama completa de posibles patrones de asociación. Los modelos DL pueden analizar e integrar conjuntamente fuentes de datos heterogéneos, lo que permite una visión más completa de las contribuciones genéticas y algunos métodos introducidos recientemente ofrecen formas de integrar diferentes tipos de datos ómicos dentro del mismo modelo y realizar inferencias entre ellos simultáneamente. Cabe destacar la familia de enfoques DeepInsight [ 18 , 19 , 20 , 21 ], donde varios estudios han demostrado un análisis transómico exitoso que incluía la variación somática del cáncer como uno de los tipos de entrada. Como este tipo de datos es similar a la variación de la línea germinal, se pueden utilizar estrategias potencialmente similares en el futuro para mejorar la anotación funcional y causal de los SNP.
Por último, el uso creciente de la IA en todas las áreas de la vida ha puesto de relieve la necesidad de que dichos sistemas se vuelvan más transparentes e interpretables. Este problema es un foco de creciente interés de investigación y la IA explicable (XAI) ahora está surgiendo como su propia subdisciplina dentro de la investigación de la IA. Como la gran mayoría de este trabajo se realizó con modelos basados en DL, la mayoría de estos métodos se pueden utilizar fácilmente con la mayoría de las arquitecturas típicas de redes neuronales. Técnicas como la atención y la atribución basada en gradientes pueden, en principio, ayudar a comprender la contribución de los factores biológicos individuales al riesgo de enfermedad y la respuesta a los medicamentos, lo que hace que los resultados sean más interpretables para biólogos y médicos. Para demostrar estos beneficios potenciales, esta revisión utilizará el método DeepFeature como un ejemplo ilustrativo, que implementa un enfoque de atribución basado en gradientes para descubrir posibles mecanismos involucrados en la eficacia de los medicamentos contra el cáncer [ 20 , 21 ].
Aquí nos centramos más en las CNN de inspiración biológica [ 27 ], que son una de las arquitecturas fundamentales ampliamente utilizadas en el dominio de la visión por computadora, y su adopción ha llevado a mejoras sin precedentes en el rendimiento. Las CNN bidimensionales (2D) son herramientas ampliamente utilizadas, particularmente para el análisis de datos de imágenes, ya que extraen características espaciales jerárquicamente, comenzando con datos de imágenes sin procesar, pasando por la detección de bordes, etc., y finalmente para la predicción de objetos. Si bien las CNN 2D han prosperado tradicionalmente en el análisis de imágenes, recientemente ha surgido un interés en su aplicación al análisis de datos ómicos. Los investigadores han contemplado la posibilidad de aprovechar la potencia de las CNN 2D para el análisis de datos tabulares u ómicos, lo que requiere la revelación de información latente (a veces llamamos «espacial») inherente entre los genes (o elementos) dentro de una muestra (o vector de características) [ 28 , 29 , 30 , 31 ]. [ 32 ] subrayaron la importancia de DL incluyendo CNN en tareas predictivas como determinar la especificidad de secuencia de proteínas de unión de ADN y ARN y señalar regiones cis-reguladoras, entre otras aplicaciones. En particular, las CNN y las redes neuronales recurrentes se han convertido en las arquitecturas de elección para modelar estos elementos reguladores con patrones de secuencia, lo que ilustra la amplia utilidad de DL en genómica. Talukder et al. exploran más a fondo las complejidades de los métodos de interpretación de redes neuronales profundas (DNN), particularmente sus aplicaciones en genómica y epigenómica [ 33 ]. Esta amplitud de aplicación también se extiende a la biología sintética, enfatizando su promesa en el mejoramiento de plantas y animales [ 34 ]. No obstante, las revisiones existentes no han abordado ampliamente cómo manejar de manera efectiva datos tabulares como datos ómicos sin patrones explícitos convirtiéndolos en representaciones adecuadas para CNN.
Con la aparición de técnicas de conversión como DeepInsight [ 18 ], se ha producido un avance revolucionario: la conversión de datos tabulares, como los datos ómicos, en representaciones similares a imágenes. Esta conversión transformadora ahora permite el aprovechamiento eficaz de las CNN para el análisis. DeepInsight, una técnica pionera, revoluciona el preprocesamiento de datos al incorporar información latente entre genes o elementos dentro de un vector de características. Esta reinvención de los datos organiza los elementos que comparten características similares en vecinos próximos, mientras que los elementos distantes siguen siendo distintos. Este contexto espacial genera un entorno rico para que las CNN funcionen no solo de manera factible sino también perspicaz. A diferencia de las técnicas de ML tradicionales, que manejan variables de forma independiente y a veces eligen las representativas, esta nueva técnica reúne variables similares cercanas y las trata como un grupo, lo que refleja la estructura detrás de los datos ómicos.
Para aclarar más, cuando los datos biológicos se transforman en un formato de imagen, las relaciones latentes entre entidades biológicas, como los genes, se codifican como proximidades espaciales dentro de la imagen. Posteriormente, el uso de una CNN con estas imágenes permite una reducción sustancial en el número de parámetros del modelo. Esta reducción se logra mediante el diseño arquitectónico de capas convolucionales, que son expertas en identificar oportunidades para compartir parámetros entre entradas apropiadas, específicamente en casos caracterizados por correlaciones lineales parciales o incluso no lineales entre características. Dada la prevalencia de tales correlaciones en datos biológicos, los modelos resultantes suelen tener mejores capacidades de generalización, al tiempo que preservan la capacidad innata de las redes neuronales para descubrir y modelar características más complejas si y cuando sea necesario. Además, estas imágenes facilitan la interpretación de los resultados al mostrar explícitamente la relación potencial entre las entidades biológicas que el modelo considera importantes, como se explicará en detalle más adelante.
Una ventaja adicional notable es la capacidad de utilizar el aprendizaje por transferencia, lo que elimina la necesidad de crear redes desde cero. Este atributo permite un aprendizaje integral en un espectro diverso de datos ómicos, lo que abre nuevas vías para un análisis integral. A través del aprendizaje por transferencia, los modelos se pueden inicializar con pesos de un modelo preentrenado [ 35 ], desarrollado típicamente utilizando conjuntos de datos de imágenes extensos y diversos como ImageNet. Estos modelos preentrenados ya han aprendido patrones esenciales de millones de imágenes naturales, capturando jerárquicamente características universales que son sorprendentemente efectivas cuando se reutilizan para tareas distintas, incluso en dominios aparentemente no relacionados como la genómica. Este enfoque permite a los investigadores capitalizar el conocimiento fundamental integrado en estos modelos preentrenados, reduciendo drásticamente el esfuerzo computacional y el tiempo requerido para el entrenamiento, y a menudo mejorando el rendimiento.
El uso del aprendizaje por transferencia con modelos entrenados previamente ofrece una ventaja única para el análisis de datos ómicos [ 18 , 19 ]. Los conjuntos de datos genómicos, a diferencia de los conjuntos de datos de imágenes disponibles públicamente, suelen tener un tamaño limitado. Aprovechar el patrón aprendido por los modelos a partir de grandes conjuntos de datos de imágenes mediante el aprendizaje por transferencia puede proporcionar una base sólida, que permite a los investigadores ajustar estos modelos para las particularidades de los datos ómicos, sin la necesidad de grandes conjuntos de entrenamiento. Además, el aprendizaje por transferencia permite la extracción de patrones intrincados y matizados de los datos ómicos que podrían pasarse por alto o ser inalcanzables al comenzar el entrenamiento del modelo desde cero. La destreza del aprendizaje por transferencia mediante CNN se muestra vívidamente en varias aplicaciones más allá del procesamiento de imágenes, lo que demuestra su potencial para revolucionar el análisis de datos en todos los campos [ 18 , 22 , 36 , 37 ].
La adaptabilidad de DeepInsight es evidente a través de sus aplicaciones en varios dominios, incluido su papel fundamental en la conformación del modelo ganador (‘Hungry for gold’) de la competencia de Kaggle.com [ 19 , 20 , 22 , 23 , 38 , 39 , 40 , 41 , 42 , 43 , 44 , 45 , 46 ]. Para una exploración en profundidad, los curiosos pueden adentrarse en un compendio integral de métodos de conversión de imágenes y sus aplicaciones, como lo explican Ye y Wang [ 47 ]. Esta progresión transformadora en la transformación y el análisis de datos significa un paso trascendental hacia adelante no solo para desentrañar los intrincados matices arraigados en los datos tabulares, sino también para mejorar sus capacidades de modelado predictivo. La representación esquemática del proceso de conversión de tabla a imagen para usar CNN se ilustra en la Fig. 1 .
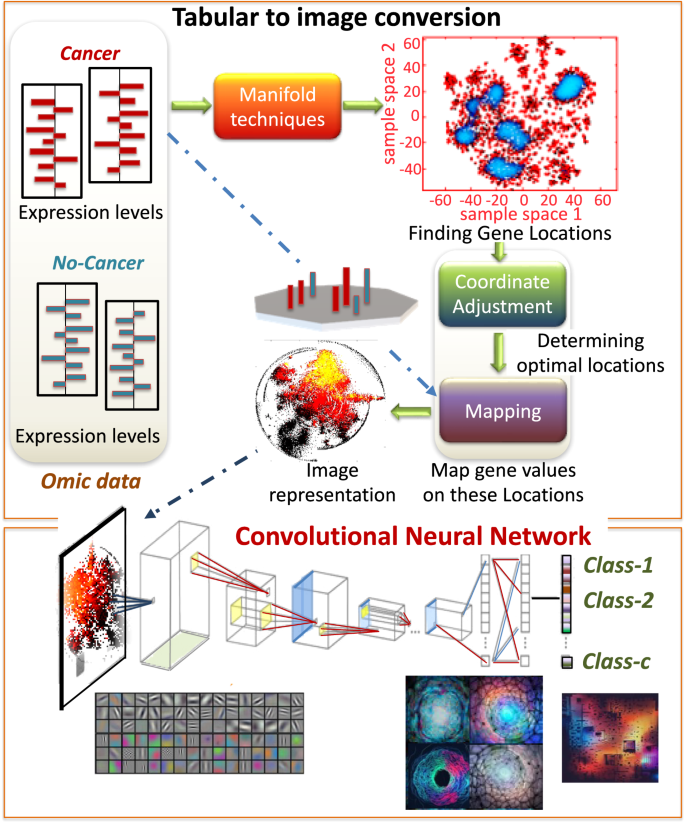
Desafíos en el avance de las aplicaciones de CNN en el análisis ómico
Si bien la combinación de conversión de tablas a imágenes con redes neuronales convolucionales para el análisis ómico ha impulsado avances significativos, aún queda un panorama de desafíos y problemas por resolver, entre ellos:
- 1.Interpretabilidad: Los modelos DL, incluidas las CNN, suelen considerarse como «cajas negras» debido a sus arquitecturas complejas. La capacidad de comprender los genes o elementos específicos que influyen en las decisiones de un modelo es fundamental para dilucidar los mecanismos biológicos, como las vías. Aunque se han introducido técnicas como DeepFeature [ 20 ], que aprovecha los mapas de activación de clases (CAM) [ 48 ], el desafío sigue abierto y requiere el desarrollo de modelos para interpretar las características aprendidas para obtener conocimientos más profundos.
- 2.Heterogeneidad de los datos: los datos ómicos son intrínsecamente heterogéneos y abarcan diversos tipos de información biológica, como la expresión génica, la metilación y la mutación. Adaptar varios tipos de datos ómicos y, al mismo tiempo, preservar cada estructura latente plantea un desafío.
- 3.Escalabilidad y tamaño de los datos: los modelos de aprendizaje automático, incluidas las redes neuronales convolucionales, exigen cantidades sustanciales de datos para una generalización eficaz. Sin embargo, los conjuntos de datos ómicos, especialmente los asociados con enfermedades raras o afecciones específicas, pueden tener tamaños de muestra limitados. Superar las limitaciones de los conjuntos de datos de pequeña escala y garantizar la solidez del modelo son consideraciones vitales.
- 4.Sobreajuste: Se sabe que los métodos tradicionales de aprendizaje automático, en particular cuando se trata de datos ómicos de alta dimensión, son susceptibles al sobreajuste. Esto llevó a comprender que la complejidad del modelo debe gestionarse con cuidado para evitar dicho sobreajuste. Sin embargo, los avances teóricos recientes están desafiando esta visión, en particular en el ámbito del aprendizaje automático. Específicamente, los algoritmos de aprendizaje automático poseen características de regularización intrínsecas dentro de su proceso de aprendizaje de propagación hacia atrás. Curiosamente, estas características pueden reducir el riesgo de sobreajuste a medida que la red escala; al contrario de lo que se podría esperar, agregar más nodos o capas puede hacer que el modelo sea más robusto. Esto cambia radicalmente nuestra comprensión tradicional de las estadísticas clásicas y el aprendizaje automático, donde una mayor complejidad del modelo generalmente exacerba el sobreajuste. Por lo tanto, si bien la importancia de equilibrar la complejidad, la capacidad y los datos del modelo sigue siendo válida, estos nuevos conocimientos sugieren que las consideraciones para lograr este equilibrio en el contexto de las redes neuronales profundas pueden ser fundamentalmente diferentes.
- 5.Ajuste de hiperparámetros: los modelos de aprendizaje automático comprenden múltiples hiperparámetros que influyen en su rendimiento. Identificar el conjunto óptimo de hiperparámetros para conjuntos de datos ómicos específicos puede requerir mucho tiempo y experiencia. Las técnicas de optimización bayesiana ofrecen vías para explorar hiperparámetros óptimos.
- 6.Recursos computacionales: el entrenamiento de modelos de aprendizaje a distancia, especialmente las redes neuronales convolucionales, puede agotar los recursos computacionales. Para los investigadores con recursos limitados, optimizar el proceso de entrenamiento y explorar técnicas como el aprendizaje por transferencia se vuelve crucial.
- 7.Relevancia biológica: si bien los modelos convierten los datos ómicos en representaciones similares a imágenes, es fundamental preservar la relevancia biológica de estas representaciones. Validar la significatividad de los datos transformados en términos de captar los mecanismos biológicos subyacentes sigue siendo un desafío.
- 8.Generalización: garantizar la generalización de un modelo en diferentes condiciones experimentales, plataformas y contextos biológicos exige atención. Si bien los esfuerzos recientes han integrado datos de células individuales de diferentes plataformas para la identificación de células en el contexto de la conversión de tablas a imágenes con la aplicación CNN [ 21 ], se justifica una mayor investigación en esta dirección.
- 9.Integración con el conocimiento del dominio: la incorporación de conocimientos específicos del dominio en el proceso de entrenamiento del modelo mejora la interpretabilidad y la relevancia de los resultados. El desarrollo de métodos para integrar sin problemas el conocimiento biológico previo con el análisis basado en CNN es prometedor.
- 10.Evaluación comparativa y comparación: una evaluación comparativa rigurosa con métodos establecidos y comparaciones entre conjuntos de datos son vitales para evaluar el verdadero potencial de un modelo.
En la figura 2 se muestra un resumen de estos problemas . Para abordar estos desafíos multifacéticos se necesita una colaboración interdisciplinaria entre expertos en aprendizaje automático, investigadores en bioinformática y biólogos. Esta colaboración es fundamental para avanzar en la integración de modelos de conversión de tablas a imágenes con redes neuronales convolucionales, lo que impulsa los horizontes del análisis y la interpretación de datos ómicos.
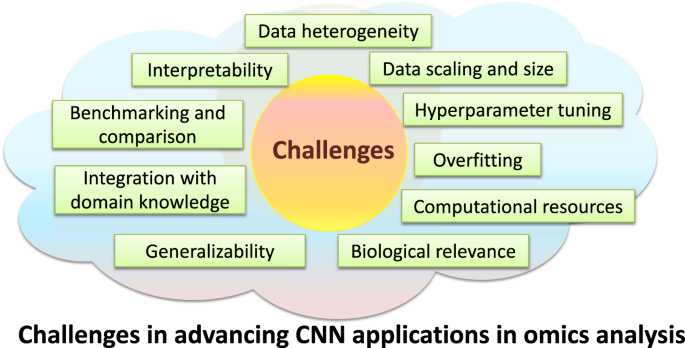
DeepInsight y DeepFeature: una nueva peculiaridad en el análisis de datos ómicos
La aplicación del aprendizaje automático a la genómica se ha producido principalmente en el ámbito del análisis de datos tabulares (similares a tablas, incluidos los vectoriales). Sin embargo, con la aparición de nuevas metodologías, ahora podemos superar la brecha entre el análisis de datos tabulares y de imágenes, mejorando la extracción de información significativa de los conjuntos de datos ómicos.
DeepInsight: transformación de datos tabulares en formato similar a imágenes y uso de CNN preentrenada
A la vanguardia de este enfoque de transformación se encuentra DeepInsight [ 18 ], una metodología diseñada para convertir datos tabulares (incluidos los datos ómicos) en representaciones similares a imágenes que reflejan la estructura latente detrás de los datos. La Figura 3 proporciona una ilustración del proceso de DeepInsight. Brevemente, un vector de características, , que contiene expresiones o elementos genéticos se transforma en una matriz de características a través de una transformación . La ubicación de las características individuales dentro de esta matriz depende de sus similitudes, como se muestra en la Figura 3a . Una vez que se determinan las ubicaciones de las características, sus valores de expresión o elementos se asignan a estas posiciones. El proceso de transformación consta de varios pasos clave, como se muestra en la Figura 3b :xMT
- 1.Colocar los genes o elementos en las coordenadas cartesianas utilizando métodos múltiples como t-SNE, UMAP o kernel PCA.
- 2.Utilizando el algoritmo de envoltura convexa para encontrar el rectángulo más pequeño que encapsula la distribución de características, seguido de una rotación para alinear con los ejes horizontal y vertical.
- 3.Conversión de las coordenadas cartesianas a un marco de píxeles.
- 4.Asignar los valores de los elementos o la expresión genética a sus posiciones correspondientes dentro de este marco de píxeles.
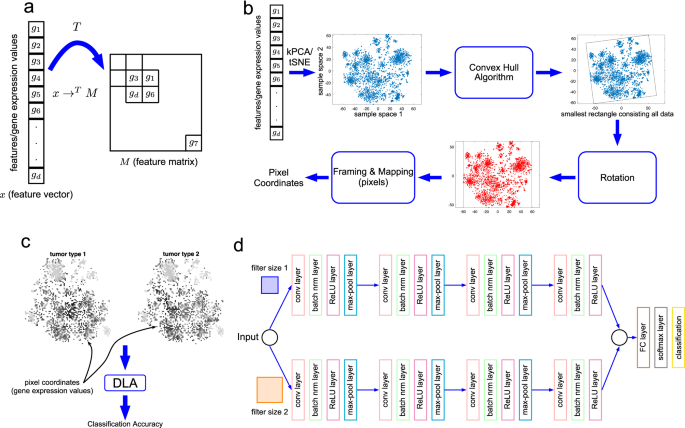
En este proceso de conversión, la similitud entre genes u otros factores de interés se representa por la cercanía relativa de sus posiciones espaciales. Esta codificación asegura que los elementos con características similares se posicionen próximos entre sí, mientras que aquellos que son diferentes se posicionen distantes. Esta transformación produce una representación de imagen equivalente al vector de características original, como se muestra en la Fig. 3c . Estas imágenes generadas sirven como entrada para las CNN en el modelado predictivo posterior, como se representa en la Fig. 3d . Otras mejoras ampliadas en este paradigma, como agregar la técnica de desenfoque a DeepInsight [ 49 ], fusión con filtrado de Gabor [ 50 ], con autoencoders [ 24 ], alineando características en diferentes capas (para evitar promediar) [ 38 , 46 ], transformando a un marco de píxeles fijos [ 45 ] y modelo de representación multifacética [ 51 ]. El DeepInsight original se ha perfeccionado aún más y Gokhale y su equipo lo adaptaron por primera vez para su integración con Vision Transformers (ViT), lo que supone un importante avance en este campo [ 24 ].
Las representaciones similares a imágenes resultantes son ideales para el análisis mediante redes neuronales convolucionales. Además, como se mencionó anteriormente, DeepInsight facilita el uso de modelos de redes neuronales convolucionales previamente entrenados, que históricamente han sobresalido en el análisis de imágenes. El beneficio de este enfoque es doble: no solo aprovecha las sólidas capacidades de las arquitecturas de redes neuronales convolucionales preexistentes, sino que también ofrece información acelerada al eliminar la necesidad de entrenar los modelos desde cero.
Para evaluar el rendimiento de DeepInsight, se examinaron varios escenarios, como se detalla en [ 18 ], incluida la predicción del tipo de cáncer, en la que el método brindó un rendimiento mejorado en relación con varios otros métodos de ML. En un estudio posterior, DeepInsight-3D [ 19 ] se comparó con múltiples arquitecturas de redes neuronales (feed forward, autoencoder, ANNF), pipeline de bosque aleatorio optimizado (AutoBorutaRF), clasificador basado en máquina de vectores de soporte y tres pipelines recientes de predicción de respuesta a fármacos (modelo de Gelleher et al., MOLI y Super.FELT). DeepInsight-3D mostró una mejora del 7-29% en el rendimiento, medido por el modelo AUC-ROC, en todos estos métodos.
DeepFeature: extracción de características con CAM
DeepFeature [ 20 ] complementa las capacidades analíticas introducidas por DeepInsight. Mientras que DeepInsight se centra en la transformación de datos, DeepFeature apunta al desafío de la interpretabilidad, particularmente en el contexto de los modelos DL. Utilizando CAMs [ 48 ], DeepFeature extrae y resalta las características fundamentales que influyen en las decisiones de un modelo, por ejemplo, la predicción. En genómica, esto se traduce en la identificación de genes o elementos clave que son cruciales para determinar resultados fenotípicos específicos o la manifestación de enfermedades. La Figura 4 ilustra la secuencia de la metodología DeepFeature. Un vector de entrada de datos tabulares se presenta en la parte superior izquierda, lo que lleva a las características o genes seleccionados que se muestran en la parte inferior derecha.
Las implicaciones biológicas son profundas, especialmente cuando se analizan los tipos de cáncer como se describió anteriormente. Al transformar los datos ómicos de varias muestras de cáncer en formatos similares a imágenes, los investigadores pueden usar las CNN para discernir patrones y diferencias que podrían ser difíciles de detectar en el análisis tabular tradicional. Las capacidades de extracción de características de DeepFeature enriquecen aún más este análisis. Al resaltar genes o elementos de importancia dentro de las CNN a través de técnicas de visualización como CAM, los investigadores pueden obtener conocimientos más profundos sobre los mecanismos moleculares que impulsan los diferentes tipos de cáncer. Cuando se aplica a la tarea de identificación del tipo de cáncer descrita anteriormente, podría extraer muchos más genes/vías relacionadas con el cáncer conocidos que los modelos estadísticos tradicionales o los métodos de ML como la regresión logística penalizada, y también podría descubrir nuevas vías para la clasificación de diferentes tipos de cáncer. Estos conocimientos tienen el potencial de dilucidar las vías que se activan o suprimen en formas específicas de cáncer, allanando el camino para estrategias terapéuticas específicas y medicina personalizada.
En resumen, la innovadora transformación de datos ómicos en imágenes ofrece un cambio de paradigma en el análisis ómico. Mediante la transformación avanzada de datos y la extracción de características, estas metodologías proporcionan una lente más refinada para explorar el complejo mundo de la genómica, en particular para comprender las complejidades de diversas enfermedades como el cáncer. Es decir, estas metodologías pueden realizar «descubrimientos científicos» a partir de «big data».
DeepInsight-3D
Para abordar la cuestión de la modalidad de datos heterogéneos en los análisis multiómicos, como se mencionó anteriormente, hemos conceptualizado y desarrollado DeepInsight-3D [ 19 ], una extensión del DeepInsight original, diseñado específicamente para análisis multiómicos.
Ampliación de DeepInsight para análisis multiómicos
DeepInsight, diseñado originalmente para transformar datos ómicos tabulares en representaciones similares a imágenes, allanó el camino para aprovechar la destreza computacional de las CNN preentrenadas para la genómica. DeepInsight-3D lleva esto a un nivel superior. Al adaptarse a datos multiómicos, integra información de diferentes tipos ómicos en un espacio tridimensional (3D) unificado. Esta representación 3D captura las interacciones sinérgicas entre diferentes tipos de datos ómicos, lo que facilita una comprensión holística y ofrece un contexto más rico para el análisis. La Figura 5 proporciona una representación gráfica del modelo DeepInsight-3D. Los datos multiómicos se muestran en el lado izquierdo, y culminan en la selección de genes después del bloque Element Decoder (en la parte inferior central de la Figura 5 ).
Aplicación a la predicción de la respuesta a fármacos contra el cáncer
Los recientes avances en los campos de la IA, especialmente el ML y el DL, han demostrado un potencial notable en el modelado predictivo de la respuesta a los fármacos en diversas enfermedades, incluido el cáncer. La aplicabilidad de estas técnicas computacionales varía desde la caracterización numérica de moléculas para algoritmos de ML [ 52 ] hasta la evaluación de la generalización de los modelos de respuesta a fármacos [ 53 ]. En particular, se han empleado métodos de DL complejos para predecir las respuestas a los fármacos en líneas celulares cancerosas, aunque aún existen desafíos como el sobreajuste a conjuntos de datos limitados [ 54 ]. Estos métodos computacionales ofrecen vías para opciones de tratamiento más precisas e individualizadas, lo que proporciona un impacto significativo en la medicina de precisión y la atención médica [ 55 ].
Una de las aplicaciones de DeepInsight-3D se encuentra en el campo de la oncología, específicamente para la predicción de la respuesta a los fármacos contra el cáncer. Aunque los datos limitados sobre la respuesta a los fármacos causan problemas de estabilidad en el modelo, este concepto es un paso adelante en el manejo de datos multimodales. Al representar datos multiómicos en 3D, DeepInsight-3D puede capturar las interacciones complejas de los genes. Cuando se combina con datos específicos de pacientes, esta herramienta ofrece predicciones sobre cómo un tumor podría responder a un fármaco contra el cáncer específico. Este tipo de predicción tiene el potencial de revolucionar la medicina al guiar las decisiones terapéuticas basadas en perfiles de pacientes individuales.
En el artículo DeepInsight-3D, se introdujeron datos multiómicos de mutaciones genéticas, expresión genética y alteraciones del número de copias para crear el modelo de predicción de la eficacia de los fármacos. El mapeo de los puntos de datos se determinó a partir de los datos de expresión por DeepInsight y se posicionaron las mutaciones y las alteraciones del número de copias en las posiciones de los genes, con diferentes colores según sus niveles. Las líneas celulares Cancer Cell Line Encyclopedia (CCLE) y Genomics of Drug Sensitivity in Cancer (GDSC) acompañadas de la eficacia de los fármacos, y los conjuntos de datos de Cancer Genome Atlas (TCGA) y xenografts derivados de pacientes (PDX) se utilizaron para aprender y probar la CNN, respectivamente. Como resultado, mostró una precisión del 72 %, que superó a otros métodos basados en el aprendizaje profundo en más del 7 %. Esto demostró claramente el poder del esquema de transformación de DeepInsight.
Selección de características con DeepFeature y análisis de rutas
Representar y predecir no es suficiente; comprender el porqué y el cómo de estas predicciones es primordial, especialmente en un entorno clínico. DeepFeature, utilizado en conjunto con DeepInsight-3D, extrae características cruciales mediante CAM, destacando regiones específicas en la representación 3D que influyen significativamente en las predicciones. Esta selección de características es crucial no solo para la interpretación del modelo, sino también para guiar las investigaciones biológicas posteriores.
Para ampliar nuestra comprensión, el análisis de las vías, posterior a la extracción de DeepFeature, descifra el significado biológico de estas características influyentes. Por ejemplo, en el contexto de la respuesta a los fármacos contra el cáncer, la identificación de las vías asociadas con la resistencia o sensibilidad a los fármacos puede arrojar luz sobre posibles dianas moleculares y estrategias terapéuticas. DeepInsight-3D ha identificado muchas vías que se sabe que están implicadas en múltiples respuestas a los fármacos: STAT3, PI3K/AKT, JAK/STAT, Rho GTPasa, degradación y reciclaje de proteínas, estructura extracelular y adhesión celular, y podría encontrar nuevas vías: metabolismo del triptófano X y endocitosis dependiente de clatrina. Dicho esto, la estabilidad es un problema con DeepInsight-3D y la escala limitada de datos puede dar lugar a predicciones incorrectas. Por lo tanto, se deben tener en cuenta estas consideraciones al estimar el modelo. Sin embargo, la integración exitosa de la multiómica a través de DeepInsight-3D, combinada con las capacidades de extracción de características de DeepFeature, es prometedora para una gran variedad de aplicaciones, desde el desarrollo de fármacos hasta la terapia personalizada.
visión profunda de sc
Desentrañando el paisaje celular con mayor precisión: aplicación a datos de scRNA-seq para la identificación de tipos de células
La secuenciación de ARN de células individuales (scRNA-seq) ha abierto nuevas fronteras en la comprensión de la heterogeneidad celular, revelando información que a menudo queda oculta en la secuenciación masiva de ARN. Sin embargo, el desafío radica en el procesamiento y la interpretación de los datos de alta dimensión producidos. Al ingresar un perfil de expresión génica para una sola célula a partir de scRNA-seq, la tarea de anotación del tipo de célula identifica el tipo de célula del que proviene el perfil. Los métodos tradicionales de anotación del tipo de célula se basan en el etiquetado manual de los resultados de agrupamiento no supervisado. Este proceso requiere el análisis de los resultados de expresión de genes marcadores específicos. Sin embargo, los genes marcadores disponibles son limitados y se superponen, especialmente para subtipos de células similares. La selección e interpretación subjetiva de las listas de genes marcadores también descuidan las complejas interrelaciones entre los genes, lo que impide aún más una anotación precisa. Aquí es donde entra en juego scDeepInsight [ 21 ], que aprovecha las fortalezas de DeepInsight y las amplía con medidas de control de calidad y normalización de lotes para atender específicamente las complejidades del análisis de células individuales. La Figura 6 presenta una descripción general de scDeepInsight en el lado izquierdo. En el lado derecho, la figura contrasta la anotación de células real con la anotación de células predicha por scDeepInsight.
A la izquierda, el flujo de trabajo de scDeepInsight progresa desde la introducción del identificador molecular hasta la generación de anotaciones celulares.
Después de procesar un conjunto de datos de referencia y los datos de consulta, se traducen en imágenes 2D, que se utilizan para entrenar el modelo CNN. Cabe destacar que solo los datos de referencia entrenan el modelo, mientras que el conjunto de consulta se clasifica. Para futuros conjuntos de consultas, el modelo existente se puede aplicar directamente sin un nuevo entrenamiento. A la derecha, una visualización UMAP de un conjunto de datos de consulta muestra los tipos de células etiquetados del estudio inicial, en contraste con un UMAP coloreado por las predicciones de scDeepInsight. (De Jia et al. [ 21 ] bajo licencia creative commons).
scDeepInsight revoluciona la anotación de tipos de células al aplicar la metodología de transformación de tabla a imagen a los datos de scRNA-seq. Esta representación transformada, combinada con la fuerza analítica de las CNN, facilita la identificación precisa y robusta de los tipos de células. En lugar de depender únicamente de marcadores conocidos, el modelo aprovecha todo el perfil transcriptómico de las células individuales, lo que ofrece una clasificación más completa. Esto se logra entrenando scDeepInsight en un conjunto de datos de referencia e identificando los tipos de células para los conjuntos de datos de consulta. La mejora del rendimiento observada fue de más del 7 % en comparación con otros métodos de la competencia.
Descubriendo nuevos tipos de células
Una de las facetas más prometedoras de scDeepInsight es su potencial para descubrir tipos de células poco comunes o no descubiertos anteriormente. Al transformar los datos de scRNA-seq en un panorama visual, se destacan los grupos que podrían pasarse por alto o fusionarse en los análisis tradicionales. Estos grupos únicos representan posibles nuevos tipos de células o estados de transición, lo que mejora nuestra comprensión de la biología de los tejidos, los procesos de desarrollo y los mecanismos de las enfermedades.
Identificación de genes marcadores
Los genes marcadores desempeñan un papel fundamental en la identificación de los tipos de células, ya que ofrecen información biológica sobre la función y la naturaleza de las distintas poblaciones celulares. Además de la clasificación, scDeepInsight también ayuda a identificar estos genes marcadores. Al aplicar ingeniería inversa a la representación en forma de imagen y vincularla con los datos genómicos, se pueden identificar genes que se expresan de forma específica en tipos de células específicos. Esto no solo consolida la identificación, sino que también proporciona una base para ensayos funcionales, orientación terapéutica y otras investigaciones biológicas.
En esencia, scDeepInsight amplifica el poder de la secuenciación de ARN de células individuales, brindando herramientas no solo para la identificación sino también para el descubrimiento. A medida que el mundo de la genómica avanza hacia una mayor resolución, herramientas como scDeepInsight serán fundamentales para garantizar que aprovechemos al máximo el potencial de los datos, lo que hará avanzar tanto la ciencia como la medicina
Conclusiones y perspectivas futuras
A medida que los límites de la genómica continúan expandiéndose, nuestras estrategias analíticas deben evolucionar al mismo tiempo. DeepInsight y sus derivados representan un salto monumental en esta progresión. Fusionan los mundos del análisis de datos basados en imágenes con los datos ómicos, lo que facilita interpretaciones matizadas que antes eran difíciles de lograr:
- 1.Redefiniendo la interpretación de datos ómicos: La transformación de datos ómicos en representaciones similares a imágenes a través de DeepInsight o tecnología similar ha ampliado sin duda nuestras capacidades analíticas y nuestra solidez al capturar estructuras y coherencias latentes detrás de los datos, por ejemplo, los datos ómicos. Su adaptabilidad, como se ve en su fusión con diversas metodologías, resalta el potencial dinámico de la técnica.
- 2.Integración multiómica holística: la aparición de modelos integradores pone de relieve la creciente necesidad de enfoques más integrales en el campo de la genómica. Dado que la dependencia de datos ómicos únicos puede llegar a ser limitada, en el futuro podríamos ver una mayor dependencia de herramientas como DeepInsight y sus derivados, por ejemplo, DeepInsight-3D, para proporcionar una perspectiva holística de los sistemas biológicos. Sus aplicaciones, especialmente en campos como la predicción de la respuesta a fármacos contra el cáncer, subrayan su posible relevancia clínica.
- 3.Descifrando la heterogeneidad celular: los análisis de células individuales, impulsados por herramientas como scDeepInsight, han transformado nuestra comprensión de los paisajes celulares. El descubrimiento de nuevos tipos de células y genes marcadores subraya su potencial para contribuir enormemente a la biología celular.Si bien la fusión de la conversión de tablas a imágenes con CNN para el análisis ómico ha impulsado avances significativos, aún existe un panorama de desafíos que requieren solución:
- 4.Interpretabilidad y relevancia biológica: la naturaleza de “caja negra” de los modelos de aprendizaje automático, incluidas las redes neuronales convolucionales, ha llevado al surgimiento de técnicas como las CAM y DeepFeature. Si bien estas herramientas son prometedoras, garantizar la interpretabilidad y preservar la relevancia biológica de las representaciones de datos son desafíos primordiales.
- 5.Desafíos de los datos, complejidad del modelo y sobreajuste: los datos ómicos son intrínsecamente heterogéneos y abarcan información como datos genómicos, epigenómicos, transcriptómicos, proteómicos y metabolómicos. La adaptación de estos diversos tipos de datos y el manejo de problemas de escalabilidad, tamaño y sobreajuste de los datos son preocupaciones importantes. Lograr un equilibrio entre la complejidad del modelo, la capacidad y los datos disponibles es esencial para evitar el sobreajuste, especialmente cuando se trabaja con datos ómicos de alta dimensión.
- 6.Desafíos técnicos: Es necesario abordar cuestiones como el ajuste de hiperparámetros, las limitaciones de recursos computacionales y la generalización del modelo en diferentes condiciones y plataformas.
- 7.Integración y evaluación comparativa: incorporar conocimientos específicos del dominio en el entrenamiento del modelo y realizar una evaluación comparativa rigurosa frente a métodos establecidos es crucial para evaluar el verdadero potencial de un modelo.
- 8.Horizontes futuros: La confluencia de la DL y la biología, tal como se manifiesta en estas metodologías, probablemente se intensificará en los próximos años. Podemos imaginar un futuro en el que la transformación y el análisis de datos ómicos en tiempo real se conviertan en estándar en los entornos clínicos, agilizando las decisiones diagnósticas y terapéuticas. Además, se prevé la aparición de modelos aún más robustos, adaptables a una amplia gama de tipos de datos ómicos.
- 9.Hacia una medicina personalizada: la culminación de estos avances apunta a personalizar las intervenciones médicas para cada individuo. Aprovechando los conocimientos de los conversores de imágenes tabulares y las redes neuronales convolucionales entrenadas en grandes conjuntos de datos, nos acercamos a la realización de una medicina verdaderamente personalizada. Ya sea que se trate de respuestas a medicamentos, descubrimiento de mecanismos moleculares o identificación de nuevos estados celulares, estas herramientas son prometedoras para diseñar tratamientos adaptados al mapa genético de cada individuo.
Los desafíos, como los que se enumeran arriba, subrayan la importancia de la colaboración interdisciplinaria entre expertos en aprendizaje automático, profesionales de la bioinformática, biólogos, investigadores médicos y médicos, y pacientes. Estas colaboraciones serán fundamentales para el avance de los modelos de aprendizaje automático y la ampliación de los horizontes del análisis de datos ómicos.
En conclusión, ahora que nos encontramos en el umbral de esta revolución analítica en genómica, es imperativo adoptar estas nuevas metodologías. Su potencial para revolucionar nuestra comprensión de la biología, combinado con sus profundas implicaciones clínicas, consolida su papel como instrumentos indispensables en nuestro esfuerzo por descifrar las complejidades de la vida.
El uso de la virtualidad en la enseñanza médica de grado y postgrado
Cara a cara: la perspectiva de un neurólogo sobre la teleeducación
Matthew W. Schelke, M.D.
A estas alturas, el inicio de cualquier conferencia de Zoom es predecible. Los micrófonos se silencian rápidamente, las cámaras se apagan y un presentador solitario habla con un mar de nombres.
Incluso si los estudiantes están (en su mayoría) escuchando, pensando y procesando, ¿es realmente lo mismo para sus cerebros que la alternativa en persona?
El cambio masivo a las videoconferencias desde el inicio de la pandemia de Covid-19 ha transformado la experiencia educativa de los estudiantes y pasantes de medicina.
Al comienzo de la pandemia, yo era residente de neurología de tercer año y tengo buenos recuerdos del estado de la educación antes de ese momento. Los educadores, los aprendices y los estudiantes siempre se reunían en persona, ya sea para conferencias, conferencias de casos o grandes rondas.
Examinamos a los pacientes con condiciones interesantes como grupo; Los breves comentarios e interacciones condujeron a ideas memorables. La educación médica ha recuperado algunas de estas tradiciones y experiencias, pero no todas.
La mayoría de las sesiones de video en educación médica hoy en día son conferencias y discusiones, que teóricamente incluyen las mismas diapositivas de PowerPoint y puntos de aprendizaje que sus versiones presenciales. Pero ahora que soy tratante y educadora-clínica, me pregunto si los aprendices y los estudiantes aprenden el mismo material a través de video, incluso si el contenido presentado es idéntico. Y como neurólogo, también me pregunto si nuestros cerebros podrían aprender el mismo material por medio de un medio completamente virtual, y creo que la respuesta es no.
La enseñanza y el aprendizaje son actividades fundamentales para el desarrollo humano.
Los psicólogos cognitivos Gergely Csibra y György Gergely han afirmado que una de las ventajas evolutivas más importantes de los seres humanos es la capacidad de la «pedagogía natural»: compartir el conocimiento por el hecho de compartir el conocimiento.1
El cerebro humano tiene redes neuronales que gobiernan el lenguaje y la imitación (el «sistema de neuronas espejo») y regiones de asociación sensorial ampliadas que codifican la identidad y la función de objetos específicos que percibimos.
Juntos, estos sistemas permiten a los seres humanos compartir conocimientos y habilidades con otros; Sin ellos, no podríamos empezar a aprender qué hace el cerebelo o cómo calcular una puntuación en una escala de trazos.
Según Csibra y Gergely, la efectividad del aprendizaje depende de «señales ostensivas», o principalmente señales no verbales que nos dicen: «¡Presta atención a esto!» La mayoría de estas señales no verbales se procesan rápidamente, y a menudo de forma inconsciente, durante las interacciones en persona: una leve sonrisa, un cambio de postura o un momento de contacto visual, por ejemplo.
Como puede atestiguar cualquier residente, no hay fuerza didáctica más poderosa que la mirada penetrante de un asistente mayor.
La teleeducación limita la transmisión de este tipo de señales, incluso si las cámaras permanecen encendidas. Las expresiones faciales rápidas, «microexpresiones» que duran menos de medio segundo, se transmiten mal a través de video. La postura es casi imposible de ver, por lo que se pierden cambios sutiles pero importantes, como una persona que se inclina hacia adelante o se sienta más recta. Incluso si las señales ostensivas son capturadas por la cámara de un participante, las transmisiones de video ligeramente retrasadas pueden impedir que coincidan perfectamente con el contenido de audio, lo que puede ser una distracción.
Las fuentes de audio también limitan la transmisión de los cambios prosódicos sutiles que señalan la importancia de palabras o frases particulares. Desde un punto de vista neurológico, las señales ostensivas pueden ser esenciales para ayudar a las personas a comprender lo que los demás están haciendo y diciendo.
La red cerebral que controla la percepción de la mirada, el lenguaje corporal y las señales prosódicas comienza en el lóbulo temporal especializado y las regiones límbicas y se proyecta hacia la corteza prefrontal medial.2
La corteza prefrontal medial envía aferencias a varias otras regiones corticales, y se propone que este control «de arriba hacia abajo» mejora el procesamiento sensoriomotor del habla, acciones, metas, y la atención de otras personas.3 En otras palabras, la corteza prefrontal medial es el vínculo clave entre las interacciones sociales y la mejora del aprendizaje. Como un ejemplo extremo de la importancia de la participación de la corteza prefrontal medial, las lesiones graves en esta parte del cerebro pueden causar mutismo acinético. Como su nombre indica, los pacientes con esta afección son incapaces de hablar o actuar, permaneciendo inmunes a los estímulos sociales.
Un paciente del neuropsicólogo Alexander Luria llegó a informar (después de cierta recuperación) que «los pensamientos no entraban en mi cabeza». 4
El deterioro de la señalización ostensiva durante las videoconferencias es mucho menos grave, pero la amortiguación de estas redes significa que los circuitos de arriba hacia abajo que mejoran el aprendizaje no están completamente activos. La señalización ostensiva es multidireccional. Durante las clases tradicionales, los estudiantes reciben señales ostensivas de los maestros, pero los maestros también reciben señales de los estudiantes que indican si los estudiantes están siguiendo la conferencia o tienen una pregunta. Muchos profesores han experimentado alienación (o alivio) al hablar a través de Zoom que se deriva de la falta de señalización en vivo de los estudiantes. Además, en las discusiones grupales, como las conferencias de casos, la capacidad de beneficiarse de perspectivas ricas e interactivas se basa en la señalización ostensiva entre todos los presentes: entre el moderador y los participantes, pero también entre los propios participantes. Tales conexiones son imposibles de replicar virtualmente con las tecnologías disponibles actualmente. No obstante, en determinadas situaciones, la teleeducación puede aumentar el aprendizaje tradicional. Por ejemplo, las conferencias que antes solo estaban disponibles para un pequeño grupo de aprendices en una sola institución ahora se pueden compartir a nivel mundial, y la popularidad de los videos educativos médicos en línea da fe de su eficacia en la democratización del conocimiento. Este alcance también puede mejorar algunos de los aspectos no cognitivos de la educación, en particular la exposición de los estudiantes y aprendices a una variedad de enfoques culturales y sociales de la atención médica. Pero hay límites en el tipo de información que se puede transmitir con éxito a través de video. Muchos videos en línea se enfocan en hechos discretos y a menudo comprobables en lugar de la compleja toma de decisiones involucrada en la atención clínica. Aunque los hechos son importantes, el desarrollo del juicio clínico y el razonamiento es crucial para la educación de cualquier aprendiz y se facilita mucho mejor con las discusiones en persona. A pesar de sus limitaciones, la videoconferencia es ahora una parte ineludible de la vida moderna. Entonces, ¿qué podemos hacer los educadores médicos para mejorar nuestras sesiones de enseñanza? Más allá de la respuesta obvia —brindar más oportunidades para las interacciones cara a cara— hay algunas intervenciones que pueden mejorar el aprendizaje virtual. En primer lugar, es posible que los profesores tengan que compensar en exceso las limitaciones del medio cuando presentan material en vídeo. Un mayor énfasis en los puntos clave y una inflexión vocal más dramática pueden ayudar a compensar las reducciones en la señalización ostensiva durante las interacciones basadas en Internet. Muchas pistas, como las microexpresiones, dependen de la resolución de las transmisiones audiovisuales, por lo que es importante tener una buena cámara y micrófono.
En segundo lugar, durante las sesiones virtuales, los educadores pueden centrarse en el aprendizaje de doble canal, en el que las imágenes desempeñan un papel crucial en las palabras de apoyo. En lugar de depender principalmente del texto, los educadores pueden desarrollar imágenes impactantes, que (cuando son efectivas) también pueden sustituir algunas señales ostensivas. Pero probablemente la mejor opción es realizar al menos algunas sesiones, particularmente la primera sesión de un curso o programa, en persona. Muchas señales ostensivas se reciben y se recuerdan subconscientemente5 ;
Si un estudiante asiste a una clase basada en video después de haber conocido al profesor y a sus compañeros en persona, su cerebro infiere algunas pistas sobre la base de los recuerdos de las interacciones cara a cara.
Muchas personas se sorprenden por los aparentes cambios de personalidad en los demás cuando los conocen en persona por primera vez después de haberlos visto solo por video. Gran parte de esta reacción se deriva de la escasez de señales ostensivas asociadas subconscientemente con esas personas.
La importancia de las vías neuronales que conectan las señales ostensivas con la corteza prefrontal medial es una de las razones por las que la teleeducación puede ser inadecuada.
Sin embargo, al igual que con cualquier otra tecnología, los educadores pueden guiar el uso de la teleeducación: la desconexión no es toda la historia, y hay formas de mejorar y aprovechar las herramientas basadas en video.
Pero como especie con un cerebro adaptado para las interacciones cara a cara, los humanos necesitan en última instancia una pedagogía cara a cara.
LA EPIDEMIA DE DENGUE Y LA PROCURACIÓN DE ÓRGANOS PARA TRASPLANTE. DOS REALIDADES QUE NOS DESAFÍAN
Laura Barcán, Julián Bibolioni, Rocío Gago, Patricia Giorgio, Melisa Martínez Ríos, Natalia Pujato, Claudia Salgueira, Astrid Smud, Elena Temporiti y Silvina Villamandos (Comisión de Infecciones en Transpalante de Órganos Sólidos, SADI).
Fundación Huésped – Sociedad Argentina de Infectología Gianantonio, Carlos Dr. (ex Pje. Peluffo) 3932 (C1202ABB), Ciudad Autónoma de Buenos Aires (CABA), Argentina redaccion.asei@huesped.org.ar
ISSN 2718-7845
Varios factores han contribuido a que el dengue sea la principal arbovirosis a nivel mundial, con aproximadamente 3,9 mil millones de personas expuestas en más de 120 países. La adaptación del vector vinculada al clima, la urbanización, las condiciones de vida, las acciones de control de vectores y el aumento del movimiento de personas son algunos de los factores que destacan Echazarreta y Couto en uno de los editoriales del número 114 de ASEI.
En la Argentina se describen casos autóctonos desde 2006, y en 2023 se constató por primera vez la continuidad de la transmisión autóctona durante el periodo invernal. En el transcurso de 2024, hasta la semana epidemiológica 24 se han notificado 498.091 casos de dengue, con una incidencia acumulada de 708 casos por cada cien mil habitantes (Boletín Epidemiológico Nacional, Ministerio de Salud 2024).
En este escenario, la procuración de órganos para trasplante se convierte en un desafío, no solo para quienes trabajan en la atención de pacientes, sino también para la sociedad en su conjunto. Y si bien en lo que va de 2024 se realizaron ya 719 trasplantes, todavía queda un largo camino por recorrer, dado que la cantidad de personas que necesitan de un órgano es 7141, casi diez veces más, de acuerdo con los datos del INCUCAI.
En ese contexto, este documento, redactado por la Comisión de Infecciones en Trasplante de Órganos Sólidos de la Sociedad Argentina de Infectología, intenta arrojar luz sobre estas dos realidades que, hoy en día, en cierto modo se superponen. El objetivo es por un lado llamar la atención acerca del potencial riesgo de transmisión del dengue de los donantes a los receptores de un trasplante de órgano sólido y, por otro, continuar la lucha para que la procuración de órganos no se detenga.
Consideramos que es un importante aporte, principalmente para quienes tienen la responsabilidad de evaluar a potenciales donantes y receptores de órganos en la situación epidemiológica actual.
María Belén Bouzas y Lautaro de Vedia Secretaría de redacción, Revista ASEI 4
5 Suplemento II: Documento de posición: recomendaciones sobre dengue en la procuración de órganos Actual. Sida Infectol., Agosto 2024 – Noviembre 2024; 32 (115) Suplemento I: 1-10,
INTRODUCCIÓN
El dengue es una enfermedad viral que puede ocurrir en forma endémica o epidémica. Es transmitido por la picadura de mosquitos del género Aedes. El agente causal es un virus de la familia Flaviviridae, del cual se reconocen cuatro serotipos: DEN 1, DEN 2, DEN 3 y DEN 4.
En nuestro país, hasta la SE 15/2024 (abril/2024) se registraron 469.272 casos de dengue, de los cuales 91% corresponden a casos autóctonos, 7% se encuentran en investigación y 2% presentan antecedentes de viaje (importados). Los casos acumulados hasta la SE15 representan 3,17 veces más que lo registrado en el mismo período de la temporada anterior (2022/2023) y 9,1 veces más que lo registrado en el mismo período de 2019/2020. Desde la semana epidemiológica 31/2023 a la 15/2024, la Argentina registró más de 333.084 casos, con 762 casos graves y 238 fallecidos. A la vez, se detectó que circulan tres serotipos en el país, el DEN 1, DEN 2 y DEN 3. Las áreas principales son la región del centro, todo el NEA y NOA.
PRESENTACIÓN
La enfermedad puede causar cuadros asintomáticos o manifestarse como enfermedad febril autolimitada, fiebre hemorrágica o síndrome de shock. Presenta un periodo de incubación de 3-15 días, la viremia suele ser de 4 a 7 días (mediana de 5 días) pero puede persistir hasta 21 días en inmunocomprometidos. La infección primaria a menudo es asintomática o se presenta como una enfermedad febril leve.
Se caracteriza por un cuadro de fiebre elevada de comienzo agudo,sin síntomasrespiratorios, con cefalea, dolor retroocular, mialgias, artralgias, vómitos, diarrea, exantema, rash eritemato-maculopapular leve, petequias u otras manifestaciones hemorrágicas. Laduración habitual del cuadro febril es menor de 7 días.
En el laboratorio se encuentra leucopenia en el 50 a 90% de los casos, con neutropenia, linfocitosis y linfocitos atípicos, plaquetopenia, hemoconcentración y leve alteración de enzimas hepáticas.
Las formas graves comienzan con un cuadro clínico de dengue clásico, pero alrededor del cuarto al séptimo día (período en el cual el paciente deja de tener fiebre) aparece hipotensión, hipotermia, manifestaciones hemorrágicas y aumento de la permeabilidad capilar, con la consecuente hemoconcentración. También aparecen plaquetopenia severa e hipoproteinemia.
El cuadro puede progresar hacia el shock y muerte. El tratamiento de soporte precoz puede reducir la mortalidad a menos del 1%.
Hay formas menos frecuentes de dengue grave producidas por la afectación directa del virus en un órgano (miocarditis, hepatitis, etc.).
Los receptores de trasplante generalmente adquieren la enfermedad por vectores durante viajes o al habitar en áreas endémicas. Después de un período de incubación, la enfermedad sepresenta abruptamente como una en trifásica: febril, crítica y de recuperación.
CUADRO CLÍNICO
Las tres fases no son claramente distinguibles en pacientes trasplantados, en quienes la duración de los síntomas es más larga y la trombocitopenia está presente en el 80% de los casos.
Hay reportes de presentaciones atípicas que incluyen colitis aguda y encefalitis. También se ha descripto síndrome hemofagocítico secundario. La mortalidad global reportada en este grupo de pacientes es del 16% (entre 0-38%), frente al 3,7 % de la población general.
En general se considera que el cuadro clínico y la evolución son muy similares a los que se producen en huéspedes sanos. Si bien se documentó un aumento de la creatinina durante el episodio febril, en receptores de trasplante renal debido a la depleción de volumen intravascular, esta cifra vuelve a los valores previos con la mejoría del cuadro. La mayoría de los casos notificados de dengue después del trasplante han culminado en la supervivencia del injerto y del paciente.
DIAGNÓSTICO
En la fase aguda (virémica) se utilizan pruebas de detección genómica (PCR) y detección del antígeno NS1. Estos métodos detectan viremia, pero es posible, sin embargo, que el virus persista en el tejido después de la eliminación de la sangre. Por esta razón, el screening de laboratorio no reemplaza totalmente la evaluación epidemiológica para una infección reciente por arbovirus.
Después de la fase virémica de la infección, la serología es el método de elección para diagnóstico. Los niveles de IgM alcanzan su punto máximo aproximadamente dos semanas después del inicio de los síntomas, y luego declinan a niveles indetectables en dos a tres meses.
TRATAMIENTO
No existe un fármaco antiviral específico para tratar el dengue. La reposición abundante de líquidos es el pilar de la terapia. Actualmente, no hay suficiente evidencia para recomendar disminuir o cambiar los regímenes de inmunosupresión. Existe un riesgo potencial de transmisión del dengue de los donantes a los receptores de un trasplante de órgano sólido. Hay escasos reportes de trasmisión de dengue por el órgano. En los casos de transmisión por injerto,
los síntomas del dengue suelen comenzar en los primeros diez días después del trasplante.
Frecuentemente se presentan con fiebre, trombocitopenia y dolor abdominal. En algunos casos se presenta bajo la forma de dengue hemorrágico con riesgo de afectación del injerto y muerte, y en otros como cuadros febriles más leves sin compromiso del injerto. Es por esto que debemos estar alerta a los síntomas del donante y realizar una anamnesis completa para la búsqueda de antecedentes de dengue de este y/o su círculo social para reforzar la sospechas diagnósticas.
Las pruebas de rutina de serología de dengue en donantes no se practican como parte del estudio pretrasplante.
En los donantes fallecidos provenientes de áreas no endémicas debe evaluarse el riesgo de exposición a arbovirus mediante la detección de viajes recientes.
Los potenciales donantes que provengan de zonas epidémicas o endémicas de dengue deberían ser testeados con prueba de antígeno dengue NS1 o pruebas de detección genómica (PCR), de estar disponibles, a fin de detectar viremia, y con IgM si pasaron más de cinco días del comienzo de un cuadro compatible.
Si el donante tiene positivo el NS1 o la deteccion genómica por PCR esdetectable, debe descartarse como donante.
En caso de IgM positiva, si se desconoce el tiempo de inicio de los síntomas o elmismo es menor a 30 días, también se deberá descartar. Si el donante tiene IgM positiva, pero con antecedente de diagnóstico hace más de 30 días, se desaconseja donarórganos hasta que se disponga de más información de seguridad (durante el brote enArgentina 2023-2024, nuestra comisión ha detectado trasmisiones posibles a receptres de donantes con dengue entre 2-3 meses previos). En acuerdo con INCUCAI, en el caso de requerimiento de trasplante de órgano por emergencia y si solo se dispusiera de un donante con NS1 o PCR para dengue negativos e IgM positiva, sin antecedentes recientes de infección o vacunación, podría disponerse del órgano con consentimiento informado del receptor.
En caso de no poder realizar dichos testeos, los órganos podrán ser distribuidos con el debido consentimiento informado al receptor.
Los órganos de potenciales donantes que provengan de zonas epidémicas con diagnóstico confirmado o sospechoso de dengue, zika o chikungunya dentro de los 30 días deben descartarse.
Los órganos de donantes con diagnóstico confirmado o sospechado de arbovirus
pueden ser considerados para trasplante después de un periodo mínimo de 30 días.
Se recomienda obtener y guardar suero de donantes provenientes de zonas de alto riesgo para dengue a fin de realizar serología ante la aparición de signos/síntomas sugestivos de esta enfermedad en el receptor.
En los donantes vivos provenientes de áreas no endémicas puede evaluarse el riesgo de
exposición mediante la detección de viajes recientes.
Se debe educar a los donantes vivos para evitar infecciones previas a la donación.
En los donantes de regiones endémicas debe diferirse si tienen antecedentes recientes de una enfermedad febril sugestiva de infección activa por arbovirus, particularmente dentro de los 30 días.
En caso de donantes vivos que se hayan aplicado recientemente vacuna contra dengue a virus atenuado, se deberá esperar al menos 30 días desde el momento de la aplicación para proceder con el trasplante.
Se recomienda obtener y guardar suero de donantes provenientes de zonas de alto riesgo para dengue a fin de realizar serología ante la aparición de signos/síntomas sugestivos de esta enfermedad en el receptor.
RECOMENDACIONES PARA CANDIDATOS A RECEPTORES DE ÓRGANOS
El receptor puede decidir recibir bajo consentimiento informado un órgano de un potencial donante que provenga de zona endémica cuando no se dispone de testeo con prueba de antígeno dengue NS1 o PCR a fin de detectar viremia.
El receptor debe realizar consulta inmediata ante fiebre de causa inexplicada posteriora la recepción de un órgano de donante con potencial exposición en área endémica.
De haber recibido la vacuna contra el dengue, deberá esperar al menos 30 días para el trasplante, por ser una vacuna a virus vivos atenuados.
Si un paciente está cursando un fallo de órgano ocasionado por dengue que compromete su vida y no ha respondido en un tiempo prudencial a medidas de sostén y se propone trasplante de urgencia, debe procederse sin restricción.
RECOMENDACIONES GENERALES
Control focal en viviendas:
Identificar y controlar todos los criaderos existentes en el interior del domicilio y peridomicilio (patios, jardines y techos): eliminar recipientes en desuso que pueden acumular agua y todos los reservorios de agua donde pueden proliferar los mosquitos.
Larvas y huevos pueden sobrevivir un año en aguas estancadas.
Para aquellos recipientes que no puedan ser eliminados: tapar, cubrir, voltear y limpiarlos con regularidad.
•
Mantener patios y jardines desmalezados para prevenir la presencia de mosquitos
adultos.
•
Prevención de picaduras: si no se puede evitar la exposición (pacientes residentes en
áreas endémicas/epidémicas):
•
Utilizar ropa de mangas y piernas largas de colores claros.
Evitar exposición al aire libre al amanecer y al atardecer.
Utilizar repelente con DEET al 25-30% (OFF® verde) y renovarlo cada 4 a 6 horas.
La vacuna disponible en la Argentina en 2024 es de virus vivos atenuados (Qdenga®)
(dos dosis con tres meses de diferencia), y está contraindicada en trasplantados y otras
situaciones de inmunosupresión. En un candidato a trasplante que se vacune debe
aguardarse 30 días desde la última dosis antes de trasplantarse.
Impacto de la infección previa por dengue en la gravedad y los resultados: metaanálisis de ensayos controlados con placebo
Alejandro Macchia 1, ✉ , Silvana Figar 2 , Cristián Biscayart 3 , Fernán González Bernaldo de Quirós 4
Nota del blog «El dengue ya es endémico en Argentina, ya está entre nosotros, se esta realizando una campaña de vinculación muy lenta, que será sobrepasada por la transmisión del virus en pocas semanas. Donde nuevamente explotarán de demanda nuestras guardia. Haremos diagnóstico de síndrome gripal sin catarro dolor muscular, plaquetas y sin serotipar. Manejándonos como el siglo pasado. No vacunando en la provincia a quienes no hayan tenido dengue, cuya evidencia es débil. De esta forma, con estas estrategias la vacunación no va a doblegar la epidemia de dengue».
Este estudio evaluó la asociación entre la infección previa por dengue confirmada serológicamente y el riesgo posterior de dengue confirmado virológicamente, dengue grave, hospitalización por dengue, muerte relacionada con el dengue y mortalidad por todas las causas.
Métodos.
Se realizó una revisión sistemática y un metanálisis siguiendo las pautas PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses). Se realizaron búsquedas en PubMed, CINAHL, MEDLINE, Cochrane Library y Web of Science para encontrar informes de ensayos controlados aleatorizados de fase III sobre la eficacia de la vacuna que tuvieran datos sobre el grupo placebo e información sobre infecciones previas y que se publicaron entre enero de 1994 y marzo de 2024. Se utilizaron modelos de efectos aleatorios para calcular los odds ratios (OR) combinados y se evaluó la heterogeneidad.
Resultados.
Se incluyeron cuatro estudios de tres ensayos de fase III. Los participantes con infección previa tuvieron una menor probabilidad de desarrollar dengue confirmado virológicamente durante el seguimiento (OR: 0,85, intervalo de confianza [IC] del 95%: 0,75 a 0,98, P = 0,024) y el mismo riesgo de hospitalización por dengue que aquellos sin infección previa (OR: 1,18, IC del 95%: 0,92 a 1,53, P = 0,198). Sin embargo, tuvieron una tasa más alta de dengue grave (OR: 2,91, IC del 95%: 1,23 a 6,87, P = 0,015). No se produjeron muertes relacionadas con el dengue durante el seguimiento. No hubo diferencias estadísticamente significativas en la mortalidad por todas las causas entre los individuos con y sin dengue previo (OR: 1,74, IC del 95%: 0,21 a 14,08, P = 0,76).
Conclusiones.
La infección previa por dengue redujo significativamente el riesgo de dengue confirmado virológicamente y aumentó el riesgo de dengue grave, pero no tuvo un efecto significativo en la hospitalización por dengue, la muerte relacionada con el dengue o la mortalidad por todas las causas durante el seguimiento. Estos hallazgos sugieren la necesidad de reconsiderar la infección previa como un factor de riesgo independiente.
Palabras clave: Dengue, dengue grave, vacunas contra el dengue, metanálisis
En el contexto de la creciente incidencia y prevalencia del dengue ( 1 , 2 ), varios estudios han analizado los factores relacionados con las infecciones graves ( 3 ). Entre estos, una segunda infección por dengue se ha identificado como un factor de riesgo significativo para el dengue grave en algunos estudios. Una revisión ( 3 ) que examinó 22 estudios encontró que tener una segunda infección por dengue se asoció con un riesgo significativamente mayor de dengue grave (odds ratio [OR]: 2,69, intervalo de confianza del 95% [IC]: 2,08 a 3,48). Estos resultados son materialmente similares a otra revisión sistemática de estudios observacionales que encontró un riesgo asociado de 1,75 (IC del 95%: 1,26 a 2,42) ( 4 ). Sin embargo, un estudio prospectivo realizado en Perú ( 5 ) que investigó el papel de las segundas infecciones por dengue en el contexto del genotipo americano del virus del dengue (es decir, DENV-2) concluyó que a pesar de la alta prevalencia de segundas infecciones por dengue, no se asociaron con un mayor riesgo de dengue grave. Esto sugiere que el genotipo americano DENV-2 podría no tener las características necesarias para inducir formas graves de la enfermedad. Otro estudio ( 6 ) examinó cómo las infecciones previas con diferentes serotipos del virus del dengue afectaron el riesgo y la gravedad de las infecciones posteriores, y encontró que la presencia de anticuerpos heterotípicos preexistentes redujo significativamente el riesgo de dengue grave en infecciones posteriores ( 6 ).
Aunque las revisiones narrativas ( 7 ) enfatizan una segunda infección como un factor predisponente para el dengue grave y la hospitalización por dengue, no todos los hallazgos son consistentes ( 3–6 ). Las razones de estas discrepancias son numerosas, pero los sesgos inherentes al uso de cohortes de estudios no controlados y el sesgo de recuerdo en pacientes con dengue grave pueden contribuir.
La aparición de ensayos controlados aleatorizados (ECA) que examinan la eficacia de diversas vacunas para prevenir el dengue confirmado virológicamente (DCV), el dengue grave, la hospitalización por dengue y la muerte relacionada con el dengue brinda una oportunidad para estudiar este tema mediante el examen de mejores evidencias. A diferencia de los estudios retrospectivos de casos y controles, los ensayos clínicos cuentan con una estrecha vigilancia prospectiva y documentación de los eventos, lo que los hace menos propensos al sesgo de observación.
Este estudio investigó el papel de las segundas infecciones por dengue en la aparición de DCV, dengue grave, hospitalización por dengue, muerte relacionada con el dengue y mortalidad por todas las causas.
MÉTODOS
Estrategia de búsqueda
Para este metanálisis se utilizaron las directrices PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses). Esta revisión implicó varias etapas: definición de palabras clave, búsqueda de artículos en bases de datos, evaluación crítica de los estudios, selección y análisis de los datos e interpretación de los resultados. El protocolo de investigación está registrado en PROSPERO (número 542370), el registro prospectivo internacional de revisiones sistemáticas. Se realizaron búsquedas en PubMed, CINAHL, MEDLINE, la Biblioteca Cochrane y la Web of Science de artículos publicados entre enero de 1994 y marzo de 2024 (la información sobre la estrategia de búsqueda está disponible a través del autor correspondiente). Además, se realizaron búsquedas manuales, incluido el escaneo de listas de referencias, para identificar artículos que podrían no haberse recuperado con la estrategia de búsqueda inicial.
Criterios de selección y elegibilidad de estudios
Dos investigadores (AM, CB) evaluaron el título y el resumen de todos los artículos para determinar los criterios de elegibilidad para la población estudiada, la intervención, las comparaciones y el diseño del estudio. Se obtuvo el texto completo de todos los estudios potencialmente elegibles y dos investigadores (AM, FQ) evaluaron su elegibilidad para su inclusión en el metanálisis. Cualquier desacuerdo se resolvió mediante discusión. Las razones para excluir algunos ensayos clínicos y el proceso de selección se registraron utilizando el diagrama de flujo PRISMA ( Figura 1 ).

Criterios de inclusión
Los estudios eran elegibles para su inclusión si eran artículos de investigación originales revisados por pares escritos en inglés que examinaban la inmunogenicidad, seguridad o eficacia de varias vacunas contra el dengue y se publicaban dentro del plazo especificado. Solo se incluyeron los estudios finales sobre cada vacuna para eliminar la duplicación. Solo se incluyeron los estudios que informaron el número de participantes con infección previa documentada en el grupo placebo o de control.
Criterios de exclusión
Se excluyeron los estudios si no estaban escritos en inglés y no eran ECA de fase III o si carecían de un grupo de control o placebo.
Extracción de datos
Dos autores (SF, CB) extrajeron datos de los estudios incluidos y verificaron su exactitud. Mediante una hoja de extracción de datos estandarizada, se extrajo la siguiente información de los estudios: dónde se registró el protocolo del estudio; características demográficas de los participantes del estudio; infección por dengue preexistente y documentada; grupo de tratamiento; región y país donde se realizó el estudio; duración del seguimiento; y datos de los resultados.
Riesgo de sesgo
El riesgo de sesgo en cada ensayo aleatorizado se evaluó utilizando la herramienta Risk of Bias 2 desarrollada por la Colaboración Cochrane. Los cinco dominios de sesgo considerados en esta herramienta son el sesgo que surge del proceso de aleatorización, debido a la desviación de las intervenciones previstas, debido a la falta de datos de resultados, en la medición del resultado y en la selección de los resultados informados.
Síntesis de datos
Se recogieron los datos necesarios de cada ensayo clínico para estimar el riesgo y el intervalo de confianza del 95% de infección por dengue/100 000 personas-año. Para cada estudio, se registraron los números totales de participantes, infecciones por dengue, casos de dengue grave, hospitalizaciones por dengue y muertes por todas las causas y muertes relacionadas con el dengue. También se registró el número de años de seguimiento en cada estudio.
Se calculó el riesgo de cada resultado por cada 100 000 personas-año para cada estudio. El riesgo se calculó dividiendo el número total de infecciones por el producto del número total de participantes multiplicado por el período de seguimiento, y luego multiplicando este resultado por 100 000. La probabilidad de cada resultado individual se calculó dividiendo el número total de eventos por el producto del número total de participantes multiplicado por el período de seguimiento. Los intervalos de confianza del 95% para los riesgos se determinaron calculando primero el error estándar de una proporción. Luego, se multiplicó 1,96 por el error estándar y se restó este valor de la estimación del riesgo para determinar el límite inferior; luego se agregó esta misma cantidad a la estimación del riesgo para determinar el límite superior. Luego, los valores finales se multiplicaron por 100 000 para expresar el riesgo por cada 100 000 personas-año. Después de estimar el riesgo y los intervalos de confianza del 95% para cada estudio, se calculó el riesgo ponderado general en todos los estudios. Para obtener el riesgo general, se calcularon los pesos de cada estudio basándose en la inversa de la varianza (es decir, el cuadrado del error estándar) de las estimaciones de riesgo del estudio. Luego, se calculó el riesgo ponderado general sumando los productos del peso y el riesgo de cada estudio y dividiendo este resultado por la suma de los pesos. El error estándar global se obtuvo tomando la raíz cuadrada de la inversa de la suma de los pesos.
Se realizaron metanálisis separados para cada uno de los resultados de interés, identificados como DCV, dengue grave, hospitalización por dengue, mortalidad general y muerte relacionada con dengue, utilizando el método de efectos aleatorios de varianza inversa para calcular la razón de probabilidades (OR) combinada para cada estudio. Cada metanálisis se presenta como un diagrama de bosque, que muestra las estimaciones centrales junto con sus intervalos de confianza del 95%. Para evaluar la heterogeneidad entre los estudios incluidos en cada metanálisis, se utilizó la estadística I² . La estadística I² mide el porcentaje de variación total entre los estudios que se debe a la heterogeneidad en lugar del azar. La heterogeneidad se consideró sustancial cuando I² superó el 40% y P < 0,10 para la prueba χ². La identificación de heterogeneidad sustancial también influyó en la decisión de utilizar un modelo de efectos aleatorios para calcular la razón de probabilidades en cada análisis. Además, se calculó la incidencia de cada resultado de interés para cada ensayo individualmente, así como colectivamente para los participantes con y sin infección previa por dengue. La incidencia se presenta sobre una base anualizada y por 100 000 personas.
Definiciones de resultados utilizados en ensayos clínicos
Los estudios de Kallás et al. ( 8 ) y Tricou et al. ( 9 ) utilizaron los criterios de 2009 de la Organización Mundial de la Salud (OMS), incluido el de los casos que requieren hospitalización por DCV. Los estudios de Capeding et al. ( 10 ), Villar et al. ( 11 ) y Forrat et al. ( 12 ) utilizaron las definiciones de la OMS de 1997 de fiebre hemorrágica del dengue, dengue grave y casos que requieren hospitalización debido a la gravedad de la infección confirmada virológicamente. Un comité de estudio independiente también adjudicó los casos de forma independiente para cada ensayo para reducir el sesgo y garantizar que los resultados informados se alinearan con el protocolo del estudio.
RESULTADOS
Identificación de estudios
Se identificaron 39 publicaciones de tres RCTs. De estos, se seleccionaron cinco estudios que contenían los datos más recientes de los tres ensayos clínicos de fase III y que examinaban los resultados de interés ( Tabla 1) (8–12 ) . El diagrama de flujo PRISMA para los estudios se muestra en la Figura 1 , y la evaluación del riesgo de sesgo se presenta en la Figura 2 .
CUADRO 1. Ensayos controlados aleatorios de vacunas contra el dengue que cumplieron los criterios de inclusión (es decir, incluyeron pacientes en el grupo placebo que tuvieron una segunda infección por dengue después de una infección por dengue previamente documentada).
| Resultado y estudio | Información del estudio | |||||
|---|---|---|---|---|---|---|
| Grupo de edad (años) | Años | Número de participantes | Número de controles | O (IC del 95%) | ||
| Dengue confirmado virológicamente | ||||||
| Kallás y otros ( 8 ) | 2–59 | 2016–2024 | 3 023 | 2 690 | 0,72 (0,49 a 1,08) | |
| Tricou y col. ( 9 ) | 4–16 | 2016–2024 | 4 854 | 1 832 | 0,97 (0,80 a 1,18) | |
| Capeding y otros ( 10 ) | 2–14 | 2011–2017 | 444 | 216 | 0,91 (0,50 a 1,86) | |
| Villar y col. ( 11 ) | 9–16 | 2011–2018 | 4 821 | 1 440 | 0,75 (0,60 a 0,95) | |
| Dengue grave | ||||||
| Kallás y otros ( 8 ) | 2–59 | 2016–2024 | 3 023 | 2 390 | 0,89 (0 a 5702) | |
| Tricou y col. ( 9 ) | 4–16 | 2016–2024 | 4 854 | 1 832 | 18,89 (0,04 a 9 881) | |
| Forrat y col. ( 12 ) | 2–8 | 2011–2018 | 135 | 101 | 2,28 (0,87 a 6,01) | |
| Forrat y col. ( 12 ) | 9–16 | 2011–2018 | 687 | 171 | 7,22 (0,98 a 53,47) | |
| Hospitalización por dengue | ||||||
| Kallás y otros ( 8 ) | 2–59 | 2016–2024 | 3 023 | 2 390 | 0,89 (0 a 5 702) | |
| Tricou y col. ( 9 ) | 4–16 | 2016–2024 | 4 854 | 1 832 | 0,93 (0,64 a 1,34) | |
| Forrat y col. ( 12 ) | 2–8 | 2011–2018 | 135 | 101 | 1,70 (1,01 a 2,89) | |
| Forrat y col. ( 12 ) | 9–16 | 2011–2018 | 687 | 171 | 1,33 (0,82 a 2,18) | |
IC: intervalo de confianza; OR: odds ratio.
Fuente: Tabla elaborada por los autores con base en los resultados de su estudio.

Incidencia en los ensayos
La incidencia de VCD durante el seguimiento fue de 1 625 casos (IC del 95%: 1 536 a 1 715) por 100 000 personas-año. La tasa de hospitalización por dengue fue de 52 casos (IC del 95%: 37 a 68) por 100 00 personas-año de seguimiento, la tasa de dengue grave fue de 22 casos (IC del 95%: 11 a 32), y la mortalidad por todas las causas fue de 8 (IC del 95%: 2 a 14). No se registraron muertes relacionadas con el dengue en ninguno de los ensayos clínicos durante los períodos de seguimiento, que fueron de 6 años en el estudio de Forrat et al. ( 12 ), 4,5 años en el estudio de Tricou et al. ( 9 ) y 2 años para el ensayo de Kallás et al. ( 8 ).
Asociaciones entre antecedentes documentados de dengue y resultados de interés
Dengue confirmado virológicamente. Se incluyeron en el metanálisis cuatro estudios con un total de 19 320 observaciones y 1 084 eventos notificados ( 8–11 ). Los participantes con antecedentes de infección por dengue tuvieron una menor incidencia de DCV durante el período de seguimiento, con un odds ratio de 0,86 (IC del 95 %: 0,75 a 0,98, P = 0,024) ( Figura 3 ). La heterogeneidad entre los estudios fue baja, con un I² del 14 % y P = 0,32 para la prueba de heterogeneidad.

Dengue grave. Se incluyeron cuatro estudios, con un total de 13 493 observaciones y 57 eventos reportados. La heterogeneidad entre los estudios fue muy baja, con un I² de 0% y P = 0,69 para la prueba de heterogeneidad. El modelo de efectos fijos mostró que los participantes con antecedentes de dengue tenían mayor riesgo de dengue grave, con un odds ratio de 2,91 (IC del 95%: 1,23 a 6,87, P = 0,0149) ( Figura 4 ).

Hospitalización por dengue. Se incluyeron cuatro estudios, con un total de 13 493 observaciones y 381 eventos reportados. Los participantes con antecedentes de dengue tuvieron la misma probabilidad de hospitalización durante el período de seguimiento que aquellos que no tenían antecedentes de dengue, con un odds ratio de 1,18 (IC del 95%: 0,92 a 1,53, P = 0,198) ( Figura 5 ). La heterogeneidad entre los estudios fue moderada, con un I² de 20% y P = 0,29 para la prueba de heterogeneidad.

Muerte relacionada con dengue. En los cuatro estudios con un total de 13 493 observaciones, no se reportaron muertes relacionadas con dengue. Dado que no se registraron eventos en ninguno de los grupos, se realizó un ajuste introduciendo un factor de continuidad de 0,1. Este ajuste permitió calcular una razón de probabilidades estimada y sus intervalos de confianza, que fueron neutros en 0,50 (IC del 95%: 0,01 a 40,05). Solo dos estudios informaron el número de muertes según la seroprevalencia en el grupo placebo del ensayo. Esto mostró que la mortalidad por todas las causas fue similar entre los participantes con y sin dengue previo (OR: 1,74, IC del 95%: 0,21 a 14,08, P = 0,76). Los resultados no cambiaron significativamente cuando se analizaron juntos dos grupos de edad en el ensayo (es decir, de 2 a 8 años y de 9 a 16 años).
DISCUSIÓN
Este metanálisis de ensayos controlados proporciona información valiosa sobre la gravedad de los eventos relacionados con una segunda infección por dengue en pacientes con dengue previamente documentado. Este metanálisis comparó las frecuencias de eventos en individuos asignados aleatoriamente al grupo placebo de ensayos de eficacia de la vacuna en función de la seroprevalencia previa.
Los pacientes seropositivos tuvieron un menor riesgo de una segunda infección por dengue, tasas de hospitalización similares y la misma mortalidad que los individuos seronegativos. Sin embargo, una mayor proporción de individuos seropositivos fueron clasificados como portadores de dengue grave que entre los seronegativos.
Los resultados de esta revisión sistemática proporcionan información que respalda una reevaluación crítica de la conceptualización actual sostenida por la comunidad médica respecto del papel de la infección previa por dengue en el empeoramiento de infecciones posteriores.
Los ensayos clínicos incluidos en este estudio ( 8–12 ) involucran todas las vacunas contra el dengue aprobadas hasta la fecha. Las autoridades sanitarias internacionales suelen tomar decisiones basadas en los resultados publicados en estos y otros estudios similares.
El hallazgo de un menor riesgo de VCD entre los participantes con una infección previa por dengue se alinea con el hecho bien conocido de que la infección previa confiere inmunidad homotípica. Sin embargo, existe evidencia de que una segunda infección con un serotipo diferente conlleva un mayor riesgo de dengue grave debido al potenciador dependiente de anticuerpos, en el que los anticuerpos preexistentes de la infección inicial pueden facilitar la entrada del virus en las células huésped, aumentando la replicación viral y la gravedad de la enfermedad ( 13 ). En individuos con una infección previa, los anticuerpos generados contra el primer serotipo pueden facilitar la entrada de un serotipo diferente en las células huésped en lugar de neutralizarlo, aumentando la replicación viral y aumentando la gravedad de la enfermedad. El potenciador dependiente de anticuerpos ha sido una de las principales hipótesis utilizadas para explicar la mayor gravedad de las segundas infecciones, y ha provocado un debate sobre las estrategias de vacunación. Si bien algunos estudios han confirmado la asociación entre el potenciador dependiente de anticuerpos y el aumento de la gravedad, otros han encontrado resultados más variables, lo que destaca la necesidad de seguir investigando este mecanismo en diferentes contextos epidemiológicos ( 14 ).
Los resultados informados en este metanálisis también resaltan esta necesidad, mostrando que el riesgo de dengue grave fue mayor en individuos con una infección previa por dengue. Sin embargo, durante el seguimiento en los ensayos clínicos, el evento que ocurrió con mayor frecuencia después de VCD no fue el dengue grave sino la hospitalización por dengue. Los resultados informados aquí muestran que el riesgo de hospitalización por dengue fue similar entre los participantes con y sin enfermedad previa. Hallazgos similares también han sido publicados por otros grupos ( 15 , 16 ), y subrayan la necesidad de reconsiderar la utilidad de la clasificación clínica actual del dengue grave y reevaluar el papel de la infección previa como factor de riesgo para eventos graves.
Los resultados de este metanálisis sugieren que la definición de dengue grave puede no reflejar adecuadamente la verdadera gravedad de la enfermedad. Sin embargo, los hallazgos resaltan la necesidad de adoptar criterios de hospitalización como indicadores más sólidos de la gravedad del dengue y de reexaminar la interpretación del riesgo asociado con infecciones previas para mejorar las estrategias de prevención y manejo de la enfermedad ( 15 , 16 ). Algunos estudios sugieren que la clasificación revisada de la OMS para el dengue grave es sensible y específica ( 13 , 16 ), mientras que otros han indicado que hay inconsistencias y discrepancias en la definición de enfermedad grave ( 17–21 ). Aunque existe consenso en que la nueva clasificación de la OMS es más simple y clara, algunos estudios han señalado que aún puede haber dificultades para usarla en entornos con recursos limitados ( 19 ) porque la falta de acceso a los diagnósticos y la variabilidad en la interpretación de los signos de advertencia pueden complicar su implementación efectiva ( 20 , 21 ).
En los ensayos aleatorizados, el número de muertes por dengue durante el seguimiento fue cero. En estudios de Brasil, este hallazgo se ha atribuido a que los participantes habían sido infectados previamente con el virus Zika ( 22 ). Si bien esto podría ser biológicamente plausible para Brasil, parece poco probable que explique la ausencia de muertes en otros países, donde la transmisión de Zika ha sido menor o solo ocasional. La ausencia de muertes por dengue en ensayos clínicos contrasta con el número sustancial de estudios observacionales que muestran claramente su letalidad ( 3 , 7 ). Puede haber varias razones para estas discrepancias. Primero, los estudios observacionales incluyen pacientes con diferentes niveles de acceso a la atención médica y pueden tener niveles más altos de comorbilidad que los reclutados en los ensayos. Además, los pacientes en estudios aleatorizados son monitoreados de cerca para detectar síntomas y probablemente reciban asistencia médica más temprana. Esta atención proactiva puede prevenir la progresión a formas graves de la enfermedad y reducir significativamente la mortalidad. En segundo lugar, también deben considerarse cuestiones metodológicas. En estudios observacionales, el sesgo de observación puede llevar a una sobreestimación del riesgo de mortalidad por dengue en pacientes con infección previa. Este sesgo puede surgir de varios factores, entre ellos, la forma en que se seleccionan y monitorean los participantes y cómo se recopilan y analizan los datos. Los pacientes con antecedentes de dengue pueden tener más probabilidades de buscar atención médica porque conocen la enfermedad, lo que genera una mayor probabilidad de ser incluidos en estudios retrospectivos en comparación con aquellos sin antecedentes de dengue.
Limitaciones
Se deben considerar las limitaciones de este metanálisis. En primer lugar, aunque solo se incluyeron ECA de fase III, la heterogeneidad en los criterios de inclusión y las definiciones de resultados entre los estudios podría haber influido en los hallazgos. En segundo lugar, el número limitado de estudios y eventos informados puede afectar la precisión y generalización de los resultados. En tercer lugar, el uso de datos de los grupos placebo de los ensayos puede no reflejar completamente las condiciones del mundo real, ya que los participantes en los ensayos clínicos a menudo reciben un seguimiento más intensivo y una atención médica superior en comparación con la población general. Es probable que en el contexto del dengue con signos de alarma, los pacientes que participan en un ensayo clínico puedan ser hospitalizados rápidamente, lo que podría llevar a resultados sesgados hacia una menor morbilidad y mortalidad. En cuarto lugar, la población de los ensayos clínicos incluidos en este metanálisis consiste en aquellos de los ensayos de fase III que probaron la eficacia de varias vacunas. Si bien la eficacia de la vacuna se puede extrapolar a otros contextos, se debe tener en cuenta que este análisis no evaluó la eficacia de la vacuna sino más bien los resultados de los participantes en el grupo placebo del ensayo como un indicador de la carga de enfermedad sin vacunación. Por tanto, los resultados obtenidos son indicativos de la carga de enfermedad en contextos epidemiológicos con alta circulación viral y no necesariamente representan otros contextos. Adicionalmente, la variabilidad en las características demográficas y geográficas de las poblaciones estudiadas podría limitar la aplicabilidad de los resultados a otras regiones y contextos.
Otra limitación de este estudio radica en la naturaleza evolutiva de la definición de dengue grave, que ha variado con el tiempo ( 21 , 23 , 24 ), incluso durante los ensayos clínicos analizados. Esta falta de una taxonomía consistente para definir la causa de la hospitalización plantea un desafío. Si bien los ensayos proporcionaron una documentación clara del evento (es decir, la hospitalización), no siempre especificaron los criterios precisos que motivaron la hospitalización. Esto podría llevar a una superposición entre los casos de VCD y dengue grave, en el que un caso de VCD podría ser hospitalizado sin ser necesariamente clasificado como dengue grave. Sin embargo, los eventos en los ensayos no se informaron por duplicado, sino solo bajo una sola categoría, por lo que los resultados se analizaron por separado.
Conclusiones
Los resultados de este metanálisis muestran que la infección previa por dengue se asocia con un mayor riesgo de dengue grave, pero no con un mayor riesgo de hospitalización por dengue ni con un aumento de la mortalidad. El dengue grave en los ensayos clínicos representó una proporción menor de eventos durante el seguimiento, mientras que la hospitalización por dengue fue más frecuente. Estos hallazgos sugieren que la definición de dengue grave debería revisarse para captar mejor la verdadera gravedad de la enfermedad, haciendo hincapié en los criterios de hospitalización como indicadores más fiables. Los resultados subrayan la necesidad de reevaluar el papel de las infecciones previas para refinar las estrategias de prevención y tratamiento del dengue.
Descargo de responsabilidad.
Los autores son los únicos responsables de las opiniones expresadas en el manuscrito, que no necesariamente reflejan la opinión o política de la Revista Panamericana de Salud Pública/Pan American Journal of Public Health o de la Organización Panamericana de la Salud.
Compromiso con el sistema nervioso central:
El virus del dengue es un flavivirus transmitido por los mosquitos Aedes aegypti y Aedes albopictus . La infección por dengue por los cuatro serotipos (DEN 1 a 4) es endémica a nivel mundial en regiones con climas tropicales y subtropicales, con un estimado de 100 a 400 millones de infecciones anuales. Entre los hospitalizados, la mortalidad es de alrededor del 1%. Se ha informado que la afectación neurológica es de alrededor del 5%. El espectro de manifestaciones neurológicas abarca tanto el sistema nervioso periférico como el central. Estas manifestaciones posiblemente podrían categorizarse en aquellas directamente relacionadas con la infección por dengue, es decir, encefalitis aguda y crónica, complicaciones indirectas que conducen a la encefalopatía por dengue y síndrome postinfeccioso debido a reacciones inmunomediadas, y manifestaciones con mecanismos inciertos, como mielitis transversa aguda, cerebelitis aguda y miositis.
La tendencia creciente de la incidencia mundial del dengue exige que se preste atención a una definición más explícita de cada manifestación neurológica para disponer de datos epidemiológicos más precisos. La carga mundial real de infección por dengue con manifestaciones neurológicas es esencial para la planificación y ejecución futuras de estrategias, especialmente en el desarrollo de antivirales y vacunas eficaces contra el virus del dengue.
En este artículo, se analizan los hallazgos recientes de diferentes espectros de manifestaciones neurológicas en la infección por dengue y brindamos una actualización sobre el desarrollo de antivirales y vacunas y sus desafíos.
Tenecteplasa
Kieu-Tram Bach ; Forshing Lui .
Actividad de Educación Continua
La tenecteplasa (TNK) es un agente fibrinolítico recombinante de bolo único que se utiliza para tratar los coágulos intravasculares. El fármaco pertenece a la clase de medicamentos del activador tisular del plasminógeno (tPA). Las indicaciones aprobadas por la FDA incluyen el infarto agudo de miocardio con elevación del segmento ST (STEMI). La tenecteplasa es el agente trombolítico de elección para el infarto agudo de miocardio. La tenecteplasa se está utilizando cada vez más como agente trombolítico en accidentes cerebrovasculares isquémicos agudos, en gran medida debido a su eficacia en comparación con la alteplasa aprobada por la FDA. Esta actividad explora las indicaciones, contraindicaciones, actividad, perfil de eventos adversos, toxicidades y monitoreo de la tenecteplasa para ayudar al equipo interprofesional en el cuidado de los pacientes que necesitan terapia trombolítica.
Objetivos:
- Identificar las indicaciones para iniciar la terapia con tenecteplasa.
- Implementar la estrategia de monitoreo adecuada para tenecteplasa.
- Evaluar el perfil potencial de eventos adversos y toxicidades asociadas con la tenecteplasa.
- Coordinar acciones y utilizar una comunicación abierta entre los miembros del equipo interprofesional para mejorar la atención y mejorar los resultados de los pacientes que reciben tenecteplasa para las afecciones indicadas.
Indicaciones
La tenecteplasa (a veces abreviada como TNK, aunque el Instituto de Prácticas Médicas Seguras lo desaconseja) es un agente trombolítico fabricado mediante tecnología de ADN recombinante. La tenecteplasa es un medicamento aprobado por la FDA específicamente indicado para reducir la mortalidad en pacientes con infarto agudo de miocardio con elevación del segmento ST (STEMI). Las indicaciones fuera de indicación incluyen la trombólisis para el tratamiento del accidente cerebrovascular isquémico agudo, la embolia pulmonar y la limpieza del catéter venoso central. Las indicaciones más utilizadas son el infarto agudo de miocardio y el accidente cerebrovascular isquémico agudo. [1] [2]
La tenecteplasa se ha convertido en el agente trombolítico preferido para el tratamiento del infarto agudo de miocardio debido a su eficacia, conveniencia y relación costo-beneficio en comparación con la alteplasa aprobada por la FDA. Si bien la tenecteplasa no está aprobada por la FDA para los accidentes cerebrovasculares isquémicos agudos, su uso fuera de indicación está aumentando debido a sus atributos favorables, como la administración intravenosa de dosis única y un menor costo en comparación con la alteplasa. La tenecteplasa, administrada en una dosis para accidentes cerebrovasculares de 0,25 mg/kg hasta 25 mg, es una opción más rentable en comparación con la alteplasa para el tratamiento de accidentes cerebrovasculares en el mercado estadounidense, con una diferencia de costo de aproximadamente $3000. [3]
Mecanismo de acción
La tenecteplasa es una variante de la alteplasa obtenida mediante bioingeniería, una versión derivada del ADN recombinante del activador tisular del plasminógeno (tPA) natural. El fármaco se deriva de tres sustituciones de aminoácidos en tres sitios (T, N y K representan las tres regiones modificadas de la proteína tPA natural). El tPA nativo es una serina proteasa que se encuentra en las células endoteliales. La tenecteplasa se une al componente de fibrina de un coágulo sanguíneo (trombo). Actúa dentro de la cascada de coagulación fibrinolítica endógena para catalizar selectivamente la escisión del plasminógeno en plasmina. La plasmina activada posteriormente degrada la fibrina, lo que da como resultado la disolución del coágulo y la recanalización del flujo sanguíneo. [4]
La tenecteplasa muestra una especificidad de fibrina mucho mayor, una mayor resistencia a la inactivación por el inhibidor endógeno del activador del plasminógeno (PAI-1) y una vida media más larga en comparación con el tPA nativo. Debido a su larga vida media, la tenecteplasa se puede administrar como una única inyección intravenosa en bolo. [4]
Administración
La tenecteplasa se presenta como un polvo liofilizado en un vial de 50 mg; se envasa con un vial separado de 10 ml de agua estéril para su reconstitución a fin de obtener una concentración final de 5 mg/ml. La solución reconstituida se puede refrigerar a una temperatura de entre 2 °C y 8 °C (36 °F y 46 °F) y debe utilizarse dentro de las 8 horas.
La tenecteplasa se administra en un único bolo intravenoso de 5 segundos en dosis escalonadas según el peso de 0,25 mg/kg o 0,50 mg/kg con una dosis máxima de 50 mg. La tenecteplasa tiene una vida media de 20 a 25 minutos.
El ensayo STREAM demostró una menor incidencia de hemorragia intracraneal (HIC) en pacientes mayores de 75 años que recibieron media dosis de tenecteplasa (0,25 mg/kg) en comparación con la dosis estándar de 0,5 mg/kg. [5]
Infarto de miocardio
El infarto agudo de miocardio (IM) se trata con trombólisis o intervención coronaria percutánea (ICP) oportunas. Si bien la ICP es el abordaje preferido, la trombólisis sigue siendo una estrategia primaria crucial para los pacientes que no pueden recibir ICP dentro del período de tratamiento preferido. [6]
El estudio CAPTIM demostró que la tenecteplasa puede ser tan eficaz como la ICP en el tratamiento del infarto agudo de miocardio con elevación del segmento ST (STEMI) cuando se administra en el ámbito prehospitalario. [7] Esta estrategia es recomendable para pacientes que no pueden recibir ICP dentro de los 90 minutos recomendados después del primer contacto médico. De hecho, hasta el 70% de los pacientes con STEMI se presentan en hospitales sin capacidad para realizar ICP, por lo que requieren ser transferidos a un centro de ICP o una estrategia de revascularización primaria alternativa. [8] Esta estrategia está respaldada además por las directrices del Colegio Estadounidense de Cardiología/Asociación Estadounidense del Corazón (ACC/AHA), que fomentan la terapia trombolítica prehospitalaria dentro de los 30 minutos posteriores al inicio de los síntomas. [9]
La tenecteplasa se puede utilizar junto con terapia antiplaquetaria y anticoagulante. El fármaco también se puede utilizar antes de someterse a una intervención coronaria percutánea. En caso de fracaso de la trombolisis con tenecteplasa, se debe considerar la realización de una intervención coronaria percutánea de rescate.
La seguridad y eficacia de la tenecteplasa antes de la ICP se siguen investigando. El ensayo ASSENT-4 se interrumpió prematuramente debido a la mortalidad hospitalaria excesiva en el grupo de estudio que recibió ICP facilitada por tenecteplasa. [10] Mientras que los estudios WEST y GRACIA-2 encontraron una eficacia comparable entre la ICP facilitada por tenecteplasa y la ICP primaria, estos estudios determinaron que el mayor beneficio se logró cuando la ICP de rutina se pospone al menos 3 a 12 horas después de la administración de tenecteplasa. [11] [12]
Accidente cerebrovascular isquémico agudo
Varios ensayos controlados aleatorizados para el ictus isquémico agudo han comparado la tenecteplasa y la alteplasa. El ensayo EXTEND-1A TNK mostró una mejor reperfusión frente a la alteplasa en lesiones con baja carga de coágulos. [13] El ensayo NOR-TEST2 con 0,4 mg/kg de tenecteplasa no logró demostrar la no inferioridad con respecto a una dosis estándar de alteplasa IV. [14] El ensayo ATTEST comparó 0,25 mg/kg de tenecteplasa y la dosis estándar de alteplasa IV y no encontró diferencias en los resultados. [15]
El ensayo TAAIS comparó las dosis de tenecteplasa en la oclusión de la arteria cerebral media (ACM) confirmada mediante tomografía computarizada (TC). El ensayo concluyó que se obtuvieron tasas de recanalización más altas y una mejoría neurológica mayor, como lo demuestra una mejora en la Escala de ictus de los Institutos Nacionales de Salud (NIHSS) en la cohorte de 0,25 mg/kg. [16] Además, este grupo de dosis demostró una mejor puntuación en la Escala de Rankin modificada (mRS) de 0 o 1 en el seguimiento de 90 días. La eficacia del grupo de dosis de 0,25 mg/kg está respaldada además por un metanálisis de 5 ensayos controlados aleatorizados, que encontró una mayor eficacia y una menor tasa de hemorragia intracraneal sintomática (sICH) con la dosis de 0,25 mg/kg en comparación con las dosis de 0,1 mg/kg y 0,4 mg/kg. [17] [18]
El ensayo AcT publicado más recientemente en Canadá es un ensayo abierto, aleatorizado y de gran escala que compara 0,25 mg/kg de tenecteplasa y alteplasa. Este ensayo demostró la no inferioridad de la tenecteplasa frente a la alteplasa. [19]
De todos los datos disponibles sobre la tenecteplasa en el ictus isquémico agudo, se puede concluir que ningún ensayo de fase 3 con resultados positivos claros muestra su superioridad sobre la alteplasa. La dosis de 0,4 mg/kg de tenecteplasa no mostró ninguna ventaja sobre la dosis de 0,25 mg/kg. Dada su vida media más larga, de modo que puede administrarse en una dosis única en bolo, y su menor coste, la tenecteplasa está ganando cada vez más aceptación en la mayoría de los centros de ictus de los EE. UU. frente a la alteplasa.
Las pautas de 2019 de la Asociación Estadounidense del Corazón/Asociación Estadounidense de Accidentes Cerebrovasculares (AHA/ASA) brindan las recomendaciones más actualizadas para el uso de tenecteplasa en el ictus isquémico agudo. [20] Las pautas de la AHA/ASA incluyen tenecteplasa en dosis de 0,25 mg/kg y 0,40 mg/kg como terapia alternativa (recomendación de clase IIB). La pauta indicó que podría ser razonable elegir tenecteplasa (un bolo intravenoso único de 0,25 mg/kg, máximo 25 mg) en lugar de alteplasa intravenosa en pacientes sin contraindicaciones para el fibrinolítico intravenoso que también sean elegibles para someterse a una trombectomía mecánica. No se ha demostrado que la tenecteplasa administrada como un bolo intravenoso único de 0,4 mg/kg sea superior o no inferior a la alteplasa, pero podría considerarse como una alternativa a la alteplasa en pacientes con deterioro neurológico menor y sin oclusión intracraneal importante.
Embolia pulmonar
Aunque la tenecteplasa no está aprobada por la FDA para su uso en la embolia pulmonar (EP), varios estudios han evaluado su eficacia y seguridad en el uso para la EP aguda. [21] [22] La tenecteplasa puede considerarse para la EP de alto riesgo o masiva. La EP de alto riesgo o masiva se define por hipotensión sostenida o shock cardiogénico y se administra en la misma dosis que el infarto agudo de miocardio.
El estudio PEITHO y su evaluación de resultados a largo plazo representaron el ensayo más grande que evaluó el uso de trombolíticos en el contexto de EP aguda. El estudio mostró que la tenecteplasa puede mejorar la hemodinámica en pacientes con EP y evidencia de tensión en el corazón derecho, pero con un mayor riesgo de hemorragia intracraneal en comparación con placebo (6,3 % frente a 1,2 %). [23] Además, no se observaron diferencias en la función a largo plazo con tenecteplasa. Hasta la fecha, ningún estudio ha comparado directamente la eficacia y seguridad de la tenecteplasa con otros trombolíticos en la EP aguda.
Efectos adversos
Los efectos adversos de la tenecteplasa, incluidos sangrado, anafilaxia, tromboembolia y arritmia, son similares a los de otros trombolíticos.
El sangrado es la complicación más frecuente del uso de tenecteplasa y trombolíticos. El sangrado puede ocurrir en cualquier parte del cuerpo, así como en los sitios de punción y quirúrgicos. La hemorragia intracraneal plantea la preocupación más importante por el aumento de la mortalidad. La incidencia de hemorragia intracraneal sintomática en pacientes que reciben tenecteplasa (2,9%) es comparable a la de los pacientes que reciben alteplasa (2,7%), otro agente trombolítico. [24] El riesgo de sangrado con tenecteplasa aumenta con el uso concomitante de anticoagulantes y agentes antiplaquetarios.
Se han descrito eventos tromboembólicos y embolización de colesterol con el uso de trombolíticos, incluida la tenecteplasa. Además, se han asociado arritmias cardíacas con el uso de trombolíticos en STEMI como un caso de reperfusión tisular.
En el estudio ASSENT-4, se observaron mayores incidencias de mortalidad, shock cardiogénico, insuficiencia cardíaca congestiva e infarto de miocardio recurrente que requirió revascularización repetida en la cohorte que recibió tenecteplasa con PCI en comparación con PCI sola. [10] En estos casos de STEMI grande, se recomienda a los médicos elegir trombólisis o PCI como estrategia de reperfusión primaria.
Contraindicaciones
La tenecteplasa está contraindicada en varias afecciones. [25] Estas incluyen las siguientes:
- Hemorragia interna activa
- Hipertensión grave no controlada
- Historia de accidente cerebrovascular
- Historia de aneurisma o malformación arteriovenosa
- Historia de neoplasia intracraneal
- Cirugía intracraneal o intraespinal en los últimos 2 meses
- Traumatismo craneoencefálico o espinal en los 2 meses anteriores
- Condiciones que aumentan el riesgo de sangrado
La tenecteplasa es un fármaco clasificado en la categoría C de la FDA para el embarazo. No hay estudios bien controlados que evalúen el riesgo de resultados adversos para la madre o el feto con la tenecteplasa. Se desconoce si la tenecteplasa se excreta en la leche materna. El embarazo es una contraindicación relativa para la tenecteplasa y solo debe administrarse después de considerar cuidadosamente los riesgos y beneficios para la paciente y el feto. [26]
Las interacciones farmacológicas significativas que contraindican el uso de tenecteplasa incluyen defibrotida y mifepristona. El uso simultáneo de tenecteplasa con defibrotida puede aumentar el riesgo de sangrado debido a efectos aditivos y anticoagulación duplicada. La mifepristona y la tenecteplasa están contraindicadas cuando se utiliza mifepristona para la interrupción del embarazo; la combinación puede aumentar el riesgo de sangrado vaginal severo o prolongado debido a efectos aditivos.
Escucha
Los pacientes que reciben tenecteplasa requieren monitoreo neurológico y cardiovascular de rutina para evaluar sangrado y reacciones de hipersensibilidad. [24]
Se deben evitar las manipulaciones y punciones no esenciales durante las primeras horas posteriores a la administración de tenecteplasa. Si no se puede evitar una punción arterial, el sitio preferido es un vaso sanguíneo de la extremidad superior que se pueda comprimir fácilmente. Se debe aplicar presión directa durante 30 minutos después de la venopunción.
Se debe realizar un examen neurológico en forma seriada para evaluar el deterioro del estado mental o cualquier déficit neurológico focal nuevo, que pueda sugerir un episodio hemorrágico. Se debe realizar una TC cerebral urgente si hay algún signo de deterioro neurológico. Si el paciente también está recibiendo anticoagulación concomitante, como heparina, se debe suspender el agente y administrar el agente de reversión adecuado. También se deben controlar otros sitios de sangrado, como sitios de punción o quirúrgicos y hematomas.
Se deben evaluar con frecuencia los signos vitales para detectar fiebre, hipotensión y taquicardia. También se debe realizar de manera rutinaria la evaluación de los signos clínicos de anafilaxia, incluidos angioedema, exantema y dificultad respiratoria. Se debe disponer de medicación de apoyo, como antihistamínicos y epinefrina intramuscular.
Debido al riesgo de arritmia cardíaca con tenecteplasa, es necesario realizar un seguimiento cardíaco. Además, durante la administración de tenecteplasa debe estar disponible un tratamiento antiarrítmico para la bradicardia y la inestabilidad ventricular.
Tenecteplasa en ACV.

Los agentes trombolíticos, incluida la tenecteplasa, se utilizan generalmente dentro de las 4,5 horas posteriores al inicio de los síntomas del accidente cerebrovascular. La información sobre si la tenecteplasa confiere beneficios más allá de las 4,5 horas es limitada. A pesar de los avances en la trombólisis intravenosa y la trombectomía mecánica para los accidentes cerebrovasculares isquémicos agudos, muchos pacientes no reúnen los requisitos para estos tratamientos que restablecen el flujo sanguíneo cerebral y reducen el daño isquémico. La alteplasa y la tenecteplasa intravenosas ahora se han establecido como tratamientos para el accidente cerebrovascular cuando se administran hasta 4,5 horas después del momento en que se supo por última vez que el paciente estaba bien. 1,2 La tenecteplasa es una variante genéticamente modificada de la alteplasa que tiene una mayor especificidad para la fibrina y una vida media más larga. Debido a que los estudios sugieren que la tenecteplasa es tan segura y eficaz como la alteplasa y se puede administrar rápidamente en lugar de requerir una infusión.
La tenecteplasa es un activador del plasminógeno específico para la fibrina producido mediante la técnica del ADN recombinante, utilizando una línea celular ovárica de hámster chino.
Métodos
Realizamos un ensayo multicéntrico, doble ciego, aleatorizado y controlado con placebo en pacientes con accidente cerebrovascular isquémico para comparar la tenecteplasa (0,25 mg por kilogramo de peso corporal, hasta 25 mg) con placebo administrado de 4,5 a 24 horas después del momento en que se supo por última vez que el paciente estaba bien. Los pacientes debían tener evidencia de oclusión de la arteria cerebral media o la arteria carótida interna y tejido recuperable según lo determinado en imágenes de perfusión. El resultado primario fue la puntuación ordinal en la escala de Rankin modificada (rango, 0 a 6, con puntuaciones más altas indicando mayor discapacidad y una puntuación de 6 indicando muerte) en el día 90. Los resultados de seguridad incluyeron muerte y hemorragia intracraneal sintomática.

Resultados
En el ensayo participaron 458 pacientes, de los cuales el 77,3% se sometió posteriormente a una trombectomía; 228 pacientes fueron asignados a recibir tenecteplasa y 230 a recibir placebo. El tiempo medio entre el momento en que se supo por última vez que el paciente estaba bien y la aleatorización fue de aproximadamente 12 horas en el grupo de tenecteplasa y aproximadamente 13 horas en el grupo placebo. La puntuación media en la escala de Rankin modificada a los 90 días fue de 3 en cada grupo. La razón de probabilidades común ajustada para la distribución de las puntuaciones en la escala de Rankin modificada a los 90 días para tenecteplasa en comparación con placebo fue de 1,13 (intervalo de confianza del 95%, 0,82 a 1,57; P = 0,45). En la población de seguridad, la mortalidad a los 90 días fue del 19,7% en el grupo de tenecteplasa y del 18,2% en el grupo placebo, y la incidencia de hemorragia intracraneal sintomática fue del 3,2% y del 2,3%, respectivamente.
Conclusiones
El tratamiento con tenecteplasa que se inició entre 4,5 y 24 horas después del inicio del accidente cerebrovascular en pacientes con oclusiones de la arteria cerebral media o de la arteria carótida interna, la mayoría de los cuales se habían sometido a una trombectomía endovascular, no produjo mejores resultados clínicos que aquellos que recibieron placebo. La incidencia de hemorragia intracerebral sintomática fue similar en los dos grupos. (Financiado por Genentech; número de TIMELESS ClinicalTrials.gov,
NCT03785678 ).
Vacunación en anillo, prevenir el brote de Ébola en Guinea y RD del Congo.
Este artículo recientemente publicado en el New England, ofrece una forma de actuar en salud pública para evitar la propagación de una enfermedad mortal como el ébola, con la vacunación a contactos y contactos de los contactos, con lo cual se logra mitigar el impacto, desde los diez días de realizada la vacunación. Si como lo leen. Cuando estudiábamos originalmente la respuesta inmunitaria esta se producía a los catorce días. Ganar este tiempo para enfermedades como esta pueden ser muchas muertes evitadas. Además de la estrategia de vacunación.

Al comienzo del brote de enfermedad por el virus del Ébola (EVE) de 2018-2020 en el este de la República Democrática del Congo (RDC), no se había autorizado ninguna vacuna. Sin embargo, la evidencia aleatorizada por conglomerados de Guinea en 2015 había indicado que la vacunación en anillo alrededor de los nuevos casos (dirigida a los contactos y contactos de contactos) con el uso de la vacuna viva de replicación rVSV-ZEBOV-GP de dosis única reducía las tasas de EVE a partir de los 10 días posteriores a la vacunación. Por lo tanto, la vacunación en anillo se agregó a las medidas de control estándar para ese brote.

Métodos
En este estudio, evaluamos la incidencia de la EVE en los primeros 9 días posteriores a la vacunación (cuando se esperaba poca protección del aislamiento de casos o la vacunación en anillo), durante los días 10 a 29 y en períodos posteriores. Establecimos 1853 anillos alrededor de nuevos casos o grupos dentro de los 21 días posteriores a la aparición de los síntomas en el caso índice y ofrecimos la vacunación a los miembros del anillo. Se hizo un seguimiento de la aparición de la EVE en los vacunados hasta el final del brote a mediados de 2020.
Resultados
Del 8 de agosto de 2018 al 14 de enero de 2020, vacunamos a 265.183 participantes. De estos vacunados, 102.515 fueron monitoreados los días 0, 3 y 21 por seguridad. Entre los contactos y contactos de contactos, se diagnosticaron 434 casos de EVE (0,2 por anillo), casi todos entre 0 y 9 días (380 casos) o entre 10 y 29 días (32 casos) después de la vacunación. Se diagnosticaron 22 casos adicionales después del día 29 durante un promedio de 170 días más de seguimiento. Cuanto antes se iniciaran las medidas de control (incluida la vacunación en anillo) después de la aparición de EVE en el caso índice, antes se reducirían las tasas de EVE entre los contactos. En cada subgrupo, las tasas de EVE cayeron repentinamente alrededor del día 10. Entre los contactos y los contactos de contactos que todavía estaban libres de enfermedad el día 10, la tasa de aparición de EVE durante los días 10 a 29 fue de 0,16 por 1000 (en 32 de 194.019 participantes). Esta tasa fue mucho menor que la tasa de 4,64 por 1000 (en 21 de 4528 participantes) que se había observado entre los miembros del anillo definidos de manera similar en Guinea, en quienes se habían iniciado rápidamente las medidas de control estándar pero la vacunación se retrasó hasta 21 días después de la formación del anillo (cociente de tasas, 0,04; intervalo de confianza del 95%, 0,02 a 0,06). No se identificaron problemas de seguridad con la vacuna.

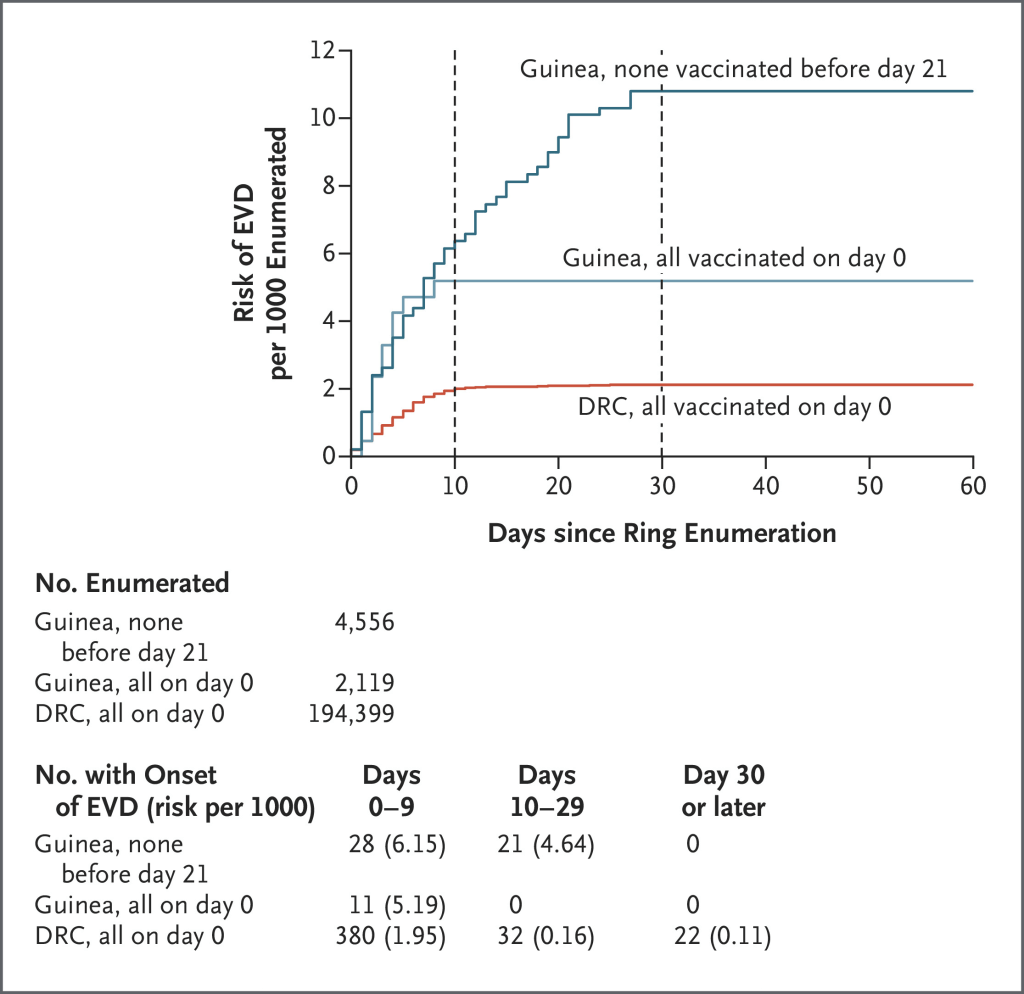
A pesar de un seguimiento minucioso de casi 200.000 contactos o contactos de contactos en la República Democrática del Congo, desde aproximadamente el día 10 después de la intervención con la vacunación en anillo y otras medidas de protección, se identificaron pocos casos adicionales de aparición de EVE entre los vacunados. Además, cuanto antes se aplicaron estas intervenciones después de la aparición de la EVE en el caso índice, antes disminuyó la incidencia de la EVE en los contactos. La asociación entre el momento de la disminución de la incidencia de la EVE entre los contactos de los participantes que recibieron el paquete de intervención proporciona evidencia de que este conjunto de intervenciones fue protector, pero no separa los efectos protectores de la vacunación de los de otras medidas. La evidencia de que la vacunación en anillo con rVSV-ZEBOV-GP mejora el efecto protector de las otras medidas se proporciona mediante la comparación de los vacunados en los anillos del este de la República Democrática del Congo con los miembros de los anillos de control en el ensayo aleatorizado por grupos de Guinea de 2015, en el que la vacunación se había pospuesto durante 21 días, pero los procedimientos para la formación del anillo y las medidas distintas de la vacunación habían sido similares a los utilizados en la República Democrática del Congo. Además, los síntomas en el tercer día de seguimiento que eran compatibles con una infección sistémica por vacuna se asociaron con una incidencia posterior ligeramente menor de EVE.La eficacia de la vacuna puede ser más fuerte contra la EVE mortal que contra la EVE no mortal, como se informó en un análisis de cohorte retrospectivo de pacientes que fueron hospitalizados durante el brote de 2018-2020 en el que los vacunados tuvieron una tasa de letalidad más baja que los no vacunados. 11 Los registros de vacunación más detallados en nuestro estudio actual proporcionan evidencia confirmatoria de una tasa de letalidad más baja entre los vacunados que entre los no vacunados y muestran una tasa de letalidad que es incluso más baja para los casos de EVE que se diagnosticaron 10 días o más después de la vacunación. En un ensayo controlado aleatorizado de terapias para la EVE entre pacientes hospitalizados, los investigadores encontraron que la tasa de letalidad podría reducirse con el uso apropiado de anticuerpos monoclonales. 12 Esos hallazgos aumentan la plausibilidad de que la vacunación no solo protegió contra la aparición de la EVE, sino que también redujo la tasa de letalidad. Durante todo el estudio se vacunó a niños y en la última parte del mismo se incluyeron bebés mayores de 6 meses, mujeres en período de lactancia y mujeres en el segundo o tercer trimestre del embarazo. Aunque nuestro estudio no incluyó un grupo de comparación controlado con placebo, no se observaron efectos secundarios graves. La vacuna rVSV-ZEBOV-GP que se utilizó en este brote ha sido precalificada por la OMS y aprobada para su uso en la Unión Europea, los Estados Unidos y varios países africanos.

La necesidad clave en un brote es la identificación rápida y confiable de los casos y la vacunación de los contactos. Los resultados de nuestro análisis de los anillos de contagio sugieren que la vacunación de los contactos de los contactos de los casos (aunque útil si las circunstancias operativas lo permiten) sería menos importante que centrarse en los contactos inmediatos. Además, la sorprendente diferencia en las tasas de aparición de la EVE entre los clasificados como contactos y los clasificados como contactos de contactos muestra que la identificación confiable de los contactos fue posible incluso en las difíciles condiciones de campo encontradas en el este de la República Democrática del Congo. Entre los vacunados, los trabajadores de la salud y los trabajadores de primera línea que no eran contactos ni contactos de contactos tenían un riesgo a corto plazo aún menor que los contactos de contactos y tendrían un riesgo a largo plazo aún menor en un brote que se hubiera controlado más rápidamente que los brotes de África occidental o el este de la República Democrática del Congo. Los contactos de tercer nivel que fueron vacunados tenían un riesgo muy bajo.
La integración de la investigación en la respuesta al brote de la República Democrática del Congo de 2018-2020 identificó tratamientos efectivos para pacientes hospitalizados y ha facilitado una mayor evaluación de la seguridad y eficacia de las vacunas, al tiempo que ayudó a controlar la transmisión de la enfermedad.
Este estudio ha demostrado la viabilidad de implementar la vacunación en anillo en un contexto de brote en combinación con las medidas tradicionales de control del ébola. La vacunación en anillo es eficaz, eficiente desde el punto de vista operativo y ahorra dosis en comparación con la vacunación de la población, y es factible para los equipos que operan en contextos inseguros.
Cirugía ERAS.

Enhanced Recovery After Surgery Guidelines and Hospital Length of Stay,
Readmission, Complications, and Mortality
A Meta-Analysisof Randomized Clinical Trials
Pregunta: ¿La adopción de pautas de recuperación mejorada después de la cirugía (ERAS) reduce la duración de la hospitalización, los reingresos hospitalarios, las complicaciones y la mortalidad?
Resultados En este metanálisis de 74 ensayos clínicos aleatorizados con 9076 participantes, las pautas ERAS se asociaron con una disminución de la duración de la hospitalización y de las complicaciones. El tipo de cirugía y el número de elementos ERAS se asociaron con estimaciones de la duración de la hospitalización.
Significado Estos hallazgos sugieren que las directrices ERAS se asociaron con una disminución de la duración de la hospitalización y de las complicaciones; las investigaciones futuras deberían centrarse en mejorar la implementación y el cumplimiento de las directrices ERAS para mejorar los resultados de los pacientes.Abstracto
Importancia No se ha completado una revisión exhaustiva de la evidencia que explora los resultados de las pautas de recuperación mejorada después de la cirugía (ERAS).
Objetivo Evaluar si las directrices ERAS están asociadas con una mejor duración de la estancia hospitalaria, readmisión hospitalaria, complicaciones y mortalidad en comparación con la atención quirúrgica habitual, y comprender las diferencias en las estimaciones basadas en el estudio y los factores del paciente.
Se realizaron búsquedas en fuentes de datos MEDLINE, Embase, Cumulative Index to Nursing and Allied Health Literature y Cochrane Central desde el inicio hasta junio de 2021.
Selección de estudios Los títulos, resúmenes y artículos de texto completo fueron examinados por dos revisores independientes. Los estudios elegibles fueron ensayos clínicos aleatorizados que examinaron la cirugía guiada por ERAS en comparación con un grupo de control e informaron sobre al menos uno de los resultados.
Extracción y síntesis de datos Los datos se resumieron por duplicado utilizando un formulario de abstracción de datos estandarizado. El estudio siguió los elementos de informe preferidos para revisiones sistemáticas y metanálisis. El riesgo de sesgo se evaluó por duplicado utilizando la herramienta Cochrane Risk of Bias. Se utilizó un metanálisis de efectos aleatorios para agrupar las estimaciones de cada resultado, y la metarregresión identificó las fuentes de heterogeneidad dentro de cada resultado.
Resultados y medidas principales Los resultados primarios fueron la duración de la estadía hospitalaria, el reingreso hospitalario dentro de los 30 días posteriores al alta índice, las complicaciones posoperatorias a los 30 días y la mortalidad posoperatoria a los 30 días.
Resultados De las 12 047 referencias identificadas, se examinaron 1493 textos completos para determinar su elegibilidad, 495 se incluyeron en la revisión sistemática y 74 ECA con 9076 participantes se incluyeron en el metanálisis. Los estudios incluidos presentaron datos de 21 países y 9 procedimientos quirúrgicos guiados por ERAS, de los cuales 15 (20,3 %) tuvieron un bajo riesgo de sesgo. La puntuación media (DE) de la lista de verificación de Informes sobre cumplimiento, resultados y elementos de investigación de ERAS fue de 13,5 (2,3). La duración de la estancia hospitalaria disminuyó en 1,88 días (IC del 95 %, 0,95-2,81 días; I 2 = 86,5 %; P < 0,001) y el riesgo de complicaciones disminuyó (riesgo relativo, 0,71; IC del 95 %, 0,59-0,87; I 2 = 78,6 %; P < 0,001) en el grupo ERAS. El riesgo de readmisión y mortalidad no fueron significativos.
Conclusiones y relevancia En este metanálisis, las directrices ERAS se asociaron con una disminución de la duración de la hospitalización y de las complicaciones. Los estudios futuros deberían apuntar a mejorar la implementación de las directrices ERAS y aumentar el alcance de las directrices.
Introducción
A nivel mundial, más de 313 millones de personas se someten a cirugía para salvar o prolongar la vida cada año y esa cifra está aumentando. 1 , 2 Si bien la cirugía es esencial para mantener la salud y la calidad de vida, consume importantes recursos de atención médica y no está exenta de complicaciones. La duración media de la estancia hospitalaria para la cirugía es de 5 días, lo que equivale a más de 7,5 millones de días-paciente cada año a un costo de al menos $1200 por día. 1 La duración de la estancia hospitalaria aumenta para los pacientes sometidos a cirugía que experimentan complicaciones posoperatorias. 3 – 10 Más de un tercio de los pacientes sometidos a cirugía experimentan complicaciones, 11 – 13 colocando a estos pacientes en mayor riesgo de complicaciones que los pacientes que no se someten a cirugía. 3 – 5 , 14 , 15 Los pacientes que experimentan complicaciones también tienen más probabilidades de requerir intervenciones adicionales, ser readmitidos en el hospital y morir, todo lo cual se asocia con un aumento de los costos. 10 , 16 – 18 Se estima que el 50% de las complicaciones son prevenibles, lo que brinda una oportunidad de utilizar estrategias basadas en evidencia para mejorar los resultados para los pacientes y los sistemas de atención de salud. 3 , 4 , 8 – 11 , 13 , 14 Además, mejorar los resultados quirúrgicos y reducir los recursos de atención de salud puede aumentar la capacidad de los pacientes para acceder a la atención quirúrgica. 8 , 9
A medida que la necesidad de cirugía continúa excediendo la capacidad de atención médica, se necesitan estrategias para garantizar que la atención sea efectiva, eficiente y segura. Una opción es implementar las pautas de recuperación mejorada después de la cirugía (ERAS). Actualmente, existen pautas ERAS para 23 tipos de cirugía 19 y programas de implementación activos en más de 20 tipos de cirugía. 20 Las pautas ERAS brindan recomendaciones para la atención perioperatoria y se ha descubierto que reducen las complicaciones, 21 la duración de la estadía hospitalaria 22 y el costo. 23 , 24 Varias revisiones sistemáticas específicas de cirugía han encontrado efectos positivos o mixtos en los resultados después de adoptar las pautas ERAS. 25 – 31 Sin embargo, no se ha realizado una revisión integral de la eficacia de ERAS en áreas quirúrgicas y dentro de poblaciones heterogéneas. Hasta donde sabemos, no hay revisiones sistemáticas que examinen estos resultados en toda la amplitud de los procedimientos quirúrgicos guiados por ERAS o que comparen los resultados por tipo de cirugía, lo que podría proporcionar una mejor comprensión de la eficacia de ERAS. El objetivo de este estudio es sintetizar la evidencia sobre la eficacia de ERAS y determinar si la adopción de las directrices ERAS mejora la duración de la estancia hospitalaria, la readmisión hospitalaria, la mortalidad y las complicaciones posoperatorias en comparación con la atención quirúrgica habitual.
Métodos
Esta revisión sistemática y metanálisis se informa utilizando la guía de informes de Elementos de informe preferidos para revisiones sistemáticas y metanálisis ( PRISMA ). 32 El protocolo se registró en el registro PROSPERO de revisiones sistemáticas ( CRD42021255973 ).Estrategia de búsqueda
La estrategia de búsqueda combinó vocabulario controlado y palabras clave para la población ( pacientes sometidos a cirugía ), la intervención ( ERAS , fast track , enhancement recovery ) y los resultados ( duración de la estancia hospitalaria , reingreso hospitalario , complicaciones , mortalidad ) y se ejecutó en MEDLINE, Embase, Cumulative Index to Nursing and Allied Health Literature y Cochrane Central Register of Controlled Trials el 18 de junio de 2021 (eAppendix 1 en Supplement 1 ). La estrategia de búsqueda no estuvo limitada por la fecha de publicación o el idioma.Criterios de elegibilidad
Se incluyeron los estudios que informaban al menos uno de los resultados entre pacientes adultos sometidos a cirugía antes y después de la implementación de las pautas ERAS. Los estudios que implementaron las pautas ERAS, incluidas las pautas basadas en ERAS (por ejemplo, ERAS, vía rápida, protocolo de recuperación mejorada), se incluyeron si los protocolos contenían elementos basados en ERAS. Cualquier diseño de estudio que comparara la intervención (pautas ERAS) y el grupo de comparación (atención habitual) se incluyó en la revisión sistemática general, pero solo los ensayos clínicos aleatorizados se incluyeron en el metanálisis.
Se excluyeron los estudios con pacientes pediátricos únicamente o aquellos que no estratificaron las estimaciones por adultos y niños. Se excluyeron los estudios que no proporcionaron estimaciones o datos suficientes para calcular las estimaciones. Se excluyeron las actas o resúmenes de congresos, revisiones, guías y comentarios. Se excluyeron los estudios con menos de 50 pacientes en total debido al alto riesgo de sesgo en estos estudios. Se incluyeron estudios publicados en cualquier idioma; sin embargo, se excluyó si no pudimos traducir el artículo. Para los estudios con múltiples manuscritos, se incluyó el manuscrito con el conjunto de datos más completo y se excluyeron los demás (datos duplicados).Selección de estudios
Covidence se utilizó para gestionar la selección de estudios. 33 En cada etapa de la selección, todos los revisores examinaron una muestra de títulos y resúmenes (n = 5) y textos completos (n = 10) para garantizar la coherencia entre los revisores y se revisaron estudios adicionales juntos hasta que se logró un κ de 0,8. Los títulos, resúmenes y textos completos fueron examinados para determinar su elegibilidad por 2 revisores independientes. Durante la selección de títulos y resúmenes, se incluyeron las referencias incluidas por al menos 1 revisor para la selección de texto completo para disminuir el riesgo de excluir estudios incorrectamente. Los desacuerdos entre revisores se resolvieron mediante discusión o consulta con un tercer revisor.Proceso de recopilación de datos
Se utilizó una base de datos estandarizada (Microsoft Excel) para resumir los datos de los estudios incluidos. La base de datos de abstracción de datos se probó de forma piloto en dos estudios. Antes de la abstracción completa de los datos, todos los revisores recibieron capacitación completando la abstracción de datos para los mismos cinco estudios; la capacitación continuó hasta que se alcanzó un κ de 0,8. Los datos fueron resumidos por un solo revisor y el 65 % de los datos fueron verificados dos veces por un revisor independiente. El diccionario de datos para el formulario de abstracción de datos estandarizado está disponible en el Apéndice electrónico 2 del Suplemento 1 .Variables
Las variables de resultado primarias fueron la duración de la hospitalización, la readmisión dentro de los 30 días posteriores al alta hospitalaria de referencia, las complicaciones posoperatorias dentro de los 30 días posteriores a la cirugía y la mortalidad dentro de los 30 días posteriores a la cirugía. Si bien las variables de resultado primarias se limitaron a los 30 días posteriores a la cirugía o la hospitalización de referencia, los datos de otros períodos de tiempo se resumieron como resultados secundarios.
Los datos adicionales extraídos de los estudios incluyeron información bibliográfica, características del estudio, datos de los pacientes, tipo de protocolo evaluado (ERAS, recuperación mejorada, vía rápida, otros), número de elementos ERAS incluidos en el protocolo (recuento) incluso si no se informó el cumplimiento de cada elemento y datos sobre el cumplimiento. Se incluye una lista completa de los datos extraídos en el diccionario de datos (apéndice electrónico 2 en el suplemento 1 ).Riesgo de sesgo en estudios individuales
El riesgo de sesgo de los estudios individuales se evaluó mediante la herramienta Cochrane de riesgo de sesgo (versión 2), 34 por 2 revisores independientes con formación de posgrado en epidemiología. Cualquier desacuerdo entre los revisores se resolvió mediante discusión. La lista de verificación de informes sobre cumplimiento, resultados e investigación de elementos de ERAS (RECOvER) evaluó la integridad de los informes. 35Análisis de datos
Las características del estudio se describieron utilizando estadísticas descriptivas según fuera apropiado. Se utilizó un metanálisis de efectos aleatorios para agrupar las estimaciones para cada variable de resultado (paquete metan). 36 , 37 El I 2 cuantificó la magnitud de la heterogeneidad entre estudios, y la estadística Q de Cochrane determinó la significancia de la heterogeneidad. Se calcularon los cocientes de riesgos (RR) para los datos informados como proporciones (es decir, mortalidad, complicaciones y readmisión), y se calcularon las diferencias de medias para los datos informados como medias (es decir, duración de la estancia hospitalaria). Las estimaciones informadas como mediana (RIC) se convirtieron a media (DE) utilizando el método Wan 38 y se agruparon.
La metarregresión exploró las posibles fuentes de heterogeneidad para cada resultado. Las posibles fuentes de heterogeneidad incluyeron la edad y el sexo del paciente, el año(s) de recopilación de datos, el tipo de cirugía, la cantidad de elementos ERAS incluidos en el protocolo, el tipo de protocolo (por ejemplo, ERAS, protocolo de recuperación mejorada, vía rápida u otro) y las puntuaciones RECOvER. El sesgo de publicación se evaluó mediante la inspección visual de un gráfico de embudo y estadísticamente utilizando el método de regresión lineal de Egger. Todos los análisis se realizaron en Stata 20.0 (StataCorp). 36 , 37 Los datos se analizaron desde septiembre de 2023 hasta febrero de 2024. Las pruebas estadísticas fueron bilaterales y la significancia se estableció en P < .05.Resultados
La estrategia de búsqueda arrojó 12 047 referencias únicas, de las cuales 1493 fueron revisadas en texto completo, 495 se incluyeron en la revisión sistemática general (eFigure en Suplemento 1 ) y 74 RCTs 39 – 112 se incluyeron en el metanálisis. Las características de cada estudio individual se incluyen en eTable 1 en Suplemento 1. Los estudios incluidos representan 9076 pacientes con 4577 pacientes en el grupo de control (no ERAS) y 4375 pacientes en el grupo ERAS. En los 54 estudios que incluyeron la edad, la edad media (DE) fue de 50,0 (12,6) años para los pacientes del grupo de control y 49,2 (12,6) años entre los pacientes del grupo ERAS. 39 , 41 – 47 , 49 – 54 , 56 , 57 , 59 , 62 – 68 , 70 , 73 , 76 , 79 , 81 – 84 , 86 , 88 , 89 , 91 , 93 – 106 , 108 – 111
Características del estudio
El año de publicación promedio (rango) fue 2019 (2009-2021). La mayoría de los estudios se realizaron en países de ingresos altos y de ingresos medios altos (57 [80,3%]); 22 (29,7%) se publicaron en China, 40, 46, 55, 56, 67-72 , 75 , 82 , 85-87 , 103 , 107-109 , 112 , 113 , 8 ( 10,8 % ) en India , 44 , 45 , 60 , 76 , 84 , 91 , 97 , 100 , 5 ( 6,8 % ) en EE. UU . 47 , 49 , 66 , 99 , 104
La mayoría de los 74 estudios examinaron los resultados de ERAS en pacientes sometidos a cirugía gastrointestinal (32 [43,2%]) 39 , 40 , 45 , 47 , 50 , 51 , 53 , 54 , 56 , 58-60 , 73 , 74 , 77 , 79 , 80 , 83 , 87 , 9298 , 100 , 102 , 103 , 105 , 112 , 114 y procedimientos quirúrgicos ginecológicos (11 [14,9%]), 41 , 43 , 49 , 52 , 65 , 89 , 90 , 110 , 111 , 115 con solo 1 (1,4%) en cirugía cardíaca . cirugía, 68 y 2 (2,7%) en urología. 44 , 106 La mayoría de los 74 estudios evaluaron los resultados de las directrices ERAS (37 [50,0%]), 39 – 46 , 48 , 52 – 54 , 57 , 68 – 71 , 73 , 75 , 78 , 82 , 87 – 91 , 98 – 101 , 104 – 108 , 110 , 111 mientras que 23 (31,1%) evaluaron protocolos de recuperación mejorada, 47 , 49 , 55 , 56 , 58 , 61 – 66 , 76 , 77 , 79 – 81 , 83 – 85 , 95 – 97 , 102 13 (17,6%) evaluaron protocolos de vía rápida, 50 , 51 , 59 , 60 , 72 , 74 , 86 , 92 – 94 , 103 , 109 , 112 , 116y 1 (1,4%) evaluó otros tipos de protocolos o vías basadas en los principios ERAS. 67 El número medio (DE) de elementos ERAS incluidos en las intervenciones (ERAS, protocolos mejorados, vía rápida, otros) fue de 11,1 (3,0) elementos de un posible total de 16. Comúnmente se incluyeron la movilización temprana (71 [96,0%]), el manejo de la analgesia posoperatoria (64 [86,5%]), la dieta posoperatoria y el manejo intestinal (63 [85,1%]) y el manejo del drenaje y el tubo (63 [85,1%]) ( Figura 1 ). Los protocolos clasificados como ERAS incluyeron más elementos que los clasificados como vía rápida, pero no fueron diferentes de los protocolos de recuperación mejorada ( F 1,493 = 9,58; P = .002). El número medio (DE) de elementos entre los estudios de ERAS fue de 11,8 (2,8), en comparación con 8,9 (2,3) en los protocolos de vía rápida, 10,6 (3,7) en los protocolos de recuperación mejorada y 11,4 (3,2) elementos con otros tipos de protocolos. El cumplimiento de los protocolos ERAS se informó en 17 (20,3%) estudios 49 , 52 , 53 , 56 , 59 , 67 , 69 , 70 , 77 , 80 , 88 – 90 , 99 , 101 , 106 , 107 pero se informó de forma inconsistente y no se pudo agrupar; el cumplimiento medio (DE) informado fue del 74,7% (10,2%) de los 9 estudios de los que pudimos sintetizar los datos. 49 , 52 , 67 , 80 , 89 , 90 , 99 , 101 , 106Metaanálisis por resultadosDuración de la estancia
De los 74 estudios incluidos, 44 estudios (62,2%) informaron una estimación general mediana o media de la duración de la estancia hospitalaria. 39 , 40 , 42 , 44 , 45 , 47 – 50 , 52 , 53 , 55 , 58 , 60 , 61 , 65 , 66 , 71 , 73 , 74 , 78 , 79 , 82 , 84 , 85 , 88 – 91 , 95 , 97 , 98 , 101 , 103 , 105 , 107 – 109 , 111 , 113 La duración media agrupada de la estancia hospitalaria fue 1,88 días (IC del 95 %, 0,95-2,81 días; I 2 = 86,5 %; P < 0,001) más corta en los grupos ERAS en comparación con los grupos de control. El ERAS también redujo la duración de la estancia hospitalaria postoperatoria (22 estudios; diferencia media, 2,83 días; IC del 95 %, 2,10-3,55 días; I 2 = 0 %; P < 0,001) en comparación con los grupos de control. El sesgo de publicación no fue significativo. 40 , 41 , 53 , 54 , 56 , 63 , 64 , 68 , 71 , 72 , 75 , 79 , 82 , 85 , 87 , 94 , 104 , 105 , 107 , 112 , 113 , 117Readmisión hospitalaria
Diecinueve de 74 estudios (41,3%) informaron reingresos hospitalarios de 30 días. El RR agrupado de reingreso hospitalario de 30 días fue 1,04 (IC del 95%, 0,81-1,35; I2 = 0%; P = .74) 39 , 43 , 44 , 52 – 54 , 65 – 67 , 69 , 79 , 80 , 89 , 94 , 97 , 101 , 102 , 105 , 112 ; con un efecto protector cuando no se especificó el período de tiempo (11 estudios, RR , 0,61; IC del 95%, 0,41-0,93; I2 = 0%; P = .02). 41 , 42 , 47 , 56 , 63 , 75 , 82 , 88 , 98 , 106 , 111 El sesgo de publicación no fue significativo.Complicaciones
Catorce de 74 estudios (18,9%) informaron una estimación general (no estratificada) de complicaciones con una estimación agrupada de 0,71 (IC del 95%, 0,59-0,87; I 2 = 78,6%; P < .001), 44 , 46 , 53 , 67 – 69 , 79 , 80 , 82 , 86 , 87 , 93 , 95 , 96 a favor de ERAS en comparación con los grupos de control. De los nueve estudios que informaron complicaciones a los 30 días, el RR agrupado fue de 0,73 (IC del 95 %, 0,56-0,94; I 2 = 86,3 %; P < 0,02), 53 , 67 , 79 , 80 , 82 , 87 , 93 , 95 , 96 a favor de ERAS sobre los grupos de control. Hubo evidencia de sesgo de publicación utilizando la prueba de Egger para efectos de estudio pequeños ( t = 2,24; IC del 95 %, 0,14-2,15; P = 0,003); sin embargo, las estimaciones se distribuyeron simétricamente tras la inspección visual del gráfico de embudo.Mortalidad
Hubo 19 de 74 estudios que informaron mortalidad postoperatoria a los 30 días, con un riesgo agrupado de 0,95 (IC del 95 %, 0,48-1,88) sin heterogeneidad entre las estimaciones ( I 2 = 0 %; P = 0,89). 40 , 44 , 50 , 53 , 54 , 57 , 69 , 70 , 77 , 78 , 87 , 89 , 92 , 93 , 95-98 , 107 Debido a que muchos estudios informaron estimaciones de mortalidad 0, se aplicó una corrección de continuidad para calcular los RR. 118 El sesgo de publicación no fue significativo .Fuentes de heterogeneidad determinadas por metarregresión
No hubo diferencias en las estimaciones agrupadas de la duración de la estancia hospitalaria en función de los ingresos del país, la puntuación de la lista de verificación RECOvER, el año de publicación, el número de elementos ERAS incluidos en el protocolo o el riesgo de sesgo. El tipo de cirugía explicó la heterogeneidad en la estimación de la duración de la estancia hospitalaria (coeficiente, 0,32; IC del 95 %, 0,17-0,48; P < 0,001). La estimación agrupada de la diferencia media en la duración de las estancias hospitalarias para los pacientes sometidos a cirugía pancreática, ortopédica y gastrointestinal fue mayor que la de otros procedimientos quirúrgicos ( Figura 2 ). Ninguna de las variables exploradas explicó la varianza en la estimación agrupada de readmisión hospitalaria a los 30 días, complicaciones o mortalidad. Estos hallazgos se pueden encontrar en la Figura 3 y la Figura 4 .Riesgo de sesgo y RECUPERACIÓN
Entre los 74 estudios incluidos, 40 (54,1%) tenían algún riesgo de sesgo, 19 (25,7%) tenían alto riesgo de sesgo y 15 (20,3%) tenían bajo riesgo de sesgo. La falta de datos de resultados se consideró una fuente de bajo riesgo de sesgo en 64 estudios (86,5%), mientras que las desviaciones de la intervención por protocolo se consideraron una fuente de alto riesgo de sesgo en 17 estudios (23,0%) (eTabla 2 en el Suplemento 1 ).
La media (DE) del número de elementos de la lista de verificación RECOvER que se incluyeron en los estudios fue de 13,5 (2,3). Los elementos notificados con más frecuencia incluyeron proporcionar contexto e importancia dentro de los antecedentes (74 [100,0 %]), explicar la importancia del estudio (73 [98,7 %]) e informar sobre el protocolo utilizado (72 [97,3 %]) ( Figura 1 ). Los elementos notificados con menos frecuencia fueron la auditoría de los resultados (10 [13,5 %]), el examen de las asociaciones entre los resultados y otras variables (13 [17,6 %]) y el informe sobre el cumplimiento de las directrices ERAS (20 [27,0 %] ( Figura 1 ).Discusión
Este estudio concluyó que el uso de las pautas ERAS se asoció con una disminución de la duración de la hospitalización y de las complicaciones. La duración de la hospitalización varió según el tipo de cirugía. Se incluyeron muchos estudios, pero aún quedan algunas lagunas en la evidencia. Por ejemplo, hubo escasez de evidencia para algunos procedimientos quirúrgicos (ninguno para cabeza y cuello y mama, y pocos estudios para cardiología), menos estudios informaron sobre la mortalidad y el cumplimiento se informó de manera inconsistente y deficiente.
Si bien las pautas ERAS se establecieron con la publicación de la pauta de la Sociedad ERAS para el cuidado perioperatorio de pacientes sometidos a cirugía de colon, 119 la recuperación mejorada como concepto se basó en protocolos de vía rápida descritos previamente. 120 – 122 En consecuencia, no es sorprendente que muchos estudios incluidos se etiquetaran como de vía rápida y que una gran proporción se centrara en la cirugía gastrointestinal. Sin embargo, este estudio no identificó ninguna diferencia en las estimaciones de la duración de la estancia hospitalaria, la readmisión, las complicaciones o la mortalidad relacionadas con el nombre del protocolo. Si bien el nombre dado al protocolo examinado no explicó la heterogeneidad entre las estimaciones, el número de elementos ERAS incluidos en los protocolos sí lo hizo para la duración de la estancia hospitalaria. Esto sugiere que el número de elementos incluidos en el protocolo es probablemente más importante que la marca del protocolo, que está respaldada por estudios previos. 123 , 124 Es alentador que la mayoría de los estudios informaron los elementos de su protocolo (90%), lo cual es importante para evaluar los resultados de ERAS, 35 pero muy pocos estudios informaron el cumplimiento de cada elemento. Lamentablemente, la mayoría de los estudios incluyeron menos del 70% (11) de los elementos tradicionales del ERAS. Si bien la cantidad de elementos del ERAS incluidos en el protocolo es importante, no fue posible evaluar qué elementos son los más importantes para los resultados del ERAS. Los estudios futuros deberían centrarse en evaluar los resultados relativos de cada elemento del ERAS para comprender los elementos básicos necesarios para lograr los beneficios del ERAS. Esto simplificará el ERAS y promoverá su adopción en entornos de menores recursos. 125 , 126
Al igual que con otras directrices, los resultados de ERAS dependen de la adopción de las directrices ERAS. 127 – 129 De hecho, se ha demostrado que un mayor cumplimiento de ERAS mejora los resultados. 129 – 131 Dado que solo alrededor del 20% de los estudios incluidos informaron el cumplimiento de ERAS, y los informes de estas estimaciones fueron demasiado heterogéneos para incluirlos en el análisis, es probable que el cumplimiento medio fuera inferior al 75% y que nuestros hallazgos subestimen los resultados de ERAS. Si el cumplimiento es importante para los resultados de ERAS, ¿cómo se puede mejorar el cumplimiento? Se han esbozado estrategias para implementar ERAS, con un enfoque en la formación de equipos y la auditoría del cumplimiento y la retroalimentación. 126 , 132 Estas estrategias están alineadas con los principios de la ciencia de la implementación y las estrategias basadas en la evidencia para la implementación efectiva de las directrices. 127 , 128 Las estrategias adicionales que se deben considerar al implementar ERAS incluyen la identificación de barreras y facilitadores para la implementación, incluidos los usuarios finales en el desarrollo de estrategias, educación y avisos y recordatorios. En conjunto , el trabajo futuro debería centrarse en estrategias para mejorar la implementación y el cumplimiento de las directrices ERAS ; cuya importancia se ha señalado. 126 Además, de acuerdo con la lista de verificación RECOvER, abogamos por una mejor presentación de informes sobre el cumplimiento general y el cumplimiento de cada elemento ERAS en estudios que exploren los resultados de las directrices ERAS.Limitaciones
Este estudio tiene limitaciones. Si bien la estrategia de búsqueda fue desarrollada por un bibliotecario con experiencia en revisiones sistemáticas, es posible que no se hayan identificado algunos estudios. Utilizando la estadística de Egger y una evaluación visual de los gráficos de embudo, no encontramos evidencia de sesgo hacia los estudios con grandes tamaños del efecto. Si bien la exhaustividad de la revisión sistemática es una fortaleza, también puede ser limitante porque los estudios incluidos fueron heterogéneos según el tipo de protocolo ERAS, el tipo de cirugía y los resultados. Además, el análisis está limitado por los datos proporcionados dentro de los estudios incluidos. Como tal, las variables que pueden estar asociadas con nuestras variables de resultado, incluido el estado socioeconómico, el estado del seguro y la complejidad quirúrgica, no se tuvieron en cuenta en el análisis. De manera similar, los pacientes sometidos a procedimientos quirúrgicos guiados por ERAS pueden ser un grupo altamente seleccionado, que no pudimos controlar. Finalmente, estos hallazgos pueden no ser generalizables a todos los tipos de cirugía porque la mayoría de los estudios exploraron la eficacia de ERAS en cirugía colorrectal y cirugía obstétrica o ginecológica. De hecho, nuestros hallazgos sugirieron que el tipo de cirugía estaba asociado con la duración de la estadía hospitalaria, pero la razón de la variación no estaba clara.Conclusiones
Este metanálisis determinó que el ERAS se asociaba con una disminución de la duración de la hospitalización (sin un aumento significativo de las readmisiones hospitalarias) y de las complicaciones. Dadas las mejoras en las especialidades, las investigaciones futuras deberían apuntar a aplicar el ERAS a nuevas especialidades quirúrgicas y en más entornos clínicos a nivel mundial.
Aplicaciones de la nanotecnología en el campo médico: una revisión
Abid Haleem a,Mohd Javaid a,Ravi Pratap Singh b,Shanay Rab c,Rajiv Sumar

Abstract
La nanotecnología tiene una amplia aplicación como nanomedicina en el campo médico. Algunas nanopartículas tienen posibles aplicaciones en nuevos instrumentos de diagnóstico, imágenes y metodologías, productos medicinales específicos, productos farmacéuticos, implantes biomédicos e ingeniería de tejidos. Hoy en día, los tratamientos de alta toxicidad se pueden administrar con mayor seguridad utilizando la nanotecnología, como los medicamentos quimioterapéuticos contra el cáncer. Además, los dispositivos portátiles pueden detectar cambios cruciales en los signos vitales, las condiciones de las células cancerosas y las infecciones que realmente están sucediendo en el cuerpo. Anticipamos que estas tecnologías brindarán a los médicos un acceso directo considerablemente mejor a datos críticos sobre las razones de los cambios en los signos de vida o enfermedad debido a la presencia tecnológica en la fuente del problema. La biomedicina se puede utilizar para terapias con análisis predictivos e inteligencia artificial. Para llevar a cabo este estudio, se identificaron y estudiaron artículos relevantes sobre nanotecnología en el campo médico de Scopus, Google Scholar, ResearchGate y otras plataformas de investigación. El estudio analiza diferentes tipos de nanopartículas utilizadas en el campo médico. Este artículo analiza las aplicaciones de la nanotecnología en el campo médico. También se describen las clases, características y usos de la nanotecnología en el ámbito de la medicina. Los científicos, los gobiernos, las organizaciones de la sociedad civil y el público en general deberán colaborar entre distintos sectores para evaluar la importancia de la nanotecnología y orientar su avance en diversos campos. La investigación actual incluye varios usos posibles de la nanotecnología en el ámbito médico. Como resultado, el estudio proporciona un informe breve y bien organizado sobre la nanotecnología que resultará valioso para investigadores, ingenieros y científicos en futuros proyectos de investigación.
1. Introducción
La nanotecnología es un término utilizado para definir áreas de la ciencia y la ingeniería en las que los fenómenos que ocurren en dimensiones nanométricas se utilizan en el diseño, caracterización, fabricación y aplicaciones de materiales, estructuras, dispositivos y sistemas. El concepto de nanotecnología se introdujo por primera vez en 1959 cuando el físico Richard Feynman presentó una presentación sobre la fabricación de cosas a nivel atómico y molecular. La nanotecnología se considera ahora la tecnología más prometedora del siglo XXI y los investigadores la han estudiado como una técnica novedosa en la investigación médica. La nanotecnología marcará el comienzo de una nueva era de productividad y prosperidad, como lo demuestra el aumento de la financiación pública para la investigación y el desarrollo de la nanotecnología durante la última década. 1 , 2 La nanotecnología puede estimular el crecimiento económico y mejorar la capacidad y la calidad en los sectores industriales. Ha contribuido sustancialmente al bienestar de la sociedad y ha moldeado la naturaleza de la vida moderna. Tiene el potencial de alterar significativamente la dinámica social, las condiciones económicas y la vida humana.
El hombre lleva cientos de años buscando remedios milagrosos para aliviar el dolor causado por enfermedades y lesiones . Muchos académicos creen que las aplicaciones de la nanotecnología en la medicina pueden ser esenciales para lograrlo. Estas aplicaciones incluyen la vigilancia, el control, la creación, la reparación y la defensa integrales de todos los sistemas biológicos humanos, empleando nanodispositivos y nanoestructuras diseñados que funcionan a nivel molecular. La nanotecnología puede transformar radicalmente la investigación médica y crear un nuevo sector de mejora humana. 3 , 4 , 5 Existe una buena línea para las aplicaciones diagnósticas, terapéuticas y preventivas de la nanotecnología. Esta tecnología puede modificar intencionalmente el cuerpo, entre otros muchos problemas. Los nanofármacos empleados han demostrado que se mejora la biodisponibilidad, se eliminan los efectos secundarios y la medicina terapéutica se absorbe de manera más eficaz. 6 – 7
La presencia y la entrada de cada molécula individual en el cerebro estructuran esencialmente una barrera de membrana altamente selectiva permeable para moléculas con coeficientes de partición altos. Recientemente se han utilizado nanopartículas en esta membrana como sistema transportador de medicamentos. En particular, las nanopartículas se inhalan y atraviesan las membranas cerebrales. Las terapias típicas y tradicionales para la trombosis vascular a menudo tienen ventajas relativamente limitadas debido a la corta vida media plasmática, muchos efectos adversos y la rápida eliminación del fármaco. Para mejorar la estabilidad e incluso la vida media del medicamento encapsulado, la inmovilización de una cantidad específica de un agente en un sistema de administración de fármacos podría superar esta restricción. La biocompatibilidad y la biodegradabilidad hacen que las nanopartículas poliméricas y los nanotransportadores liposomales se empleen a menudo. 8 , 9 , 10
La ciencia y la tecnología se han utilizado para el diagnóstico de enfermedades, el tratamiento y la prevención de traumatismos, el alivio del dolor y la conservación y mejora de la salud humana mediante instrumentos moleculares y la comprensión molecular del cuerpo humano. La mayoría de los usos comerciales actuales en medicina en nanotecnologías apuntan al suministro de medicamentos. Se pueden introducir nuevos modos de acción y los compuestos medicinales existentes son más específicos y biodisponibles. Las nanosondas , los sistemas nanoelectrónicos sensoriales integrados y las estructuras químicas multifuncionales para la administración de fármacos y la focalización de enfermedades son aplicaciones futuras en nanotecnología. 11 , 12 , 13
Ya se ha logrado un gran éxito en la mejora de la administración de medicamentos con nanotecnología. Algunos compuestos específicos pueden mejorar la orientación y la entrada de medicamentos en la célula y mejorar la obtención de imágenes, la focalización intracelular y la liberación controlada de genes terapéuticos. Por lo tanto, los médicos podrían detectar y mejorar su influencia sobre las células enfermas y los tumores para optimizar las dosis de la terapia. En combinación con otras formas de tratamiento personalizado, la nanometría se puede personalizar para centrarse en un paciente individual que solo tiene células enfermas, lo que minimiza los efectos adversos y el daño tisular . Los científicos ya han logrado algunos avances que promueven el desarrollo celular para tratar el daño de la médula espinal . Nanopartículas magnéticas y nanopartes sensibles a enzimas que se dirigen a los tumores cerebrales; muestras de nanopartículas inteligentes para la administración de productos farmacológicos intracelulares y la obtención de imágenes de expresión genética; puntos cuantitativos para detectar y cuantificar el cáncer cerebral humano. 14 , 15 , 16 En el área de la atención médica, la nanotecnología abre nuevos límites en la industria de las ciencias de la vida. La nanotecnología es muy prometedora en la manipulación de cosas a nivel atómico para cambiar muchas partes del tratamiento médico, como el diagnóstico, el control de enfermedades, el funcionamiento de equipos, la medicina regenerativa, el desarrollo de vacunas y la administración de medicamentos. También abre el camino a través de sofisticados instrumentos de investigación para desarrollar medicamentos que mejoren los tratamientos para diversas dolencias. La nanotecnología se puede utilizar para la medicación de células particulares en el cuerpo, reduciendo así los riesgos de fracaso y rechazo. 17 , 18 , 19
Hemos identificado cuatro objetivos de investigación principales de este documento como se detalla a continuación:
(1) identificar los tipos de nanotecnología y nanopartículas con sus usos en el campo médico;
(2) discutir las clases y la taxonomía de los materiales basados en la nanotecnología para la esfera médica;
(3) identificar y discutir las características asociadas y las características de la nanotecnología para el dominio médico; y
(4) identificar las aplicaciones contemporáneas y futuras de la nanotecnología para el campo médico.
2. Necesidad de la nanotecnología en el campo médico
Los descubrimientos en el campo de la nanotecnología y los nanofármacos son muy amplios y de amplio alcance. La nanomedicina ha experimentado modificaciones impresionantes que han llevado a los fármacos a un nuevo nivel con importantes resultados en el ámbito de la atención sanitaria. Es necesario estudiar las importantes capacidades de la nanotecnología en el ámbito de la atención sanitaria. En medicina, se están llevando a cabo investigaciones exhaustivas sobre las mejores prácticas y metodologías, incluidas la nefrología, la terapia genética para enfermedades cardiovasculares y la terapia contra el cáncer. Se ha producido un importante desarrollo en el tratamiento tradicional, y la calidad de las nanopartículas y la nanotecnología ha mejorado y ha mostrado resultados alentadores. 20 – 21 La terapia genética también ha sacado partido de los nanofármacos. Varias investigaciones se han centrado en las aplicaciones de vectores virales que se cree que son sistemas para la administración de medicamentos.22 , 23 , 24
Los nanobots que apuntan a células cancerosas específicas para tabletas inteligentes envían datos a los investigadores para garantizar que los pacientes reciban su tratamiento correctamente. La nanotecnología ofrece la posibilidad de realizar diagnósticos in vitro al sustituir los procedimientos existentes por alternativas más económicas y fáciles de utilizar. Las nanopartículas pueden funcionar como agentes de imagen molecular dentro de esos dispositivos e introducir alteraciones genéticas relacionadas con el cáncer y características funcionales de las células tumorales. Además, los recubrimientos basados en nanotecnología funcional incluyen con frecuencia los siguientes nanomateriales , según la función deseada: dióxido de titanio, dióxido de silicio , negro de carbono, óxido de hierro , óxido de zinc y plata. Los instrumentos y procedimientos mejoran las evaluaciones de caracterización fisicoquímica, la seguridad y la eficacia de los nanomateriales y las nanosuperficies integradas en la ingeniería de dispositivos médicos . Los científicos desempeñan un papel crucial en la creación de bienes que incluyen materiales novedosos , sensores y sistemas de almacenamiento de energía. 25 – 26
3. En el campo médico se utilizan distintos tipos de nanopartículas .
Las nanopartículas tienen una importante relación superficie-volumen debido a su tamaño a nanoescala, lo que les permite absorber grandes cantidades de medicamentos y moverse rápidamente por el torrente sanguíneo. Su mayor superficie les confiere capacidades distintivas, ya que aumenta sus cualidades mecánicas, magnéticas, ópticas y catalíticas, lo que permite su uso en más aplicaciones farmacéuticas. Las nanopartículas se clasifican en tres áreas según su composición química: orgánicas, inorgánicas y basadas en carbono. 27 , 28 , 29 La figura 1 muestra algunas clasificaciones primarias de las nanopartículas. Las proteínas, los carbohidratos, los lípidos y otras moléculas orgánicas se sintetizan en nanopartículas orgánicas con una dimensión específica, como un radio de menos de 100 nm.

Las nanopartículas inorgánicas no son tóxicas, son hidrófilas, biocompatibles y muy estables en comparación con los materiales orgánicos. Las nanopartículas inorgánicas incluyen metales elementales, óxidos metálicos y sales metálicas, entre otras cosas. Los fulerenos , los nanotubos de carbono , el grafeno y sus derivados son ejemplos de nanomateriales basados en carbono. Estos materiales han despertado la atención de varios campos, incluidas las aplicaciones biomédicas, debido a sus dimensiones estructurales inusuales y sus propiedades mecánicas, eléctricas, térmicas, ópticas y químicas excepcionales. Las nanopartículas generalmente conservan las propiedades químicas de sus materiales a granel, lo que puede ser beneficioso al seleccionar una nanopartícula para diversas aplicaciones. 30 ,31 ,32
Las nanopartículas reaccionan a la luz calentándose lo suficiente para destruir las células cancerosas. Los investigadores creen que las nanopartículas pueden ponerse directamente en circulación y convertirse en tumores cancerosos en el futuro. Las píldoras inteligentes son liberadores de medicamentos con sensores ingeribles que pueden manejarse de forma inalámbrica y ajustarse para controlar una dosis de medicamento en función de los datos recopilados en todo el cuerpo. La nanomedicina se enfrenta a obstáculos inherentes como toda tecnología innovadora y revolucionaria; principalmente, se ha utilizado ampliamente en aplicaciones clínicas. El impacto ambiental de la nanotecnología se acumula en los tejidos y órganos vivos y puede hacerse asequible a gran escala. Los nanobots son un avance significativo en la nanomedicina. 34 , 35 , 36 , 37
4. Clases y taxonomía de materiales basados en nanotecnología para el ámbito médico
La figura 2 explora las diversas clases y categorizaciones de diferentes materiales basados en nanotecnología que tienen aplicaciones y utilidades especiales en el campo de la medicina. Se han reportado varias clases en la literatura disponible, a saber: nanopartículas metálicas , dendrímeros , liposomas , polímeros biodegradables , nanomateriales basados en carbono, nanocompuestos de hidrogel y muchos otros también que respaldan y amplían la utilización y los servicios en el campo médico a través del concepto de nanotecnología. 38 – 39

Las nanofibras se han utilizado en apósitos para heridas , textiles quirúrgicos e implantes, tecnología de tejidos y componentes de órganos artificiales. Los científicos están creando vendajes inteligentes que se absorben en el tejido cuando la herida ha cicatrizado. En estos vendajes inteligentes, las nanofibras incrustadas pueden incluir coagulación, antibióticos e incluso sensores para detectar síntomas infecciosos. 40 ,41 ,42 La nanomedicina garantiza una vida más larga y ayudará a las personas que viven más tiempo y las apoyará de una manera positiva para la Tierra y requiere la eliminación de sus recursos naturales. Otro enfoque de la nanotecnología puede ser a través de nanomáquinas para prepararse para la colonización del espacio mediante la construcción de estructuras y la creación de ecosistemas para otros planetas. Los investigadores también están investigando formas de modificar la fisiología humana para adaptarse mejor a las condiciones atmosféricas de otros mundos.
En aplicaciones sanitarias, la nanomedicina utiliza la nanotecnología, como la terapia y el diagnóstico de diferentes enfermedades, utilizando nanopartículas, biosensores nanoelectrónicos y nanotecnología molecular. Proporciona la capacidad de evaluar el cuerpo de la persona, la medicación y el equipo médico a nivel nanométrico, lo que garantiza que la medicina sea mucho más precisa. El sector sanitario está utilizando esta tecnología para diagnósticos y equipos médicos. Los rápidos avances en nanotecnología significan que se están desarrollando nuevos diagnósticos y terapias con mejores tasas de éxito. Actualmente, la nanomedicina se utiliza para el desarrollo de medicamentos inteligentes y el cáncer. 43 , 44 , 45En los últimos años, esta tecnología se ha utilizado para producir nuevas nanopartículas y las industrias han cambiado significativamente. La aplicación médica de la nanotecnología implica el desarrollo de dispositivos biomecánicos microscópicos, como nanomáquinas y nanorobots. Los productos basados en la nanotecnología suelen ser costosos, lo que dificulta su producción generalizada. Estos productos ayudarán a difundir esta tecnología al ofrecer opciones de producción asequibles. Las nanopartículas pueden aumentar sensiblemente la glucosa y reaccionar con la liberación de insulina, eliminando la necesidad de la autoobservación y autocontrol de la insulina. Las nanopartículas implantadas en la circulación humana pueden identificar enfermedades de forma proactiva al detectar ciertas enzimas indicativas del crecimiento de tumores. 46 , 47 , 48 Si se aplica a la atención sanitaria, la nanotecnología puede suponer un avance sustancial en el diagnóstico, el tratamiento y la prevención de enfermedades. Los innovadores están cada vez más interesados en los posibles usos sanitarios de la nanotecnología, que puede conducir a la industria hacia una nueva era de crecimiento. El diagnóstico y la terapia dependen ahora de la experiencia clínica y de la interpretación de datos biométricos externos; se espera que el énfasis de la investigación futura se derive directamente de los datos de la nanotecnología en el lugar de la enfermedad. Al permitir que nuestros cuerpos utilicen mecánica artificial, esta tecnología ayuda a todos, desde dentro hacia fuera, a definir medicamentos proactivos, preventivos y personalizados. El uso de nanomateriales es uno de los ejemplos más mencionados. La manipulación de dispositivos y sistemas a escala nanométrica ofrece numerosas oportunidades para diagnosticar y tratar enfermedades y realizar pruebas más precisas. 49 , 50 , 51
Los nanomateriales se utilizan en la industria de la salud para el diagnóstico, la terapia, el control y la prevención de enfermedades. El desarrollo de medicamentos mejores y más seguros, actividades centradas en los tejidos y nanomedicamentos personalizados está impulsado por las nanopartículas. Esta tecnología, por ejemplo, se utiliza para la desinfección de superficies y equipos de protección personal durante la pandemia de la enfermedad por coronavirus de 2019. Las nanopartículas pueden transportar medicamentos al lugar exacto requerido, mejorando sustancialmente su eficacia y restringiendo la toxicidad para otros tejidos del cuerpo. 52 , 53 , 54 Para la administración de medicamentos al cerebro en el caso de enfermedades difíciles de tratar, también se pueden desarrollar nanopartículas para superar la barrera hematoencefálica.
5. Características y rasgos asociados de la nanotecnología para el ámbito médico
Las diversas características y funciones clásicas asociadas de la nanotecnología al ámbito médico incluyen (1) tratamiento de heridas ; (2) tratamientos antibacterianos; (3) minimización del daño a las células sanas; y (4) técnica de diagnóstico de nanomedicina. El uso de nanovesículas, nanopartículas, nanotubos de carbono , etc., ha hecho que las aplicaciones de los principios basados en la nanotecnología sean más efectivas y productivas para la medicina, donde la precisión y la inteligencia son esenciales en un ámbito más amplio. 55 – 56 Para los métodos médicos preventivos, las nanotecnologías son tan buenas como las reactivas. Los monitores portátiles pueden diseñarse para transmitir datos a los sistemas hospitalarios, simplificando el cuidado de los pacientes ancianos, que a menudo requieren atención en lugares remotos. De manera similar, los nanomateriales, considerados durante mucho tiempo como progenitores de las neoplasias malignas metastásicas, pueden utilizarse para controlar las células tumorales circulantes. La industria tecnológica utiliza átomos y moléculas individuales, en particular la nanociencia, con implicaciones futuristas para la ciencia, la ingeniería y la tecnología. Puede tener un impacto e influencia notables para desarrollar, caracterizar, desarrollar e implementar átomos y moléculas particulares. La medicina, la energía, la producción de alimentos, los productos químicos básicos, los cosméticos, la agricultura, el equipamiento, la biotecnología y los textiles, entre otros, están cambiando fundamentalmente. 57 , 58 , 59
5.1 . Tratamiento de heridas
Las células de una persona pueden crear tejidos y órganos a partir de un santo grial para la cirugía reconstructiva y de trasplante para pacientes que pueden haberlos perdido debido a una enfermedad o daño. La investigación en este tema, apoyada por el conocimiento de la topografía de los tejidos a escala nanométrica, intenta construir tejidos cuya función y estructura sean similares a las que se encuentran en la naturaleza del organismo. Los nanogeneradores, las nanopartículas de polímeros y una solución precisa podrían ayudar a curar mejor y más rápidamente las heridas de las personas. Las nanopartículas solo se pueden conectar con imágenes y ligandos diana a las células o tejidos. Esto permite a los cirujanos y radiólogos distinguir el tejido enfermo del sano de manera más efectiva, mejorar el tratamiento de la enfermedad y reducir el peligro de dañar el tejido sano. La nanotecnología ha afectado enormemente la velocidad y la especificidad de las evaluaciones de biomarcadores en los fluidos corporales. 60 , 61 , 62
La nanotecnología emplea las propiedades creadas en la escala nanométrica, que difieren de las del mismo material en una escala mayor en física, química o biología. Además, el tamaño nanométrico también incluye muchos de los mecanismos biológicos del cuerpo humano que permiten atravesar barreras naturales para acceder a nuevos sitios de administración e interactuar con el ADN o pequeñas proteínas en diferentes niveles, en la sangre o dentro de los tejidos o células del cuerpo. La nanociencia es más avanzada y ofrece posibilidades para medicamentos especializados y específicos con menos efectos adversos y más fáciles de usar. La materia de tamaño nanométrico con precisión nanométrica se controla y maneja mediante la nanotecnología. Estos pueden incluir átomos, moléculas o estructuras biológicas importantes. 63 – 64
5.2 . Tratamientos antibacterianos
La nanomedicina se ha extendido a varias disciplinas, incluida la administración de medicamentos, los instrumentos de diagnóstico e imagen, las plataformas de alto rendimiento para la detección, el desarrollo de vacunas, los antimicrobianos, los dispositivos portátiles, etc. 65 – 66 El uso de nanopartículas de oro y puntos cuánticos , el empleo de luz infrarroja y la limpieza mejorada de los instrumentos podrían usarse para tratamientos antibacterianos. La nanotecnología es cada vez más optimista sobre el hecho de proporcionar un progreso sustancial en la detección y el tratamiento de enfermedades tal como se aplica a la medicina. Se espera que los medicamentos proporcionen medicamentos, diagnóstico, tratamiento celular y fabricación de materiales biocompatibles. El uso de la nanotecnología en la terapéutica abarca la nanomedicina y el desarrollo de agentes a nanoescala para diversos tratamientos de enfermedades. La nanotecnología manipula un artículo para producir compuestos con características extraordinariamente diversas y únicas a nivel atómico y molecular.
5.3 . Minimizar el daño a las células sanas.
Los innovadores en nanotecnología médica están diseñando métodos para administrar medicamentos de manera más eficiente, como por ejemplo, apuntar directamente a las células cancerosas mediante terapia. Los resultados de los pacientes mejoran y se informa de un daño mínimo a las células sanas, lo que podría causar daño durante la quimioterapia con nanopartículas que localizan y destruyen las células cancerosas. Los médicos también pueden proporcionar un tratamiento térmico con mayor precisión mediante el uso de la nanotecnología junto con la quimioterapia. Los nanotubos vinculados a anticuerpos atraídos por tumores absorben la luz láser, lo que puede hacer que el tumor se incinere en dicha terapia. 67 – 68 El uso de materiales biobiológicos, no biológicos, biomiméticos o híbridos también está muy extendido en la nanomedicina.
5.4 . Técnica de diagnóstico en nanomedicina
Las aplicaciones de la nanotecnología para el diagnóstico, que incluyen el uso de nanotubos de carbono , la aplicación de nanotubos de oro y detecciones rápidas y económicas, hicieron posible la identificación de enfermedades en una etapa más temprana. Esta técnica utiliza instrumentos de tamaños submicrométricos para diagnosticar, prevenir y curar mejor las enfermedades y mejorar la calidad de vida general de los pacientes. El desarrollo de medicamentos regenerativos se acelera sustancialmente gracias a la nanotecnología. Los nuevos enfoques permiten la piel, los huesos, los cartílagos u otros tejidos protésicos en pacientes con insuficiencia orgánica o lesiones graves . El uso de la nanotecnología cambia la función celular de manera más efectiva para imitar los efectos de los tejidos y órganos naturales. 69 , 70 , 71
6. Principales áreas de aplicación de la nanotecnología en el ámbito médico
La nanotecnología acelera el proceso utilizando un dispositivo portátil compacto que toma muestras pequeñas y permite un procesamiento y análisis casi instantáneos. Las pruebas de diagnóstico in vitro seguirán aumentando el tamaño de las muestras y los biosensores. Las formulaciones de nanopartículas, cuando se utilizan para óxidos de hierro y polímeros especiales, aumentarán su capacidad de obtención de imágenes al utilizar dosis más bajas y más efectivas de los compuestos de diagnóstico, lo que permite la detección temprana de anomalías genéticas, tumores y toda la variedad de estados patológicos. La nanomedicina, como la biotecnología, ha sido motivo de preocupación en ciertas áreas, particularmente en lo que respecta a la seguridad y la privacidad. 72 , 73 , 74 , 75 Los inmunoensayos son aplicaciones apropiadas debido a la conectividad robusta entre anticuerpos y antígenos, lo que conduce a excelentes sensibilidades. Los sensores inmunológicos regenerativos son un nuevo desafío interesante que permite la repetitividad para la rigidez estadística y el monitoreo semicontinuo. La nanomedicina es un tema muy inmaduro en el cáncer, por lo que la clínica necesita determinar la posible influencia. 76 , 77 , 78 , 79 , 80 , 81 , 82 , 83 , 84 , 85
6.1 . Diagnóstico
En la última década, la imagenología se ha convertido en una herramienta poderosa para diagnosticar enfermedades. Los avances en resonancia magnética y
tomografía computarizada son impresionantes. Sin embargo, la nanotecnología ofrece instrumentos para diagnóstico in vitro e in vivo que son sensibles y muy precisos, mucho más allá de las capacidades de los equipos modernos. Como cualquier avance en el diagnóstico, el objetivo final es permitir a los médicos diagnosticar una enfermedad lo antes posible. Se prevé que la nanotecnología permita diagnósticos celulares y, posiblemente, diagnósticos subcelulares.
6.2 . Ingeniería de tejidos y tratamiento celular
La medicina regenerativa, especialmente la ingeniería de tejidos y el tratamiento celular, son otros campos potenciales de la nanomedicina. La nanotecnología proporciona un «andamiaje» estructural esencial para crear nuevas estructuras funcionales que se parecen a los tejidos naturales en los que se pueden introducir células vivas y estimular su proliferación. Los nuevos tejidos se benefician de la biocompatibilidad de las nanopartículas y las células con la fuente de muestra. El tejido resultante puede entonces ser regulado y los médicos pueden influir en los procesos de formación, desarrollo y reparación celular.
6.3 . Desarrollo de la terapia
Se prevé que el efecto más significativo de la nanomedicina en la administración y el tratamiento de medicamentos se logrará en la terapia. Las nanopartículas permiten a los médicos concentrar los medicamentos en la causa de la enfermedad, mejorando la eficiencia y disminuyendo los efectos adversos. También brindan nuevas oportunidades para regular las liberaciones terapéuticas. La nanomedicina ha obtenido enormes beneficios en la instrumentación y la síntesis farmacéutica con varios tipos de nanofármacos y aplicaciones de transporte y diagnóstico de fármacos. Se está desarrollando un campo de investigación para producir nanopartículas y tratamientos basados en la nanotecnología.
6.4 . Administración de fármacos
Los sistemas de administración de fármacos basados en la nanotecnología incluyen inicialmente nanopartículas que contienen uno o más fármacos terapéuticos que pueden unirse o dispersarse y adsorberse en matrices poliméricas . En los últimos años, ha habido un desarrollo significativo en la producción de nanofármacos utilizando imágenes, tratamientos y diagnósticos. Los sistemas de nanofármacos se centran principalmente en mejorar la biodisponibilidad de la administración a tejidos específicos, prolongar la vida media de los medicamentos inyectables y administrar medicamentos por vía oral. Los nanofármacos se administran en niveles más bajos, con mejoras notables en sus efectos farmacológicos y una reducción del peligro para la salud y de los efectos adversos.
6.5 . Detección de enfermedades
La nanomedicina es una aplicación fascinante para la prevención, detección, terapia y control de enfermedades, desde nanopartículas de bioingeniería que atacan y matan células y la implantación de tejidos biocompatibles hasta biosensores implantados de tamaño nanométrico. Sin embargo, si bien las aplicaciones básicas de la nanomedicina, como medicamentos personalizados e instrumentos médicos, ya se han utilizado en la medicina convencional para usos más ambiciosos, como dispositivos nanomédicos de múltiples partes, las propiedades únicas de las nanopartículas se pueden aprovechar a nivel molecular. Existe una mayor área de superficie para la adhesión química en esta pequeña escala, lo que facilita la manipulación de moléculas en partículas finas, ajustando el comportamiento de las partículas. Los nanomateriales también son lo suficientemente pequeños como para ingresar a las células vivas.
6.6 . Detección de oxígeno corporal .
Los nanosensores pueden detectar concentraciones de oxígeno y dióxido de carbono en el cuerpo y la presencia de materiales peligrosos. La detección de órganos digestivos malignos y sensibilidad a los alimentos permite que los programas de dieta y nutrición individuales formen parte de sus usos. El daño a las células sanas es una preocupación importante durante el tratamiento con quimioterapia y radiación frecuentes. Se emplean nuevos métodos nanomédicos para tratar el cáncer de piel, lo que permite un suministro adecuado a ubicaciones tumorales específicas y apuntar a células con efectos secundarios menos dañinos de la medicación y otras terapias teóricas. Una nueva forma de identificar células cancerosas en la circulación, llamada NanoFlares, se está utilizando con la nanomedicina. Las NanoFlares son partículas diseñadas para unirse a los objetivos genéticos de las células cancerosas y emitir luz cuando se identifica ese objetivo genético en particular.
6.7 . Asistencia sanitaria económica
La nanomedicina genera grandes esperanzas de una asistencia sanitaria mejor, eficiente y económica para millones de personas y puede ofrecer buenas respuestas a numerosas enfermedades. La nanotecnología influye en casi todas las áreas de la medicina actual, desde el diagnóstico hasta el seguimiento de enfermedades, pasando por la cirugía, la quimioterapia o la medicina regenerativa. Las ventajas que puede aportar la nanotecnología están beneficiando actualmente a muchos sectores de la atención médica. El diagnóstico a escala nanométrica es otro campo en alza de la nanomedicina. El objetivo es diagnosticar una enfermedad lo antes posible. Muchos pacientes con insuficiencia orgánica o lesiones graves esperan nuevos enfoques de la medicina regenerativa. La piel, el hueso y el cartílago artificiales están progresando, y algunos de ellos ya están en el mercado.
6.8 . Mejorar la eficacia de los medicamentos.
La administración de fármacos mediante materiales inteligentes y nanopartículas es un área de investigación prometedora que puede ayudar a las compañías farmacéuticas a mejorar la eficiencia de los medicamentos existentes y eliminar algunos efectos secundarios sistemáticos. Consiste en conjuntos de agentes de transporte, dispositivos de imagen y medicamentos que se crean para dirigirse a los tejidos afectados y monitorear el proceso simultáneamente. En otras palabras, las demandas funcionales específicas deben distinguirse en las características físico-químicas necesarias y conectarse con el comportamiento biológico.
6.9 . Manejo de la enfermedad
La nanotecnología proporciona una herramienta extra eficaz para prevenir y controlar enfermedades, ya que la resistencia bacteriana a los antibióticos está aumentando en todo el mundo. La eficiencia de las membranas bacterianas a escala nanométrica puede ser aún mayor con compuestos antimicrobianos, como la nanoplata. Estas características pueden minimizar la necesidad de antibióticos cuando se integran en materiales tradicionales, al tiempo que protegen al paciente de infecciones. La nanotecnología tiene el potencial de revolucionar el tratamiento de los pacientes. Esta tecnología en la I+D de las ciencias biológicas y en otras áreas de vanguardia de la atención sanitaria aún está lejos de volverse omnipresente. La situación económica en la que la nanotecnología se encuentra a la vanguardia del tratamiento sanitario puede volverse ahora demasiado difícil y peligrosa para justificar inversiones, dado el creciente costo médico y el gasto en I+D de las ciencias biológicas. El tratamiento con analgésicos orales normalmente se realizaría más fácilmente y haría que el paciente se sintiera lo suficientemente cómodo.
6.10 . Lucha contra el cáncer
En la lucha actual contra el cáncer, la nanotecnología se considera uno de los avances más prometedores en el suministro de medicamentos. Normalmente, no se trata de productos farmacéuticos, sino de nanopartículas que pueden transportar medicamentos estándar contra el cáncer a los tumores con menos efectos adversos y permitir la eliminación selectiva de células cancerosas en terapias no tradicionales. Si se permite la administración de nanopartículas para quimioterapia, se puede administrar más medicamento citotóxico en el lugar de destino y se reduce la toxicidad y la eficacia fuera del objetivo.
6.11 . Útil para enfermedades cardiovasculares
En el campo de la medicina, la nanomedicina utiliza conocimientos nanotecnológicos para prevenir y tratar enfermedades graves, como enfermedades cardiovasculares y cardíacas. Los materiales a escala nanométrica, como las nanopartículas biocompatibles y los nanobots médicos, han ayudado a los médicos a comprender los objetivos de acción de un ser vivo gracias a los recientes avances en nanotecnología.
6.12 . Nanobots
El avance más significativo de la nanomedicina son los nanobots, que pueden emplearse para reparar células dañadas y reemplazar componentes intracelulares completos. También pueden reproducirse para reparar un defecto genético o reemplazar una molécula de ADN para erradicar una enfermedad. Los nanobots en medicina pueden ofrecer perspectivas de salud rentables, como desbloquear arterias o reemplazar un órgano por completo. Aunque los nanotransportadores pueden proporcionar concentraciones de dosis exactas a regiones específicas, su pequeño tamaño conduce a un compromiso paradójico entre volumen y fabricación. El comportamiento coordinado y la comunicación a través de la inteligencia artificial permitirán a los nanobots cumplir con sus tareas de manera metódica y eficiente. Los nanobots podrían programarse individualmente, buscarse y circular en distintas direcciones. Un nanobot individual podría conectarse con amigos y compañeros de trabajo, cada uno con sus propias pautas, para pedirles que agruparan sus recubrimientos, cargas o tamaños para monitorear la existencia, el diagnóstico o la orientación de los tejidos enfermos de manera más eficiente.
6.13 . Mejor procedimiento preventivo
El objetivo fundamental de la nanomedicina es convertir la atención sanitaria en un procedimiento totalmente preventivo. Se puede solucionar antes de que llegue al nivel en que se necesite tratamiento mediante la detección temprana del malestar. La nanomedicina tiene como objetivo mejorar la calidad de vida humana mediante la eliminación de arrugas, exceso de grasa y celulitis, el fortalecimiento muscular y óseo, la recuperación del cabello y la rehabilitación de la visión. Las nanopartículas presentes en los productos de limpieza y en los equipos de protección personal se pueden utilizar para inhibir la transmisión. La nanomedicina se podría utilizar para regular el sistema inmunológico y mejorar las respuestas inmunitarias contra las infecciones.
6.14 . Radioterapia
En el campo de la radioterapia, la nanotecnología también puede mejorar. Las nanopartículas de radiación que atraen los tumores pueden concentrar la radiación para aumentar la eficacia del tratamiento y, al mismo tiempo, mantener el tejido sano. Las aplicaciones de la nanotecnología no se limitan al tratamiento del cáncer. Los nanosensores también pueden detectar ataques cardíacos y accidentes cerebrovasculares antes que el paciente. Las partículas de nanotecnología pueden controlar continuamente la sangre para buscar células endoteliales que existían antes de un ataque. Al restablecer el sistema inmunológico, las nanotecnologías también han prometido dejar de atacar al cuerpo del paciente.
La nanomedicina tiene el potencial de detectar y prevenir numerosas enfermedades, incluido el cáncer. En ensayos clínicos , la nanomedicina cuenta actualmente con cientos de artículos que abordan todos los principales trastornos cardiovasculares, neurológicos, musculoesqueléticos e inflamatorios. 86 , 87 , 88 , 89 Es útil para la obtención de imágenes médicas, diagnósticos y biomateriales, lo que permite aplicaciones tecnológicas en todo el sector de la atención sanitaria. Para que el siguiente nivel de medicamentos, terapias e inverosimilitudes novedosas esté disponible para médicos y pacientes, existe la necesidad de avances genuinos en la atención sanitaria, la nanomedicina como un instrumento vital para la medicina personalizada, dirigida y regenerativa. 90 , 91 , 92 Proporciona nuevas herramientas esenciales para abordar el principal problema que enfrentan las personas mayores y se considera fundamental para una atención sanitaria mejor y más económica. Es fundamental hacer que los medicamentos y tratamientos sean accesibles para todos. 93 , 94 , 95
7 . Discusión
La nanomedicina es un campo médico emergente que utiliza la experiencia nanotecnológica para prevenir y tratar enfermedades graves, como el cáncer, las enfermedades cardiovasculares y otras. Los últimos avances en nanotecnología han permitido a los médicos sensibilizar los objetivos de acción en un cuerpo vivo mediante el uso de componentes a escala nanométrica, incluida la biocompatibilidad de nanopartículas y nanobots. Los investigadores también están utilizando la nanomedicina para estimular la inmunoterapia . En los últimos años se han producido grandes avances en la nanomedicina que han ampliado el mercado de la nanomedicina. Las aplicaciones de la nanomedicina, como el diagnóstico mediante nanomáquinas, ofrecen la capacidad de controlar la química interna del órgano y permiten el acceso directo a las regiones enfermas. Los tratamientos nanomédicos han demostrado varias ventajas significativas, entre ellas, un mejor suministro de agua y una actividad biológica prolongada al proteger las cargas útiles contra entornos biológicos potencialmente destructivos. Las nanopartículas se pueden emplear para probar biomoléculas como biomarcadores y marcadores tumorales. Los productos nanomédicos van desde la quimioterapia hasta los agentes biológicos, pasando por la inmunoterapia y más. La nanotecnología también puede ser utilizada por moléculas que identifican enfermedades para mejorar el diagnóstico selectivo. El uso más prometedor de la nanomedicina en la quimioterapia se ha producido en aquellos casos en los que las capacidades únicas y las características complejas de estos instrumentos de administración de última generación podrían mejorar significativamente la eficiencia y, al mismo tiempo, reducir el potencial.En el diverso campo de la nanotecnología, casi todos los aspectos de la industria, desde los medicamentos hasta las máquinas, están experimentando enormes avances. Su uso extensivo significa que su relación beneficio-riesgo se ha convertido en tema de discusión global. La nanotecnología tiene graves efectos sociales y económicos y poca conciencia pública de sus amenazas. Las industrias y las empresas farmacéuticas se entregan a esta tecnología por los impactos inmediatos y a largo plazo de los productos basados en nanotecnología.
La nanorrobótica se puede utilizar para monitorear enfermedades y farmacocinética y mejorar la eficiencia de la atención médica y la administración de medicamentos en la terapia del cáncer. La nanorrobótica también se utiliza para mantener y ensamblar sistemas avanzados. El uso extensivo de la nanorrobótica también está impulsando el aumento de los ingresos del mercado en el sector médico.
8 . Alcance futuro
En el futuro, la nanomedicina desempeñará un papel crucial en la medicina personalizada, desde la predicción hasta el seguimiento. Los materiales a escala nanométrica son la base de sensores y biomarcadores cada vez más sensibles, que pueden utilizarse para identificar más enfermedades en una fase preliminar de forma simultánea y precisa. La nanomedicina permite un mapeo altamente preciso de la enfermedad con una mayor focalización y sensibilidad química. Después de diagnosticar una afección, la nanomedicina puede emplearse de manera más eficiente para atacar las células, al tiempo que se reducen los efectos secundarios y el daño a las células sanas. Ya se están utilizando varios productos, incluida la doxorrubicina nanoencapsulada mencionada anteriormente . En esencia, los desafíos futuros incluyen avances en la carga y liberación de medicamentos y el mayor desarrollo del potencial para diagnosticar y tratar las nanopartículas metálicas .Como toda tecnología avanzada, la nanomedicina debe contrarrestar su atractivo potencial frente a los peligros del futuro. Como ocurre con cualquier dispositivo y tratamiento médico, la nanomedicina debe controlarse rigurosamente y evaluarse a fondo antes de tratar a los pacientes con todo su potencial, se deben realizar evaluaciones de toxicidad y estudios clínicos en varias etapas. En el futuro, la nanotecnología puede detectar problemas sobre el terreno en lugar de depender de una combinación de datos procedentes de sensores externos, conocimientos médicos y algoritmos de diagnóstico probabilísticos. El uso de la nanotecnología por parte de los atletas también podría ser una aplicación adicional para evaluar qué músculos tienen una circulación excelente y desarrollan menos ácido láctico, lo que permitiría a los atletas reaccionar ante sus músculos menos efectivos modificando la frecuencia y el entrenamiento. Estos pueden ajustar su eficiencia y maximizar su potencial muscular menos efectivo.
9. Limitaciones
Los problemas de reproducibilidad y control de calidad de los nanomateriales, el establecimiento de escalabilidad y mayores tasas de producción, y la gestión de subproductos no deseados de la nanoingeniería son barreras científicas y tecnológicas importantes. El precio sigue siendo muy alto, mientras que las nanopartículas siguen siendo desconocidas en cuanto a sus consecuencias para la salud y el medio ambiente. Por lo tanto, continúan los obstáculos estructurales para la implementación; los inversores siguen siendo cautelosos y las inversiones nanoterapéuticas son relativamente reticentes para las industrias farmacéuticas. Aunque la nanotecnología tiene muchas nuevas aplicaciones potenciales, su uso en las ciencias biológicas está limitado por ciertos obstáculos que deben eliminarse con mayor frecuencia antes de su uso. La aplicación de la nanotecnología in vivo todavía plantea preocupaciones sobre su influencia a corto y largo plazo en el cuerpo. Debido al pequeño número de partículas en los tratamientos, estas partículas pueden eludir completamente el sistema inmunológico, sortear obstáculos naturales y acumularse en tejidos específicos, lo que ocasionalmente puede dar lugar a una masa que el cuerpo no puede percibir fácilmente.
10. Conclusión
La revolución de la atención sanitaria está impulsada por la nanotecnología, que hace hincapié en la gestión preventiva de la salud de la población. La nanotecnología ayuda a resolver el problema de la administración de tratamientos específicos, reduce el peligro de efectos secundarios y maximiza la eficacia terapéutica. Esta tecnología es adecuada para identificar, tratar y realizar terapias genéticas contra el cáncer. La nanomedicina es el uso más prometedor de la nanorrobótica . Sus aplicaciones abarcan varios campos, como la creación de vacunas, la administración de medicamentos, equipos portátiles, equipos de diagnóstico y obtención de imágenes y productos antimicrobianos. Se prevé que el desarrollo de medicamentos más eficaces, dispositivos mejorados y la detección temprana de diversas enfermedades conduzcan a la nanomedicina. La combinación de medicamentos estándar contra el cáncer con tecnologías a nanoescala puede atravesar intactos y circular dentro del cerebro. Esta tecnología ofrece enormes mercados potenciales y beneficios, clases completas de medicamentos actuales. La nanomedicina se produce mediante una mezcla crítica de manganeso y citrato utilizando técnicas nanotecnológicas. Es posible desarrollar mecanismos personalizados para la administración de medicamentos, nuevos métodos de diagnóstico y dispositivos médicos a nanoescala.












