Parte 10 de 10
Autor: Carlos Alberto Díaz. Profesor Titular Universidad ISALUD.
Criterios de priorización.
No existe acuerdo para establecer la priorización de las tecnologías sanitarias, la innovación, a saber: la efectividad clínica, costo efectividad, impacto presupuestario, impacto en la equidad, aceptabilidad, impacto organizacional, priorización de grupos vulnerables, disponibilidad de alternativas, carga de enfermedad, gravedad de la condición, pronóstico en el corto plazo.
Citaría algunos criterios explicitos de priorización.
La prevalencia epidémica, carga de enfermedad y carga sanitaria.
Actuar sobre las patologías que generan mayor cantidad de años potencialmente perdidos.
Frecuencia de los procesos, priorizando en dos niveles o fortaleciendo fundamentalmente la atención primaria, para una mejor contención y postergar las complicaciones.
Impacto económico.
Impacto clínico. Curación.
Carencia de alternativas.
Gravedad del proceso.
Mejorar la accesibilidad.
Vías de distribución diferentes para dispositivos y medicamentos
Evaluar localmente antes de liberar su uso. Especialmente por el cociente particular de costo efectividad incremental para el país y no con evaluaciones de países desarrollados.
Establecer una regulación pública en el mercado distinta de la actual, con bajas barreras de accesibilidad y libertad para fijar precios de venta.
Generando una mayor fortaleza en la gobernanza del sector, utilizando las herramientas actuales como la superintendencia, la gestión de la obra social para jubilados y pensionados y el COFESA, para el sector público de las provincias. No esperando la agencia de evaluación de tecnologías o una ley complementaria de salud, que será sometida a todas las presiones y seguramente salga como un híbrido gatopardista.
Priorización vía judicialización
Esta es una de las priorizaciones que más afecta la justicia social, porque no atiende el componente sistémico o poblacional, sino el individuo, en una asignación injusta, se pueden distraer fondos en indicaciones fútiles.
la judicialización atenta contra la justicia distributiva, no promueve la eficiencia, no siempre es efectiva, afecta negociaciones de precio, porque ante el amparo judicial el precio es lo que fija el proveedor o productor. Son ejemplos de la realidad reciente el nursinensen o el eculizimab.
Da lugar a la preponderancia de la variabilidad generada por la teoría del médico entusiasta.
Canales de difusión de la tecnología.
Las sociedades científicas secularmente tuvieron prestigio, pero algunas de ellas, en determinados países han sido coaptadas por el complejo industrial médico, por los laboratorios farmacéuticos, por los fabricantes de dispositivos o de tecnología diagnóstica.

Cabe preguntarse, preguntarnos, si la priorización es la que determina el valor social de las intervenciones sanitarias, que son: la gravedad de la patología, su estadio, el potencial de mejora o los beneficios-utilidad-efectividad, la edad, el costo de la intervención, las características personales de los beneficiarios. [i]
La gravedad de la patología es uno de los factores más importantes a considerar, ese umbral de gravedad puede estar en el 30% de la salud normal para ser priorizable. Luego de la gravedad vienen los beneficios de los tratamientos, las evidencias disponibles sugieren que la sociedad tiende a conceder al menos la misma prioridad a quienes gozan de menor potencial de mejora, que el estado de salud que alcanza el paciente después del tratamiento, existiendo un menor apoyo de priorización del paciente con menor potencial de mejora.
Con respecto a la edad, existe evidencia que muestra un apoyo limitado a utilizarla como criterio de racionamiento. Hay una tendencia más favorable a atribuir un mayor peso a los jóvenes frente a los mayores, pero no es como valor social una relación monótona decreciente, sino que hay puntos de inflexión correspondiente a relaciones no lineales.
Los factores que más han concitado la predisposición de los decisores a priorizar sobre su base son: la existencia de personas que dependen del paciente (niños y/o ancianos), la responsabilidad (los estilos de vida) y la clase social.
La priorización es curar, o cuidar a pacientes con niños a cargo, priorizar a los no fumadores de los fumadores, o a los que tienen un estilo de vida responsable, que a los que no lo tienen.
También existe evidencia que hay priorización en el sector público a los que pertenecen a clase sociales más bajas.
No ocurre con nuestro sector de prepagas, ni con otros, que se vincula más a capacidad de pago. Existe evidencia que los ciudadanos están dispuestos a renunciar a la maximización de las ganancias en salud para la sociedad, con el fin de beneficiar a determinados grupos de población, siempre que no estén afectados o que sean sujetos de necesidad.
Desafíos:
Como se expresó, el desafío esta provocado por las tensiones que genera el alza de los precios de las nuevas tecnologías, por encima del crecimiento económico, imposibles de financiar a esos precios y con estos recursos. La presión alcista nunca fue tan fuerte. Acompañados de un déficit de gobernanza, de falta de incentivos, para la eficiencia, o que puedan decir que estamos en busca de un modelo.
Falta de un espacio de colaboración público-privada. Falta absoluta de consensos en política sanitaria. La inoperancia del “buenísmo” en la justicia y en la normativa emanada del Congreso Nacional. Hacen que se impongan amparos que exijan cobertura de prestaciones de bajo valor terapéutico. En este contexto, dar más cobertura y universalismo, será como dar “barra libre, a un grupo de alcohólicos”.Los desafíos estarán en adoptar innovaciones costo efectivas, que, siendo aprobadas y cubiertas por los principales financiadores, se compre adecuadamente, al menor precio posible, impulsando mecanismos de competencias. Boldrin y Levine subrayan que las innovaciones contenidas en la protección de las patentes, que no remedian el mantenimiento de los secretos industriales y que no contribuyen a la comunicación de las ideas.[i]
Hacer las prestaciones más efectivas y con menos desperdicios para poder reasignar recursos a los medicamentos innovadores. Desarrollar políticas de calidad institucional y de las prestaciones, disminuir los eventos adversos, acreditar procesos. Pero no solo de los establecimientos hospitalarios, sino de los sistemas de salud: Municipales, provinciales, Nacionales. La prescripción ambulatoria. Identificar conflictos de intereses con los médicos.
Generar una agencia de evaluación de tecnologías creíble y que sus dictámenes sean compartidos y convalidados. Primero la efectividad clínica, luego la coste efectividad y la evaluación económica de la mejora incremental. Que esta institución incorpore sus dictámenes, como requisitos para guiar la toma de decisiones sobre financiación y priorización. Siguiendo la estela de otros países, a la cabeza de ello el Reino Unido, Suecia, Holanda, y España. La información que proporciona los ACE se presenta en términos del coste incremental por unidad de efectividad en salud ganada de una tecnología frente a su comparador, los Años de Vida Ajustados por Calidad. Esto genera un valor umbral, el del coste efectividad incremental. Pero no es absoluto.

[i] Boldrin M. Levine DK. The case against patents. Journal of economic perspectives. 2013. 27.1 3-22
[i] Abellán Perpiñan JM. ¿Cómo debería financiarse la innovación en un escenario de gesto público restrictivo? Capítulo 4. 89-116. Innovación y regulación en Biomedicina: Obligados a entenderse. 2017.
Conclusiones:
Desarrollar una agencia de tecnologías de salud, que sea vinculante en sus determinaciones para las obras sociales. Resultaría una medida institucional fundacional. Lo importante sería generar una dinámica adecuada en las nuevas incorporaciones y además revisar los casos más conflictivos. La conformación independiente y con solvencia técnica. Que sus dictámenes sirvan para orientar la aprobación, la cobertura, las indicaciones.
Fortalecer la primera relación de agencia en una atención primaria fortalecida, para que se contenga la necesidad de la población y se den respuestas. Tecnología en atención primaria ampliada, Una atención primaria basada en equipos interdisciplinares que tengan población a cargo, recursos diagnósticos y de tratamiento,
Historia clínica y recetas electrónicas. Generar un sistema de información compatible en el sistema de cobertura universal de salud, debe ser una tecnología de innovación, que se debería revisar, para generar BIG DATA de nuestro sistema de salud. Revisar experiencias internacionales. Realizar inversión importante en todos los centros hospitalarios públicos, centros de atención primaria, y exigir su implementación en los financiadores y las obras sociales, para que en cinco años se empiecen a observar datos.
Redes multihospitalarias.Generar un sistema que replique la innovación generada en la experiencia de la provincia de buenos aires. Donde exista un establecimiento de referencia y la población este nominalizada.
Formas de pago por desempeño, para pagar por compromisos de gestión, de esa forma incentivar la calidad y la eficiencia.
Sistemas locales de salud. Esta tecnología de gestión pública de salud sería una herramienta indispensable, para disminuir las desigualdades injustas. Implementar redes. Cooperación público municipal-provincial, como asi también entre público y privado.
Contratos e incentivos para la formación de recursos humanos indispensables: enfermeros, anestesistas, terapistas pediátricos, neonatólogos, excelentes clínicos, terapistas intensivos, cirujanos infantiles, médicos de familia o generalistas.
Colocar a todos los habitantes bajo programa de atención. Es un cambio radical, generará un modelo de atención diferente centrado en la persona, la familia y el entorno de salud con las instalaciones y el personal adecuado, para que sean la puerta de entrada y los protagonistas en la transición del cuidado.
Hospitales actualizados tecnológicamente, con planteles completos y que hayan revisado los procesos pensando en los usuarios.[i]
Desarrollar un mercado de biosimilares.Continuar aumentado la inversión en los clústeres tecnológicos e implementar nuevos actores institucionales. Desarrollar estrategias regionales con Brasil, Colombia y México.
Revisar el esquema arancelario de las tecnologías sanitarias.Favorecer el acceso al país de las tecnologías efectivas en otros sistemas, para que lleguen con menores aranceles y esto sea un incentivo económico.
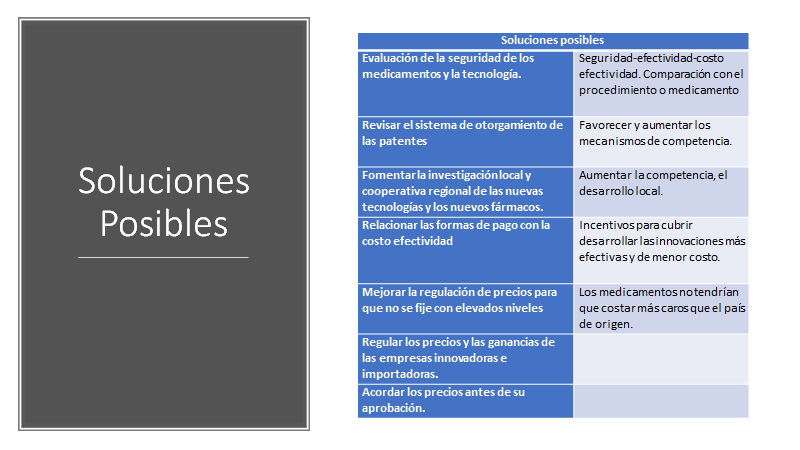
Regular precio de los medicamentos con precios de referencia, vinculados con la comparación con países centrales.Establecer un esquema de precio de referencia, con los laboratorios propietarios de tecnología, para que el precio en nuestro país sea igual que en los países centrales y no más costosos como hoy.
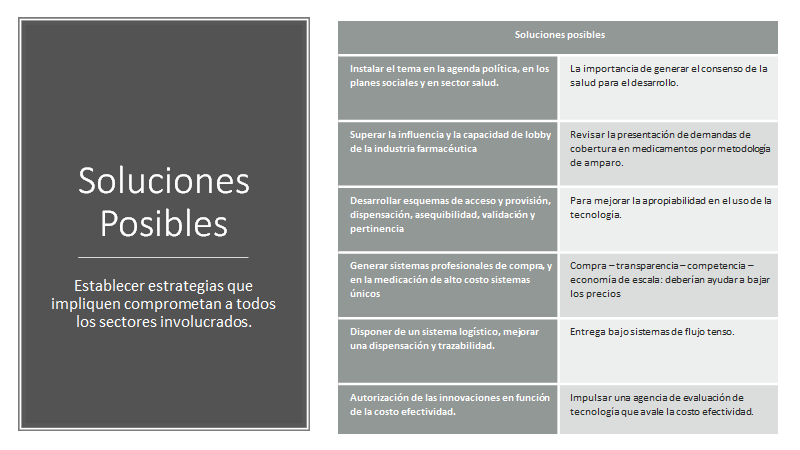
Instalar el tema en la agenda política. Parece que será muy difícil instalar el tema en la gestión política de salud de la Argentina en estos momentos. Recomponer la ética. El sistema técnico de toma de decisiones. Los sistemas de información de consumos. Evitar los conflictos de intereses.
Eludir la influencia y la capacidad de lobby de la industria farmacéutica. Generando competencia, gestión de compras profesional.
Desarrollar esquemas de acceso y provisión que construyan equidad. Pero las medidas que se impulsen será preservar los negocios, los niveles de venta, las inversiones, la innovación, la propiedad del conocimiento, su difusión adecuada, generar conocimiento para aumentar la adhesión, pero no los precios y se estimulará la competencia.
Generar en el estado un sistema de comprador único, para todas estas innovaciones, que se trazarán de acuerdo con el paciente que sea prescripto y quién lo realice. La oferta de comprador eficiente y responsable, no único, pero si servir de ser una referencia que vencer. Poner en dificultades a los que compran a mayor valor las tecnologías.
Disponer de un sistema logístico-dispensación y trazabilidad para poder entregar los medicamentos a sus pacientes en tiempo y forma. La logística de flujo tenso. Acortar tiempo de entrega de los bienes. De instalación de nuevas tecnologías.
Evaluar la seguridad y los resultados en enfermedades raras que no tenían tratamiento. Las evaluaciones, la priorización cambia si se consideran enfermedades raras, situaciones especiales, también si la intervención incentivará más la innovación científica, no hay terapias disponibles, que los pacientes sean socialmente desfavorecidos, que el tratamiento que coloquemos prolonga la vida, la condición que es tratada es limitada en el tiempo. Las intervenciones ante enfermedades raras en general, y los medicamentos huérfanos en particular, no poder reunir escasas evidencias sobre su eficacia y efectividad. [i] [ii]
[i] Espín J, Brosa M, Oliva J, Trapero-Bertrán M y Key4Value-GrupoIII. Cuestiones controvertidas en evaluación económica (III): La evaluación económica de intervenciones sanitarias en tres situaciones especiales: Enfermedades raras, los tratamientos al final de la vida y las externalidades en las evaluaciones. Rev Esp Salud Pub. 2015; 89(3): en prensa. Disponible en: http://www.msssi.gob.es/biblioPublic/publicaciones/recursos_propios/resp/revista_cdrom/vol89/vol89_3/RS893C_J B. pdf
[ii] López-Bastida J, Oliva J, Antoñanzas F, García-Altés A, Gisbert R, Mar J y Puig-Junoy J. Propuesta de guía para la evaluación económica aplicada a las tecnologías sanitarias. Gac Sanit. 2010; 24: 154-70
[i] González López Valcárcel B. Zozaya González N. Tecnologías para nacer y tecnologías para morir ¿Cuál es el papel de los incentivos en la velocidad del proceso de adopción de las innovaciones? Capítulo 8. 2017.
Fomentar la investigación para incrementar el desarrollo de nuevos fármacos.Generar una oferta competitiva de laboratorios, tecnología e investigadores para desarrollar trabajos que se necesitan en fase 2 para pasar la fase siguiente.
Mejorar la regulación de precios de la innovación farmacéutica. Contratos de riesgo compartido. Monto de tratamientos. Acordar precios diferenciales en función de un país desigual y tener mucha gente de bajos ingresos.
Controlar con racionalidad la prescripción médica, la demanda Creciente de la población más informada y los incentivos del mercado, desde el complejo industrial médico.
Regular los precios y las ganancias de las empresas innovadoras e importadoras de las innovaciones. Si cumplen con el ahorro de costos y la mejora en la calidad y cantidad de vida, no deberían pagar impuestos.
Impulsar mayor competencia dentro de este mercado. Estados Unidos en 2009 despliega la Ley de Competencia e Innovación Biológicos Precio (Ley de biosimilares) crea una aprobación rápida vía FDA (Food Drugs Administration) para autorizar la comercialización de productos biológicos genéricos con el ánimo de reducir los costos de la atención sanitaria (Stroud, 2011).[i] Esta aprobación acelerada elimina la necesidad de los ensayos en humanos reduciendo los costos para los fabricantes de genéricos, promoviendo la competencia de precios después de la expiración de la patente del medicamento original (Stroud, 2011).
[i] Stroud J. The illusion of interchangeability: The benefits and dangers of Guidance plus rulemarking in the FDA Biosimilar approval process. 2011.599-643
Es imperativo, prioritario y racionalizador, privilegiar el análisis y la inserción de la innovación en los recursos de diagnóstico y tratamiento.
Lo que resulta fundamental son tres cosas, primero si es innovación o no, segundo si es seguro o no, su aplicación y tercero, si el precio que se fija tiene relación a los costos de producción.
La primera consideración se justifica en que muchas de las iniciativas postuladas no son innovaciones, no brindan los resultados que prometen, y lo más importante que se pone en los precios de las presentaciones no responden, no responden a ninguna lógica de costo de producción. Por lo tanto, incurren en rentabilidad abusiva, teñido de opacidad en la inserción en un mercado protegido, bajo las patentes, el poder del lobby. Quedando en claro que no es el precio, el único factor, sino la seguridad, la mejora en los resultados, la pertinencia, la efectividad, los elementos fundamentales para su prescripción e indicación. Este análisis debe estar en manos de los grandes compradores, la superintendencia de servicios de salud, la futura agencia de tecnología, y los Ministerios de Salud, para priorizar y aliviar la tensión innovación-regulación.
Por lo tanto, como quedó expresado, esto no será posible si no hay una mejora institucional, de la gobernanza y de la función de rectoría, de las competencias instaladas en el sector público, más profesionalismos gerenciales, menos gestores-comisarios políticos.
Será muy difícil implementar la innovación sanitaria costo efectiva, sin una mejor calidad de la política y de las instituciones que la están condicionando. Fomento de la transparencia en precio y en las negociaciones.
Actualizar las tecnologías tuteladas, para detener el desfinanciamiento actual de las obras sociales, los subsidios cruzados desde la seguridad social a los monotributistas, desde las obras sociales que reciben jubilados por 192 pesos y el costo de la cápita es de 2000. [i]
Este documento quiere además dar testimonio que las innovaciones, correctamente utilizadas, controlados los precios, financiando la investigación, permitirá que se genere un acceso equitativo, mayor cobertura, mejor financiación y servicio, exigiendo que estos proveedores se adecuen a las limitaciones en las transformaciones del sector tanto económicas, organizativas y del conocimiento.
[i] Nieto Rueda J. La financiación y fijación de precios de medicamentos desde la perspectiva de la regulación económica eficiente y la promoción de la competencia. Comentarios al Informe de la CNMC. Boletín Informativo Economía y Salud. 2016, nº 87. Accesible en: http://www.aes.es/boletines/news.php?idB=28&idN=1407