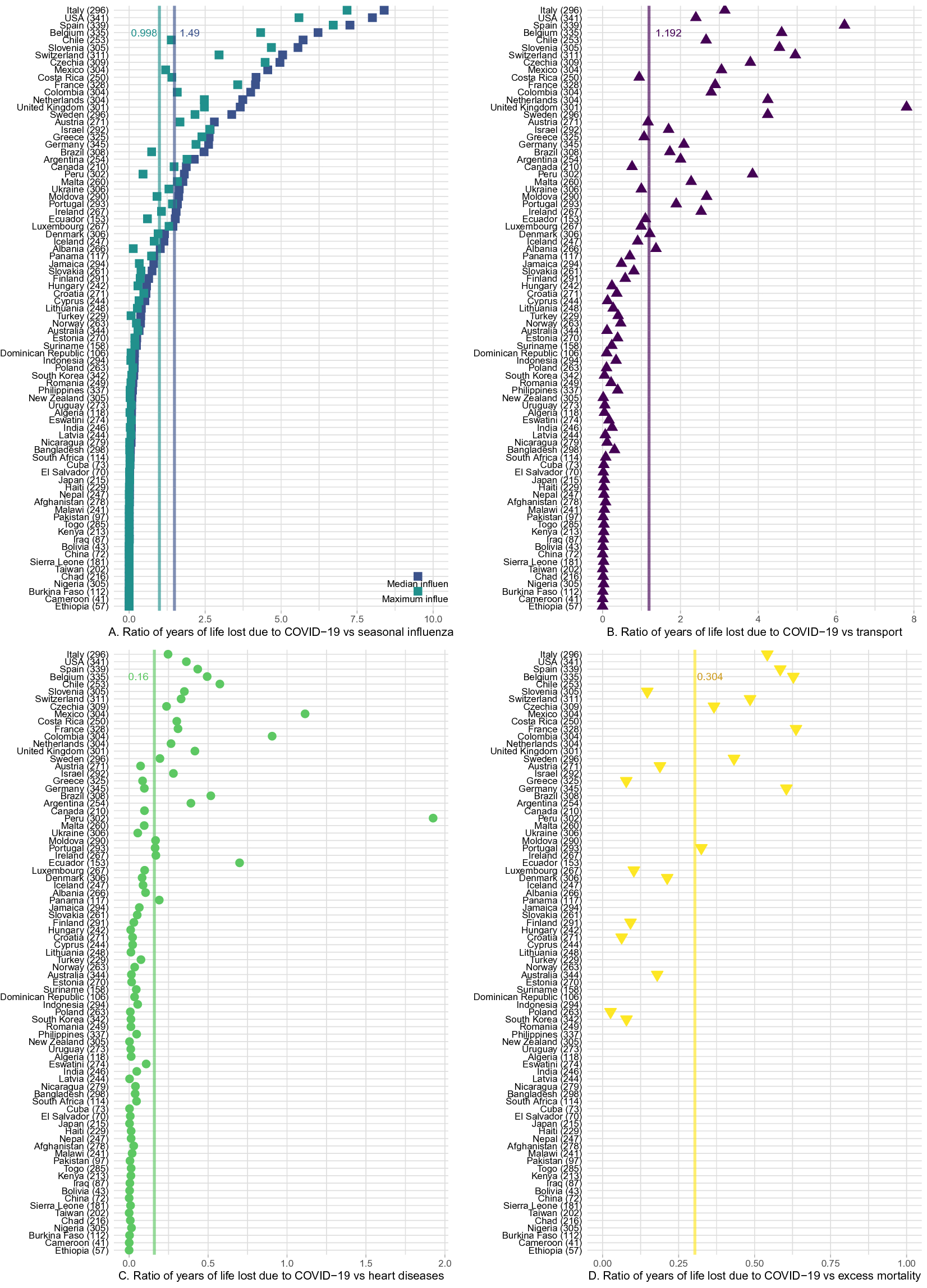
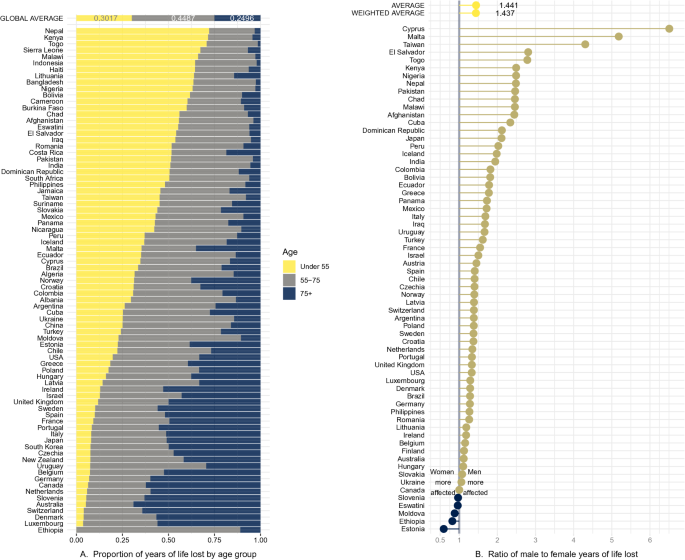
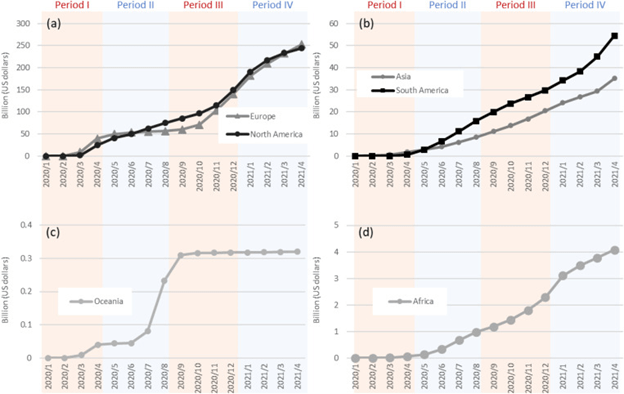
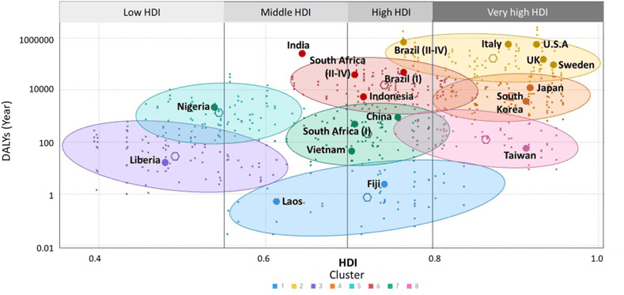
Geerts J et al JAMA. Journal 8 de Julio 2021.
Pregunta ¿Qué imperativos de liderazgo son más esenciales para los líderes de la salud después de las etapas de emergencia de la pandemia de COVID-19?
Hallazgos En esta declaración de consenso, 32 coautores de 17 países con experiencia en diversos aspectos del liderazgo de la salud, la atención médica, la salud pública y campos relacionados describen 10 imperativos para guiar a los líderes a través de la recuperación de las etapas de emergencia de la pandemia. Las capacidades clave de liderazgo y las preguntas de reflexión se presentan para guiar a los líderes y estructurar las revisiones de desempeño.
Lo que significa que los líderes que implementan este marco de manera más efectiva están en una posición ideal para abordar las necesidades urgentes y las desigualdades en los sistemas de salud y para cocrear una cultura dentro de sus organizaciones que sirva mejor a su gente.abstracto
Importancia La pandemia de COVID-19 es la mayor prueba global de liderazgo sanitario de nuestra generación. Existe una necesidad urgente de proporcionar orientación a los líderes a todos los niveles durante la etapa de recuperación previa a la resolución sin precedentes.
Objetivo Crear un marco de imperativos de liderazgo basado en la evidencia y la experiencia que sirva como un recurso para guiar a los líderes de salud y salud pública durante la etapa posterior a la emergencia de la pandemia.
Revisión de la evidencia Una búsqueda bibliográfica en PubMed, MEDLINE y Embase reveló 10 910 artículos publicados entre 2000 y 2021 que incluían los términos liderazgo y variaciones de emergencia, crisis, desastre, pandemia, COVID-19o salud pública. Utilizando la guía de informes de excelencia de los Estándares para la Mejora de la Calidad para el desarrollo de declaraciones de consenso, esta evaluación adoptó un enfoque Delphi modificado de 6 rondas que involucró a 32 coautores expertos de 17 países que participaron en la creación y validación de un marco que describe los imperativos esenciales de liderazgo.
Conclusiones Los 10 imperativos del marco son: (1) reconocer al personal y celebrar los éxitos; 2) prestar apoyo al bienestar del personal; (3) desarrollar una comprensión clara del contexto local y global actual, junto con proyecciones informadas; (4) prepararse para futuras emergencias (personal, recursos, protocolos, planes de contingencia, coaliciones y capacitación); (5) reevaluar las prioridades explícita y regularmente y proporcionar propósito, significado y dirección; (6) maximizar el desempeño del equipo, la organización y el sistema y discutir las mejoras; (7) gestionar la acumulación de servicios en pausa y considerar mejoras evitando el agotamiento y la angustia moral; (8) sostener el aprendizaje, las innovaciones y las colaboraciones, e imaginar las posibilidades futuras; (9) proporcionar comunicación regular y generar confianza; y (10) en consulta con la salud pública y otros líderes, proporcionar información y recomendaciones de seguridad al gobierno, otras organizaciones, el personal y la comunidad para mejorar la atención equitativa e integrada y la preparación para emergencias en todo el sistema.
Conclusiones y relevancia Los líderes que implementan estos imperativos de manera más efectiva están en una posición ideal para abordar las necesidades urgentes y las desigualdades en los sistemas de salud y para cocrear con sus organizaciones un futuro que sirva mejor a las partes interesadas y las comunidades.Introducción
La pandemia de COVID-19 es la mayor prueba mundial de liderazgo sanitario de nuestra generación. 1,2 Aunque se dispone de algunas lecciones de epidemias a partir de las experiencias del síndrome respiratorio agudo severo (SRAS) y el síndrome respiratorio de Oriente Medio (MERS), pocas jurisdicciones estaban preparadas para gestionar esta crisis de manera eficaz. 3–5 El COVID-19 ha puesto de relieve la interdependencia mundial,2,4,6 y, en consecuencia, el Dr. Tedros Adhanom Ghebreyesus, director general de la Organización Mundial de la Salud (OMS), declaró: «La mayor amenaza a la que nos enfrentamos ahora no es el virus en sí, es la falta de solidaridad global y liderazgo global». 7.
La pandemia ha puesto al descubierto y exacerbado las brechas y las grandes desigualdades en los sistemas de salud,5,8,9, incluidos los problemas estructurales, sociales, políticos y económicos subyacentes de una manera innegablemente gráfica. 6 En consecuencia, se ha pedido un cambio social sistémico y se ha presionado a los gobiernos para que aborden estas cuestiones y garanticen que se satisfagan las necesidades de las poblaciones prioritarias y en riesgo. 10
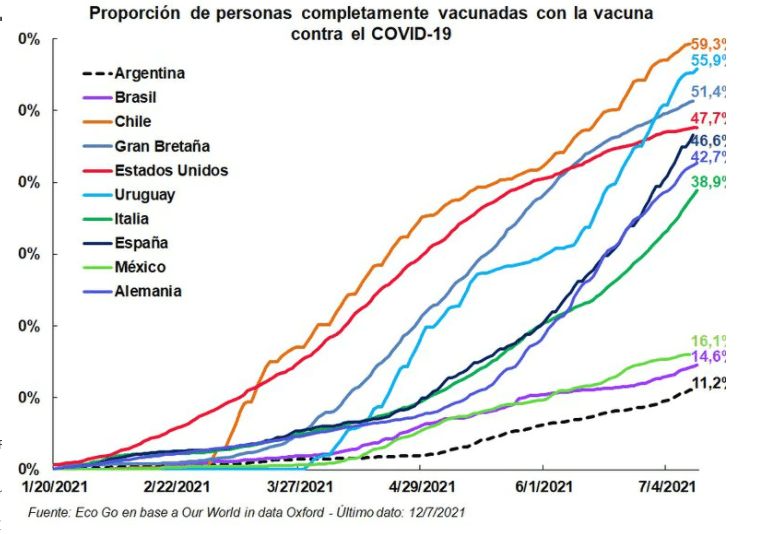
Incluso con la distribución generalizada de vacunas, los plazos previstos para lograr la inmunidad de rebaño internacional se han ido alargando11 y algunos expertos sugieren que existe una necesidad crítica de prepararse para el potencial endémico de los resurgimientos persistentes y estacionales del virus. 12,13 Además, una carta del Dr. Tedros y 26 jefes de Estado afirmaba que «la cuestión no es si, sino cuándo» surgirán futuras pandemias,2 que el Dr. Mike Ryan, director ejecutivo del Programa de Emergencias Sanitarias de la OMS, sugiere que puede ser aún más letal. 14.
La naturaleza sin precedentes y en alto riesgo de este fenómeno mundial pone de relieve la necesidad urgente de una orientación clara para apoyar a los dirigentes de todos los niveles a navegar el curso de esta crisis y prepararse para las que vendrán. 2,15El contexto: 4 etapas de una crisis
La pandemia de COVID-19 y otras crisis globales se pueden entender en un modelo novedoso de 4 etapas progresivas superpuestas: 1) escalada, 2) emergencia, 3) recuperación y 4) resolución. 16 La etapa de escalamiento (etapa 1) se caracteriza predominantemente por una comprensión cada vez mayor, a menudo basada en información limitada, errática o sin fundamento, de que una amenaza externa está invadiendo, y por la necesidad de preparativos rápidos. La etapa de emergencia (etapa 2) se centra en el liderazgo al inicio de una amenaza, cuando es directa y local. La etapa de recuperación (etapa 3) es altamente caprichosa porque, aunque es menos aguda que la fase anterior, puede haber fatiga o agotamiento generalizado del personal y de la comunidad, junto con una amenaza potencial prolongada de volver a un estado de emergencia en cualquier momento en reacción a un resurgimiento. La etapa de resolución (etapa 4) implica abordar las repercusiones de la crisis y, posteriormente, establecer prioridades, idealmente junto con una discusión creativa colectiva de oportunidades y estrategias postcrisis para lograr una nueva (y esperemos) mejor realidad.
El avance a través de estas etapas puede no ser lineal dada la naturaleza volátil de las crisis, y la superposición es inevitable, especialmente a medida que surgen y amainan los resurgimientos. A nivel mundial, la amenaza del COVID-19 está lejos de terminar, ya que aunque varias jurisdicciones han resistido las olas iniciales de la pandemia y ahora están en la etapa de recuperación, otras permanecen en la agonía de la tormenta o pronto pueden regresar a ella antes de la transición a la recuperación.La etapa de recuperación: Etapa 3
Este informe se centra en los imperativos de liderazgo durante la etapa de recuperación, que requiere el mayor espectro de capacidades en cualquier etapa de una crisis y en comparación con las situaciones no críticas. El desafío único de liderazgo durante la etapa 3 es equilibrar las prioridades en competencia, mantener el compromiso y la motivación del personal, y evitar el agotamiento dentro de un entorno poste-emergencia que sigue siendo volátil, incierto, complejo y ambiguo (conocido en la teoría de la gestión como VUCA). 4,17 Cuanto más tiempo persista cada entrega de la etapa de recuperación y con mayor frecuencia se deba reevaluar las prioridades, reprogramar y reorganizar la logística a medida que cambia la situación, más desafiante se vuelve el liderazgo en este contexto. 18 La etapa 3 también ofrece oportunidades sin precedentes a todos los niveles para capitalizar las improvisaciones, innovaciones, colaboraciones y lecciones aprendidas durante las etapas de emergencia para mejorar el rendimiento y la atención y abordar las necesidades y desigualdades en las comunidades. 9
La etapa de recuperación exige una versatilidad más allá de la capacidad de cualquier líder individual. En contraste con un enfoque directivo, de arriba hacia abajo, que se aplica comúnmente en emergencias, el sello distintivo de la efectividad en la etapa de recuperación es una mejor distribución del liderazgo en todo el sistema, más allá del «organigrama» inmediato. En este contexto, es esencial un enfoque evolutivo, experimental, adaptativo, coordinado y colaborativo. Para tener éxito, se requiere alineación en torno a un propósito compartido y objetivos comunes, así como líderes que liberen cierto control y establezcan y mantengan altos niveles de confianza entre las partes interesadas clave. 5,19–22Propósito del Marco
El propósito de crear un marco de liderazgo basado en la evidencia y la experiencia para la etapa de recuperación de la pandemia de COVID-19 era que potencialmente sirviera como un recurso para guiar a los líderes de salud y salud pública, incluidos aquellos en roles de liderazgo posicionales o informales en todos los niveles y en organizaciones de cualquier tamaño. El marco también podría proporcionar una estructura para las revisiones de los líderes individuales, el equipo y el desempeño organizacional, que podría usarse para aumentar la resiliencia, la capacidad, la innovación y la preparación para emergencias de la organización.
Aunque existe un cuerpo establecido de conocimientos que es relevante para la etapa de emergencia, incluyendo estudios sobre preparación para desastres,23,24 gestión de recursos de crisis,25 y liderazgo en crisis,26,27 hasta donde sabemos, no hay un marco comparable en la literatura para la etapa de recuperación. La necesidad de una orientación creíble es urgente, especialmente si las predicciones de los expertos son correctas y esta pandemia se vuelve endémica, en cuyo caso las variaciones de la etapa 3 pueden convertirse en la nueva realidad. 12 Además, la medida en que los dirigentes aplican efectivamente los imperativos en la etapa de recuperación está directamente relacionada con el éxito en las iteraciones posteriores de la etapa de emergencia (etapa 2), así como durante la etapa de resolución (etapa 4). 4,9,28
Un marco basado en la evidencia y la experiencia: 10 imperativos para los líderes de la salud durante la etapa de recuperación de una crisis
Después de 6 rondas de revisiones, nuestro equipo llegó a un consenso sobre 10 imperativos de liderazgo para la etapa de recuperación de la crisis covid-19, con las capacidades correspondientes para cada uno y preguntas de reflexión para que los líderes autoevaluen su liderazgo y capacidad organizativa (Tabla). Los imperativos se presentan en 6 grupos (Figura): enfoque de las personas (1 y 2); exploración ambiental (enfoque presente y futuro) (3); aprendizaje y preparación (enfoque pasado y futuro) (4); recalibrar, optimizar, organizar (enfoque actual) (5, 6 y 7); prever (enfoque futuro) (8); y comunicación de crisis (9 y 10).Enfoque en las personasReconocer al personal y celebrar los éxitos
Después de la etapa de emergencia, para aumentar y mantener la moral, hay una necesidad esencial de reconocer y celebrar la dedicación, la resiliencia y los logros del personal. 5,9,37,38 El reconocimiento puede revitalizar e inspirar a individuos, equipos, organizaciones y comunidades, así como aumentar su desempeño. 39,40 Esta es también una oportunidad para reforzar a través de la alabanza los comportamientos que se consideran vitales para mejorar los resultados de los pacientes en el futuro, incluyendo que la respuesta exitosa a la crisis se basa en el liderazgo y las contribuciones, grandes y pequeñas, de todos en la organización.Proporcionar apoyo para el bienestar del personal
El agotamiento y los problemas de salud mental han aumentado durante la pandemia, particularmente entre los profesionales de la salud, ya que muchos han quedado traumatizados por experiencias de primera mano o por la incertidumbre sostenida, el riesgo para la salud y el agotamiento. 21,41–43 Además de su trabajo profesional, muchos también han tenido que cuidar de parientes ancianos y/o manejar a los niños en el hogar debido a los cierres de guarderías y escuelas, ya que los límites entre el trabajo y la vida en el hogar se han desdibujado de manera deleténea. 18 Cuanto más persista la pandemia, mayor será la probabilidad de que la crisis se detecte y latente en las personas. 21,43,44 Los líderes deben demostrar inteligencia emocional,42 empatía,45 cuidado y compasión,9 y la iniciativa de involucrar al personal de primera línea en su entorno de trabajo. 5,21,46 Allí, los líderes pueden medir su nivel de estrés, comprender sus desafíos, solicitar sus comentarios basados en datos a nivel de unidad y / o sus experiencias, y fomentar su bienestar y resiliencia. 5,47 Visitar las líneas del frente también permite a los líderes ver el impacto de sus decisiones en el punto de atención. Involucrarse con el personal en el campo requiere que los líderes tengan la confianza de que sus colegas pueden sustituirlos de manera efectiva e informarán cualquier cosa urgente de inmediato.
Para desempeñarse de manera efectiva, así como para recuperarse y sanar, el personal necesita acceso a espacios psicológicamente seguros donde puedan expresar confusión, expresar preocupaciones francas y admitir errores sin temor a repercusiones negativas indebidas. 9,18,21,48,49 Ser consciente de la frustración, la culpa y la ansiedad experimentadas por aquellos cuyo trabajo, investigación o aprendizaje / capacitación han sido inevitablemente interrumpidos por la crisis también es indispensable. 5 Cuando sea apropiado, los líderes deben identificar y abordar las preocupaciones no laborales del personal (por ejemplo, preocupaciones familiares o financieras) que pueden afectar negativamente su desempeño. 50 Es esencial que los líderes reconozcan la importancia de las formas tradicionales de sanación —el humor y la risa— y se den cuenta de que, como afirman Empson y Howard-Grenville, «Salir de una experiencia profundamente disruptiva lleva tiempo». 18.
Cambiar de dirección con demasiada frecuencia, innecesariamente o sin una estrategia claramente comunicada también puede contribuir a la fatiga y el agotamiento del personal. 9 El personal necesita descansos esenciales para descansar y recuperarse y para mantener la capacidad organizativa, así como estrategias formales de prevención del agotamiento basadas en sus aportes con respecto a qué componentes serán más significativos. 9,43 Es esencial comunicar la volatilidad de la situación al personal, al tiempo que se infunde confianza en que están en ella a largo plazo y que estarán preparados y apoyados para superar la adversidad, incluso cuando los propios dirigentes experimenten incertidumbre. 5,49 Los líderes también deben promover y modelar el autocuidado. 37 Esto incluye tomarse el tiempo para reflexionar y comunicar adecuadamente sus propias luchas, ya sea a colegas o a un confidente de confianza, y considerar compartir la carga de trabajo más ampliamente. 9,21 Aquellos que experimentan agotamiento o que se sienten abrumados deben tener descanso, recibir apoyo o se les debe permitir la transición a otros roles con un reconocimiento agradecido de sus contribuciones. 43 Los artistas destacados deben ser priorizados para la promoción y la planificación de la sucesión que se basa en la equidad, la diversidad y la inclusión que refleja las comunidades locales que se sirven.Análisis del medio ambienteDesarrollar una comprensión clara del contexto local y global actual, junto con proyecciones informadas
Comprender el contexto local y global actual de esta crisis incluye apreciar su naturaleza VUCA, con la consiguiente humildad y aceptación de que nadie tiene todas las respuestas. 21,37,51 El liderazgo en situaciones complejas y caóticas implica experimentar basado en información imperfecta y contradictoria, incluso de expertos, y preparar a las personas para esperar contratiempos, fallas y adaptaciones en respuesta a resultados en tiempo real. 8,49,52
Para mantenerse actualizados, los líderes deben identificar fuentes confiables de información y expertos clave para ayudar a guiar las decisiones y la formulación de políticas. 5,6,53,54 Esta pandemia ha puesto de relieve explícitamente el papel crucial que deben desempeñar los expertos, así como las consecuencias cuando se ignoran. 8 Cuando se enfrentan a «problemas perversos», un término utilizado en la teoría de la planificación para describir conjuntos complejos e interrelacionados de cuestiones para las que no hay soluciones claras83,en lugar de mostrar una dependencia excesiva de respuestas claras de expertos individuales, el papel del líder es hacer las preguntas correctas a diversos colegas con experiencia relevante, desafiar las suposiciones, fomentar el debate y los enfoques innovadores, y aprovechar su inteligencia colectiva para determinar las prioridades y los próximos pasos. 54
Los líderes también deben analizar la pandemia utilizando el pensamiento sistémico para reconocer la interconectividad de los eventos y los posibles efectos dominó de cómo los desarrollos en otras jurisdicciones podrían afectar en última instancia a sus organizaciones y comunidades, que Heifetz ha descrito como tomar un punto de vista estratégico «desde el balcón». 46 Esto también implica entender qué cambios en el panorama es probable que sean temporales y específicos de una pandemia o etapa frente a los que pueden ser permanentes. 9,21
Este proceso implica el monitoreo de la vigilancia y los datos de notificación de casos sobre cómo el virus se propaga y afecta a los ciudadanos, directa e indirectamente. Es importante centrarse también en qué poblaciones se están viendo afectadas de manera desproporcionada e incorporar estrategias de mitigación oportunas para contrarrestar los impactos. La realización periódica de evaluaciones de riesgos y el modelado de escenarios para proyectar las consecuencias de posibles eventos y respuestas futuras, incluidos los beneficios y los costos de cada uno, es vital para la conciencia situacional y para la resiliencia organizacional y del sistema al anticipar y prepararse para las posibilidades futuras. 9,51,55,56 Del mismo modo, los ejercicios estratégicos de previsión, que implican imaginar escenarios futuros, aclarar supuestos y desarrollar estrategias de respuesta, mejoran la capacidad de sentir, dar forma y adaptarse a eventos futuros, así como de tomar decisiones progresivamente mejores y más oportunas en el presente. 9,28 Los resultados en curso de estos procesos deberían impulsar la acción y la dotación de recursos. 49Aprendizaje y preparaciónPrepárese para futuras emergencias (personal, recursos, protocolos, planes de contingencia, coaliciones y capacitación)
Prepararse activamente para futuras emergencias en la etapa de recuperación es vital2,5,12 y comienza con análisis e informes introspectivos del desempeño individual, departamental, organizacional e interorganizacional durante las primeras etapas de la pandemia. 9,21,49,57 Las lecciones aprendidas deben derivarse de la evaluación sistemática de: lo que funcionó bien; qué fortalezas se pueden aprovechar; y qué no funcionó bien, por qué y qué se necesita para aumentar la infraestructura y manifestar los valores organizacionales. El marco presentado en este artículo se puede utilizar para estructurar este proceso, que debe estar informado por datos de resultados operativos y clínicos y por comentarios anónimos de múltiples fuentes de las partes interesadas clave, incluido el personal de primera línea, las partes interesadas externas, los pacientes, las familias y otros que han sido altamente críticos y / o desproporcionadamente afectados por la crisis. Este proceso debe incluir considerar de qué manera los protocolos operativos de emergencia, las estructuras, las políticas y los planes de contingencia deben mejorarse y actualizarse sobre la base de las aportaciones de las partes interesadas,5, así como las mejores prácticas de liderazgo. 49 Los líderes deben comprometerse a actuar y a obtener recursos para estas sugerencias porque la implementación de las lecciones de experiencias anteriores de pandemias ha demostrado mejorar la eficacia de la respuesta de emergencia posterior y las operaciones actuales. 5,9,58 También es importante identificar a los equipos e individuos que han tenido un desempeño admirable9 y aquellos que deben ser apoyados con capacitación adicional o reasignados. También es valioso discernir colaborativamente si ciertas capacidades, condiciones o capacitación previa contribuyeron significativamente a las diferencias en el rendimiento, ya que esto puede ayudar a identificar cómo seleccionar a los mejores líderes y prepararlos para desempeñarse bajo presión.
Después de esta revisión, el siguiente paso es garantizar que se edistas, tecnológicos y materiales necesarios, lo que incluye una cadena de suministro confiable que responda a la urgencia de la crisis. 49 Esto puede implicar el abastecimiento creativo cuando el suministro es escaso; sin embargo, operar sin los recursos necesarios causa una enorme ansiedad entre el personal y puede poner en peligro su seguridad y eficacia. 5,21,43,59
Las situaciones complejas y de alta presión a menudo fomentan la formación de nuevas coaliciones a medida que diversos grupos se unen para lograr un objetivo compartido que produzca una respuesta adaptativa. 21,60 Estas coaliciones simbióticas a través de silos y con organizaciones asociadas deben mantenerse para proporcionar una atención continua de mayor calidad y aumentar la capacidad del sistema. 53
La capacitación del personal debe centrarse en el proceso de aclarar las funciones y responsabilidades, la adopción coherente de decisiones en situaciones complejas, la asignación de recursos productivos, las aptitudes de comunicación en situaciones de crisis y la adaptabilidad para adaptar las respuestas a las circunstancias fluctuantes, la información imperfecta y las diversas necesidades y funciones del personal. 37 La evidencia muestra que las intervenciones de desarrollo de liderazgo pueden contribuir eficazmente a mejorar con éxito los resultados a nivel individual, organizacional y de beneficio para los pacientes. 61,62 Los líderes necesitan poder confiar en su personal para ejecutar bajo presión e improvisar con la resolución de problemas ad hoc y soluciones creativas5; se debe asegurar al personal que se le apoyará en sus decisiones53 y que las prácticas satisfactorias pueden dar lugar a nuevas normas de procedimiento. 9
Informar adecuadamente sobre el desempeño y los resultados de la pandemia, particularmente durante la etapa de recuperación, es una oportunidad de desarrollo e inversión que no debe desaprovechándose, particularmente en términos de adaptabilidad individual y del sistema, resiliencia, preparación para emergencias y viabilidad futura. 5,55,56,63Recalibrar, optimizar y organizarReevaluar las prioridades de forma explícita y regular y proporcionar propósito, significado y dirección
Es vital renovar las prioridades y proporcionar orientación regularmente a medida que evoluciona la situación,64 especialmente dada la tendencia de las crisis a descarrilar los planes estratégicos de la organización. 37 La etapa de recuperación crea oportunidades sin precedentes para verificar las suposiciones subyacentes y reevaluar con las partes interesadas clave lo que más importa a la organización, incluyendo lo que debe priorizarse y qué servicios deben ser descargados, estacionados o administrados en otro lugar. 9,18 El ciclo iterativo de evaluación periódica de las prioridades debe considerar cómo abordar las necesidades de los grupos de población que han sido pasados por alto o subatendidos5 y cómo equilibrar los beneficios potenciales de las mejoras propuestas y el costo anticipado de la fatiga por el cambio en los niveles de energía y la resistencia de las personas. La comunicación frecuente puede ayudar a reducir la confusión. 37de53
Especialmente a medida que aumenta la incertidumbre, los líderes deben inspirar a las personas con el significado y el propósito37 comunicando explícitamente las constantes ,lo que no está cambiando, a pesar de la volatilidad, como los compromisos con los valores y prioridades fundamentales, para mantener los mejores intereses de las personas a la vanguardia de la toma de decisiones y para superar la adversidad. 5,40,65 Esto es vital para evitar sucumbir a lo que se ha llamado el síndrome de «esperarlo» (hasta la resolución final). 16 Este síndrome se caracteriza por un prolongado estado de existencia similar al limbo —simplemente atornado junto con la apatía y la alegría, la pasión, la productividad y la ambición agotadas— que está marcado únicamente por el paso del tiempo. Separar claramente las constantes definitorias de las transponibles (es decir, estructuras, programas, procesos, procedimientos) es un imperativo y desafío clave de liderazgo, especialmente cuando estos últimos se han arraigado tan profundamente en la cultura que son tratados como constantes e impiden la optimización y la innovación. 66 Las crisis presentan una oportunidad única para iluminar esta distinción.
Por último, es esencial evitar centrarse exclusivamente en la gestión de prioridades a corto plazo. Ser ambidiestro, es decir, considerar simultáneamente las posibilidades futuras («explorar») y las obligaciones y oportunidades presentes («explotar»), es crucial para la preparación para el futuro, el aumento de la adaptabilidad de la organización y el sistema, y la mejora de la toma de decisiones oportuna. 19,67–69Maximice el rendimiento del equipo, la organización y el sistema y analice las mejoras
Dentro de cada contexto evolutivo de la crisis, los líderes necesitan reexaminar críticamente las condiciones para el desempeño del equipo superior, la organización y el sistema en colaboración con el personal. 9 Este reexamen incluye la colaboración interorganizacional, las estructuras de gestión, el personal, la programación, el cálculo de costos y el logro del equilibrio óptimo entre el tiempo en persona y el horario flexible para la atención virtual, el trabajo, la educación y la capacitación. Este proceso es una oportunidad para liberarse del incumplimiento de «la forma en que siempre lo hemos hecho» y debe basarse en las experiencias, los resultados y las lecciones de las adaptaciones planificadas e improvisadas en etapas tempranas de la crisis. 5,9,18 Sin sacrificar la alineación y coordinación de la organización o el sistema, en la medida de lo posible, estas decisiones deben confiarse a los líderes más cercanos al trabajo e informados por el aporte de los mejores actores y equipos. Esto puede incluir permitir que los equipos de alto rendimiento mantengan parte de la autonomía que se les concedió durante la etapa de emergencia. También es importante acordar indicadores de éxito para las mejoras propuestas. El objetivo de discutir enfoques óptimos es mejorar la prestación de atención efectiva y eficiente, la participación de70 empleados y la capacidad y resiliencia de la organización y el sistema, así como motivar y unificar a las personas bajo un propósito compartido. 53Administre el retraso de los servicios en pausa y considere mejoras mientras evita el agotamiento y la angustia moral
La gestión de la reintegración de los servicios que se detuvieron o que las personas evitaron debido al miedo durante la etapa de emergencia, incluidas las cirugías, los procedimientos y las pruebas de diagnóstico y la detección, debe hacerse de manera estratégica, en lugar de simplemente reanudar las operaciones anteriores. Las decisiones de reintegración deben estar alineadas con la evidencia proporcionada por la investigación de resultados71 y depender de la capacidad organizacional y las directivas de salud pública. 72 La resiliencia del personal, el agotamiento y la culpa y la angustia moral causadas por el impacto de los retrasos en el servicio en los pacientes y las familias también deben ser las principales consideraciones. 43 Tal vez sea necesario recuperar la confianza pública en el sistema de salud mediante una estrategia de comunicación eficaz. A pesar de los desafíos logísticos, las discusiones sobre reintegración presentan oportunidades para la optimización a través de mejoras en los procesos y servicios, como un mayor acceso a las consultas con especialistas y una mejor clasificación en un enfoque de «elegir sabiamente»,73, así como para considerar qué servicios deben ser despriorizados, descontinuados o podrían ser administrados por organizaciones colegiadas.PreviendoMantener el aprendizaje, las innovaciones y las colaboraciones, e imaginar posibilidades futuras
Mirando hacia el futuro, es vital durante la etapa de recuperación discutir cómo capitalizar y comprometerse a mantener las lecciones aprendidas, las innovaciones exitosas, las colaboraciones y las coaliciones. La urgencia de las crisis puede encender una innovación sin precedentes,5,9,28 que puede sortear las barreras individuales y organizativas tradicionales al cambio. Estas barreras incluyen una resistencia arraigada al cambio, una adhesión rígida a los modelos, rutinas y procesos mentales y operativos tradicionales, una burocracia excesiva y escepticismo con respecto a la verosimilitud de introducir ideas de fuentes u organizaciones externas. 5,74,75 Los líderes deben aprovechar el impulso creativo y los éxitos de las etapas anteriores y asegurar el espacio para reimaginar posibles mejoras y oportunidades futuras, en lugar de retrasar este proceso hasta que la pandemia haya terminado. 5,16,22,53 Es crucial asegurarse de que la gente entienda que no hay vuelta al status quo anterior o a «negocios como [antes] de costumbre.» 9,11 En cambio, las discusiones deben comenzar desde una premisa de incertidumbre permanente y con un enfoque en prosperar en un contexto en evolución mientras se imaginan, inventan y comunican los beneficios de varios futuros mejores en el mundo endémico. 8,9,28
El concepto de organizaciones de aprendizaje proporciona un modelo útil para una cultura que puede facilitar las mejoras necesarias del sistema para la resiliencia y la sostenibilidad continuas. En este entorno, las personas de todos los niveles pueden, dentro de los límites apropiados, proponer nuevas ideas e innovar espontáneamente sin pedir permiso, sin dejar de estar coordinadas y alineadas con la estrategia. 76 Este enfoque combina el propósito y la confianza centralizados con el poder juiciosamente descentralizado. 20 La previsión estratégica, la adaptabilidad, la innovación, la colaboración (a través de silos, organizaciones, comunidades y disciplinas) y la reevaluación continua de las condiciones óptimas de trabajo deben institucionalizarse e integrarse en la cultura organizacional. 18,22,28 Este tipo de cultura aumenta la capacidad organizacional y la viabilidad futura,67 mejora la eficacia del equipo y la organización de manera complementaria en el presente,28 y contribuye a funcionar como un sistema adaptativo complejo que evoluciona con el entorno cambiante. 77 Aunque lo ideal sería que se integrara en todo el sistema, puede aplicarse a nivel de equipo y unidad en consonancia con la estrategia general. 78Comunicación de crisisProporcionar comunicación regular y generar confianza
La base de todos los imperativos es la necesidad esencial de que los líderes proporcionen y participen en una comunicación regular, clara e inequívoca con su personal y las partes interesadas de una manera que engendre confianza. 5,8,21,79 Cultivar una cultura de confianza requiere inculcar la certeza de que los líderes están tomando decisiones basadas en la mejor evidencia disponible y siempre poniendo la salud y el bienestar de su gente y comunidades a la vanguardia. 65 Esto también implica anclar los mensajes en realismo, ser transparentes cuando hay poca evidencia y aclarar el proceso y los criterios por los cuales se toman las decisiones y sus correspondientes plazos. 5,49,65 También es importante desacreditar selectiva y consistentemente la información falsa,6,58, incluidos los mensajes transmitidos en las redes sociales, que es parte de la «infodemia». 5,8,80
Generar confianza puede significar compartir información detallada e incluso sensible o controvertida con la comunidad. También es fundamental que los líderes creen entornos donde los desafíos constructivos sean bienvenidos, que reconozcan sus propios errores, que sean explícitos sobre lo que podría haber salido mal, por qué y lo que han aprendido en el proceso. 5,9 Por último, es importante destacar los logros9 e inspirar confianza y esperanza de que el compromiso de las personas, la organización y la comunidad de prosperar en la crisis y salir de ella será finalmente exitoso. 49En consulta con la salud pública y otros líderes, proporcione información y recomendaciones de seguridad al gobierno, otras organizaciones, el personal y la comunidad para mejorar la atención equitativa e integrada y la preparación para emergencias en todo el sistema
Los líderes de la salud tienen una oportunidad y una responsabilidad únicas de influir en los cambios estructurales a largo plazo que se requieren para que los sistemas de atención de la salud aborden las necesidades de todas las personas, incluidos los determinantes sociales de la salud. 6,8 Históricamente, las crisis internacionales han encendido lo que Narayan et al8 han descrito como «un punto de inflexión para la acción colectiva proactiva [altruista]». La cooperación regional e internacional es fundamental para prevenir eficazmente el movimiento de enfermedades, reforzar el liderazgo mundial y abordar eficazmente las necesidades prioritarias. 2,4,5,8,58 Los líderes de salud y salud pública deben recopilar su experiencia y aprendizaje experiencial para asesorar al gobierno, en consulta con científicos sociales y conductuales y líderes de sociedades profesionales, otros sectores y organizaciones comunitarias sobre lo que se necesita para abordar las necesidades inmediatas y anticipadas, así como para fortalecer la capacidad de respuesta coordinada futura a emergencias. 5,8,58,81 Esto también implica destacar las brechas, las áreas prioritarias y los recursos requeridos, y hacer recomendaciones de política que se basen en los aportes de la comunidad. 82 Los líderes de Primera Línea tienen la misma responsabilidad de hacer recomendaciones para mejoras a los líderes senior en sus propias organizaciones en función de su experiencia y requisitos.
Los líderes de salud y salud pública tienen un papel adicional de informar e involucrar al personal y a la comunidad como parte de una estrategia de salud pública formal, coordinada y no partidista. 4,5 Servir como abanderados de seguridad es además importante en jurisdicciones donde los mensajes de funcionarios gubernamentales, expertos y líderes de salud no están alineados. 1Limitaciones
Este marco tiene varias limitaciones. Se centra en un fenómeno sin precedentes, cuya naturaleza evoluciona constantemente. También reconocemos que a pesar de la naturaleza diversa de nuestro equipo de autores en términos de experiencia y ubicación geográfica, sería beneficioso validar nuestro marco en otros contextos a nivel mundial. En tercer lugar, nos hemos desviado del método tradicional delphi de incluir las aportaciones de expertos internacionales en la materia sobre el tema como encuestados al elevarlos al papel de coautores, lo que tiene implicaciones en el proceso y los resultados. Nuestra opinión es que la coautoría aumenta el nivel de responsabilidad que los expertos en la materia asumen para el marco final, lo que aumenta su calidad y credibilidad.Conclusiones
A nuestro conocimiento, la literatura ha descuidado la etapa crucial de la recuperación de la respuesta de la crisis. El marco de 10 imperativos que presentamos brinda apoyo a los líderes de salud y salud pública mientras navegan por los desafíos y oportunidades entrelazados durante la fase más dinámica de la prueba de liderazgo desalentadora que es COVID-19.
Las organizaciones, comunidades, jurisdicciones y naciones cuyos líderes distribuyen el liderazgo de manera más efectiva e implementan los imperativos están en una posición ideal para abordar las necesidades urgentes y las desigualdades en los sistemas de salud y para prosperar con propósito, significado y la cocreación de un futuro que sirva mejor a su gente. Esta cocreación debe comenzar ahora. Institucionalizar los imperativos e integrarlos en la cultura y las políticas organizacionales y de todo el sistema garantizará que la adaptabilidad, la capacidad y la innovación necesarias para una capacidad de respuesta formidable, resiliencia y mejor equidad en la atención médica se mantengan mucho después de que esta pandemia haya terminado.







![Model for improvement [2].](https://oup.silverchair-cdn.com/oup/backfile/Content_public/Journal/intqhc/33/1/10.1093_intqhc_mzaa051/1/mzaa051f1.jpeg?Expires=1629587275&Signature=ME4aClh2sbHWhdAeJB7dE4-4mbKx2mFToCnXtfBwG8Du8wLOwJWTyZA7cnlu1wcJJnVzCY2ZvmKTPSleYHmlUen~kQ1Dt1OH~YVqHejjZzm6UBFC0Xu31RIOWx41nfraedUX2D4V-hiyvghwDm9JfZYbKPdpBFGOCv4f7OXptrxtRIY7KaW8o16q38wp5HipOQfoyaJJPSyKGwEo8Jsl2M02OM1V26rZ5wQMOmxO-iRjtjGJvXMQXB-XkxewCLUsYc4L8M2R3oDjC5sH~7ODXPbPYJil3CTAn7vRSvIF7HvM1U--beftPfkvMwBz34WMfooN2cNA45a4vehCTVdvJg__&Key-Pair-Id=APKAIE5G5CRDK6RD3PGA)