Este mes de OCTUBRE el blog va a intentar trabajar sobre motivación, incentivos, remuneración, contratación, magnetismo de los hospitales, y sobre la calidad basada en la experiencia del paciente. Indagar un gran desafío de cambio de la gestión hospitalaria en el área de su talento humano.
Recopilación de trabajos.
En la actualidad, la formación de médicos especialistas está en pleno debate debido a la escasez de médicos en algunas especialidades y, sobre todo, a la dificultad de retenerlos en determinadas zonas geográficas alejadas de los grandes núcleos urbanos. Algunos factores como la apertura del mercado europeo y la evolución de la iniciativa privada amplían el problema.
La relación que existe entre motivación, satisfacción y rendimiento en el trabajo es directa. Por esta razón, se considera crucial conocer los aspectos motivacionales de los futuros profesionales médicos, qué aspectos les provoca satisfacción en el trabajo y a qué factores les dan importancia.
Esperanza Suárez Ruz
Doctora en Sociología. Especialidad: Recursos Humanos. Universidad Politécnica de Valencia.
Isabel Barrachina Martínez
Doctora Ingeniera. Profesora del Departamento de Economía y Ciencias Sociales. Universidad Politécnica de Valencia.
David Vivas Consuelo
Doctor en Medicina. Profesor de Economía Aplicada. Centro de Investigación en Economía y Ciencias Sociales. Universidad Politécnica de Valencia.
Garantizar un aporte suficiente de profesionales médicos se torna urgente, en un país como España, en el que la formación de estos profesionales tiene una duración aproximada de diez años. La formación de los Médicos Internos Residentes (MIR) españoles es una de las mejores de Europa, pero también una de las más costosas. Se realiza con dinero de la administración española. El retorno de dicha inversión se produce cuando el profesional decide seguir desarrollando su carrera médica en España.
Uno de sus objetivos prioritarios de las administraciones públicas es lograr que los profesionales a los que forman permanezcan trabajando en sus servicios sanitarios. De ahí que sea interesante conocer los factores motivacionales que actúan sobre ellos con el fin de retenerlos.
La adecuada planificación de los recursos humanos en sanidad es fundamental para garantizar una asistencia sanitaria de calidad ya que, los profesionales sanitarios constituyen el componente central de la provisión de servicios de salud en todos los países [1]. La efectividad de los sistemas y la calidad de los servicios de salud dependen del desempeño de los profesionales sanitarios. Dicho desempeño está íntimamente relacionado con su cualificación (formación más experiencia) y su motivación.
Los profesionales sanitarios suponen el 10% de la fuerza de trabajo en Europa y el 60‐80% del gasto de los sistemas de salud. Según la OMS (Organización Mundial de la Salud) España destinó en el 2006 el 8% del PIB a la salud(*1).
Los recursos humanos se identifican como el componente más restrictivo para alcanzar los objetivos del siglo XXI.
La escasez de médicos especialistas en algunas áreas es un problema común en la mayoría de servicios de salud autonómicos españoles.
Para prevenir la escasez se deben tener en cuenta, por el lado de la oferta sanitaria, las próximas jubilaciones de los profesionales médicos y las prácticas médicas actuales, así como el desarrollo de nuevas tecnologías y, por el lado, de la demanda, la evolución y composición de la población, cada vez más envejecida y la afluencia de inmigrantes que requiere más profesionales en algunas especialidades. Dicha carencia se agrava en determinadas zonas alejadas de grandes ciudades y, en ocasiones, de modo estacional, por los movimientos vacacionales hacia el litoral.
Para asegurar que el número de médicos especialistas será el suficiente para garantizar una atención de calidad es preciso realizar una planificación correcta de los recursos humanos y conforme a las necesidades presentes y futuras realizar la gestión de plazas para la formación especializada. Pero además, es importante asegurar un contingente necesario de médicos en las diferentes especialidades que deseen desarrollar su trabajo en el Sistema Nacional de Salud español.
Para reclutar y conservar a médicos es necesario reflexionar sobre su motivación. La mayor parte de los esfuerzos destinados a la motivación se reducen a incentivos económicos. Sin embargo, hay otros factores no relacionados con lo económico que pueden influir en la motivación y en el desempeño de los profesionales médicos.
Aplicar medidas que motiven a los médicos internos residentes (en adelante, MIR) a querer ejercer su profesión en centros del sistema de salud español pasa necesariamente por conocer cómo valoran los diferentes aspectos motivacionales y qué grado de satisfacción tienen con los mismos. No debe olvidarse que los MIR son los futuros profesionales médicos con los que contará nuestro Sistema Nacional de Salud.
Esta investigación se ha realizado con el fin de conocer los factores motivacionales de los MIR para poder plantear medidas de cara a la retención de profesionales médicos en lugares deficitarios.
Diseño de la encuesta
En la encuesta se preguntó sobre la importancia y satisfacción de diez factores diferentes:
Las variables introducidas son cualitativas con escala ordinal, es decir, cada una de las preguntas se valoran de 1 a 5, según el grado de acuerdo sobre una afirmación concreta. Los resultados son de porcentajes de cada opción. Para obtener proporción en acuerdo con la afirmación se sumarán los porcentajes obtenidos en las opciones de acuerdo y totalmente de acuerdo.
Previamente al diseño de la encuesta definitiva se pasó la encuesta a una muestra de MIR elegida al azar con un número determinado dentro de cada especialización y en base a los resultados del premuestreo se definió la encuesta definitiva.
Los resultados de la encuesta se interpretan en el apartado 5, a la luz de las teorías de motivación de Vroom [2], Herzberg [3] y Pérez López [4], quien tras analizar las dimensiones de la motivación humana aportadas por diferentes autores las clasifica en: extrínseca, intrínseca y trascendente.
Principales cambios en la profesión médica en españa: reflexiones para el futuro
La profesión médica está experimentando fuertes cambios en las últimas décadas. Entre ellos hay que destacar los siguientes [5]: 1) feminización de la profesión médica; 2) envejecimiento de los profesionales médicos; 3) formación y especialidades; 4) aumento de la demanda de médicos en el sector privado; 5) desplazamiento de los médicos españoles hacia Europa en búsqueda de mejores oportunidades; y 6) cambios en la legislación europea: aplicación de directivas laborales europeas.
En las siguientes páginas se explicarán los cinco primeros aspectos por entender que están íntimamente relacionados con la motivación de los profesionales médicos.
Feminización de la profesión médica
Por lo que respecta al factor feminización [6], debe destacarse que, como ocurre en otras universidades españolas, en las facultades de medicina de España las mujeres son mayoría. Dos de cada tres nuevos médicos son mujeres(*2), y éstas tienden a elegir determinadas especialidades, más compatibles con la vida familiar –relación inversa con el número de guardias‐, o por afinidad con los pacientes –obstetricia, especialidades pediátricas‐. La planificación debería tener en cuenta que la feminización de la medicina implicará la introducción de ajustes para compatibilizar profesión y familia. Por tanto, igual que sucede en otros sectores de la economía, deberían empezar a plantearse medidas flexibles para conciliar vida y trabajo en el sector sanitario [7].
(*2) http://www.elpais.com/articulo/sociedad/Faltan/medicos/estan/mal/rep…
Envejecimiento de los profesionales médicos
En cuanto factor envejecimiento se observa lo siguiente. Las pirámides de edad de los médicos españoles son desiguales, territorialmente y por especialidades. Las mayores divergencias territoriales afectan a los médicos jóvenes (porcentajes máximos en Baleares y mínimos en Galicia y Ceuta y Melilla).
Las especialidades tradicionales están muy envejecidas, lo cual representa una amenaza [8]. En la próxima década se jubilarán una gran parte de los facultativos especialistas de los hospitales. El recambio debería estar ya en marcha. No parece haber correlación estadística, sin embargo, entre las dinámicas de jubilación y de formación MIR.
Formación y especialidades
Los MIR son médicos en formación que han firmado con la dirección de los hospitales y de las áreas de atención primaria un contrato de trabajo para su formación en distintas especialidades tras superar una prueba nacional selectiva (MIR). A menudo, este contrato representa para ellos la primera relación laboral que mantienen: tiene la característica especial de ser un contrato en formación y se regula por la Ley 44/2003, de 21 de noviembre, de ordenación de las profesiones sanitarias. El número de plazas MIR que se convoca anualmente es demasiado rígido y no está pensado para preparar el futuro, en cuanto a número de especialistas que se necesitarán, sino que se mantienen los que existían anteriormente [10].
En cuanto a la preferencia de elección de plazas para la formación, parece ser que uno de los factores que actúa es la posibilidad de realizar la especialidad en la Comunidad Autónoma en la que viven. Tal y como señalan algunos autores, el 70% se queda en su Comunidad Autónoma, y el 40% de los que se van a otras Comunidades fue porque no pudieron disponer de plaza en la suya propia. Otro factor que influye es en la elección del centro de formación es la existencia de un idioma comunitario [9]. En cuanto a la elección de especialidad influye la posibilidad de poder ejercer la profesión en el sector privado combinándolo con el trabajo en el sector público.
Esta formación postgraduada debe contemplarse como un factor determinante sobre uno de los elementos capitales del sistema sanitario, su componente o factor humano. El conocimiento de sus preferencias y aspectos motivacionales deben utilizarse como un elemento más de gestión del sistema sanitario y su evaluación, comprensión y modulación debiera introducirse de pleno en cualquier estrategia de la Administración dirigida a la gestión de los recursos humanos del sistema sanitario.
En la actualidad, no existe una previsión de las necesidades de especialistas; así se ha pasado de épocas de importante excedente a otras de escasez de profesionales médicos. De esta manera, cabe resaltar, un estudio sobre la dinámica de la formación médica especializada en el sistema nacional de salud español detecta importantes excesos de especialistas [11]. Sin embargo, en un estudio reciente realizado en España se muestra que existe un déficit de cardiólogos [12], unos 260 en 2004, en torno al 13% de los efectivos. La escasez de determinados especialistas se agrava en algunas localidades alejadas de las grandes ciudades.
La planificación del cálculo de las necesidades debe contemplar el número de especialistas preciso pero también la capacitación de los mismos. Es decir, que no sólo basta garantizar la sustitución cuantitativa, sino que también es necesario hacerlo desde el punto de vista cualitativo. Se debe garantizar la transmisión del conocimiento y la capacidad de respuesta a las necesidades del sistema. Además de los MIR que inician su formación, un pequeño porcentaje no termina la especialidad porque decide cambiar a otras especialidades. De hecho, incluso se observan casos de plazas que quedan vacantes. Entre aquellos que terminan la especialidad algunos continúan su vida profesional en el mismo hospital en que realizaron la formación o en otros lugares de la Autonomía que les ha formado, mientras que otro porcentaje se desplaza a otras Comunidades Autónomas, otros países o a la empresa privada.
El número de puestos de trabajo sin cubrir que se anuncian en prensa especializada y en Internet, o el hecho de que los sistemas públicos contraten médicos sin la titulación exigible, acogiéndose a la excepcionalidad y a la necesidad, sugieren que hay problemas para cubrir plazas de ciertas especialidades. Entre estas especialidades se encuentran la anestesia, sobre todo en determinadas zonas poco atractivas, como pequeñas localidades sin hospitales docentes.
Todas estas razones están ocasionando déficits selectivos de profesionales que se deberían afrontar con instrumentos de diversa índole, con incentivos financieros y profesionales para el reclutamiento y la retención de los profesionales en las “zonas frágiles” [13].
Hasta el momento no se están utilizando incentivos económicos, tales como pluses salariales, como instrumento para atraer recursos profesionales escasos a las zonas poco atractivas. En España, las remuneraciones de los médicos están por debajo de las homólogas europeas.
La experiencia de lo que ocurre en otros países podría servir como reflexión a lo que podría suceder en España de no tomar las medidas oportunas. Por ejemplo, en Alemania el ratio de abandono de la carrera de medicina está aumentando progresivamente así como el número de médicos que se están desplazando hacia profesiones no médicas. Las causas del abandono se deben a la insatisfacción con los incentivos existentes, tanto monetarios como no monetarios durante la formación y práctica de la medicina. Entre los médicos que permanecieron ejerciendo, se detecta una insatisfacción similar que se refleja en una huelga en 2006 donde se reclaman mejores salarios y condiciones laborales [14].
Aumento de la demanda de médicos en el sector privado
La fuerte demanda de trabajo por parte del sector privado es otra fuente de déficit. Según datos del Registro Mercantil, entre 1997 y 2002 el empleo total del sector privado lucrativo “actividades hospitalarias” aumentó un 40% en España. Sin embargo, esos datos no parecen concordar con la Estadística de Establecimientos Sanitarios con Régimen de Internado (EESCRI), según la cual el número de médicos que trabajan en hospitales privados lucrativos solamente aumentó un 8% entre 1995 y 2002 (el número de colegiados creció un 14,3% en ese período).
Desplazamiento de los médicos españoles hacia Europa en busca de mejores oportunidades
Las mejores condiciones laborales y mejores salarios de otros países europeos está provocando que algunos médicos españoles deseen irse a ejercer su carrera profesional fuera de España. Entre los destinos elegidos cabe señalar Francia, Portugal o Reino Unido (González P y Barber P, 2006). Los datos de empleo de nuestros profesionales en el exterior indican que se está produciendo una salida continua de médicos y enfermeras a países de la Unión Europea. A principios de 2001, el ministro de sanidad de Reino Unido y la ministra de sanidad de España (Celia Villalobos) firmaron un convenio para facilitar la contratación de médicos y enfermeros por parte del Servicio Público de Salud inglés.
En el momento actual, a efectos de planificación de las necesidades de médicos especialistas, únicamente se puede actuar sobre la oferta de formación de especialistas dentro de la Comunidad. Para una correcta planificación resulta interesante conocer, por un lado, las necesidades reales por sustitución de los profesionales actuales y, por otro, qué factores determinan la permanencia de profesionales en España y cuáles influyen en que no lo hagan.
Los cambios señalados son importantes para planificar el futuro reclutamiento y la retención de médicos, así como para la mejora de la productividad y la calidad de los servicios proporcionados por el componente esencial del sistema de asistencia médica.
Revisión de la teorías de la motivación en el trabajo
Es evidente que todas las personas a la hora de realizar un determinado trabajo esperan algo a cambio. Los motivos que llevan a las personas a realizar, especialmente bien, un trabajo o que les impulsan a no realizarlo todo lo bien que lo podrían hacer son diversos. Sin embargo, no todas las personas otorgan la misma importancia o el mismo valor a los diferentes motivos.
La teoría de las expectativas de Vroom pone de manifiesto que una de las variables que influye de forma decisiva en la fuerza motivacional es la valencia, definida como el valor que le da la persona a lo que recibirá por realizar determinada actividad. Para Vroom, la fuerza motivacional está en función de tres variables: expectativa, instrumentalidad y valencia.
La expectativa se define como la probabilidad subjetiva y a priori de alcanzar lo que la persona se propone si se esfuerza. Por tanto, la expectativa pone en relación el esfuerzo y el rendimiento.
La instrumentalidad es la consecuencia o consecuencias (conseguir un mayor prestigio, aumento de sueldo, aprendizaje, etc.) calculadas a priori, de haber conseguido lo que la persona se ha propuesto.
Por último, la valencia es la valoración que la persona realiza sobre las diferentes instrumentalidades o, lo que es lo mismo, el grado de importancia que se le concede a aquello que la persona piensa que puede conseguir: por ejemplo, mayor prestigio, una subida de sueldo, aprendizaje, etc. Vroom asegura que las tres variables influyen en la fuerza motivacional.
Si la expectativa o la valencia son bajas, la fuerza motivacional lo será también. Cuando la expectativa es baja la persona piensa que por mucho que se esfuerce no logrará nada, por tanto, no se esforzará. Lo mismo sucede con la valencia: si lo que pienso que puedo conseguir (instrumentalidades) por realizar una determinada actividad,, no lo valoro en un grado razonable (valencia), no me esforzaré. De ahí que lo que se ofrezca por realizar un trabajo deba estar en consonancia con lo que a la persona le importa. Si no, el derroche de energía será en vano.
El esquema de Pérez López agrupa los diferentes motivos, señalados por diferentes autores en tres dimensiones de la motivación: extrínseca, intrínseca y trascendente.
La dimensión extrínseca recoge todos aquellos motivos que tienen que ver con aspectos externos al trabajo en sí mismo. Dicho de una manera más sencilla, la motivación extrínseca es la que consigue que un individuo se mueva (realice bien un trabajo) por lo que espera obtener a cambio. Por tanto, la dimensión extrínseca de la motivación se ve reflejada en el cuestionario cuando se pregunta sobre la importancia y satisfacción de los siguientes factores: retribución, seguridad o estabilidad en el trabajo, prestigio y respeto.
La dimensión intrínseca de la motivación recoge aquellos motivos que nos llevan a actuar por la repercusión que esa acción tiene sobre nosotros mismos. Se puede afirmar que alguien se mueve por motivación intrínseca si al actuar pone el acento en la sustantividad de la acción y no en torno a ella. La dimensión intrínseca de la motivación se ve reflejada en la encuesta cuando se pregunta sobre la importancia y la satisfacción de factores como desarrollo profesional, aprendizaje de cosas nuevas o autonomía a la hora de realizar el trabajo. Es importante destacar que la motivación intrínseca consigue rendimientos por encima del mínimo.
Por último, la dimensión trascendente de la motivación recoge aquellos motivos que tienen que ver con la consecución de logros para otras personas distintas a la que ejecuta la acción. La motivación trascendente, por tanto, es aquella que impulsa a las personas a moverse por las consecuencias (positivas) que sus acciones tienen sobre otros. Es la única motivación orientada a otros e implica cierta madurez a nivel profesional. Tanto la extrínseca como la intrínseca consiguen satisfacer aspectos para el sujeto que realiza la acción; en el caso de la extrínseca, por lo que se espera obtener y en el caso de la intrínseca, por lo que se espera cambiar internamente. La motivación trascendente es tan poderosa como las otras dos y curiosamente es a la que menos atención se le presta cuando se indaga sobre la motivación en el trabajo. En todos los trabajos la motivación trascendente es muy importante, pero en el caso de los médicos, por motivos obvios, esta dimensión debe estar muy desarrollada para ejercer la profesión en toda su plenitud. La dimensión trascendente de la motivación puede observarse en la encuesta cuando se pregunta sobre la importancia y satisfacción de las repercusiones positivas para otros (pacientes, hospital, etc.).
La teoría de Herzberg distingue entre factores higiénicos y motivadores. En la terminología de Herzberg los denominados factores higiénicos son aquellos que si están ausentes generan insatisfacción, pero su presencia no garantiza que se produzca satisfacción. Los factores motivadores para Herzberg son los que tienen que ver con la tarea en sí misma (gusto por realizarla, etc.). No se debe olvidar que el hecho de contar con medios materiales insuficientes genera insatisfacción, pero lo contrario no genera satisfacción. Lo mismo sucede con el ambiente de trabajo: el hecho de que el ambiente de trabajo sea bueno no consigue que los MIR estén contentos con su trabajo, pero si el ambiente es malo la insatisfacción que genera puede repercutir en el rendimiento del médico residente. Conviene resaltar, pues, que ambos factores, higiénicos y motivadores, tienen consecuencias directas sobre el rendimiento y, en cierta medida, son interdependientes.
El gusto por la tarea que se realiza que, según Herzberg es un factor motivador, puede verse ensombrecido por un ambiente de trabajo descuidado. En este caso, la insatisfacción generada por los factores higiénicos puede llevar a afectar a los factores motivadores, que dejan de tener sentido por las incomodidades que el individuo se encontraría al estar encerrado en un ambiente físico que le desagrada. Aun siendo el contenido del trabajo interesante (factor motivador), un ambiente poco agradable (en el que la iluminación afecte a la vista, los ruidos impidan la concentración necesaria, no se cuente con los medios materiales y tecnológicos adecuados, etc.) acabará por hacer perder el interés por levantarse e ir a trabajar y mitigará el deseo de rendir al máximo.
Es decir, para que se produzca un buen desempeño es necesario que el trabajo sea atractivo (factor motivador), pero también que se produzca un cierto grado de cumplimiento de los factores higiénicos.
Resultados y discusión
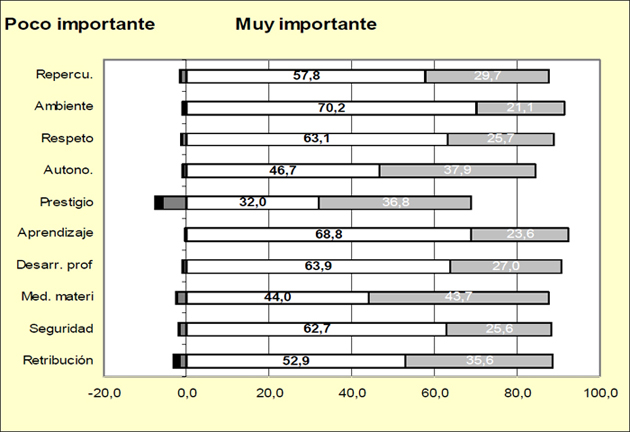
El gráfico 1 muestra el grado de importancia que se concede a cada factor en el desempeño del trabajo. La barra hacia la derecha muestra el porcentaje de MIR que opina que el factor es muy importante, mientras que la barra hacia la izquierda muestra el porcentaje que concede escasa importancia al factor.
Gráfico 1. Importancia de los diferentes factores emocionales.
Fuente: Elaboración propia (2006) a partir de datos facilitados por la Conselleria de Sanidad de la Comunidad Valenciana.
Como puede observarse, todos los motivos extrínsecos, excepto el prestigio, son valorados como muy importantes para más de la mitad de los encuestados. El porcentaje de encuestados que valora como muy importante la seguridad y estabilidad en el empleo (62,7%) y el respeto de los demás (63,1%) está por encima del porcentaje de personas que valora la retribución como muy importante.
Por lo referente a la motivación intrínseca, el cuestionario recoge tres motivos intrínsecos: la “oportunidad de desarrollo profesional”, la “oportunidad de aprender cosas nuevas” y la “autonomía a la hora de realizar un trabajo”. Casi dos tercios de los encuestados (en concreto el 58,96%) considera la motivación intrínseca como muy importante en el desempeño de su trabajo.
El “desarrollo profesional” tiene una valencia muy alta (es considerado como muy importante) para casi el 64% (63,9%) de los encuestados; “aprender cosas nuevas” es considerado muy importante para casi el 70% (68,8%) de los encuestados y la “autonomía a la hora de realizar el trabajo” es considerada como muy importante para el 46,9%. Como puede observarse, una amplia mayoría de MIR (casi el 70%) considera importantísimo aprender cosas nuevas en el desempeño de su trabajo.
Por lo que respecta a la satisfacción con respecto al aprendizaje son más del 90% (91,7%) los que se sienten satisfechos o muy satisfechos con el aprendizaje obtenido en su trabajo actual.
El cuestionario ha recogido la dimensión transcendente en el motivo que alude a “las repercusiones positivas para otros (pacientes, hospital…).
La motivación trascendente es considerada para el 57,8% de los MIR con el grado máximo de importancia; es decir, en una escala de 1 a 5 (siendo 1 muy poco importante y 5 muy importante), el 57,8% de los encuestados valoran con un 5 el grado de importancia que tiene, en el desempeño de su trabajo, las repercusiones positivas para los pacientes.
A la vista de los resultados es importante señalar que, aunque las tres dimensiones de la motivación (extrínseca, intrínseca y trascendente) son muy importantes, para más de la mitad de los encuestados, la que obtiene cifras más altas es la intrínseca (58,96%), seguida de la trascendente (57,8%). La dimensión extrínseca queda en último lugar (52,9%). Hay más encuestados que consideran muy importante el motivo “repercusión positiva para los pacientes” (57,8%) que encuestados que consideran muy importante la retribución (54,1%).
Dentro de la dimensión intrínseca, los motivos “desarrollo profesional” y “aprender cosas nuevas” aglutina el número mayor de personas que los consideran como muy importante (el 63,9% en el primer caso y el 68,8% en el segundo caso). Este último resultado no es de extrañar si se tiene en cuenta que la población a la que se le pregunta está comenzando su carrera profesional y en ese momento es lógico que el aprendizaje y desarrollo profesional se valoren en grado alto.
La teoría de Herzberg distingue entre factores higiénicos y motivadores. El cuestionario incluye como factores higiénicos la importancia y satisfacción de ambiente de trabajo y medios materiales y tecnológicos. La mayoría de encuestados (70,2%) considera como muy importante (es decir, señalaron 5 en una escala de 1 a 5), en el desempeño de su trabajo, contar con un ambiente de trabajo bueno. Sin embargo, sólo el 39,6% asegura estar muy satisfecho con este aspecto. Trasladando este resultado a la teoría de Herzberg se puede concluir que el factor higiénico “ambiente de trabajo” genera insatisfacción para algunos MIR.
Respecto al factor higiénico “medios materiales y tecnológicos” se observa que el 44% los considera muy importantes para el desempeño de su trabajo y sólo el 6,9% considera estar satisfecho con los medios de los que dispone.
El dato anterior debe ser tenido en cuenta ya que, el incumplimiento de los factores higiénicos contribuye al estrés tanto como el incumplimiento de los factores motivadores. Téngase en cuenta que uno de los errores de Taylor (Taylor F, 1941) y sus seguidores consistió precisamente en no darse cuenta de que por mucho que incrementase el salario, llegado un determinado nivel, la fatiga de los empleados asociada a un ambiente de trabajo en el que el ritmo de trabajo lo marcaban las máquinas, impedía el aumento de la productividad que se calculaba sobre el papel.
Importancia y satisfacción de los factores motivacionales
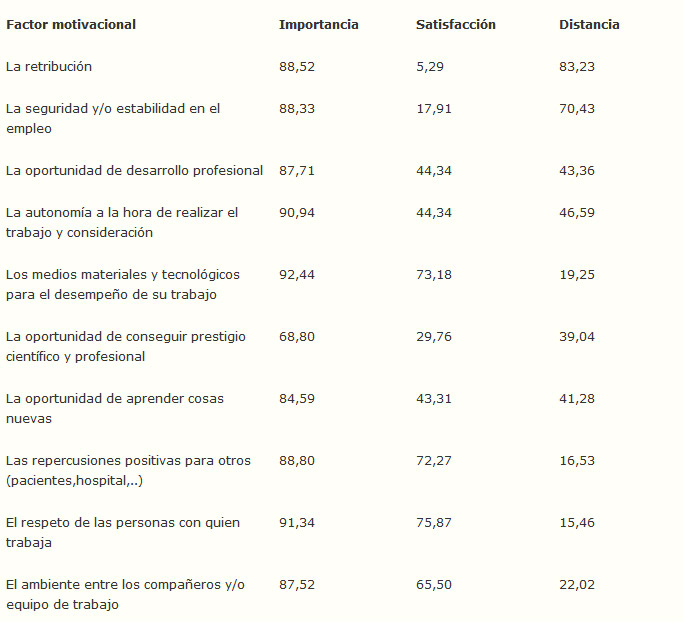
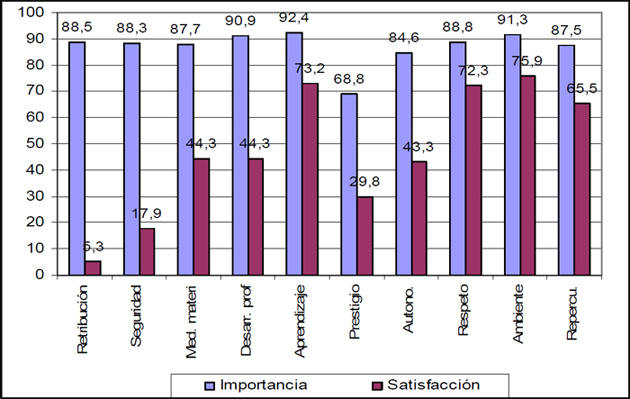
La encuesta preguntaba sobre la importancia y satisfacción de ciertos factores en el desempeño del trabajo actual. Es de interés señalar la diferencia que se produce entre lo que se considera importante y lo que se considera satisfecho. La tabla 3 muestra, para cada factor motivacional, el porcentaje que está de acuerdo en que es muy importante y el porcentaje que está satisfecho con el factor, así como la diferencia entre los dos porcentajes. Ésta tabla se representa gráficamente en los gráficos 4 y 5.
Tabla 3. Importancia frente a satisfacción con el factor.
Como puede observarse en la tabla 3 y en los gráficos 4 y 5, la distancia mayor entre importancia y satisfacción se produce en los casos de la “retribución” y “estabilidad en el empleo”.
Es importante conocer este dato debido a que la distancia significa “desmotivación” en el factor en el que se produce. En el caso de la retribución se podría concluir que una parte importante de los encuestados siente que no están adecuadamente retribuidos. Debe tenerse en cuenta que la retribución representa una forma de reconocimiento de la labor de una persona. Probablemente lo que duele de no sentirse bien retribuido no es el dinero en sí mismo, sino la falta de reconocimiento de la labor realizada [15]. El dinero, en este sentido, es considerado como una medida del valor y utilidad que mi trabajo tiene para los demás.
También podría estar sucediendo lo que contempló Adams [16] al analizar la motivación. La teoría de Adams señala que la comparación entre empleados se produce con bastante frecuencia y es causa de desmotivación por parte de aquellos que salen perdiendo. En efecto, el individuo no sólo analiza lo que aporta y lo que recibe por parte de la organización en la que trabaja, sino que además mira a su alrededor y analiza lo que aportan los demás y lo que reciben, sacando conclusiones que pueden desmotivar si perciben un trato injusto en el balance con los otros profesionales que le rodean.
En el caso de que este sentimiento se produzca en médicos cuya motivación intrínseca y trascendente sea baja, la insatisfacción sufrida debido al sentimiento de inequidad puede llevar a tratar de reducir la desigualdad que se percibe a través de comportamientos como descender el ritmo de trabajo conscientemente o no subirlo aún sabiendo que podría hacerlo sin demasiado esfuerzo (gráfico 4).
Gráfico 4. Importancia frente a satisfacción con el factor.
Por otra parte, los factores donde se produce un nivel de satisfacción bastante alto son: “la oportunidad de aprender cosas nuevas”, “las repercusiones positivas para otros (pacientes, hospital…)”, “el respeto de las personas con las que se trabaja” y “el ambiente entre los compañeros de trabajo” (gráfico 5).
Gráfico 5. Distancia entre la importancia concedida al factor y la satisfacción actual.
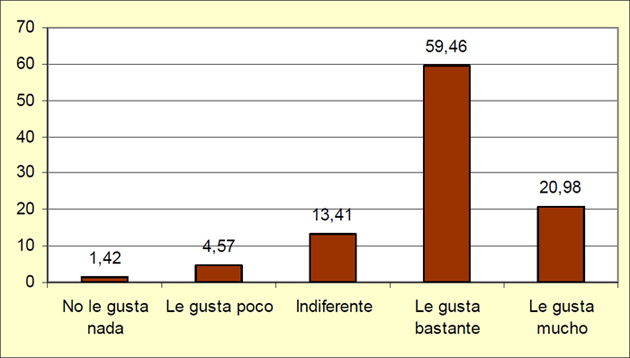
En líneas generales se puede decir que al 80,5% de los residentes les gusta el trabajo que realizan en el hospital. Este dato se ha obtenido sumando el porcentaje de personas que otorgan un 4 (59,46%) y un 5 (20,98%) en una escala de 1 a 5, siendo el 1 muy poco y el 5 mucho. Por tanto, se puede concluir que a la mayoría de los MIR encuestados les gusta el trabajo que realizan en el hospital. El gráfico 6 muestra los porcentajes de respuesta de cada una de las opciones.
Gráfico 6. Porcentaje de respuesta de cada una de las opciones sobre si les gusta el trabajo que realizan en el hospital.
El resultado anterior es muy importante si se tiene en cuenta que el gusto por el trabajo (motivo intrínseco) es uno de los motivos que lleva al rendimiento por encima del mínimo. El rendimiento en el trabajo y el buen desempeño tiene más que ver con el gusto de la tarea en si misma que con la retribución que se otorga. En esta línea es útil la aportación de Mcgregor [17], quien de forma reiterada advierte que motivar a los trabajadores ofreciéndoles únicamente incentivos económicos no mejora la calidad de su trabajo sino sólo la calidad de vida fuera del trabajo.
Cabe añadir que un individuo que se sienta bien retribuido pero que no le guste su trabajo tiene más probabilidad de rendir menos o ausentarse que aquel que le gusta la actividad que desarrolla. Al hablar de rendimiento, en este caso, nos referimos a aquello que el individuo genera con su trabajo y comparte con la organización para la que trabaja. La anterior aclaración es importante puesto que un individuo motivado intrínsecamente, que le guste la tarea que realiza, seguirá trabajando (es decir, generando) incluso aunque vea incumplidos los factores higiénicos. Sin embargo, y aquí estaría el quid de la cuestión, lo que no está tan claro es que quiera compartir todos sus hallazgos con la organización para la que trabaja.
Conclusiones
Las conclusiones que caben resaltar del estudio realizado son:
Por lo tanto, existen factores motivadores no salariales que se pueden poner en marcha para que a los profesionales médicos les interesen ciertos puestos de trabajo que en estos momentos tienen dificultades para cubrirse. Podría mejorarse la motivación de estos profesionales dándole un mayor impulso al desarrollo profesional y reforzando la utilidad que su trabajo tiene para la sociedad.
Bibliografía
1.- Dubois C, Meckee M, Nolte E. Human resources for health in Europe. Copenhagen: Open University Press, McGraw‐Hill Education; 2006.
2.- Vroom V.. Work and motivation. New York: John Wiley & Sons; 1964.
3.- Herzberg F. One more time, how do you motivate employees? Harvard Business Review. 1968;January‐february.
4.- Pérez López JA. Fundamentos de la dirección de empresas. Madrid: Rialp; 1993.
5.- González B, Barber P. Planificación y formación de médicos en España. Una perspectiva europea. En: Hidalgo A, Del Llano J, Pérez S. Recursos Humanos para la salud: suficiencia, adecuación y mejora. Barcelona: Masson; 2006. p. 1‐20.
6.- Alapont Raga V. Nuevos aires en la profesión médica. Revista Valencia Médica. 2006 septiembre‐octubre;(44):3. Disponible en: http://www.comv.es/web/archivos/Vmoct061.pdf
7.- Lázaro Casajús M. La doble condición de mujer y médico: ¿con qué condición?. Revista Valencia Médica. 2006 septiembre‐octubre;(44):14. Disponible en: http://www.comv.es/web/archivos/Vmoct061.pdf
8.- Pombo C, García Pérez MA. Demografía médica en España. Mirando al futuro. Madrid: Fundación CESM; 2005.
9.- González B, Barber P. El programa MIR como innovación y como mecanismo de asignación de recursos humanos. Innovaciones en Gestión Clínica y Sanitaria. Barcelona: Masson; 2005.
10.- González López Valcárcel B, Barber P. Los recursos humanos y sus desequilibrios mitigables. Gac Sanit. 2006;20(sup1):103‐9.
11.- Alonso MI. La dinámica de la formación médica especializada en el sistema nacional de salud español. Revista Asturiana de Economía. 2003;(27).
12.- González B, Barber P. Oferta y necesidad de especialistas en España 2007‐2030. Madrid: Ministerio de Sanidad y Consumo; 2007.
13.- Berland Y. Commission Démographie Médicale. Paris ; 2006. Disponible en: http://www.securite‐sociale.fr/communications/rapports/2006/berland/rapport_berland.pdf
14.- Janus K, Amelung VE, Gaitanides M, Schwartz FW. German physicians “on strike” ‐ Shedding light on the roots of physician dissatisfaction. Health Policy. 2007;82(3): 357‐65.
15.- Pin Arboledas JR, Suárez Ruz E. Una vez más, ¿nos motiva realmente el sueldo? En: Ginebra G. (coord.). Pagar bien y no sólo con dinero. Barcelona: Ariel; 2005.
16.- Adams JS. Towards and understanding of inequity. J Abnorm Soc Psychol. 1963;67:422‐36.
17.- McGregor DM. The Human Side of Enterprise. Japan: McGraw‐Hill Kogakusha; 1960.
Artículos completos
Impact of population morbidity on health care costs in a health district.Pharmaceutical cost and multimorbidity with type 2 diabetes mellitus using electronic health record data.
Análisis de costes en el Área de Imagen Médica de grandes hospitales españoles.
Análisis del gasto sanitario por paciente y riesgo clínico por morbilidad en el departamento de Marina Salud (Alicante).
Predictability of pharmaceutical spending in primary health services using Clinical Risk Groups.
Pharmaceutical cost management in an ambulatory setting using a risk adjustment tool.
Is Health Related Quality of Life (HRQoL) a valid indicator for health systems evaluation?
Atención a mujeres inmigrantes en un programa de mediación intercultural en salud.